1Химическая организация клетки.ppt
- Количество слайдов: 59
 Химическая организация клетки
Химическая организация клетки
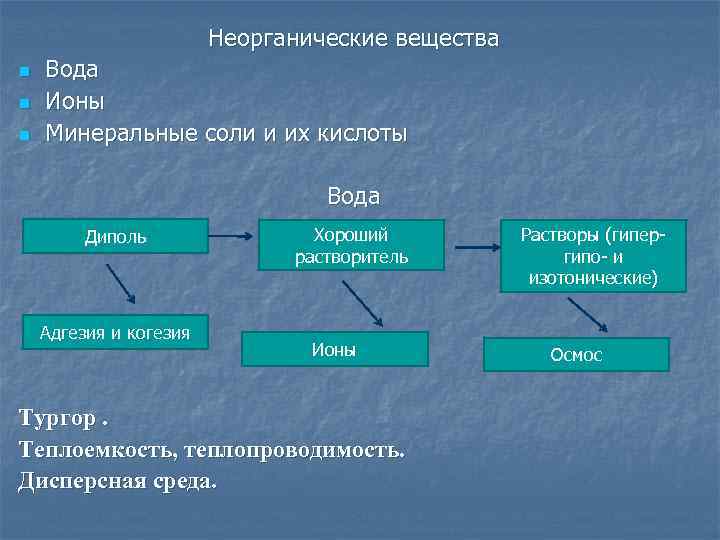 Неорганические вещества n n n Вода Ионы Минеральные соли и их кислоты Вода Диполь Адгезия и когезия Хороший растворитель Ионы Тургор. Теплоемкость, теплопроводимость. Дисперсная среда. Растворы (гипер- гипо- и изотонические) Осмос
Неорганические вещества n n n Вода Ионы Минеральные соли и их кислоты Вода Диполь Адгезия и когезия Хороший растворитель Ионы Тургор. Теплоемкость, теплопроводимость. Дисперсная среда. Растворы (гипер- гипо- и изотонические) Осмос
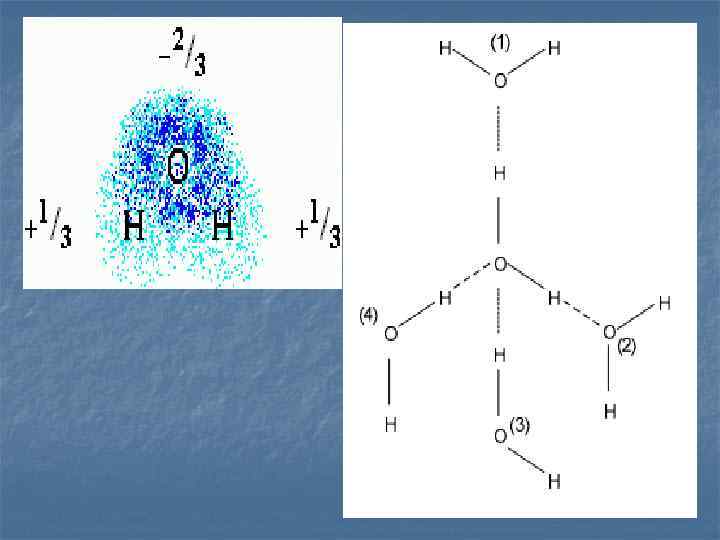
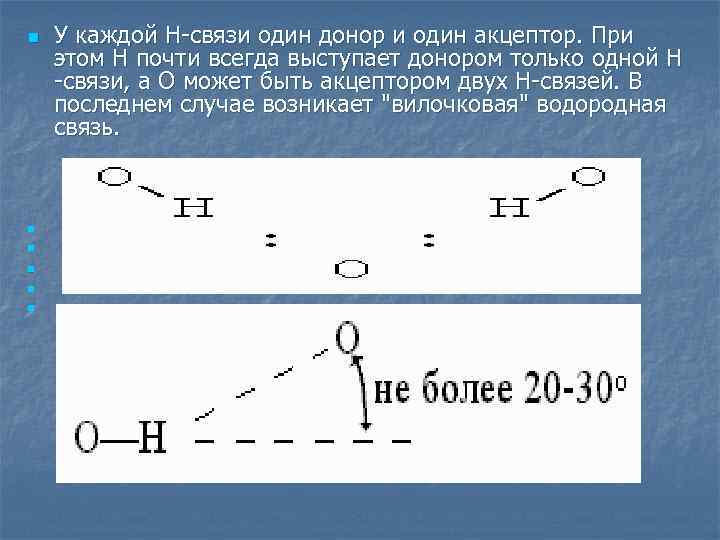 n n n У каждой Н-связи один донор и один акцептор. При этом Н почти всегда выступает донором только одной Н -связи, а О может быть акцептором двух Н-связей. В последнем случае возникает "вилочковая" водородная связь.
n n n У каждой Н-связи один донор и один акцептор. При этом Н почти всегда выступает донором только одной Н -связи, а О может быть акцептором двух Н-связей. В последнем случае возникает "вилочковая" водородная связь.
 Вода является компонентом буферной системы. Буферность – это способность поддерживать слабощелочную реакцию. Выделяют: фосфатный буфер (Н 2 РО 4¯, НРО 4²¯) внутри клетки с р. Н 6, 9 – 7, 4 и бикарбонатный (Н 2 СО 3 и НСО 3¯) во внеклеточной среде с р. Н 7, 4. n Другими неорганическими компонентами клетки являются ионы : катионы (К+, Na+, Са 2+, Mg 2+) и анионы (Cl ¯, НРО 4¯ и др. ). Ионы участвуют в поддержании полярности мембраны, а в нейронах разность потенциалов обеспечивает проведение и передачу нервного возбуждения и. т. д.
Вода является компонентом буферной системы. Буферность – это способность поддерживать слабощелочную реакцию. Выделяют: фосфатный буфер (Н 2 РО 4¯, НРО 4²¯) внутри клетки с р. Н 6, 9 – 7, 4 и бикарбонатный (Н 2 СО 3 и НСО 3¯) во внеклеточной среде с р. Н 7, 4. n Другими неорганическими компонентами клетки являются ионы : катионы (К+, Na+, Са 2+, Mg 2+) и анионы (Cl ¯, НРО 4¯ и др. ). Ионы участвуют в поддержании полярности мембраны, а в нейронах разность потенциалов обеспечивает проведение и передачу нервного возбуждения и. т. д.
 Выделяют четыре группы органических веществ: белки, углеводы, липиды нуклеиновые кислоты. Основу органических веществ составляют атомы С, способные вступать друг с другом в прочные ковалентные связи и образовывать разные по форме каркасы органических молекул. Все они могут быть представлены в виде: - мономеров - малые низкомолекулярные органические молекулы, которые являются строительными блоками для полимеров - полимеры – крупные высокомолекулярные макромолекулы. l l l Мономеры Полимеры Простые сахара полисахариды l Аминокислоты белки l Нуклеотиды нуклеиновые кислоты l Полимеры в зависимости от состава мономеров делятся на: l l Гемопилимеры Липиды не являются биополимерами Гетерополимеры
Выделяют четыре группы органических веществ: белки, углеводы, липиды нуклеиновые кислоты. Основу органических веществ составляют атомы С, способные вступать друг с другом в прочные ковалентные связи и образовывать разные по форме каркасы органических молекул. Все они могут быть представлены в виде: - мономеров - малые низкомолекулярные органические молекулы, которые являются строительными блоками для полимеров - полимеры – крупные высокомолекулярные макромолекулы. l l l Мономеры Полимеры Простые сахара полисахариды l Аминокислоты белки l Нуклеотиды нуклеиновые кислоты l Полимеры в зависимости от состава мономеров делятся на: l l Гемопилимеры Липиды не являются биополимерами Гетерополимеры
 Процессинг молекул прошедших первичный синтез Вновь синтезированные молекулы белка, углеводов, н. к. , липидов подвергаются процессингу (созревание), который включает в себя: 1. конформационные изменения молекул – приобретение 2, 3, 4, конформации, за счет внесения дополнительных химических связей между радикалами молекулы; 2. химическая модификация – присоединение дополнительных химических компонентов, в случае если молекула является сложноорганизованной.
Процессинг молекул прошедших первичный синтез Вновь синтезированные молекулы белка, углеводов, н. к. , липидов подвергаются процессингу (созревание), который включает в себя: 1. конформационные изменения молекул – приобретение 2, 3, 4, конформации, за счет внесения дополнительных химических связей между радикалами молекулы; 2. химическая модификация – присоединение дополнительных химических компонентов, в случае если молекула является сложноорганизованной.
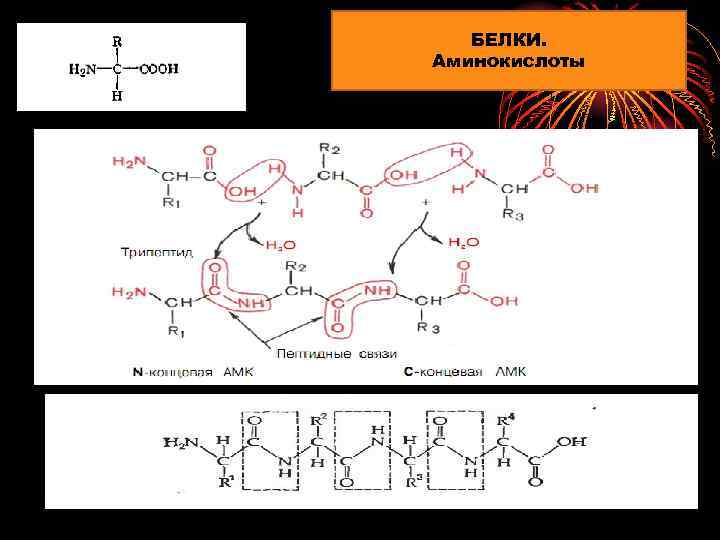 БЕЛКИ. Аминокислоты
БЕЛКИ. Аминокислоты
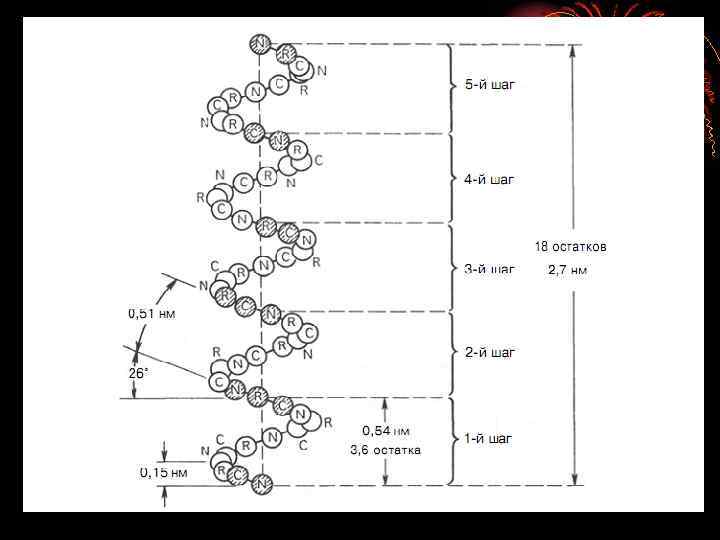
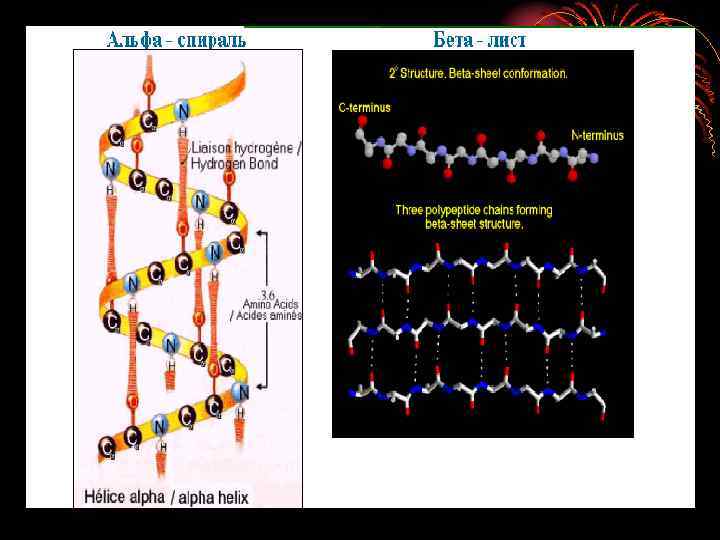

 Самостоятельно: 1. Простые белки - прошедшие только конформационные изменения (примеры), и сложные белки – прошедшие и конформационные изменения и химические модификации (примеры); 2. Функции белков; 3. Ферменты – свойства, механизм работы, классификация.
Самостоятельно: 1. Простые белки - прошедшие только конформационные изменения (примеры), и сложные белки – прошедшие и конформационные изменения и химические модификации (примеры); 2. Функции белков; 3. Ферменты – свойства, механизм работы, классификация.
 Нуклеиновые кислоты характеризуются: 1. Состоят из практически идентичных мономерных звеньев 2. Имеют 1, 2, 3 – пространственно-конформационную организацию 3. способны ассоциироваться с н. к. и белками 4. являются самореплицирующимися структурами 5. Определяют наследственность и воспроизведение наследственной информации в ряду поколений 6. Вступают в процесс созревания (процессинг). Н. К. (полимеры) ДНК РНК Нуклеотиды (мономеры)
Нуклеиновые кислоты характеризуются: 1. Состоят из практически идентичных мономерных звеньев 2. Имеют 1, 2, 3 – пространственно-конформационную организацию 3. способны ассоциироваться с н. к. и белками 4. являются самореплицирующимися структурами 5. Определяют наследственность и воспроизведение наследственной информации в ряду поколений 6. Вступают в процесс созревания (процессинг). Н. К. (полимеры) ДНК РНК Нуклеотиды (мономеры)
 1. Принцип комплементарности – правило Чаргафа (А=Т; Ц=Г или А-Т/Ц-Г= 1). Принцип комлементарности Уотсона и Крика. 2. Формирование гетероциклов (комплементарных пар) А-Т, Г-Ц; 3. Три компонента нуклеотидов – моносахарид-С 5, азотистое основание, остатки фосфорной кислоты. - Формирование гликозитной связи; - формирование фосфоэфирной связи; - формирование фосфодиэфирных связей (реакция этерификации между ОН-группой С 3 одного нуклеода и ОН-группой фосфатного остатка другого) с формирование 5 ` и 3` - конца с образованием одноцепочечной н. к. ; Наличие 2 и 3 -х водородных связей между гетероциклами в дуплексе ДНК. Стекинг взаимодействия – ковалентные гидрофобные связи.
1. Принцип комплементарности – правило Чаргафа (А=Т; Ц=Г или А-Т/Ц-Г= 1). Принцип комлементарности Уотсона и Крика. 2. Формирование гетероциклов (комплементарных пар) А-Т, Г-Ц; 3. Три компонента нуклеотидов – моносахарид-С 5, азотистое основание, остатки фосфорной кислоты. - Формирование гликозитной связи; - формирование фосфоэфирной связи; - формирование фосфодиэфирных связей (реакция этерификации между ОН-группой С 3 одного нуклеода и ОН-группой фосфатного остатка другого) с формирование 5 ` и 3` - конца с образованием одноцепочечной н. к. ; Наличие 2 и 3 -х водородных связей между гетероциклами в дуплексе ДНК. Стекинг взаимодействия – ковалентные гидрофобные связи.

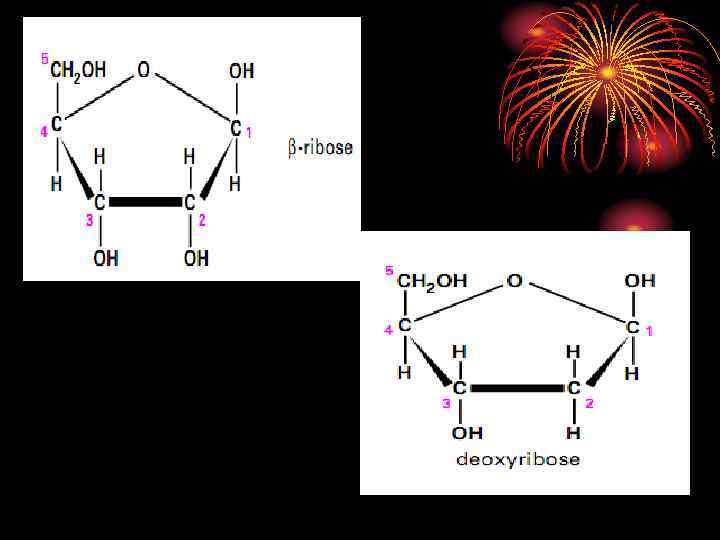


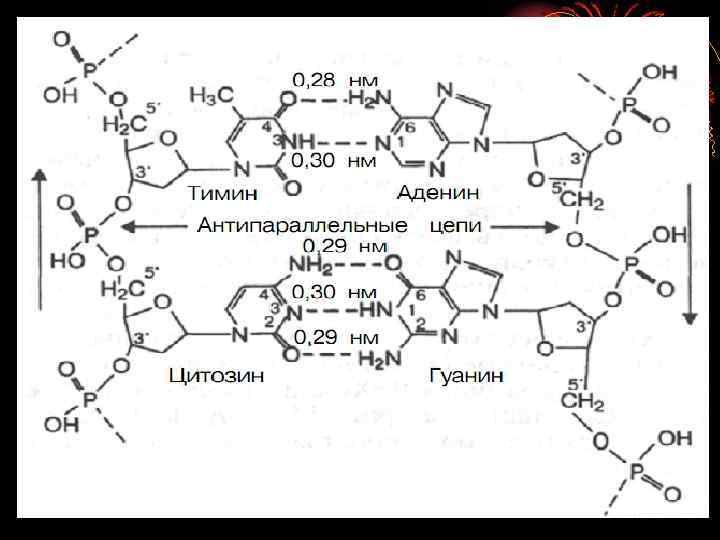
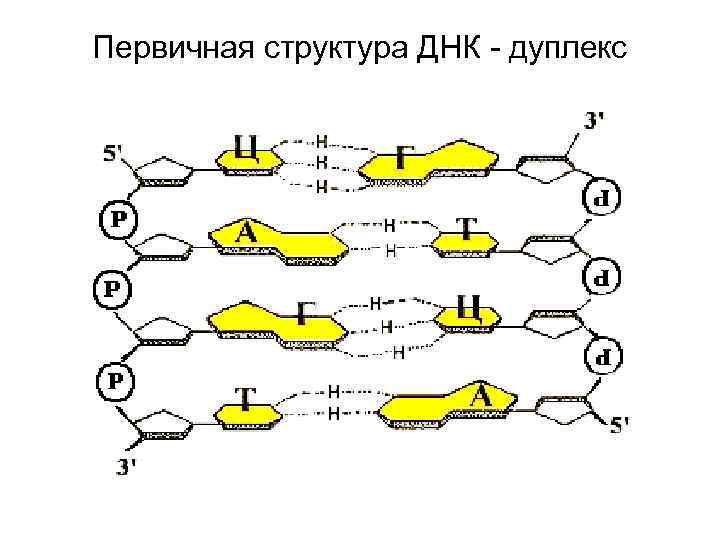 Первичная структура ДНК - дуплекс
Первичная структура ДНК - дуплекс

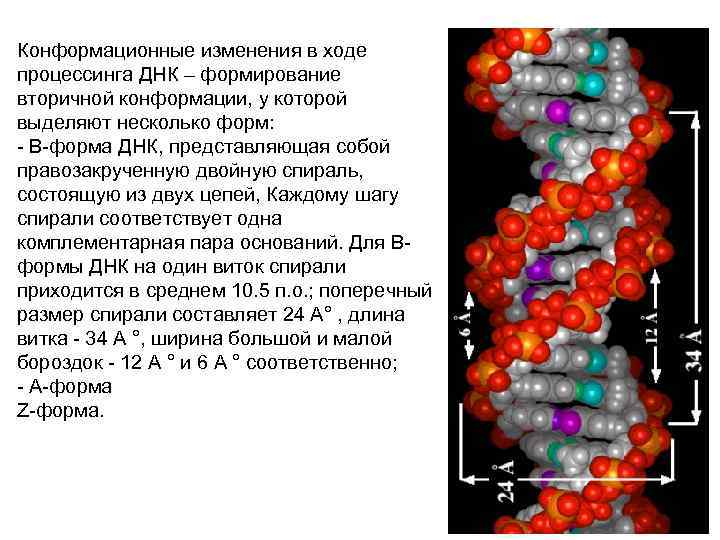 Конформационные изменения в ходе процессинга ДНК – формирование вторичной конформации, у которой выделяют несколько форм: - B-форма ДНК, представляющая собой правозакрученную двойную спираль, состоящую из двух цепей, Каждому шагу спирали соответствует одна комплементарная пара оснований. Для Bформы ДНК на один виток спирали приходится в среднем 10. 5 п. о. ; поперечный размер спирали составляет 24 A° , длина витка - 34 A °, ширина большой и малой бороздок - 12 A ° и 6 A ° соответственно; - А-форма Z-форма.
Конформационные изменения в ходе процессинга ДНК – формирование вторичной конформации, у которой выделяют несколько форм: - B-форма ДНК, представляющая собой правозакрученную двойную спираль, состоящую из двух цепей, Каждому шагу спирали соответствует одна комплементарная пара оснований. Для Bформы ДНК на один виток спирали приходится в среднем 10. 5 п. о. ; поперечный размер спирали составляет 24 A° , длина витка - 34 A °, ширина большой и малой бороздок - 12 A ° и 6 A ° соответственно; - А-форма Z-форма.

 Химическая модификация ДНК 1. 2. 3. Ассоциация с белка гистонами и негистоновыми белками – формирование уровней компактизации ДНК. А так же обеспечение регуляции активности генов. Метилирование.
Химическая модификация ДНК 1. 2. 3. Ассоциация с белка гистонами и негистоновыми белками – формирование уровней компактизации ДНК. А так же обеспечение регуляции активности генов. Метилирование.
 Назначение молекулы ДНК n n n Генетическая информация, закодированная в последовательности нуклеотидов, служит двум целям: во-первых, она необходима для синтеза белковых молекул, во-вторых, обеспечивает передачу самой себя в ряду клеточных поколений и поколений организмов. Обе функции основаны на том, что молекула ДНК служит в первом случае, для транскрипции - перекодирования информации в структуру молекул РНК, которая определяет достаточно жесткий уровень соответствия между данным геном и белковым продуктом, и во втором случае - для репликации или копирования информации в дочерних молекулах ДНК, что при формировании молодых клеток обеспечивает наследственную стабильность организма и вида.
Назначение молекулы ДНК n n n Генетическая информация, закодированная в последовательности нуклеотидов, служит двум целям: во-первых, она необходима для синтеза белковых молекул, во-вторых, обеспечивает передачу самой себя в ряду клеточных поколений и поколений организмов. Обе функции основаны на том, что молекула ДНК служит в первом случае, для транскрипции - перекодирования информации в структуру молекул РНК, которая определяет достаточно жесткий уровень соответствия между данным геном и белковым продуктом, и во втором случае - для репликации или копирования информации в дочерних молекулах ДНК, что при формировании молодых клеток обеспечивает наследственную стабильность организма и вида.
 Коды ДНК Код укладки РНК. Около половины генома эукариот транскрибируется в виде молекул РНК, имеющих компактную вторичную и третичную структуру, которая формируется на основе комплементарных взаимодействий между основаниями, а также комплиментарных взаимодействий с различными белками. Правильного действия этих молекул требуется укладка в уникальную вторичную структуру, на уровне ДНК обусловленную кодом укладки. 2. Хроматиновый код. Эукариотическая ДНК практически полностью включена в хроматин и почти вся упакована в нуклеосомы. Элементарная структурная единица хроматина состоит из гистонового кора и закрученного вокруг него фрагмента ДНК размером 146 п. н. 3. Конформационный код. Определяемая контекстом локальная конформация молекул ДНК является одним из факторов специфичности ДНК - белкового узнавания.
Коды ДНК Код укладки РНК. Около половины генома эукариот транскрибируется в виде молекул РНК, имеющих компактную вторичную и третичную структуру, которая формируется на основе комплементарных взаимодействий между основаниями, а также комплиментарных взаимодействий с различными белками. Правильного действия этих молекул требуется укладка в уникальную вторичную структуру, на уровне ДНК обусловленную кодом укладки. 2. Хроматиновый код. Эукариотическая ДНК практически полностью включена в хроматин и почти вся упакована в нуклеосомы. Элементарная структурная единица хроматина состоит из гистонового кора и закрученного вокруг него фрагмента ДНК размером 146 п. н. 3. Конформационный код. Определяемая контекстом локальная конформация молекул ДНК является одним из факторов специфичности ДНК - белкового узнавания.
 n Фундаментальная единица упаковки хроматина, нуклеосома, была открыта более 25 лет назад (Kornberg and Lorch, 1999). Около 146 п. о. ДНК находится в непосредственном контакте с гистоновым октамером. Намотанная на кор нуклеосомная ДНК имеет форму левозакрученной суперспирали из 1. 8 витков. Гистоновый кор можно представить в виде цилиндра.
n Фундаментальная единица упаковки хроматина, нуклеосома, была открыта более 25 лет назад (Kornberg and Lorch, 1999). Около 146 п. о. ДНК находится в непосредственном контакте с гистоновым октамером. Намотанная на кор нуклеосомная ДНК имеет форму левозакрученной суперспирали из 1. 8 витков. Гистоновый кор можно представить в виде цилиндра.
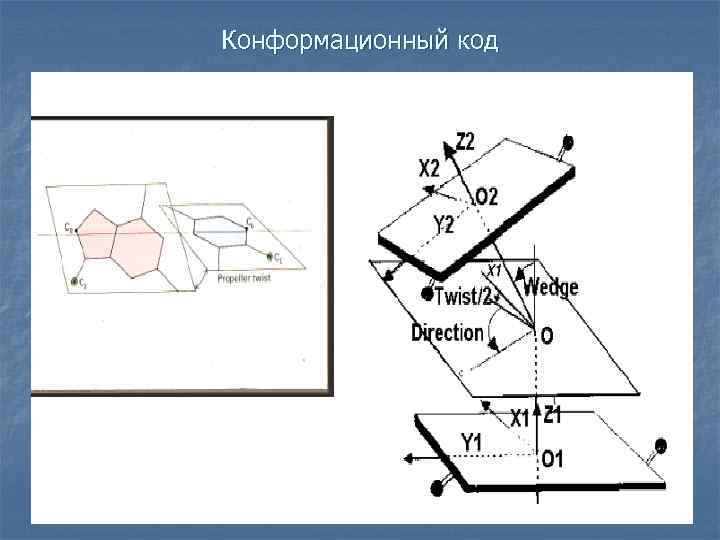 Конформационный код
Конформационный код
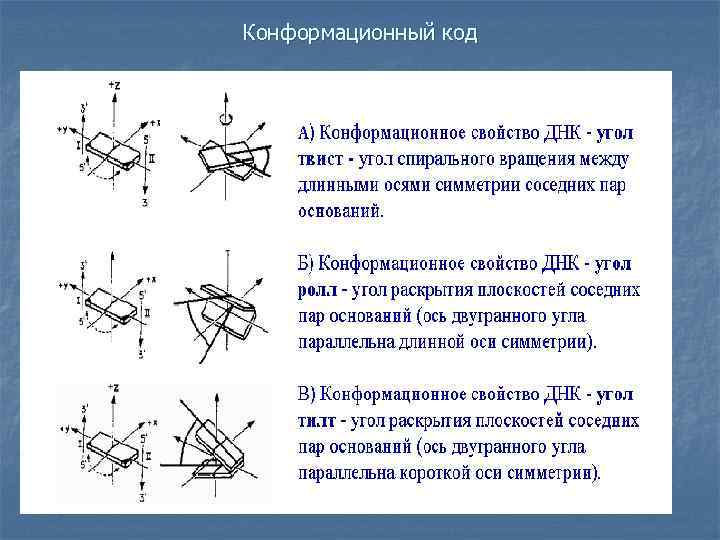 Конформационный код
Конформационный код
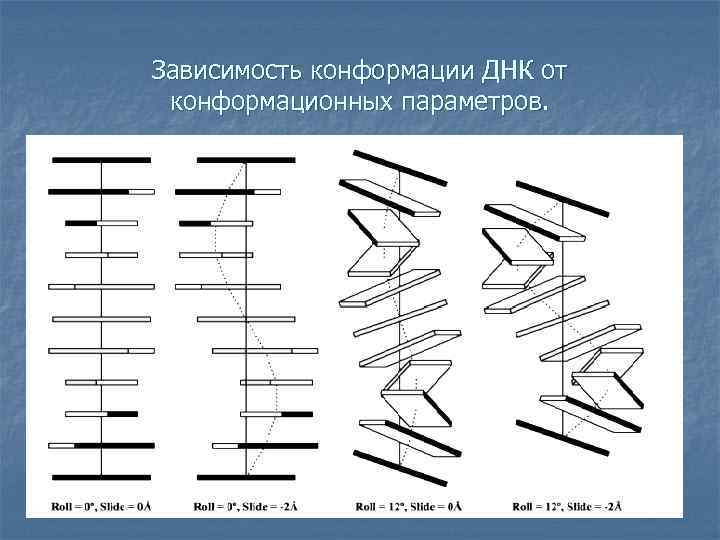 Зависимость конформации ДНК от конформационных параметров.
Зависимость конформации ДНК от конформационных параметров.
 Профиль температуры плавления нуклеосомной ДНК. Схема пространственного расположения на поверхности гистонового октамера районов, различающихся по энергетике жёсткости изгиба ДНК.
Профиль температуры плавления нуклеосомной ДНК. Схема пространственного расположения на поверхности гистонового октамера районов, различающихся по энергетике жёсткости изгиба ДНК.
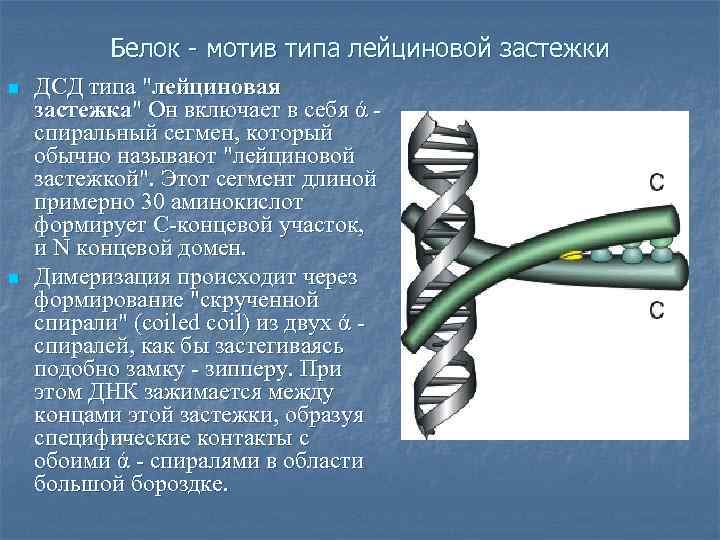 Белок - мотив типа лейциновой застежки n n ДСД типа "лейциновая застежка" Он включает в себя ά спиральный сегмен, который обычно называют "лейциновой застежкой". Этот сегмент длиной примерно 30 аминокислот формирует C-концевой участок, и N концевой домен. Димеризация происходит через формирование "скрученной спирали" (coiled coil) из двух ά спиралей, как бы застегиваясь подобно замку - зипперу. При этом ДНК зажимается между концами этой застежки, образуя специфические контакты с обоими ά - спиралями в области большой бороздке.
Белок - мотив типа лейциновой застежки n n ДСД типа "лейциновая застежка" Он включает в себя ά спиральный сегмен, который обычно называют "лейциновой застежкой". Этот сегмент длиной примерно 30 аминокислот формирует C-концевой участок, и N концевой домен. Димеризация происходит через формирование "скрученной спирали" (coiled coil) из двух ά спиралей, как бы застегиваясь подобно замку - зипперу. При этом ДНК зажимается между концами этой застежки, образуя специфические контакты с обоими ά - спиралями в области большой бороздке.
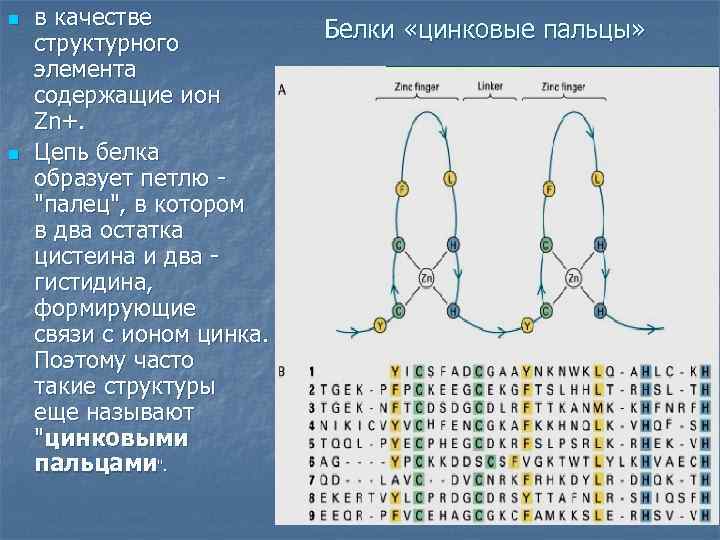 n n в качестве структурного элемента содержащие ион Zn+. Цепь белка образует петлю - "палец", в котором в два остатка цистеина и два - гистидина, формирующие связи с ионом цинка. Поэтому часто такие структуры еще называют "цинковыми пальцами". Белки «цинковые пальцы»
n n в качестве структурного элемента содержащие ион Zn+. Цепь белка образует петлю - "палец", в котором в два остатка цистеина и два - гистидина, формирующие связи с ионом цинка. Поэтому часто такие структуры еще называют "цинковыми пальцами". Белки «цинковые пальцы»
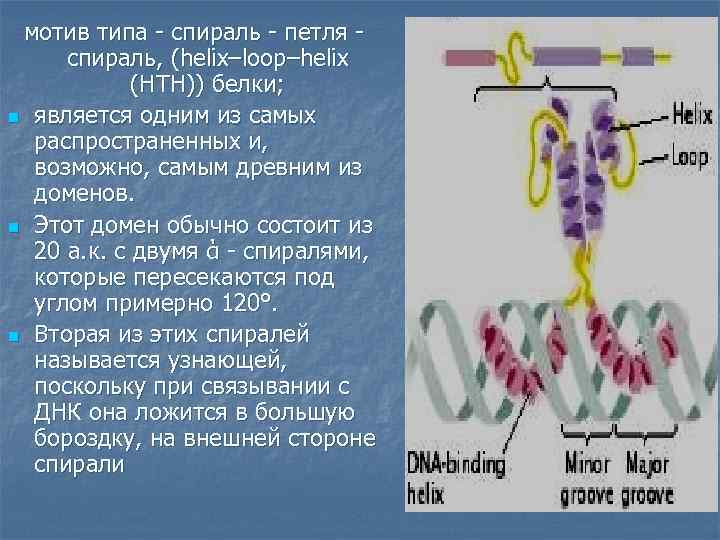 мотив типа - спираль - петля - спираль, (helix–loop–helix (HTH)) белки; n является одним из самых распространенных и, возможно, самым древним из доменов. n Этот домен обычно состоит из 20 а. к. с двумя ά - спиралями, которые пересекаются под углом примерно 120°. n Вторая из этих спиралей называется узнающей, поскольку при связывании с ДНК она ложится в большую бороздку, на внешней стороне спирали
мотив типа - спираль - петля - спираль, (helix–loop–helix (HTH)) белки; n является одним из самых распространенных и, возможно, самым древним из доменов. n Этот домен обычно состоит из 20 а. к. с двумя ά - спиралями, которые пересекаются под углом примерно 120°. n Вторая из этих спиралей называется узнающей, поскольку при связывании с ДНК она ложится в большую бороздку, на внешней стороне спирали
 Бета скэфолд. n n Большинство ДСД этого класса содержат достаточно выраженный скэффолд из β -нитей, на котором располагаются ά спирали, петли и сами β -нити. Факторы этого типа образуют с ДНК обширные контакты. Одни из них могут охватывать половину витка ДНК. В других случаях ДНК закручена вокруг белкового ядра. ТФ связываются с АТ богатыми участками, окруженными по краям последовательностями, богатыми CG парами, и при этом взаимодействия осуществляются путем контактов по малой бороздке ДНК. Подобные взаимодействия сильно искажают конформацию ДНК.
Бета скэфолд. n n Большинство ДСД этого класса содержат достаточно выраженный скэффолд из β -нитей, на котором располагаются ά спирали, петли и сами β -нити. Факторы этого типа образуют с ДНК обширные контакты. Одни из них могут охватывать половину витка ДНК. В других случаях ДНК закручена вокруг белкового ядра. ТФ связываются с АТ богатыми участками, окруженными по краям последовательностями, богатыми CG парами, и при этом взаимодействия осуществляются путем контактов по малой бороздке ДНК. Подобные взаимодействия сильно искажают конформацию ДНК.
 Виды РНК. Размер в нуклеотидах. Функция. l l l g. РНК – геномные РНК некоторых вирусов (10`4 -10 ` 5). Несут наследственную информацию m. РНК –информационные (матричные, мессенжерные). РНК 10 ` 2 -10 ` 5. Являются матрицами для синтеза белка t. PHK – транспортные (трансферные) РНК. 70 -90 н. п. Участвуют в синтезе белка (поставляют аминокислоты для включения в белок) r. РНК – рибосомные РНК 10 ` 2 -10 ` 5 Участвуют в синтезе белка (являются строительными блоками рибосом) s. IРНК – малые РНК 20 -300 Участвуют в упаковке рибопротеиновых частиц, сплайсинге, некоторых регуляторных событиях и проч.
Виды РНК. Размер в нуклеотидах. Функция. l l l g. РНК – геномные РНК некоторых вирусов (10`4 -10 ` 5). Несут наследственную информацию m. РНК –информационные (матричные, мессенжерные). РНК 10 ` 2 -10 ` 5. Являются матрицами для синтеза белка t. PHK – транспортные (трансферные) РНК. 70 -90 н. п. Участвуют в синтезе белка (поставляют аминокислоты для включения в белок) r. РНК – рибосомные РНК 10 ` 2 -10 ` 5 Участвуют в синтезе белка (являются строительными блоками рибосом) s. IРНК – малые РНК 20 -300 Участвуют в упаковке рибопротеиновых частиц, сплайсинге, некоторых регуляторных событиях и проч.
 РНК n n Главное химическое различие между ДНК и РНК состоит в том, что сахарный остаток мономера РНК - это рибоза, азотистых оснований и в ДНК, и в РНК четыре вида: два пуриновых - аденин (А) и гуанин (G) -и два пиримидиновых - цитозин (С) и урацил (U) или его метилированное производное тимин (Т)
РНК n n Главное химическое различие между ДНК и РНК состоит в том, что сахарный остаток мономера РНК - это рибоза, азотистых оснований и в ДНК, и в РНК четыре вида: два пуриновых - аденин (А) и гуанин (G) -и два пиримидиновых - цитозин (С) и урацил (U) или его метилированное производное тимин (Т)
 • • • В зависимости от степени зрелости предназначения РНК могут находиться в трех конформациях первичная – одна полинуклеотидная цепь; вторичная - отдельные участки этой цепи (до 20 -30 нуклеотидных пар) могут быть комплементарны между собой и образовывают спиральную структуру за счет связей между аденином и урацилом (пара A-U) и гуанином и цитозином (пара G-C), между спирализованными участками располагаются одноцепочечные петли; третичная структура – в ее создании и поддержании участвуют неканонические взаимодействия, с образованием угола L – образной молекулы
• • • В зависимости от степени зрелости предназначения РНК могут находиться в трех конформациях первичная – одна полинуклеотидная цепь; вторичная - отдельные участки этой цепи (до 20 -30 нуклеотидных пар) могут быть комплементарны между собой и образовывают спиральную структуру за счет связей между аденином и урацилом (пара A-U) и гуанином и цитозином (пара G-C), между спирализованными участками располагаются одноцепочечные петли; третичная структура – в ее создании и поддержании участвуют неканонические взаимодействия, с образованием угола L – образной молекулы
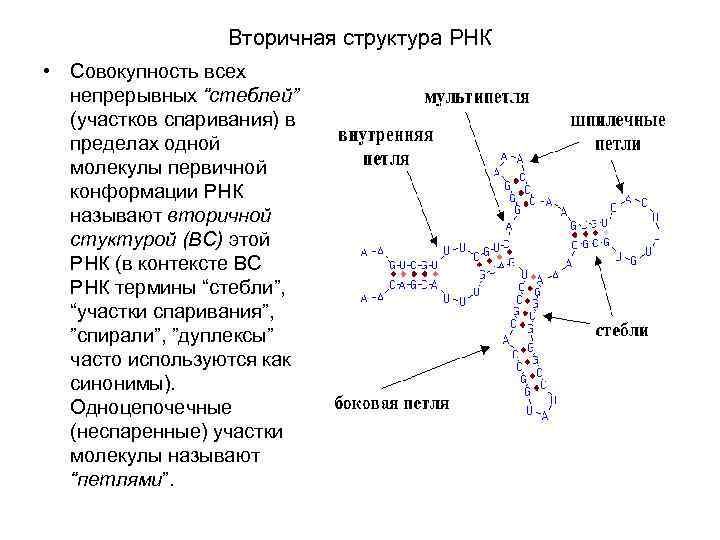 Вторичная структура РНК • Совокупность всех непрерывных “стеблей” (участков спаривания) в пределах одной молекулы первичной конформации РНК называют вторичной стуктурой (ВС) этой РНК (в контексте ВС РНК термины “стебли”, “участки спаривания”, ”спирали”, ”дуплексы” часто используются как синонимы). Одноцепочечные (неспаренные) участки молекулы называют “петлями”.
Вторичная структура РНК • Совокупность всех непрерывных “стеблей” (участков спаривания) в пределах одной молекулы первичной конформации РНК называют вторичной стуктурой (ВС) этой РНК (в контексте ВС РНК термины “стебли”, “участки спаривания”, ”спирали”, ”дуплексы” часто используются как синонимы). Одноцепочечные (неспаренные) участки молекулы называют “петлями”.
 n n Длина цепей т. РНК от 74 -95 н. п. Все т РНК кончаются 3' конце ССАон Антикодоновый триплет находится в середине - IGC, с 5' конца от него всегда 2 пиримидиновым основания, а с 3' конца два пуриновых (один из которых может быть пиримидиновым) эти семь нуклеотидных оснований называются «антикодоновая петля» (АС - петля), Первичная структура РНК
n n Длина цепей т. РНК от 74 -95 н. п. Все т РНК кончаются 3' конце ССАон Антикодоновый триплет находится в середине - IGC, с 5' конца от него всегда 2 пиримидиновым основания, а с 3' конца два пуриновых (один из которых может быть пиримидиновым) эти семь нуклеотидных оснований называются «антикодоновая петля» (АС - петля), Первичная структура РНК
 Функции элементов «клеверного листка» - к акцепторному участку присоединяется аминокислота - антикодон узнает кодон м. РНК - псевдоуридиловая петля участвует в связывании т. РНК с рибосомой - дигидроуридиловая петля нужна для присоединения к т. РНК аминоацил – т. РНК – синтетазы - функции добавочной цепи остаются не вполне ясными. Но известно, что фермент аминоацил-т. РНК -синтетаза узнает свою т. РНК по специфическим участкам в т. РНК: антикодон, акцепторный черешок, Vn.
Функции элементов «клеверного листка» - к акцепторному участку присоединяется аминокислота - антикодон узнает кодон м. РНК - псевдоуридиловая петля участвует в связывании т. РНК с рибосомой - дигидроуридиловая петля нужна для присоединения к т. РНК аминоацил – т. РНК – синтетазы - функции добавочной цепи остаются не вполне ясными. Но известно, что фермент аминоацил-т. РНК -синтетаза узнает свою т. РНК по специфическим участкам в т. РНК: антикодон, акцепторный черешок, Vn.
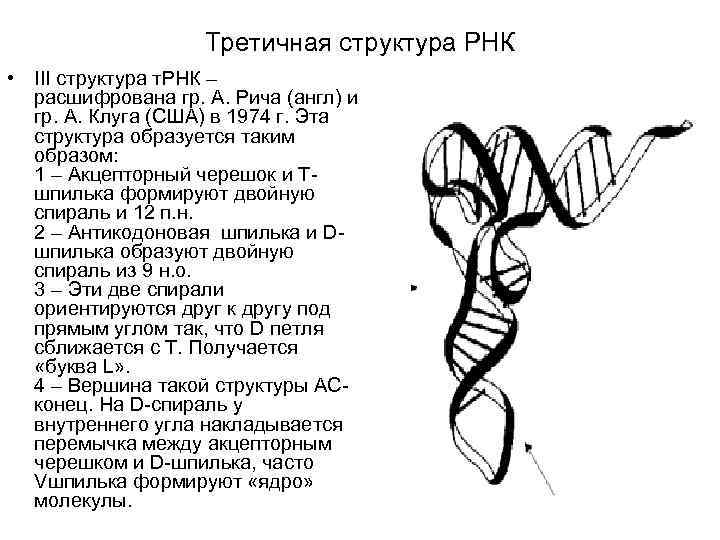 Третичная структура РНК • III структура т. РНК – расшифрована гр. А. Рича (англ) и гр. А. Клуга (США) в 1974 г. Эта структура образуется таким образом: 1 – Акцепторный черешок и Тшпилька формируют двойную спираль и 12 п. н. 2 – Антикодоновая шпилька и Dшпилька образуют двойную спираль из 9 н. о. 3 – Эти две спирали ориентируются друг к другу под прямым углом так, что D петля сближается с Т. Получается «буква L» . 4 – Вершина такой структуры АСконец. На D-спираль у внутреннего угла накладывается перемычка между акцепторным черешком и D-шпилька, часто Vшпилька формируют «ядро» молекулы.
Третичная структура РНК • III структура т. РНК – расшифрована гр. А. Рича (англ) и гр. А. Клуга (США) в 1974 г. Эта структура образуется таким образом: 1 – Акцепторный черешок и Тшпилька формируют двойную спираль и 12 п. н. 2 – Антикодоновая шпилька и Dшпилька образуют двойную спираль из 9 н. о. 3 – Эти две спирали ориентируются друг к другу под прямым углом так, что D петля сближается с Т. Получается «буква L» . 4 – Вершина такой структуры АСконец. На D-спираль у внутреннего угла накладывается перемычка между акцепторным черешком и D-шпилька, часто Vшпилька формируют «ядро» молекулы.
 Гены р. РНК в хромосоме ядрышка отделены друг от друга нетранскрибируемым участком ДНК –спейсер. При соединении с генами РНК-полимеразы (их около 100) веером расходятся от ДНК первичные транскрипты прер. РНК – «елочка» . Верхушка каждой «елочки» - начало транскрипции, конец гена р. РНК – нижняя крона. Транскрипция осуществляется РНК-полимеразой I. l В начале формируются первичные транскрипты генов р. РНК – 45 S-прер-РНК (из 13000 нуклеотидов) – эта молекула перед выходом из ядра подвергается процессингу. Конформационные изменения: 45 S-прер-РНК разрезается на три фрагмента l 28 S(26) – РНК (5000 нуклеотидов) l 18 S(16) – РНК (2000 нуклеотидов) l 5, 8 S(5) – РНК (160 нуклеотидов), l остальная часть ≈6000 нуклеотидов расщепляется в ядре. Каждый из фрагментов приобретает вторичную конформацию. l Химическая модификация – ассоциация с белками. Зрелые р. РНК – это малая и большая субъединица рибосомы. l
Гены р. РНК в хромосоме ядрышка отделены друг от друга нетранскрибируемым участком ДНК –спейсер. При соединении с генами РНК-полимеразы (их около 100) веером расходятся от ДНК первичные транскрипты прер. РНК – «елочка» . Верхушка каждой «елочки» - начало транскрипции, конец гена р. РНК – нижняя крона. Транскрипция осуществляется РНК-полимеразой I. l В начале формируются первичные транскрипты генов р. РНК – 45 S-прер-РНК (из 13000 нуклеотидов) – эта молекула перед выходом из ядра подвергается процессингу. Конформационные изменения: 45 S-прер-РНК разрезается на три фрагмента l 28 S(26) – РНК (5000 нуклеотидов) l 18 S(16) – РНК (2000 нуклеотидов) l 5, 8 S(5) – РНК (160 нуклеотидов), l остальная часть ≈6000 нуклеотидов расщепляется в ядре. Каждый из фрагментов приобретает вторичную конформацию. l Химическая модификация – ассоциация с белками. Зрелые р. РНК – это малая и большая субъединица рибосомы. l

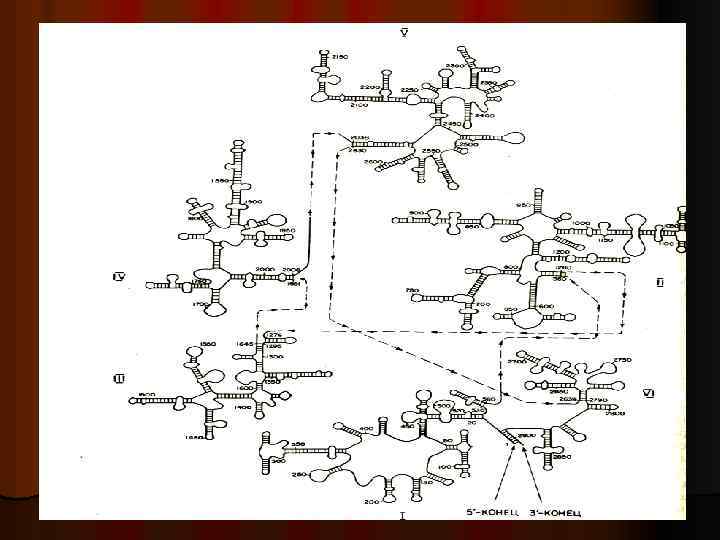
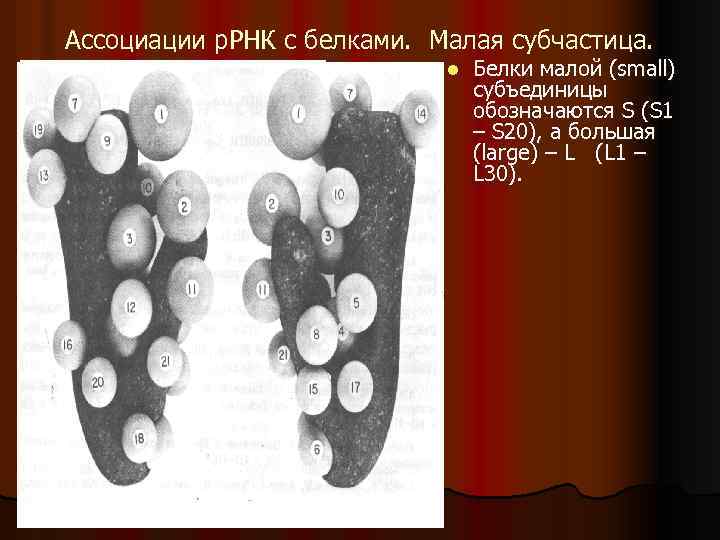 Ассоциации р. РНК с белками. Малая субчастица. l Белки малой (small) субъединицы обозначаются S (S 1 – S 20), а большая (large) – L (L 1 – L 30).
Ассоциации р. РНК с белками. Малая субчастица. l Белки малой (small) субъединицы обозначаются S (S 1 – S 20), а большая (large) – L (L 1 – L 30).
 Сравнение контуров 30 S субчастицы и ее 16 SРНК. головка – тело – боковой выступ (платформа) поперечная борозда (шея), которая отделяет головку от тела. Главные черты вторичной структуры для 16 S являются (как и для других):
Сравнение контуров 30 S субчастицы и ее 16 SРНК. головка – тело – боковой выступ (платформа) поперечная борозда (шея), которая отделяет головку от тела. Главные черты вторичной структуры для 16 S являются (как и для других):
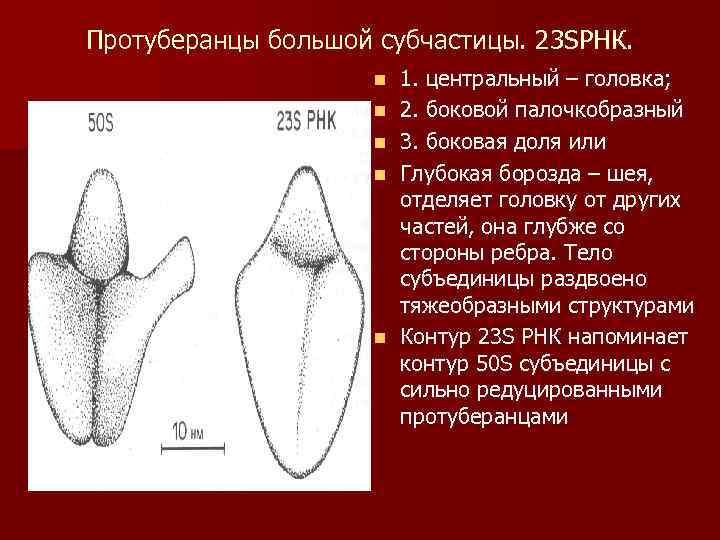 Протуберанцы большой субчастицы. 23 SРНК. n n n 1. центральный – головка; 2. боковой палочкобразный 3. боковая доля или Глубокая борозда – шея, отделяет головку от других частей, она глубже со стороны ребра. Тело субъединицы раздвоено тяжеобразными структурами Контур 23 S РНК напоминает контур 50 S субъединицы с сильно редуцированными протуберанцами
Протуберанцы большой субчастицы. 23 SРНК. n n n 1. центральный – головка; 2. боковой палочкобразный 3. боковая доля или Глубокая борозда – шея, отделяет головку от других частей, она глубже со стороны ребра. Тело субъединицы раздвоено тяжеобразными структурами Контур 23 S РНК напоминает контур 50 S субъединицы с сильно редуцированными протуберанцами
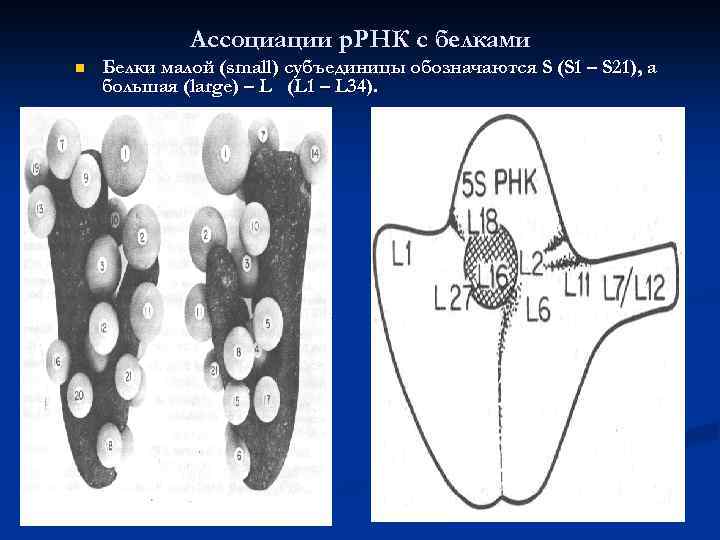 Ассоциации р. РНК с белками n Белки малой (small) субъединицы обозначаются S (S 1 – S 21), а большая (large) – L (L 1 – L 34).
Ассоциации р. РНК с белками n Белки малой (small) субъединицы обозначаются S (S 1 – S 21), а большая (large) – L (L 1 – L 34).
 Формирование рабочей рибосомы l Две субъединицы объединяются в полную рибосому. Контактирующей стороной у 50 S является сторона, когда головка сверху, а стержень справа. Ассоциация происходит «головка к головке, выступ к выступу» . 30 S закрывает лишь часть 50 S стороны, в районе основания стержня участки открыты (глаз).
Формирование рабочей рибосомы l Две субъединицы объединяются в полную рибосому. Контактирующей стороной у 50 S является сторона, когда головка сверху, а стержень справа. Ассоциация происходит «головка к головке, выступ к выступу» . 30 S закрывает лишь часть 50 S стороны, в районе основания стержня участки открыты (глаз).
 Структурно-функциональные карманы рибосом. 1. борозда, которая разделяет две субъединицы, она имеет расширение – глаз. Т. е. между субъединицами есть полость, именно здесь располагаются молекулы пептидил – т. РНК и, образуется т. РНК связывающий центр рибосомы; 2. в малой субъединице область шеи – это центр, где располагается участок связывания м. РНК и через него м. РНК протягивается; 3. в шее большой субъединицы располагается каталитический центр (пептидилтрансферазный); 4. Каждая м. РНК в рибосоме взаимодействует антикодоном а. а. т-РНК , а акцепторным концом с пептидил-трансферазным центром. Антикодон сидит на шее малой субъединицы, а акцепторный участок – в шее большой субъединицы; 5. подвижный палочкообразный выступ большой субъединицы – площадка – это место посадки аминоацил-т. РНК + EF 1. Палочкообразный выступ взаимодействует с EF 1 и ориентируется перпендикулярно с образованием кармана между большой и малой субъединицей. Этот карман принимает другой белок – EF 2 (который нужен для транслокации рибосомы); 6. «боковое ребро» - большой субъединицы и тело малой субъединицы участвуют в ассоциации субъединиц в «рабочую» рибосому
Структурно-функциональные карманы рибосом. 1. борозда, которая разделяет две субъединицы, она имеет расширение – глаз. Т. е. между субъединицами есть полость, именно здесь располагаются молекулы пептидил – т. РНК и, образуется т. РНК связывающий центр рибосомы; 2. в малой субъединице область шеи – это центр, где располагается участок связывания м. РНК и через него м. РНК протягивается; 3. в шее большой субъединицы располагается каталитический центр (пептидилтрансферазный); 4. Каждая м. РНК в рибосоме взаимодействует антикодоном а. а. т-РНК , а акцепторным концом с пептидил-трансферазным центром. Антикодон сидит на шее малой субъединицы, а акцепторный участок – в шее большой субъединицы; 5. подвижный палочкообразный выступ большой субъединицы – площадка – это место посадки аминоацил-т. РНК + EF 1. Палочкообразный выступ взаимодействует с EF 1 и ориентируется перпендикулярно с образованием кармана между большой и малой субъединицей. Этот карман принимает другой белок – EF 2 (который нужен для транслокации рибосомы); 6. «боковое ребро» - большой субъединицы и тело малой субъединицы участвуют в ассоциации субъединиц в «рабочую» рибосому
 Процессинг м. РНК включает в себя: 1) кэпирование 5'-конца, заключающееся в присоединении к этому концу м. РНК так называемой шапочки (кэп-структуры), «КЭП» – это модифицированный (N 7 – метелированный) остаток гуанозин-5` – ТФ. У эукариотов есть специальное ферментная система, которая включает гуанилилтрансферазу и метилтрансферазу, они и осуществляют это «копирование» м. РНК. На 5 -`к. чаще располагаются G и A. 3'-к у м. РНК свободен с цис-гликольной группой. 2) полиаденилирование 3'-конца. Около половины м. РНК эукариот полиаденилируются на 3'-конце во время процессинга в клеточном ядре. Сигналом ядерного полиаденилирования 3'-конца служит последовательность AAUAAA, расположенная за 10 -20 нуклеотидов от этого конца. Активация белкового синтеза в развитии сопровождается полиаденилированием этих м. РНК в цитоплазме. Для цитоплазматического полиаденилирования м. РНК должны содержать в 3' -нетранслируемой области наряду с элементом ядерного полиаденилирования дополнительную последовательность - элемент цитоплазматического полиаденилирования. Такой последовательностью у амфибий является (U)6 AUAAAG. Поли(А)-хвост на м. РНК узнается особым поли(А)-связывающим белком, который участвует в инициации трансляции м. РНК по кэп-зависимому механизму. l .
Процессинг м. РНК включает в себя: 1) кэпирование 5'-конца, заключающееся в присоединении к этому концу м. РНК так называемой шапочки (кэп-структуры), «КЭП» – это модифицированный (N 7 – метелированный) остаток гуанозин-5` – ТФ. У эукариотов есть специальное ферментная система, которая включает гуанилилтрансферазу и метилтрансферазу, они и осуществляют это «копирование» м. РНК. На 5 -`к. чаще располагаются G и A. 3'-к у м. РНК свободен с цис-гликольной группой. 2) полиаденилирование 3'-конца. Около половины м. РНК эукариот полиаденилируются на 3'-конце во время процессинга в клеточном ядре. Сигналом ядерного полиаденилирования 3'-конца служит последовательность AAUAAA, расположенная за 10 -20 нуклеотидов от этого конца. Активация белкового синтеза в развитии сопровождается полиаденилированием этих м. РНК в цитоплазме. Для цитоплазматического полиаденилирования м. РНК должны содержать в 3' -нетранслируемой области наряду с элементом ядерного полиаденилирования дополнительную последовательность - элемент цитоплазматического полиаденилирования. Такой последовательностью у амфибий является (U)6 AUAAAG. Поли(А)-хвост на м. РНК узнается особым поли(А)-связывающим белком, который участвует в инициации трансляции м. РНК по кэп-зависимому механизму. l .
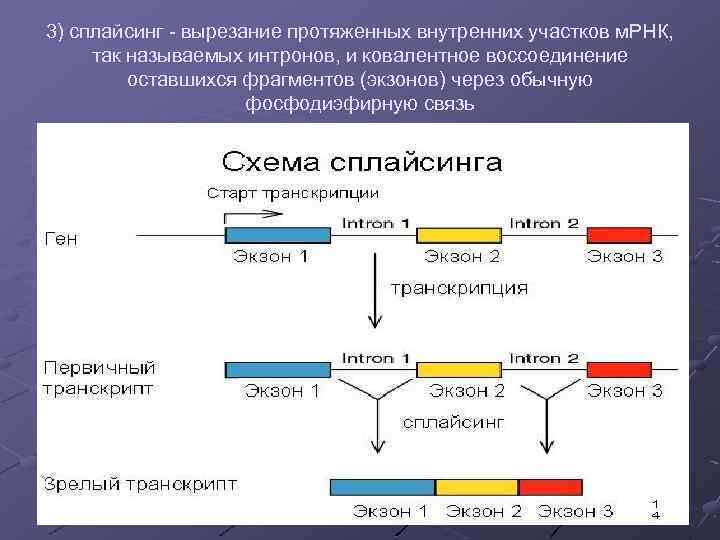 3) сплайсинг - вырезание протяженных внутренних участков м. РНК, так называемых интронов, и ковалентное воссоединение оставшихся фрагментов (экзонов) через обычную фосфодиэфирную связь
3) сплайсинг - вырезание протяженных внутренних участков м. РНК, так называемых интронов, и ковалентное воссоединение оставшихся фрагментов (экзонов) через обычную фосфодиэфирную связь
 Расположение функциональных участков на молекуле м. РНК. 1 -ый кодон на м. РНК должен кодировать метионин, таким инициирующим кодоном является АУГ (реже ГУГ, УУГ и GUG, который соответствует в таблице генетического кода аминокислоте валину. у прокариот). Прежде, чем выйти из ядра м. РНК претерпевает серию ковалентных модификаций: 5' конец РНК (который синтезируется первым в процессе транскрипции) кэпируется, остальная часть РНК растет от 5' к 3' концу до сигнала терминации, фермент А-полимераза присоединяется к 3' концу, чем завершается образование первичного РНК-транскрипта. Этот процесс называется полиаденилирование. Кэпирование и полиаденилирование протекают с участием РНКполимеразы II. Ядро покидает 5% м. РНК, .
Расположение функциональных участков на молекуле м. РНК. 1 -ый кодон на м. РНК должен кодировать метионин, таким инициирующим кодоном является АУГ (реже ГУГ, УУГ и GUG, который соответствует в таблице генетического кода аминокислоте валину. у прокариот). Прежде, чем выйти из ядра м. РНК претерпевает серию ковалентных модификаций: 5' конец РНК (который синтезируется первым в процессе транскрипции) кэпируется, остальная часть РНК растет от 5' к 3' концу до сигнала терминации, фермент А-полимераза присоединяется к 3' концу, чем завершается образование первичного РНК-транскрипта. Этот процесс называется полиаденилирование. Кэпирование и полиаденилирование протекают с участием РНКполимеразы II. Ядро покидает 5% м. РНК, .
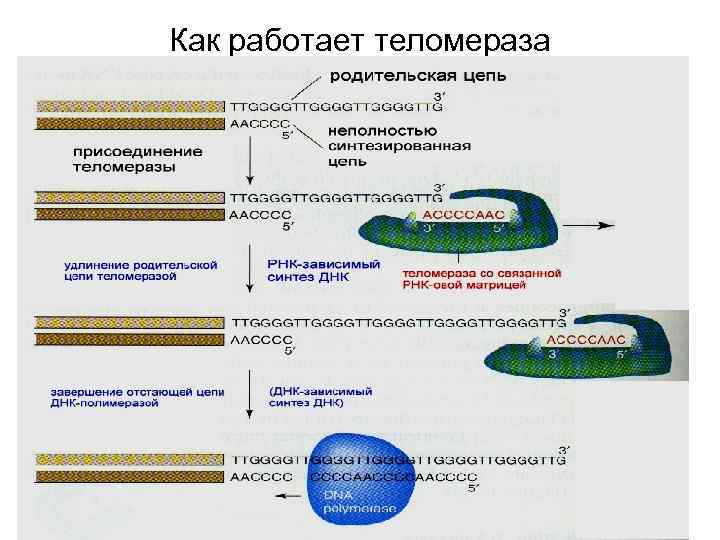 Как работает теломераза
Как работает теломераза
 Проблема кодирования в молекулярной биологии. 1. Г. Гамов предположил, что генетический код является триплетным, то есть три соседних основания полинуклеотидной цепи. Он же поставил вопросы и о других свойствах генетического кода: перекрываемости, запятых между кодонами, вырожденности. 2. В 1961 году Ф. Крик и С. Бреннер экспериментально показали, что делеция (вырезание) одного нуклеотида, может быть скомпенсирована вставкой нуклеотида вблизи делеции. В опытах с делециями и вставками Крик, Барнет, Бреннер и Уотс-Тобин (1961) также подтвердили, что код является триплетным 3. Опыты Г. Виттманна каждое основание РНК входит в состав лишь одного триплета (кодона). 4. Полная расшифровка генетического кода, проведенная М. Ниренбергом и С. Очоа, была закончена к 1966 году. Она показала, что 61 из 64 возможных триплетов м. РНК кодируют одну из двадцати стандартных аминокислот, включающихся в белок. Т. е. генетический код оказался сильно вырожденным, и многие аминокислоты кодируются двумя или более кодонами. Три триплета, не участвующие в кодировании аминокислот, - UAA, UAG и UGA - оказались сигналами на окончание синтеза белка (сигналами терминации).
Проблема кодирования в молекулярной биологии. 1. Г. Гамов предположил, что генетический код является триплетным, то есть три соседних основания полинуклеотидной цепи. Он же поставил вопросы и о других свойствах генетического кода: перекрываемости, запятых между кодонами, вырожденности. 2. В 1961 году Ф. Крик и С. Бреннер экспериментально показали, что делеция (вырезание) одного нуклеотида, может быть скомпенсирована вставкой нуклеотида вблизи делеции. В опытах с делециями и вставками Крик, Барнет, Бреннер и Уотс-Тобин (1961) также подтвердили, что код является триплетным 3. Опыты Г. Виттманна каждое основание РНК входит в состав лишь одного триплета (кодона). 4. Полная расшифровка генетического кода, проведенная М. Ниренбергом и С. Очоа, была закончена к 1966 году. Она показала, что 61 из 64 возможных триплетов м. РНК кодируют одну из двадцати стандартных аминокислот, включающихся в белок. Т. е. генетический код оказался сильно вырожденным, и многие аминокислоты кодируются двумя или более кодонами. Три триплета, не участвующие в кодировании аминокислот, - UAA, UAG и UGA - оказались сигналами на окончание синтеза белка (сигналами терминации).
 Перекодирующие сигналы в м. РНК или второй генетический код. n Иногда инициация с метионина может происходить и на других кодонах: AUA и AUU (кодонах изолейцина), UUG и, возможно, CUG (кодонах лейцина). У эукариот инициация происходит, с первого AUG, однако только в том случае, если этот AUG находится в оптимальном контексте: за два нуклеотида до него обязательно должен находиться пурин (A или G), а непосредственно за ним должен следовать G. На эффективность инициации у эукариот определенное влияние могут оказывать также нуклеотиды и в других положениях вблизи инициирующего кодона. Самым оптимальным для узнавания инициирующего кодона у млекопитающих считается следующее его окружение: GCCGCCA / GCCAUGGA / CU. n Терминирующие кодоны узнаются специальными белками - факторами терминации. Надежность узнавания этих триплетов не столь высока, и иногда терминирующий триплет может прочитываться как кодон аминокислоты. Для повышения надежности процесса терминации терминирующие кодоны обычно дублируются. Первым при этом, как правило, выступает кодон UAA (основной терминирующий триплет), а вслед за ним на очень близком расстоянии в той же рамке считывания следует один из запасных терминирующих триплетов - UAG или UGA.
Перекодирующие сигналы в м. РНК или второй генетический код. n Иногда инициация с метионина может происходить и на других кодонах: AUA и AUU (кодонах изолейцина), UUG и, возможно, CUG (кодонах лейцина). У эукариот инициация происходит, с первого AUG, однако только в том случае, если этот AUG находится в оптимальном контексте: за два нуклеотида до него обязательно должен находиться пурин (A или G), а непосредственно за ним должен следовать G. На эффективность инициации у эукариот определенное влияние могут оказывать также нуклеотиды и в других положениях вблизи инициирующего кодона. Самым оптимальным для узнавания инициирующего кодона у млекопитающих считается следующее его окружение: GCCGCCA / GCCAUGGA / CU. n Терминирующие кодоны узнаются специальными белками - факторами терминации. Надежность узнавания этих триплетов не столь высока, и иногда терминирующий триплет может прочитываться как кодон аминокислоты. Для повышения надежности процесса терминации терминирующие кодоны обычно дублируются. Первым при этом, как правило, выступает кодон UAA (основной терминирующий триплет), а вслед за ним на очень близком расстоянии в той же рамке считывания следует один из запасных терминирующих триплетов - UAG или UGA.
 Кодовый словарь
Кодовый словарь
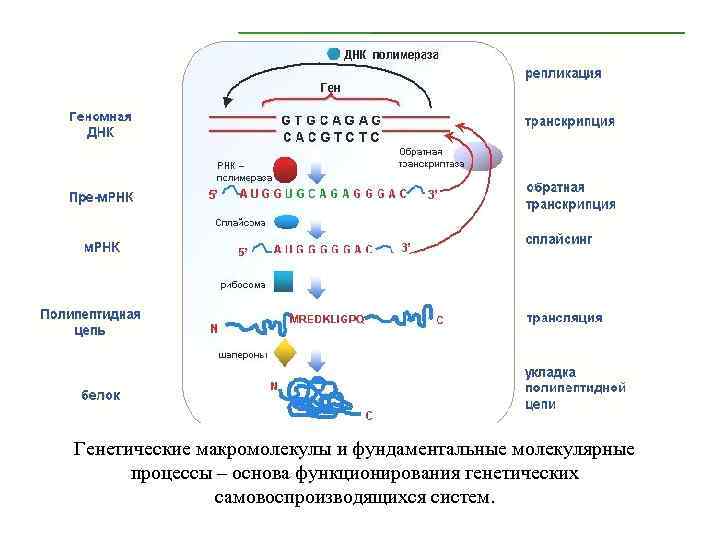 Генетические макромолекулы и фундаментальные молекулярные процессы – основа функционирования генетических самовоспроизводящихся систем.
Генетические макромолекулы и фундаментальные молекулярные процессы – основа функционирования генетических самовоспроизводящихся систем.


