ХИМИЧЕСКАЯ КИНЕТИКА, ХИМИЧЕСКОЕ РАВНОВЕСИЕ.ppt
- Количество слайдов: 41
 ХИМИЧЕСКАЯ КИНЕТИКА, ХИМИЧЕСКОЕ РАВНОВЕСИЕ • Раздел химии, который изучает скорость и механизм химических превращений, называется химической кинетикой. • Реакции между веществами, которые находятся в разных агрегатных состояниях или в разных фазах, называются гетерогенными. • В гомогенных реакциях исходные вещества могут находиться в одинаковом агрегатном состоянии (в одной фазе).
ХИМИЧЕСКАЯ КИНЕТИКА, ХИМИЧЕСКОЕ РАВНОВЕСИЕ • Раздел химии, который изучает скорость и механизм химических превращений, называется химической кинетикой. • Реакции между веществами, которые находятся в разных агрегатных состояниях или в разных фазах, называются гетерогенными. • В гомогенных реакциях исходные вещества могут находиться в одинаковом агрегатном состоянии (в одной фазе).
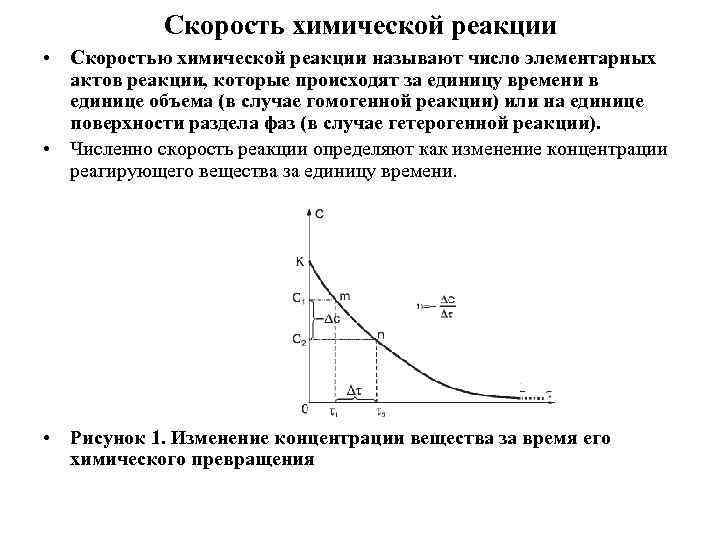 Скорость химической реакции • Скоростью химической реакции называют число элементарных актов реакции, которые происходят за единицу времени в единице объема (в случае гомогенной реакции) или на единице поверхности раздела фаз (в случае гетерогенной реакции). • Численно скорость реакции определяют как изменение концентрации реагирующего вещества за единицу времени. • Рисунок 1. Изменение концентрации вещества за время его химического превращения
Скорость химической реакции • Скоростью химической реакции называют число элементарных актов реакции, которые происходят за единицу времени в единице объема (в случае гомогенной реакции) или на единице поверхности раздела фаз (в случае гетерогенной реакции). • Численно скорость реакции определяют как изменение концентрации реагирующего вещества за единицу времени. • Рисунок 1. Изменение концентрации вещества за время его химического превращения
 • Средняя скорость химической реакции определяется по формуле: • Если отнести изменение концентрации к бесконечно малому промежутку времени, то возможно определить мгновенную скорость реакции V на данный момент как производную от концентрации от времени: • Изменение скорости химической реакции можно наблюдать по изменению какого либо свойства системы: если одно из исходных веществ или продуктов реакции газ – по изменению объема либо давления в закрытой посудине при постоянной температуре. Иногда изменение скорости можно наблюдать по появлению осадка, изменением окраски, электропроводности и т. д.
• Средняя скорость химической реакции определяется по формуле: • Если отнести изменение концентрации к бесконечно малому промежутку времени, то возможно определить мгновенную скорость реакции V на данный момент как производную от концентрации от времени: • Изменение скорости химической реакции можно наблюдать по изменению какого либо свойства системы: если одно из исходных веществ или продуктов реакции газ – по изменению объема либо давления в закрытой посудине при постоянной температуре. Иногда изменение скорости можно наблюдать по появлению осадка, изменением окраски, электропроводности и т. д.
 • Скорость химической реакции зависит от ряда факторов: природы реагирующих веществ, концентрации, температуры, поверхности соприкосновения (для гетеро генных реакций), наличия катализаторов, освещения для фотохимических реакций.
• Скорость химической реакции зависит от ряда факторов: природы реагирующих веществ, концентрации, температуры, поверхности соприкосновения (для гетеро генных реакций), наличия катализаторов, освещения для фотохимических реакций.
 Зависимость скорости реакции от концентрации реагирующих веществ Необходимым условием возможности взаимодействия между двумя частичками (атомами, молекулами, ионами) является их взаимное столкновения (сближение до такого расстояния, на котором электроны и атомы одной частички попадают в сферу действия электрических полей другой частички). Поэтому скорость гомогенных реакций зависит от числа столкновений частичек за единицу времени, а число столкновений пропорционально концентрации реагирующих веществ. Закон действующих масс, (Гульдберг и Ваaге): Скорость химической реакции при постоянной температуре прямо пропорциональна произведению концентраций реагирующих веществ в степени их стехиометрических коэффициентов в уравнении реакции.
Зависимость скорости реакции от концентрации реагирующих веществ Необходимым условием возможности взаимодействия между двумя частичками (атомами, молекулами, ионами) является их взаимное столкновения (сближение до такого расстояния, на котором электроны и атомы одной частички попадают в сферу действия электрических полей другой частички). Поэтому скорость гомогенных реакций зависит от числа столкновений частичек за единицу времени, а число столкновений пропорционально концентрации реагирующих веществ. Закон действующих масс, (Гульдберг и Ваaге): Скорость химической реакции при постоянной температуре прямо пропорциональна произведению концентраций реагирующих веществ в степени их стехиометрических коэффициентов в уравнении реакции.
 Следовательно, скорость реакции Выражается соотношением: Где СА и СВ – концентрации веществ А и В, моль/л; к – коэффициент пропорциональности; для каждой реакции при постоянной температуре он является постоянной величиной, которая называют константой скорости химической реакции. Величина к численно равна скорости реакции при условии, что концентрации реагирующих веществ или их произведение равняются единице.
Следовательно, скорость реакции Выражается соотношением: Где СА и СВ – концентрации веществ А и В, моль/л; к – коэффициент пропорциональности; для каждой реакции при постоянной температуре он является постоянной величиной, которая называют константой скорости химической реакции. Величина к численно равна скорости реакции при условии, что концентрации реагирующих веществ или их произведение равняются единице.
![Для реакции V=k[H 2] • [NO]2 Для реакции V=k[N 2] • [H 2]3 Закон Для реакции V=k[H 2] • [NO]2 Для реакции V=k[N 2] • [H 2]3 Закон](https://present5.com/presentation/3/105405628_132624044.pdf-img/105405628_132624044.pdf-7.jpg) Для реакции V=k[H 2] • [NO]2 Для реакции V=k[N 2] • [H 2]3 Закон действующих масс для гетерогенных реакций не учитывает концентрации твердого вещества, потому что интенсивность взаимодействия зависит от величины площади соприкосновения. Концентрация твердого вещества принимается за постоянную величину, которая входит в величину константы скорости, например:
Для реакции V=k[H 2] • [NO]2 Для реакции V=k[N 2] • [H 2]3 Закон действующих масс для гетерогенных реакций не учитывает концентрации твердого вещества, потому что интенсивность взаимодействия зависит от величины площади соприкосновения. Концентрация твердого вещества принимается за постоянную величину, которая входит в величину константы скорости, например:
 • Отметим специфическую особенность гетерогенных систем, где скорость реакции зависит от величины поверхности твердой фазы, и для увеличения скорости реакции нужно измельчать твердое вещество и перемешивать его. Так, уголь в топках современных котлов сжигают в виде пыли, вдуваемой в топку котла при помощи подогретого воздуха. • При математической записи закона действующих масс влияние поверхности твердой фазы на скорость реакции учитывается через величину константы скорости реакции. • Например, для реакции
• Отметим специфическую особенность гетерогенных систем, где скорость реакции зависит от величины поверхности твердой фазы, и для увеличения скорости реакции нужно измельчать твердое вещество и перемешивать его. Так, уголь в топках современных котлов сжигают в виде пыли, вдуваемой в топку котла при помощи подогретого воздуха. • При математической записи закона действующих масс влияние поверхности твердой фазы на скорость реакции учитывается через величину константы скорости реакции. • Например, для реакции
 Молекулярность и порядок реакции • Молекулярность реакции определяется числом молекул, которые принимают участие в элементарном акте химического взаимодействия. • Классифицируют на мономолекулярные, например • бимолекулярные, например • и тримолекулярные
Молекулярность и порядок реакции • Молекулярность реакции определяется числом молекул, которые принимают участие в элементарном акте химического взаимодействия. • Классифицируют на мономолекулярные, например • бимолекулярные, например • и тримолекулярные
 Поскольку одновременное столкновение даже 3 х молекул маловероятно, то реакции, в которых принимают участие больше трех молекул, практически неизвестны, и такие реакции нужно рассматривать как ряд последовательных стадий. Порядок реакции определяют суммой показателей степеней концентраций в математическом выражении закона действующих масс. Чаще всего молекулярность и порядок реакции совпадают, но не всегда, например: Оно характеризуется кинетическим уравнением первого порядка.
Поскольку одновременное столкновение даже 3 х молекул маловероятно, то реакции, в которых принимают участие больше трех молекул, практически неизвестны, и такие реакции нужно рассматривать как ряд последовательных стадий. Порядок реакции определяют суммой показателей степеней концентраций в математическом выражении закона действующих масс. Чаще всего молекулярность и порядок реакции совпадают, но не всегда, например: Оно характеризуется кинетическим уравнением первого порядка.
 Влияние температуры на скорость реакции Правило Вант-Гоффа: С повышением температуры на каждые 10ºС скорость гомогенной реакции увеличивается в 2 -4 раза: Где Vt 1 и Vt 2 скорости реакций соответственно при начальной и конечной температурах, γ – температурный коэффициент скорости реакции. Зависимость константы скорости реакции от температуры более точно выражает уравнение Аррениуса: Где Z – общее число столкновений между молекулами в секунду; Т – температура; к – константа; R – газовая постоянная (8, 314 Дж/(моль • К)); е – основание натуральных логарифмов; Еакт – энергия активации, к. Дж/моль.
Влияние температуры на скорость реакции Правило Вант-Гоффа: С повышением температуры на каждые 10ºС скорость гомогенной реакции увеличивается в 2 -4 раза: Где Vt 1 и Vt 2 скорости реакций соответственно при начальной и конечной температурах, γ – температурный коэффициент скорости реакции. Зависимость константы скорости реакции от температуры более точно выражает уравнение Аррениуса: Где Z – общее число столкновений между молекулами в секунду; Т – температура; к – константа; R – газовая постоянная (8, 314 Дж/(моль • К)); е – основание натуральных логарифмов; Еакт – энергия активации, к. Дж/моль.
 Теория активации • Для осуществления химической реакции необходимо столкновение реагирующих частиц, при котором стает возможным перераспределение электронной плотности и возникновение новых связей. Но не каждое столкновение приводит к химическому взаимодействию. Результативными являются столкновения, которые имеют избыток энергии (активными). Избыточная энергия, которая необходима для преодоления сил отталкивания (энергетического барьера), который возникает между электронными оболочками реагирующих частиц, называется энергией активации. Ее выражают в к. Дж/моль. • При повышении температуры энергия системы возрастает, соответственно возрастает и число активных частиц. Активные частицы (активированные комплексы) принимают участие в перераспределении химических связей. Они менее стойкие, чем исходные вещества или продукты реакции.
Теория активации • Для осуществления химической реакции необходимо столкновение реагирующих частиц, при котором стает возможным перераспределение электронной плотности и возникновение новых связей. Но не каждое столкновение приводит к химическому взаимодействию. Результативными являются столкновения, которые имеют избыток энергии (активными). Избыточная энергия, которая необходима для преодоления сил отталкивания (энергетического барьера), который возникает между электронными оболочками реагирующих частиц, называется энергией активации. Ее выражают в к. Дж/моль. • При повышении температуры энергия системы возрастает, соответственно возрастает и число активных частиц. Активные частицы (активированные комплексы) принимают участие в перераспределении химических связей. Они менее стойкие, чем исходные вещества или продукты реакции.
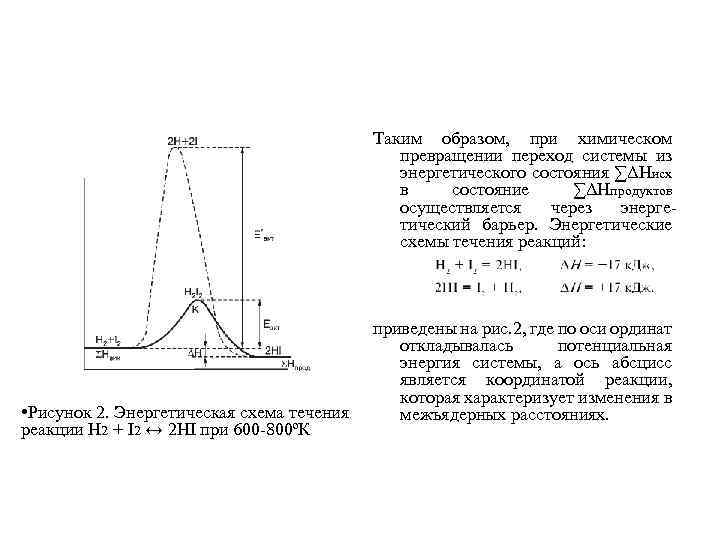 Таким образом, при химическом превращении переход системы из энергетического состояния ∑ΔНисх в состояние ∑ΔНпродуктов осуществляется через энерге тический барьер. Энергетические схемы течения реакций: • Рисунок 2. Энергетическая схема течения реакции H 2 + I 2 ↔ 2 HI при 600 800ºК приведены на рис. 2, где по оси ординат откладывалась потенциальная энергия системы, а ось абсцисс является координатой реакции, которая характеризует изменения в межъядерных расстояниях.
Таким образом, при химическом превращении переход системы из энергетического состояния ∑ΔНисх в состояние ∑ΔНпродуктов осуществляется через энерге тический барьер. Энергетические схемы течения реакций: • Рисунок 2. Энергетическая схема течения реакции H 2 + I 2 ↔ 2 HI при 600 800ºК приведены на рис. 2, где по оси ординат откладывалась потенциальная энергия системы, а ось абсцисс является координатой реакции, которая характеризует изменения в межъядерных расстояниях.
 Если реакция экзотермическая, то общий запас энергии продуктов реакции меньше, чем исходных веществ. Соответственно, вследствие такой реакции система переходит на более низкий энергетический уровень. Разность начального и конечного энергетического состояний системы (∑ΔНисх ∑ΔНпродуктов) и составляет тепловой эффект реакции. Уровень К определяет тот наименьший запас энергии, которым должны характеризоваться молекулы, чтобы их столкновения могли приводить к химической реакции. Разность между этим и исходным уровнями энергии и есть энергия активации реакции. Рис. 3. Схема течения реакции H 2 + I 2 ↔ 2 HI
Если реакция экзотермическая, то общий запас энергии продуктов реакции меньше, чем исходных веществ. Соответственно, вследствие такой реакции система переходит на более низкий энергетический уровень. Разность начального и конечного энергетического состояний системы (∑ΔНисх ∑ΔНпродуктов) и составляет тепловой эффект реакции. Уровень К определяет тот наименьший запас энергии, которым должны характеризоваться молекулы, чтобы их столкновения могли приводить к химической реакции. Разность между этим и исходным уровнями энергии и есть энергия активации реакции. Рис. 3. Схема течения реакции H 2 + I 2 ↔ 2 HI
 Итак, схема течения реакции между водородом и иодом имеет вид: исходные вещества – промежуточное соединение – конечные продукты. Активные молекулы Н 2 и I 2 при столкновении объединяются в активированный комплекс Н 2…I 2, в котором одновременно с разрывом связей Н Н и I I образуются связи Н I. Вследствие образования активированного комплекса энергия активации реакции (168 к. Дж/моль) оказывается значительно меньше, чем энергия, которая необходима для полного разрыва связей Н Н и I I. Поэтому для совершения большинства реакций каждая пара частиц должна пройти через конфигурацию, промежуточную между исходной и конечной. Такую конфигурацию называют активированным комплексом, а энергию, которая необходима для превращения реагирующих частиц в состояние активированного комплекса – энергией активации.
Итак, схема течения реакции между водородом и иодом имеет вид: исходные вещества – промежуточное соединение – конечные продукты. Активные молекулы Н 2 и I 2 при столкновении объединяются в активированный комплекс Н 2…I 2, в котором одновременно с разрывом связей Н Н и I I образуются связи Н I. Вследствие образования активированного комплекса энергия активации реакции (168 к. Дж/моль) оказывается значительно меньше, чем энергия, которая необходима для полного разрыва связей Н Н и I I. Поэтому для совершения большинства реакций каждая пара частиц должна пройти через конфигурацию, промежуточную между исходной и конечной. Такую конфигурацию называют активированным комплексом, а энергию, которая необходима для превращения реагирующих частиц в состояние активированного комплекса – энергией активации.
 Радикальные реакции проходят через проме жуточное образование свободных радикалов и атомов. Свободными радикалами являются ча стички, у которых есть неспаренные электроны. Их можна представить себе как обломки молекул. Свободными радикалами могут быть атомы (Н • , Cl • , Br • ), а также некоторые молекулы (NO, NO 2). Свободные радикалы чрезвычайно реакционно способны. Реакции между ними протекают по цепному механизму.
Радикальные реакции проходят через проме жуточное образование свободных радикалов и атомов. Свободными радикалами являются ча стички, у которых есть неспаренные электроны. Их можна представить себе как обломки молекул. Свободными радикалами могут быть атомы (Н • , Cl • , Br • ), а также некоторые молекулы (NO, NO 2). Свободные радикалы чрезвычайно реакционно способны. Реакции между ними протекают по цепному механизму.
 Цепные реакции характеризуются появлением в системе активированной частички (радикала), которая обусловливает последовательное взаимодействие большого количества реагирующих веществ. Образование свободных радикалов происходит при нагревании, освещении, под действием рентгеновского излучения, электрическом разряде. Например, цепной является реакция водорода и хлора с образованием хлористого водорода:
Цепные реакции характеризуются появлением в системе активированной частички (радикала), которая обусловливает последовательное взаимодействие большого количества реагирующих веществ. Образование свободных радикалов происходит при нагревании, освещении, под действием рентгеновского излучения, электрическом разряде. Например, цепной является реакция водорода и хлора с образованием хлористого водорода:
 Цепные реакции состоят из трех стадий: зарождения, развития и обрыва цепи. Реакция взаимодействия водорода с хлором инициируется действием света. Сначала под действием кванта света молекула Cl 2 распадается на атомы хлора (зарождение цепи): Образованные атом хлора легко взаимодействуют с молекулами водорода: Атом водорода, в свою очередь, легко взаимодействует с молекулой хлора: Затем элементарные акты реакции повторяются, формируется ряд процессов, которые чередуются – цепочка реакций (развитие цепи):
Цепные реакции состоят из трех стадий: зарождения, развития и обрыва цепи. Реакция взаимодействия водорода с хлором инициируется действием света. Сначала под действием кванта света молекула Cl 2 распадается на атомы хлора (зарождение цепи): Образованные атом хлора легко взаимодействуют с молекулами водорода: Атом водорода, в свою очередь, легко взаимодействует с молекулой хлора: Затем элементарные акты реакции повторяются, формируется ряд процессов, которые чередуются – цепочка реакций (развитие цепи):
 Поглощение 1 кванта света приводит к образованию около 100 000 молекул хлористого водорода. Заканчивается цепочка реакций обрывом цепи, столкновением двух свободных радикалов: Обрыв цепи происходит также при взаимодействии радикалов с какими нибудь примесями или сталкиваются со стенками посудины. Образование хлороводорода – это неразветвленный тип цепных реакций. Второй тип цепных реакций – разветвленные цепные реакции: взаимодействие свободного радикала с молекулой исходного вещества приводит к образованию двух или более свободных радикалов. Один из них продолжает цепь, а остальные начинают новые цепи.
Поглощение 1 кванта света приводит к образованию около 100 000 молекул хлористого водорода. Заканчивается цепочка реакций обрывом цепи, столкновением двух свободных радикалов: Обрыв цепи происходит также при взаимодействии радикалов с какими нибудь примесями или сталкиваются со стенками посудины. Образование хлороводорода – это неразветвленный тип цепных реакций. Второй тип цепных реакций – разветвленные цепные реакции: взаимодействие свободного радикала с молекулой исходного вещества приводит к образованию двух или более свободных радикалов. Один из них продолжает цепь, а остальные начинают новые цепи.
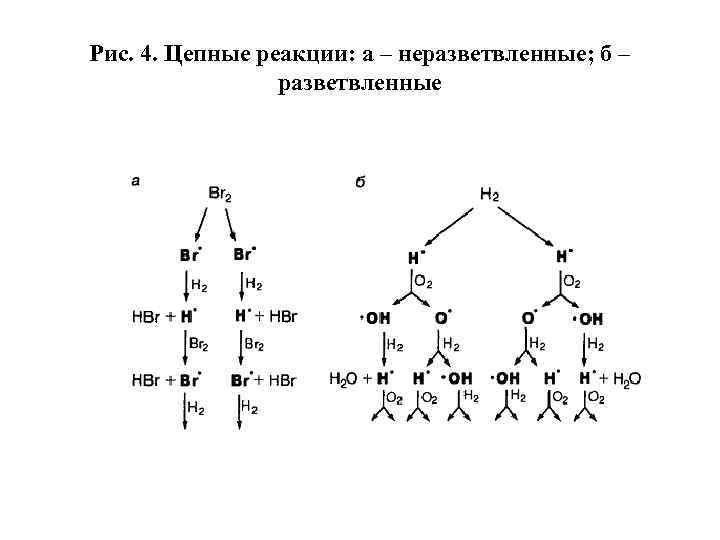 Рис. 4. Цепные реакции: а – неразветвленные; б – разветвленные
Рис. 4. Цепные реакции: а – неразветвленные; б – разветвленные
 К разветвленным цепным реакциям принадлежит реакция окисления водорода кислородом с образованием воды. В смеси водорода с кислородом при нагревании или электрическом разряде начинается реакция: А потом цепь разветвляется: Радикалы, которые образуются в двух первых реакциях, обеспечивают развитие неразветвленной цепи. Атом кислорода, который имеет два неспаренных электрона, образует две дополнительные цепи радикалами • ОН и • О • или • ОН и • Н, которые начинают ветвление. Такое быстрое образование радикалов может привести к взрыву. Цепные реакции очень распространены. По цепному механизму идет большинство реакций окисления углеводородов, процессы полимеризации, реакции получения альдегидов, спиртов, кислот. Особенно важны цепные реакции в биологических процессах.
К разветвленным цепным реакциям принадлежит реакция окисления водорода кислородом с образованием воды. В смеси водорода с кислородом при нагревании или электрическом разряде начинается реакция: А потом цепь разветвляется: Радикалы, которые образуются в двух первых реакциях, обеспечивают развитие неразветвленной цепи. Атом кислорода, который имеет два неспаренных электрона, образует две дополнительные цепи радикалами • ОН и • О • или • ОН и • Н, которые начинают ветвление. Такое быстрое образование радикалов может привести к взрыву. Цепные реакции очень распространены. По цепному механизму идет большинство реакций окисления углеводородов, процессы полимеризации, реакции получения альдегидов, спиртов, кислот. Особенно важны цепные реакции в биологических процессах.
 Катализ Изменение скорости химической реакции в присутствии особых веществ – катализаторов, называют катализом. Катализаторы – это вещества, которые изменяют скорость химической реакции, но сами вследствие реакции остаются неизменными. Катализаторы чаще всего ускоряют химическую реакцию (позитивный катализ). Катализаторы, которые замедляют скорость химической реакции, называются ингибиторами (негативный катализ). Катализ может быть гомогенным и гетерогенным. В первом случае реагирующие вещества и катализатор находятся в одной фазе (газ, раствор), во втором – в разных (твердое вещество в растворе либо газе).
Катализ Изменение скорости химической реакции в присутствии особых веществ – катализаторов, называют катализом. Катализаторы – это вещества, которые изменяют скорость химической реакции, но сами вследствие реакции остаются неизменными. Катализаторы чаще всего ускоряют химическую реакцию (позитивный катализ). Катализаторы, которые замедляют скорость химической реакции, называются ингибиторами (негативный катализ). Катализ может быть гомогенным и гетерогенным. В первом случае реагирующие вещества и катализатор находятся в одной фазе (газ, раствор), во втором – в разных (твердое вещество в растворе либо газе).
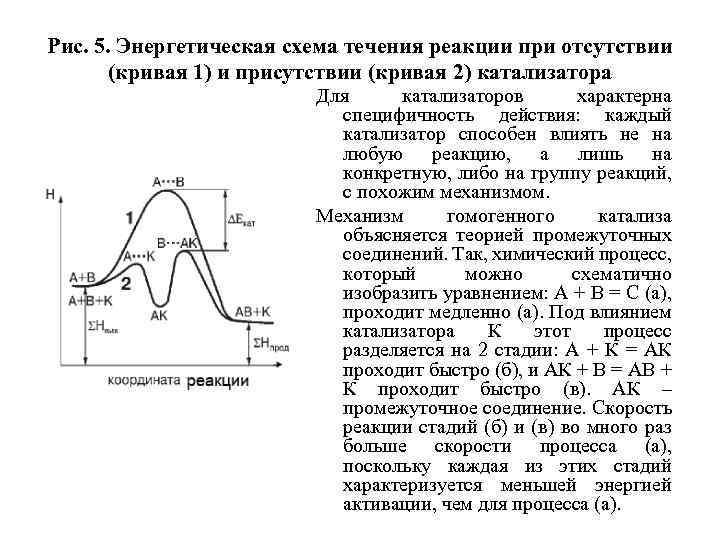 Рис. 5. Энергетическая схема течения реакции при отсутствии (кривая 1) и присутствии (кривая 2) катализатора Для катализаторов характерна специфичность действия: каждый катализатор способен влиять не на любую реакцию, а лишь на конкретную, либо на группу реакций, с похожим механизмом. Механизм гомогенного катализа объясняется теорией промежуточных соединений. Так, химический процесс, который можно схематично изобразить уравнением: А + В = С (а), проходит медленно (а). Под влиянием катализатора К этот процесс разделяется на 2 стадии: А + К = АК проходит быстро (б), и АК + В = АВ + К проходит быстро (в). АК – промежуточное соединение. Скорость реакции стадий (б) и (в) во много раз больше скорости процесса (а), поскольку каждая из этих стадий характеризуется меньшей энергией активации, чем для процесса (а).
Рис. 5. Энергетическая схема течения реакции при отсутствии (кривая 1) и присутствии (кривая 2) катализатора Для катализаторов характерна специфичность действия: каждый катализатор способен влиять не на любую реакцию, а лишь на конкретную, либо на группу реакций, с похожим механизмом. Механизм гомогенного катализа объясняется теорией промежуточных соединений. Так, химический процесс, который можно схематично изобразить уравнением: А + В = С (а), проходит медленно (а). Под влиянием катализатора К этот процесс разделяется на 2 стадии: А + К = АК проходит быстро (б), и АК + В = АВ + К проходит быстро (в). АК – промежуточное соединение. Скорость реакции стадий (б) и (в) во много раз больше скорости процесса (а), поскольку каждая из этих стадий характеризуется меньшей энергией активации, чем для процесса (а).
 Величина ΔЕкат указывает на снижение энергии активации химической реакции под влиянием катализатора. Примером гомогенного катализа может служить гомогенная реакция окисления SO 2 до SO 3 кислородом в присутствии катализатора – оксида азота(II). Без катализатора диоксид серы, образующийся, в частности, как примесь при сгорании угля, очень медленно окисляется кислородом, и поэтому долго сохраняется в атмосфере. При производстве серной кислоты камерным способом процесс окисления диоксида серы до триоксида катализируется оксидом азота(П), который открывает для реакции новый путь, не включающий медленной стадии взаимодействия диоксида серы с молекулярным кислородом: NO + O 2 = NO 2 SO 2 + NO 2 = S 03 + NO
Величина ΔЕкат указывает на снижение энергии активации химической реакции под влиянием катализатора. Примером гомогенного катализа может служить гомогенная реакция окисления SO 2 до SO 3 кислородом в присутствии катализатора – оксида азота(II). Без катализатора диоксид серы, образующийся, в частности, как примесь при сгорании угля, очень медленно окисляется кислородом, и поэтому долго сохраняется в атмосфере. При производстве серной кислоты камерным способом процесс окисления диоксида серы до триоксида катализируется оксидом азота(П), который открывает для реакции новый путь, не включающий медленной стадии взаимодействия диоксида серы с молекулярным кислородом: NO + O 2 = NO 2 SO 2 + NO 2 = S 03 + NO
 Наиболее распространенными катализаторами жидкофазных реакций являются кислоты и основания, комплексы переходных металлов и биологические катализаторы (ферменты). Примером высокоселективного и наиболее эффективного ка тализа может служить ферментативный катализ. Ферменты катализируют почти все физиологически важные реакции, которые в присутствии ферментов быстро идут в мягких условиях при невысокой температуре. Многие ферменты выделены из природных соединений в индивидуальном состоянии, все они представляют сложные полимерные соединения — белки и комплексы белков с низкомолекулярными соединениями. Полимерные молекулы ферментов имеют размеры коллоидных частиц, поэтому их иногда относят к микрогетерогенным катализаторам, занимающим промежуточное положение между гомогенными и гетерогенными катализаторами.
Наиболее распространенными катализаторами жидкофазных реакций являются кислоты и основания, комплексы переходных металлов и биологические катализаторы (ферменты). Примером высокоселективного и наиболее эффективного ка тализа может служить ферментативный катализ. Ферменты катализируют почти все физиологически важные реакции, которые в присутствии ферментов быстро идут в мягких условиях при невысокой температуре. Многие ферменты выделены из природных соединений в индивидуальном состоянии, все они представляют сложные полимерные соединения — белки и комплексы белков с низкомолекулярными соединениями. Полимерные молекулы ферментов имеют размеры коллоидных частиц, поэтому их иногда относят к микрогетерогенным катализаторам, занимающим промежуточное положение между гомогенными и гетерогенными катализаторами.
 Механизмы ферментативных реакций чрезвычайно сложны, причем трудности в их изучении усугубляются отсутствием точных сведений о структуре большинства ферментов. В огромной полимерной моле куле фермента имеется несколько различных активных центров, кото рые могут взаимодействовать с молекулами исходного вещества (или субстрата, как принято его называть в учении о катализе). Ранее считалось, что высокая специфичность действия фермента объясня ется точным стереохимическим и электронным соответствием актив ных центров ферментов к молекул субстрата так называемая концеп ция "ключа и замка". Позднее оказалось, что механизм действия ферментов более сложен и гибок. В случае гетерогенного катализа реакционная смесь и катализатор образуют две фазы. Как правило, катализатор – твердое вещество, а реагирующие вещества – газы либо жидкости. Гетерогенные катали тические реакции происходят на поверхности катализатора. При этом очень большое значение имеет поверхность соприкосновения реакци онной смеси с катализатором. Поэтому твердые катализаторы обычно используются в измельченном состоянии, чтобы площадь соприкос новения между ними и реагирующими веществами была как можно больше. В неорганическом гетерогенном катализе катализаторами являются губчатая или измельченная платина, соли меди, никеля, ртути, оксида ванадия (V), алюминия, железа(III).
Механизмы ферментативных реакций чрезвычайно сложны, причем трудности в их изучении усугубляются отсутствием точных сведений о структуре большинства ферментов. В огромной полимерной моле куле фермента имеется несколько различных активных центров, кото рые могут взаимодействовать с молекулами исходного вещества (или субстрата, как принято его называть в учении о катализе). Ранее считалось, что высокая специфичность действия фермента объясня ется точным стереохимическим и электронным соответствием актив ных центров ферментов к молекул субстрата так называемая концеп ция "ключа и замка". Позднее оказалось, что механизм действия ферментов более сложен и гибок. В случае гетерогенного катализа реакционная смесь и катализатор образуют две фазы. Как правило, катализатор – твердое вещество, а реагирующие вещества – газы либо жидкости. Гетерогенные катали тические реакции происходят на поверхности катализатора. При этом очень большое значение имеет поверхность соприкосновения реакци онной смеси с катализатором. Поэтому твердые катализаторы обычно используются в измельченном состоянии, чтобы площадь соприкос новения между ними и реагирующими веществами была как можно больше. В неорганическом гетерогенном катализе катализаторами являются губчатая или измельченная платина, соли меди, никеля, ртути, оксида ванадия (V), алюминия, железа(III).
 Гетерогенный катализ очень удобен тем, что катализатор не смешивается с реагентами и не возникает проблемы отделения его от продуктов реакции. Первые гетерогенно каталитические реакции были осуществлены еще в конце XVIII века дегидратация этилового спирта на активной глине (Пристли): С 2 Н 5 ОН → С 2 Н 4 + Н 20 и дегидрирование этилового спирта на меди, железе, никеле, серебре, церии (Ван Марум): С 2 Н 5 ОН → СН 3 СНО + Н 2 В настоящее время гетерогенный катализ применяется в промышленности в огромных масштабах, поэтому значительная часть добываемых платиновых металлов идет на производство катализаторов.
Гетерогенный катализ очень удобен тем, что катализатор не смешивается с реагентами и не возникает проблемы отделения его от продуктов реакции. Первые гетерогенно каталитические реакции были осуществлены еще в конце XVIII века дегидратация этилового спирта на активной глине (Пристли): С 2 Н 5 ОН → С 2 Н 4 + Н 20 и дегидрирование этилового спирта на меди, железе, никеле, серебре, церии (Ван Марум): С 2 Н 5 ОН → СН 3 СНО + Н 2 В настоящее время гетерогенный катализ применяется в промышленности в огромных масштабах, поэтому значительная часть добываемых платиновых металлов идет на производство катализаторов.
 Твердые катализаторы применяются при синтезе аммиака из азота и водорода, для крекинга и риформинга нефти, приводящих к повышению выхода высокооктанового бензина, в каталитических дожигателях, которые уменьшают токсичность выхлопных газов и т. д. Трудно перечислить даже важнейшие процессы многотоннажного неорганического и органического синтезов, которые основаны на гетерогенном катализе. Механизмы действия гетерогенных катализаторов включают следующие основные стадии: Ш движение реагирующих веществ к поверхности катализато ра (диффузия); Ш адсорбция реагентов поверхностью катализатора; Ш их взаимодействие на поверхности; Ш десорбция продуктов реакции с освобождением поверхности катализатора.
Твердые катализаторы применяются при синтезе аммиака из азота и водорода, для крекинга и риформинга нефти, приводящих к повышению выхода высокооктанового бензина, в каталитических дожигателях, которые уменьшают токсичность выхлопных газов и т. д. Трудно перечислить даже важнейшие процессы многотоннажного неорганического и органического синтезов, которые основаны на гетерогенном катализе. Механизмы действия гетерогенных катализаторов включают следующие основные стадии: Ш движение реагирующих веществ к поверхности катализато ра (диффузия); Ш адсорбция реагентов поверхностью катализатора; Ш их взаимодействие на поверхности; Ш десорбция продуктов реакции с освобождением поверхности катализатора.
 Энергия адсорбции способствует разрыхлению и поляризации определенных химических связей, активирует сами реагирующие молекулы, что особенно важно в случае кратносвязанных неполярных молекул типа N 2 или 02. Энергия адсорбции должна быть достаточной для этого, но не слишком высокой, чтобы продукт в дальнейшем не задерживался на поверхности катализатора. В зависимости от условий проведения процесса и его особенностей лимитирующей может оказаться любая из этих стадий. С точки зрения понимания действия катализатора вторая стадия наиболее интересна. Адсорбция реагирующих молекул на поверхности катализатора обеспечивает их благоприятную взаимную ориентацию в течение времени, необходимого для взаимодействия.
Энергия адсорбции способствует разрыхлению и поляризации определенных химических связей, активирует сами реагирующие молекулы, что особенно важно в случае кратносвязанных неполярных молекул типа N 2 или 02. Энергия адсорбции должна быть достаточной для этого, но не слишком высокой, чтобы продукт в дальнейшем не задерживался на поверхности катализатора. В зависимости от условий проведения процесса и его особенностей лимитирующей может оказаться любая из этих стадий. С точки зрения понимания действия катализатора вторая стадия наиболее интересна. Адсорбция реагирующих молекул на поверхности катализатора обеспечивает их благоприятную взаимную ориентацию в течение времени, необходимого для взаимодействия.
 В качестве примера обратимся к хорошо известному синтезу Габера, с помощью которого в мире ежегодно синтезируют десятки миллионов тонн аммиака. Катализатором обычно служит железо, специально активированное добавками таких оксидов, как А 12 О 3, К 2 О и Са. О. Главным препятствием для прямого протекания реакции служит огромная энергия тройной связи N≡N в молекуле азота (942 к. Дж/моль), поэтому необходимыми стадиями каталитического процесса являются адсорбция азота поверхностью катализатора и его последующая диссоциация. Не анализируя полностью сложный механизм этого процесса, отметим только его важнейшие стадии: Здесь "(адc)" означает, что частица адсорбирована поверхностью катализатора. Отметим, что требования к гетерогенному катализатору не ограничиваются лишь подходящей энергией адсорбции, большую роль играет пространственное расположение адсорбированных молекул и электронное строение поверхностного слоя катализатора. Действительно, в некоторых случаях разные катализаторы приводят к выделению разных продуктов из одних и тех же исходных веществ.
В качестве примера обратимся к хорошо известному синтезу Габера, с помощью которого в мире ежегодно синтезируют десятки миллионов тонн аммиака. Катализатором обычно служит железо, специально активированное добавками таких оксидов, как А 12 О 3, К 2 О и Са. О. Главным препятствием для прямого протекания реакции служит огромная энергия тройной связи N≡N в молекуле азота (942 к. Дж/моль), поэтому необходимыми стадиями каталитического процесса являются адсорбция азота поверхностью катализатора и его последующая диссоциация. Не анализируя полностью сложный механизм этого процесса, отметим только его важнейшие стадии: Здесь "(адc)" означает, что частица адсорбирована поверхностью катализатора. Отметим, что требования к гетерогенному катализатору не ограничиваются лишь подходящей энергией адсорбции, большую роль играет пространственное расположение адсорбированных молекул и электронное строение поверхностного слоя катализатора. Действительно, в некоторых случаях разные катализаторы приводят к выделению разных продуктов из одних и тех же исходных веществ.
 Химическое равновесие Химические реакции бывают обратимые и необратимые. Необратимые реакции проходят только в одном направлении и проходят практически до конца. Например: Конечные продукты этих реакций невозможно соединить между собой, чтобы получить исходные вещества.
Химическое равновесие Химические реакции бывают обратимые и необратимые. Необратимые реакции проходят только в одном направлении и проходят практически до конца. Например: Конечные продукты этих реакций невозможно соединить между собой, чтобы получить исходные вещества.
 Обратимые реакции одновременно идут в двух взаимно противоположных направлениях и не проходят до конца. Например, реакция При температуре в несколько сот градусов практически необратима (идет с образованием воды), но при 2000ºС начинает происходить вторая реакция – обратная водяной пар разлагается на водород и кислород. Через некоторое время скорость прямой реакции стает равной скорости обратной реакции, и наступает состояние динамического равновесия. За единицу времени образуется такое же количество молекул воды, которое распадается на молекулы водорода и кислорода. В состоянии равновесия концентрации исходных веществ и продуктов реакции при этих условиях остаются неизменными. Такие концентрации называются равновесными.
Обратимые реакции одновременно идут в двух взаимно противоположных направлениях и не проходят до конца. Например, реакция При температуре в несколько сот градусов практически необратима (идет с образованием воды), но при 2000ºС начинает происходить вторая реакция – обратная водяной пар разлагается на водород и кислород. Через некоторое время скорость прямой реакции стает равной скорости обратной реакции, и наступает состояние динамического равновесия. За единицу времени образуется такое же количество молекул воды, которое распадается на молекулы водорода и кислорода. В состоянии равновесия концентрации исходных веществ и продуктов реакции при этих условиях остаются неизменными. Такие концентрации называются равновесными.
 Для реакции В соответствии с законом действующих масс, скорость прямой V 1 и обратной V 2 реакций выражается уравнениями: В состоянии равновесия скорость прямой и обратной реакций равны, следовательно , или
Для реакции В соответствии с законом действующих масс, скорость прямой V 1 и обратной V 2 реакций выражается уравнениями: В состоянии равновесия скорость прямой и обратной реакций равны, следовательно , или
![Отношение констант скоростей прямой и обратной реакций называется константой химического равновесия: следовательно, где [A], Отношение констант скоростей прямой и обратной реакций называется константой химического равновесия: следовательно, где [A],](https://present5.com/presentation/3/105405628_132624044.pdf-img/105405628_132624044.pdf-34.jpg) Отношение констант скоростей прямой и обратной реакций называется константой химического равновесия: следовательно, где [A], [B], [C], [D] – равновесные концентрации веществ А, В, С, D; a, b, c, d – показатели степени, которые численно равны стехиометрическим коэффициентам в уравнении реакции. Выражения констант равновесия некоторых гомогенных реакций приведены ниже:
Отношение констант скоростей прямой и обратной реакций называется константой химического равновесия: следовательно, где [A], [B], [C], [D] – равновесные концентрации веществ А, В, С, D; a, b, c, d – показатели степени, которые численно равны стехиометрическим коэффициентам в уравнении реакции. Выражения констант равновесия некоторых гомогенных реакций приведены ниже:
 Для гетерогенных реакций в выражении константы равновесия входят концентрации лишь тех веществ, которые находятся в газовой или жидкой фазах: Величина константы равновесия зависит от природы реагирующих веществ и температуры. Константа равновесия определяет глубину прохождения процесса в момент достижения состояния равновесия. Чем больше величина К, тем полнее взаимодействуют вещества.
Для гетерогенных реакций в выражении константы равновесия входят концентрации лишь тех веществ, которые находятся в газовой или жидкой фазах: Величина константы равновесия зависит от природы реагирующих веществ и температуры. Константа равновесия определяет глубину прохождения процесса в момент достижения состояния равновесия. Чем больше величина К, тем полнее взаимодействуют вещества.
 Итак, закон действующих масс для обратимых реакций: константа химического равновесия прямо пропорциональна произведению концентраций продуктов реакции и обратно пропорциональна произведению концентраций исходных веществ, причем концентрации записывают в степени, которая равна их стехиометрическим коэффициентам в уравнении реакции.
Итак, закон действующих масс для обратимых реакций: константа химического равновесия прямо пропорциональна произведению концентраций продуктов реакции и обратно пропорциональна произведению концентраций исходных веществ, причем концентрации записывают в степени, которая равна их стехиометрическим коэффициентам в уравнении реакции.
 Смещение химического равновесия. Принцип Ле Шателье Истинное химическое равновесие может устанавливаться только в закрытой системе. Скорость установления равновесия зависит как от природы реагирующих веществ, так и от условий. В гетерогенных системах, особенно при невысоких температурах, равновесие иногда устанавливается десятки, сотни и даже тысячи часов, а если реакция кинетически заторможена, то система так и остается неравновесной. Например, равновесие в системе железо кислород при стандартных условиях практически нацело сдвинуто в сторону образования Fе 203 , однако кислород можно годами хранить в стальном баллоне и с ним ничего не происходит. Напротив, в гомогенных газовых системах или в водных растворах большинство реакций протекает с очень большой скоростью и равновесие устанавливается практически мгновенно. Химическая система, пришедшая в состояние равновесия, будет находиться в нем до тех пор, пока условия сохраняются неизменными. Выйти из состояния равновесия самопроизвольно система не может. Если же изменить условия, то система перейдет в новое равновесное состояние.
Смещение химического равновесия. Принцип Ле Шателье Истинное химическое равновесие может устанавливаться только в закрытой системе. Скорость установления равновесия зависит как от природы реагирующих веществ, так и от условий. В гетерогенных системах, особенно при невысоких температурах, равновесие иногда устанавливается десятки, сотни и даже тысячи часов, а если реакция кинетически заторможена, то система так и остается неравновесной. Например, равновесие в системе железо кислород при стандартных условиях практически нацело сдвинуто в сторону образования Fе 203 , однако кислород можно годами хранить в стальном баллоне и с ним ничего не происходит. Напротив, в гомогенных газовых системах или в водных растворах большинство реакций протекает с очень большой скоростью и равновесие устанавливается практически мгновенно. Химическая система, пришедшая в состояние равновесия, будет находиться в нем до тех пор, пока условия сохраняются неизменными. Выйти из состояния равновесия самопроизвольно система не может. Если же изменить условия, то система перейдет в новое равновесное состояние.
 Изменение состояния равновесия в результате изменения условий принято называть смещением химического равновесия. Во многих случаях нет необходимости в точных расчетах, достаточно выяснить направление смещения равновесия, т. е. определить, концентрации каких веществ будут увеличиваться, а каких уменьшаться. Чаще всего приходится сталкиваться со смещением равновесия в результате следующих изменений условий: Ш изменения концентрации (парциального давления) одного из реагирующих веществ; Ш изменения общего давления или объема; Ш изменения температуры. При изменении концентрации какого либо вещества нарушается основное условие равновесия: ΔGT = 0, и в системе протекает процесс, восстанавливающий это условие.
Изменение состояния равновесия в результате изменения условий принято называть смещением химического равновесия. Во многих случаях нет необходимости в точных расчетах, достаточно выяснить направление смещения равновесия, т. е. определить, концентрации каких веществ будут увеличиваться, а каких уменьшаться. Чаще всего приходится сталкиваться со смещением равновесия в результате следующих изменений условий: Ш изменения концентрации (парциального давления) одного из реагирующих веществ; Ш изменения общего давления или объема; Ш изменения температуры. При изменении концентрации какого либо вещества нарушается основное условие равновесия: ΔGT = 0, и в системе протекает процесс, восстанавливающий это условие.
 Изменение общего давления или общего объема влияет на состояние равновесия только в том случае, если в процессе реакции меняется число молей газообразных веществ. Например, увеличение общего давления существенно увеличивает выход аммиака по реакции: и не сказывается на выходе HI по реакции
Изменение общего давления или общего объема влияет на состояние равновесия только в том случае, если в процессе реакции меняется число молей газообразных веществ. Например, увеличение общего давления существенно увеличивает выход аммиака по реакции: и не сказывается на выходе HI по реакции
 Если реакция протекает без изменения числа молей газа, то изменение общего давления или общего объема практически не сказывается на состоянии равновесия. При увеличении общего давления (уменьшении общего объема) равновесие смещается в сторону веществ, занимающих меньший объем, т. е. в сторону с меньшим числом газовых молей. И наоборот. При повышении температуры равновесие смещается в сторону эндотермической реакции, а при понижении температуры - в сторону экзотермической.
Если реакция протекает без изменения числа молей газа, то изменение общего давления или общего объема практически не сказывается на состоянии равновесия. При увеличении общего давления (уменьшении общего объема) равновесие смещается в сторону веществ, занимающих меньший объем, т. е. в сторону с меньшим числом газовых молей. И наоборот. При повышении температуры равновесие смещается в сторону эндотермической реакции, а при понижении температуры - в сторону экзотермической.
 Влияние изменения условий на состояние равновесия может быть выражено одним общим термодинамическим положением, известным под названием принципа Ле Шателье: Если на равновесную систему оказать воздействие, изменив внешние условия, равновесие в системе сместится так, чтобы уменьшить эффект, произведенный оказанным воздействием. Основные закономерности смещения равновесия, разобранные выше, вполне согласуются с этим принципом и могут быть легко предсказаны на его основе.
Влияние изменения условий на состояние равновесия может быть выражено одним общим термодинамическим положением, известным под названием принципа Ле Шателье: Если на равновесную систему оказать воздействие, изменив внешние условия, равновесие в системе сместится так, чтобы уменьшить эффект, произведенный оказанным воздействием. Основные закономерности смещения равновесия, разобранные выше, вполне согласуются с этим принципом и могут быть легко предсказаны на его основе.


