Химическая кинетика. Химическое равновесие. Рассматриваемые вопросы:
















лекция_кинетика..ppt
- Количество слайдов: 19
 Химическая кинетика. Химическое равновесие. Рассматриваемые вопросы: 1. Общие понятия 2. Факторы, определяющие скорость реакций 3. Химическое равновесие. 4. Смещение химического равновесия. Принцип Ле-Шателье
Химическая кинетика. Химическое равновесие. Рассматриваемые вопросы: 1. Общие понятия 2. Факторы, определяющие скорость реакций 3. Химическое равновесие. 4. Смещение химического равновесия. Принцип Ле-Шателье
 ХИМИЧЕСКАЯ КИНЕТИКА – (от греч. кинетикос – движущий) наука о механизмах химических реакций и закономерностях их протекания во времени. Гомогенные реакции: Н 2 (г) + Cl 2 (г) = 2 HCl (г) Н 2 SO 4(ж) +2 Na. OH(ж) = Na 2 SO 4(ж) + 2 H 2 O(ж) Гетерогенные реакции: Mg. O(т) + 2 HNO 3(ж) = Mg(NO 3)2(ж) + 2 H 2 O(ж)
ХИМИЧЕСКАЯ КИНЕТИКА – (от греч. кинетикос – движущий) наука о механизмах химических реакций и закономерностях их протекания во времени. Гомогенные реакции: Н 2 (г) + Cl 2 (г) = 2 HCl (г) Н 2 SO 4(ж) +2 Na. OH(ж) = Na 2 SO 4(ж) + 2 H 2 O(ж) Гетерогенные реакции: Mg. O(т) + 2 HNO 3(ж) = Mg(NO 3)2(ж) + 2 H 2 O(ж)
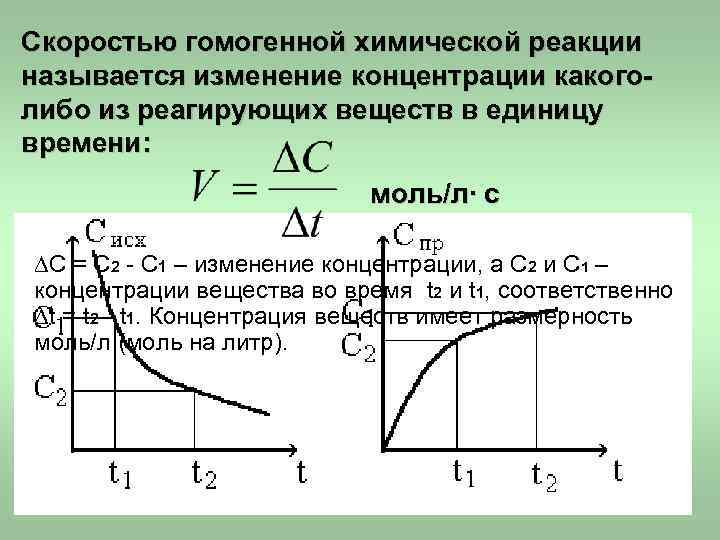
 Скоростью гомогенной химической реакции называется изменение концентрации какого- либо из реагирующих веществ в единицу времени: моль/л∙ с С = С 2 - С 1 – изменение концентрации, а C 2 и C 1 – концентрации вещества во время t 2 и t 1, соответственно t = t 2 - t 1. Концентрация веществ имеет размерность моль/л (моль на литр).
Скоростью гомогенной химической реакции называется изменение концентрации какого- либо из реагирующих веществ в единицу времени: моль/л∙ с С = С 2 - С 1 – изменение концентрации, а C 2 и C 1 – концентрации вещества во время t 2 и t 1, соответственно t = t 2 - t 1. Концентрация веществ имеет размерность моль/л (моль на литр).
 Факторы, определяющие скорость реакций 1. Концентрация 2. Температура А + В = С 3. и [B] – концентрации реагирующих веществ, тогда [A] Природа вещества 4. Катализатор v = k[A][B], где v - скорость реакции, а k - коэффициент пропорциональности, называемый константой скорости реакции. Для реакции 2 А + В = D или А + В = D уравнение скорости реакции соответственно примет вид 2 v = k[A][A][B] или v = k [A] [B].
Факторы, определяющие скорость реакций 1. Концентрация 2. Температура А + В = С 3. и [B] – концентрации реагирующих веществ, тогда [A] Природа вещества 4. Катализатор v = k[A][B], где v - скорость реакции, а k - коэффициент пропорциональности, называемый константой скорости реакции. Для реакции 2 А + В = D или А + В = D уравнение скорости реакции соответственно примет вид 2 v = k[A][A][B] или v = k [A] [B].
 Закон действующих масс (Гульберг и Вааге 1867 г). При постоянной температуре, скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ взятых в степенях, равных Като Максимилан их стехиометрическим Гульдберг коэффициентам. 1836 -1902 а в Петер Вааге а. А + в. В = д. Д, V= k[A] [B] 1833 -1900
Закон действующих масс (Гульберг и Вааге 1867 г). При постоянной температуре, скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ взятых в степенях, равных Като Максимилан их стехиометрическим Гульдберг коэффициентам. 1836 -1902 а в Петер Вааге а. А + в. В = д. Д, V= k[A] [B] 1833 -1900
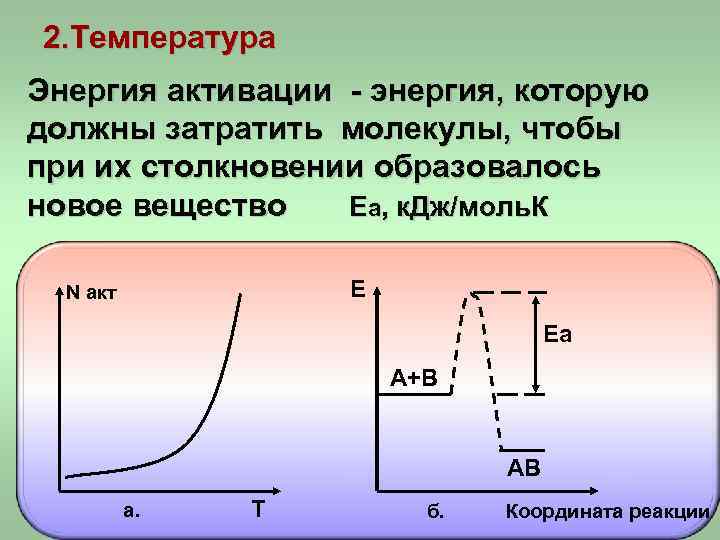
 2. Температура Энергия активации - энергия, которую должны затратить молекулы, чтобы при их столкновении образовалось новое вещество Еа, к. Дж/моль. К N акт Е Еа А+В АВ а. Т б. Координата реакции
2. Температура Энергия активации - энергия, которую должны затратить молекулы, чтобы при их столкновении образовалось новое вещество Еа, к. Дж/моль. К N акт Е Еа А+В АВ а. Т б. Координата реакции
 Правило Вант-Гоффа (1866 г). При повышении температуры на 10 градусов скорость реакции увеличивается от 2 до 4 раз. Якоб Хендрик Вант-Гофф 1852 -1911 Vт2 и Vт1 скорости реакции при температуре Т 2 и Т 1, - температурный коэффициент реакции, показывающий во сколько раз увеличивается скорость данной реакции при повышении температуры на 10 градусов.
Правило Вант-Гоффа (1866 г). При повышении температуры на 10 градусов скорость реакции увеличивается от 2 до 4 раз. Якоб Хендрик Вант-Гофф 1852 -1911 Vт2 и Vт1 скорости реакции при температуре Т 2 и Т 1, - температурный коэффициент реакции, показывающий во сколько раз увеличивается скорость данной реакции при повышении температуры на 10 градусов.
 Уравнение Аррениуса (1887 г. ) Сванте Аррениус Еа – энергия активации 1859 -1927 R – универсальная постоянная равная 8. 31 Дж/моль. К Т - температура в градусах Кельвина А - предэкспонентциальный множитель e – основание натурального логарифма
Уравнение Аррениуса (1887 г. ) Сванте Аррениус Еа – энергия активации 1859 -1927 R – универсальная постоянная равная 8. 31 Дж/моль. К Т - температура в градусах Кельвина А - предэкспонентциальный множитель e – основание натурального логарифма
 или Скорость реакции увеличивается с ростом температуры по экспоненциальному закону. Чем меньше энергия активации, тем при более низкой температуре начинается химическая реакция, и, следовательно, тем выше ее скорость
или Скорость реакции увеличивается с ростом температуры по экспоненциальному закону. Чем меньше энергия активации, тем при более низкой температуре начинается химическая реакция, и, следовательно, тем выше ее скорость
 3. Природа вещества • Еа< 40 к. Дж/моль. К, то реакция протекает мгновенно со взрывом. • При Еа>120 к. Дж/моль. К скорость реакции очень медленная (протекает месяцы, годы), что делает затруднительным ее измерение. • При Еа=40 - 120 к. Дж/моль. К скорость реакции лежит в пределах поддающихся экспериментальному определению.
3. Природа вещества • Еа< 40 к. Дж/моль. К, то реакция протекает мгновенно со взрывом. • При Еа>120 к. Дж/моль. К скорость реакции очень медленная (протекает месяцы, годы), что делает затруднительным ее измерение. • При Еа=40 - 120 к. Дж/моль. К скорость реакции лежит в пределах поддающихся экспериментальному определению.
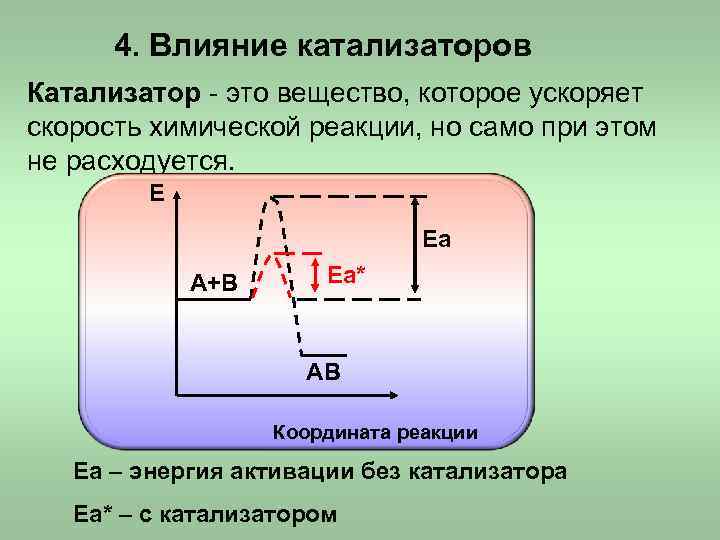
 4. Влияние катализаторов Катализатор - это вещество, которое ускоряет скорость химической реакции, но само при этом не расходуется. Е Еа А+В Еа* АВ Координата реакции Еа – энергия активации без катализатора Еа* – с катализатором
4. Влияние катализаторов Катализатор - это вещество, которое ускоряет скорость химической реакции, но само при этом не расходуется. Е Еа А+В Еа* АВ Координата реакции Еа – энергия активации без катализатора Еа* – с катализатором
 Вещества, замедляющие скорость реакции называется ингибиторами гетерогенных Особенности кинетики реакций • Скорость реакции зависит от площади реакционной поверхности S. • Скорость реакции во многом определяется скоростью подвода реагента к реакционной поверхности и отвода от нее продуктов реакции. • Концентрации веществ, находящихся в твердом состоянии не входят в уравнение закона действующих масс, поскольку остаются постоянными. Пример: 2 C + O 2= 2 CO, тогда V= k[O 2]S, т. к С - твердое в-во.
Вещества, замедляющие скорость реакции называется ингибиторами гетерогенных Особенности кинетики реакций • Скорость реакции зависит от площади реакционной поверхности S. • Скорость реакции во многом определяется скоростью подвода реагента к реакционной поверхности и отвода от нее продуктов реакции. • Концентрации веществ, находящихся в твердом состоянии не входят в уравнение закона действующих масс, поскольку остаются постоянными. Пример: 2 C + O 2= 2 CO, тогда V= k[O 2]S, т. к С - твердое в-во.
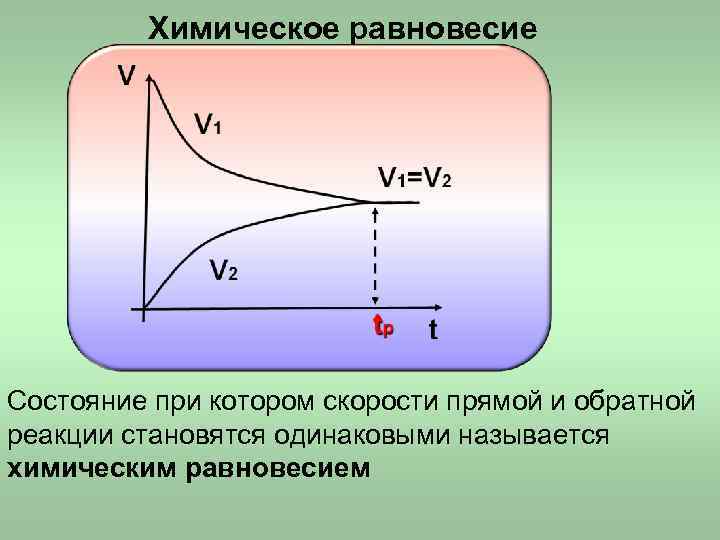
 Химическое равновесие Состояние при котором скорости прямой и обратной реакции становятся одинаковыми называется химическим равновесием
Химическое равновесие Состояние при котором скорости прямой и обратной реакции становятся одинаковыми называется химическим равновесием
 Н 2 + Cl 2 2 HCl 2 V 1= K 1[H 2][Cl 2] и V 2= K 2[HCl] При постоянной температуре константа равновесия -равна отношению произведения 2 концентрации продуктов реакции к. K 2[HCl] V 1 = V 2 , тогда K 1[H 2][Cl 2] = произведению концентраций исходных веществ, взятых2 в степенях их k 1 [HCl] стехиометрических= Kp k 2 = коэффициентов. [H 2][Cl 2] а. А + b. B c. C + d. D
Н 2 + Cl 2 2 HCl 2 V 1= K 1[H 2][Cl 2] и V 2= K 2[HCl] При постоянной температуре константа равновесия -равна отношению произведения 2 концентрации продуктов реакции к. K 2[HCl] V 1 = V 2 , тогда K 1[H 2][Cl 2] = произведению концентраций исходных веществ, взятых2 в степенях их k 1 [HCl] стехиометрических= Kp k 2 = коэффициентов. [H 2][Cl 2] а. А + b. B c. C + d. D
 Смещение химического G = - RTln. KP, откуда равновесия - Влияние концентрации При изменении концентрации какого-либо из реагирующих веществ в системе, равновесие смещается в сторону расходования этого вещества, при уменьшении концентрации в сторону его образования.
Смещение химического G = - RTln. KP, откуда равновесия - Влияние концентрации При изменении концентрации какого-либо из реагирующих веществ в системе, равновесие смещается в сторону расходования этого вещества, при уменьшении концентрации в сторону его образования.
 - Влияние давления (для реакций с участием газа) При увеличении давления (Р) в системе равновесие сдвигается в сторону реакции, приводящей к уменьшению числа молекул газообразных веществ, т. е. в сторону понижения давления. При уменьшении давления в системе равновесие смещается в сторону возрастания числа молекул газа, т. е. в сторону повышения давления Увеличение P 2 NO + O 2 ↔ 2 NO 2 Уменьшение P
- Влияние давления (для реакций с участием газа) При увеличении давления (Р) в системе равновесие сдвигается в сторону реакции, приводящей к уменьшению числа молекул газообразных веществ, т. е. в сторону понижения давления. При уменьшении давления в системе равновесие смещается в сторону возрастания числа молекул газа, т. е. в сторону повышения давления Увеличение P 2 NO + O 2 ↔ 2 NO 2 Уменьшение P
 - Влияние температуры При повышении температуры равновесие смещается в направлении эндотермической реакции При понижении температуры в направлении экзотермической реакции.
- Влияние температуры При повышении температуры равновесие смещается в направлении эндотермической реакции При понижении температуры в направлении экзотермической реакции.
 Принцип Ле-Шателье Если на систему находящуюся в состоянии химического равновесия оказывается какое- либо воздействие то, равновесие смещается в сторону той реакции (прямой Анри Луи или обратной), при которой Ле-Шателье данное воздействие 1850 -1936 ослабляется.
Принцип Ле-Шателье Если на систему находящуюся в состоянии химического равновесия оказывается какое- либо воздействие то, равновесие смещается в сторону той реакции (прямой Анри Луи или обратной), при которой Ле-Шателье данное воздействие 1850 -1936 ослабляется.
 Литература: 1. Н. Л. Глинка Общая химия 2. Н. С Ахметов Общая и неорганическая химия 3. И. Г Хомченко Общая химия 4. Шиманович И. Е. , Павлович М. Л. И др. Общая химия в формулах определениях, схемах.
Литература: 1. Н. Л. Глинка Общая химия 2. Н. С Ахметов Общая и неорганическая химия 3. И. Г Хомченко Общая химия 4. Шиманович И. Е. , Павлович М. Л. И др. Общая химия в формулах определениях, схемах.

