Химическая кинетика.ppt
- Количество слайдов: 66
 Химическая кинетика
Химическая кинетика
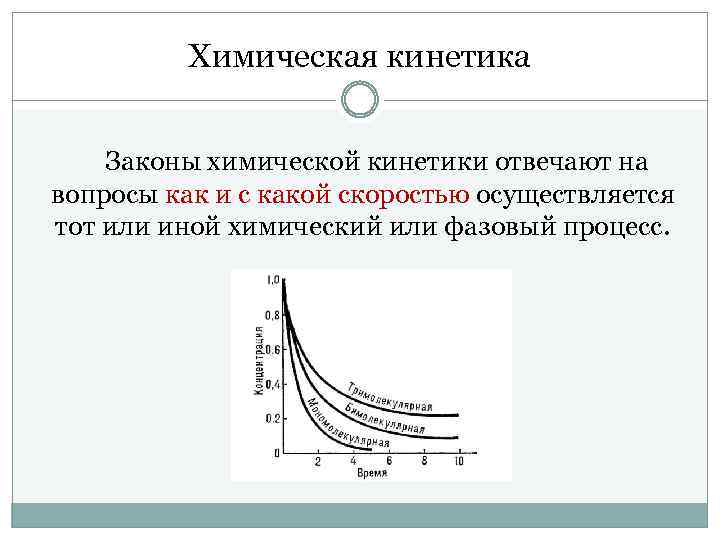 Химическая кинетика Законы химической кинетики отвечают на вопросы как и с какой скоростью осуществляется тот или иной химический или фазовый процесс.
Химическая кинетика Законы химической кинетики отвечают на вопросы как и с какой скоростью осуществляется тот или иной химический или фазовый процесс.
 Химическая кинетика Скорость химической реакции – это число элементарных актов химической реакции, происходящих в единицу времени в единице объема (для гомогенных реакций) или на единице поверхности (для гетерогенных реакций).
Химическая кинетика Скорость химической реакции – это число элементарных актов химической реакции, происходящих в единицу времени в единице объема (для гомогенных реакций) или на единице поверхности (для гетерогенных реакций).
 Химическая кинетика В случае необратимых химических реакций очевидно, что концентрации исходных веществ во времени постоянно уменьшаются, а концентрации продуктов реакции увеличиваются. Скорость реакции тогда считается положительной, поэтому математически определение средней скорости реакции в интервале времени Δt можно записать следующим образом:
Химическая кинетика В случае необратимых химических реакций очевидно, что концентрации исходных веществ во времени постоянно уменьшаются, а концентрации продуктов реакции увеличиваются. Скорость реакции тогда считается положительной, поэтому математически определение средней скорости реакции в интервале времени Δt можно записать следующим образом:
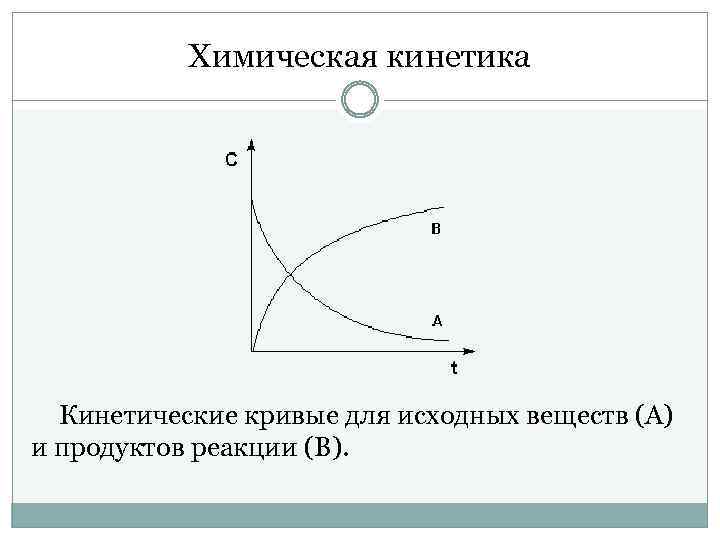 Химическая кинетика Кинетические кривые для исходных веществ (А) и продуктов реакции (В).
Химическая кинетика Кинетические кривые для исходных веществ (А) и продуктов реакции (В).
 Химическая кинетика Закон действия масс В основе химической кинетики лежит основной постулат химической кинетики: скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в некоторых степенях
Химическая кинетика Закон действия масс В основе химической кинетики лежит основной постулат химической кинетики: скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в некоторых степенях
 Химическая кинетика Для реакции a. A + b. B = c. C + d. D уравнение скорости прямой реакции будет выглядеть так: v=k × [A]a × [B]b, а обратной – так: v=k’ × [C]c × [D]d, где А, B, C, D – химические вещества-участники реакции; a, b, c, d - стехиометрические коэффициенты; k – константа скорости химической реакции; [ ] – концентрации веществ, моль/л.
Химическая кинетика Для реакции a. A + b. B = c. C + d. D уравнение скорости прямой реакции будет выглядеть так: v=k × [A]a × [B]b, а обратной – так: v=k’ × [C]c × [D]d, где А, B, C, D – химические вещества-участники реакции; a, b, c, d - стехиометрические коэффициенты; k – константа скорости химической реакции; [ ] – концентрации веществ, моль/л.
 Химическая кинетика Порядок реакции Для того, чтобы записать кинетическое уравнение, необходимо экспериментально определить величину константы скорости и показателей степени при концентрациях реагирующих веществ. 1. Константа скорости численно равна скорости реакции при концентрациях всех реагирующих веществ 1 моль/л. 2. Показатель степени при концентрации каждого из реагирующих веществ в кинетическом уравнении химической реакции – это частный порядок реакции по данному компоненту. Сумма показателей степени в кинетическом уравнении химической реакции (a+b или c+d) представляет собой общий порядок реакции.
Химическая кинетика Порядок реакции Для того, чтобы записать кинетическое уравнение, необходимо экспериментально определить величину константы скорости и показателей степени при концентрациях реагирующих веществ. 1. Константа скорости численно равна скорости реакции при концентрациях всех реагирующих веществ 1 моль/л. 2. Показатель степени при концентрации каждого из реагирующих веществ в кинетическом уравнении химической реакции – это частный порядок реакции по данному компоненту. Сумма показателей степени в кинетическом уравнении химической реакции (a+b или c+d) представляет собой общий порядок реакции.
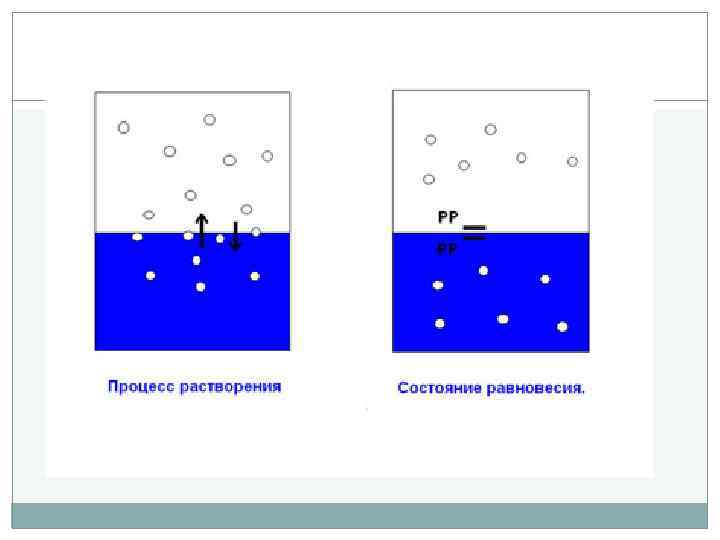
 Химическая кинетика Реакции нулевого порядка: Скорость такой реакции постоянна во времени и не зависит от концентраций реагирующих веществ. Это многие гетерогенные реакции при условии, что скорость диффузии реагентов к поверхности меньше скорости их химического превращения. Например, растворение газов в жидком растворителе.
Химическая кинетика Реакции нулевого порядка: Скорость такой реакции постоянна во времени и не зависит от концентраций реагирующих веществ. Это многие гетерогенные реакции при условии, что скорость диффузии реагентов к поверхности меньше скорости их химического превращения. Например, растворение газов в жидком растворителе.
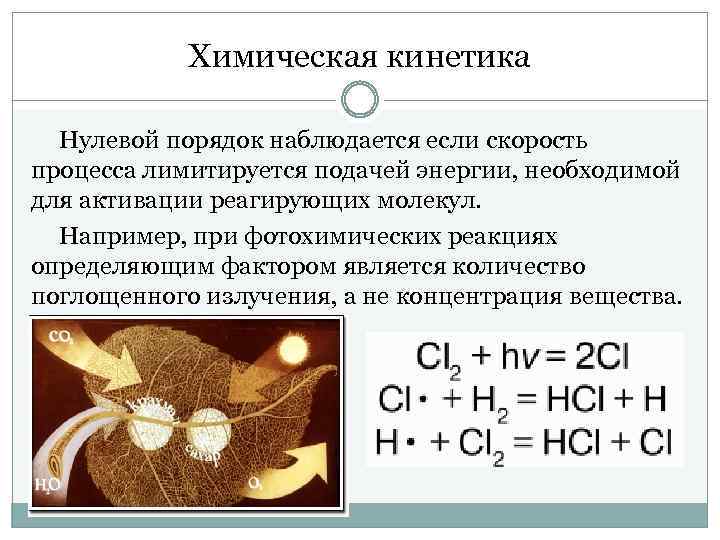 Химическая кинетика Нулевой порядок наблюдается если скорость процесса лимитируется подачей энергии, необходимой для активации реагирующих молекул. Например, при фотохимических реакциях определяющим фактором является количество поглощенного излучения, а не концентрация вещества.
Химическая кинетика Нулевой порядок наблюдается если скорость процесса лимитируется подачей энергии, необходимой для активации реагирующих молекул. Например, при фотохимических реакциях определяющим фактором является количество поглощенного излучения, а не концентрация вещества.
 Химическая кинетика Часто в каталитических реакциях скорость зависит от концентрации катализатора, а не от концентрации реагирующих веществ. Например, реакция гидрирования этилена на платине; скорость данной реакции определяется поверхностью катализатора и не зависит от концентраций реагентов.
Химическая кинетика Часто в каталитических реакциях скорость зависит от концентрации катализатора, а не от концентрации реагирующих веществ. Например, реакция гидрирования этилена на платине; скорость данной реакции определяется поверхностью катализатора и не зависит от концентраций реагентов.
 Химическая кинетика Реакции первого порядка: Примером может служить реакция разложения диметилового эфира: CH 3 OCH 3= CH 4 + H 2 + CO Кинетическое уравнение:
Химическая кинетика Реакции первого порядка: Примером может служить реакция разложения диметилового эфира: CH 3 OCH 3= CH 4 + H 2 + CO Кинетическое уравнение:
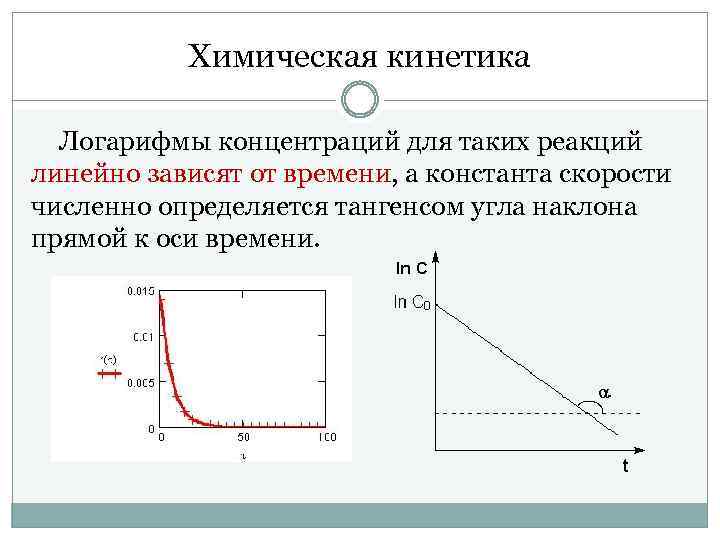 Химическая кинетика Логарифмы концентраций для таких реакций линейно зависят от времени, а константа скорости численно определяется тангенсом угла наклона прямой к оси времени.
Химическая кинетика Логарифмы концентраций для таких реакций линейно зависят от времени, а константа скорости численно определяется тангенсом угла наклона прямой к оси времени.
 Химическая кинетика Реакции второго порядка: либо Примеры: H 2 + I 2 = 2 HI 2 H 2 O = 2 H 2 + O 2
Химическая кинетика Реакции второго порядка: либо Примеры: H 2 + I 2 = 2 HI 2 H 2 O = 2 H 2 + O 2
 Химическая кинетика Для реакций второго порядка характерна линейная зависимость обратной концентрации от времени и константа скорости равна тангенсу угла наклона прямой к оси времени:
Химическая кинетика Для реакций второго порядка характерна линейная зависимость обратной концентрации от времени и константа скорости равна тангенсу угла наклона прямой к оси времени:
 Химическая кинетика Физический смысл порядка химической реакции заключается в следующем: порядок реакции равен числу одновременно изменяющихся концентраций. Порядок реакции может быть равен сумме коэффициентов в стехиометрическом уравнении реакции; однако в общем случае порядок реакции определяется только из экспериментальных данных и зависит от условий проведения реакции.
Химическая кинетика Физический смысл порядка химической реакции заключается в следующем: порядок реакции равен числу одновременно изменяющихся концентраций. Порядок реакции может быть равен сумме коэффициентов в стехиометрическом уравнении реакции; однако в общем случае порядок реакции определяется только из экспериментальных данных и зависит от условий проведения реакции.
 Химическая кинетика Например, реакция гидролиза этилового эфира уксусной кислоты СН 3 СООС 2 Н 5 + Н 2 О –> СН 3 СООН + С 2 Н 5 ОН Если проводить реакцию при близких концентрациях эфира и воды, то общий порядок реакции равен двум и кинетическое уравнение имеет вид:
Химическая кинетика Например, реакция гидролиза этилового эфира уксусной кислоты СН 3 СООС 2 Н 5 + Н 2 О –> СН 3 СООН + С 2 Н 5 ОН Если проводить реакцию при близких концентрациях эфира и воды, то общий порядок реакции равен двум и кинетическое уравнение имеет вид:
 Химическая кинетика При проведении этой же реакции в условиях избытка одного из реагентов, концентрация вещества, находящегося в избытке, практически не меняется и может быть включена в константу скорости. Тогда кинетическое уравнение принимает вид: 1) в избытке воды: где
Химическая кинетика При проведении этой же реакции в условиях избытка одного из реагентов, концентрация вещества, находящегося в избытке, практически не меняется и может быть включена в константу скорости. Тогда кинетическое уравнение принимает вид: 1) в избытке воды: где
 Химическая кинетика 2) в избытке этилацетата: где В этих случаях мы имеем дело с реакцией псевдопервого порядка.
Химическая кинетика 2) в избытке этилацетата: где В этих случаях мы имеем дело с реакцией псевдопервого порядка.
 Химическая кинетика Молекулярность реакции Кроме порядка, в кинетике принято классифицировать реакции по молекулярности: молекулярность элементарной реакции – это число частиц, которые, согласно экспериментально установленному механизму реакции, участвуют в элементарном акте химического взаимодействия. Мономолекулярные – реакции, в которых происходит химическое превращение одной молекулы (изомеризация, диссоциация и т. д. ): N 2 O 4 —> 2 NO 2 (Cu. OH)2 CO 3 —> Cu. O + H 2 O + CO 2 HNO 3 —> H+ + NO 3 -
Химическая кинетика Молекулярность реакции Кроме порядка, в кинетике принято классифицировать реакции по молекулярности: молекулярность элементарной реакции – это число частиц, которые, согласно экспериментально установленному механизму реакции, участвуют в элементарном акте химического взаимодействия. Мономолекулярные – реакции, в которых происходит химическое превращение одной молекулы (изомеризация, диссоциация и т. д. ): N 2 O 4 —> 2 NO 2 (Cu. OH)2 CO 3 —> Cu. O + H 2 O + CO 2 HNO 3 —> H+ + NO 3 -
 Химическая кинетика Бимолекулярные – реакции, элементарный акт которых осуществляется при столкновении двух частиц (одинаковых или различных): СН 3 Вr + КОН –> СН 3 ОН + КВr Тримолекулярные – реакции, элементарный акт которых осуществляется при столкновении трех частиц: О 2 + NО –> 2 NО 2 Реакции с молекулярностью более трёх неизвестны.
Химическая кинетика Бимолекулярные – реакции, элементарный акт которых осуществляется при столкновении двух частиц (одинаковых или различных): СН 3 Вr + КОН –> СН 3 ОН + КВr Тримолекулярные – реакции, элементарный акт которых осуществляется при столкновении трех частиц: О 2 + NО –> 2 NО 2 Реакции с молекулярностью более трёх неизвестны.
 Химическая кинетика Взаимосвязи между понятиями молекулярности и порядка реакции не существует, поскольку: - порядок реакции характеризует кинетическое уравнение реакции, - молекулярность – механизм реакции.
Химическая кинетика Взаимосвязи между понятиями молекулярности и порядка реакции не существует, поскольку: - порядок реакции характеризует кинетическое уравнение реакции, - молекулярность – механизм реакции.
 Химическая кинетика Сложные реакции Сложными называют химические реакции, протекающие более чем в одну стадию. Например: 2 НI + Н 2 О 2 –> I 2 + 2 Н 2 О Данная реакция является двухстадийной: 1) НI + Н 2 О 2 –> НIО + Н 2 О 2) НIО + НI –> I 2 + Н 2 О
Химическая кинетика Сложные реакции Сложными называют химические реакции, протекающие более чем в одну стадию. Например: 2 НI + Н 2 О 2 –> I 2 + 2 Н 2 О Данная реакция является двухстадийной: 1) НI + Н 2 О 2 –> НIО + Н 2 О 2) НIО + НI –> I 2 + Н 2 О
 Химическая кинетика Скорость первой стадии V 1 много больше скорости второй стадии V 2 и общая скорость реакции определяется скоростью более медленной стадии, называемой лимитирующей. Поэтому, данная сложная реакция является реакцией второго порядка, и её кинетическое уравнение имеет следующий вид:
Химическая кинетика Скорость первой стадии V 1 много больше скорости второй стадии V 2 и общая скорость реакции определяется скоростью более медленной стадии, называемой лимитирующей. Поэтому, данная сложная реакция является реакцией второго порядка, и её кинетическое уравнение имеет следующий вид:
 Химическая кинетика Реакция является сложной, если экспериментально определенные частные порядки реакции не совпадают с коэффициентами при исходных веществах в стехиометрическом уравнении реакции. Виды сложных реакций: 1) Последовательные реакции - протекают таким образом, что вещества, образующиеся в результате одной стадии, являются исходными веществами для другой стадии. А –> В –> С –>. . . Число стадий и веществ, принимающих участие в каждой из стадий, может быть различным.
Химическая кинетика Реакция является сложной, если экспериментально определенные частные порядки реакции не совпадают с коэффициентами при исходных веществах в стехиометрическом уравнении реакции. Виды сложных реакций: 1) Последовательные реакции - протекают таким образом, что вещества, образующиеся в результате одной стадии, являются исходными веществами для другой стадии. А –> В –> С –>. . . Число стадий и веществ, принимающих участие в каждой из стадий, может быть различным.
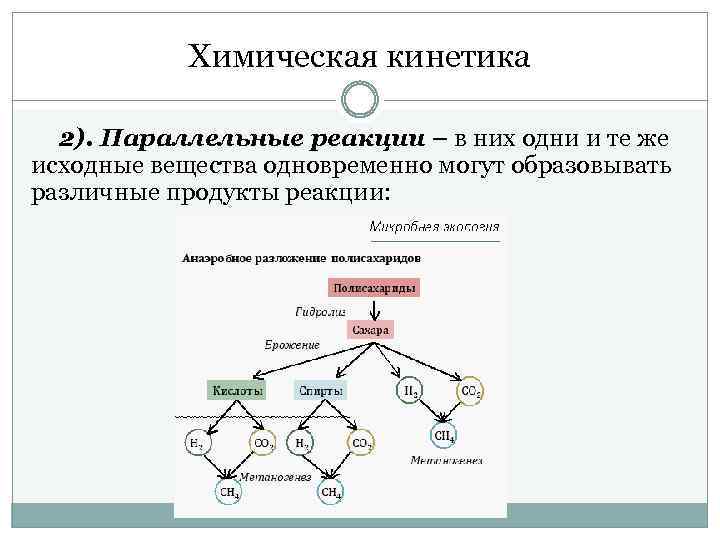 Химическая кинетика 2). Параллельные реакции – в них одни и те же исходные вещества одновременно могут образовывать различные продукты реакции:
Химическая кинетика 2). Параллельные реакции – в них одни и те же исходные вещества одновременно могут образовывать различные продукты реакции:
 Химическая кинетика 3). Сопряжённые реакции - сложные реакции, протекающие по схеме: 1) А + В –> С 2) А + D –> Е, причём одна из реакций может протекать самостоятельно, а вторая возможна только при наличии первой. Вещество А, общее для обеих реакций, носит название актор, вещество В – индуктор, вещество D, взаимодействующее с А только при наличии первой реакции – акцептор.
Химическая кинетика 3). Сопряжённые реакции - сложные реакции, протекающие по схеме: 1) А + В –> С 2) А + D –> Е, причём одна из реакций может протекать самостоятельно, а вторая возможна только при наличии первой. Вещество А, общее для обеих реакций, носит название актор, вещество В – индуктор, вещество D, взаимодействующее с А только при наличии первой реакции – акцептор.
 Химическая кинетика Например, бензол в водном растворе не окисляется пероксидом водорода, но при добавлении солей Fe(II) происходит превращение его в фенол и дифенил. На первой стадии образуются свободные радикалы: Fe 2+ + H 2 O 2 –> Fe 3+ + OH– + OH • которые реагируют с ионами Fe 2+ и бензолом: Fe 2+ + OH • –> Fe 3+ + OH– C 6 H 6 + OH • –> C 6 H 5 • + H 2 O Происходит также рекомбинация радикалов: C 6 H 5 • + OH • –> C 6 H 5 ОН C 6 H 5 • + C 6 H 5 • –> C 6 H 5–C 6 H 5 Так, обе реакции протекают с участием общего промежуточного свободного радикала OH • .
Химическая кинетика Например, бензол в водном растворе не окисляется пероксидом водорода, но при добавлении солей Fe(II) происходит превращение его в фенол и дифенил. На первой стадии образуются свободные радикалы: Fe 2+ + H 2 O 2 –> Fe 3+ + OH– + OH • которые реагируют с ионами Fe 2+ и бензолом: Fe 2+ + OH • –> Fe 3+ + OH– C 6 H 6 + OH • –> C 6 H 5 • + H 2 O Происходит также рекомбинация радикалов: C 6 H 5 • + OH • –> C 6 H 5 ОН C 6 H 5 • + C 6 H 5 • –> C 6 H 5–C 6 H 5 Так, обе реакции протекают с участием общего промежуточного свободного радикала OH • .
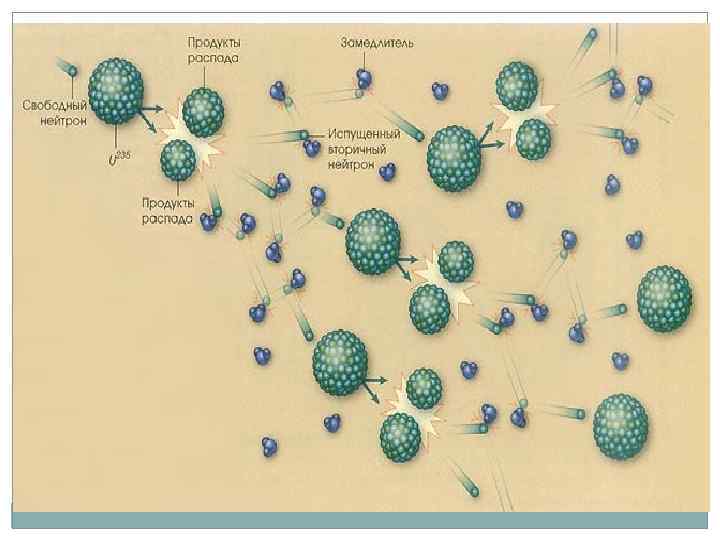
 Химическая кинетика 4). Цепные реакции – это реакции, состоящие из ряда взаимосвязанных стадий, когда частицы, образующиеся в результате каждой стадии, генерируют последующие стадии. Как правило, цепные реакции протекают с участием свободных радикалов. Для всех цепных реакций характерны три типичные стадии: 1. Зарождение цепи (инициация): Сl 2 + hν –> 2 Сl • 2. Развитие цепи: Н 2 + Сl • –> НСl + Н • + Сl 2 –> НСl + Сl • 3. Обрыв цепи (рекомбинация): Н • + Н • –> Н 2 Сl • + Сl • –> Сl 2 Н • + Сl • –> НСl
Химическая кинетика 4). Цепные реакции – это реакции, состоящие из ряда взаимосвязанных стадий, когда частицы, образующиеся в результате каждой стадии, генерируют последующие стадии. Как правило, цепные реакции протекают с участием свободных радикалов. Для всех цепных реакций характерны три типичные стадии: 1. Зарождение цепи (инициация): Сl 2 + hν –> 2 Сl • 2. Развитие цепи: Н 2 + Сl • –> НСl + Н • + Сl 2 –> НСl + Сl • 3. Обрыв цепи (рекомбинация): Н • + Н • –> Н 2 Сl • + Сl • –> Сl 2 Н • + Сl • –> НСl
 Химическая кинетика Константа скорости и правило Вант-Гоффа Константа скорости реакции – это функция от температуры; повышение температуры, как правило, увеличивает константу скорости: при повышении температуры на каждые 10 градусов константа скорости элементарной химической реакции увеличивается в 2 – 4 раза Величина, показывающая, во сколько раз ТОЧНО увеличивается константа скорости при повышении температуры на 10 градусов, есть температурный коэффициент константы скорости реакции γ.
Химическая кинетика Константа скорости и правило Вант-Гоффа Константа скорости реакции – это функция от температуры; повышение температуры, как правило, увеличивает константу скорости: при повышении температуры на каждые 10 градусов константа скорости элементарной химической реакции увеличивается в 2 – 4 раза Величина, показывающая, во сколько раз ТОЧНО увеличивается константа скорости при повышении температуры на 10 градусов, есть температурный коэффициент константы скорости реакции γ.
 Химическая кинетика Тогда, математически правило Вант-Гоффа можно записать следующим образом: и Однако правило Вант-Гоффа применимо лишь в узком температурном интервале; при очень высоких и очень низких температурах γ становится равным единице (т. е. скорость химической реакции перестает зависеть от температуры).
Химическая кинетика Тогда, математически правило Вант-Гоффа можно записать следующим образом: и Однако правило Вант-Гоффа применимо лишь в узком температурном интервале; при очень высоких и очень низких температурах γ становится равным единице (т. е. скорость химической реакции перестает зависеть от температуры).
 Химическая кинетика Энергия активации В любой системе с химическими веществами число столкновений молекул очень велико и, если бы каждое столкновение приводило к химическому взаимодействию частиц, все реакции протекали бы практически мгновенно. В реальности столкновения молекул эффективны только в том случае, если молекулы обладают некоторым запасом энергии – энергией активации.
Химическая кинетика Энергия активации В любой системе с химическими веществами число столкновений молекул очень велико и, если бы каждое столкновение приводило к химическому взаимодействию частиц, все реакции протекали бы практически мгновенно. В реальности столкновения молекул эффективны только в том случае, если молекулы обладают некоторым запасом энергии – энергией активации.
 Химическая кинетика энергия активации - это минимальная энергия, которой должны обладать молекулы, чтобы их столкновение могло привести к химическому взаимодействию
Химическая кинетика энергия активации - это минимальная энергия, которой должны обладать молекулы, чтобы их столкновение могло привести к химическому взаимодействию
 Химическая кинетика Рассмотрим путь некоторой элементарной реакции А + В –> С Поскольку химическое взаимодействие частиц связано с разрывом старых химических связей и образованием новых, считается, что всякая элементарная реакция проходит через образование некоторого неустойчивого промежуточного соединения, называемого активированным комплексом: А –> K* –> B
Химическая кинетика Рассмотрим путь некоторой элементарной реакции А + В –> С Поскольку химическое взаимодействие частиц связано с разрывом старых химических связей и образованием новых, считается, что всякая элементарная реакция проходит через образование некоторого неустойчивого промежуточного соединения, называемого активированным комплексом: А –> K* –> B
 Химическая кинетика Образование активированного комплекса всегда требует затраты некоторого количества энергии, что вызвано: - отталкиванием электронных оболочек и атомных ядер при сближении частиц ; - необходимостью построения определенной пространственной конфигурации атомов в активированном комплексе и, как следствие, перераспределения электронной плотности.
Химическая кинетика Образование активированного комплекса всегда требует затраты некоторого количества энергии, что вызвано: - отталкиванием электронных оболочек и атомных ядер при сближении частиц ; - необходимостью построения определенной пространственной конфигурации атомов в активированном комплексе и, как следствие, перераспределения электронной плотности.
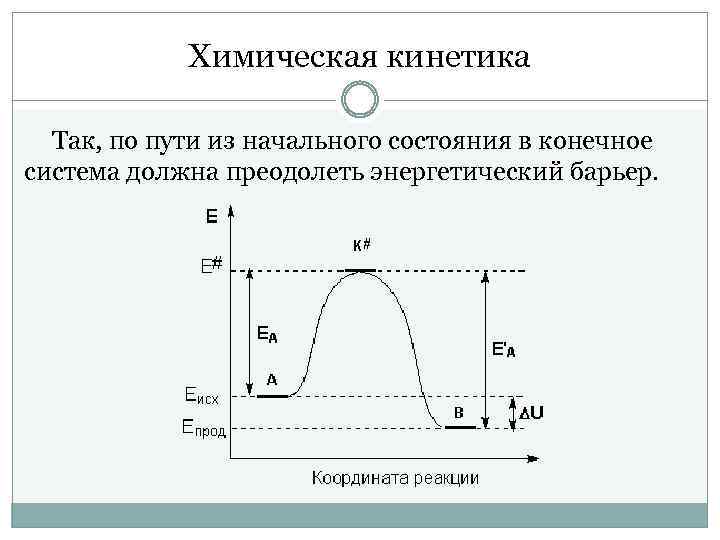 Химическая кинетика Так, по пути из начального состояния в конечное система должна преодолеть энергетический барьер.
Химическая кинетика Так, по пути из начального состояния в конечное система должна преодолеть энергетический барьер.
 Химическая кинетика Температура – это мера средней кинетической энергии частиц. Поэтому повышение температуры приводит к увеличению количества частиц, энергия которых больше энергии активации, что приводит к увеличению константы скорости реакции: n. Е/N – доля частиц, обладающих энергией E; Ei - средняя энергия частиц при температуре Ti (T 1 < T 2 < T 3)
Химическая кинетика Температура – это мера средней кинетической энергии частиц. Поэтому повышение температуры приводит к увеличению количества частиц, энергия которых больше энергии активации, что приводит к увеличению константы скорости реакции: n. Е/N – доля частиц, обладающих энергией E; Ei - средняя энергия частиц при температуре Ti (T 1 < T 2 < T 3)
 Химическая кинетика Кинетика обратимых реакций Химические реакции часто являются обратимыми, т. е. могут протекать в двух противоположных направлениях: А + В <–> D + C скорость уменьшения концентрации исходных веществ при протекании прямой реакции определяется уравнением: а скорость возрастания концентрации исходных веществ в результате протекания обратной реакции – уравнением:
Химическая кинетика Кинетика обратимых реакций Химические реакции часто являются обратимыми, т. е. могут протекать в двух противоположных направлениях: А + В <–> D + C скорость уменьшения концентрации исходных веществ при протекании прямой реакции определяется уравнением: а скорость возрастания концентрации исходных веществ в результате протекания обратной реакции – уравнением:
 Химическая кинетика По мере протекания двусторонней реакции: - скорость прямой реакции уменьшается, - скорость обратной реакции – увеличивается. В некоторый момент времени скорости прямой и обратной реакции становятся равными и концентрации реагентов перестают изменяться. Так в закрытой системе устанавливается химическое равновесия; при этом константа равновесия будет равна отношению констант скоростей прямой и обратной реакции: или
Химическая кинетика По мере протекания двусторонней реакции: - скорость прямой реакции уменьшается, - скорость обратной реакции – увеличивается. В некоторый момент времени скорости прямой и обратной реакции становятся равными и концентрации реагентов перестают изменяться. Так в закрытой системе устанавливается химическое равновесия; при этом константа равновесия будет равна отношению констант скоростей прямой и обратной реакции: или
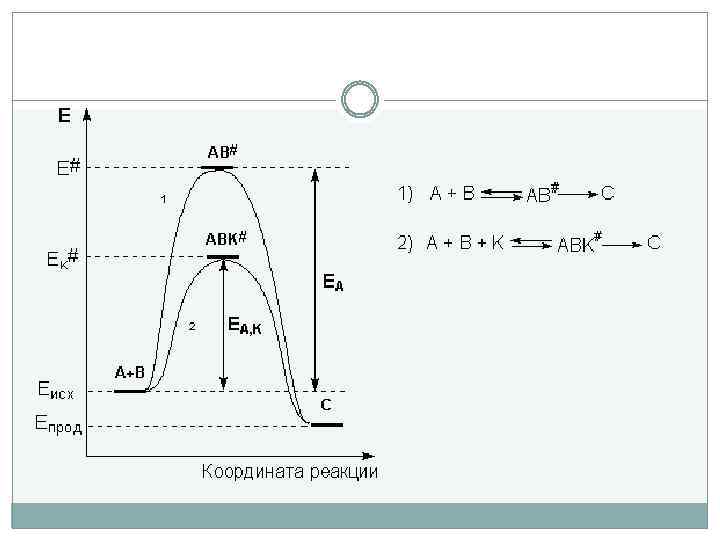
 Химическая кинетика Катализ В некоторых химических реакциях в структуру активированного комплекса могут входить вещества, не являющиеся реагентами. При этом энергия активации процесса очевидно изменяется и реакция идёт по пути с наименьшим активационным барьером. Это явление катализа. катализ – это явление изменения скорости химической реакции в присутствии веществ, состояние и количество которых после реакции остаются неизменными
Химическая кинетика Катализ В некоторых химических реакциях в структуру активированного комплекса могут входить вещества, не являющиеся реагентами. При этом энергия активации процесса очевидно изменяется и реакция идёт по пути с наименьшим активационным барьером. Это явление катализа. катализ – это явление изменения скорости химической реакции в присутствии веществ, состояние и количество которых после реакции остаются неизменными
 Химическая кинетика Различают положительный и отрицательный катализ - соответственно увеличение и уменьшение скорости реакции (хотя часто под термином "катализ" подразумевают только положительный катализ, а отрицательный катализ называют ингибированием). вещество, входящее в структуру активированного комплекса, но не являющееся реагентом, называется катализатором
Химическая кинетика Различают положительный и отрицательный катализ - соответственно увеличение и уменьшение скорости реакции (хотя часто под термином "катализ" подразумевают только положительный катализ, а отрицательный катализ называют ингибированием). вещество, входящее в структуру активированного комплекса, но не являющееся реагентом, называется катализатором
 Химическая кинетика Особые характеристики катализаторов: 1. специфичность - способность ускорять только одну реакцию или группу однотипных реакций и не влиять на скорость других реакций; 2. селективность катализатора – это способность ускорять одну из возможных при данных условиях параллельных реакций. Благодаря этому можно, применяя различные катализаторы, из одних и тех же исходных веществ получать различные продукты: [Cu]: СО + Н 2 –> СН 3 ОН [Ni]: СО + Н 2 –> СН 4 + Н 2 О [Cu]: С 2 Н 5 ОН –> СН 3 СНО + Н 2 [Al 2 О 3]: С 2 Н 5 ОН –> С 2 Н 4 + Н 2 О
Химическая кинетика Особые характеристики катализаторов: 1. специфичность - способность ускорять только одну реакцию или группу однотипных реакций и не влиять на скорость других реакций; 2. селективность катализатора – это способность ускорять одну из возможных при данных условиях параллельных реакций. Благодаря этому можно, применяя различные катализаторы, из одних и тех же исходных веществ получать различные продукты: [Cu]: СО + Н 2 –> СН 3 ОН [Ni]: СО + Н 2 –> СН 4 + Н 2 О [Cu]: С 2 Н 5 ОН –> СН 3 СНО + Н 2 [Al 2 О 3]: С 2 Н 5 ОН –> С 2 Н 4 + Н 2 О
 Химическая кинетика ОДНАКО! 1. наличие катализатора не влияет на величину изменения термодинамического потенциала в результате процесса и, следовательно, никакой катализатор не может сделать возможным самопроизвольное протекание термодинамически невозможного процесса (ΔG или ΔF которого больше нуля). 2. катализатор не изменяет величину константы равновесия для обратимых реакций; влияние катализатора в этом случае заключается только в ускорении достижения равновесного состояния.
Химическая кинетика ОДНАКО! 1. наличие катализатора не влияет на величину изменения термодинамического потенциала в результате процесса и, следовательно, никакой катализатор не может сделать возможным самопроизвольное протекание термодинамически невозможного процесса (ΔG или ΔF которого больше нуля). 2. катализатор не изменяет величину константы равновесия для обратимых реакций; влияние катализатора в этом случае заключается только в ускорении достижения равновесного состояния.
 Химическая кинетика Типы катализа В зависимости от фазового состояния реагентов и катализатора различают: 1. гомогенный катализ – реагенты и катализатор находятся в одной фазе; 2. гетерогенный катализ – каталитические реакции, идущие на поверхности раздела фаз, образуемых катализатором и реагирующими веществами.
Химическая кинетика Типы катализа В зависимости от фазового состояния реагентов и катализатора различают: 1. гомогенный катализ – реагенты и катализатор находятся в одной фазе; 2. гетерогенный катализ – каталитические реакции, идущие на поверхности раздела фаз, образуемых катализатором и реагирующими веществами.
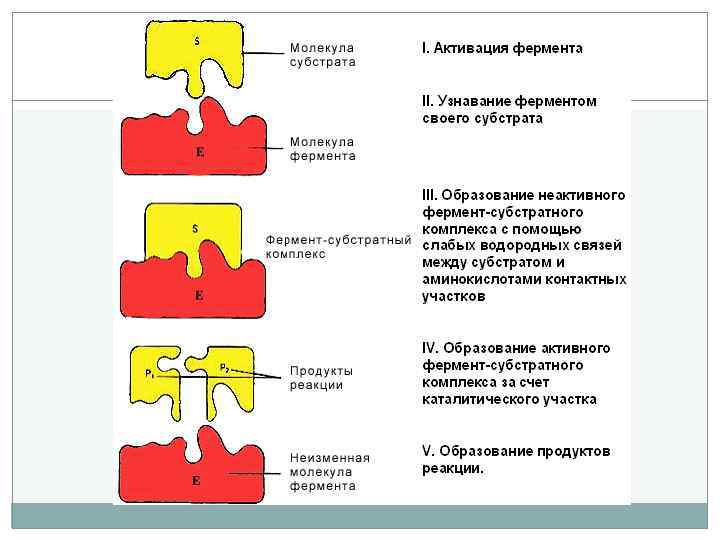
 Химическая кинетика 3. ферментативный катализ – каталитические реакции, протекающие с участием ферментов – биологических катализаторов белковой природы. Ферментативный катализ имеет характерные особенности: - высокая активность (на несколько порядков выше активности неорганических катализаторов); например, константа скорости реакции разложения перекиси водорода, катализируемой ионами Fе 2+, составляет 56 с-1; константа скорости этой же реакции, катализируемой ферментом каталазой, равна 3, 5· 107 с-1
Химическая кинетика 3. ферментативный катализ – каталитические реакции, протекающие с участием ферментов – биологических катализаторов белковой природы. Ферментативный катализ имеет характерные особенности: - высокая активность (на несколько порядков выше активности неорганических катализаторов); например, константа скорости реакции разложения перекиси водорода, катализируемой ионами Fе 2+, составляет 56 с-1; константа скорости этой же реакции, катализируемой ферментом каталазой, равна 3, 5· 107 с-1
 Химическая кинетика - высокая специфичность. например, амилаза катализирует процесс расщепления крахмала, представляющего собой цепь одинаковых глюкозных звеньев, но не катализирует гидролиз сахарозы, молекула которой составлена из глюкозного и фруктозного фрагментов.
Химическая кинетика - высокая специфичность. например, амилаза катализирует процесс расщепления крахмала, представляющего собой цепь одинаковых глюкозных звеньев, но не катализирует гидролиз сахарозы, молекула которой составлена из глюкозного и фруктозного фрагментов.
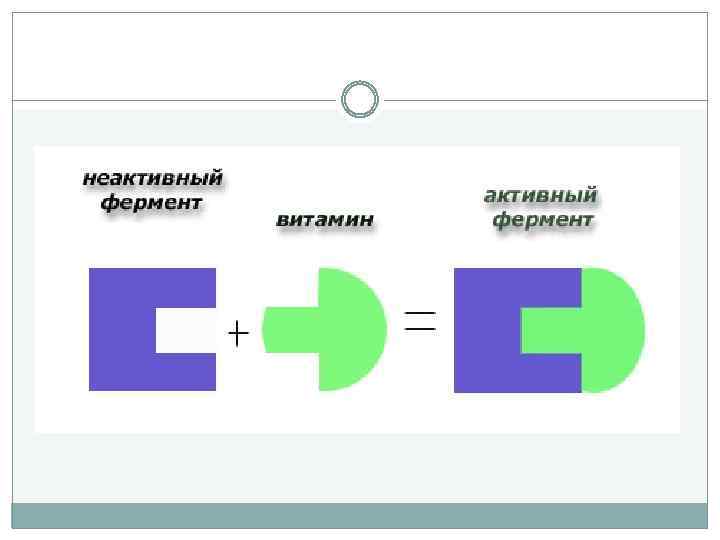
 Химическая кинетика Характерной особенностью действия ферментов является также высокая чувствительность активности ферментов к внешним условиям. Ферменты активны лишь в достаточно узком интервале р. Н и температуры; по обе стороны от этого интервала активность ферментов снижается.
Химическая кинетика Характерной особенностью действия ферментов является также высокая чувствительность активности ферментов к внешним условиям. Ферменты активны лишь в достаточно узком интервале р. Н и температуры; по обе стороны от этого интервала активность ферментов снижается.
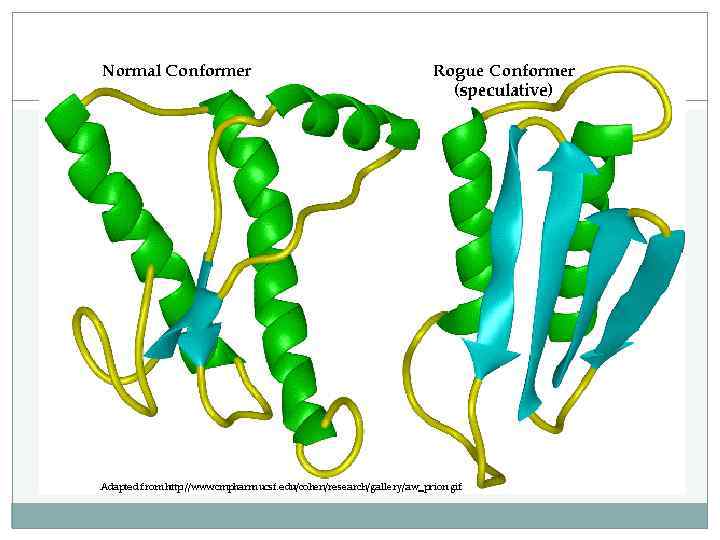
 Химическое равновесие — это такое состояние химической системы, в котором обратимо протекает одна или несколько химических реакций, причём скорости в каждой паре «прямая реакция – обратная реакция» равны между собой. Для системы, находящейся в химическом равновесии, также не изменяются со временем концентрация реагентов, температура и другие параметры системы.
Химическое равновесие — это такое состояние химической системы, в котором обратимо протекает одна или несколько химических реакций, причём скорости в каждой паре «прямая реакция – обратная реакция» равны между собой. Для системы, находящейся в химическом равновесии, также не изменяются со временем концентрация реагентов, температура и другие параметры системы.
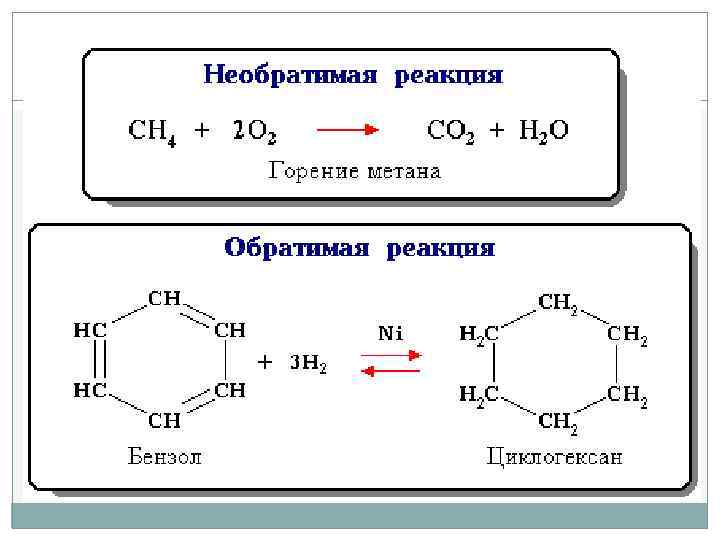
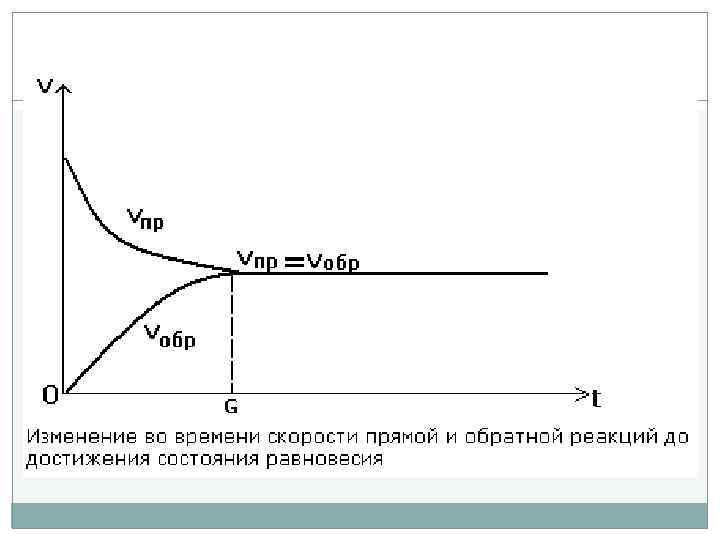
 Химическое равновесие Важно знать о способах смещения равновесия реакции в ту или иную сторону. Возможность смещения химического равновесия зависит подчиняется закономерности – принципу Ле-Шателье: если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какоелибо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, направленные на нейтрализацию внешнего воздействия
Химическое равновесие Важно знать о способах смещения равновесия реакции в ту или иную сторону. Возможность смещения химического равновесия зависит подчиняется закономерности – принципу Ле-Шателье: если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какоелибо из условий равновесия (температура, давление, концентрация, внешнее электромагнитное поле), то в системе усиливаются процессы, направленные на нейтрализацию внешнего воздействия
 Химическое равновесие Факторы влияющие на химическое равновесие: 1) температура: при увеличении температуры химическое равновесие смещается в сторону эндотермической (поглощение) реакции, а при понижении в сторону экзотермической (выделение) реакции. Ca. CO 3 ↔ Ca. O+CO 2 -Q N 2+3 H 2↔ 2 NH 3 +Q t↑ →, t↓ ← t↑ ←, t↓ →
Химическое равновесие Факторы влияющие на химическое равновесие: 1) температура: при увеличении температуры химическое равновесие смещается в сторону эндотермической (поглощение) реакции, а при понижении в сторону экзотермической (выделение) реакции. Ca. CO 3 ↔ Ca. O+CO 2 -Q N 2+3 H 2↔ 2 NH 3 +Q t↑ →, t↓ ← t↑ ←, t↓ →
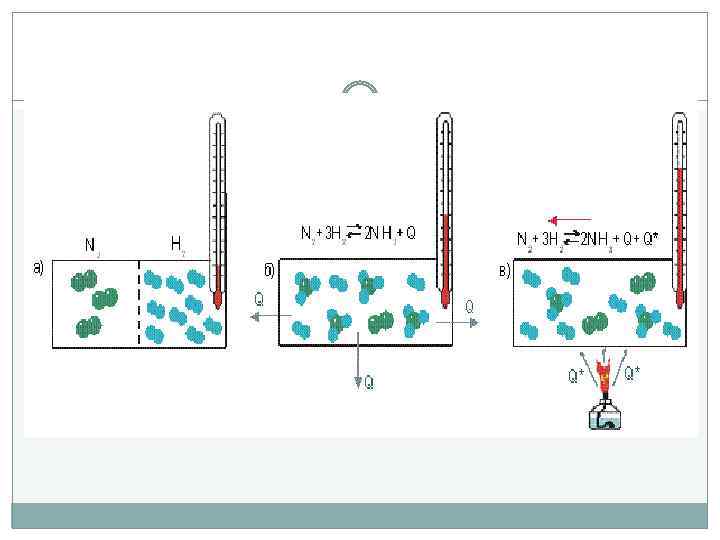
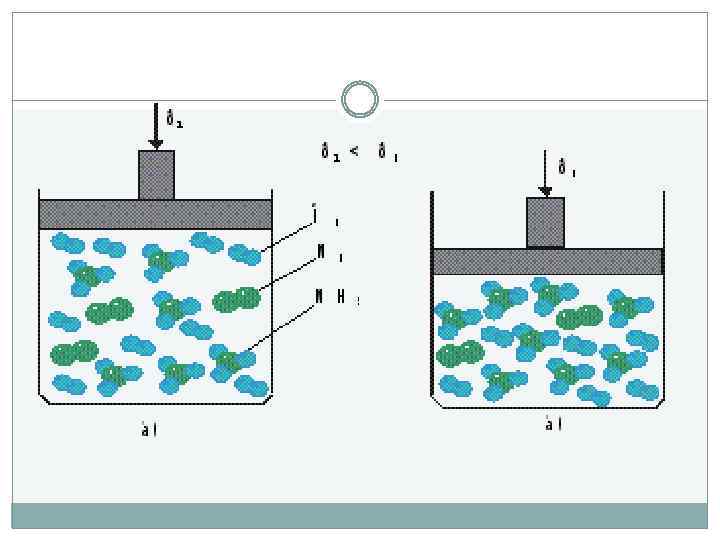
 Химическое равновесие 2) давление: при увеличении давления химическое равновесие смещается в сторону меньшего объёма веществ, а при понижении в сторону большего объёма. Этот принцип действует только на газы, т. е. если в реакции участвуют твердые вещества, то они в расчет не берутся. Ca. CO 3= Ca. O + CO 2 1 моль N 2 + 3 H 2 ↔ 2 NH 3 1 моль 3 моль 2 моль P↑ ←, P↓ → Р↑ →, Р↓←
Химическое равновесие 2) давление: при увеличении давления химическое равновесие смещается в сторону меньшего объёма веществ, а при понижении в сторону большего объёма. Этот принцип действует только на газы, т. е. если в реакции участвуют твердые вещества, то они в расчет не берутся. Ca. CO 3= Ca. O + CO 2 1 моль N 2 + 3 H 2 ↔ 2 NH 3 1 моль 3 моль 2 моль P↑ ←, P↓ → Р↑ →, Р↓←
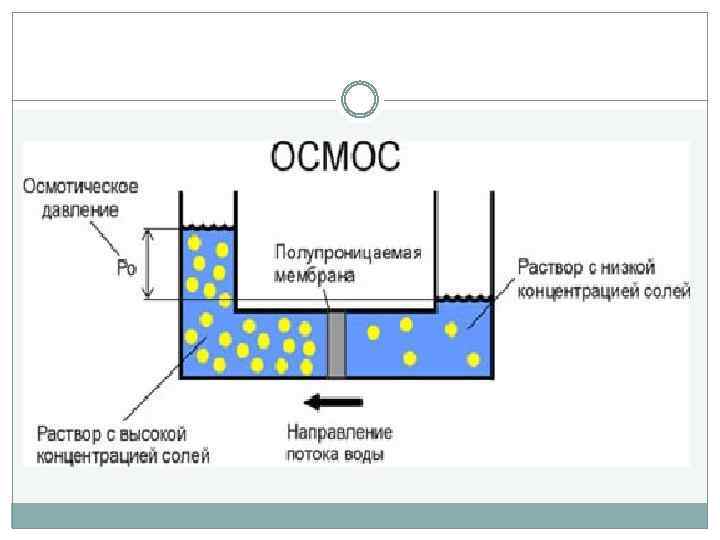
 Химическое равновесие 3) Концентрация веществ: при увеличении концентрации одного из исходных веществ химическое равновесие смещается в сторону продуктов реакции, а при увеличении концентрации продуктов реакции – в сторону исходных веществ. S 2+2 O 2=2 SO 2 [S], [O]↑ →, [SO 2]↑ ← Катализаторы не влияют на смещение химического равновесия!
Химическое равновесие 3) Концентрация веществ: при увеличении концентрации одного из исходных веществ химическое равновесие смещается в сторону продуктов реакции, а при увеличении концентрации продуктов реакции – в сторону исходных веществ. S 2+2 O 2=2 SO 2 [S], [O]↑ →, [SO 2]↑ ← Катализаторы не влияют на смещение химического равновесия!
 Слайды на «тройку» По кинетике: 2, 3, 4, 6, 7, 8, 9, 14, 15, 16, 17, 22, 23, 34, 35, 37, 38, 39, 41, 44, 45. По химическому равновесию: 56, 59, 60, 62, 64.
Слайды на «тройку» По кинетике: 2, 3, 4, 6, 7, 8, 9, 14, 15, 16, 17, 22, 23, 34, 35, 37, 38, 39, 41, 44, 45. По химическому равновесию: 56, 59, 60, 62, 64.


