 Химическая кинетика Расположение односторонних реакций, характеризующиеся графиками зависимости логарифма концентрации от времени (линии 1 – 4) в порядке возрастания константы скорости: 4<3<1<2 Расположение односторонних реакций, характеризующиеся графиками зависимости логарифма концентрации от времени (линии 1 – 4) в порядке возрастания времени полупревращения: 2<1<3<4
Химическая кинетика Расположение односторонних реакций, характеризующиеся графиками зависимости логарифма концентрации от времени (линии 1 – 4) в порядке возрастания константы скорости: 4<3<1<2 Расположение односторонних реакций, характеризующиеся графиками зависимости логарифма концентрации от времени (линии 1 – 4) в порядке возрастания времени полупревращения: 2<1<3<4
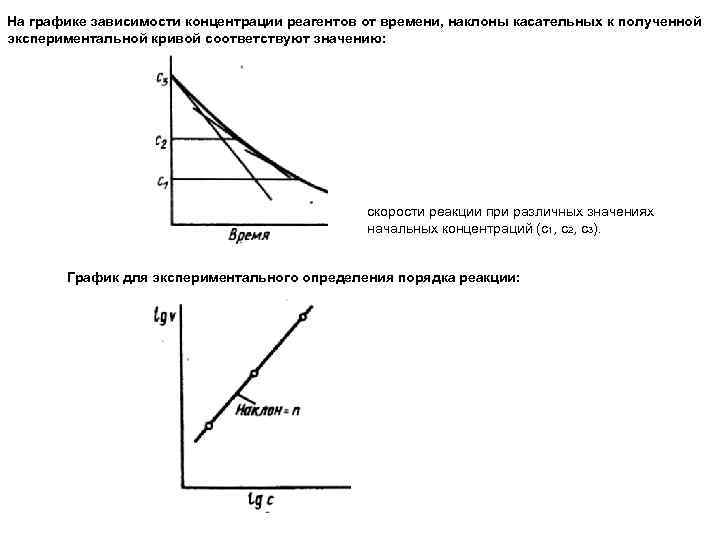 На графике зависимости концентрации реагентов от времени, наклоны касательных к полученной экспериментальной кривой соответствуют значению: скорости реакции при различных значениях начальных концентраций (с1, с2, с3). График для экспериментального определения порядка реакции:
На графике зависимости концентрации реагентов от времени, наклоны касательных к полученной экспериментальной кривой соответствуют значению: скорости реакции при различных значениях начальных концентраций (с1, с2, с3). График для экспериментального определения порядка реакции:
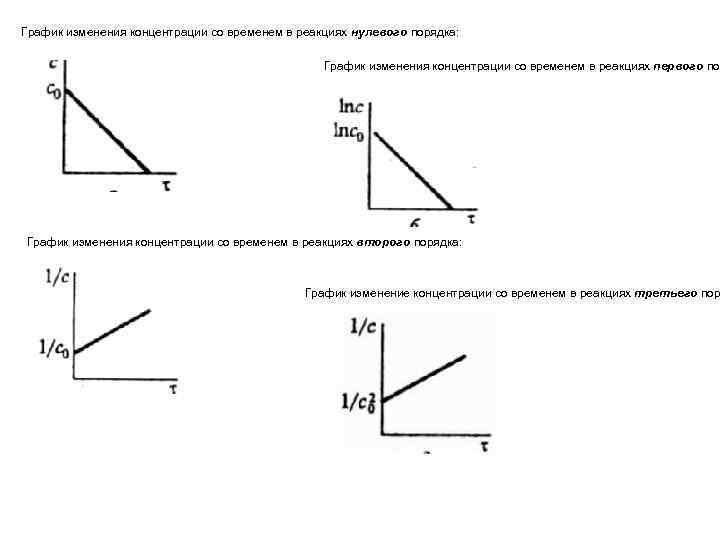 График изменения концентрации со временем в реакциях нулевого порядка: График изменения концентрации со временем в реакциях первого пор График изменения концентрации со временем в реакциях второго порядка: График изменение концентрации со временем в реакциях третьего пор
График изменения концентрации со временем в реакциях нулевого порядка: График изменения концентрации со временем в реакциях первого пор График изменения концентрации со временем в реакциях второго порядка: График изменение концентрации со временем в реакциях третьего пор
 Основной постулат: скорость химической реакции пропорциональна концентрации реагирующих веществ, взятых в некоторых степенях к – константа скорости химической реакции С – концентрация исходных веществ
Основной постулат: скорость химической реакции пропорциональна концентрации реагирующих веществ, взятых в некоторых степенях к – константа скорости химической реакции С – концентрация исходных веществ
 Элементарные реакции. Молекулярность Элементарные реакции – это реакции, протекающие в одну стадию, без образования промежуточных продуктов Молекулярность – число молекул, участвующих в элементарной реакции. Мономолекулярные реакции: Бимолекулярные реакции: Тримолекулярные реакции:
Элементарные реакции. Молекулярность Элементарные реакции – это реакции, протекающие в одну стадию, без образования промежуточных продуктов Молекулярность – число молекул, участвующих в элементарной реакции. Мономолекулярные реакции: Бимолекулярные реакции: Тримолекулярные реакции:
 Порядок реакции по веществу – это показатель степени при концентрации вещества в уравнение для скорости реакции Общий порядок реакции – это сумма порядков по каждому веществу, вступающему в реакцию
Порядок реакции по веществу – это показатель степени при концентрации вещества в уравнение для скорости реакции Общий порядок реакции – это сумма порядков по каждому веществу, вступающему в реакцию
 Кинетика необратимой реакции I-ого порядка размерность к: с-1 С 0 – начальная концентрация веществ (t=0)
Кинетика необратимой реакции I-ого порядка размерность к: с-1 С 0 – начальная концентрация веществ (t=0)
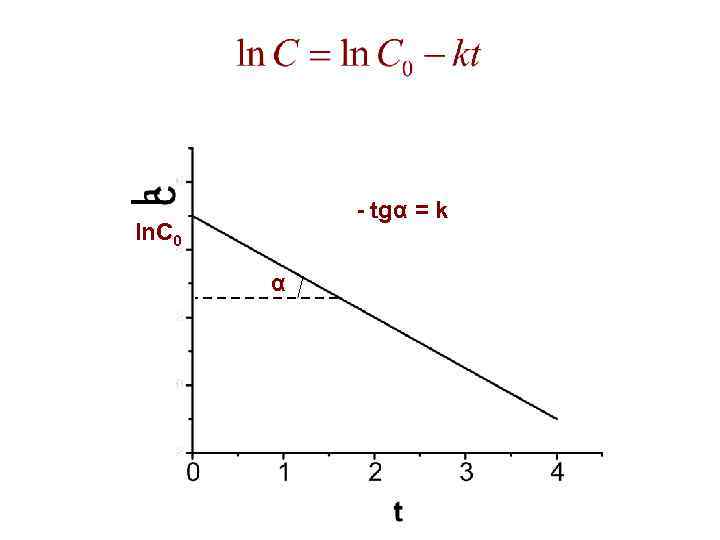 - tgα = k ln. С 0 α
- tgα = k ln. С 0 α
 Кинетика необратимой реакции II-ого порядка размерность к: л/(моль×с)
Кинетика необратимой реакции II-ого порядка размерность к: л/(моль×с)
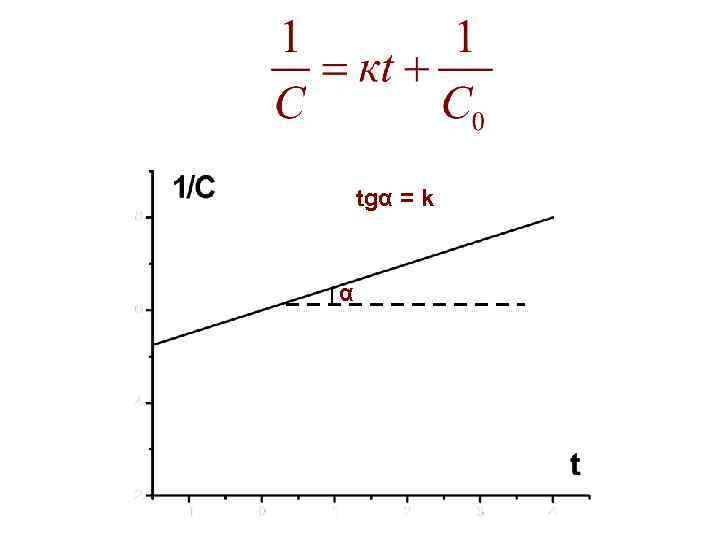 tgα = k α
tgα = k α
 Время полупревращения t 1/2 – время, за которое прореагирует половина начального количества исходного вещества Реакции I-ого порядка: Реакции II-ого порядка:
Время полупревращения t 1/2 – время, за которое прореагирует половина начального количества исходного вещества Реакции I-ого порядка: Реакции II-ого порядка:
 КИНЕТИЧЕСКИЕ УРАВНЕНИЯ РЕАКЦИЙ РАЗЛИЧНЫХ ПОРЯДКОВ И ИХ РЕШЕНИЯ
КИНЕТИЧЕСКИЕ УРАВНЕНИЯ РЕАКЦИЙ РАЗЛИЧНЫХ ПОРЯДКОВ И ИХ РЕШЕНИЯ