Химическая кинетика и равновесие.ppt
- Количество слайдов: 32
 Химическая кинетика и равновесие
Химическая кинетика и равновесие
 Химическая кинетика - раздел химии, изучающий скорости химической реакции. Химические реакции могут протекать в однородной фазе (гомогенные): HCl + Na. OH = Na. Cl + H 2 O и на границе раздела фаз (гетерогенные) : Zn + 2 HCl = H 2 + Zn. Cl 2
Химическая кинетика - раздел химии, изучающий скорости химической реакции. Химические реакции могут протекать в однородной фазе (гомогенные): HCl + Na. OH = Na. Cl + H 2 O и на границе раздела фаз (гетерогенные) : Zn + 2 HCl = H 2 + Zn. Cl 2
 Скорость гетерогенной реакции - это изменение количества вещества, вступающего в реакцию ( или образующегося в результате ее) за единицу времени на единице поверхности раздела фаз: Vгетер = ± ∆n / (∆ S) (1)
Скорость гетерогенной реакции - это изменение количества вещества, вступающего в реакцию ( или образующегося в результате ее) за единицу времени на единице поверхности раздела фаз: Vгетер = ± ∆n / (∆ S) (1)
 Скорость гомогенной реакции- это изменение количества вещества, вступающего в реакцию ( или образующегося в результате ее) за единицу времени в единице объема системы: Vгом. = ± ∆n / (∆ V) (2) т. к. С = ∆n/V (С- молярная конц-я) , то Vгом. = ± ∆С / ∆ (3)
Скорость гомогенной реакции- это изменение количества вещества, вступающего в реакцию ( или образующегося в результате ее) за единицу времени в единице объема системы: Vгом. = ± ∆n / (∆ V) (2) т. к. С = ∆n/V (С- молярная конц-я) , то Vгом. = ± ∆С / ∆ (3)
 Скорость реакции зависит от различных факторов: -природа реагирующих веществ; -концентрация реагентов; -температура; -присутствие катализатора.
Скорость реакции зависит от различных факторов: -природа реагирующих веществ; -концентрация реагентов; -температура; -присутствие катализатора.
 1. Зависимость скорости реакции от природы реагирующих веществ Вещества с ионными и ковалентными полярными связями в водных растворах взаимодействуют с высокими скоростями. Это связано с их диссоциацией на ионы, которые легко реагируют друг с другом. KCl + Ag. NO 3 Ag. Cl + Na. NO 3 Ag+ + Cl- Ag. Cl
1. Зависимость скорости реакции от природы реагирующих веществ Вещества с ионными и ковалентными полярными связями в водных растворах взаимодействуют с высокими скоростями. Это связано с их диссоциацией на ионы, которые легко реагируют друг с другом. KCl + Ag. NO 3 Ag. Cl + Na. NO 3 Ag+ + Cl- Ag. Cl
 Вещества с неполярными и малополярными ковалентными связями взаимодействуют с различной V. Все зависит от их химической активности. Например, реакция взаимодействия H 2 с F 2 протекает очень быстро (со взрывом) при комнатной температуре, а реакция между H 2 и Br 2 идет медленно при нагревании: H 2 + F 2 2 HF H 2 +Br 2 2 HBr
Вещества с неполярными и малополярными ковалентными связями взаимодействуют с различной V. Все зависит от их химической активности. Например, реакция взаимодействия H 2 с F 2 протекает очень быстро (со взрывом) при комнатной температуре, а реакция между H 2 и Br 2 идет медленно при нагревании: H 2 + F 2 2 HF H 2 +Br 2 2 HBr
 2. Влияние концентрации реагирующих веществ Взаимодействие между молекулами воз-можно при взаимном столкновении, когда атомы одной молекулы попадают в сферу действия электрических полей, создаваемых атомами другой молекулы. Именно в этих условиях происходят переходы электронов, в результате которых образуются новые мо-лекулы. Не каждое столкновение приводит к взаимодействию, а небольшая часть их.
2. Влияние концентрации реагирующих веществ Взаимодействие между молекулами воз-можно при взаимном столкновении, когда атомы одной молекулы попадают в сферу действия электрических полей, создаваемых атомами другой молекулы. Именно в этих условиях происходят переходы электронов, в результате которых образуются новые мо-лекулы. Не каждое столкновение приводит к взаимодействию, а небольшая часть их.
 Чем больше число соударений, т. е. чем выше концентрация исходных веществ, тем выше V. Закон действующих масс (закон К. Гульдберга и П. Вааге): При постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях, равных их стехиометрическим коэффициентам в уравнении реакции.
Чем больше число соударений, т. е. чем выше концентрация исходных веществ, тем выше V. Закон действующих масс (закон К. Гульдберга и П. Вааге): При постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях, равных их стехиометрическим коэффициентам в уравнении реакции.
 Для реакции 2 А + В С кинетическое уравнение согласно закону действующих масс имеет вид: V = k C A 2 CB , где CA и CB - концентрации веществ А и В соответственно; k – константа скорости реакции. Константа скорости зависит от природы реагирующих веществ, температуры и наличия катализатора, но не зависит от их концентрации.
Для реакции 2 А + В С кинетическое уравнение согласно закону действующих масс имеет вид: V = k C A 2 CB , где CA и CB - концентрации веществ А и В соответственно; k – константа скорости реакции. Константа скорости зависит от природы реагирующих веществ, температуры и наличия катализатора, но не зависит от их концентрации.
 Она численно равна скорости химической реакции в условиях, когда концентрация каждого из исходных веществ равна 1 моль/л. Закон действия масс справедлив для простых реакций. Если реакция протекает через ряд последовательных или параллельных стадий, то закон применим к каждой из них в отдельности, но не к реакции в целом.
Она численно равна скорости химической реакции в условиях, когда концентрация каждого из исходных веществ равна 1 моль/л. Закон действия масс справедлив для простых реакций. Если реакция протекает через ряд последовательных или параллельных стадий, то закон применим к каждой из них в отдельности, но не к реакции в целом.
 Концентрации твердых веществ в кинетическое уравнение реакции не входят. Для гетерогенной реакции WO 3(тв) + 3 H 2 (г) W(тв) + 3 H 2 O(г) кинетическое уравнение имеет 3 вид: V = k CH 2
Концентрации твердых веществ в кинетическое уравнение реакции не входят. Для гетерогенной реакции WO 3(тв) + 3 H 2 (г) W(тв) + 3 H 2 O(г) кинетическое уравнение имеет 3 вид: V = k CH 2
 В химической кинетике реакции классифицируются по двум параметрам: по молекулярности и по порядку реакции. Молекулярность реакции определяется числом молекул, одновременным взаимодействием которых осуществляется химическое превращение. По этому признаку реакции разделяют на моно-, би-, тримолекулярные. Вероятность одновременного столкновения трех молекул очень мала.
В химической кинетике реакции классифицируются по двум параметрам: по молекулярности и по порядку реакции. Молекулярность реакции определяется числом молекул, одновременным взаимодействием которых осуществляется химическое превращение. По этому признаку реакции разделяют на моно-, би-, тримолекулярные. Вероятность одновременного столкновения трех молекул очень мала.
 Такие реакции протекают более сложным путем – через последовательные или параллельные стадии. Мономолекулярная реакция : I 2 2 I, V = k CI 2 Бимолекулярная реакция: H 2 +I 2 2 HI V = k CI 2 CH 2 или 2 HI H 2 +I 2 V = k CHI 2 Тримолекулярные реакции: 2 NO +O 2 2 NO 2 V = k CNO 2 CO 2
Такие реакции протекают более сложным путем – через последовательные или параллельные стадии. Мономолекулярная реакция : I 2 2 I, V = k CI 2 Бимолекулярная реакция: H 2 +I 2 2 HI V = k CI 2 CH 2 или 2 HI H 2 +I 2 V = k CHI 2 Тримолекулярные реакции: 2 NO +O 2 2 NO 2 V = k CNO 2 CO 2
 Общий порядок реакции – сумма степеней в кинетическом уравнении. Порядок химической реакции по данному компоненту – это число, равное степени, в которой концентрация вещества входит в кинетическое уравнение. Например, реакция: а. А + b. В с. С +d. Д, V = k C А а CВb. Общий порядок реакции n =а+b , порядок по компоненту А равен а, по компоненту В – b.
Общий порядок реакции – сумма степеней в кинетическом уравнении. Порядок химической реакции по данному компоненту – это число, равное степени, в которой концентрация вещества входит в кинетическое уравнение. Например, реакция: а. А + b. В с. С +d. Д, V = k C А а CВb. Общий порядок реакции n =а+b , порядок по компоненту А равен а, по компоненту В – b.
 Реакции подразделяются на реакции первого, второго и третьего порядка. Для простых реакции порядок реакции и молекулярность совпадают. Для многостадийных процессов, они не совпадают. Скорость всего процесса определяется наименьшей скоростью , с которой протекает одна из стадий процесса. Кинетическое уравнение записывают только для данной стадии, ее называют лимитирующей.
Реакции подразделяются на реакции первого, второго и третьего порядка. Для простых реакции порядок реакции и молекулярность совпадают. Для многостадийных процессов, они не совпадают. Скорость всего процесса определяется наименьшей скоростью , с которой протекает одна из стадий процесса. Кинетическое уравнение записывают только для данной стадии, ее называют лимитирующей.
 3. Влияние температуры на скорость реакции. Правило Вант-Гоффа : При повышении температуры на 10 С скорость химической реакции увеличивается в 2 -4 раза. - температурный коэффициент, показывает во сколько раз изменяется V при изменении t на 10 С, Vt 1 и Vt 2 – скорости реакции при температурах t 1 и t 2.
3. Влияние температуры на скорость реакции. Правило Вант-Гоффа : При повышении температуры на 10 С скорость химической реакции увеличивается в 2 -4 раза. - температурный коэффициент, показывает во сколько раз изменяется V при изменении t на 10 С, Vt 1 и Vt 2 – скорости реакции при температурах t 1 и t 2.
 При повышении t увеличивается число столкновений молекул. Однако согласно расчетам общее число столкновений молекул при увеличении температуры на 10 возрастает лишь в 1, 6 раза, тогда как число прореагировавших молекул возрастает на 200 - 400%. С. Аррениус предположил, что причина состоит в увеличении числа активных молекул, т. е. таких, столкновение которых приводит к образованию продукта.
При повышении t увеличивается число столкновений молекул. Однако согласно расчетам общее число столкновений молекул при увеличении температуры на 10 возрастает лишь в 1, 6 раза, тогда как число прореагировавших молекул возрастает на 200 - 400%. С. Аррениус предположил, что причина состоит в увеличении числа активных молекул, т. е. таких, столкновение которых приводит к образованию продукта.
 Энергия активации(Еа)-это энергия, которой должны обладать молекулы для эффективного столкновения; R – универсальная газовая постоянная (8, 31 Дж/(моль*К), Т -температура (К), k-константа скорости реакции.
Энергия активации(Еа)-это энергия, которой должны обладать молекулы для эффективного столкновения; R – универсальная газовая постоянная (8, 31 Дж/(моль*К), Т -температура (К), k-константа скорости реакции.
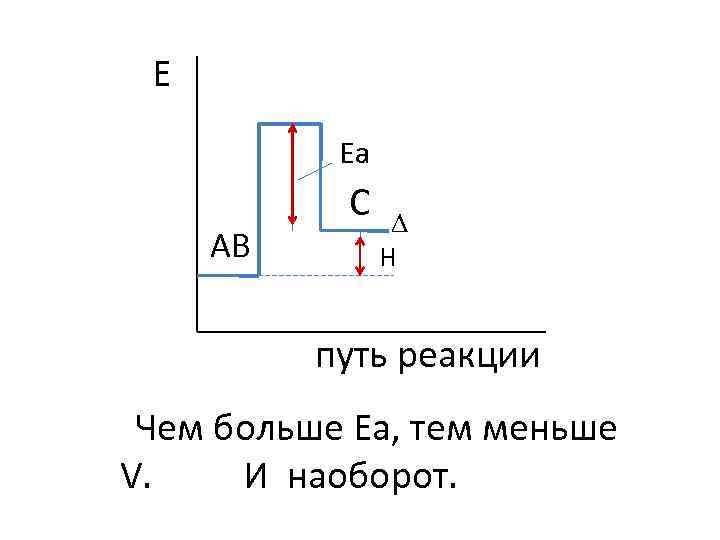 Е Еа АВ С Н путь реакции Чем больше Еа, тем меньше V. И наоборот.
Е Еа АВ С Н путь реакции Чем больше Еа, тем меньше V. И наоборот.
 В ходе реакции разрываются или ослабляются связи между атомами в молекулах исходных веществ. При этом образуется неустойчивое промежуточное соединение - активированный комплекс, обладающее большим запасом энергии. При его распаде образуются продукты реакции. Разность между энергией активированного комплекса и средней энергией исходных молекул и есть энергия активации.
В ходе реакции разрываются или ослабляются связи между атомами в молекулах исходных веществ. При этом образуется неустойчивое промежуточное соединение - активированный комплекс, обладающее большим запасом энергии. При его распаде образуются продукты реакции. Разность между энергией активированного комплекса и средней энергией исходных молекул и есть энергия активации.
 4. Влияние катализатора на скорость химической реакции Катализаторами называют вещества, которые изменяют скорость реакции, а сами к концу процесса остаются неизменным как по составу, так и по массе. Явление изменения скорости реакции в присутствии катализаторов называется катализом. Катализ бывает положительным и отрицательным, гомогенным и гетерогенным.
4. Влияние катализатора на скорость химической реакции Катализаторами называют вещества, которые изменяют скорость реакции, а сами к концу процесса остаются неизменным как по составу, так и по массе. Явление изменения скорости реакции в присутствии катализаторов называется катализом. Катализ бывает положительным и отрицательным, гомогенным и гетерогенным.
 Суть катализа состоит в том, что катализатор (положительный катализ), образуя с реагентом промежуточное соединение, понижает энергию активации реакции. A +B = AB A + K = AK AK + B = AB + K При отрицательном катализе (ингибирование) энергия активации увеличивается.
Суть катализа состоит в том, что катализатор (положительный катализ), образуя с реагентом промежуточное соединение, понижает энергию активации реакции. A +B = AB A + K = AK AK + B = AB + K При отрицательном катализе (ингибирование) энергия активации увеличивается.
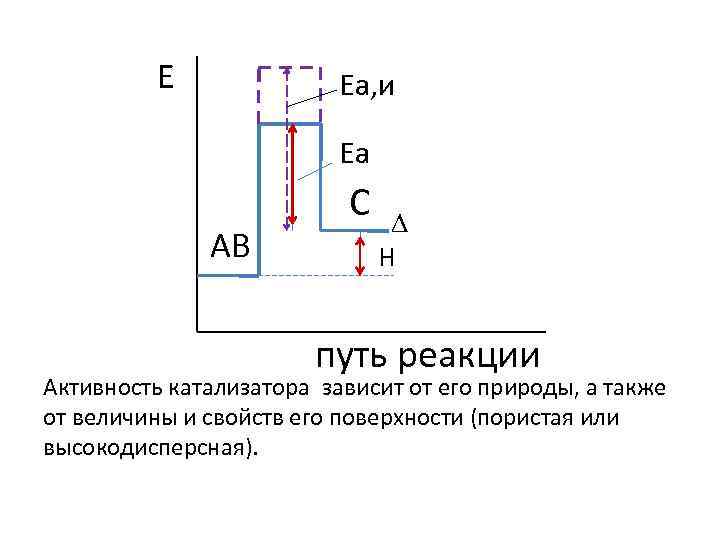 Е Еа, и Еа АВ С Н путь реакции Активность катализатора зависит от его природы, а также от величины и свойств его поверхности (пористая или высокодисперсная).
Е Еа, и Еа АВ С Н путь реакции Активность катализатора зависит от его природы, а также от величины и свойств его поверхности (пористая или высокодисперсная).
 Химическое равновесие Большинство химических процессов являются обратимыми. Для общего случая можно записать a. A + b. B c. C + d. D Скорость прямой реакции имеет выражение V 1 = k 1[A]a[B]b. По мере снижения концентрации реагентов она убывает. Накопление продуктов реакции создает условия для протекания обратного процесса, скорость которого V 2 = k 2[C]c[D]d возрастает.
Химическое равновесие Большинство химических процессов являются обратимыми. Для общего случая можно записать a. A + b. B c. C + d. D Скорость прямой реакции имеет выражение V 1 = k 1[A]a[B]b. По мере снижения концентрации реагентов она убывает. Накопление продуктов реакции создает условия для протекания обратного процесса, скорость которого V 2 = k 2[C]c[D]d возрастает.
 Через некоторое время скорости уравняются. Состояние системы, при котором скорости прямой и обратной реакции равны, называется химическим равновесием. Концентрации реагентов и продуктов, отвечающие состоянию равновесия, называются равновесными концентрациями.
Через некоторое время скорости уравняются. Состояние системы, при котором скорости прямой и обратной реакции равны, называется химическим равновесием. Концентрации реагентов и продуктов, отвечающие состоянию равновесия, называются равновесными концентрациями.
 Если скорости равны Oтношение их констант – величинa постоянная (константа равновесия)
Если скорости равны Oтношение их констант – величинa постоянная (константа равновесия)
 Закон действующих масс для ХР : Отношение произведений равновесных концентраций веществ левой и правой частей уравнения, возведенных в степени их стехиометрических коэффициентов, представляют постоянную величину, независимо от условий, при которых осуществляется реакция, если температура остается постоянной.
Закон действующих масс для ХР : Отношение произведений равновесных концентраций веществ левой и правой частей уравнения, возведенных в степени их стехиометрических коэффициентов, представляют постоянную величину, независимо от условий, при которых осуществляется реакция, если температура остается постоянной.
 Действие различных внешних факторов приводит к смещению химического равновесия. Принцип Ле Шателье: Внешнее воздействие на систему, находящуюся в состоянии равновесия, приводит к смещению равновесия в направлении, при котором эффект произведенного воздействия ослабляется.
Действие различных внешних факторов приводит к смещению химического равновесия. Принцип Ле Шателье: Внешнее воздействие на систему, находящуюся в состоянии равновесия, приводит к смещению равновесия в направлении, при котором эффект произведенного воздействия ослабляется.
 Температура – ее повышение ускоряет прямую и обратную реакции в разной степени. Эндотермический процесс ускоряется больше, поэтому повышение температуры способствует смещению равновесия в сторону эндотермической реакции. Давление (для реакций в газовой фазе). Если реакция идет с увеличением числа молей газа, то уменьшение давления смещает равновесие вправо.
Температура – ее повышение ускоряет прямую и обратную реакции в разной степени. Эндотермический процесс ускоряется больше, поэтому повышение температуры способствует смещению равновесия в сторону эндотермической реакции. Давление (для реакций в газовой фазе). Если реакция идет с увеличением числа молей газа, то уменьшение давления смещает равновесие вправо.
 Концентрация. С увеличением концентрации одного из реагентов равновесие смещается вправо, при добавлении в реакционную смесь одного из продуктов превращения равновесие смещается влево. Использование катализаторов не смещает равновесие, т. к. ускоряет (замедляет) скорость как прямой, так и обратной реакции, но способствует более быстрому установлению равновесия.
Концентрация. С увеличением концентрации одного из реагентов равновесие смещается вправо, при добавлении в реакционную смесь одного из продуктов превращения равновесие смещается влево. Использование катализаторов не смещает равновесие, т. к. ускоряет (замедляет) скорость как прямой, так и обратной реакции, но способствует более быстрому установлению равновесия.
 Например, для равновесной реакции 3 H 2+N 2 2 NH 3; Н 0 сместить ХР вправо можно: 1. Увеличивая [N 2]или [H 2], или уменьшая концентрацию [NH 3] 2. Повысив давление, Р 3. Понизив температуру, Т
Например, для равновесной реакции 3 H 2+N 2 2 NH 3; Н 0 сместить ХР вправо можно: 1. Увеличивая [N 2]или [H 2], или уменьшая концентрацию [NH 3] 2. Повысив давление, Р 3. Понизив температуру, Т


