кинетика 2.ppt
- Количество слайдов: 55
 ХИМИЧЕСКАЯ КИНЕТИКА ФИЗИЧЕСКАЯ ХИМИЯ. ЛЕКЦИИ. Чигорина Татьяна Михайловна
ХИМИЧЕСКАЯ КИНЕТИКА ФИЗИЧЕСКАЯ ХИМИЯ. ЛЕКЦИИ. Чигорина Татьяна Михайловна
 Что изучает химическая кинетика? Химическая кинетика изучает скорости протекания химических процессов и их механизм Основные задачи химической кинетики: расчёт скоростей реакций и определение кинетических кривых, т. е. зависимости концентраций реагирующих веществ от времени (прямая задача) определение механизмов реакций по кинетическим кривым (обратная задача) Знание механизма реакции, факторов, влияющих на скорость реакции позволяет управлять скоростью химической реакции 2
Что изучает химическая кинетика? Химическая кинетика изучает скорости протекания химических процессов и их механизм Основные задачи химической кинетики: расчёт скоростей реакций и определение кинетических кривых, т. е. зависимости концентраций реагирующих веществ от времени (прямая задача) определение механизмов реакций по кинетическим кривым (обратная задача) Знание механизма реакции, факторов, влияющих на скорость реакции позволяет управлять скоростью химической реакции 2
 Скорость химической реакции Скорость гомогенной химической реакции (в газовой фазе или в растворе) – это изменение концентрации одного из реагентов или продуктов реакции в единицу времени в единице объёма: Знак (+) используют, если скорость определяют по продукту, а (-) – если по исходному веществу Скорость химической реакции может быть измерена по любому компоненту, участвующему в реакции. Она всегда положительна, поэтому знак перед производной dni/dτ определяется тем, является ли вещество исходным реагентом (тогда dni/dτ отрицательна) или продуктом (тогда dni/dτ положительна) Если реакция протекает при постоянном объёме, скорость определяют как изменение молярной концентрации ci в единицу времени: 3
Скорость химической реакции Скорость гомогенной химической реакции (в газовой фазе или в растворе) – это изменение концентрации одного из реагентов или продуктов реакции в единицу времени в единице объёма: Знак (+) используют, если скорость определяют по продукту, а (-) – если по исходному веществу Скорость химической реакции может быть измерена по любому компоненту, участвующему в реакции. Она всегда положительна, поэтому знак перед производной dni/dτ определяется тем, является ли вещество исходным реагентом (тогда dni/dτ отрицательна) или продуктом (тогда dni/dτ положительна) Если реакция протекает при постоянном объёме, скорость определяют как изменение молярной концентрации ci в единицу времени: 3
 Скорость химической реакции Если химическая реакция описывается стехиометрическим уравнением a. A + b. B → r. R + s. S то изменение количеств реагентов и продуктов Δni в результате её протекания связаны между собой соотношениями: С учётом стехиометрических коэффициентов скорость реакции равна где i – стехиометрический коэффициент у вещества, по которому рассчитывают скорость реакции Тогда скорость приводится к общему знаменателю и независимо от того, по изменению какого конкретного реагента или продукта она определялась, будет численно одинакова, т. е. 4
Скорость химической реакции Если химическая реакция описывается стехиометрическим уравнением a. A + b. B → r. R + s. S то изменение количеств реагентов и продуктов Δni в результате её протекания связаны между собой соотношениями: С учётом стехиометрических коэффициентов скорость реакции равна где i – стехиометрический коэффициент у вещества, по которому рассчитывают скорость реакции Тогда скорость приводится к общему знаменателю и независимо от того, по изменению какого конкретного реагента или продукта она определялась, будет численно одинакова, т. е. 4
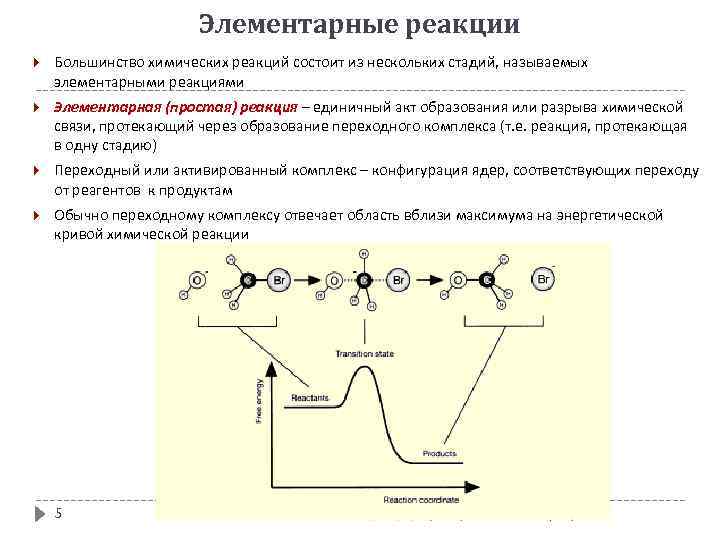 Элементарные реакции Большинство химических реакций состоит из нескольких стадий, называемых элементарными реакциями Элементарная (простая) реакция – единичный акт образования или разрыва химической связи, протекающий через образование переходного комплекса (т. е. реакция, протекающая в одну стадию) Переходный или активированный комплекс – конфигурация ядер, соответствующих переходу от реагентов к продуктам Обычно переходному комплексу отвечает область вблизи максимума на энергетической кривой химической реакции 5
Элементарные реакции Большинство химических реакций состоит из нескольких стадий, называемых элементарными реакциями Элементарная (простая) реакция – единичный акт образования или разрыва химической связи, протекающий через образование переходного комплекса (т. е. реакция, протекающая в одну стадию) Переходный или активированный комплекс – конфигурация ядер, соответствующих переходу от реагентов к продуктам Обычно переходному комплексу отвечает область вблизи максимума на энергетической кривой химической реакции 5
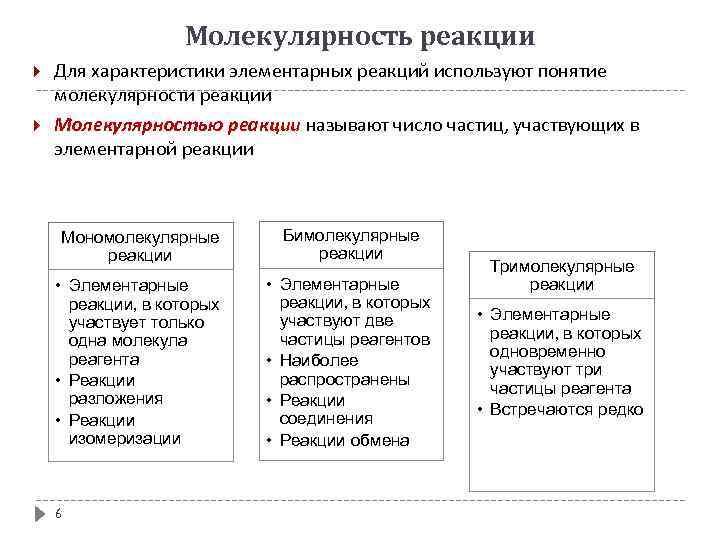 Молекулярность реакции Для характеристики элементарных реакций используют понятие молекулярности реакции Молекулярностью реакции называют число частиц, участвующих в элементарной реакции Мономолекулярные реакции Бимолекулярные реакции • Элементарные реакции, в которых участвует только одна молекула реагента • Реакции разложения • Реакции изомеризации • Элементарные реакции, в которых участвуют две частицы реагентов • Наиболее распространены • Реакции соединения • Реакции обмена 6 Тримолекулярные реакции • Элементарные реакции, в которых одновременно участвуют три частицы реагента • Встречаются редко
Молекулярность реакции Для характеристики элементарных реакций используют понятие молекулярности реакции Молекулярностью реакции называют число частиц, участвующих в элементарной реакции Мономолекулярные реакции Бимолекулярные реакции • Элементарные реакции, в которых участвует только одна молекула реагента • Реакции разложения • Реакции изомеризации • Элементарные реакции, в которых участвуют две частицы реагентов • Наиболее распространены • Реакции соединения • Реакции обмена 6 Тримолекулярные реакции • Элементарные реакции, в которых одновременно участвуют три частицы реагента • Встречаются редко
 Механизм реакции Сложная реакция состоит из нескольких элементарных реакций Совокупность элементарных реакций называют механизмом реакции Скорость сложной реакции определяется скоростью самой медленной её стадии (лимитирующая стадия) Уравнение химической реакции не отражает её механизма По уравнению реакции нельзя сказать, является ли реакция элементарной или сложной 7
Механизм реакции Сложная реакция состоит из нескольких элементарных реакций Совокупность элементарных реакций называют механизмом реакции Скорость сложной реакции определяется скоростью самой медленной её стадии (лимитирующая стадия) Уравнение химической реакции не отражает её механизма По уравнению реакции нельзя сказать, является ли реакция элементарной или сложной 7
 Факторы, влияющие на скорость реакции Природа реагирующих веществ (тип химических связей в молекулах реагентов, прочность связей, строение кристаллической решётки, строение электронной оболочки атома, прочность связывания внешних электронов и др. Концентрация реагентов Температура Давление Катализатор Степень перемешивания веществ 8
Факторы, влияющие на скорость реакции Природа реагирующих веществ (тип химических связей в молекулах реагентов, прочность связей, строение кристаллической решётки, строение электронной оболочки атома, прочность связывания внешних электронов и др. Концентрация реагентов Температура Давление Катализатор Степень перемешивания веществ 8
 Постулаты химической кинетики Законы химической кинетики основаны на двух принципах (постулатах): скорость химической реакции пропорциональна концентрациям реагентов суммарная скорость нескольких последовательных превращений, широко различающихся по скорости, определяется скоростью наиболее медленной стадии 9
Постулаты химической кинетики Законы химической кинетики основаны на двух принципах (постулатах): скорость химической реакции пропорциональна концентрациям реагентов суммарная скорость нескольких последовательных превращений, широко различающихся по скорости, определяется скоростью наиболее медленной стадии 9
 Влияние концентрации реагирующих веществ на скорость реакции Функциональная зависимость скорости химической реакции от концентраций компонентов называется кинетическим уравнением реакции Основной постулат химической кинетики или закон действующих масс: скорость химической реакции при постоянной температуре в каждый момент времени пропорциональна текущим концентрациям реагирующих веществ, возведённым в некоторые степени Для необратимой элементарной химической реакции a. A + b. B → r. R + s. S скорость равна где k – константа скорости химической реакции; зависит только от температуры a и b – порядки реакции по реагентам (частные порядки) соответственно А и В, совпадают со стехиометрическим коэффициентом Их сумма a + b = n называется общим порядком реакции 10
Влияние концентрации реагирующих веществ на скорость реакции Функциональная зависимость скорости химической реакции от концентраций компонентов называется кинетическим уравнением реакции Основной постулат химической кинетики или закон действующих масс: скорость химической реакции при постоянной температуре в каждый момент времени пропорциональна текущим концентрациям реагирующих веществ, возведённым в некоторые степени Для необратимой элементарной химической реакции a. A + b. B → r. R + s. S скорость равна где k – константа скорости химической реакции; зависит только от температуры a и b – порядки реакции по реагентам (частные порядки) соответственно А и В, совпадают со стехиометрическим коэффициентом Их сумма a + b = n называется общим порядком реакции 10
 Порядок сложной реакции по веществу в общем случае не совпадает с коэффициентами в уравнении реакции Общий порядок реакции равен сумме показателей степеней в уравнении скорости реакции Для реакции a. A + b. B + d. D → r. R + s. S + q. Q кинетическое уравнение где частные порядки α, β и δ находят экспериментально В общем случае α≠a, β≠b и δ≠d, т. е. молекулярность и порядок реакции не совпадают Общий порядок реакции равен сумме показателей степеней в уравнении скорости реакции: n=α+β+δ Порядок реакции может быть положительным и отрицательным, целым и дробным 11
Порядок сложной реакции по веществу в общем случае не совпадает с коэффициентами в уравнении реакции Общий порядок реакции равен сумме показателей степеней в уравнении скорости реакции Для реакции a. A + b. B + d. D → r. R + s. S + q. Q кинетическое уравнение где частные порядки α, β и δ находят экспериментально В общем случае α≠a, β≠b и δ≠d, т. е. молекулярность и порядок реакции не совпадают Общий порядок реакции равен сумме показателей степеней в уравнении скорости реакции: n=α+β+δ Порядок реакции может быть положительным и отрицательным, целым и дробным 11
 Лекция 1. Кинетические уравнения 0, 1, 2, 3 порядков
Лекция 1. Кинетические уравнения 0, 1, 2, 3 порядков
 Реакции нулевого порядка Реакциями нулевого порядка по данному веществу являются реакции в закрытой системе про постоянном подводе одного из веществ, обеспечивающем его концентрацию постоянной, или при содержании малорастворимой твёрдой фазы при условии, что скорость растворения велика (т. е. ) Скорость этих реакций не зависит от концентрации реагирующих веществ и равна константе скорости: v=k Кинетическое уравнение: Разделяя переменные и интегрируя, получим: (или ) Особенности реакций нулевого порядка: 1. 2. 3. 13 Концентрация исходного вещества линейно уменьшается во времени Константа скорости и время, необходимое для достижения заданной концентрации Время полупревращения (период полураспада) – время, за которое превращается половина вещества (т. е. С=1/2 С₀) Кинетическая кривая реакции нулевого порядка
Реакции нулевого порядка Реакциями нулевого порядка по данному веществу являются реакции в закрытой системе про постоянном подводе одного из веществ, обеспечивающем его концентрацию постоянной, или при содержании малорастворимой твёрдой фазы при условии, что скорость растворения велика (т. е. ) Скорость этих реакций не зависит от концентрации реагирующих веществ и равна константе скорости: v=k Кинетическое уравнение: Разделяя переменные и интегрируя, получим: (или ) Особенности реакций нулевого порядка: 1. 2. 3. 13 Концентрация исходного вещества линейно уменьшается во времени Константа скорости и время, необходимое для достижения заданной концентрации Время полупревращения (период полураспада) – время, за которое превращается половина вещества (т. е. С=1/2 С₀) Кинетическая кривая реакции нулевого порядка
 Примеры реакций нулевого порядка Реакции нулевого порядка встречаются в гетерогенных процессах, гетерогенном катализе и всегда указывают на протекание сложной реакции, состоящей из нескольких последовательных стадий Лимитирующей стадией является диффузия, поэтому химическое превращение не влияет на скорость Гетерогенная реакция горения углерода С (т) + О₂(г) = СО₂(г) при большом парциальном давлении кислорода (например, когда применяют дутье), израсходованный кислород практически сразу восполняется; при уменьшении парциального давления кислорода до определенной величины порядок реакции становится первым Гидрирование этилена на платине: С₂Н₄+Н₂ => (Pt) => C₂H₆ Скорость реакции здесь определяется площадью поверхности катализатора и не зависит от концентрации реагирующих веществ Разложение на платиновой проволоке оксида азота (I) или аммиака 2 N₂O => (Pt) => 2 N₂+O₂ 2 NH₃ => (Pt) =>N₂+3 H₂ Омыление малорастворимого сложного эфира водой в разбавленном водном растворе (эфир в избытке), чтобы в системе присутствовал эфирный слой, то расход эфира будет постоянно восполняться из эфирного слоя Фотохимические реакции (скорость процесса лимитируется подачей энергии, необходимой для активации реагирующих молекул) 14
Примеры реакций нулевого порядка Реакции нулевого порядка встречаются в гетерогенных процессах, гетерогенном катализе и всегда указывают на протекание сложной реакции, состоящей из нескольких последовательных стадий Лимитирующей стадией является диффузия, поэтому химическое превращение не влияет на скорость Гетерогенная реакция горения углерода С (т) + О₂(г) = СО₂(г) при большом парциальном давлении кислорода (например, когда применяют дутье), израсходованный кислород практически сразу восполняется; при уменьшении парциального давления кислорода до определенной величины порядок реакции становится первым Гидрирование этилена на платине: С₂Н₄+Н₂ => (Pt) => C₂H₆ Скорость реакции здесь определяется площадью поверхности катализатора и не зависит от концентрации реагирующих веществ Разложение на платиновой проволоке оксида азота (I) или аммиака 2 N₂O => (Pt) => 2 N₂+O₂ 2 NH₃ => (Pt) =>N₂+3 H₂ Омыление малорастворимого сложного эфира водой в разбавленном водном растворе (эфир в избытке), чтобы в системе присутствовал эфирный слой, то расход эфира будет постоянно восполняться из эфирного слоя Фотохимические реакции (скорость процесса лимитируется подачей энергии, необходимой для активации реагирующих молекул) 14
 Реакции первого порядка Это реакции типа А => продукты Скорость реакции прямо пропорциональна концентрации, т. е. кинетическое уравнение: Разделяя переменные и интегрируя, получим Кинетические кривые реакций первого порядка: 15
Реакции первого порядка Это реакции типа А => продукты Скорость реакции прямо пропорциональна концентрации, т. е. кинетическое уравнение: Разделяя переменные и интегрируя, получим Кинетические кривые реакций первого порядка: 15
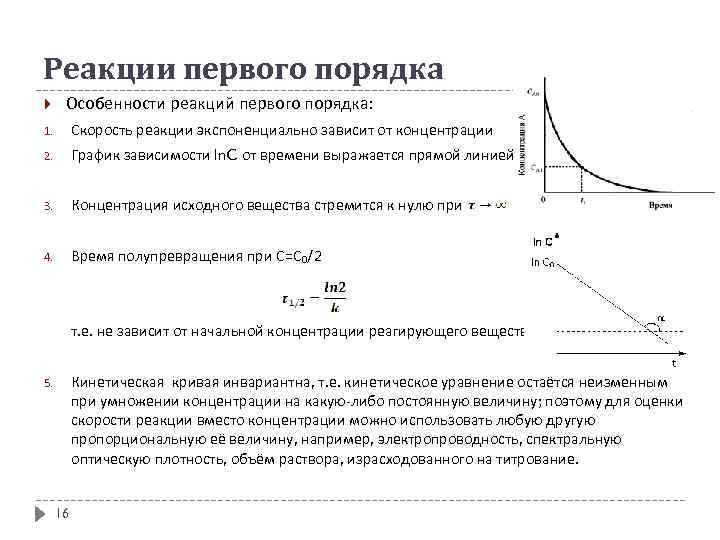 Реакции первого порядка Особенности реакций первого порядка: 1. Скорость реакции экспоненциально зависит от концентрации 2. График зависимости ln. C от времени выражается прямой линией 3. Концентрация исходного вещества стремится к нулю при 4. Время полупревращения при С=С₀/2 т. е. не зависит от начальной концентрации реагирующего вещества Кинетическая кривая инвариантна, т. е. кинетическое уравнение остаётся неизменным при умножении концентрации на какую-либо постоянную величину; поэтому для оценки скорости реакции вместо концентрации можно использовать любую другую пропорциональную её величину, например, электропроводность, спектральную оптическую плотность, объём раствора, израсходованного на титрование. 5. 16
Реакции первого порядка Особенности реакций первого порядка: 1. Скорость реакции экспоненциально зависит от концентрации 2. График зависимости ln. C от времени выражается прямой линией 3. Концентрация исходного вещества стремится к нулю при 4. Время полупревращения при С=С₀/2 т. е. не зависит от начальной концентрации реагирующего вещества Кинетическая кривая инвариантна, т. е. кинетическое уравнение остаётся неизменным при умножении концентрации на какую-либо постоянную величину; поэтому для оценки скорости реакции вместо концентрации можно использовать любую другую пропорциональную её величину, например, электропроводность, спектральную оптическую плотность, объём раствора, израсходованного на титрование. 5. 16
 Примеры реакций первого порядка Разложение оксида азота (V) в газовой фазе Разложение ацетона Радиоактивный распад Гидролиз в растворе Инверсия тростникового сахара в кислотной среде Реакции изомеризации 17
Примеры реакций первого порядка Разложение оксида азота (V) в газовой фазе Разложение ацетона Радиоактивный распад Гидролиз в растворе Инверсия тростникового сахара в кислотной среде Реакции изомеризации 17
 Реакции второго порядка В реакции участвуют два реагента Возможны два случая Случай 1. А+В→продукты, начальные концентрации веществ равны, т. е. Кинетическое уравнение Разделяя переменные и интегрируя в пределах от С₀ до С, получим Из этого уравнения следует, что концентрация исходных веществ зависит от времени следующим образом: 18
Реакции второго порядка В реакции участвуют два реагента Возможны два случая Случай 1. А+В→продукты, начальные концентрации веществ равны, т. е. Кинетическое уравнение Разделяя переменные и интегрируя в пределах от С₀ до С, получим Из этого уравнения следует, что концентрация исходных веществ зависит от времени следующим образом: 18
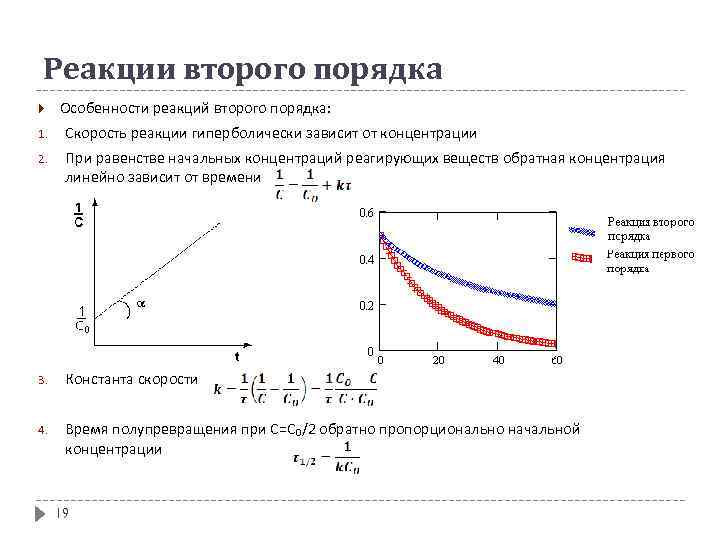 Реакции второго порядка Особенности реакций второго порядка: 1. Скорость реакции гиперболически зависит от концентрации 2. При равенстве начальных концентраций реагирующих веществ обратная концентрация линейно зависит от времени 3. Константа скорости 4. Время полупревращения при С=С₀/2 обратно пропорционально начальной концентрации 19
Реакции второго порядка Особенности реакций второго порядка: 1. Скорость реакции гиперболически зависит от концентрации 2. При равенстве начальных концентраций реагирующих веществ обратная концентрация линейно зависит от времени 3. Константа скорости 4. Время полупревращения при С=С₀/2 обратно пропорционально начальной концентрации 19
 Реакции второго порядка Случай 2. А+В→продукты, начальные концентрации веществ не равны, т. е. Кинетическое уравнение Разделяя переменные и интегрируя, получим Время полупревращения 20
Реакции второго порядка Случай 2. А+В→продукты, начальные концентрации веществ не равны, т. е. Кинетическое уравнение Разделяя переменные и интегрируя, получим Время полупревращения 20
 Примеры реакций второго порядка 1. Газофазное разложение иодоводорода 2. Разложение оксида азота (IV) 3. Разложение гипохлорит-иона в растворе 4. Газофазное образование иодоводорода 5. Радикальные реакции, например: 21
Примеры реакций второго порядка 1. Газофазное разложение иодоводорода 2. Разложение оксида азота (IV) 3. Разложение гипохлорит-иона в растворе 4. Газофазное образование иодоводорода 5. Радикальные реакции, например: 21
 Реакции n-го порядка Это реакции типа n. А→продукты Кинетическое уравнение Решение уравнения: Время полупревращения 22
Реакции n-го порядка Это реакции типа n. А→продукты Кинетическое уравнение Решение уравнения: Время полупревращения 22
 Реакции других порядков Необычный — дробный или отрицательный — порядок реакции однозначно указывает на её сложный механизм В растворах, если реакция происходит между молекулой и ионом, возможен порядок 3/2 Реакция окисления СО кислородом на поверхности платины 2 СО+О 2→ 2 СО 2 имеет отрицательный (минус первый) порядок по СО: т. е. при увеличении концентрации СО скорость реакции уменьшается 23
Реакции других порядков Необычный — дробный или отрицательный — порядок реакции однозначно указывает на её сложный механизм В растворах, если реакция происходит между молекулой и ионом, возможен порядок 3/2 Реакция окисления СО кислородом на поверхности платины 2 СО+О 2→ 2 СО 2 имеет отрицательный (минус первый) порядок по СО: т. е. при увеличении концентрации СО скорость реакции уменьшается 23
 Лекция 2. ОПРЕДЕЛЕНИЕ ПОРЯДКА РЕАКЦИИ
Лекция 2. ОПРЕДЕЛЕНИЕ ПОРЯДКА РЕАКЦИИ
 Определение порядка реакции Методы определения порядка реакции базируются на методах вычислительной математики, которые позволяют по кинетическим кривым, полученным экспериментально, найти порядки реакции по отдельным реагентам Интегральные методы Дифференциальные методы • Используют дифференциальные кинетические уравнения для обработки экспериментальных данных о зависимости концентраций реагирующих веществ от времени • Метод Вант-Гоффа 25 • Используют интегральные кинетические уравнения для обработки экспериментальных данных о зависимости концентраций реагирующих веществ от времени • Метод подстановки • Метод Оствальда. Нойеса • Метод полупревращения
Определение порядка реакции Методы определения порядка реакции базируются на методах вычислительной математики, которые позволяют по кинетическим кривым, полученным экспериментально, найти порядки реакции по отдельным реагентам Интегральные методы Дифференциальные методы • Используют дифференциальные кинетические уравнения для обработки экспериментальных данных о зависимости концентраций реагирующих веществ от времени • Метод Вант-Гоффа 25 • Используют интегральные кинетические уравнения для обработки экспериментальных данных о зависимости концентраций реагирующих веществ от времени • Метод подстановки • Метод Оствальда. Нойеса • Метод полупревращения
 Метод Вант-Гоффа Порядок реакции определяют по скоростям превращения Для реакции А+В→продукты записывают уравнение закона действующих масс: Для определения порядка реакции по веществу А проводят серию экспериментов при постоянной начальной концентрации вещества В ( ) В этих условиях При различных значениях измеряют начальные скорости и строят график зависимости от , который выражается прямой линией Тангенс угла наклона прямой равен порядку реакции по веществу А (tgα=n) Аналогично по данным другой серии экспериментов определяют порядок реакции по веществу В Порядок реакции можно определить и расчётным путём: 26
Метод Вант-Гоффа Порядок реакции определяют по скоростям превращения Для реакции А+В→продукты записывают уравнение закона действующих масс: Для определения порядка реакции по веществу А проводят серию экспериментов при постоянной начальной концентрации вещества В ( ) В этих условиях При различных значениях измеряют начальные скорости и строят график зависимости от , который выражается прямой линией Тангенс угла наклона прямой равен порядку реакции по веществу А (tgα=n) Аналогично по данным другой серии экспериментов определяют порядок реакции по веществу В Порядок реакции можно определить и расчётным путём: 26
 Метод подстановки Заключается в том, что экспериментальные данные последовательно подставляют в интегральные кинетические уравнения для реакций целых порядков и рассчитывают константу скорости k Если для выбранного порядка значения k приблизительно постоянны, то изучаемая реакция имеет данный порядок Если ни одно из кинетических уравнений не даёт удовлетворительного результата, то порядок реакции не является целым, т. е. реакция описывается более сложным кинетическим уравнением Правильность выбора уравнения проверяется графически по линейности получаемого графика в соответствующих координатах Способ трудоёмок и позволяет определить только целые порядки реакции 27
Метод подстановки Заключается в том, что экспериментальные данные последовательно подставляют в интегральные кинетические уравнения для реакций целых порядков и рассчитывают константу скорости k Если для выбранного порядка значения k приблизительно постоянны, то изучаемая реакция имеет данный порядок Если ни одно из кинетических уравнений не даёт удовлетворительного результата, то порядок реакции не является целым, т. е. реакция описывается более сложным кинетическим уравнением Правильность выбора уравнения проверяется графически по линейности получаемого графика в соответствующих координатах Способ трудоёмок и позволяет определить только целые порядки реакции 27
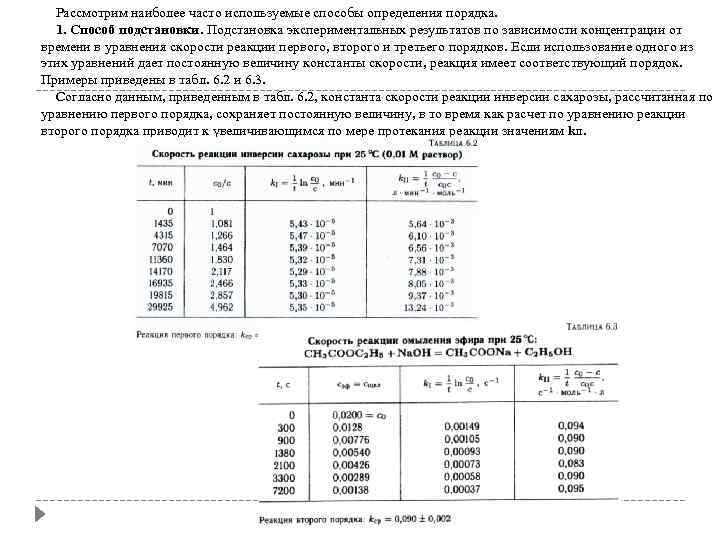 Рассмотрим наиболее часто используемые способы определения порядка. 1. Способ подстановки. Подстановка экспериментальных результатов по зависимости концентрации от времени в уравнения скорости реакции первого, второго и третьего порядков. Если использование одного из этих уравнений дает постоянную величину константы скорости, реакция имеет соответствующий порядок. Примеры приведены в табл. 6. 2 и 6. 3. Согласно данным, приведенным в табл. 6. 2, константа скорости реакции инверсии сахарозы, рассчитанная по уравнению первого порядка, сохраняет постоянную величину, в то время как расчет по уравнению реакции второго порядка приводит к увеличивающимся по мере протекания реакции значениям k. II.
Рассмотрим наиболее часто используемые способы определения порядка. 1. Способ подстановки. Подстановка экспериментальных результатов по зависимости концентрации от времени в уравнения скорости реакции первого, второго и третьего порядков. Если использование одного из этих уравнений дает постоянную величину константы скорости, реакция имеет соответствующий порядок. Примеры приведены в табл. 6. 2 и 6. 3. Согласно данным, приведенным в табл. 6. 2, константа скорости реакции инверсии сахарозы, рассчитанная по уравнению первого порядка, сохраняет постоянную величину, в то время как расчет по уравнению реакции второго порядка приводит к увеличивающимся по мере протекания реакции значениям k. II.
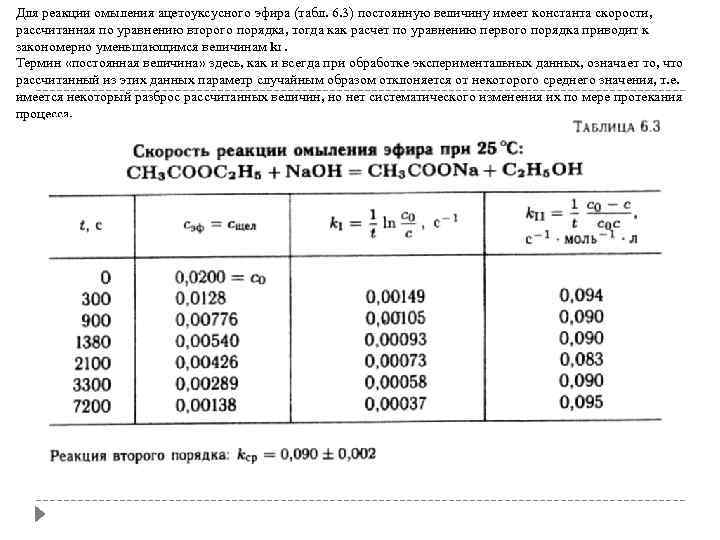 Для реакции омыления ацетоуксусного эфира (табл. 6. 3) постоянную величину имеет константа скорости, рассчитанная по уравнению второго порядка, тогда как расчет по уравнению первого порядка приводит к закономерно уменьшающимся величинам k. I. Термин «постоянная величина» здесь, как и всегда при обработке экспериментальных данных, означает то, что рассчитанный из этих данных параметр случайным образом отклоняется от некоторого среднего значения, т. е. имеется некоторый разброс рассчитанных величин, но нет систематического изменения их по мере протекания процесса.
Для реакции омыления ацетоуксусного эфира (табл. 6. 3) постоянную величину имеет константа скорости, рассчитанная по уравнению второго порядка, тогда как расчет по уравнению первого порядка приводит к закономерно уменьшающимся величинам k. I. Термин «постоянная величина» здесь, как и всегда при обработке экспериментальных данных, означает то, что рассчитанный из этих данных параметр случайным образом отклоняется от некоторого среднего значения, т. е. имеется некоторый разброс рассчитанных величин, но нет систематического изменения их по мере протекания процесса.
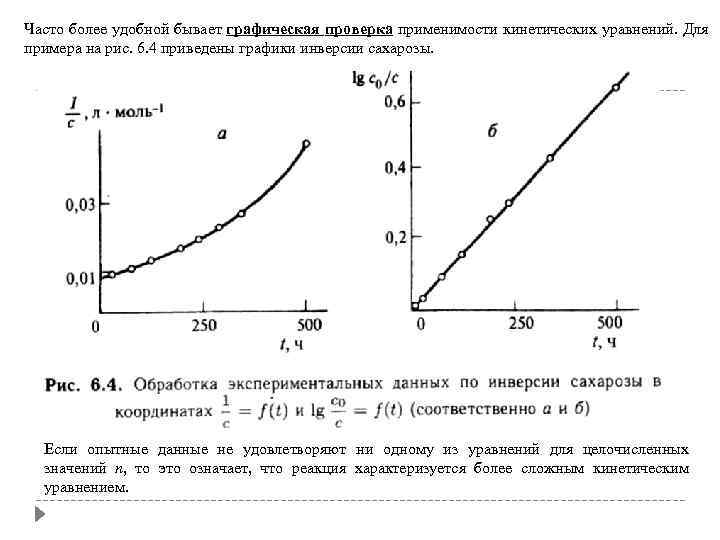 Часто более удобной бывает графическая проверка применимости кинетических уравнений. Для примера на рис. 6. 4 приведены графики инверсии сахарозы. Если опытные данные не удовлетворяют ни одному из уравнений для целочисленных значений n, то это означает, что реакция характеризуется более сложным кинетическим уравнением.
Часто более удобной бывает графическая проверка применимости кинетических уравнений. Для примера на рис. 6. 4 приведены графики инверсии сахарозы. Если опытные данные не удовлетворяют ни одному из уравнений для целочисленных значений n, то это означает, что реакция характеризуется более сложным кинетическим уравнением.
 2. Способ Вант-Гоффа основан на графическом представлении экспериментальных результатов в логарифмических координатах: lgw= Если прологарифмировать уравнение w = k· cn , получим lg w = lg k + n·lg c График зависимости lgw от lg c должен быть прямой, тангенс угла наклона которой равен порядку реакции. Величины скорости находятся графическим дифференцированием кинетической кривой w =
2. Способ Вант-Гоффа основан на графическом представлении экспериментальных результатов в логарифмических координатах: lgw= Если прологарифмировать уравнение w = k· cn , получим lg w = lg k + n·lg c График зависимости lgw от lg c должен быть прямой, тангенс угла наклона которой равен порядку реакции. Величины скорости находятся графическим дифференцированием кинетической кривой w =
 Метод Оствальда-Нойеса Порядок реакции определяют по времени достижения определённой доли превращения α: Отсюда порядок реакции 32
Метод Оствальда-Нойеса Порядок реакции определяют по времени достижения определённой доли превращения α: Отсюда порядок реакции 32
 Метод полупревращения Частный случай метода Оствальда-Нойеса Порядок реакции определяют по периоду полупревращения (α=1/2) Метод Оствальда-Нойеса и метод полупревращения позволяют определять любые значения порядка реакции, включая дробные и отрицательные 33
Метод полупревращения Частный случай метода Оствальда-Нойеса Порядок реакции определяют по периоду полупревращения (α=1/2) Метод Оствальда-Нойеса и метод полупревращения позволяют определять любые значения порядка реакции, включая дробные и отрицательные 33
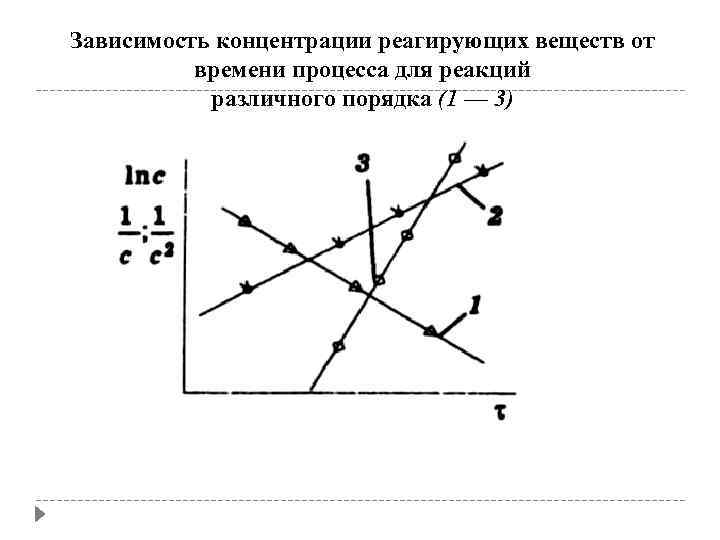 Зависимость концентрации реагирующих веществ от времени процесса для реакций различного порядка (1 — 3)
Зависимость концентрации реагирующих веществ от времени процесса для реакций различного порядка (1 — 3)
 Лекция 3. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ. УРАВНЕНИЕ АРРЕНИУСА
Лекция 3. ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ. УРАВНЕНИЕ АРРЕНИУСА
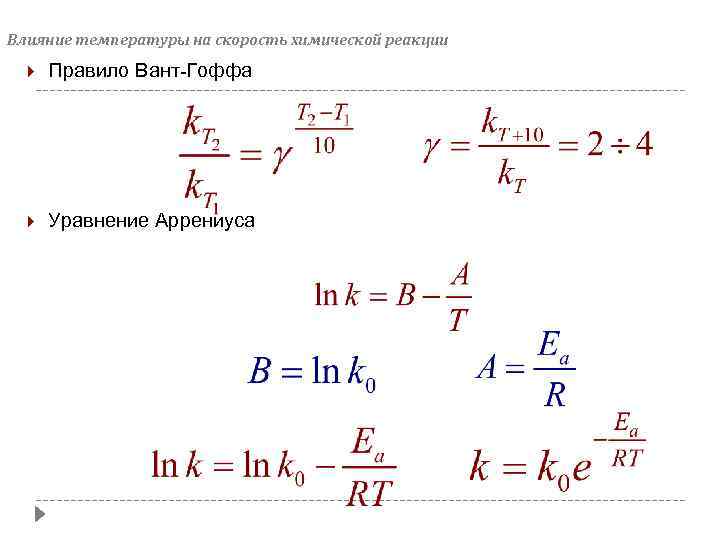 Влияние температуры на скорость химической реакции Правило Вант-Гоффа Уравнение Аррениуса
Влияние температуры на скорость химической реакции Правило Вант-Гоффа Уравнение Аррениуса
 ЗАВИСИМОСТЬ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ: ЭМПИРИЧЕСКОЕ ПРАВИЛО ВАНТ-ГОФФА Ʋ 2/Ʋ 1 = γΔt/10, Δt = T –T 2 1 Ʋ 2 = Ʋ 1 • γΔt/10, где γ = 2 ÷ 4 Данное правило применимо только для областей низких температур!!!
ЗАВИСИМОСТЬ СКОРОСТИ ОТ ТЕМПЕРАТУРЫ: ЭМПИРИЧЕСКОЕ ПРАВИЛО ВАНТ-ГОФФА Ʋ 2/Ʋ 1 = γΔt/10, Δt = T –T 2 1 Ʋ 2 = Ʋ 1 • γΔt/10, где γ = 2 ÷ 4 Данное правило применимо только для областей низких температур!!!
 Влияние температуры на скорость реакции Скорость большинства реакций увеличивается с ростом температуры, т. к. при этом возрастает энергия сталкивающихся частиц и повышается вероятность того, что при столкновении произойдёт химическое превращение Основное влияние температура оказывает на константу скорости реакции Зависимость скорости реакции от температуры описывается правилом Вант-Гоффа и уравнением Аррениуса Правило Вант-Гоффа: при повышении температуры на 10 градусов скорость большинства химических реакций увеличивается в 2 -4 раза: Температурный коэффициент скорости Правило является приближённым и применимо в ограниченном интервале температур (реакции в растворах, 0 -120°С, не слишком быстрые реакции) Скорость реакции при температуре Т₂ можно определить по формуле: 38
Влияние температуры на скорость реакции Скорость большинства реакций увеличивается с ростом температуры, т. к. при этом возрастает энергия сталкивающихся частиц и повышается вероятность того, что при столкновении произойдёт химическое превращение Основное влияние температура оказывает на константу скорости реакции Зависимость скорости реакции от температуры описывается правилом Вант-Гоффа и уравнением Аррениуса Правило Вант-Гоффа: при повышении температуры на 10 градусов скорость большинства химических реакций увеличивается в 2 -4 раза: Температурный коэффициент скорости Правило является приближённым и применимо в ограниченном интервале температур (реакции в растворах, 0 -120°С, не слишком быстрые реакции) Скорость реакции при температуре Т₂ можно определить по формуле: 38
 Влияние температуры на скорость химических реакций очень существенно, и описывается эмпирическим правилом Вант-Гоффа. При повышении температуры на каждые 10 градусов скорость реакции увеличивается примерно в 2 -4 раза. ( - температурный коэффициент или коэффициент Вант-Гоффа). Или Более строго влияние температуры описывает уравнение Аррениуса: k – постоянная скорости реакции; А – предэкспоненциальный множитель; R – универсальная газовая постоянная; T – абсолютная температура (0 K); Eа – энергия активации. Так как, температура входит в показатель степени, скорость химической реакции очень чувствительна к изменению температуры. С ростом температуры число активных молекул возрастает, скорость химической реакции увеличивается.
Влияние температуры на скорость химических реакций очень существенно, и описывается эмпирическим правилом Вант-Гоффа. При повышении температуры на каждые 10 градусов скорость реакции увеличивается примерно в 2 -4 раза. ( - температурный коэффициент или коэффициент Вант-Гоффа). Или Более строго влияние температуры описывает уравнение Аррениуса: k – постоянная скорости реакции; А – предэкспоненциальный множитель; R – универсальная газовая постоянная; T – абсолютная температура (0 K); Eа – энергия активации. Так как, температура входит в показатель степени, скорость химической реакции очень чувствительна к изменению температуры. С ростом температуры число активных молекул возрастает, скорость химической реакции увеличивается.
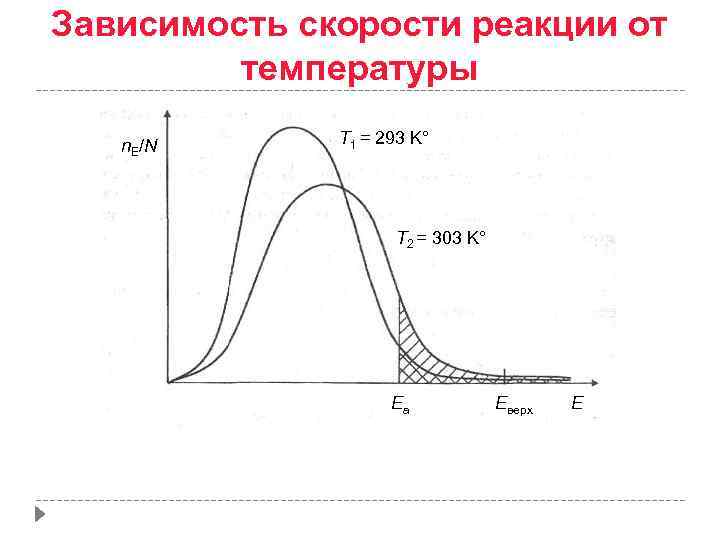 Зависимость скорости реакции от температуры n. E/N T 1 = 293 K° T 2 = 303 K° Ea Eверх Изменение вида кривой распределения при повышении температуры E
Зависимость скорости реакции от температуры n. E/N T 1 = 293 K° T 2 = 303 K° Ea Eверх Изменение вида кривой распределения при повышении температуры E
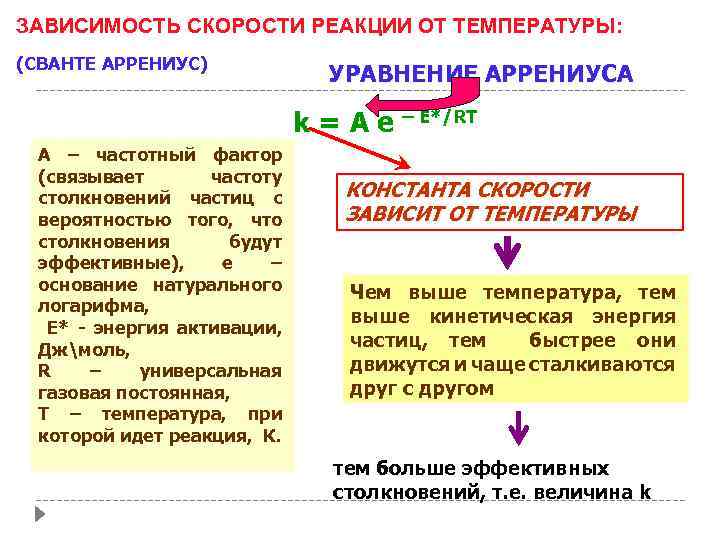 ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ: (СВАНТЕ АРРЕНИУС) УРАВНЕНИЕ АРРЕНИУСА k = А е – Е*/RT А – частотный фактор (связывает частоту столкновений частиц с вероятностью того, что столкновения будут эффективные), е – основание натурального логарифма, Е* - энергия активации, Джмоль, R – универсальная газовая постоянная, T – температура, при которой идет реакция, К. КОНСТАНТА СКОРОСТИ ЗАВИСИТ ОТ ТЕМПЕРАТУРЫ Чем выше температура, тем выше кинетическая энергия частиц, тем быстрее они движутся и чаще сталкиваются друг с другом тем больше эффективных столкновений, т. е. величина k
ЗАВИСИМОСТЬ СКОРОСТИ РЕАКЦИИ ОТ ТЕМПЕРАТУРЫ: (СВАНТЕ АРРЕНИУС) УРАВНЕНИЕ АРРЕНИУСА k = А е – Е*/RT А – частотный фактор (связывает частоту столкновений частиц с вероятностью того, что столкновения будут эффективные), е – основание натурального логарифма, Е* - энергия активации, Джмоль, R – универсальная газовая постоянная, T – температура, при которой идет реакция, К. КОНСТАНТА СКОРОСТИ ЗАВИСИТ ОТ ТЕМПЕРАТУРЫ Чем выше температура, тем выше кинетическая энергия частиц, тем быстрее они движутся и чаще сталкиваются друг с другом тем больше эффективных столкновений, т. е. величина k
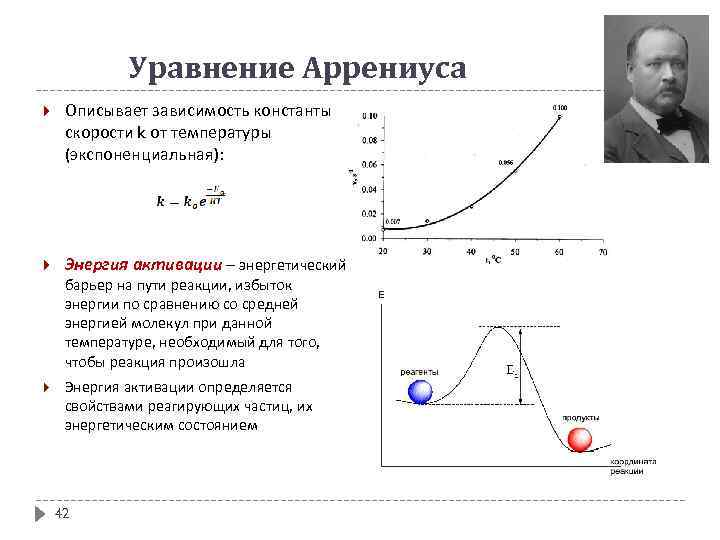 Уравнение Аррениуса Описывает зависимость константы скорости k от температуры (экспоненциальная): Энергия активации – энергетический барьер на пути реакции, избыток энергии по сравнению со средней энергией молекул при данной температуре, необходимый для того, чтобы реакция произошла Энергия активации определяется свойствами реагирующих частиц, их энергетическим состоянием 42
Уравнение Аррениуса Описывает зависимость константы скорости k от температуры (экспоненциальная): Энергия активации – энергетический барьер на пути реакции, избыток энергии по сравнению со средней энергией молекул при данной температуре, необходимый для того, чтобы реакция произошла Энергия активации определяется свойствами реагирующих частиц, их энергетическим состоянием 42
 Энергия активации Для того, чтобы совершить элементарный акт химического взаимодействия, реагирующие частицы должны столкнуться друг с другом. Однако, не каждое столкновение частиц приводит к их химическому взаимодействию. Это происходит в том случае, когда частицы приближаются на расстояние, при котором становится возможным перераспределение электронной плотности и возникновение новых химических связей. Следовательно, сталкивающиеся частицы должны обладать энергией, достаточной для преодоления сил отталкивания (энергетического барьера), возникающих между их электронными оболочками. Такие, реакционно-способные частицы называют активными, а энергия, необходимая для преодоления энергетического барьера, называется энергией активации реакции. Группировку частиц, находящихся в процессе взаимодействия (т. е. перераспределения связей), называют активированным комплексом. Реакции, требующие для своего протекания значительной энергии активации, начинаются с разрыва или ослабления связей в молекулах исходных веществ. При этом вещества переходят в неустойчивое промежуточное состояние, характеризующееся большим запасом энергии. Это состояние и есть активированный комплекс. Именно для его образования необходима энергия активации. Он существует очень короткое время, неустойчивый активированный комплекс распадается с образованием продуктов реакции, при этом энергия выделяется.
Энергия активации Для того, чтобы совершить элементарный акт химического взаимодействия, реагирующие частицы должны столкнуться друг с другом. Однако, не каждое столкновение частиц приводит к их химическому взаимодействию. Это происходит в том случае, когда частицы приближаются на расстояние, при котором становится возможным перераспределение электронной плотности и возникновение новых химических связей. Следовательно, сталкивающиеся частицы должны обладать энергией, достаточной для преодоления сил отталкивания (энергетического барьера), возникающих между их электронными оболочками. Такие, реакционно-способные частицы называют активными, а энергия, необходимая для преодоления энергетического барьера, называется энергией активации реакции. Группировку частиц, находящихся в процессе взаимодействия (т. е. перераспределения связей), называют активированным комплексом. Реакции, требующие для своего протекания значительной энергии активации, начинаются с разрыва или ослабления связей в молекулах исходных веществ. При этом вещества переходят в неустойчивое промежуточное состояние, характеризующееся большим запасом энергии. Это состояние и есть активированный комплекс. Именно для его образования необходима энергия активации. Он существует очень короткое время, неустойчивый активированный комплекс распадается с образованием продуктов реакции, при этом энергия выделяется.
 Энергия активации есть минимальная энергия, которой должны обладать молекулы, чтобы их столкновение могло привести к химическому взаимодействию. Рассмотрим путь некоторой элементарной реакции А + В ––> С Поскольку химическое взаимодействие частиц связано с разрывом старых химических связей и образованием новых, считается, что всякая элементарная реакция проходит через образование некоторого неустойчивого промежуточного соединения, называемого активированным комплексом: А ––> K# ––> B Образование активированного комплекса всегда требует затраты некоторого количества энергии, что вызвано, во-первых, отталкиванием электронных оболочек и атомных ядер при сближении частиц и, во-вторых, необходимостью построения определенной пространственной конфигурации атомов в активированном комплексе и перераспределения электронной плотности. Таким образом, по пути из начального состояния в конечное система должна преодолеть своего рода энергетический барьер. Энергия активации реакции приближённо равна превышению средней энергии активированного комплекса над средним уровнем энергии реагентов. Очевидно, что если прямая реакция является экзотермической, то энергия активации обратной реакции Е'А выше, нежели энергия активации прямой реакции EA. Энергии активации прямой и обратной реакции связаны друг с другом через изменение внутренней энергии в ходе реакции. Вышесказанное можно проиллюстрировать с помощью энергетической диаграммы химической реакции (рис. 1). Рис. 1. Энергетическая диаграмма химической реакции. Eисх – средняя энергия частиц исходных веществ, Eпрод – средняя энергия частиц продуктов реакции.
Энергия активации есть минимальная энергия, которой должны обладать молекулы, чтобы их столкновение могло привести к химическому взаимодействию. Рассмотрим путь некоторой элементарной реакции А + В ––> С Поскольку химическое взаимодействие частиц связано с разрывом старых химических связей и образованием новых, считается, что всякая элементарная реакция проходит через образование некоторого неустойчивого промежуточного соединения, называемого активированным комплексом: А ––> K# ––> B Образование активированного комплекса всегда требует затраты некоторого количества энергии, что вызвано, во-первых, отталкиванием электронных оболочек и атомных ядер при сближении частиц и, во-вторых, необходимостью построения определенной пространственной конфигурации атомов в активированном комплексе и перераспределения электронной плотности. Таким образом, по пути из начального состояния в конечное система должна преодолеть своего рода энергетический барьер. Энергия активации реакции приближённо равна превышению средней энергии активированного комплекса над средним уровнем энергии реагентов. Очевидно, что если прямая реакция является экзотермической, то энергия активации обратной реакции Е'А выше, нежели энергия активации прямой реакции EA. Энергии активации прямой и обратной реакции связаны друг с другом через изменение внутренней энергии в ходе реакции. Вышесказанное можно проиллюстрировать с помощью энергетической диаграммы химической реакции (рис. 1). Рис. 1. Энергетическая диаграмма химической реакции. Eисх – средняя энергия частиц исходных веществ, Eпрод – средняя энергия частиц продуктов реакции.
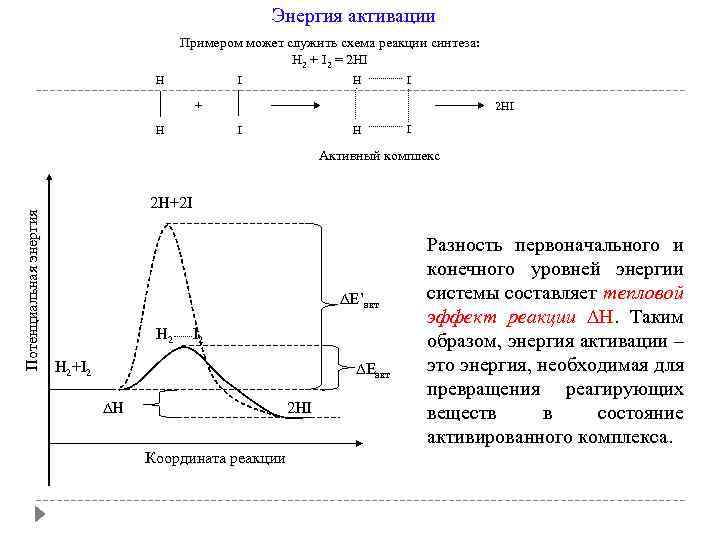 Энергия активации Примером может служить схема реакции синтеза: H 2 + I 2 = 2 HI H I + H 2 HI I H I Потенциальная энергия Активный комплекс 2 H+2 I E’акт H 2 I 2 H 2+I 2 Eакт H 2 HI Координата реакции Разность первоначального и конечного уровней энергии системы составляет тепловой эффект реакции ∆Н. Таким образом, энергия активации – это энергия, необходимая для превращения реагирующих веществ в состояние активированного комплекса.
Энергия активации Примером может служить схема реакции синтеза: H 2 + I 2 = 2 HI H I + H 2 HI I H I Потенциальная энергия Активный комплекс 2 H+2 I E’акт H 2 I 2 H 2+I 2 Eакт H 2 HI Координата реакции Разность первоначального и конечного уровней энергии системы составляет тепловой эффект реакции ∆Н. Таким образом, энергия активации – это энергия, необходимая для превращения реагирующих веществ в состояние активированного комплекса.
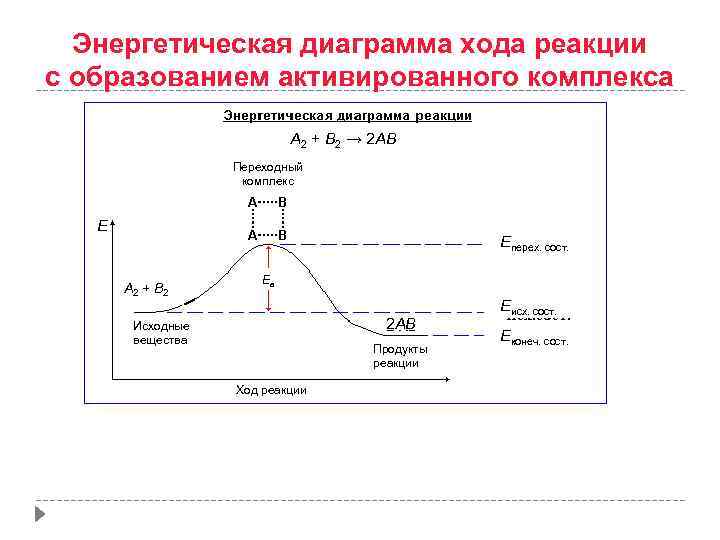 Энергетическая диаграмма хода реакции с образованием активированного комплекса A 2 + B 2 → 2 AB Переходный комплекс E Еперех. сост. A 2 + B 2 Ea 2 AB Исходные вещества Продукты реакции Еисх. сост. Еконеч. сост. Ход реакции [А…В]# переходное (активированный комплекс) АВ конечное (продукты реакции)
Энергетическая диаграмма хода реакции с образованием активированного комплекса A 2 + B 2 → 2 AB Переходный комплекс E Еперех. сост. A 2 + B 2 Ea 2 AB Исходные вещества Продукты реакции Еисх. сост. Еконеч. сост. Ход реакции [А…В]# переходное (активированный комплекс) АВ конечное (продукты реакции)
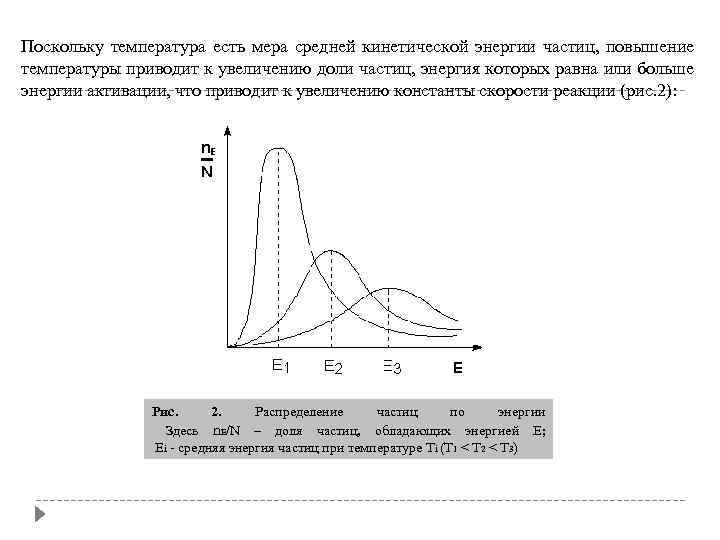 Поскольку температура есть мера средней кинетической энергии частиц, повышение температуры приводит к увеличению доли частиц, энергия которых равна или больше энергии активации, что приводит к увеличению константы скорости реакции (рис. 2): Рис. 2. Распределение частиц по энергии Здесь n. Е/N – доля частиц, обладающих энергией E; Ei - средняя энергия частиц при температуре Ti (T 1 < T 2 < T 3)
Поскольку температура есть мера средней кинетической энергии частиц, повышение температуры приводит к увеличению доли частиц, энергия которых равна или больше энергии активации, что приводит к увеличению константы скорости реакции (рис. 2): Рис. 2. Распределение частиц по энергии Здесь n. Е/N – доля частиц, обладающих энергией E; Ei - средняя энергия частиц при температуре Ti (T 1 < T 2 < T 3)
 Рассмотрим термодинамический вывод выражения, описывающего зависимость константы скорости реакции от температуры и величины энергии активации – уравнения Аррениуса. Согласно уравнению изобары Вант-Гоффа, Поскольку константа равновесия есть отношение констант скоростей прямой и обратной реакции, можно переписать предыдущее выражение следующим образом: Представив изменение энтальпии реакции ΔHº в виде разности двух величин E 1 и E 2, получаем: Здесь С – некоторая константа. Постулировав, что С = 0, получаем уравнение Аррениуса, где E A – энергия активации:
Рассмотрим термодинамический вывод выражения, описывающего зависимость константы скорости реакции от температуры и величины энергии активации – уравнения Аррениуса. Согласно уравнению изобары Вант-Гоффа, Поскольку константа равновесия есть отношение констант скоростей прямой и обратной реакции, можно переписать предыдущее выражение следующим образом: Представив изменение энтальпии реакции ΔHº в виде разности двух величин E 1 и E 2, получаем: Здесь С – некоторая константа. Постулировав, что С = 0, получаем уравнение Аррениуса, где E A – энергия активации:
 После неопределенного интегрирования выражения получим уравнение Аррениуса в интегральной форме: Здесь A – постоянная интегрирования. Из уравнения (3) нетрудно показать физический смысл предэкспоненциального множителя A, который равен константе скорости реакции при температуре, стремящейся к бесконечности. Как видно из выражения (2), логарифм константы скорости линейно зависит от обратной температуры (рис. 3); величину энергии активации EA и логарифм предэкспоненциального множителя A можно определить графически (тангенс угла наклона прямой к оси абсцисс и отрезок, отсекаемый прямой на оси ординат). Зная энергию активации реакции и константу скорости при какой-либо температуре T 1, по уравнению Аррениуса можно рассчитать величину константы скорости при любой температуре T 2: Рис. 3. Зависимость логарифма константы скорости химической реакции от обратной температуры.
После неопределенного интегрирования выражения получим уравнение Аррениуса в интегральной форме: Здесь A – постоянная интегрирования. Из уравнения (3) нетрудно показать физический смысл предэкспоненциального множителя A, который равен константе скорости реакции при температуре, стремящейся к бесконечности. Как видно из выражения (2), логарифм константы скорости линейно зависит от обратной температуры (рис. 3); величину энергии активации EA и логарифм предэкспоненциального множителя A можно определить графически (тангенс угла наклона прямой к оси абсцисс и отрезок, отсекаемый прямой на оси ординат). Зная энергию активации реакции и константу скорости при какой-либо температуре T 1, по уравнению Аррениуса можно рассчитать величину константы скорости при любой температуре T 2: Рис. 3. Зависимость логарифма константы скорости химической реакции от обратной температуры.
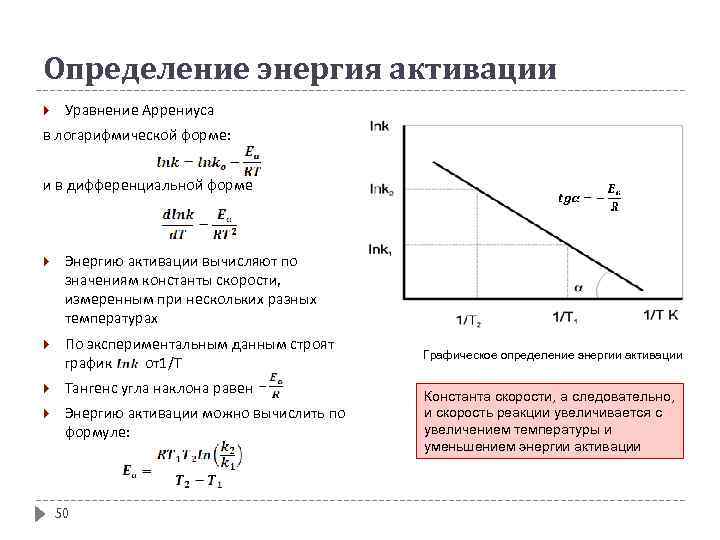 Определение энергия активации Уравнение Аррениуса в логарифмической форме: и в дифференциальной форме Энергию активации вычисляют по значениям константы скорости, измеренным при нескольких разных температурах По экспериментальным данным строят график от1/Т Тангенс угла наклона равен Энергию активации можно вычислить по формуле: 50 Графическое определение энергии активации Константа скорости, а следовательно, и скорость реакции увеличивается с увеличением температуры и уменьшением энергии активации
Определение энергия активации Уравнение Аррениуса в логарифмической форме: и в дифференциальной форме Энергию активации вычисляют по значениям константы скорости, измеренным при нескольких разных температурах По экспериментальным данным строят график от1/Т Тангенс угла наклона равен Энергию активации можно вычислить по формуле: 50 Графическое определение энергии активации Константа скорости, а следовательно, и скорость реакции увеличивается с увеличением температуры и уменьшением энергии активации
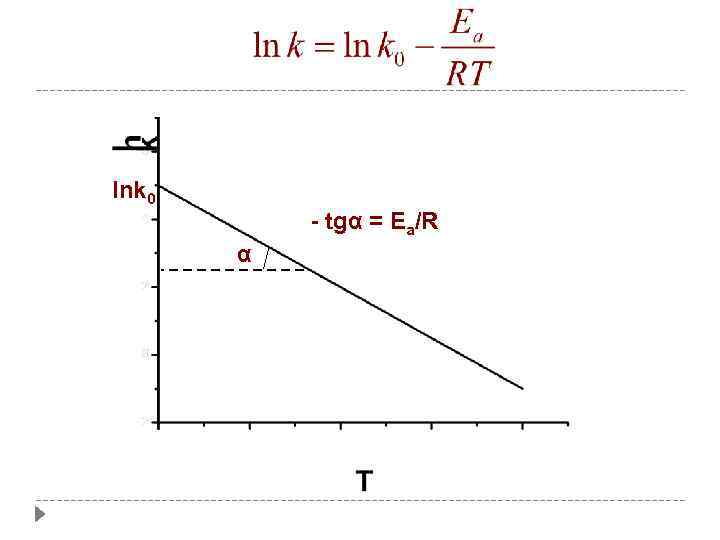 lnk 0 - tgα = Ea/R α
lnk 0 - tgα = Ea/R α
 КОНСТАНТЫ СКОРОСТИ ЭЛЕМЕНТАРНЫХ РЕАКЦИЙ, ОПРЕДЕЛЕННЫЕ В РАМКАХ ТЕОРИИ СТОЛКНОВЕНИЙ Скорость бимолекулярной реакции равна числу таких столкновений реагирующих частиц в единице объема за единицу времени, при которых сталкивающиеся частицы обладают энергией, достаточной для преодоления этого барьера. Согласно Максвелл-Больцмановскому распределению частиц по энергиям, доля столкновений, в которых молекулы имеют энергию большую Е 0, равна ехр (-E 0/RT). Скорость бимолекулярной реакции WA+B A + B C + D может быть выражена следующим уравнением WA+B = у AB VAB n. A n. B exp (-E 0/RT) n – концентрация, V – относит. скорость, у- сечение столкновений Представленная ниже температурная зависимость скорости реакции называется законом Аррениуса : k = A* exp (-E 0/RT) Е 0 – энергия активации, величина A* называется предэкспоненциальным фактором или предэкспонентом , A* имеет слабую зависимость от температуры (как T 0, 5) по сравнению с экспоненциальным фактором ехр (-E 0/RT). Кинетическая теория газов дает для значения A * величину 1013 cм 3 мoл-1 с-1 или 10 -10 cм 3 /молекул·с (эту величину обычно записывают как 10 -10 cм 3 / с), называемую нормальным значением предэкспоненциального фактора для бимолекулярной реакции.
КОНСТАНТЫ СКОРОСТИ ЭЛЕМЕНТАРНЫХ РЕАКЦИЙ, ОПРЕДЕЛЕННЫЕ В РАМКАХ ТЕОРИИ СТОЛКНОВЕНИЙ Скорость бимолекулярной реакции равна числу таких столкновений реагирующих частиц в единице объема за единицу времени, при которых сталкивающиеся частицы обладают энергией, достаточной для преодоления этого барьера. Согласно Максвелл-Больцмановскому распределению частиц по энергиям, доля столкновений, в которых молекулы имеют энергию большую Е 0, равна ехр (-E 0/RT). Скорость бимолекулярной реакции WA+B A + B C + D может быть выражена следующим уравнением WA+B = у AB VAB n. A n. B exp (-E 0/RT) n – концентрация, V – относит. скорость, у- сечение столкновений Представленная ниже температурная зависимость скорости реакции называется законом Аррениуса : k = A* exp (-E 0/RT) Е 0 – энергия активации, величина A* называется предэкспоненциальным фактором или предэкспонентом , A* имеет слабую зависимость от температуры (как T 0, 5) по сравнению с экспоненциальным фактором ехр (-E 0/RT). Кинетическая теория газов дает для значения A * величину 1013 cм 3 мoл-1 с-1 или 10 -10 cм 3 /молекул·с (эту величину обычно записывают как 10 -10 cм 3 / с), называемую нормальным значением предэкспоненциального фактора для бимолекулярной реакции.
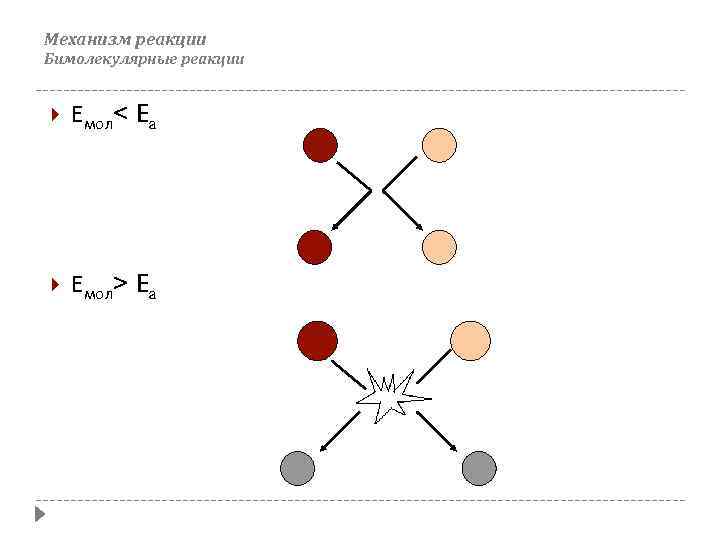 Механизм реакции Бимолекулярные реакции Емол< Ea Емол> Ea
Механизм реакции Бимолекулярные реакции Емол< Ea Емол> Ea
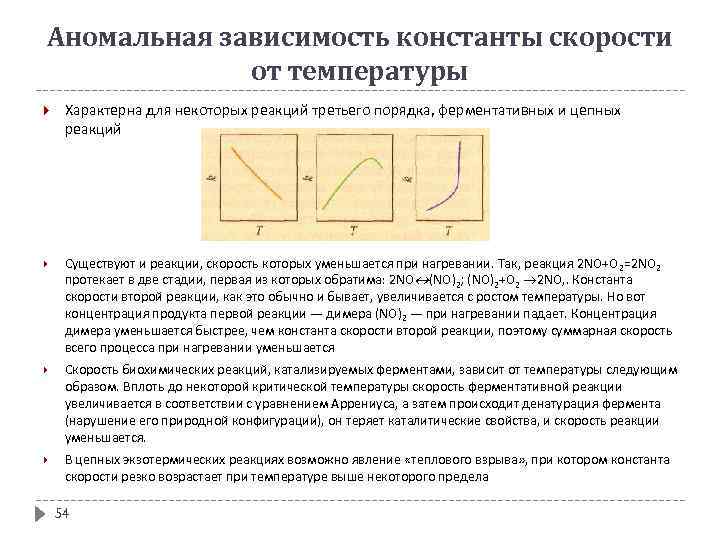 Аномальная зависимость константы скорости от температуры Характерна для некоторых реакций третьего порядка, ферментативных и цепных реакций Существуют и реакции, скорость которых уменьшается при нагревании. Так, реакция 2 NO+О 2=2 NO 2 протекает в две стадии, первая из которых обратима: 2 NO (NO)2; (NO)2+O 2 2 NO, . Константа скорости второй реакции, как это обычно и бывает, увеличивается с ростом температуры. Но вот концентрация продукта первой реакции — димера (NO)2 — при нагревании падает. Концентрация димера уменьшается быстрее, чем константа скорости второй реакции, поэтому суммарная скорость всего процесса при нагревании уменьшается Скорость биохимических реакций, катализируемых ферментами, зависит от температуры следующим образом. Вплоть до некоторой критической температуры скорость ферментативной реакции увеличивается в соответствии с уравнением Аррениуса, а затем происходит денатурация фермента (нарушение его природной конфигурации), он теряет каталитические свойства, и скорость реакции уменьшается. В цепных экзотермических реакциях возможно явление «теплового взрыва» , при котором константа скорости резко возрастает при температуре выше некоторого предела 54
Аномальная зависимость константы скорости от температуры Характерна для некоторых реакций третьего порядка, ферментативных и цепных реакций Существуют и реакции, скорость которых уменьшается при нагревании. Так, реакция 2 NO+О 2=2 NO 2 протекает в две стадии, первая из которых обратима: 2 NO (NO)2; (NO)2+O 2 2 NO, . Константа скорости второй реакции, как это обычно и бывает, увеличивается с ростом температуры. Но вот концентрация продукта первой реакции — димера (NO)2 — при нагревании падает. Концентрация димера уменьшается быстрее, чем константа скорости второй реакции, поэтому суммарная скорость всего процесса при нагревании уменьшается Скорость биохимических реакций, катализируемых ферментами, зависит от температуры следующим образом. Вплоть до некоторой критической температуры скорость ферментативной реакции увеличивается в соответствии с уравнением Аррениуса, а затем происходит денатурация фермента (нарушение его природной конфигурации), он теряет каталитические свойства, и скорость реакции уменьшается. В цепных экзотермических реакциях возможно явление «теплового взрыва» , при котором константа скорости резко возрастает при температуре выше некоторого предела 54
 Сложные реакции, возникающие в результате нарушения равновесного Максвелл-Больцмановского распределения молекул по энергиям. Теория Линдемана. Наблюдаемая зависимость от давления констант скорости реакций диссоциации молекул показывает, что эти реакции не являются элементарными. Частицы получают энергию, необходимую для разрыва связи в мономолекулярной реакции, в результате столкновений с другими молекулами, которые их активируют. При низких давлениях, когда столкновения происходят редко, частица не может набрать необходимую энергию. Химическая реакция также может вызвать нарушение равновесного Максвелл-Больцмановского распределения молекул по энергиям. Зависимость от давления констант скорости мономолекулярных реакций может быть объяснена в рамках следующей простой схемы реакций, предложенной Линдеманом (1922 г): активация дезактивация реакция обр. В В результате первой реакции (столкновение частицы А с другой молекулой) происходит образование возбужденной частицы А*, которая может дезактивироваться в результате следующего столкновения, если до этого не произойдет мономолекулярная реакция с образованием продукта В.
Сложные реакции, возникающие в результате нарушения равновесного Максвелл-Больцмановского распределения молекул по энергиям. Теория Линдемана. Наблюдаемая зависимость от давления констант скорости реакций диссоциации молекул показывает, что эти реакции не являются элементарными. Частицы получают энергию, необходимую для разрыва связи в мономолекулярной реакции, в результате столкновений с другими молекулами, которые их активируют. При низких давлениях, когда столкновения происходят редко, частица не может набрать необходимую энергию. Химическая реакция также может вызвать нарушение равновесного Максвелл-Больцмановского распределения молекул по энергиям. Зависимость от давления констант скорости мономолекулярных реакций может быть объяснена в рамках следующей простой схемы реакций, предложенной Линдеманом (1922 г): активация дезактивация реакция обр. В В результате первой реакции (столкновение частицы А с другой молекулой) происходит образование возбужденной частицы А*, которая может дезактивироваться в результате следующего столкновения, если до этого не произойдет мономолекулярная реакция с образованием продукта В.


