Л6 - Химич.Кинетика.ppt
- Количество слайдов: 23
 . Химическая кинетика — это учение о скорости и механизме химических реакций. Скорость химической реакции — это количество элементарных актов взаимодействия в единицу времени в единице объёма [для гомогенной среды] или на единице поверхности раздела фаз [в гетерогенной среде].
. Химическая кинетика — это учение о скорости и механизме химических реакций. Скорость химической реакции — это количество элементарных актов взаимодействия в единицу времени в единице объёма [для гомогенной среды] или на единице поверхности раздела фаз [в гетерогенной среде].
 • Скорость гомогенной реакции зависит от: • • - природы реагирующих веществ; - концентрации реагентов; - температуры; - катализатора. ВЛИЯНИЕ ПРИРОДЫ РЕАГИРУЮЩИХ ВЕЩЕСТВ -----их состава ( фтор и иод), -----вид частиц, которые участвуют в реакции: атомы, молекулы, ионы или радикалы.
• Скорость гомогенной реакции зависит от: • • - природы реагирующих веществ; - концентрации реагентов; - температуры; - катализатора. ВЛИЯНИЕ ПРИРОДЫ РЕАГИРУЮЩИХ ВЕЩЕСТВ -----их состава ( фтор и иод), -----вид частиц, которые участвуют в реакции: атомы, молекулы, ионы или радикалы.
 ВЛИЯНИЕ КОНЦЕНТРАЦИИ РЕАГЕНТОВ • • • • законом действующих масс (1867 г. К. М. Гульдберг и П. Вааге. ) : Скорость простой гомогенной реакции при постоянной температуре пропорциональна произведению концентраций реагирующих веществ, возведенных в степени, численно равные их стехиометрическим коэффициентам. a. A + b. B = d. D v = K • CАa • CВb, где К — константа скорости -численно равна скорости при концентрации в -в равной 1 моль/л. Константа скорости реакции ---не зависит от концентрации, ----зависит от природы реагирующих веществ, температуры, катализатора. В случае гетерогенных реакций в уравнения закона действующих масс входят концентрации только тех веществ, которые находятся в газовой фазе или в растворе. Например, для реакции горения угля: С + О 2 = СО 2 v = K[O 2] [концентрация твёрдого вещества входит в константу скорости].
ВЛИЯНИЕ КОНЦЕНТРАЦИИ РЕАГЕНТОВ • • • • законом действующих масс (1867 г. К. М. Гульдберг и П. Вааге. ) : Скорость простой гомогенной реакции при постоянной температуре пропорциональна произведению концентраций реагирующих веществ, возведенных в степени, численно равные их стехиометрическим коэффициентам. a. A + b. B = d. D v = K • CАa • CВb, где К — константа скорости -численно равна скорости при концентрации в -в равной 1 моль/л. Константа скорости реакции ---не зависит от концентрации, ----зависит от природы реагирующих веществ, температуры, катализатора. В случае гетерогенных реакций в уравнения закона действующих масс входят концентрации только тех веществ, которые находятся в газовой фазе или в растворе. Например, для реакции горения угля: С + О 2 = СО 2 v = K[O 2] [концентрация твёрдого вещества входит в константу скорости].
 • • • • • Молекулярность — это минимальное число различных частиц, участвующих в элементарном акте химического взаимодействия. СН 4 → С + 2 Н 2 -мономолекулярная Н 2 + I 2 → 2 HI - би 2 KMn. O 4 + 5 H 2 C 2 O 4 + 3 H 2 SO 4 → K 2 SO 4 + 2 Mn. SO 4 + 8 H 2 O + 10 CO 2 три Порядок реакции — это сумма показателей степеней в математическом выражении закона действия масс: a. A + b. B = d. D v = K • CА a • CВ b , n = a + b … — общий порядок реакции. Показатель степени при какой-либо одной концентрации определяет порядок реакции по данному компоненту. Например, а — показывает порядок реакции по компоненту А и т. д. Различают реакции I порядка: С + О 2 = СО 2 v = K[O 2] В реакциях II порядка скорость : H 2 + I 2 = 2 HI v = K[H 2][I 2] уравнение II порядка: 1 + 1 = 2 2 Н 2 О ↔ 2 Н 2 + О 2 v = K[H 2 O]2 прямая реакция II порядка, а обратная — III порядка: v 2[O ] 2 + 1 = 3 = K[H 2] 2 Реакция III порядка в газовой фазе — окисление оксида азота [II]: 2 NO + O 2 → 2 NO 2 Катализатор повышает порядок реакций, например: v = K 1 • [Н 2 О 2] • [кат. ] 1 + 1 = 2
• • • • • Молекулярность — это минимальное число различных частиц, участвующих в элементарном акте химического взаимодействия. СН 4 → С + 2 Н 2 -мономолекулярная Н 2 + I 2 → 2 HI - би 2 KMn. O 4 + 5 H 2 C 2 O 4 + 3 H 2 SO 4 → K 2 SO 4 + 2 Mn. SO 4 + 8 H 2 O + 10 CO 2 три Порядок реакции — это сумма показателей степеней в математическом выражении закона действия масс: a. A + b. B = d. D v = K • CА a • CВ b , n = a + b … — общий порядок реакции. Показатель степени при какой-либо одной концентрации определяет порядок реакции по данному компоненту. Например, а — показывает порядок реакции по компоненту А и т. д. Различают реакции I порядка: С + О 2 = СО 2 v = K[O 2] В реакциях II порядка скорость : H 2 + I 2 = 2 HI v = K[H 2][I 2] уравнение II порядка: 1 + 1 = 2 2 Н 2 О ↔ 2 Н 2 + О 2 v = K[H 2 O]2 прямая реакция II порядка, а обратная — III порядка: v 2[O ] 2 + 1 = 3 = K[H 2] 2 Реакция III порядка в газовой фазе — окисление оксида азота [II]: 2 NO + O 2 → 2 NO 2 Катализатор повышает порядок реакций, например: v = K 1 • [Н 2 О 2] • [кат. ] 1 + 1 = 2
![Влияние температуры: • Правило Вант-Гоффа [1884] читается так: где • При повышении температуры на Влияние температуры: • Правило Вант-Гоффа [1884] читается так: где • При повышении температуры на](https://present5.com/presentation/3/-30500059_18307528.pdf-img/-30500059_18307528.pdf-5.jpg) Влияние температуры: • Правило Вант-Гоффа [1884] читается так: где • При повышении температуры на 10˚ скорость химической реакции увеличивается в 2 -4 раза. vt 2 — скорость реакции при конечной температуре; vt 1 — скорость реакции при начальной температуре; γ — температурный коэффициент, зависящий от природы реагирующих веществ Kt˚ — константа скорости при t˚, Kt˚+10˚ — константа скорости при t˚+10˚.
Влияние температуры: • Правило Вант-Гоффа [1884] читается так: где • При повышении температуры на 10˚ скорость химической реакции увеличивается в 2 -4 раза. vt 2 — скорость реакции при конечной температуре; vt 1 — скорость реакции при начальной температуре; γ — температурный коэффициент, зависящий от природы реагирующих веществ Kt˚ — константа скорости при t˚, Kt˚+10˚ — константа скорости при t˚+10˚.
 • В 1889 г. С. Аррениус предположил, что влияние температуры сводится к увеличению числа активных молекул • • где К — константа скорости реакции; е — основание натуральных логарифмов, Т — абсолютная температура, R — газовая постоянная; Еакт — энергия активации [к. Дж/моль], А — предэкспоненциальный множитель или коэффициент, равный общему числу соударений за единицу времени в единице объёма. Для ионных реакций энергия активации мала [менее 40 к. Дж/моль], для синтеза • аммиака она высока [выше 120 к. Дж/моль],
• В 1889 г. С. Аррениус предположил, что влияние температуры сводится к увеличению числа активных молекул • • где К — константа скорости реакции; е — основание натуральных логарифмов, Т — абсолютная температура, R — газовая постоянная; Еакт — энергия активации [к. Дж/моль], А — предэкспоненциальный множитель или коэффициент, равный общему числу соударений за единицу времени в единице объёма. Для ионных реакций энергия активации мала [менее 40 к. Дж/моль], для синтеза • аммиака она высока [выше 120 к. Дж/моль],
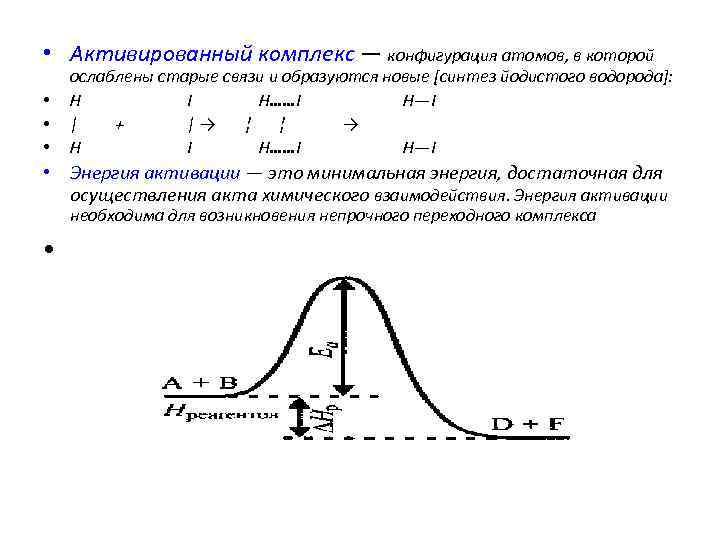 • Активированный комплекс — конфигурация атомов, в которой • • • ослаблены старые связи и образуются новые [синтез йодистого водорода]: H I H……I H—I | + |→ ¦ ¦ → H I H……I H—I • Энергия активации — это минимальная энергия, достаточная для осуществления акта химического взаимодействия. Энергия активации необходима для возникновения непрочного переходного комплекса •
• Активированный комплекс — конфигурация атомов, в которой • • • ослаблены старые связи и образуются новые [синтез йодистого водорода]: H I H……I H—I | + |→ ¦ ¦ → H I H……I H—I • Энергия активации — это минимальная энергия, достаточная для осуществления акта химического взаимодействия. Энергия активации необходима для возникновения непрочного переходного комплекса •
 • Катализом называется явление изменения скорости реакции под воздействием небольших добавок специфических веществ, количество которых в ходе реакции не изменяется. • Характерными признаками катализаторов являются следующие: • 1. Действие катализаторов строго специфично. • Al 2 O 3 C 2 H 4 + 2 H 2 O C 2 H 5 OH • Cu CH 3—C=O + H 2 • • H • 2. Неизменность количества катализатора и его химического состава к концу реакции. • 3. Количество катализатора незначительно по сравнению с количеством реагирующих веществ. • 4. Константа равновесия в обратимых реакциях не изменяется. Катализаторы не смещают химического равновесия, они в равной степени влияют и на прямую и на обратную реакцию.
• Катализом называется явление изменения скорости реакции под воздействием небольших добавок специфических веществ, количество которых в ходе реакции не изменяется. • Характерными признаками катализаторов являются следующие: • 1. Действие катализаторов строго специфично. • Al 2 O 3 C 2 H 4 + 2 H 2 O C 2 H 5 OH • Cu CH 3—C=O + H 2 • • H • 2. Неизменность количества катализатора и его химического состава к концу реакции. • 3. Количество катализатора незначительно по сравнению с количеством реагирующих веществ. • 4. Константа равновесия в обратимых реакциях не изменяется. Катализаторы не смещают химического равновесия, они в равной степени влияют и на прямую и на обратную реакцию.
 • По влиянию на скорость реакции • 1. Положительный катализ увеличивает скорость реакции [пример: горение сахара в присутствии солей лития ускоряется]. • 2. Отрицательный катализ уменьшает скорость реакции [пример: ионы Hg 2+ замедляют реакцию: • 2 KIO 3 + 5 Na 2 SO 3 + H 2 SO 4 = I 2 + 5 Na 2 SO 4 + K 2 SO 4 + H 2 O ]. • вещества, которые усиливают действие катализатора — промоторы, активаторы [для платины промоторами являются железо, алюминий, оксид кремния]; • Вещества, понижающие активность катализатора, - каталитические яды [мышьяк, сероводород, синильная кислота отравляют платину].
• По влиянию на скорость реакции • 1. Положительный катализ увеличивает скорость реакции [пример: горение сахара в присутствии солей лития ускоряется]. • 2. Отрицательный катализ уменьшает скорость реакции [пример: ионы Hg 2+ замедляют реакцию: • 2 KIO 3 + 5 Na 2 SO 3 + H 2 SO 4 = I 2 + 5 Na 2 SO 4 + K 2 SO 4 + H 2 O ]. • вещества, которые усиливают действие катализатора — промоторы, активаторы [для платины промоторами являются железо, алюминий, оксид кремния]; • Вещества, понижающие активность катализатора, - каталитические яды [мышьяк, сероводород, синильная кислота отравляют платину].
 • По различным механизмам катализа различают: • 1. Гомогенный. • 2. Гетерогенный. • 3. Микрогетерогенный. • 4. Аутокатализ. • 5. Катализ в скрытой форме. • 6. Ферментативный.
• По различным механизмам катализа различают: • 1. Гомогенный. • 2. Гетерогенный. • 3. Микрогетерогенный. • 4. Аутокатализ. • 5. Катализ в скрытой форме. • 6. Ферментативный.
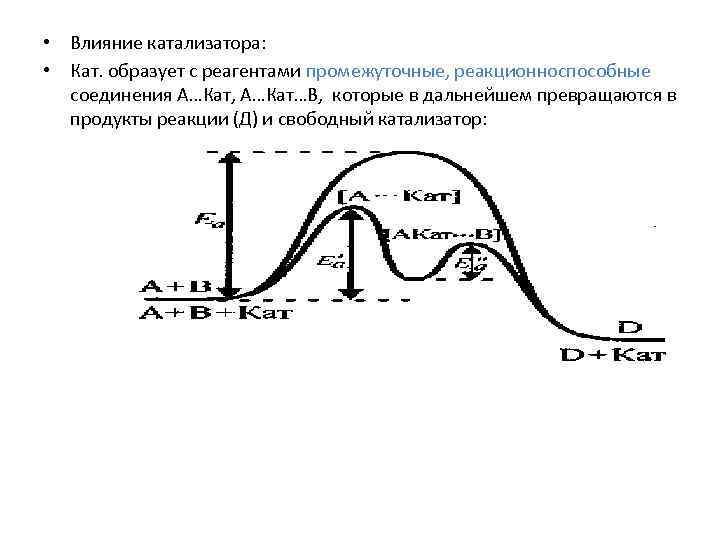 • Влияние катализатора: • Кат. образует с реагентами промежуточные, реакционноспособные соединения А…Кат, А…Кат…В, которые в дальнейшем превращаются в продукты реакции (Д) и свободный катализатор:
• Влияние катализатора: • Кат. образует с реагентами промежуточные, реакционноспособные соединения А…Кат, А…Кат…В, которые в дальнейшем превращаются в продукты реакции (Д) и свободный катализатор:
 • При гомогенном катализе реагирующие вещества и катализатор составляют одну фазу — газовую или жидкую. • нитрозный способ получения серной кислоты: • 2 SO 2 + O 2 = 2 SO 3 • C катализаторjv – NO -2 стадии, энергия активации которых ниже: • O 2 + 2 NO = 2 NO 2 • 2 SO 2 + 2 NO 2 = 2 SO 3 + 2 NO • A K AK B AK AB K
• При гомогенном катализе реагирующие вещества и катализатор составляют одну фазу — газовую или жидкую. • нитрозный способ получения серной кислоты: • 2 SO 2 + O 2 = 2 SO 3 • C катализаторjv – NO -2 стадии, энергия активации которых ниже: • O 2 + 2 NO = 2 NO 2 • 2 SO 2 + 2 NO 2 = 2 SO 3 + 2 NO • A K AK B AK AB K
 • Механизм гетерогенного катализа различен. в присутствии Mn. O 2 : • 2 KCl. O 3 = 2 KCl + 3 O 2 • 1/ 2 KCl. O 3 + 4 Mn. O 2 = 2 KCl + 2 Mn 2 O 7 • 2/ 2 Mn 2 O 7 = 4 Mn. O 2 + 3 O 2 • Разновидностью гетерогенного катализа является микрогетерогенный катализ, когда катализатор находится в коллоидном состоянии [ВМС] — ферменты. • Они обладают высокой специфичностью, их активаторами являются микроэлементы
• Механизм гетерогенного катализа различен. в присутствии Mn. O 2 : • 2 KCl. O 3 = 2 KCl + 3 O 2 • 1/ 2 KCl. O 3 + 4 Mn. O 2 = 2 KCl + 2 Mn 2 O 7 • 2/ 2 Mn 2 O 7 = 4 Mn. O 2 + 3 O 2 • Разновидностью гетерогенного катализа является микрогетерогенный катализ, когда катализатор находится в коллоидном состоянии [ВМС] — ферменты. • Они обладают высокой специфичностью, их активаторами являются микроэлементы
 • Аутокатализ — катализ, при котором катализатором является один из продуктов реакции, например: • 2 KMn. O 4 + 5 H 2 C 2 O 4 + 3 H 2 SO 4 = 2 Mn. SO 4 + 10 CO 2 + K 2 SO 4 + 8 H 2 O • Катализатором служат образующиеся ионы Mn 2+. • Катализ в скрытой форме. : • ---- Вода, даже в виде следов, оказывается активным катализатором. Например, при её отсутствии хлор не реагирует с металлами, фтористоводородная кислота не разъедает стекло и т. д. • ------Каталитическое влияние в скрытой форме оказывают стенки сосуда: • реакция Н 2 с О 2 в стеклянном сосуде идёт при температуре 450˚, а в платиновом — при обычной.
• Аутокатализ — катализ, при котором катализатором является один из продуктов реакции, например: • 2 KMn. O 4 + 5 H 2 C 2 O 4 + 3 H 2 SO 4 = 2 Mn. SO 4 + 10 CO 2 + K 2 SO 4 + 8 H 2 O • Катализатором служат образующиеся ионы Mn 2+. • Катализ в скрытой форме. : • ---- Вода, даже в виде следов, оказывается активным катализатором. Например, при её отсутствии хлор не реагирует с металлами, фтористоводородная кислота не разъедает стекло и т. д. • ------Каталитическое влияние в скрытой форме оказывают стенки сосуда: • реакция Н 2 с О 2 в стеклянном сосуде идёт при температуре 450˚, а в платиновом — при обычной.
 • • Ферментативный катализ. ферменты — биологические катализаторы. У ферментов имеется ряд уникальных свойств: 1. Это самые эффективные катализаторы, их активность в 106– 109 раз превышает активность небиологических катализаторов. 2. Ферменты очень специфичны. 3. Способны переходить от состояния с низкой активностью к состоянию с высокой активностью. 4. В процессе протекания каталитической реакции может происходить постепенная инактивация фермента. 5. Ферменты более чувствительны к изменению внешних условий [температуры, р. Н среды, присутствию ингибиторов и активаторов].
• • Ферментативный катализ. ферменты — биологические катализаторы. У ферментов имеется ряд уникальных свойств: 1. Это самые эффективные катализаторы, их активность в 106– 109 раз превышает активность небиологических катализаторов. 2. Ферменты очень специфичны. 3. Способны переходить от состояния с низкой активностью к состоянию с высокой активностью. 4. В процессе протекания каталитической реакции может происходить постепенная инактивация фермента. 5. Ферменты более чувствительны к изменению внешних условий [температуры, р. Н среды, присутствию ингибиторов и активаторов].
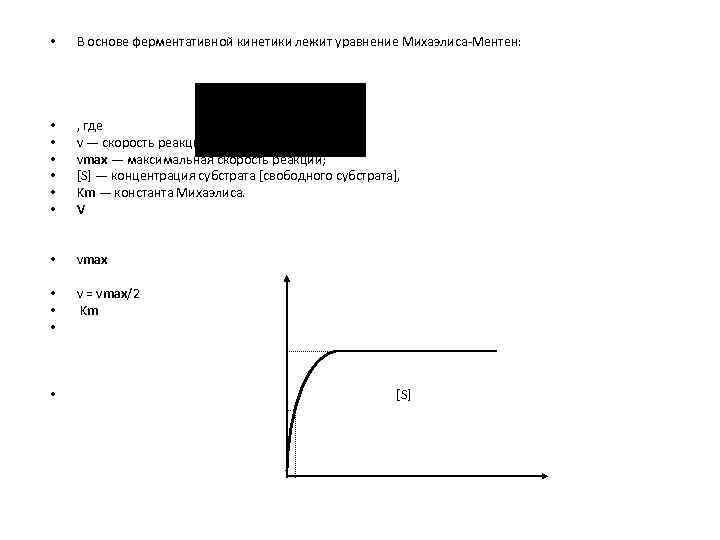 • В основе ферментативной кинетики лежит уравнение Михаэлиса-Ментен: • • • , где v — скорость реакции; vmax — максимальная скорость реакции; [S] — концентрация субстрата [свободного субстрата], Km — константа Михаэлиса. V • vmax • • • v = vmax/2 Km • [S]
• В основе ферментативной кинетики лежит уравнение Михаэлиса-Ментен: • • • , где v — скорость реакции; vmax — максимальная скорость реакции; [S] — концентрация субстрата [свободного субстрата], Km — константа Михаэлиса. V • vmax • • • v = vmax/2 Km • [S]
 • • • Ингибирование ферментов. Ингибиторами ферментов являются: антибиотики, антивирусные средства, противоопухолевые средства, инсектициды, гербициды. Ингибирование конкурентное: ингибитор и субстрат имеют сходные структуры и ингибитор связывает фермент. Ингибитор связывается обратимо. Пример: сульфаниламидные препараты имеют сходство с пара-аминобензойной кислотой, необходимой для синтеза нуклеиновых кислот микроорганизмов. Нужно повысить концентрацию субстрата, чтобы вытеснить ингибитор. Ингибирование неконкурентное: ингибитор, субстрат и фермент образуют тройной комплекс. Повышение концентрации субстрата не помогает. Существует и необратимое ингибирование, когда ингибиторы ковалентно связываются с ферментом [ионы ртути, свинца, мышьяка, пенициллин]. Активаторами ферментов являются ионы калия, натрия, хлора и др
• • • Ингибирование ферментов. Ингибиторами ферментов являются: антибиотики, антивирусные средства, противоопухолевые средства, инсектициды, гербициды. Ингибирование конкурентное: ингибитор и субстрат имеют сходные структуры и ингибитор связывает фермент. Ингибитор связывается обратимо. Пример: сульфаниламидные препараты имеют сходство с пара-аминобензойной кислотой, необходимой для синтеза нуклеиновых кислот микроорганизмов. Нужно повысить концентрацию субстрата, чтобы вытеснить ингибитор. Ингибирование неконкурентное: ингибитор, субстрат и фермент образуют тройной комплекс. Повышение концентрации субстрата не помогает. Существует и необратимое ингибирование, когда ингибиторы ковалентно связываются с ферментом [ионы ртути, свинца, мышьяка, пенициллин]. Активаторами ферментов являются ионы калия, натрия, хлора и др
 • По характеру промежуточного взаимодействия катализ различают: 1. Кислотно-основной. 2. Окислительно-восстановительный. 3. Металлокомплексный. Кислотно-основной катализ [Оствальд, Аррениус]. При кислотно-основном катализе катализаторами являются ионы Н+ [Н 3 О+] и ОН–. При гетерогенном кислотно-основном катализе катализаторами могут быть нерастворимые кислоты и основания, реакции: этерификации спиртов, гидролиз сложных эфиров [ускоряется кислотами], гидролиз крахмала и др. Окислительно-восстановительный катализ — промежуточное взаимодействие связано с переходами электронов между катализатором и реагирующим веществом. Например: 2 SO 2 + O 2 = 2 SO 3 NO — катализатор • О 2 + 2 NO = 2 NO 2 • • 2 NO 2 + 2 SO 2 = 2 SO 3 + 2 NO
• По характеру промежуточного взаимодействия катализ различают: 1. Кислотно-основной. 2. Окислительно-восстановительный. 3. Металлокомплексный. Кислотно-основной катализ [Оствальд, Аррениус]. При кислотно-основном катализе катализаторами являются ионы Н+ [Н 3 О+] и ОН–. При гетерогенном кислотно-основном катализе катализаторами могут быть нерастворимые кислоты и основания, реакции: этерификации спиртов, гидролиз сложных эфиров [ускоряется кислотами], гидролиз крахмала и др. Окислительно-восстановительный катализ — промежуточное взаимодействие связано с переходами электронов между катализатором и реагирующим веществом. Например: 2 SO 2 + O 2 = 2 SO 3 NO — катализатор • О 2 + 2 NO = 2 NO 2 • • 2 NO 2 + 2 SO 2 = 2 SO 3 + 2 NO
 • • • • Кинетика сложных реакций. Сложные реакции подразделяются на параллельные, последовательные, сопряжённые и цепные. А. Параллельные реакции — связанная система реакций, имеющих одни и те же исходные реагенты, но различные продукты реакции. Скорость системы параллельных реакций равна сумме скоростей отдельных реакций: v 1 4 KCl + 6 O 2 4 KCl. O 3 vобщ = v 1 + v 2 3 KCl. O 4 + KCl Б. Последовательные реакции — связанная система реакций, в которой продукты предыдущих стадий расходуются в последующих реакциях. Скорость реакции= скорости самой медленной (лимитирующей) стадии. 2 NO + O 2 = N 2 O 4 v 1 1/ 2 NO ↔ [NO]2 v 2 2/ [NO]2 + O 2 ↔ N 2 O 4
• • • • Кинетика сложных реакций. Сложные реакции подразделяются на параллельные, последовательные, сопряжённые и цепные. А. Параллельные реакции — связанная система реакций, имеющих одни и те же исходные реагенты, но различные продукты реакции. Скорость системы параллельных реакций равна сумме скоростей отдельных реакций: v 1 4 KCl + 6 O 2 4 KCl. O 3 vобщ = v 1 + v 2 3 KCl. O 4 + KCl Б. Последовательные реакции — связанная система реакций, в которой продукты предыдущих стадий расходуются в последующих реакциях. Скорость реакции= скорости самой медленной (лимитирующей) стадии. 2 NO + O 2 = N 2 O 4 v 1 1/ 2 NO ↔ [NO]2 v 2 2/ [NO]2 + O 2 ↔ N 2 O 4
 • В. Сопряжённые реакции —реакции, каждая из которых происходит только при условии протекания другой реакции, причем обе реакции имеют общий промежуточный продукт • 1/ 6 Fe. O + 2 H 2 Cr. O 4 = 3 Fe 2 O 3[катализатор!] + Cr 2 O 3 + 2 H 2 O • 2/ 6 HI + 2 H 2 Cr. O 4 = 3 I 2 + Cr 2 O 3 + 5 H 2 O • Г. Цепные реакции — связанная система сложных реакций, протекающих последовательно, параллельно и сопряжённо с участием свободных радикалов [горение, взрывы, фотохимические реакции]. • Основные стадии реакции: • а/ зарождение цепи; • б/ разветвление цепи; • в/ продолжение цепи; • г/ обрыв цепи.
• В. Сопряжённые реакции —реакции, каждая из которых происходит только при условии протекания другой реакции, причем обе реакции имеют общий промежуточный продукт • 1/ 6 Fe. O + 2 H 2 Cr. O 4 = 3 Fe 2 O 3[катализатор!] + Cr 2 O 3 + 2 H 2 O • 2/ 6 HI + 2 H 2 Cr. O 4 = 3 I 2 + Cr 2 O 3 + 5 H 2 O • Г. Цепные реакции — связанная система сложных реакций, протекающих последовательно, параллельно и сопряжённо с участием свободных радикалов [горение, взрывы, фотохимические реакции]. • Основные стадии реакции: • а/ зарождение цепи; • б/ разветвление цепи; • в/ продолжение цепи; • г/ обрыв цепи.
 • Цепные реакции можно подразделить на неразветвлённые и разветвлённые. неразветвлённая реакция: • Cl 2 + hν = Cl • + Cl • • H 2 + Cl • = HCl + H • • H • + Cl 2 = HCl + Cl • • К разветвленным реакциям - полимеризации, крекинг, сгорание топлива в двигателях, окисление и др. , например, ядерные цепные реакции
• Цепные реакции можно подразделить на неразветвлённые и разветвлённые. неразветвлённая реакция: • Cl 2 + hν = Cl • + Cl • • H 2 + Cl • = HCl + H • • H • + Cl 2 = HCl + Cl • • К разветвленным реакциям - полимеризации, крекинг, сгорание топлива в двигателях, окисление и др. , например, ядерные цепные реакции
 • • • фотохимические реакции — реакции, происходящие под действием лучей света [видимых, инфракрасных, ультрафиолетовых]. Эффективность фотохимической реакции определяется так называемым квантовым выходом γ: γ = число молекул продукта реакции число поглощённых квантов • • Фотохимические реакции бывают различных типов: а/ синтез вещества [фотосинтез] и б/ разложение веществ под действием света [фотолиз : hν 2 HCl → H 2 + Cl 2 Фотосинтез, происходящий в растениях — сложный окислительновосстановительный процесс, сочетающий фотохимические реакции с ферментативными. | CO 2 + 2 H 2 O → [H—C—OH]n + O 2 |
• • • фотохимические реакции — реакции, происходящие под действием лучей света [видимых, инфракрасных, ультрафиолетовых]. Эффективность фотохимической реакции определяется так называемым квантовым выходом γ: γ = число молекул продукта реакции число поглощённых квантов • • Фотохимические реакции бывают различных типов: а/ синтез вещества [фотосинтез] и б/ разложение веществ под действием света [фотолиз : hν 2 HCl → H 2 + Cl 2 Фотосинтез, происходящий в растениях — сложный окислительновосстановительный процесс, сочетающий фотохимические реакции с ферментативными. | CO 2 + 2 H 2 O → [H—C—OH]n + O 2 |
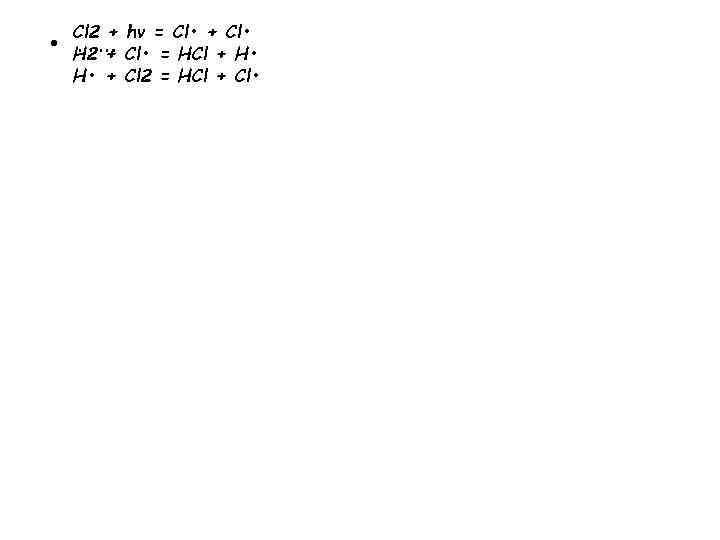 • Cl 2 + hν = Cl • + Cl • ……. H 2 + Cl • = HCl + H • + Cl 2 = HCl + Cl •
• Cl 2 + hν = Cl • + Cl • ……. H 2 + Cl • = HCl + H • + Cl 2 = HCl + Cl •


