Химическая кинетика и равновесие испр.ppt
- Количество слайдов: 46
 Химическая кинетика Авторы презентации: доцент, к. х. н. Е. М. Мясоедов доцент, к. т. н. Ю. В. Устинова Редактор: профессор, д. х. н. В. И. Сидоров
Химическая кинетика Авторы презентации: доцент, к. х. н. Е. М. Мясоедов доцент, к. т. н. Ю. В. Устинова Редактор: профессор, д. х. н. В. И. Сидоров
 Система – это область пространства, включающая тело или группу тел, условно или при помощи реальных границ отделённых от окружающей среды. Фаза – это однородная по составу и свойствам часть системы, отделенная от других её частей поверхностью раздела, при переходе через которую резко изменяются её состав или свойства. Однофазные системы называют гомогенными. Многофазные системы – гетерогенными.
Система – это область пространства, включающая тело или группу тел, условно или при помощи реальных границ отделённых от окружающей среды. Фаза – это однородная по составу и свойствам часть системы, отделенная от других её частей поверхностью раздела, при переходе через которую резко изменяются её состав или свойства. Однофазные системы называют гомогенными. Многофазные системы – гетерогенными.
 Химическая кинетика изучает скорости химических реакций и механизм их протекания. Химическая реакция – превращение молекул (с изменением их состава и структуры). В основе кинетики – принцип соударений молекул. В гомогенных системах столкновения между молекулами происходят во всём объёме системы (гомогенные реакции). В гетерогенных – на границе раздела фаз (гетерогенные реакции).
Химическая кинетика изучает скорости химических реакций и механизм их протекания. Химическая реакция – превращение молекул (с изменением их состава и структуры). В основе кинетики – принцип соударений молекул. В гомогенных системах столкновения между молекулами происходят во всём объёме системы (гомогенные реакции). В гетерогенных – на границе раздела фаз (гетерогенные реакции).
 Скорость реакции обратно пропорциональна времени, за которое происходят химические превращения (быстрые и медленные реакции). Скорость химической реакции определяется числом молекул вещества, вступивших в реакцию, или образовавшихся в результате реакции в единицу времени в единице объёма гомогенной системы, или на единице площади раздела фаз в гетерогенной системе.
Скорость реакции обратно пропорциональна времени, за которое происходят химические превращения (быстрые и медленные реакции). Скорость химической реакции определяется числом молекул вещества, вступивших в реакцию, или образовавшихся в результате реакции в единицу времени в единице объёма гомогенной системы, или на единице площади раздела фаз в гетерогенной системе.
 Скорость гомогенных химических реакций Средняя скорость реакции определяется изменением концентрации вещества за промежуток времени Мгновенная скорость реакции при
Скорость гомогенных химических реакций Средняя скорость реакции определяется изменением концентрации вещества за промежуток времени Мгновенная скорость реакции при
 Факторы, влияющие на скорость химической реакции: – природа реагирующих веществ (прочность химических связей, структура молекул, энергетические факторы и т. д. ), – концентрация реагирующих веществ (частота соударений молекул), – температура в системе (частота соударений молекул), – наличие катализатора.
Факторы, влияющие на скорость химической реакции: – природа реагирующих веществ (прочность химических связей, структура молекул, энергетические факторы и т. д. ), – концентрация реагирующих веществ (частота соударений молекул), – температура в системе (частота соударений молекул), – наличие катализатора.
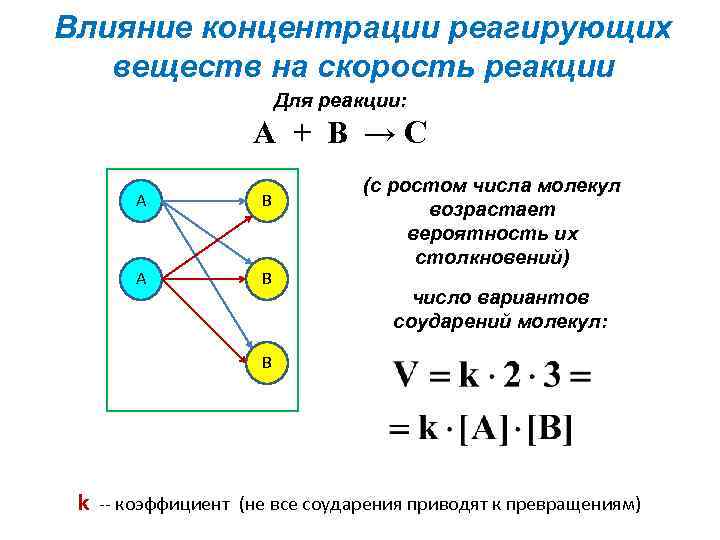 Влияние концентрации реагирующих веществ на скорость реакции Для реакции: А + В →С A B (с ростом числа молекул возрастает вероятность их столкновений) число вариантов соударений молекул: B k -- коэффициент (не все соударения приводят к превращениям)
Влияние концентрации реагирующих веществ на скорость реакции Для реакции: А + В →С A B (с ростом числа молекул возрастает вероятность их столкновений) число вариантов соударений молекул: B k -- коэффициент (не все соударения приводят к превращениям)
 Более сложные реакции можно представить в виде нескольких последовательных элементарных стадий: Для реакции: 2 А + В → С А + В → АВ А + АВ → С
Более сложные реакции можно представить в виде нескольких последовательных элементарных стадий: Для реакции: 2 А + В → С А + В → АВ А + АВ → С
 Закон действующих масс (открыт Гульдбергом и Вааге) При постоянной температуре скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ, взятых в степенях, равных стехиометрическим коэффициентам в уравнении реакции.
Закон действующих масс (открыт Гульдбергом и Вааге) При постоянной температуре скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ, взятых в степенях, равных стехиометрическим коэффициентам в уравнении реакции.
 Математическое выражение закона действующих масс в общем виде: или V – скорость реакции; k – константа скорости реакции (отражает долю столкновений, приводящих к продукту реакции; CA или [A] – концентрация вещества A (моль/л); CB или [B] – концентрация вещества B (моль/л); m, n – стехиометрические коэффициенты.
Математическое выражение закона действующих масс в общем виде: или V – скорость реакции; k – константа скорости реакции (отражает долю столкновений, приводящих к продукту реакции; CA или [A] – концентрация вещества A (моль/л); CB или [B] – концентрация вещества B (моль/л); m, n – стехиометрические коэффициенты.
 Для конкретной реакции, например: или k – константа скорости химической реакции Величина k зависит от природы реагирующих веществ и температуры. Величина k не зависит от концентраций веществ. Константа скорости химической реакции численно равна величине скорости реакции при концентрациях веществ 1 моль/л.
Для конкретной реакции, например: или k – константа скорости химической реакции Величина k зависит от природы реагирующих веществ и температуры. Величина k не зависит от концентраций веществ. Константа скорости химической реакции численно равна величине скорости реакции при концентрациях веществ 1 моль/л.
 Одновременное столкновение более 2 молекул маловероятно. Реакции с участием более 3 молекул происходят в несколько элементарных стадий. Закон действующих масс справедлив для каждой стадии, а не для реакции в целом. Основной постулат химической кинетики При постоянной температуре скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ, взятых в некоторых степенях.
Одновременное столкновение более 2 молекул маловероятно. Реакции с участием более 3 молекул происходят в несколько элементарных стадий. Закон действующих масс справедлив для каждой стадии, а не для реакции в целом. Основной постулат химической кинетики При постоянной температуре скорость химической реакции прямо пропорциональна произведению молярных концентраций реагирующих веществ, взятых в некоторых степенях.
 Показатель степени в кинетическом уравнении – порядок реакции по данному веществу. p. A – порядок реакции по веществу А p. B – порядок реакции по веществу B. Общий порядок реакции – сумма порядков по всем реагентам: p = p. A + p. B Порядок реакции часто не совпадает с коэффициентами в уравнении, т. к. зависит от числа стадий, механизма реакции и т. д. Порядок реакции может быть целым, дробным, равным нулю. Его определяют опытным путём.
Показатель степени в кинетическом уравнении – порядок реакции по данному веществу. p. A – порядок реакции по веществу А p. B – порядок реакции по веществу B. Общий порядок реакции – сумма порядков по всем реагентам: p = p. A + p. B Порядок реакции часто не совпадает с коэффициентами в уравнении, т. к. зависит от числа стадий, механизма реакции и т. д. Порядок реакции может быть целым, дробным, равным нулю. Его определяют опытным путём.
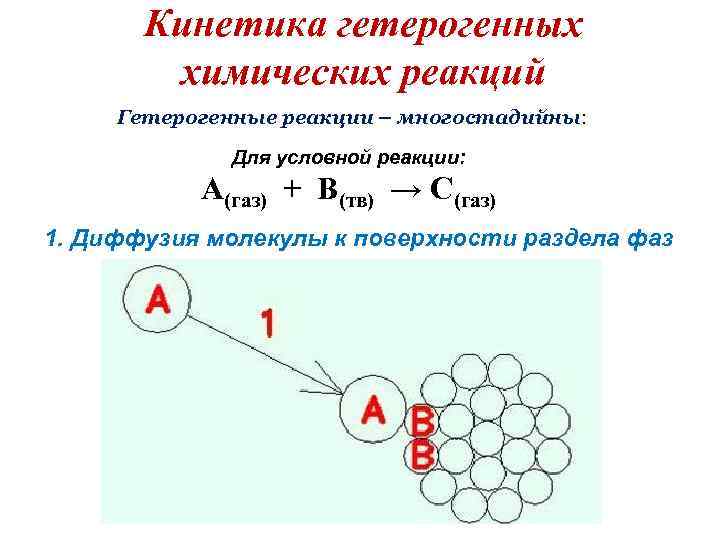 Кинетика гетерогенных химических реакций Гетерогенные реакции – многостадийны: Для условной реакции: А(газ) + В(тв) → С(газ) 1. Диффузия молекулы к поверхности раздела фаз
Кинетика гетерогенных химических реакций Гетерогенные реакции – многостадийны: Для условной реакции: А(газ) + В(тв) → С(газ) 1. Диффузия молекулы к поверхности раздела фаз
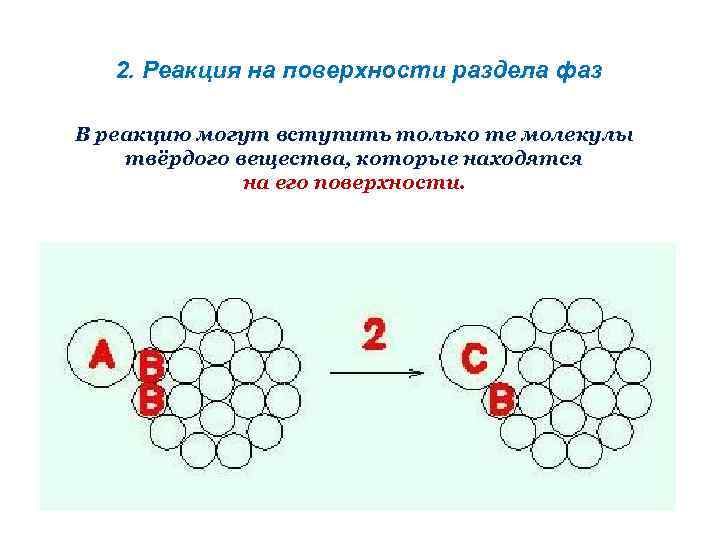 2. Реакция на поверхности раздела фаз В реакцию могут вступить только те молекулы твёрдого вещества, которые находятся на его поверхности.
2. Реакция на поверхности раздела фаз В реакцию могут вступить только те молекулы твёрдого вещества, которые находятся на его поверхности.
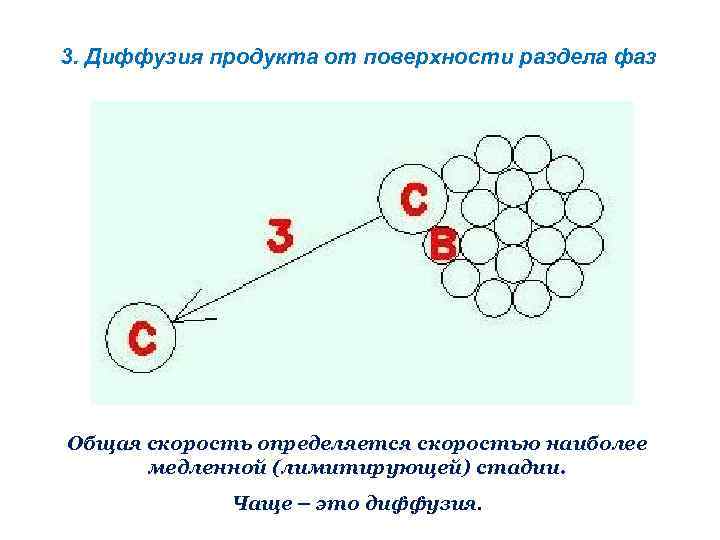 3. Диффузия продукта от поверхности раздела фаз Общая скорость определяется скоростью наиболее медленной (лимитирующей) стадии. Чаще – это диффузия.
3. Диффузия продукта от поверхности раздела фаз Общая скорость определяется скоростью наиболее медленной (лимитирующей) стадии. Чаще – это диффузия.
 Закон действующих масс для гетерогенных реакций Например: Формально: Горение угля Но общая концентрация твёрдого вещества не влияет на скорость (реагирует только с поверхности). На скорость гетерогенного процесса влияет только удельная поверхность ( Sс ) твёрдого вещества (отношение общей поверхности тела к его объёму или массе).
Закон действующих масс для гетерогенных реакций Например: Формально: Горение угля Но общая концентрация твёрдого вещества не влияет на скорость (реагирует только с поверхности). На скорость гетерогенного процесса влияет только удельная поверхность ( Sс ) твёрдого вещества (отношение общей поверхности тела к его объёму или массе).
 За небольшой промежуток времени удельная поверхность Sc = Const, поэтому Концентрация твёрдых веществ не влияет на скорость гетерогенной реакции. В выражении закона действующих масс она условно принимается за 1.
За небольшой промежуток времени удельная поверхность Sc = Const, поэтому Концентрация твёрдых веществ не влияет на скорость гетерогенной реакции. В выражении закона действующих масс она условно принимается за 1.
 Зависимость скорости реакции от температуры Уравнение Аррениуса k – константа скорости химической реакции; А – предэкспоненциальный множитель (предэкспонента) (учитывает долю результативных столкновений молекул); e = 2, 718 – основание натурального логарифма; T – абсолютная температура; R = 8, 314 Дж/(моль·K) – универсальная газовая постоянная.
Зависимость скорости реакции от температуры Уравнение Аррениуса k – константа скорости химической реакции; А – предэкспоненциальный множитель (предэкспонента) (учитывает долю результативных столкновений молекул); e = 2, 718 – основание натурального логарифма; T – абсолютная температура; R = 8, 314 Дж/(моль·K) – универсальная газовая постоянная.
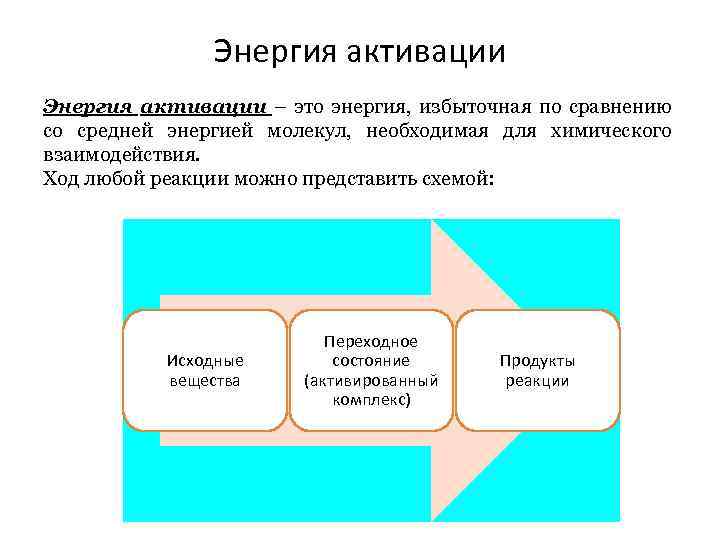 Энергия активации – это энергия, избыточная по сравнению со средней энергией молекул, необходимая для химического взаимодействия. Ход любой реакции можно представить схемой: Исходные вещества Переходное состояние (активированный комплекс) Продукты реакции
Энергия активации – это энергия, избыточная по сравнению со средней энергией молекул, необходимая для химического взаимодействия. Ход любой реакции можно представить схемой: Исходные вещества Переходное состояние (активированный комплекс) Продукты реакции
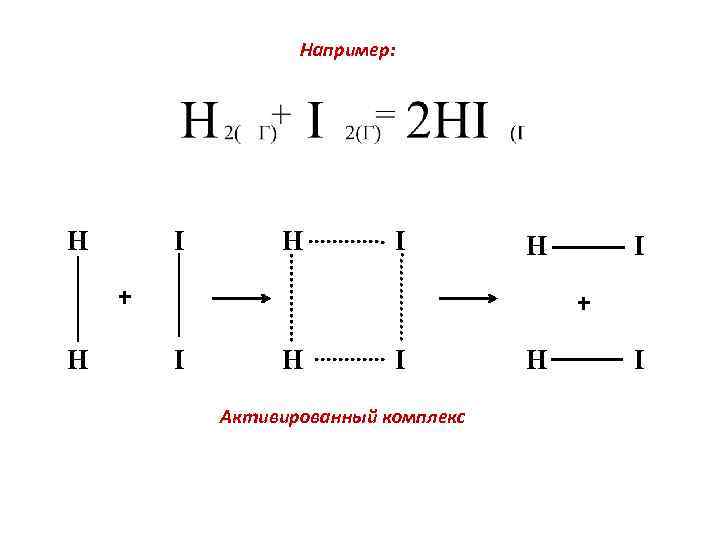 Например: H I H + H I + I H I Активированный комплекс H I
Например: H I H + H I + I H I Активированный комплекс H I
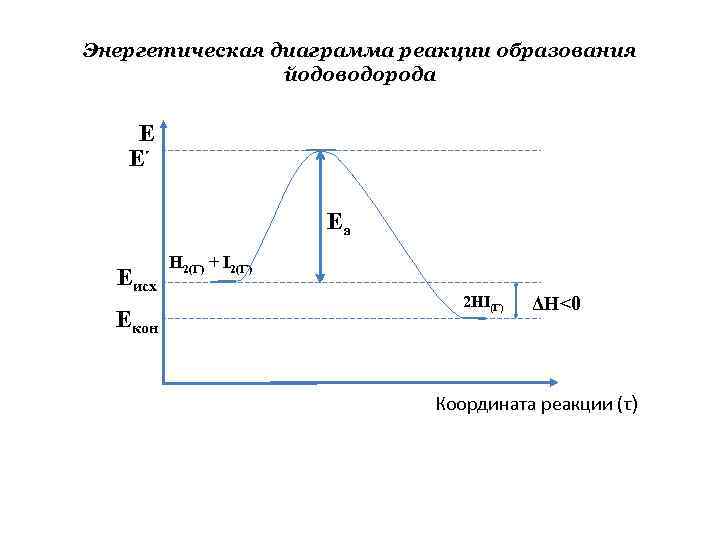 Энергетическая диаграмма реакции образования йодоводорода E E ׳ Ea Eисх Eкон H 2(Г) + I 2(Г) 2 HI(Г) ΔH<0 Координата реакции (τ)
Энергетическая диаграмма реакции образования йодоводорода E E ׳ Ea Eисх Eкон H 2(Г) + I 2(Г) 2 HI(Г) ΔH<0 Координата реакции (τ)
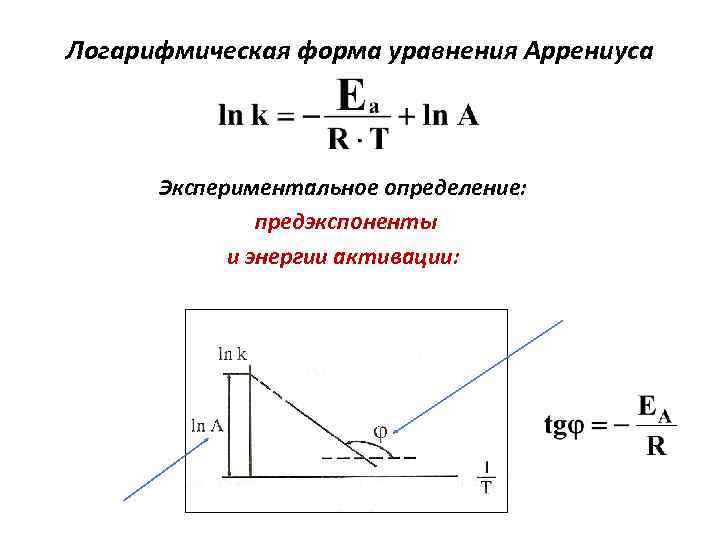 Логарифмическая форма уравнения Аррениуса Экспериментальное определение: предэкспоненты и энергии активации:
Логарифмическая форма уравнения Аррениуса Экспериментальное определение: предэкспоненты и энергии активации:
 Для разбавленных газовых систем: Правило Вант-Гоффа: при изменении температуры на каждые 100 скорость реакции изменяется в 2 – 4 раза. или V 2 – скорость реакции при температуре t 2 V 1 – скорость реакции при температуре t 1 k 2 – константа скорости реакции при температуре t 2 k 1 – константа скорости реакции при температуре t 1 g =2– 4 (температурный коэффициент скорости химической реакции)
Для разбавленных газовых систем: Правило Вант-Гоффа: при изменении температуры на каждые 100 скорость реакции изменяется в 2 – 4 раза. или V 2 – скорость реакции при температуре t 2 V 1 – скорость реакции при температуре t 1 k 2 – константа скорости реакции при температуре t 2 k 1 – константа скорости реакции при температуре t 1 g =2– 4 (температурный коэффициент скорости химической реакции)
 Катализ, катализаторы. Катализ – изменение скорости реакции под действием катализаторов. Положительный катализ – ускорение, отрицательный – замедление реакции. Катализатор – вещество, которое увеличивает скорость химической реакции, формально не расходуясь, или возобновляясь в ней. Ингибитор – вещество, замедляющее химическую реакцию. Катализатор образует промежуточное соединение с одним из реагирующих веществ, но не входит в состав продукта и восстанавливается в неизменном виде.
Катализ, катализаторы. Катализ – изменение скорости реакции под действием катализаторов. Положительный катализ – ускорение, отрицательный – замедление реакции. Катализатор – вещество, которое увеличивает скорость химической реакции, формально не расходуясь, или возобновляясь в ней. Ингибитор – вещество, замедляющее химическую реакцию. Катализатор образует промежуточное соединение с одним из реагирующих веществ, но не входит в состав продукта и восстанавливается в неизменном виде.
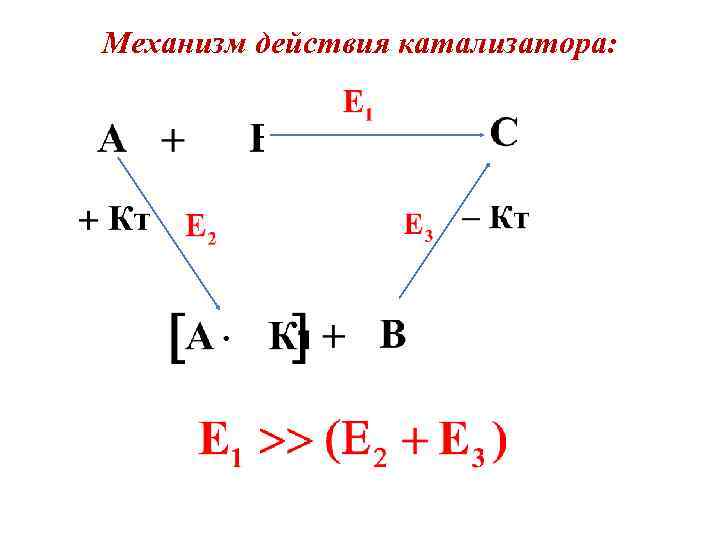 Механизм действия катализатора:
Механизм действия катализатора:
 Виды катализа: • • • гомогенный катализ; гетерогенный катализ: электрокатализ; фотокатализ; ферментативный катализ и др.
Виды катализа: • • • гомогенный катализ; гетерогенный катализ: электрокатализ; фотокатализ; ферментативный катализ и др.
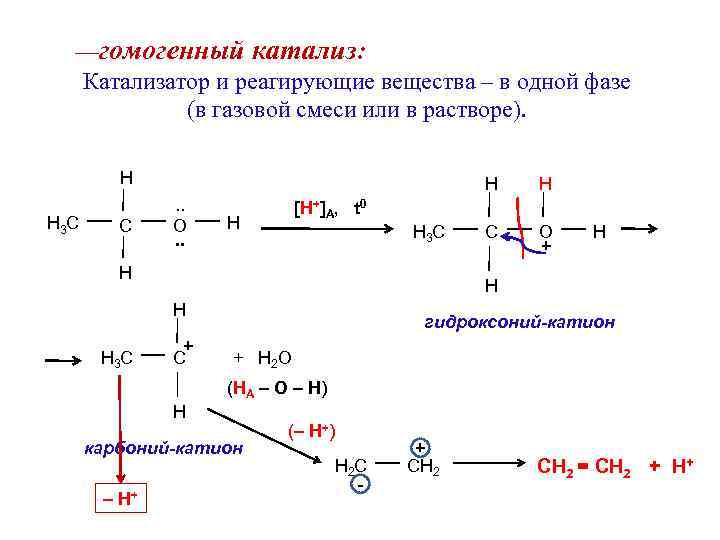 —гомогенный катализ: Катализатор и реагирующие вещества – в одной фазе (в газовой смеси или в растворе). H H 3 C C H. . O. . C O + [H+]A, t 0 H H 3 C H + C гидроксоний-катион + H 2 O (HA – O – H) H карбоний-катион – H+ (– H+) H 2 C - + CH 2 = CH 2 + H+
—гомогенный катализ: Катализатор и реагирующие вещества – в одной фазе (в газовой смеси или в растворе). H H 3 C C H. . O. . C O + [H+]A, t 0 H H 3 C H + C гидроксоний-катион + H 2 O (HA – O – H) H карбоний-катион – H+ (– H+) H 2 C - + CH 2 = CH 2 + H+
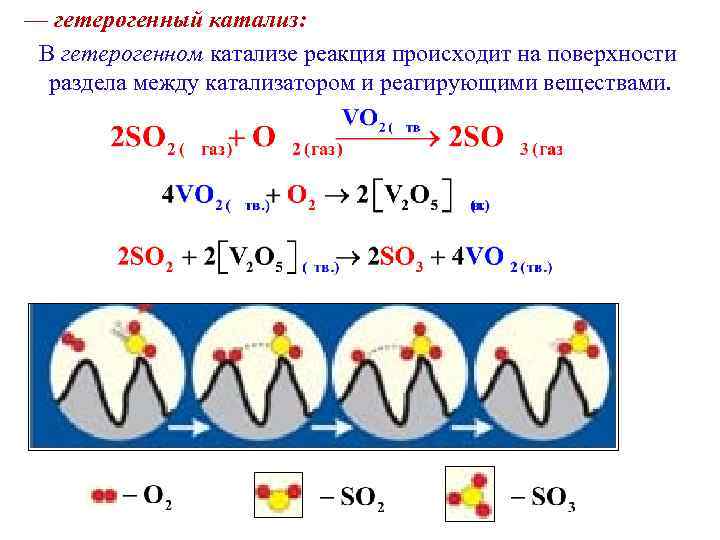 — гетерогенный катализ: В гетерогенном катализе реакция происходит на поверхности раздела между катализатором и реагирующими веществами.
— гетерогенный катализ: В гетерогенном катализе реакция происходит на поверхности раздела между катализатором и реагирующими веществами.
 — электрокатализ: В электрокатализе реакция происходит на поверхности электрода в контакте с раствором или под действием электрического тока. Например, электрокаталитическое окисление предельных углеводородов (C 1 - C 6) на Pt-электроде до СО 2 — сложная цепь промежуточных стадий, включающей разрыв связей С — С, С — Н, хемосорбцию фрагментов исходных молекул на поверхности металла -катализатора, участие в отдельных стадиях адсорбированных молекул Н 2 О или частиц ОН– и т. п.
— электрокатализ: В электрокатализе реакция происходит на поверхности электрода в контакте с раствором или под действием электрического тока. Например, электрокаталитическое окисление предельных углеводородов (C 1 - C 6) на Pt-электроде до СО 2 — сложная цепь промежуточных стадий, включающей разрыв связей С — С, С — Н, хемосорбцию фрагментов исходных молекул на поверхности металла -катализатора, участие в отдельных стадиях адсорбированных молекул Н 2 О или частиц ОН– и т. п.
 — фотокатализ: При фотокатализе реакцию стимулирует энергия поглощающегося излучения. Цепные (самоподдерживающиеся) реакции: 1) инициирование цепи: радикал (частица с неспаренным электроном) 2) развитие цепи:
— фотокатализ: При фотокатализе реакцию стимулирует энергия поглощающегося излучения. Цепные (самоподдерживающиеся) реакции: 1) инициирование цепи: радикал (частица с неспаренным электроном) 2) развитие цепи:
 3) обрыв цепи: Квантовый выход от 1 до 107 молекул
3) обрыв цепи: Квантовый выход от 1 до 107 молекул
 — ферментативный катализ: Ферменты (энзимы) – белковые макромолекулы, являются катализаторами в биологических системах. Например, в организме человека – около 3000 ферментов.
— ферментативный катализ: Ферменты (энзимы) – белковые макромолекулы, являются катализаторами в биологических системах. Например, в организме человека – около 3000 ферментов.
 Химическое равновесие
Химическое равновесие
 Необратимые химические реакции Химические реакции делят на обратимые и необратимые. К необратимым реакциям относят реакции, в которых хотя бы одно из исходных веществ расходуется полностью, например: Чаще всего необратимые реакции происходят в незамкнутых системах
Необратимые химические реакции Химические реакции делят на обратимые и необратимые. К необратимым реакциям относят реакции, в которых хотя бы одно из исходных веществ расходуется полностью, например: Чаще всего необратимые реакции происходят в незамкнутых системах
 Обратимые химические реакции: продукты одной реакции – исходные вещества для другой, и наоборот: Особенность обратимых реакций – в том, что они не идут до конца, в системе всегда остается каждое из исходных веществ Обычно происходят в замкнутых системах
Обратимые химические реакции: продукты одной реакции – исходные вещества для другой, и наоборот: Особенность обратимых реакций – в том, что они не идут до конца, в системе всегда остается каждое из исходных веществ Обычно происходят в замкнутых системах
 Скорость прямой и обратной реакций по закону действующих масс: Со временем концентрации веществ A и В уменьшаются; С и D – увеличиваются
Скорость прямой и обратной реакций по закону действующих масс: Со временем концентрации веществ A и В уменьшаются; С и D – увеличиваются
 При выравнивании скоростей прямой и обратной реакций наступает динамическое состояние химического равновесия В состоянии химического равновесия концентрации всех веществ сохраняются неизменными.
При выравнивании скоростей прямой и обратной реакций наступает динамическое состояние химического равновесия В состоянии химического равновесия концентрации всех веществ сохраняются неизменными.
 Константа химического равновесия Величина Кр зависит от температуры и природы веществ, и не зависит от их концентраций и катализатора. Константа равновесия определяет соотношение между равновесными концентрациями продуктов и исходных веществ. Для гомогенной реакции:
Константа химического равновесия Величина Кр зависит от температуры и природы веществ, и не зависит от их концентраций и катализатора. Константа равновесия определяет соотношение между равновесными концентрациями продуктов и исходных веществ. Для гомогенной реакции:
 Для гетерогенной реакции в замкнутой системе: В выражении константы равновесия: Не учитывают концентрации твёрдых веществ
Для гетерогенной реакции в замкнутой системе: В выражении константы равновесия: Не учитывают концентрации твёрдых веществ
 Смещение химического равновесия
Смещение химического равновесия
 При изменении внешних параметров химической системы: • концентрации реагентов; • давления; • температуры, скорость прямой и обратной реакций могут меняться неодинаково. Это приводит к изменению равновесных концентраций при сохранении величины константы равновесия. Изменение равновесных концентраций – смещение химического равновесия (вправо – в сторону прямой реакции, или влево – в сторону обратной реакции)
При изменении внешних параметров химической системы: • концентрации реагентов; • давления; • температуры, скорость прямой и обратной реакций могут меняться неодинаково. Это приводит к изменению равновесных концентраций при сохранении величины константы равновесия. Изменение равновесных концентраций – смещение химического равновесия (вправо – в сторону прямой реакции, или влево – в сторону обратной реакции)
 Принцип Ле-Шателье – Брауна Анри Луи Ле-Шателье 1850 -1936 гг. Если на систему, находящуюся в состоянии химического равновесия оказать внешнее воздействие, то равновесие смещается таким образом, чтобы уменьшить это воздействие.
Принцип Ле-Шателье – Брауна Анри Луи Ле-Шателье 1850 -1936 гг. Если на систему, находящуюся в состоянии химического равновесия оказать внешнее воздействие, то равновесие смещается таким образом, чтобы уменьшить это воздействие.
 Влияние концентраций веществ на состояние равновесия: Для гомогенной реакции в растворе: красный равновесие «Добавили – расходуется , убавили – восполняется»
Влияние концентраций веществ на состояние равновесия: Для гомогенной реакции в растворе: красный равновесие «Добавили – расходуется , убавили – восполняется»
 Влияние давления – объёма газовой системы (твёрдые, жидкие – не меняют объём) Повышение давления (уменьшение объёма) – в сторону уменьшения числа молекул газов, понижение давления (увеличение объёма) – в сторону увеличения числа молекул газов. Для гомогенной реакции: равновесие
Влияние давления – объёма газовой системы (твёрдые, жидкие – не меняют объём) Повышение давления (уменьшение объёма) – в сторону уменьшения числа молекул газов, понижение давления (увеличение объёма) – в сторону увеличения числа молекул газов. Для гомогенной реакции: равновесие
 Влияние температуры При повышении температуры – в сторону эндотермической реакции (– Q , H 0) При понижении – в сторону экзотермической (+Q, H 0) ( H 0) равновесие
Влияние температуры При повышении температуры – в сторону эндотермической реакции (– Q , H 0) При понижении – в сторону экзотермической (+Q, H 0) ( H 0) равновесие


