5.КИНЕТИКА.ppt
- Количество слайдов: 27
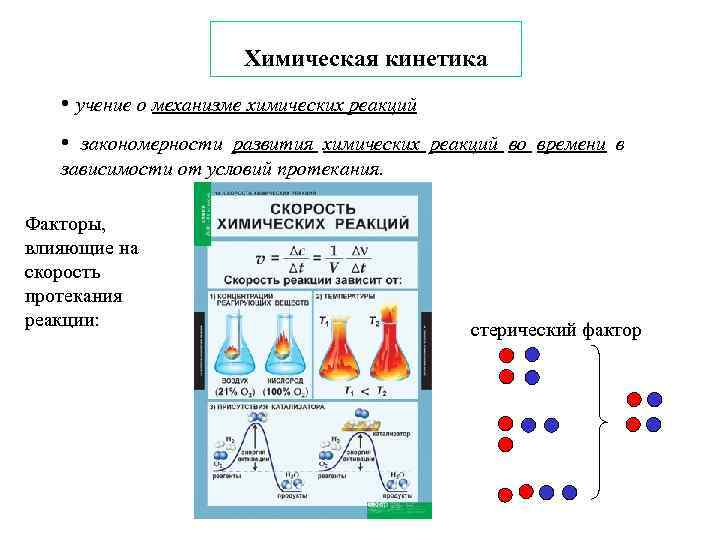 Химическая кинетика • учение о механизме химических реакций • закономерности развития химических реакций во времени в зависимости от условий протекания. Факторы, влияющие на скорость протекания реакции: cтерический фактор
Химическая кинетика • учение о механизме химических реакций • закономерности развития химических реакций во времени в зависимости от условий протекания. Факторы, влияющие на скорость протекания реакции: cтерический фактор
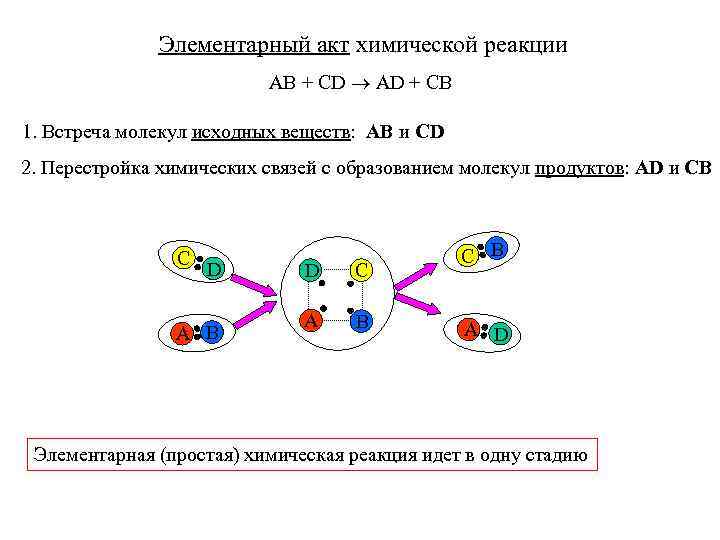 Элементарный акт химической реакции AB + CD AD + CB 1. Встреча молекул исходных веществ: AB и CD 2. Перестройка химических связей с образованием молекул продуктов: AD и CB C D A B D C A B C B A D Элементарная (простая) химическая реакция идет в одну стадию
Элементарный акт химической реакции AB + CD AD + CB 1. Встреча молекул исходных веществ: AB и CD 2. Перестройка химических связей с образованием молекул продуктов: AD и CB C D A B D C A B C B A D Элементарная (простая) химическая реакция идет в одну стадию
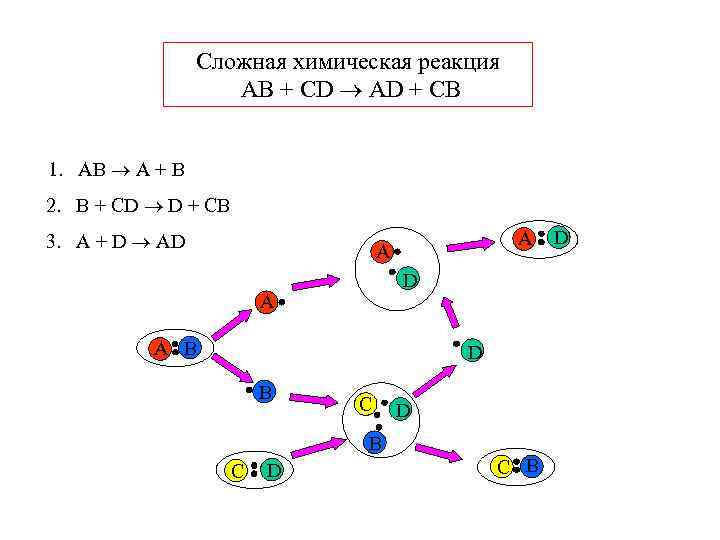 Сложная химическая реакция AB + CD AD + CB 1. AB A + B 2. B + CD D + CB 3. A + D AD A A B D B C D D C B D
Сложная химическая реакция AB + CD AD + CB 1. AB A + B 2. B + CD D + CB 3. A + D AD A A B D B C D D C B D
 Частицы, участвующие в элементарной химической реакции: • Молекулы 2 NO + O 2 2 NO 2 • Ионы H+ + OH- H 2 O • Радикалы H + Cl HCl макромолекулы (~102 – 106 атомов) поверхностные атомы или молекулы
Частицы, участвующие в элементарной химической реакции: • Молекулы 2 NO + O 2 2 NO 2 • Ионы H+ + OH- H 2 O • Радикалы H + Cl HCl макромолекулы (~102 – 106 атомов) поверхностные атомы или молекулы
 Элементарная гомогенная реакция AA + BB DD • реакционное пространство V - объем • Число частиц, участвующих в элементарном химическом акте: A + B молекулярность реакции мономолекулярные бимолекулярные тримолекулярные A + B =1 A + B =2 A + B =3 АВ А + В АВ 2 А + В А 2 В • скорость элементарной химической реакции - число элементарных актов (r), совершающихся в единицу времени (t) в единице реакционного объема:
Элементарная гомогенная реакция AA + BB DD • реакционное пространство V - объем • Число частиц, участвующих в элементарном химическом акте: A + B молекулярность реакции мономолекулярные бимолекулярные тримолекулярные A + B =1 A + B =2 A + B =3 АВ А + В АВ 2 А + В А 2 В • скорость элементарной химической реакции - число элементарных актов (r), совершающихся в единицу времени (t) в единице реакционного объема:
 Скорость элементарной реакции AA + BB DD
Скорость элементарной реакции AA + BB DD
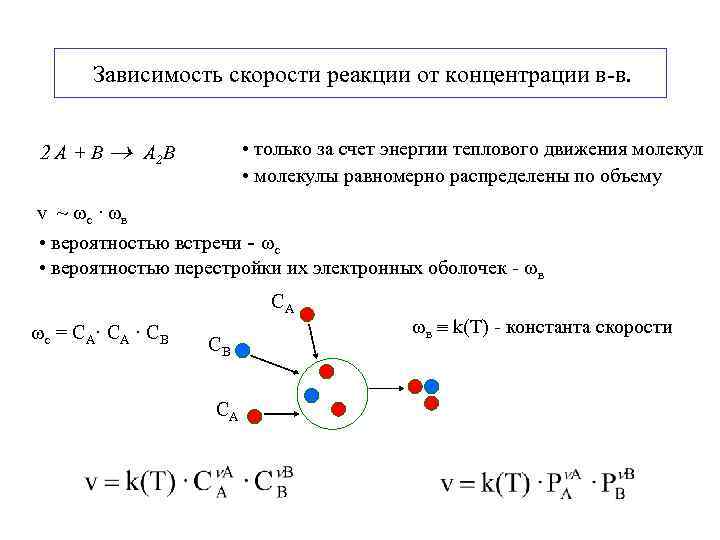 Зависимость скорости реакции от концентрации в-в. 2 А + В А 2 В • только за счет энергии теплового движения молекул • молекулы равномерно распределены по объему v ~ с · в • вероятностью встречи - с • вероятностью перестройки их электронных оболочек - в СА с = СА· СА · СВ СВ СА в k(T) - константа скорости
Зависимость скорости реакции от концентрации в-в. 2 А + В А 2 В • только за счет энергии теплового движения молекул • молекулы равномерно распределены по объему v ~ с · в • вероятностью встречи - с • вероятностью перестройки их электронных оболочек - в СА с = СА· СА · СВ СВ СА в k(T) - константа скорости
 Кинетические уравнения. Кинетическое уравнение необратимой реакции первого порядка A B + D время полупревращения (полураспада)
Кинетические уравнения. Кинетическое уравнение необратимой реакции первого порядка A B + D время полупревращения (полураспада)
 Кинетическое уравнение необратимой реакции второго порядка A + A A 2 A + B AB A + BС AB + С x+y =2
Кинетическое уравнение необратимой реакции второго порядка A + A A 2 A + B AB A + BС AB + С x+y =2
 Методы определения порядка реакции • Метод определения • Графический метод • Метод подбора времени полупревращения кинетического уравнения Порядок реакции 1 2 3 Зависимость концентрации от времени Выражение для константы Выражение для периода скорости полупревращения
Методы определения порядка реакции • Метод определения • Графический метод • Метод подбора времени полупревращения кинетического уравнения Порядок реакции 1 2 3 Зависимость концентрации от времени Выражение для константы Выражение для периода скорости полупревращения
 Зависимость скорости реакции от температуры • Якоб Генрик ВАНТ-ГОФФ (van't Hoff) • При повышении температуры на каждые 10 градусов константа скорости элементарной химической реакции увеличивается в 2 – 4 раза. • Величина, показывающая, во сколько раз увеличивается константа скорости при повышении температуры на 10 градусов, есть температурный коэффициент константы скорости реакции γ.
Зависимость скорости реакции от температуры • Якоб Генрик ВАНТ-ГОФФ (van't Hoff) • При повышении температуры на каждые 10 градусов константа скорости элементарной химической реакции увеличивается в 2 – 4 раза. • Величина, показывающая, во сколько раз увеличивается константа скорости при повышении температуры на 10 градусов, есть температурный коэффициент константы скорости реакции γ.
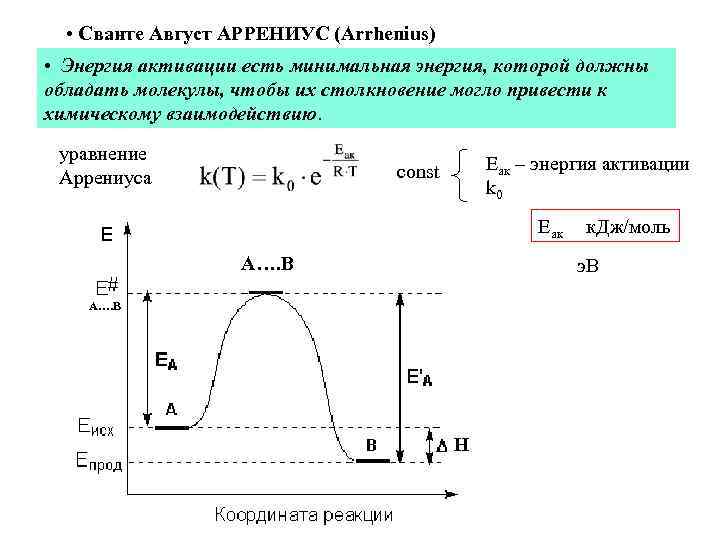 • Сванте Август АРРЕНИУС (Arrhenius) • Энергия активации есть минимальная энергия, которой должны обладать молекулы, чтобы их столкновение могло привести к химическому взаимодействию. уравнение Аррениуса Еак – энергия активации k 0 const Еак к. Дж/моль A…. B э. В A…. B H
• Сванте Август АРРЕНИУС (Arrhenius) • Энергия активации есть минимальная энергия, которой должны обладать молекулы, чтобы их столкновение могло привести к химическому взаимодействию. уравнение Аррениуса Еак – энергия активации k 0 const Еак к. Дж/моль A…. B э. В A…. B H
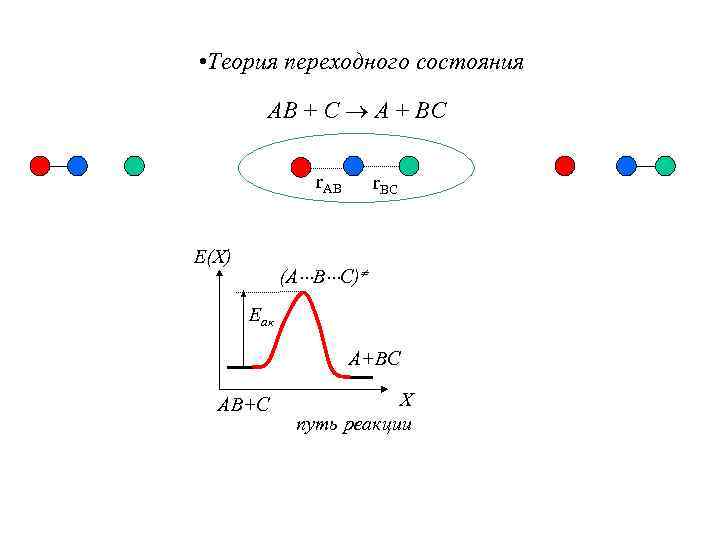 • Теория переходного состояния АВ + С А + ВС r. AB Е(X) r. BC (А В С) Еак А+ВС АВ+С X путь реакции
• Теория переходного состояния АВ + С А + ВС r. AB Е(X) r. BC (А В С) Еак А+ВС АВ+С X путь реакции
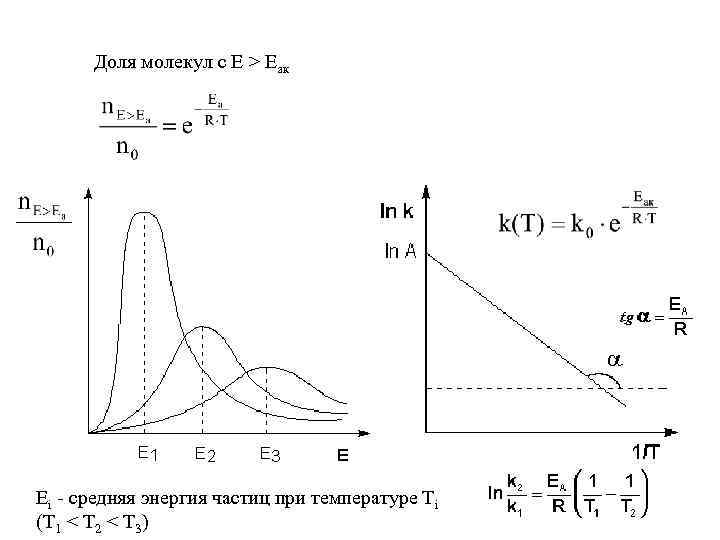 Доля молекул с Е > Еак Ei - средняя энергия частиц при температуре Ti (T 1 < T 2 < T 3)
Доля молекул с Е > Еак Ei - средняя энергия частиц при температуре Ti (T 1 < T 2 < T 3)
 Сложные химические реакции 2 НI + Н 2 О 2 ––> I 2 + 2 Н 2 О 1) НI + Н 2 О 2 ––> НIО + Н 2 О V 1 2) НIО + НI ––> I 2 + Н 2 О V 2 V 1 >> V 2 Лимитирующая стадия
Сложные химические реакции 2 НI + Н 2 О 2 ––> I 2 + 2 Н 2 О 1) НI + Н 2 О 2 ––> НIО + Н 2 О V 1 2) НIО + НI ––> I 2 + Н 2 О V 2 V 1 >> V 2 Лимитирующая стадия
 Сложные химические реакции AA + BB DD скоростью реакции по i–му компоненту Лимитирующая стадия формально простые (x + y ) - порядок реакции уравнение Аррениуса Еак - энергия активации k 0 - предэкспоненциальный множитель
Сложные химические реакции AA + BB DD скоростью реакции по i–му компоненту Лимитирующая стадия формально простые (x + y ) - порядок реакции уравнение Аррениуса Еак - энергия активации k 0 - предэкспоненциальный множитель
 Цепной механизм химической реакции Цепные реакции - ряд регулярно повторяющихся многостадийных элементарных реакций с участием активных частиц (радикалов R ), которые взаимодействуют с молекулами реагентов с образованием продуктов реакции и новых активных частиц. А В • Зарождение цепи А R + R • Развитие цепи А + R R + В • Обрыв цепи R + R А длина цепи - число актов взаимодействия от зарождения до обрыва цепи - неразветвленный цепной процесс-коэфф. размножения n = 1 - разветвленный цепной процесс n 1(число активн. частиц образ. в элемент. акте)
Цепной механизм химической реакции Цепные реакции - ряд регулярно повторяющихся многостадийных элементарных реакций с участием активных частиц (радикалов R ), которые взаимодействуют с молекулами реагентов с образованием продуктов реакции и новых активных частиц. А В • Зарождение цепи А R + R • Развитие цепи А + R R + В • Обрыв цепи R + R А длина цепи - число актов взаимодействия от зарождения до обрыва цепи - неразветвленный цепной процесс-коэфф. размножения n = 1 - разветвленный цепной процесс n 1(число активн. частиц образ. в элемент. акте)
 Примеры 1. Неразветвленный цепной процесс H 2 + Br 2 2 HBr - зарождение цепи Br 2+ h 2 Br H 2+ h 2 H - развитие цепи Br + H 2 HBr + H H + Br 2 HBr + Br - обрыв цепи + + Br + Br 2 H + Br HBr + 2. Разветвленный цепной процесс 2 H 2 + O 2 2 H 2 O - зарождение цепи H 2+ h 2 H O 2+ h 2 O - развитие цепи H + O 2 OH + O O + H 2 OH + H 2 O + H - обрыв цепи H + H H 2 OH + H H 2 O + +
Примеры 1. Неразветвленный цепной процесс H 2 + Br 2 2 HBr - зарождение цепи Br 2+ h 2 Br H 2+ h 2 H - развитие цепи Br + H 2 HBr + H H + Br 2 HBr + Br - обрыв цепи + + Br + Br 2 H + Br HBr + 2. Разветвленный цепной процесс 2 H 2 + O 2 2 H 2 O - зарождение цепи H 2+ h 2 H O 2+ h 2 O - развитие цепи H + O 2 OH + O O + H 2 OH + H 2 O + H - обрыв цепи H + H H 2 OH + H H 2 O + +
 Индуцированные реакции Фотохимические реакции h погл. • Число молекул, подвергшихся первичному фотохимическому превращению, равно числу поглощенных веществом квантов электромагнитного излучения Радиационно–химические реакции ионизирующее излучение частица или квант Е ~50 э. В (~ кэ. В, Мэ. В) электроны, протоны, a-частицы, осколки тяжёлых ядер первичные акты взаимодействия А В+, В–, ē, В–, В • радиолиз - квантовый выход ; 1 вторичные химические реакции 10 -14 – 10 -7 с
Индуцированные реакции Фотохимические реакции h погл. • Число молекул, подвергшихся первичному фотохимическому превращению, равно числу поглощенных веществом квантов электромагнитного излучения Радиационно–химические реакции ионизирующее излучение частица или квант Е ~50 э. В (~ кэ. В, Мэ. В) электроны, протоны, a-частицы, осколки тяжёлых ядер первичные акты взаимодействия А В+, В–, ē, В–, В • радиолиз - квантовый выход ; 1 вторичные химические реакции 10 -14 – 10 -7 с
 B A тв B 0 B Гетерогенные реакции газ • 1. Диффузия реагентов к реакционной зоне, находящейся на поверхности раздела фаз. • 2. Активированная адсорбция частиц реагентов на поверхности. • 3. Химическое превращение адсорбированных частиц. • 4. Десорбция образовавшихся продуктов реакции. • 5. Диффузия продуктов реакции из реакционной зоны. • 1, 5 - Диффузионные стадии (выс. Т) • 3 -4 -Кинетические стадии
B A тв B 0 B Гетерогенные реакции газ • 1. Диффузия реагентов к реакционной зоне, находящейся на поверхности раздела фаз. • 2. Активированная адсорбция частиц реагентов на поверхности. • 3. Химическое превращение адсорбированных частиц. • 4. Десорбция образовавшихся продуктов реакции. • 5. Диффузия продуктов реакции из реакционной зоны. • 1, 5 - Диффузионные стадии (выс. Т) • 3 -4 -Кинетические стадии
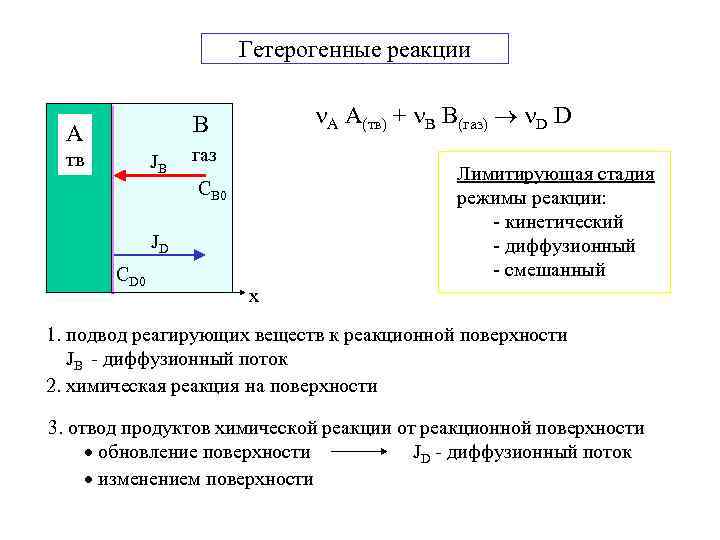 Гетерогенные реакции А A(тв) + В B(газ) D D B A тв JB газ Лимитирующая стадия режимы реакции: - кинетический - диффузионный - смешанный CB 0 JD CD 0 x 1. подвод реагирующих веществ к реакционной поверхности JB - диффузионный поток 2. химическая реакция на поверхности 3. отвод продуктов химической реакции от реакционной поверхности обновление поверхности JD - диффузионный поток изменением поверхности
Гетерогенные реакции А A(тв) + В B(газ) D D B A тв JB газ Лимитирующая стадия режимы реакции: - кинетический - диффузионный - смешанный CB 0 JD CD 0 x 1. подвод реагирующих веществ к реакционной поверхности JB - диффузионный поток 2. химическая реакция на поверхности 3. отвод продуктов химической реакции от реакционной поверхности обновление поверхности JD - диффузионный поток изменением поверхности
 А A(тв) + В B(газ) D D • Кинетический режим • Диффузионный режим(J-дифф. поток) D =f(T) – коэффициент диффузии
А A(тв) + В B(газ) D D • Кинетический режим • Диффузионный режим(J-дифф. поток) D =f(T) – коэффициент диффузии
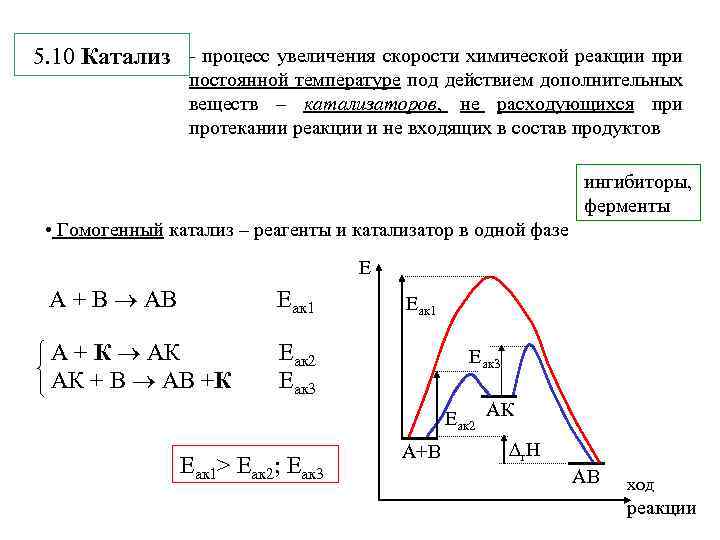 5. 10 Катализ - процесс увеличения скорости химической реакции при постоянной температуре под действием дополнительных веществ – катализаторов, не расходующихся при протекании реакции и не входящих в состав продуктов ингибиторы, ферменты • Гомогенный катализ – реагенты и катализатор в одной фазе Е А + В АВ Еак 1 А + К АК Еак 2 АК + В АВ +К Еак 3 Еак 2 АК Еак 1> Еак 2; Еак 3 А+В r. H АВ ход реакции
5. 10 Катализ - процесс увеличения скорости химической реакции при постоянной температуре под действием дополнительных веществ – катализаторов, не расходующихся при протекании реакции и не входящих в состав продуктов ингибиторы, ферменты • Гомогенный катализ – реагенты и катализатор в одной фазе Е А + В АВ Еак 1 А + К АК Еак 2 АК + В АВ +К Еак 3 Еак 2 АК Еак 1> Еак 2; Еак 3 А+В r. H АВ ход реакции
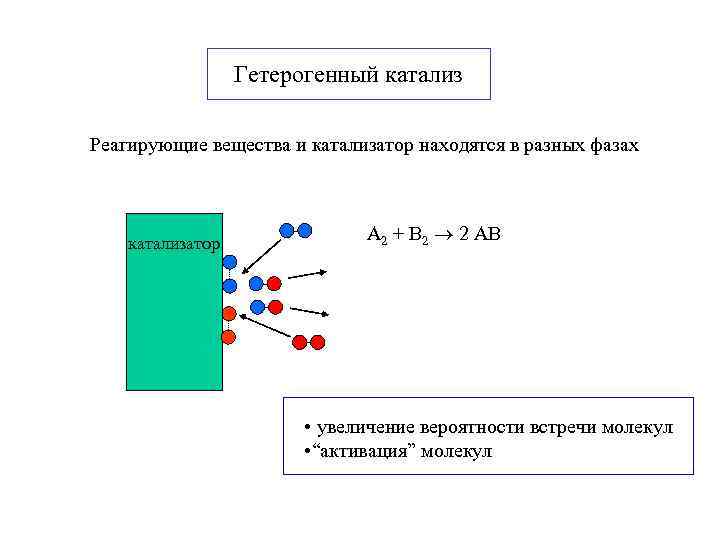 Гетерогенный катализ Реагирующие вещества и катализатор находятся в разных фазах катализатор А 2 + В 2 2 АВ • увеличение вероятности встречи молекул • “активация” молекул
Гетерогенный катализ Реагирующие вещества и катализатор находятся в разных фазах катализатор А 2 + В 2 2 АВ • увеличение вероятности встречи молекул • “активация” молекул
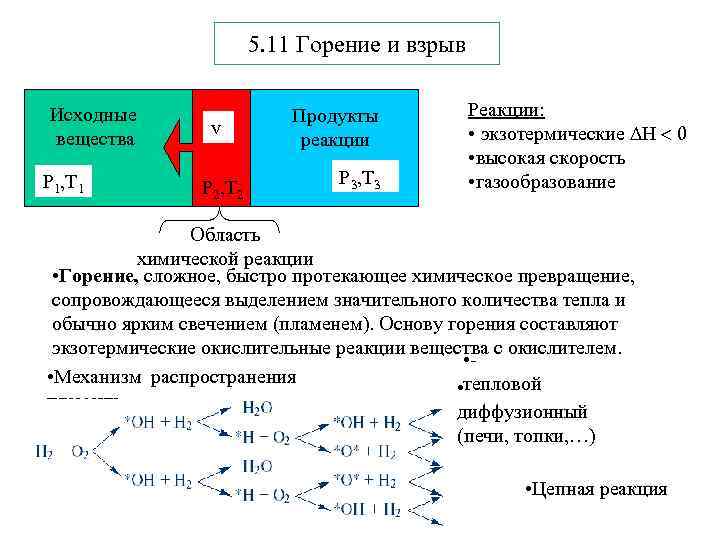 5. 11 Горение и взрыв Исходные вещества Р 1, Т 1 v Р 2, Т 2 Продукты реакции Р 3, Т 3 Реакции: • экзотермические Н 0 • высокая скорость • газообразование Область химической реакции • Горение, сложное, быстро протекающее химическое превращение, сопровождающееся выделением значительного количества тепла и обычно ярким свечением (пламенем). Основу горения составляют экзотермические окислительные реакции вещества с окислителем. • • Механизм распространения • тепловой - пламени диффузионный (печи, топки, …) • Цепная реакция
5. 11 Горение и взрыв Исходные вещества Р 1, Т 1 v Р 2, Т 2 Продукты реакции Р 3, Т 3 Реакции: • экзотермические Н 0 • высокая скорость • газообразование Область химической реакции • Горение, сложное, быстро протекающее химическое превращение, сопровождающееся выделением значительного количества тепла и обычно ярким свечением (пламенем). Основу горения составляют экзотермические окислительные реакции вещества с окислителем. • • Механизм распространения • тепловой - пламени диффузионный (печи, топки, …) • Цепная реакция
 2 способа воспламенения: - самовоспламенение -вынужденное воспламенение, или зажигание (накалённым телом, пламенем, электрической искрой и др. ). • Горение (лин. скорость области хим. реакции) v 10 -3 -102 м с; теплопередача, диффузия • Взрыв v ~ 103 -104 м с; vmax - макс. скорость звука в веществе • Взрыв, процесс освобождения большого количества энергии в ограниченном объёме за короткий промежуток времени. вещество, заполняющее объём, в котором происходит освобождение энергии, превращается в сильно нагретый газ с высоким давлением. Газ воздействует на окружающую среду, вызывая её движение - ударная волна
2 способа воспламенения: - самовоспламенение -вынужденное воспламенение, или зажигание (накалённым телом, пламенем, электрической искрой и др. ). • Горение (лин. скорость области хим. реакции) v 10 -3 -102 м с; теплопередача, диффузия • Взрыв v ~ 103 -104 м с; vmax - макс. скорость звука в веществе • Взрыв, процесс освобождения большого количества энергии в ограниченном объёме за короткий промежуток времени. вещество, заполняющее объём, в котором происходит освобождение энергии, превращается в сильно нагретый газ с высоким давлением. Газ воздействует на окружающую среду, вызывая её движение - ударная волна
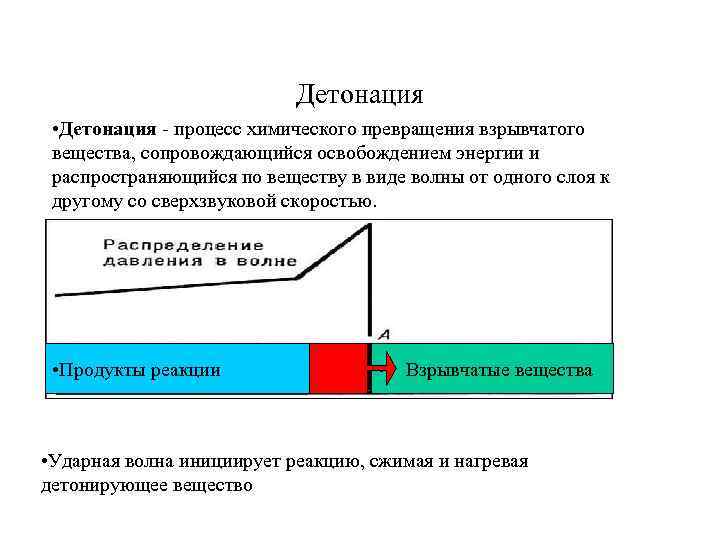 Детонация • Детонация - процесс химического превращения взрывчатого вещества, сопровождающийся освобождением энергии и распространяющийся по веществу в виде волны от одного слоя к другому со сверхзвуковой скоростью. • Продукты реакции • Взрывчатые вещества • Ударная волна инициирует реакцию, сжимая и нагревая детонирующее вещество
Детонация • Детонация - процесс химического превращения взрывчатого вещества, сопровождающийся освобождением энергии и распространяющийся по веществу в виде волны от одного слоя к другому со сверхзвуковой скоростью. • Продукты реакции • Взрывчатые вещества • Ударная волна инициирует реакцию, сжимая и нагревая детонирующее вещество


