Лекция 3 (биофак и физфак) 21 февраля 2015.ppt
- Количество слайдов: 93

Хемотаксис и Воспаление Лекция 3
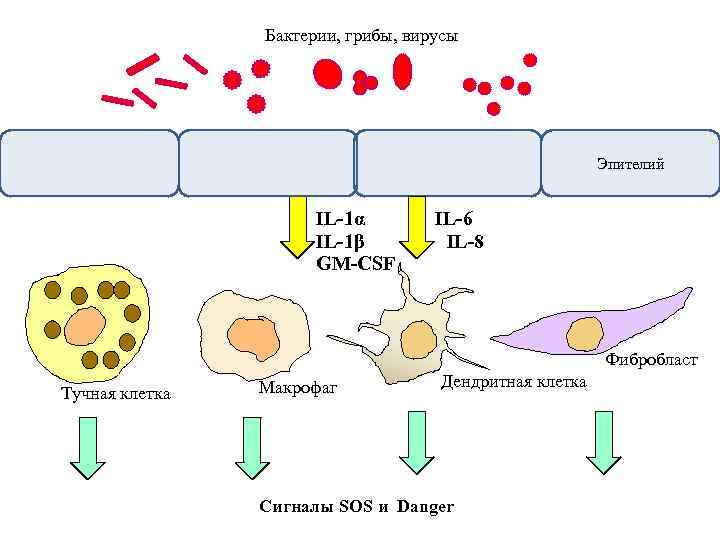
Бактерии, грибы, вирусы Эпителий IL-1α IL-1β GM-CSF IL-6 IL-8 Фибробласт Тучная клетка Макрофаг Дендритная клетка Сигналы SOS и Danger
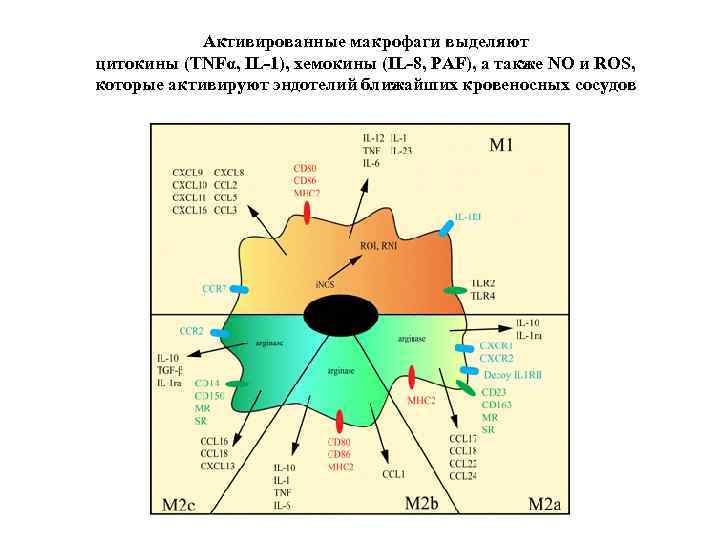
Активированные макрофаги выделяют цитокины (TNFα, IL-1), хемокины (IL-8, PAF), а также NO и ROS, которые активируют эндотелий ближайших кровеносных сосудов
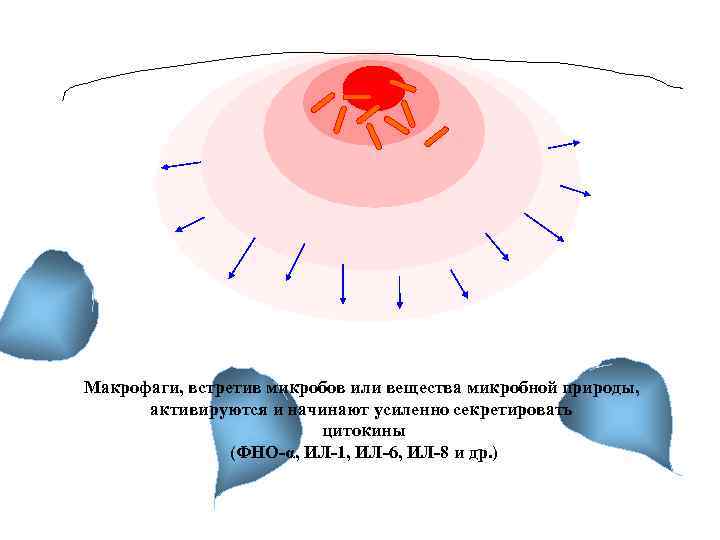
Макрофаги, встретив микробов или вещества микробной природы, активируются и начинают усиленно секретировать цитокины (ФНО-α, ИЛ-1, ИЛ-6, ИЛ-8 и др. )
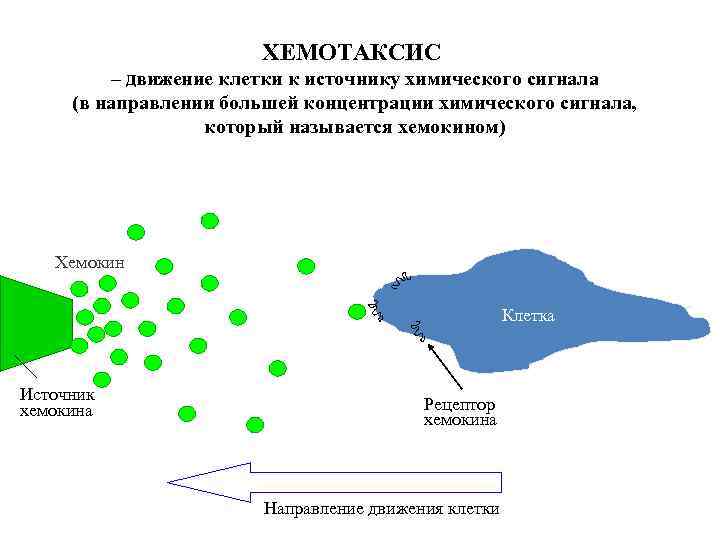
ХЕМОТАКСИС – движение клетки к источнику химического сигнала (в направлении большей концентрации химического сигнала, который называется хемокином) Хемокин Клетка Источник хемокина Рецептор хемокина Направление движения клетки
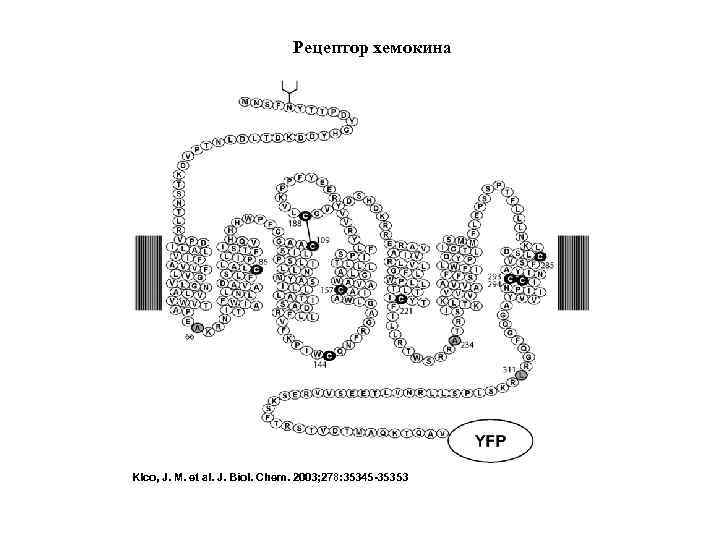
Рецептор хемокина Klco, J. M. et al. J. Biol. Chem. 2003; 278: 35345 -35353
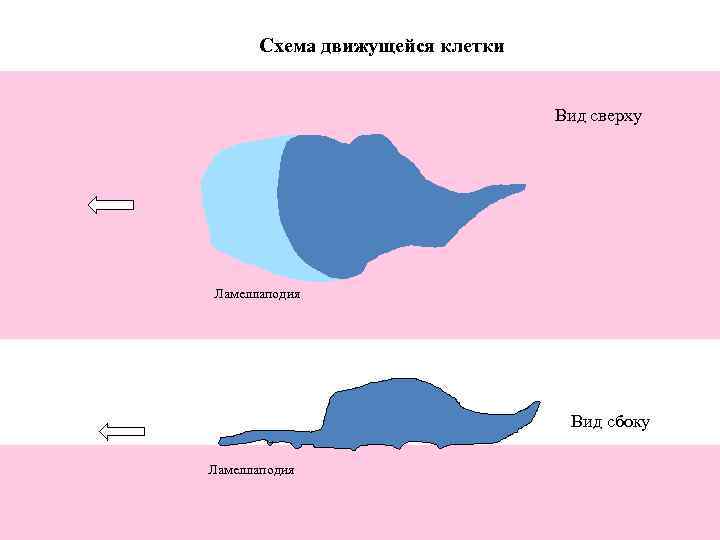
Схема движущейся клетки Вид сверху Ламеллаподия Вид сбоку Ламеллаподия
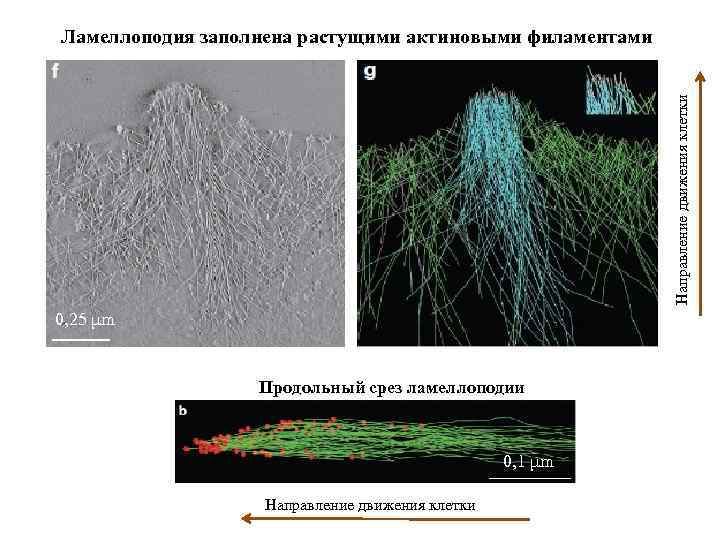
Направление движения клетки Ламеллоподия заполнена растущими актиновыми филаментами 0, 25 μm Центральный пучок Продольный срез ламеллоподии 0, 1 μm Направление движения клетки
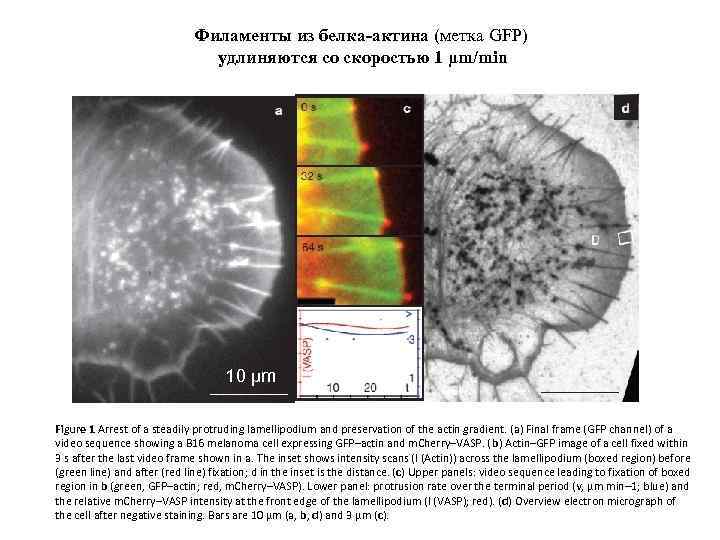
Филаменты из белка-актина (метка GFP) удлиняются со скоростью 1 μm/min 10 μm Figure 1 Arrest of a steadily protruding lamellipodium and preservation of the actin gradient. (a) Final frame (GFP channel) of a video sequence showing a B 16 melanoma cell expressing GFP–actin and m. Cherry–VASP. (b) Actin–GFP image of a cell fixed within 3 s after the last video frame shown in a. The inset shows intensity scans (I (Actin)) across the lamellipodium (boxed region) before (green line) and after (red line) fixation; d in the inset is the distance. (c) Upper panels: video sequence leading to fixation of boxed region in b (green, GFP–actin; red, m. Cherry–VASP). Lower panel: protrusion rate over the terminal period (v, μm min– 1; blue) and the relative m. Cherry–VASP intensity at the front edge of the lamellipodium (I (VASP); red). (d) Overview electron micrograph of the cell after negative staining. Bars are 10 μm (a, b, d) and 3 μm (c).

Как актиновые филаменты вытягиваются внутри ламеллоподии на переднем фронте движущейся клетки Figure 6 Hypothetical scheme of actin network generation in lamellipodia. In response to signalling events (including those downstream of Rac), nucleation-promoting factors (the WAVE complex), longation complexes (Ena/VASP proteins) and nucleator/elongators (formins) are recruited to the membrane. We suggest that WAVE, VASP and formins associate in different combinations in multimolecular complexes to regulate the balance between network and bundle formation. Possible schemes are indicated. (a) Single actin filaments are nucleated by the docking of the Arp 2/3 complex onto the WAVE complex. (b) Filaments elongate, initially tethered via the WAVE WH 2 domain, with the Arp 2/3 complex on the filament minus end. (c) VASP molecules associated with the WAVE complex take over the role of filament elongation (as oligomers) through common binding partners, releasing WAVE for further nucleation events. (d) Some growing actin plus ends tethered by VASP oligomers and associated proteins come together by lateral flow in the membrane and (e) initiate the formation of a filament pair through recruitment of an actin-bundling protein (X-linker). (f) Filament pairs could also be nucleated and elongated directly by formins (a doublet making up one ring) in combination with a bundling protein. Finally, long cross-linking proteins (such as filamin and α ‑actinin) stabilize the network by forming filament interconnections (not shown). For clarity, the filament density in the scheme is lower than in the real cell. NATURE CELL BIOLOGY, Vol 12 | NUMBER 5 | MAY 2010

Что важно для движения клетки: • Вытягивать филоподии • Закрепиться вытянутой филоподией за субстрат • Из нескольких соседних филоподий образовать ламеллоподию • Подтянуть тело клетки

Movies

В ответ на инфекцию дендритные клетки накапливаются в поверхностном слое эпителия Обозначения: Epithelium – это самый поверхностный слой эпителиальных клеток LP (lamina propria ) ткань под эпителием, внутренняя ткань ворсинки, где обитает большое количество макрофагов и дендритных клеток
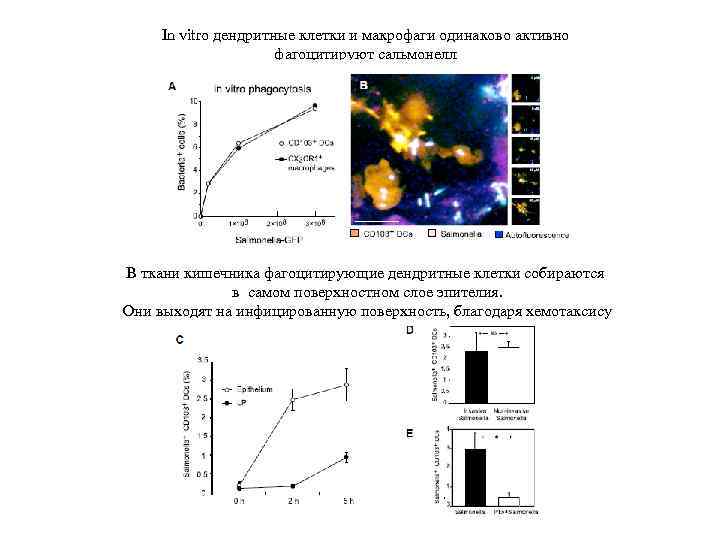
In vitro дендритные клетки и макрофаги одинаково активно фагоцитируют сальмонелл В ткани кишечника фагоцитирующие дендритные клетки собираются в самом поверхностном слое эпителия. Они выходят на инфицированную поверхность, благодаря хемотаксису

Хемотаксис позволяет призвать сотни макрофагов и дендритных клеток из участков ткани, ближайших к месту вторжения инфекции. При микроскопии кишечной ворсинки видно, что в каждой ворсинке содержатся десятки макрофагов и дендритных клеток. Но иногда и такого количества защитников недостаточно. Что делать, кого еще можно звать на помощь? Есть огромный резерв защитников. Он циркулирует в крови. Нужно только умело позвать, и эти защитники придут и помогут.
• Из очага инфекции происходит диффузия веществ, влияющих на ближайшие кровеносные сосуды • В результате изменения сосудов из крови в пораженную ткань выходят защитные молекулы и клетки.
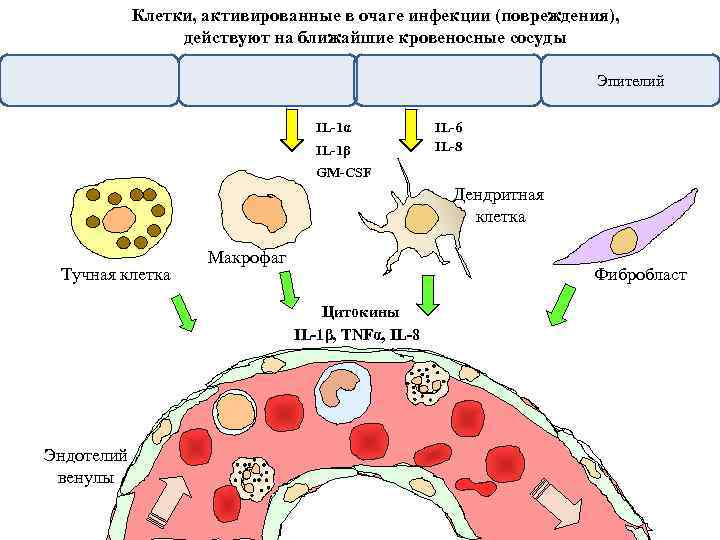
Клетки, активированные в очаге инфекции (повреждения), действуют на ближайшие кровеносные сосуды Эпителий IL-1α IL-1β IL-6 IL-8 GM-CSF Дендритная клетка Тучная клетка Макрофаг Фибробласт Цитокины IL-1β, TNFα, IL-8 Эндотелий венулы
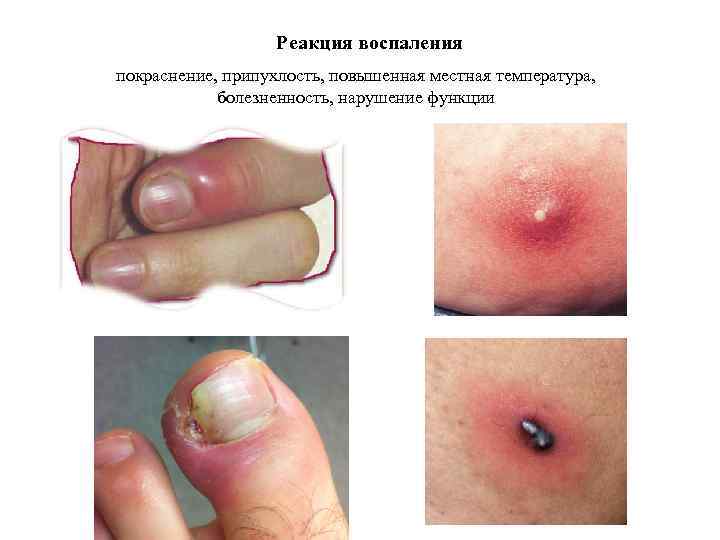
Реакция воспаления покраснение, припухлость, повышенная местная температура, болезненность, нарушение функции

Воспаление – это защитная реакция, которая развивается, когда местная (пограничная) защита не справилась с инфекцией или повреждением. При воспалении защиту осуществляет весь организм.
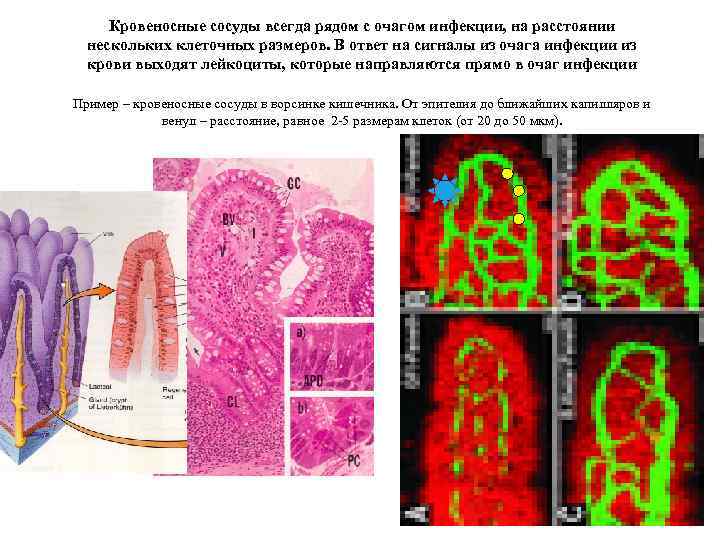
Кровеносные сосуды всегда рядом с очагом инфекции, на расстоянии нескольких клеточных размеров. В ответ на сигналы из очага инфекции из крови выходят лейкоциты, которые направляются прямо в очаг инфекции Пример – кровеносные сосуды в ворсинке кишечника. От эпителия до ближайших капилляров и венул – расстояние, равное 2 -5 размерам клеток (от 20 до 50 мкм).
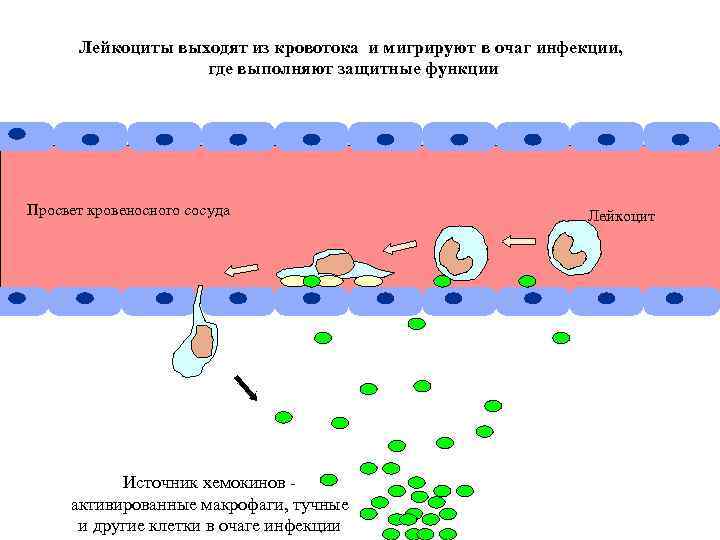
Лейкоциты выходят из кровотока и мигрируют в очаг инфекции, где выполняют защитные функции Просвет кровеносного сосуда Источник хемокинов активированные макрофаги, тучные и другие клетки в очаге инфекции Лейкоцит
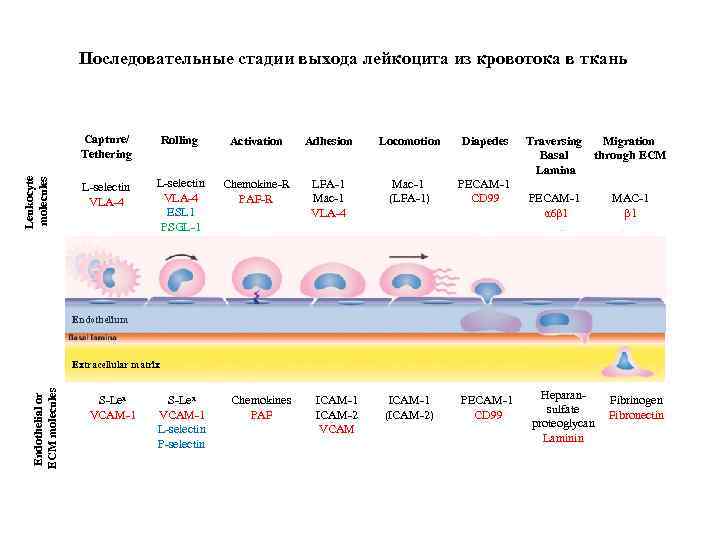
Последовательные стадии выхода лейкоцита из кровотока в ткань Leukocyte molecules Capture/ Tethering Rolling Activation Adhesion Locomotion Diapedes L-selectin VLA-4 ESL 1 PSGL-1 Chemokine-R PAF-R LFA-1 Mac-1 VLA-4 Mac-1 (LFA-1) PECAM-1 CD 99 ICAM-1 (ICAM-2) PECAM-1 CD 99 Traversing Migration Basal through ECM Lamina PECAM-1 α 6β 1 MAC-1 β 1 Heparansulfate proteoglycan Laminin Fibrinogen Fibronectin Endothelium Endothelial or ECM molecules Extracellular matrix S-Lex VCAM-1 L-selectin P-selectin Chemokines PAF ICAM-1 ICAM-2 VCAM

Всеми стадиями выхода лейкоцитов из кровотока управляют цитокины, молекулы межклеточной адгезии, молекулы внеклеточного матрикса
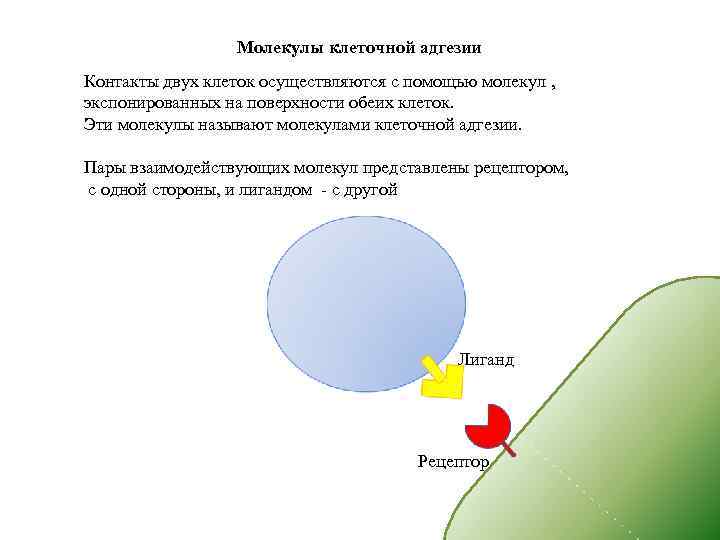
Молекулы клеточной адгезии Контакты двух клеток осуществляются с помощью молекул , экспонированных на поверхности обеих клеток. Эти молекулы называют молекулами клеточной адгезии. Пары взаимодействующих молекул представлены рецептором, с одной стороны, и лигандом - с другой Лиганд Рецептор
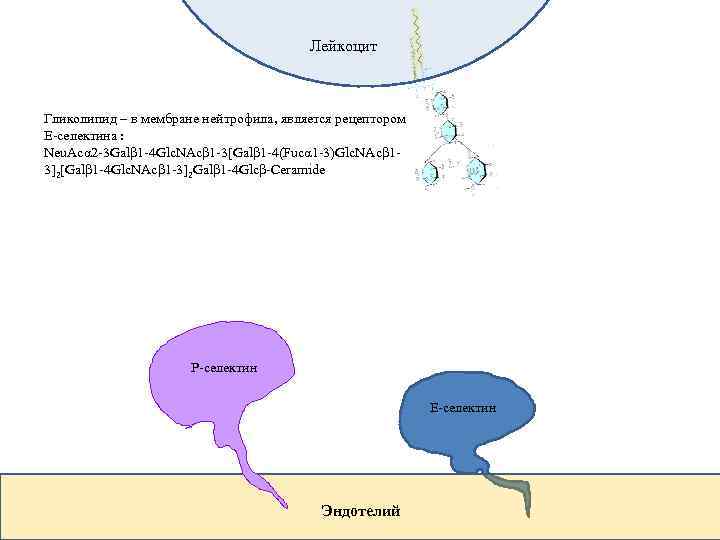
Лейкоцит Гликолипид – в мембране нейтрофила, является рецептором Е-селектина : Neu. Acα 2 -3 Galβ 1 -4 Glc. NAcβ 1 -3[Galβ 1 -4(Fucα 1 -3)Glc. NAcβ 13]2[Galβ 1 -4 Glc. NAcβ 1 -3]2 Galβ 1 -4 Glcβ-Ceramide P-селектин Е-селектин Эндотелий

СЕЛЕКТИНЫ белки клеточной мембраны, предназначены для образования контактов с другими клетками, имеют сродство к определенным олигосахаридным структурам Лектиновый домен Домен ФРЭ Домен CCP
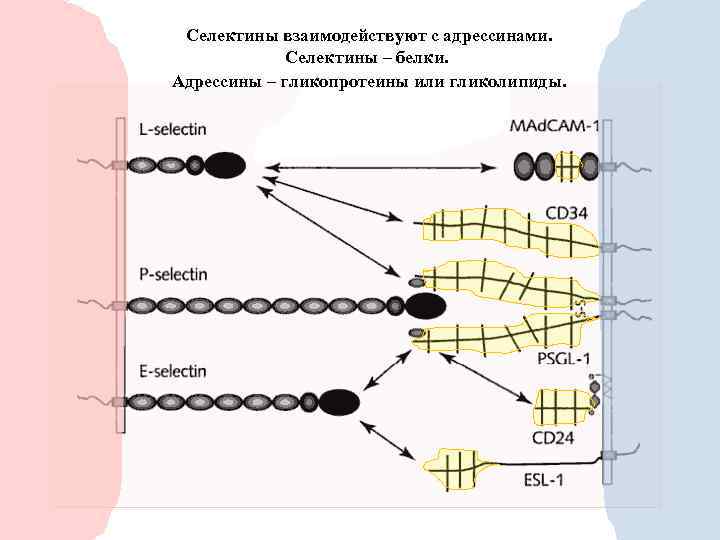
Селектины взаимодействуют с адрессинами. Селектины – белки. Адрессины – гликопротеины или гликолипиды.
Молекулы адгезии обильно представлены на поверхности эндотелия
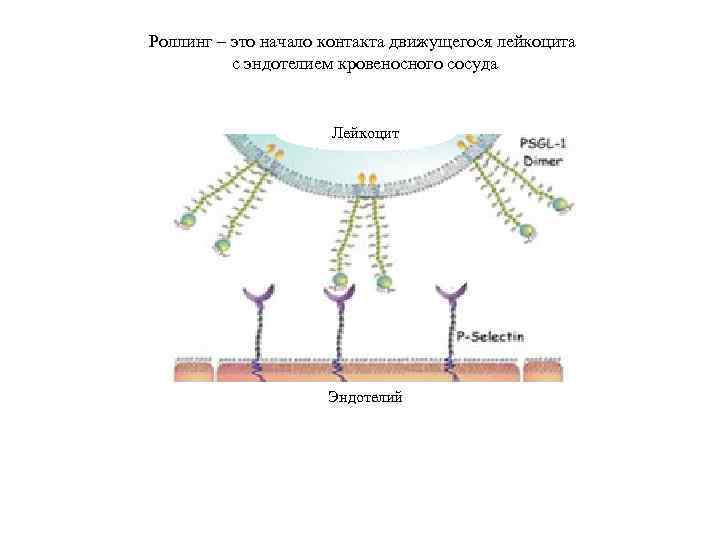
Роллинг – это начало контакта движущегося лейкоцита с эндотелием кровеносного сосуда Лейкоцит Эндотелий
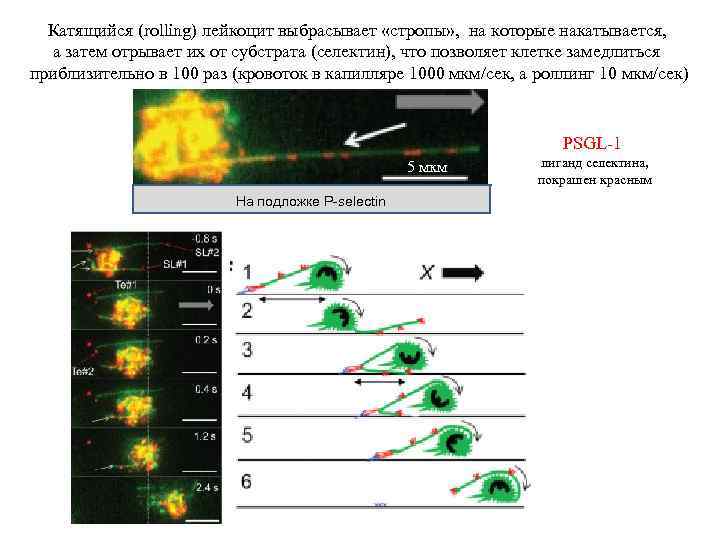
Катящийся (rolling) лейкоцит выбрасывает «стропы» , на которые накатывается, а затем отрывает их от субстрата (селектин), что позволяет клетке замедлиться приблизительно в 100 раз (кровоток в капилляре 1000 мкм/сек, а роллинг 10 мкм/сек) PSGL-1 5 мкм На подложке P-selectin лиганд селектина, покрашен красным

Адгезия лейкоцита на эндотелии, распластывание и движение по поверхности эндотелиальной клетки определяются взаимодействием другой пары молекул – интегрина и лиганда интегрина (CAM, от cell adhesion molecules)
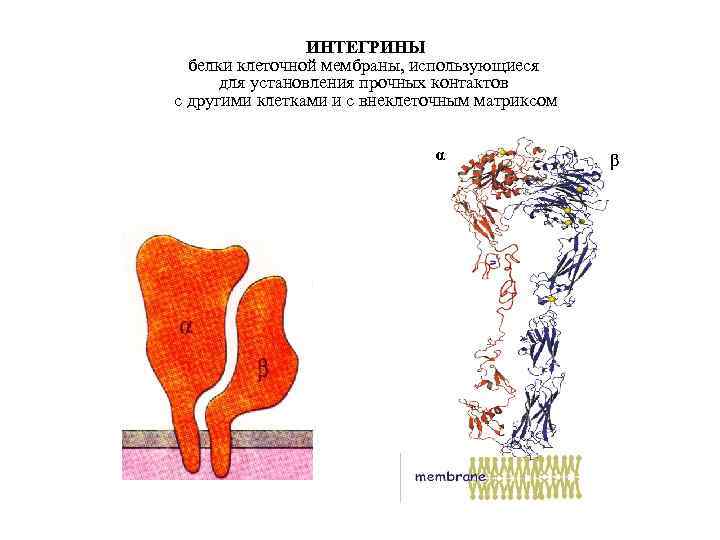
ИНТЕГРИНЫ белки клеточной мембраны, использующиеся для установления прочных контактов с другими клетками и с внеклеточным матриксом α β
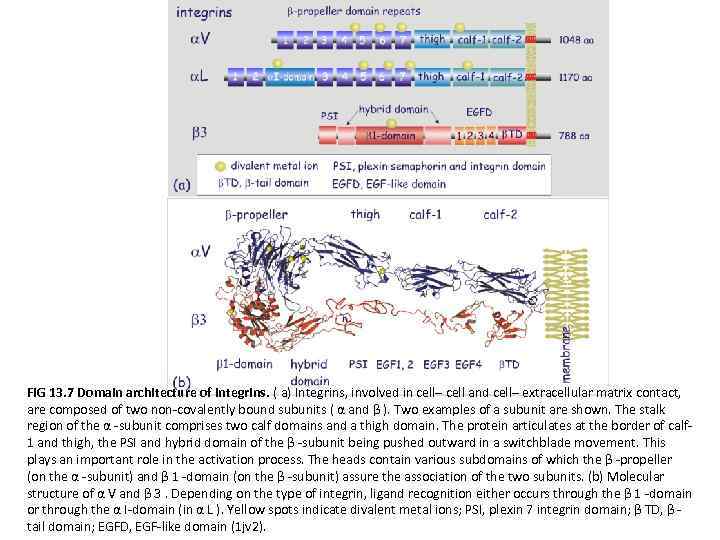
FIG 13. 7 Domain architecture of integrins. ( a) Integrins, involved in cell– cell and cell– extracellular matrix contact, are composed of two non-covalently bound subunits ( α and β ). Two examples of a subunit are shown. The stalk region of the α -subunit comprises two calf domains and a thigh domain. The protein articulates at the border of calf 1 and thigh, the PSI and hybrid domain of the β -subunit being pushed outward in a switchblade movement. This plays an important role in the activation process. The heads contain various subdomains of which the β -propeller (on the α -subunit) and β 1 -domain (on the β -subunit) assure the association of the two subunits. (b) Molecular structure of α V and β 3. Depending on the type of integrin, ligand recognition either occurs through the β 1 -domain or through the α I-domain (in α L ). Yellow spots indicate divalent metal ions; PSI, plexin 7 integrin domain; β TD, β tail domain; EGFD, EGF-like domain (1 jv 2).
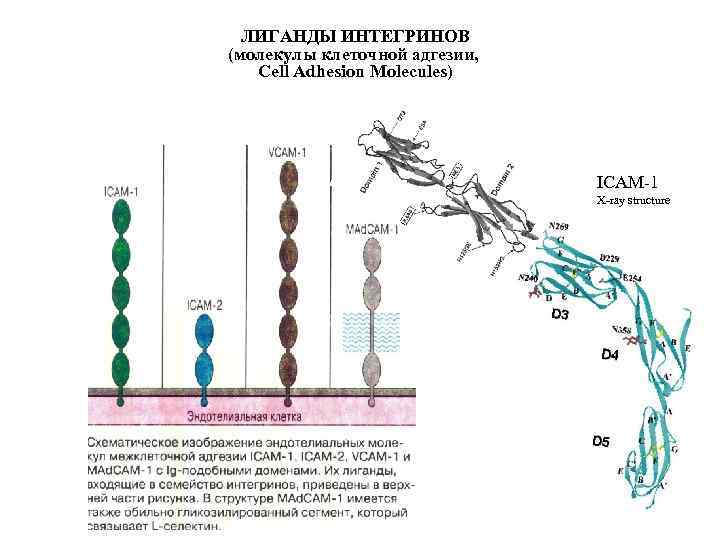
ЛИГАНДЫ ИНТЕГРИНОВ (молекулы клеточной адгезии, Cell Adhesion Molecules) ICAM-1 X-ray structure
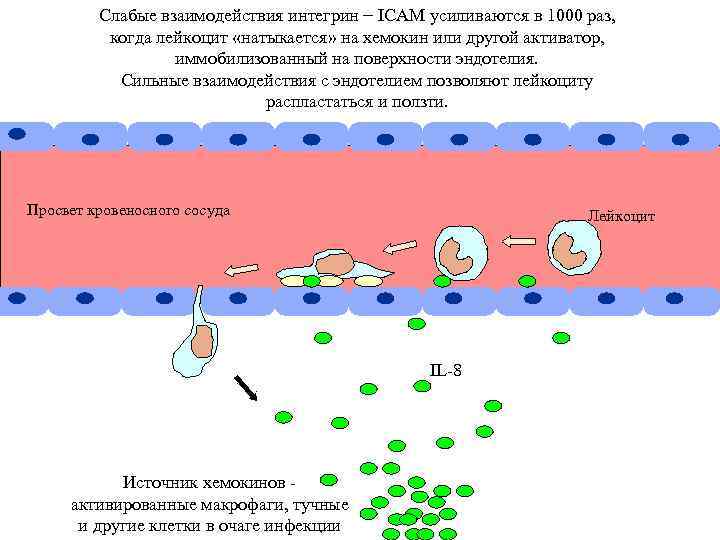
Слабые взаимодействия интегрин − ICAM усиливаются в 1000 раз, когда лейкоцит «натыкается» на хемокин или другой активатор, иммобилизованный на поверхности эндотелия. Сильные взаимодействия с эндотелием позволяют лейкоциту распластаться и ползти. Просвет кровеносного сосуда Лейкоцит IL-8 Источник хемокинов активированные макрофаги, тучные и другие клетки в очаге инфекции
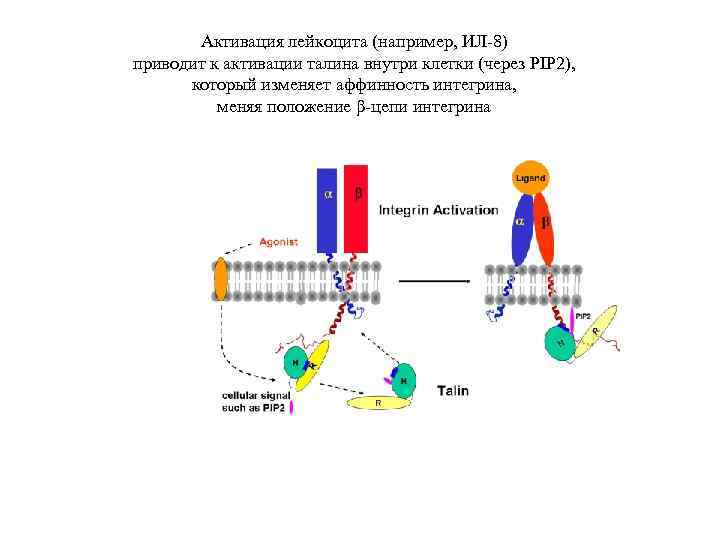
Активация лейкоцита (например, ИЛ-8) приводит к активации талина внутри клетки (через PIP 2), который изменяет аффинность интегрина, меняя положение β-цепи интегрина
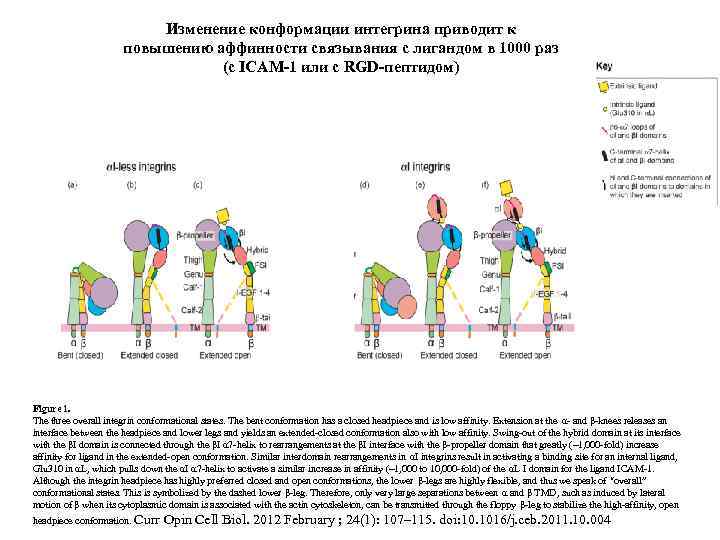
Изменение конформации интегрина приводит к повышению аффинности связывания с лигандом в 1000 раз (с ICAM-1 или с RGD-пептидом) Figure 1. The three overall integrin conformational states. The bent conformation has a closed headpiece and is low affinity. Extension at the α- and β-knees releases an interface between the headpiece and lower legs and yields an extended-closed conformation also with low affinity. Swing-out of the hybrid domain at its interface with the βI domain is connected through the βI α 7 -helix to rearrangements at the βI interface with the β-propeller domain that greatly (~1, 000 -fold) increase affinity for ligand in the extended-open conformation. Similar interdomain rearrangements in αI integrins result in activating a binding site for an internal ligand, Glu 310 in αL, which pulls down the αI α 7 -helix to activate a similar increase in affinity (~1, 000 to 10, 000 -fold) of the αL I domain for the ligand ICAM-1. Although the integrin headpiece has highly preferred closed and open conformations, the lower β-legs are highly flexible, and thus we speak of “overall” conformational states. This is symbolized by the dashed lower β-leg. Therefore, only very large separations between α and β TMD, such as induced by lateral motion of β when its cytoplasmic domain is associated with the actin cytoskeleton, can be transmitted through the floppy β-leg to stabilize the high-affinity, open headpiece conformation. Curr Opin Cell Biol. 2012 February ; 24(1): 107– 115. doi: 10. 1016/j. ceb. 2011. 10. 004
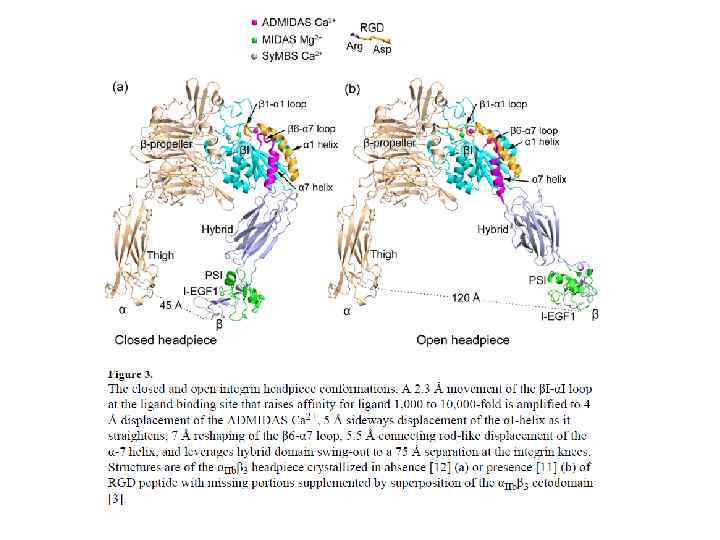

Интегрин представляет собой редкий случай, когда мембранная молекула сигналит в двух направлениях Изнутри – наружу (Inside – out) Внутри клетки сигнал с G-белка меняет таллин и актиновые филаменты, что раздвигает ножки интегрина, повышая аффинность внеклеточной части в 1000 раз Снаружи – внутрь (Outside – in) Высокоаффинное связывание с лигандом вызывает кластеризацию интегрина, что формирует сигнал внутри клетки. Лейкоцит не просто распластывается. Он сильно активируется ( «взрыв» продукции ROS и других противоинфекционных веществ).
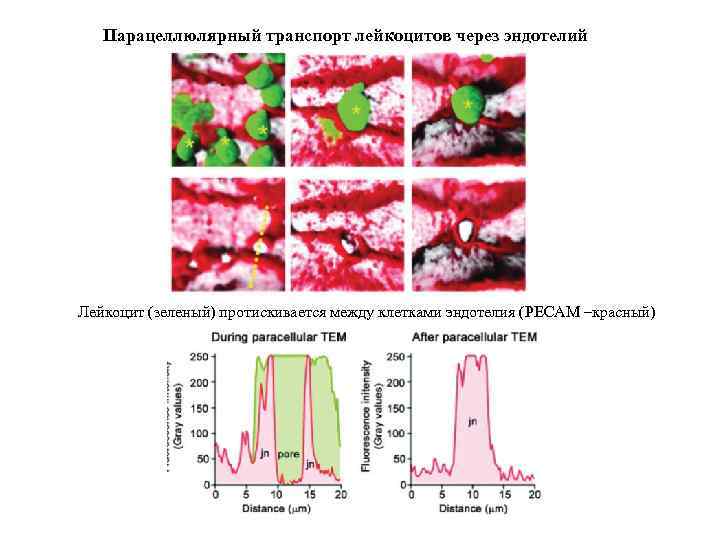
Парацеллюлярный транспорт лейкоцитов через эндотелий Лейкоцит (зеленый) протискивается между клетками эндотелия (PECAM –красный)
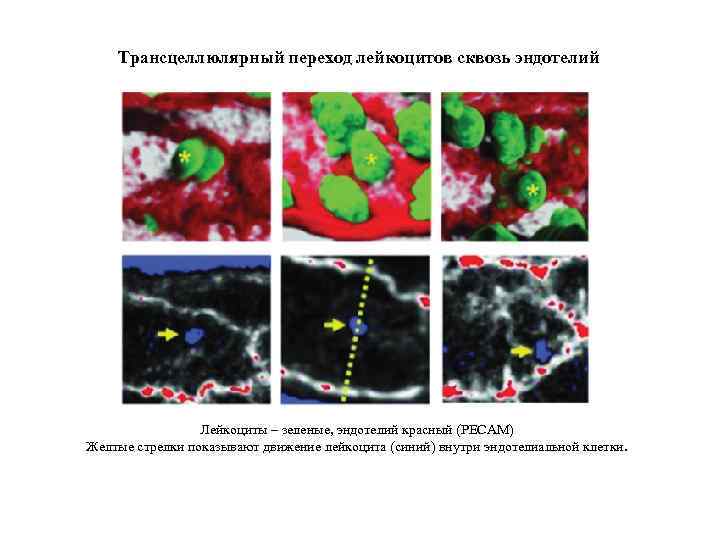
Трансцеллюлярный переход лейкоцитов сквозь эндотелий Лейкоциты – зеленые, эндотелий красный (PECAM) Желтые стрелки показывают движение лейкоцита (синий) внутри эндотелиальной клетки.
Во время прохождения между эндотелиальными клетками лейкоцит устанавливает контактные взаимодействия, используя молекулы CD 31, CD 99 и JAM, имитируя контакты между самими эндотелиальными клетками
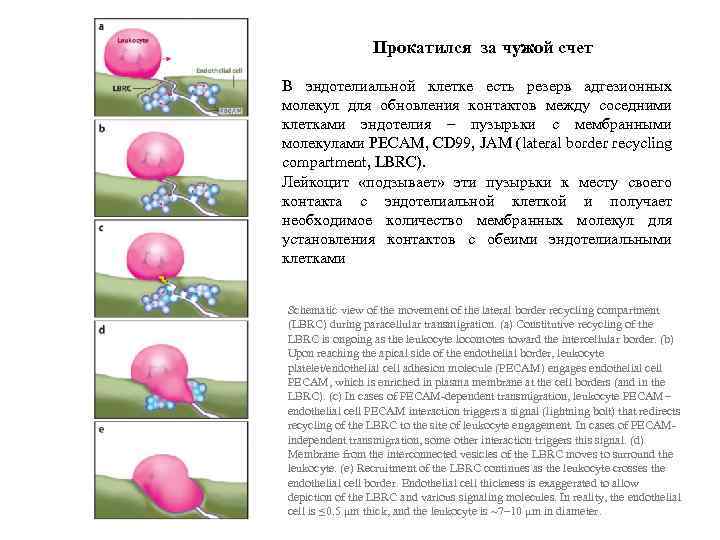
Прокатился за чужой счет В эндотелиальной клетке есть резерв адгезионных молекул для обновления контактов между соседними клетками эндотелия – пузырьки с мембранными молекулами PECAM, CD 99, JAM (lateral border recycling compartment, LBRC). Лейкоцит «подзывает» эти пузырьки к месту своего контакта с эндотелиальной клеткой и получает необходимое количество мембранных молекул для установления контактов с обеими эндотелиальными клетками Schematic view of the movement of the lateral border recycling compartment (LBRC) during paracellular transmigration. (a) Constitutive recycling of the LBRC is ongoing as the leukocyte locomotes toward the intercellular border. (b) Upon reaching the apical side of the endothelial border, leukocyte platelet/endothelial cell adhesion molecule (PECAM) engages endothelial cell PECAM, which is enriched in plasma membrane at the cell borders (and in the LBRC). (c) In cases of PECAM-dependent transmigration, leukocyte PECAM– endothelial cell PECAM interaction triggers a signal (lightning bolt) that redirects recycling of the LBRC to the site of leukocyte engagement. In cases of PECAMindependent transmigration, some other interaction triggers this signal. (d) Membrane from the interconnected vesicles of the LBRC moves to surround the leukocyte. (e) Recruitment of the LBRC continues as the leukocyte crosses the endothelial cell border. Endothelial cell thickness is exaggerated to allow depiction of the LBRC and various signaling molecules. In reality, the endothelial cell is ≤ 0. 5 μm thick, and the leukocyte is ~7– 10 μm in diameter.
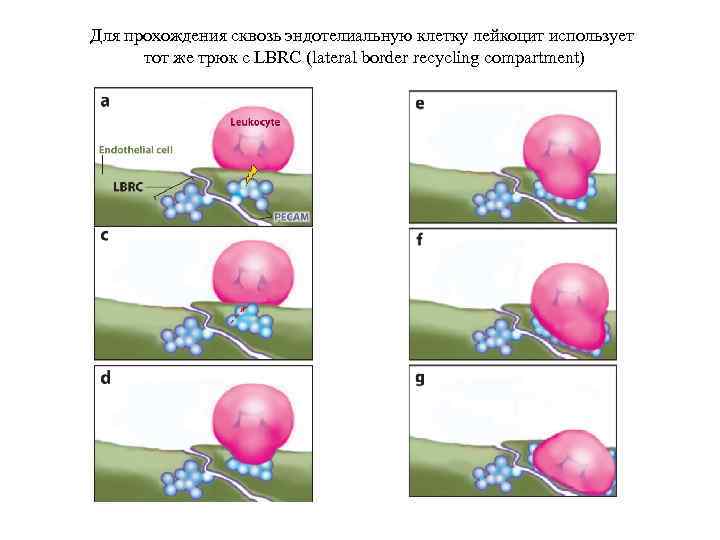
Для прохождения сквозь эндотелиальную клетку лейкоцит использует тот же трюк с LBRC (lateral border recycling compartment)

Кроме прохождения слоя эндотелиальных клеток, лейкоцит должен пройти сквозь базальную мембрану и слой перицитов
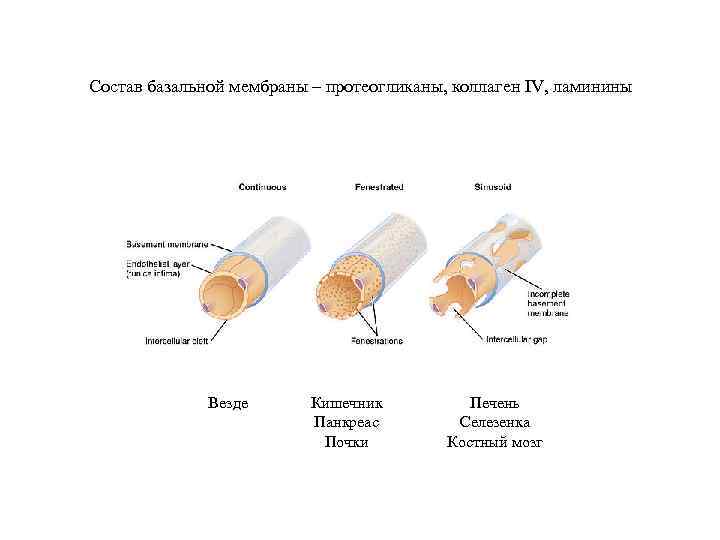
Состав базальной мембраны – протеогликаны, коллаген IV, ламинины Везде Кишечник Панкреас Почки Печень Селезенка Костный мозг

В стенке венулы базальная мембрана имеет небольшие дефекты (matrix proteins low expression levels). Под влиянием IL-1β дефекты увеличиваются. Именно в эти микроскопические щели и выползают нейтрофилы. Средний размер щели 8 -10 кв. мкм (4 x 2 мкм) После IL-1β щели увеличиваются Средний размер щели 14 -18 кв. мкм (5 x 3 мкм)
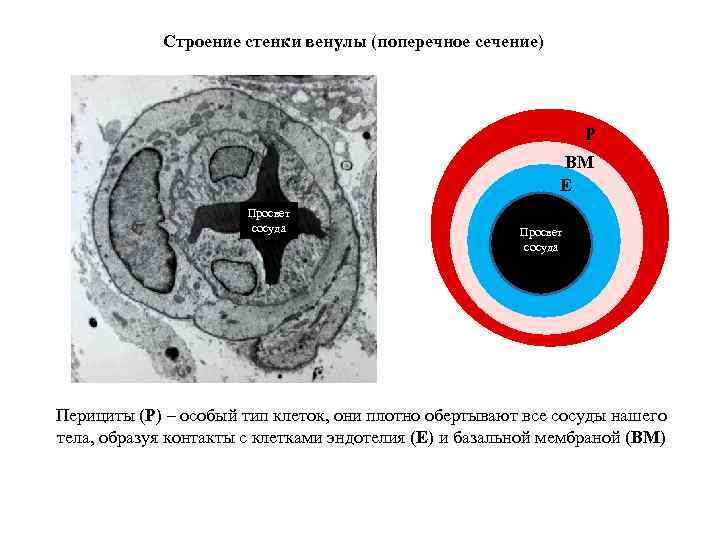
Строение стенки венулы (поперечное сечение) P BM E Просвет сосуда Перициты (P) – особый тип клеток, они плотно обертывают все сосуды нашего тела, образуя контакты с клетками эндотелия (E) и базальной мембраной (BM)
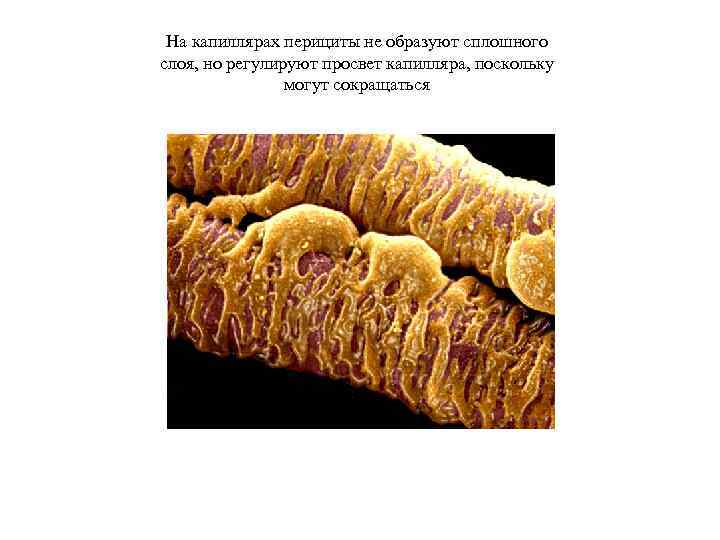
На капиллярах перициты не образуют сплошного слоя, но регулируют просвет капилляра, поскольку могут сокращаться
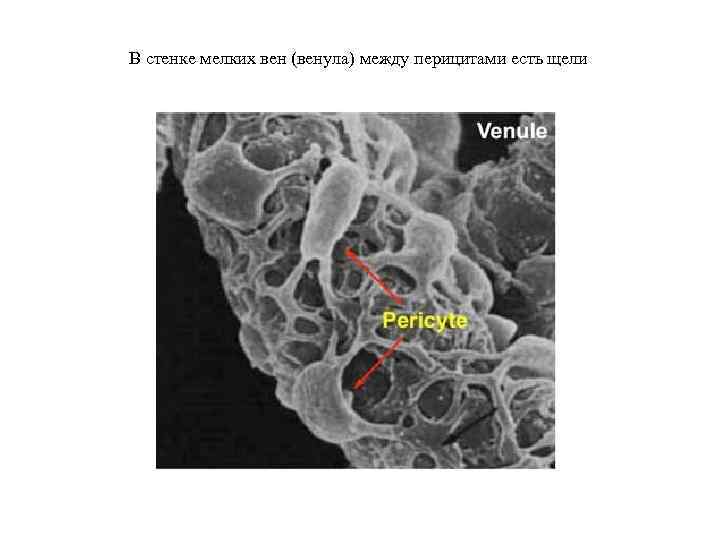
В стенке мелких вен (венула) между перицитами есть щели
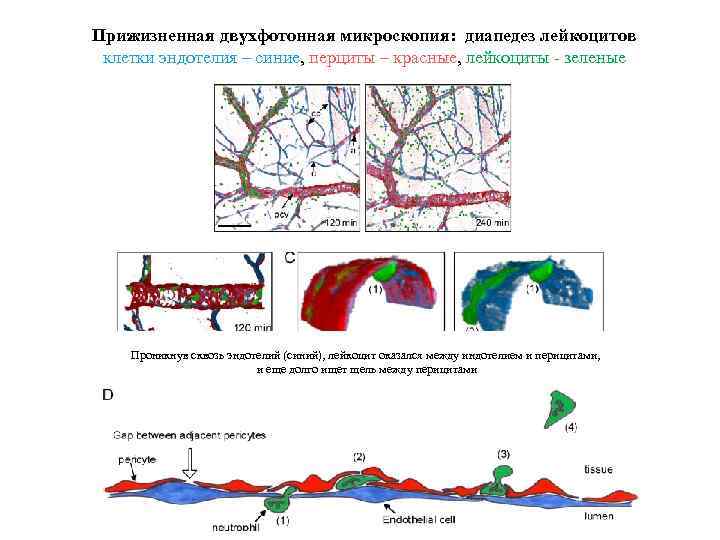
Прижизненная двухфотонная микроскопия: диапедез лейкоцитов клетки эндотелия – синие, перциты – красные, лейкоциты - зеленые Проникнув сквозь эндотелий (синий), лейкоцит оказался между индотелием и перицитами, и еще долго ищет щель между перицитами
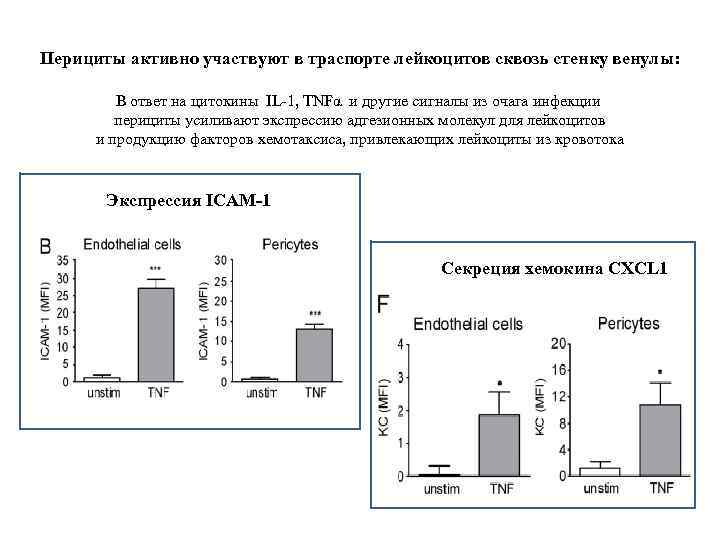
Перициты активно участвуют в траспорте лейкоцитов сквозь стенку венулы: В ответ на цитокины IL-1, TNFα и другие сигналы из очага инфекции перициты усиливают экспрессию адгезионных молекул для лейкоцитов и продукцию факторов хемотаксиса, привлекающих лейкоциты из кровотока Экспрессия ICAM-1 Секреция хемокина CXCL 1
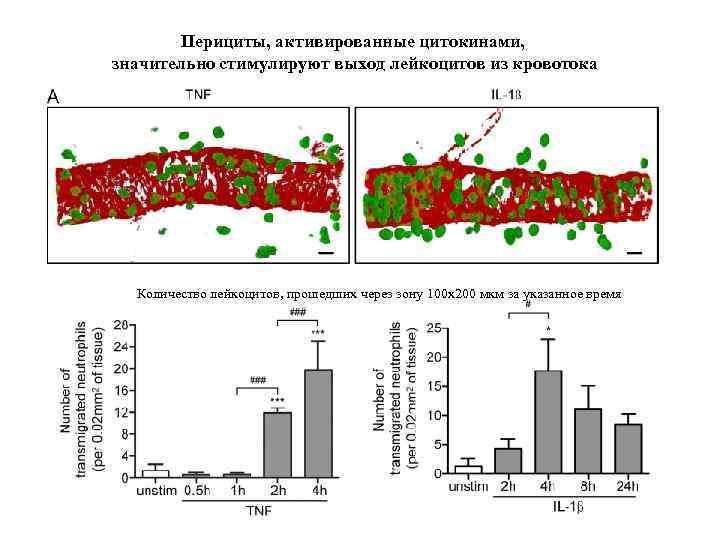
Перициты, активированные цитокинами, значительно стимулируют выход лейкоцитов из кровотока Количество лейкоцитов, прошедших через зону 100 x 200 мкм за указанное время

Свершилось чудо: из целого сосуда вышли защитные клетки – лейкоциты. Ни эритроциты, ни даже тромбоциты вместе с ними не вышли. Следовательно, целостность стенки сосуда действительно была сохранена. Лейкоциты вышли точно в том месте, где они нужны для защиты. Больше нигде в организме этого не произошло. Очень полезное событие и очень точное по локализации. Мало того, в первый день вышли одни защитники, во второй – другие, в третий – третьи. Это еще одно удивительное чудо.
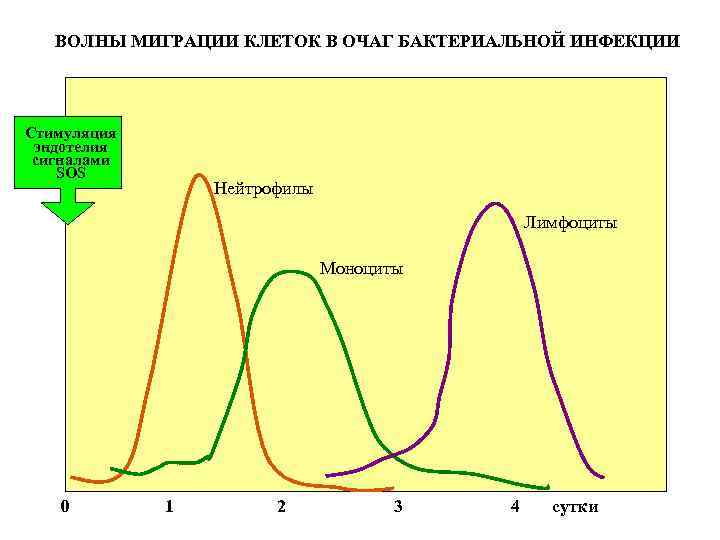
ВОЛНЫ МИГРАЦИИ КЛЕТОК В ОЧАГ БАКТЕРИАЛЬНОЙ ИНФЕКЦИИ Стимуляция эндотелия сигналами SOS Нейтрофилы Лимфоциты Моноциты 0 1 2 3 4 сутки

Миниконкурс на лучшую идею, как устроить очередное чудо – волны миграции разных клеток в разное время
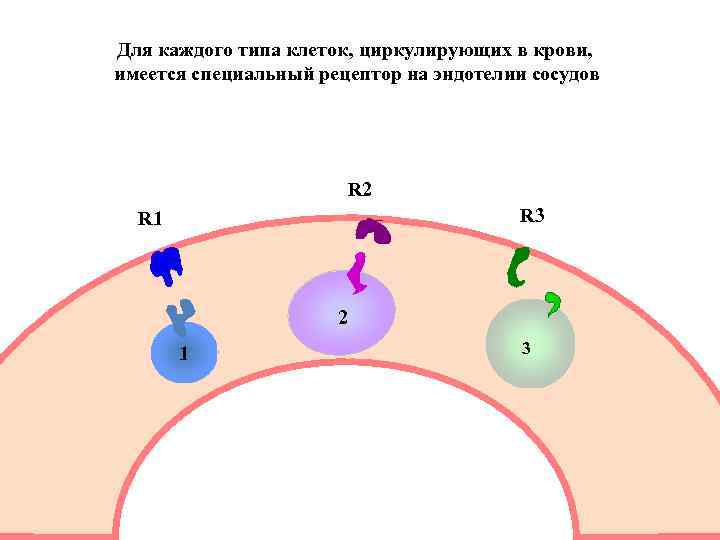
Для каждого типа клеток, циркулирующих в крови, имеется специальный рецептор на эндотелии сосудов R 2 R 3 R 1 2 1 3

Разные рецепторы адгезии выставляются на эндотелии активированного сосуда не одновременно, а последовательно
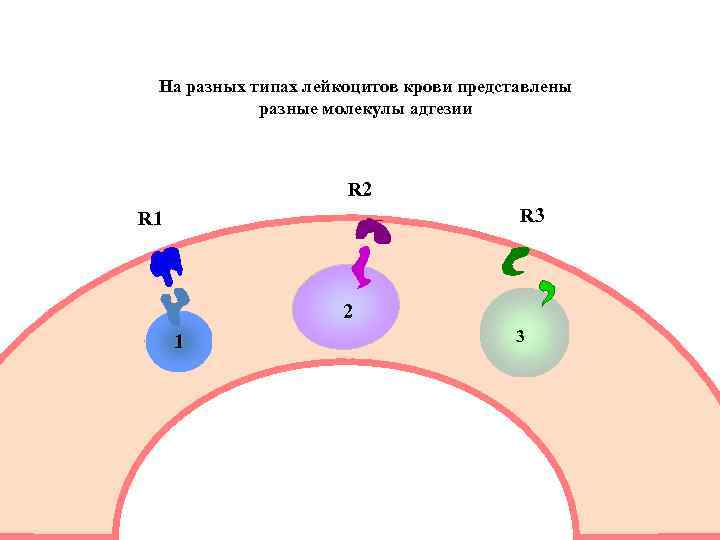
На разных типах лейкоцитов крови представлены разные молекулы адгезии R 2 R 3 R 1 2 1 3
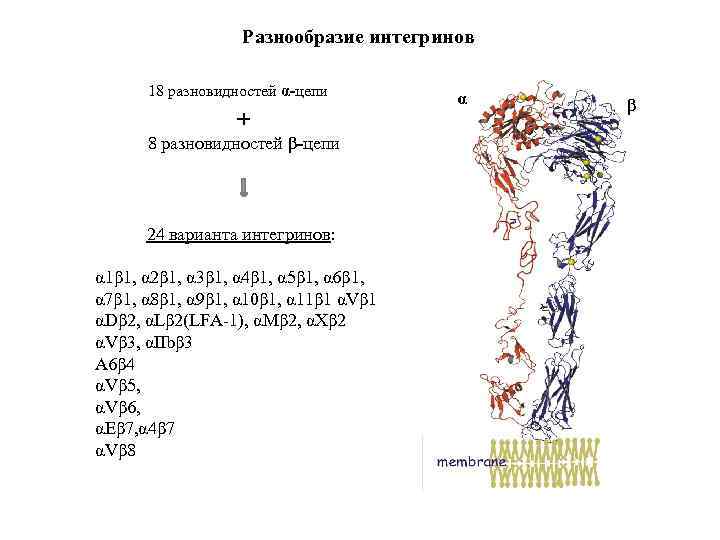
Разнообразие интегринов 18 разновидностей α-цепи + 8 разновидностей β-цепи 24 варианта интегринов: α 1β 1, α 2β 1, α 3β 1, α 4β 1, α 5β 1, α 6β 1, α 7β 1, α 8β 1, α 9β 1, α 10β 1, α 11β 1 αVβ 1 αDβ 2, αLβ 2(LFA-1), αMβ 2, αXβ 2 αVβ 3, αIIbβ 3 Α 6β 4 αVβ 5, αVβ 6, αEβ 7, α 4β 7 αVβ 8 α β
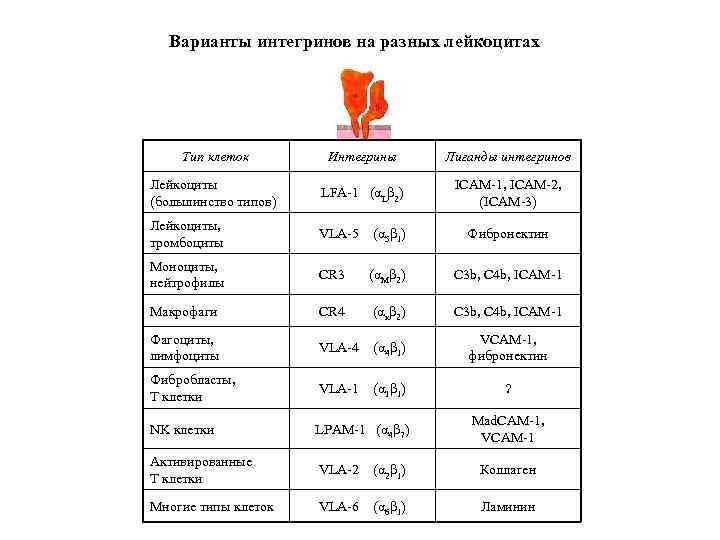
Варианты интегринов на разных лейкоцитах Тип клеток Интегрины Лиганды интегринов Лейкоциты (большинство типов) LFA-1 (αLβ 2) ICAM-1, ICAM-2, (ICAM-3) Лейкоциты, тромбоциты VLA-5 (α 5β 1) Фибронектин Моноциты, нейтрофилы CR 3 (αMβ 2) C 3 b, C 4 b, ICAM-1 Макрофаги CR 4 (αxβ 2) C 3 b, C 4 b, ICAM-1 Фагоциты, лимфоциты VLA-4 (α 4β 1) VCAM-1, фибронектин Фибробласты, Т клетки VLA-1 (α 1β 1) ? NK клетки LPAM-1 (α 4β 7) Активированные Т клетки VLA-2 (α 2β 1) Коллаген Многие типы клеток VLA-6 (α 6β 1) Ламинин Mad. CAM-1, VCAM-1
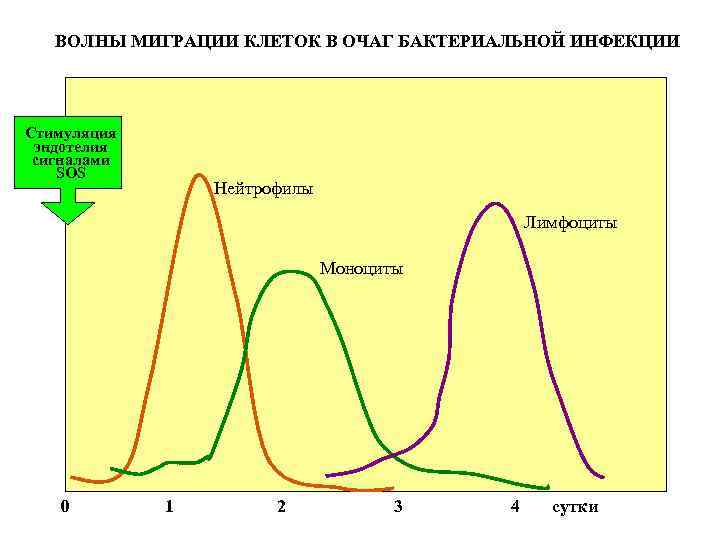
ВОЛНЫ МИГРАЦИИ КЛЕТОК В ОЧАГ БАКТЕРИАЛЬНОЙ ИНФЕКЦИИ Стимуляция эндотелия сигналами SOS Нейтрофилы Лимфоциты Моноциты 0 1 2 3 4 сутки
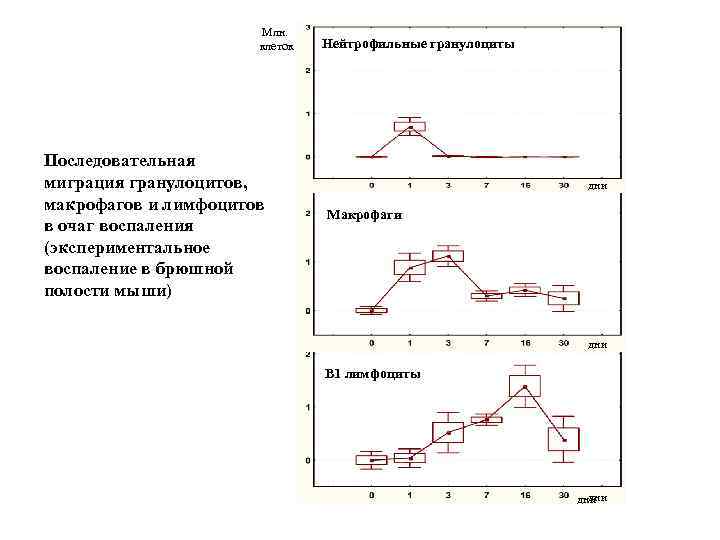
Млн. клеток Последовательная миграция гранулоцитов, макрофагов и лимфоцитов в очаг воспаления (экспериментальное воспаление в брюшной полости мыши) Нейтрофильные гранулоциты дни Макрофаги дни B 1 лимфоциты дни
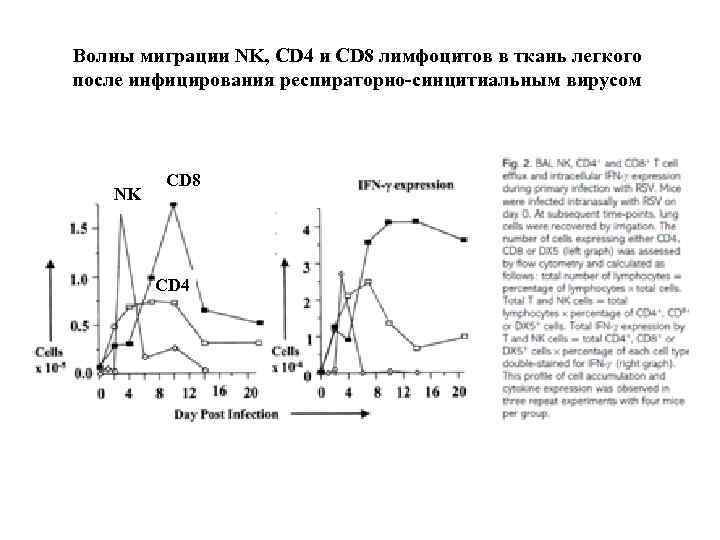
Волны миграции NK, CD 4 и CD 8 лимфоцитов в ткань легкого после инфицирования респираторно-синцитиальным вирусом NK CD 8 CD 4

Необходимые составляющие выхода лейкоцитов из кровотока в ткань 1. Активирующий цитокин из очага инфекции должен достичь кровеносного сосуда и оказаться иммобилизованным на его эндотелии. 2. Активирующие вещества (цитокины) должны вызвать экспрессию адгезионных молекул на поверхности эндотелия. 3. Активирующие вещества (цитокины, гистамин) должны вызвать повреждение плотных контактов (tight junctions) между клетками эндотелия 4. Лейкоцит должен найти активирующий цитокин на поверхности эндотелия, активироваться, изменить интегрин, распластаться. 5. Лейкоцит должен почуять фактор хемотаксиса (тоже иммобилизован) и неуклонно ползти к его источнику, развивая большое механическое усилие – вспомните фильм хемотаксис с преодолением препятствия в виде пипетки. 6. Лейкоцит должен иметь молекулы, комплементарные молекулам межклеточных контактов, чтобы на время встать в монослой эндотелия, как полноценный участник этого слоя. 7. Лейкоциту необходимы молекулы для взаимодействия с перицитом – распластывание, движение, прохождение в щели между перицитами 8. Лейкоцит должен уметь проходить сквозь плотный волокнистый гель – базальную мембрану, построенную из протеогликанов и фибриллярных белков. Нужны ферменты, расплавляющие базальную мембрану. Пример – аминопептидаза (CD 13), без которой моноциты не могут выходить в ткань, в частности, в брюшную полость.

Регуляция проницаемости сосудов для растворимых веществ
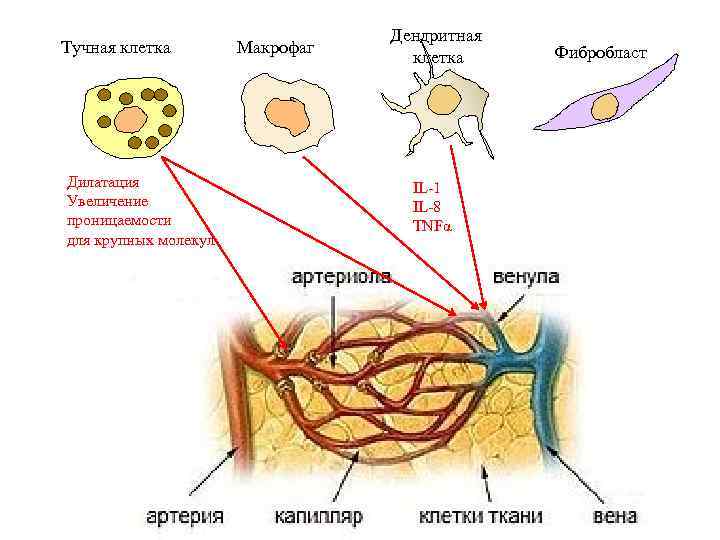
Тучная клетка Дилатация Увеличение проницаемости для крупных молекул Макрофаг Дендритная клетка IL-1 IL-8 TNFα Фибробласт
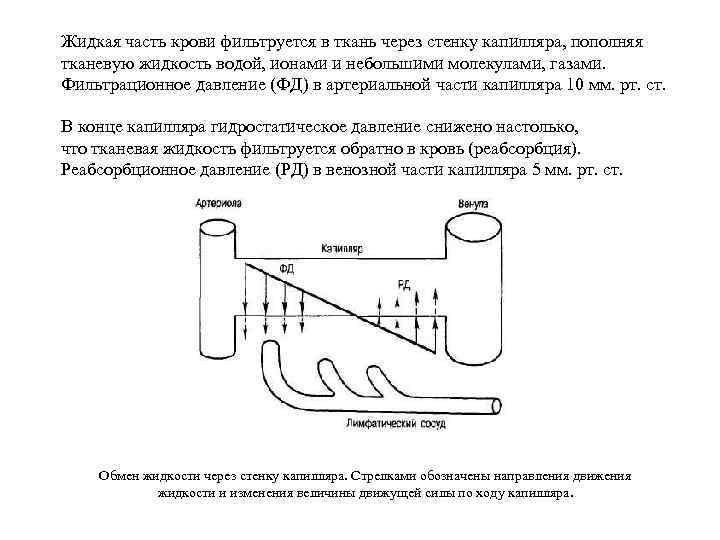
Жидкая часть крови фильтруется в ткань через стенку капилляра, пополняя тканевую жидкость водой, ионами и небольшими молекулами, газами. Фильтрационное давление (ФД) в артериальной части капилляра 10 мм. рт. ст. В конце капилляра гидростатическое давление снижено настолько, что тканевая жидкость фильтруется обратно в кровь (реабсорбция). Реабсорбционное давление (РД) в венозной части капилляра 5 мм. рт. ст. Обмен жидкости через стенку капилляра. Стрелками обозначены направления движения жидкости и изменения величины движущей силы по ходу капилляра.

Фильтрационное давление (ФД) обеспечивает фильтрацию жидкости в артериальном конце капилляра, в результате чего она перемещается из капилляров в интерстициальное пространство. ФД является результатом взаимодействия разнонаправленных сил: способствуют фильтрации гидростатическое давление крови (ГДк = 30 мм рт. ст. ) и онкотическое давление тканевой жидкости (ОДт = 5 мм рт. ст. ). Препятствует фильтрации онкотическое давление плазмы крови (ОДк = 25 мм рт. ст. ). Гидростатическое давление в интерстиции колеблется около нуля (т. е. оно несколько ниже или выше атмосферного), поэтому ФД равно: ФД = ГДк + ОДт - ОДк = 30 + 5 - 25 = 10 (мм рт. ст. ) По мере продвижения крови по капилляру ГДк снижается до 15 мм рт. ст. , поэтому силы, способствующие фильтрации, становятся меньше сил, противодействующих фильтрации. Таким образом, формируется реабсорбционное давление (РД), обеспечивающее перемещение жидкости в венозном конце изинтерстиция в капилляры. РД = ОДк - ГДк - ОДт = 25 - 15 - 5 = 5 (мм рт. ст. ) Соотношение и направления сил, обеспечивающих фильтрацию и реабсорбцию жидкости в капиллярах, показаны на рисунке слева. Таким образом, фильтрационное давление больше, чем реабсорбционное, но поскольку проницаемость для воды венозной части микроциркуляторного русла выше проницаемости артериального конца капилляра, то количество фильтрата лишь незначительно превышает количество реабсорбируемой жидкости; излишек воды из тканей удаляется через лимфатическую систему.
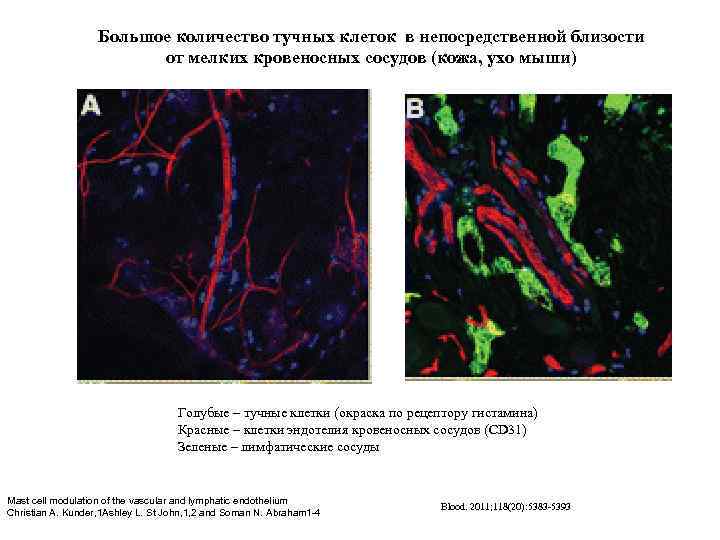
Большое количество тучных клеток в непосредственной близости от мелких кровеносных сосудов (кожа, ухо мыши) Голубые – тучные клетки (окраска по рецептору гистамина) Красные – клетки эндотелия кровеносных сосудов (CD 31) Зеленые – лимфатические сосуды Mast cell modulation of the vascular and lymphatic endothelium Christian A. Kunder, 1 Ashley L. St John, 1, 2 and Soman N. Abraham 1 -4 Blood. 2011; 118(20): 5383 -5393
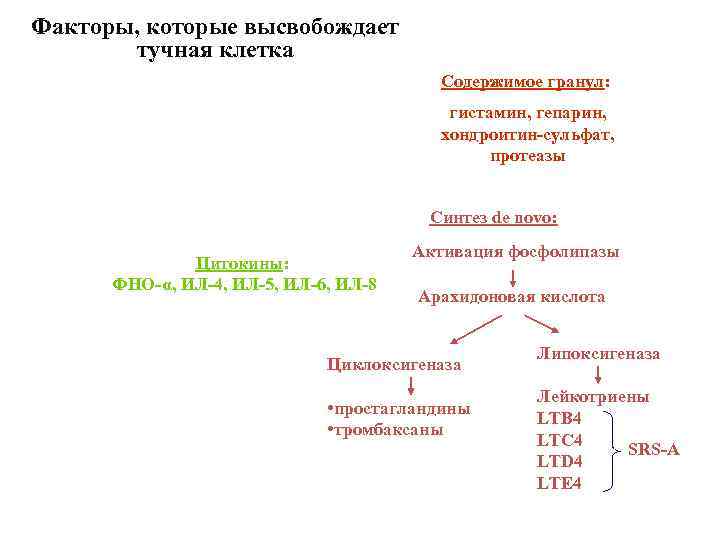
Факторы, которые высвобождает тучная клетка Содержимое гранул: гистамин, гепарин, хондроитин-сульфат, протеазы Синтез de novo: Цитокины: ФНО-α, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-8 Активация фосфолипазы Арахидоновая кислота Циклоксигеназа • простагландины • тромбаксаны Липоксигеназа Лейкотриены LTB 4 LTC 4 SRS-A LTD 4 LTE 4
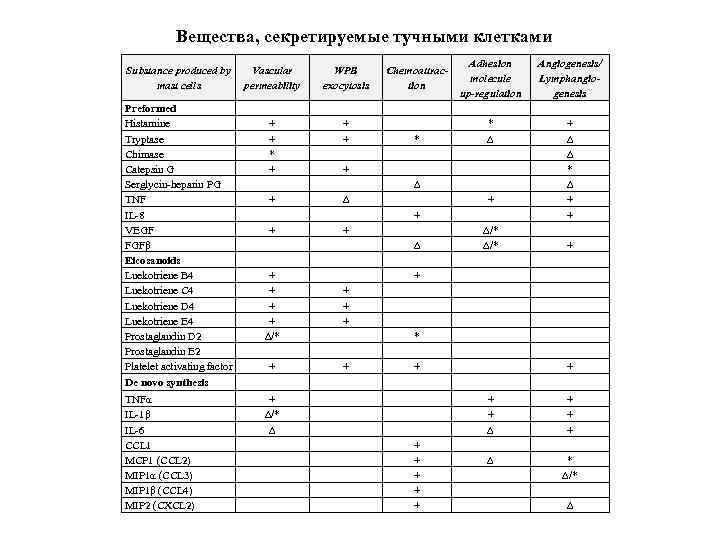
Вещества, секретируемые тучными клетками Substance produced by mast cells Preformed Histamine Tryptase Chimase Catepsin G Serglycin-heparin PG TNF IL-8 VEGF FGFβ Eicosanoids Luekotriene B 4 Luekotriene C 4 Luekotriene D 4 Luekotriene E 4 Prostaglandin D 2 Prostaglandin E 2 Platelet activating factor De novo synthesis TNFα IL-1β IL-6 CCL 1 MCP 1 (CCL 2) MIP 1α (CCL 3) MIP 1β (CCL 4) MIP 2 (CXCL 2) Vascular permeability WPB exocytosis + + * + + Chemoattraction ∆ * Adhesion molecule up-regulation Angiogenesis/ Lymphangiogenesis * ∆ + ∆ ∆ * ∆ + + + + ∆/* + + + ∆/* + * + + ∆/* ∆ + + + ∆ * ∆/* ∆
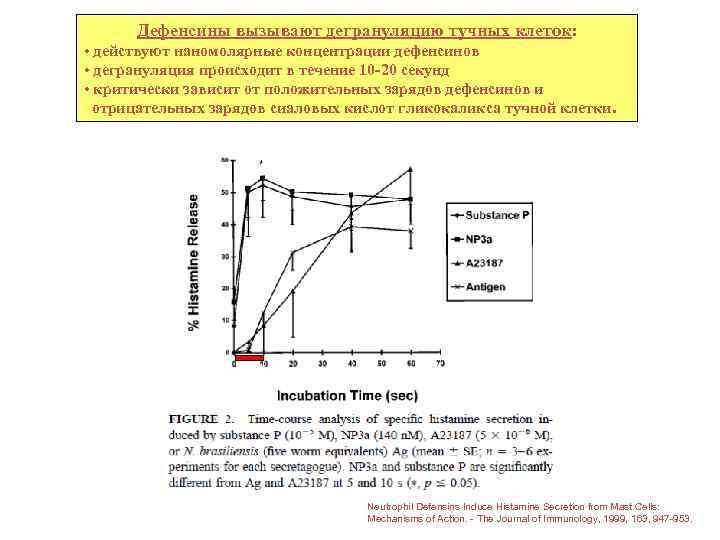
Дефенсины вызывают дегрануляцию тучных клеток: • действуют наномолярные концентрации дефенсинов • дегрануляция происходит в течение 10 -20 секунд • критически зависит от положительных зарядов дефенсинов и отрицательных зарядов сиаловых кислот гликокаликса тучной клетки. Neutrophil Defensins Induce Histamine Secretion from Mast Cells: Mechanisms of Action. - The Journal of Immunology, 1999, 163, 947 -953.

Гистамин образуется в организме при декарбоксилировании аминокислоты гистидина, катализируемого гистидиндекарбоксилазой Гистамин депонируется в тучных клетках в виде комплекса с гепарином, свободный гистамин быстро деактивируется диаминоксидазой (гистаминазой) либо метилируется гистамин-N-метилтрансферазой. Im-CH 2 NH 2 + O 2 + H 2 O →Im-CH 2 CHO + NH 3 + H 2 O 2 Конечные метаболиты гистамина — имидазолилуксусная кислота и Nметигистамин выводятся с мочой.

Рецепторы гистамина В организме существуют специфические рецепторы, для которых гистамин является естественным лигандом. В настоящее время различают три подгруппы гистаминовых (Н) рецепторов: Н 1 -, Н 2 - и Н 3 -рецепторы. Тип Локализация Эффекты H 1 рецепторы Гладкие мышцы, эндотелий, центральная нервная система (постсинаптические) Вазодилатация, бронхоконстрикция, спазм гладкой мускулатуры бронхов, раздвижение клеток эндотелия (и, как следствие, транссудации жидкости в околососудистое пространство, отек и крапивница), стимуляция секреции гормонов гипофизом. H 2 рецепторы Париетальные клетки желудка Стимуляция секреции желудочного сока. H 3 рецепторы Центральная и периферическая нервная система (пресинаптические) Подавление высвобождения нейромедиаторов (ГАМК, ацетилхолина, серотонина, норадреналина).
Меченые декстраны различной длинны удобны для определения калибра молекулярных «пор» в стенке кровеносных сосудов. Декстран – полимер глюкозы.
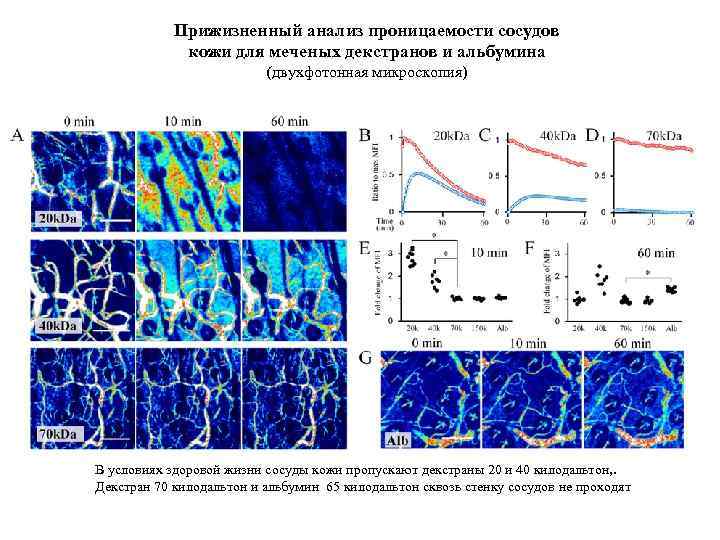
Прижизненный анализ проницаемости сосудов кожи для меченых декстранов и альбумина (двухфотонная микроскопия) В условиях здоровой жизни сосуды кожи пропускают декстраны 20 и 40 килодальтон, . Декстран 70 килодальтон и альбумин 65 килодальтон сквозь стенку сосудов не проходят
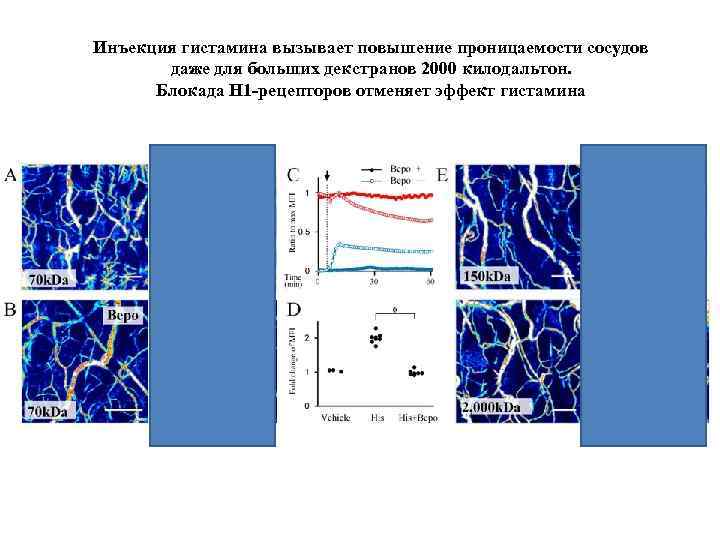
Инъекция гистамина вызывает повышение проницаемости сосудов даже для больших декстранов 2000 килодальтон. Блокада H 1 -рецепторов отменяет эффект гистамина
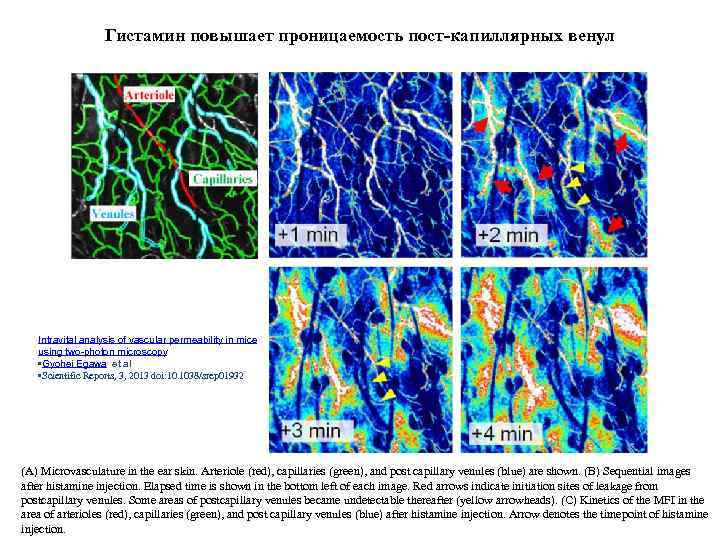
Гистамин повышает проницаемость пост-капиллярных венул Intravital analysis of vascular permeability in mice using two-photon microscopy • Gyohei Egawa et al • Scientific Reports, 3, 2013 doi: 10. 1038/srep 01932 (A) Microvasculature in the ear skin. Arteriole (red), capillaries (green), and post capillary venules (blue) are shown. (B) Sequential images after histamine injection. Elapsed time is shown in the bottom left of each image. Red arrows indicate initiation sites of leakage from postcapillary venules. Some areas of postcapillary venules became undetectable thereafter (yellow arrowheads). (C) Kinetics of the MFI in the area of arterioles (red), capillaries (green), and post capillary venules (blue) after histamine injection. Arrow denotes the timepoint of histamine injection.

Просвет мелкой вены

Обширная область контакта двух клеток эндотелия сформирована тремя видами молекулярных «замков» − адгезионный, щелевидный и плотный контакты
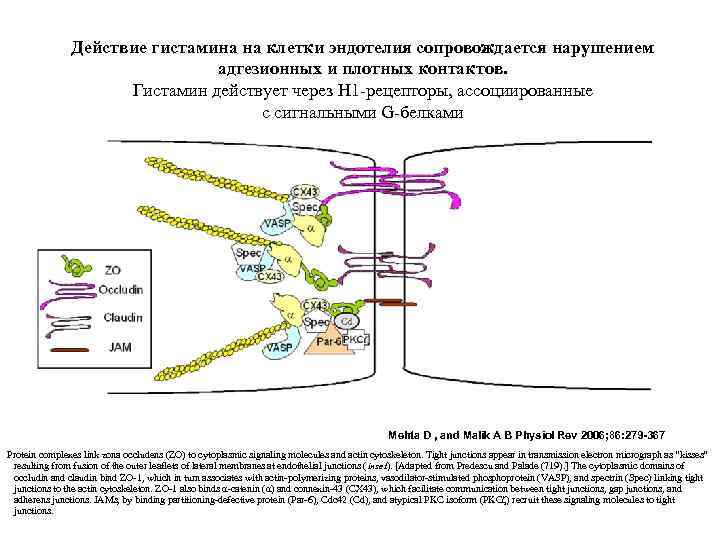
Действие гистамина на клетки эндотелия сопровождается нарушением адгезионных и плотных контактов. Гистамин действует через H 1 -рецепторы, ассоциированные с сигнальными G-белками Mehta D , and Malik A B Physiol Rev 2006; 86: 279 -367 Protein complexes link zona occludens (ZO) to cytoplasmic signaling molecules and actin cytoskeleton. Tight junctions appear in transmission electron micrograph as ”kisses“ resulting from fusion of the outer leaflets of lateral membranes at endothelial junctions ( inset). [Adapted from Predescu and Palade (719). ] The cytoplasmic domains of occludin and claudin bind ZO-1, which in turn associates with actin-polymerizing proteins, vasodilator-stimulated phosphoprotein (VASP), and spectrin (Spec) linking tight junctions to the actin cytoskeleton. ZO-1 also binds α-catenin (α) and connexin-43 (CX 43), which facilitate communication between tight junctions, gap junctions, and adherens junctions. JAMs, by binding partitioning-defective protein (Par-6), Cdc 42 (Cd), and atypical PKC isoform (PKCζ) recruit these signaling molecules to tight junctions.
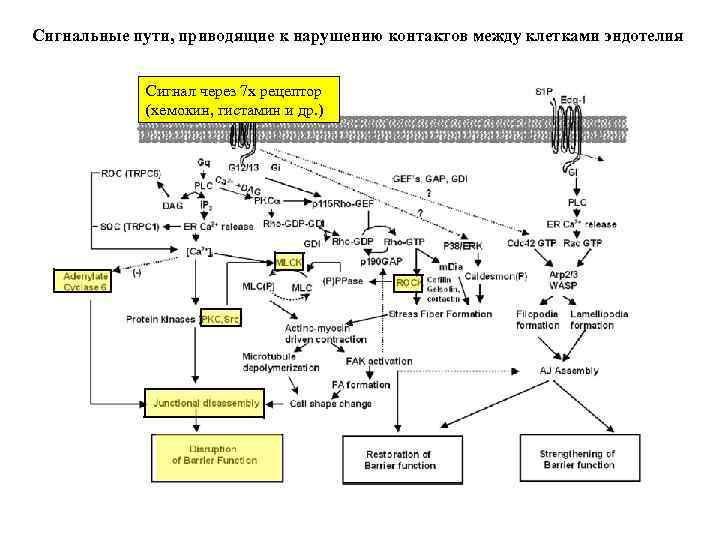
Сигнальные пути, приводящие к нарушению контактов между клетками эндотелия Сигнал через 7 x рецептор (хемокин, гистамин и др. )

Какие крупные молекулы защитят от инфекции: • C-реактивный белок, • маннан-связывающий лектин, • гамма-глобулины, • альфа-глобулины, • белки комплемента

Системные эффекты цитокинов и других медиаторов воспаления вовлекают в процесс защиты весь организм: 1. Продукция защитных белков в печени 2. Продукция защитных клеток в костном мозге 3. Гликонеогенез (превращение запасов жира в энергетические субстраты) 4. Пирогенный эффект 5. Изменения в эндокринной системе 6. Изменения в ЦНС и вегетативной нервной системе

Общая логика воспаления 1. Реакция системная – задействован весь организм, но при этом все делается для победы в очаге вторжения (Пришельцы в фокусе). Попадание в цель очень точное. 2. Реакция каскадная со множеством звеньев, позволяющих «раскручивать» большую защиту при малых инициирующих сигналах. 3. Реакция не специфична в отношении индуктора (причины). Однотипная защита развивается против самых разных индукторов. 4. Реакция эффективная, но травматичная. Может наносить серьезные повреждения собственным органам и тканям. 5. Реакция избыточная, с большим уровнем надежности (патрулирование клетками и молекулами в пределах всего организма, хотя проблема сосредоточена в относительно небольшом фрагменте тела). 6. Реакция регулируется во времени в очень широком диапазоне. Быстрая защита (проницаемость для молекул) начинается в течение минут. Медленная фаза – направленная миграция клеток развертывается в течение часов –десятков часов, и может продолжаться многие месяцы и годы.



Транспорт альбумина с помощью кавеолей и рецептора gp 60 В эндотелиальной клетке много кавеолей – они составляют 15% объема клетки
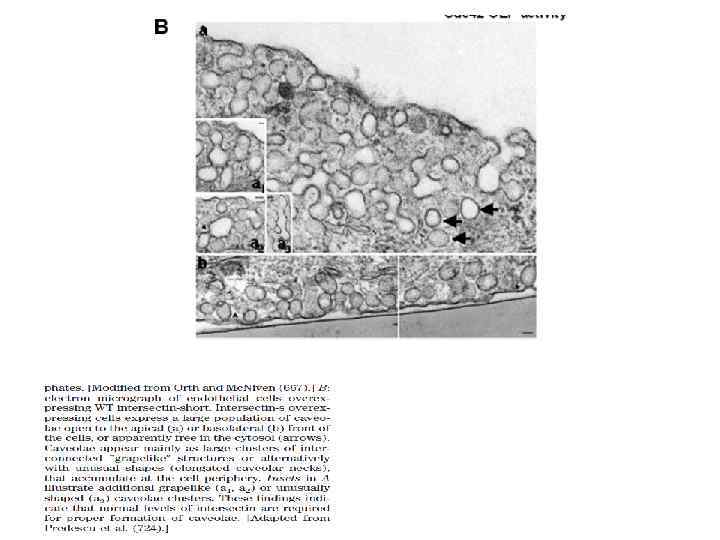
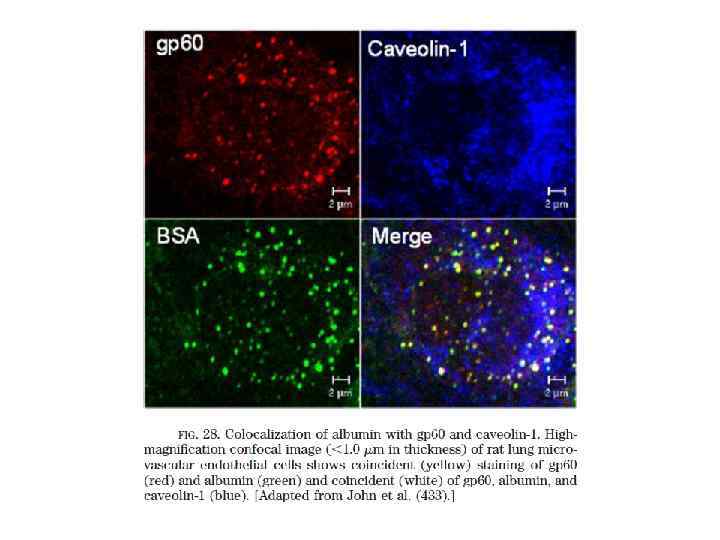
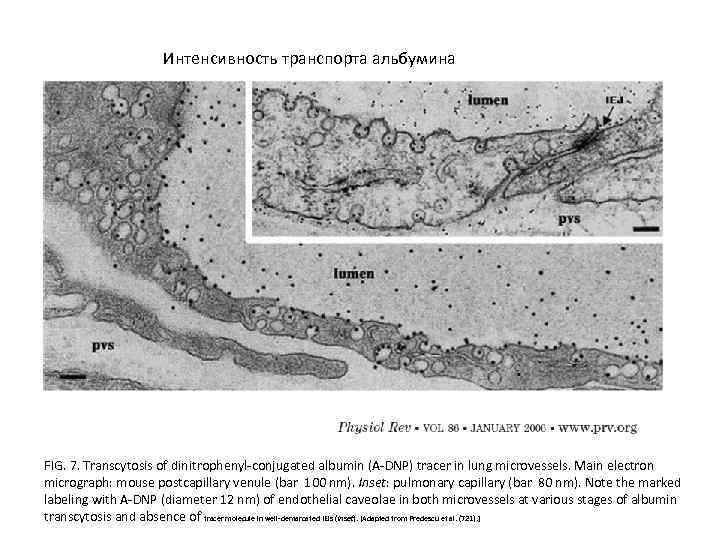
Интенсивность транспорта альбумина FIG. 7. Transcytosis of dinitrophenyl-conjugated albumin (A-DNP) tracer in lung microvessels. Main electron micrograph: mouse postcapillary venule (bar 100 nm). Inset: pulmonary capillary (bar 80 nm). Note the marked labeling with A-DNP (diameter 12 nm) of endothelial caveolae in both microvessels at various stages of albumin transcytosis and absence of tracer molecule in well-demarcated IEJs (inset). [Adapted from Predescu et al. (721). ]
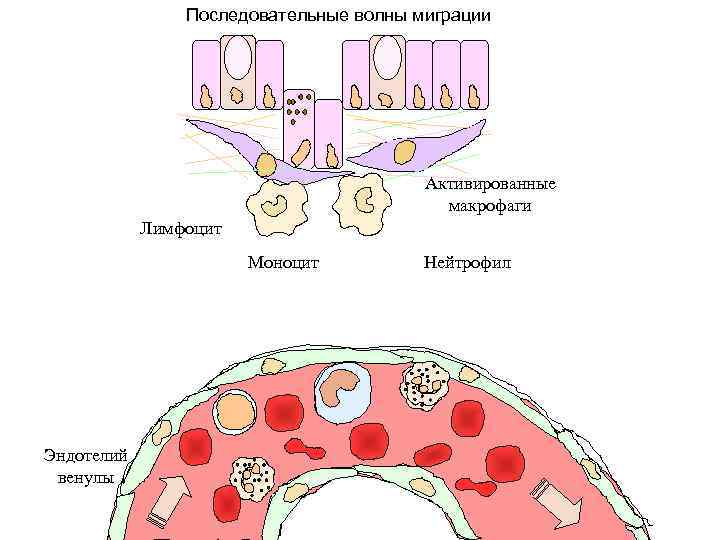
Последовательные волны миграции Активированные макрофаги Лимфоцит Моноцит Эндотелий венулы Нейтрофил
Лекция 3 (биофак и физфак) 21 февраля 2015.ppt