05_Khemilyuminestsentsia_1-2011.ppt
- Количество слайдов: 31
 Хемилюминесценция Ю. А. Владимиров 2011
Хемилюминесценция Ю. А. Владимиров 2011
 Участие ВЗО и НСО в межмолекулярных взаимодействиях
Участие ВЗО и НСО в межмолекулярных взаимодействиях
 Что такое хемилюминесценция (ХЛ)? Хемилюминесценция (ХЛ) — это свечение, сопровождающее химическую реакцию. Процесс хемилюминесценции включает в себя две стадии: A + B P* P* P + фотон Образование продукта в электроном возбужденном состоянии (хемилюминесцентная реакция) Испускание кванта света (люминесценция)
Что такое хемилюминесценция (ХЛ)? Хемилюминесценция (ХЛ) — это свечение, сопровождающее химическую реакцию. Процесс хемилюминесценции включает в себя две стадии: A + B P* P* P + фотон Образование продукта в электроном возбужденном состоянии (хемилюминесцентная реакция) Испускание кванта света (люминесценция)
 Механизм генерации возбужденных состояний при химических реакциях
Механизм генерации возбужденных состояний при химических реакциях
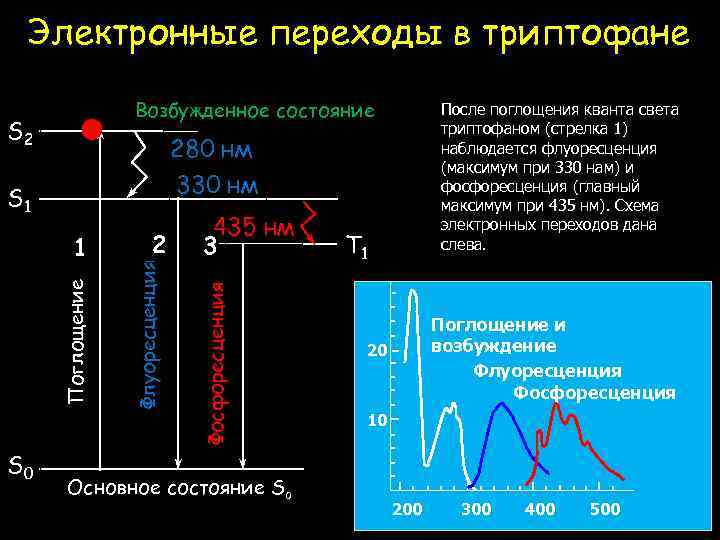 Электронные переходы в триптофане Возбужденное состояние S 2 280 нм 330 нм 2 Флуоресценция Поглощение 1 435 нм 3 Фосфоресценция S 1 S 0 После поглощения кванта света триптофаном (стрелка 1) наблюдается флуоресценция (максимум при 330 нам) и фосфоресценция (главный максимум при 435 нм). Схема электронных переходов дана слева. Основное состояние So T 1 Поглощение и возбуждение Флуоресценция Фосфоресценция 20 10 200 300 400 500
Электронные переходы в триптофане Возбужденное состояние S 2 280 нм 330 нм 2 Флуоресценция Поглощение 1 435 нм 3 Фосфоресценция S 1 S 0 После поглощения кванта света триптофаном (стрелка 1) наблюдается флуоресценция (максимум при 330 нам) и фосфоресценция (главный максимум при 435 нм). Схема электронных переходов дана слева. Основное состояние So T 1 Поглощение и возбуждение Флуоресценция Фосфоресценция 20 10 200 300 400 500
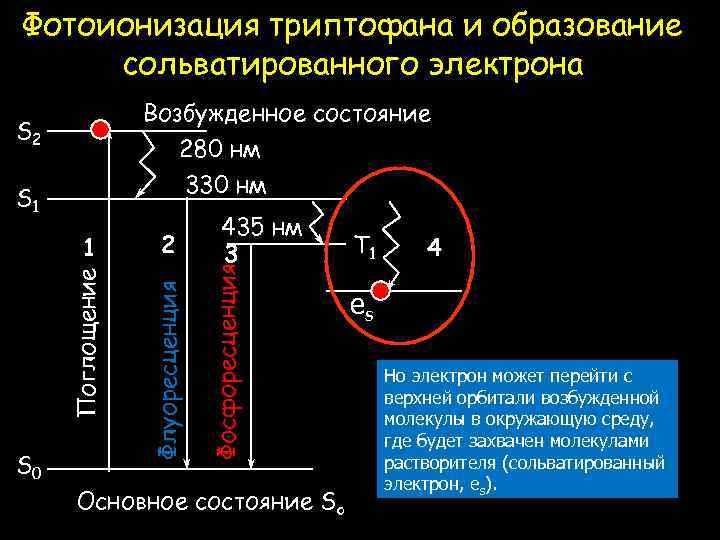 Фотоионизация триптофана и образование сольватированного электрона Возбужденное состояние S 2 280 нм 330 нм S 0 2 Флуоресценция Поглощение 1 435 нм 3 Фосфоресценция S 1 Основное состояние So T 1 4 es Но электрон может перейти с верхней орбитали возбужденной молекулы в окружающую среду, где будет захвачен молекулами растворителя (сольватированный электрон, es).
Фотоионизация триптофана и образование сольватированного электрона Возбужденное состояние S 2 280 нм 330 нм S 0 2 Флуоресценция Поглощение 1 435 нм 3 Фосфоресценция S 1 Основное состояние So T 1 4 es Но электрон может перейти с верхней орбитали возбужденной молекулы в окружающую среду, где будет захвачен молекулами растворителя (сольватированный электрон, es).
 Термолюминесценция УФоблученного триптофана S 2 435 нм 3 Фосфоресценция S 1 Возбужденное состояние S 0 5 T 1 es Термолюминесценция Основное состояние So Сольватированный электрон устойчив лишь при низких температурах (ниже 77 К). При нагревании даже до 100 К он возвращается на триплетный уровень возбужденной молекулы (Т 1) и наблюдается свечение, по спектру близкое к фосфоресценции. Оно называется термолюминесценцией.
Термолюминесценция УФоблученного триптофана S 2 435 нм 3 Фосфоресценция S 1 Возбужденное состояние S 0 5 T 1 es Термолюминесценция Основное состояние So Сольватированный электрон устойчив лишь при низких температурах (ниже 77 К). При нагревании даже до 100 К он возвращается на триплетный уровень возбужденной молекулы (Т 1) и наблюдается свечение, по спектру близкое к фосфоресценции. Оно называется термолюминесценцией.
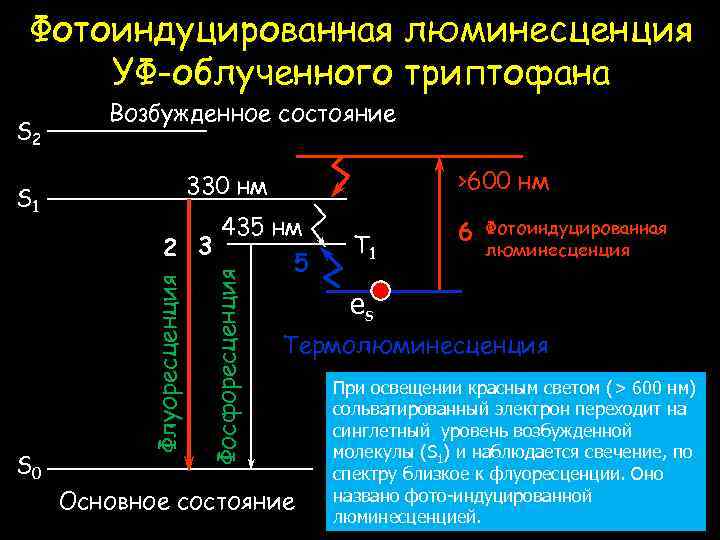 Фотоиндуцированная люминесценция УФ-облученного триптофана S 2 Возбужденное состояние S 1 435 нм Фосфоресценция Флуоресценция 2 3 S 0 >600 нм 330 нм 5 T 1 6 Фотоиндуцированная люминесценция es Термолюминесценция Основное состояние При освещении красным светом (> 600 нм) сольватированный электрон переходит на синглетный уровень возбужденной молекулы (S 1) и наблюдается свечение, по спектру близкое к флуоресценции. Оно названо фото-индуцированной люминесценцией.
Фотоиндуцированная люминесценция УФ-облученного триптофана S 2 Возбужденное состояние S 1 435 нм Фосфоресценция Флуоресценция 2 3 S 0 >600 нм 330 нм 5 T 1 6 Фотоиндуцированная люминесценция es Термолюминесценция Основное состояние При освещении красным светом (> 600 нм) сольватированный электрон переходит на синглетный уровень возбужденной молекулы (S 1) и наблюдается свечение, по спектру близкое к флуоресценции. Оно названо фото-индуцированной люминесценцией.
 Рекомбинационное свечение как химическая реакция 1. Запасание энергии: AH + фотон AH+ + e¯ 2. ХЛ реакция: AH+ + e¯ 3 AH 3. Эмиссия фотона: 3 AH 1 AH + фосфоресценция Почему рекомбинационное свечение происходит преимущественно с триплетого уровня продукта реакции?
Рекомбинационное свечение как химическая реакция 1. Запасание энергии: AH + фотон AH+ + e¯ 2. ХЛ реакция: AH+ + e¯ 3 AH 3. Эмиссия фотона: 3 AH 1 AH + фосфоресценция Почему рекомбинационное свечение происходит преимущественно с триплетого уровня продукта реакции?
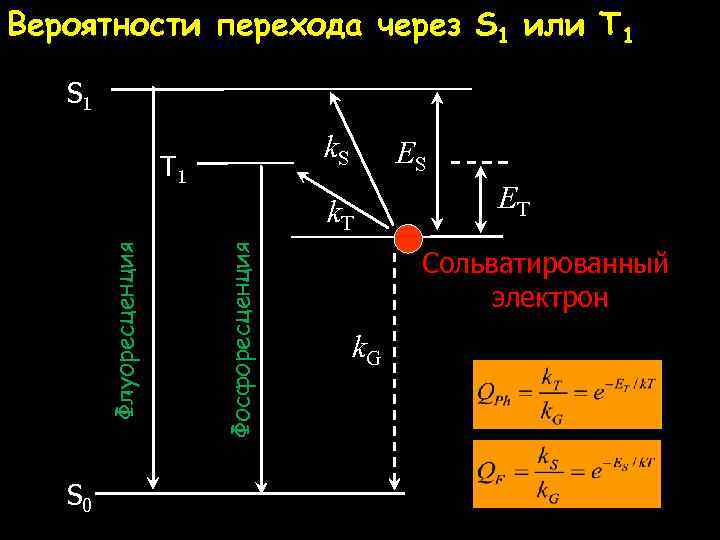 Вероятности перехода через S 1 или T 1 S 1 k. S T 1 ES S 0 Фосфоресценция Флуоресценция k. T ET Сольватированный электрон k. G
Вероятности перехода через S 1 или T 1 S 1 k. S T 1 ES S 0 Фосфоресценция Флуоресценция k. T ET Сольватированный электрон k. G
 Эмпирические законы хемилюминесценции 1. Правило Одюбера: энергия фотона ХЛ равна сумме энергии активации и тепловому эффекту реакции. 2. Спектры хемилюминесценции близки к спектрам фосфоресценции, а не к спектрам флуоресценции. Почему?
Эмпирические законы хемилюминесценции 1. Правило Одюбера: энергия фотона ХЛ равна сумме энергии активации и тепловому эффекту реакции. 2. Спектры хемилюминесценции близки к спектрам фосфоресценции, а не к спектрам флуоресценции. Почему?
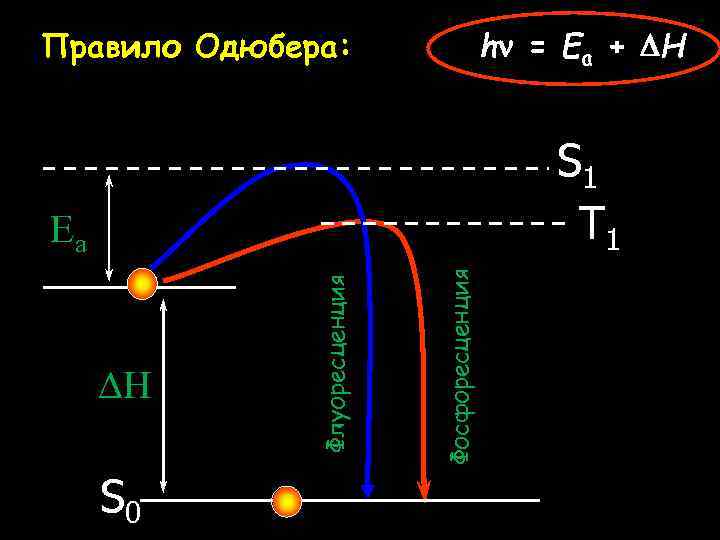 Правило Одюбера: hn = Ea + DH S 1 T 1 S 0 Фосфоресценция DH Флуоресценция Ea
Правило Одюбера: hn = Ea + DH S 1 T 1 S 0 Фосфоресценция DH Флуоресценция Ea
 Виды хемилюминесценции в живых системах
Виды хемилюминесценции в живых системах
 Виды хемилюминесценции в живых системах 1. Биолюминесценция (БЛ). 2. Митогенетические лучи (МЛ). 3. Сверхслабое свечение (Собственная хемилюминесценция - СХЛ) клеток и тканей. 4. Активированная хемилюминесценция (АХЛ). 5. Индуцированная ХЛ • Фотохемилюминесценция (ФХЛ) • Радиолюминесценция (РЛ) • Электролюминесценция (ЭЛ) • Триболюминесценция (Тр. Л) • Термолюминесценция (Тер. Л)
Виды хемилюминесценции в живых системах 1. Биолюминесценция (БЛ). 2. Митогенетические лучи (МЛ). 3. Сверхслабое свечение (Собственная хемилюминесценция - СХЛ) клеток и тканей. 4. Активированная хемилюминесценция (АХЛ). 5. Индуцированная ХЛ • Фотохемилюминесценция (ФХЛ) • Радиолюминесценция (РЛ) • Электролюминесценция (ЭЛ) • Триболюминесценция (Тр. Л) • Термолюминесценция (Тер. Л)
 Что дает изучение ХЛ для медицины? 1. Изучение механизма реакций, сопровождающихся свечением (ХЛ-реакции). • Изучение первичных стадий фотобиологических процессов. • Изучение цепного окисления липидов. • Изучение «активных форм кислорода» . • Изучение механизма действия антиоксидантов. 2. Применение ХЛ в лабораторной клинической диагностике. • Оценка уровня свободных радикалов. • Определение активности фагоцитов. • Определение окисляемости липопротеинов. • Определение антиоксидантов.
Что дает изучение ХЛ для медицины? 1. Изучение механизма реакций, сопровождающихся свечением (ХЛ-реакции). • Изучение первичных стадий фотобиологических процессов. • Изучение цепного окисления липидов. • Изучение «активных форм кислорода» . • Изучение механизма действия антиоксидантов. 2. Применение ХЛ в лабораторной клинической диагностике. • Оценка уровня свободных радикалов. • Определение активности фагоцитов. • Определение окисляемости липопротеинов. • Определение антиоксидантов.
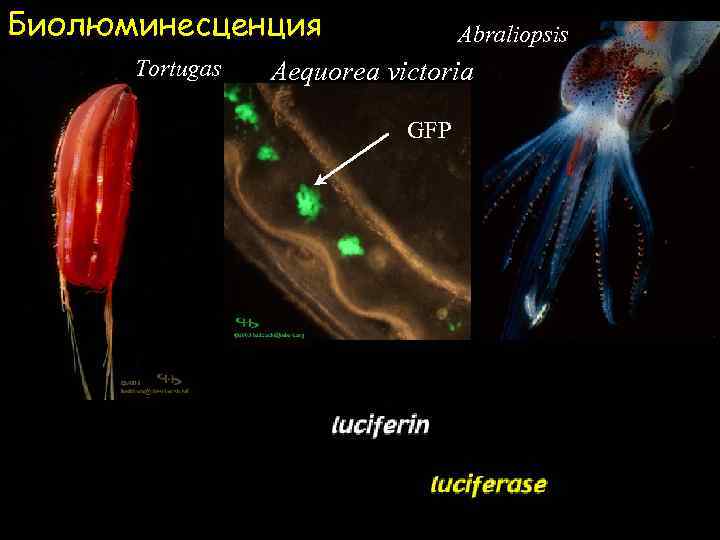 Биолюминесценция Tortugas Abraliopsis Aequorea victoria GFP Hydroid
Биолюминесценция Tortugas Abraliopsis Aequorea victoria GFP Hydroid
 Биолюминесценция (БЛ) Биолюминесценция – это видимое глазом (т. е. весьма интенсивное) свечение некоторых организмов, связанное со специфическими ферментативными реакциями. Специфический фермент называется люциферазой, а его субсбтрат – люциферином
Биолюминесценция (БЛ) Биолюминесценция – это видимое глазом (т. е. весьма интенсивное) свечение некоторых организмов, связанное со специфическими ферментативными реакциями. Специфический фермент называется люциферазой, а его субсбтрат – люциферином
 Происхождение биолюминесценции Большинство люциферинов представляет собой слегка измененные или совсем неизмененные коферменты, участвующие в окислительновосстановительном метаболизме. Отчего бы это? Лучше светиться, чем окисляться
Происхождение биолюминесценции Большинство люциферинов представляет собой слегка измененные или совсем неизмененные коферменты, участвующие в окислительновосстановительном метаболизме. Отчего бы это? Лучше светиться, чем окисляться
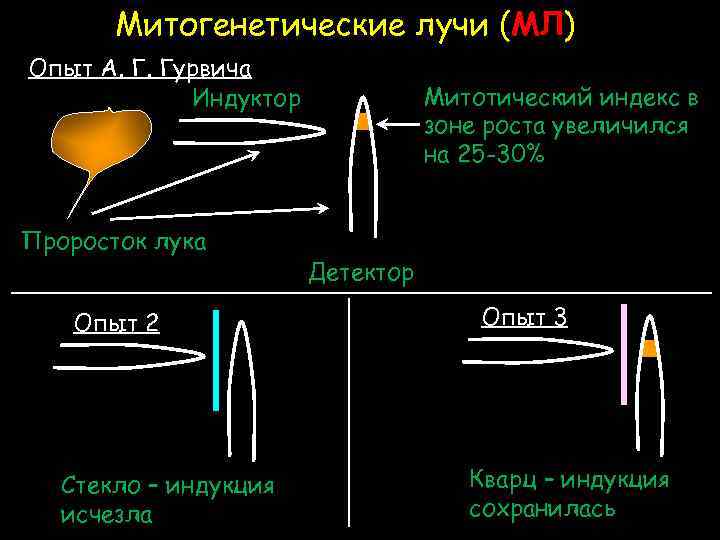 Митогенетические лучи (МЛ) Опыт А. Г. Гурвича Индуктор Проросток лука Опыт 2 Стекло – индукция исчезла Митотический индекс в зоне роста увеличился на 25 -30% Детектор Опыт 3 Кварц – индукция сохранилась
Митогенетические лучи (МЛ) Опыт А. Г. Гурвича Индуктор Проросток лука Опыт 2 Стекло – индукция исчезла Митотический индекс в зоне роста увеличился на 25 -30% Детектор Опыт 3 Кварц – индукция сохранилась
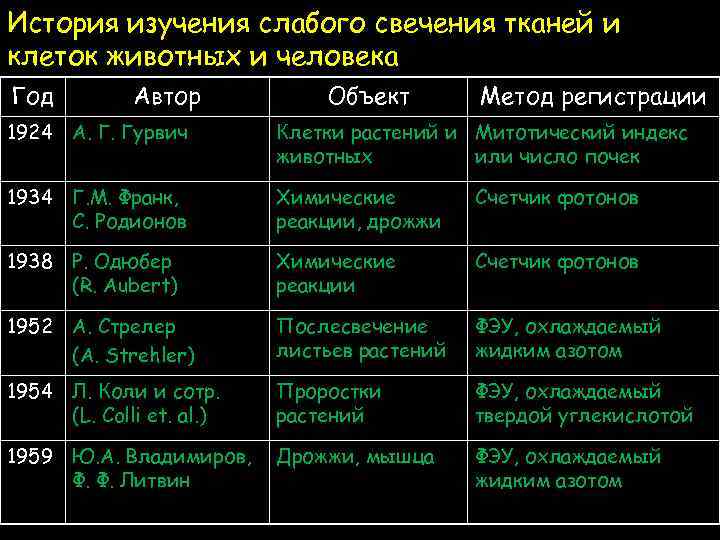 История изучения слабого свечения тканей и клеток животных и человека Год Автор Объект Метод регистрации 1924 А. Г. Гурвич Клетки растений и Митотический индекс животных или число почек 1934 Г. М. Франк, С. Родионов Химические реакции, дрожжи Счетчик фотонов 1938 Р. Одюбер (R. Aubert) Химические реакции Счетчик фотонов 1952 А. Стрелер (A. Strehler) Послесвечение листьев растений ФЭУ, охлаждаемый жидким азотом 1954 Л. Коли и сотр. (L. Colli et. al. ) Проростки растений ФЭУ, охлаждаемый твердой углекислотой 1959 Ю. А. Владимиров, Ф. Ф. Литвин Дрожжи, мышца ФЭУ, охлаждаемый жидким азотом
История изучения слабого свечения тканей и клеток животных и человека Год Автор Объект Метод регистрации 1924 А. Г. Гурвич Клетки растений и Митотический индекс животных или число почек 1934 Г. М. Франк, С. Родионов Химические реакции, дрожжи Счетчик фотонов 1938 Р. Одюбер (R. Aubert) Химические реакции Счетчик фотонов 1952 А. Стрелер (A. Strehler) Послесвечение листьев растений ФЭУ, охлаждаемый жидким азотом 1954 Л. Коли и сотр. (L. Colli et. al. ) Проростки растений ФЭУ, охлаждаемый твердой углекислотой 1959 Ю. А. Владимиров, Ф. Ф. Литвин Дрожжи, мышца ФЭУ, охлаждаемый жидким азотом
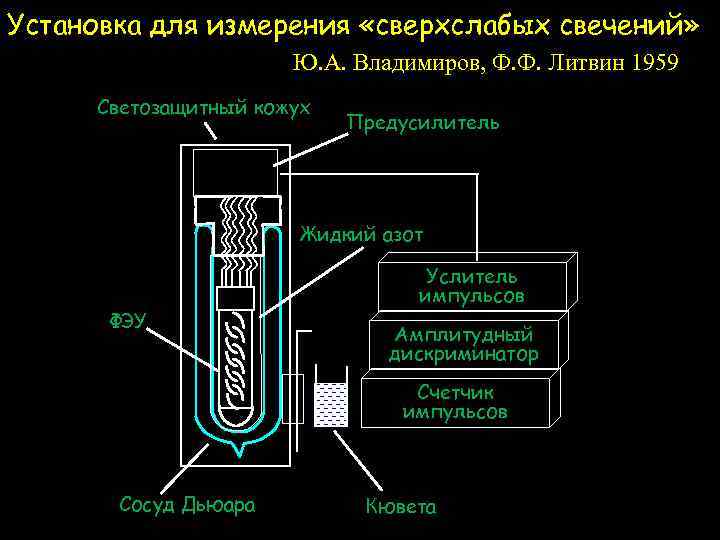 Установка для измерения «сверхслабых свечений» Ю. А. Владимиров, Ф. Ф. Литвин 1959 Светозащитный кожух Предусилитель Жидкий азот ФЭУ Услитель импульсов Амплитудный дискриминатор Счетчик импульсов Сосуд Дьюара Кювета
Установка для измерения «сверхслабых свечений» Ю. А. Владимиров, Ф. Ф. Литвин 1959 Светозащитный кожух Предусилитель Жидкий азот ФЭУ Услитель импульсов Амплитудный дискриминатор Счетчик импульсов Сосуд Дьюара Кювета
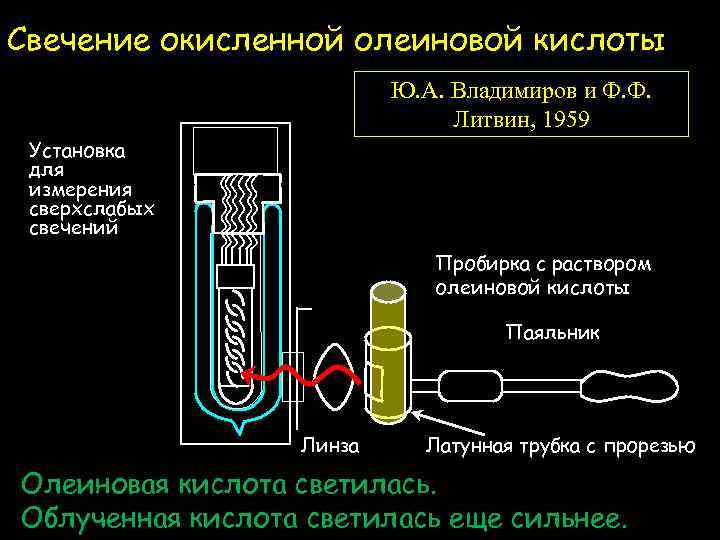 Свечение окисленной олеиновой кислоты Ю. А. Владимиров и Ф. Ф. Литвин, 1959 Установка для измерения сверхслабых свечений Пробирка с раствором олеиновой кислоты Паяльник Линза Латунная трубка с прорезью Олеиновая кислота светилась. Облученная кислота светилась еще сильнее.
Свечение окисленной олеиновой кислоты Ю. А. Владимиров и Ф. Ф. Литвин, 1959 Установка для измерения сверхслабых свечений Пробирка с раствором олеиновой кислоты Паяльник Линза Латунная трубка с прорезью Олеиновая кислота светилась. Облученная кислота светилась еще сильнее.
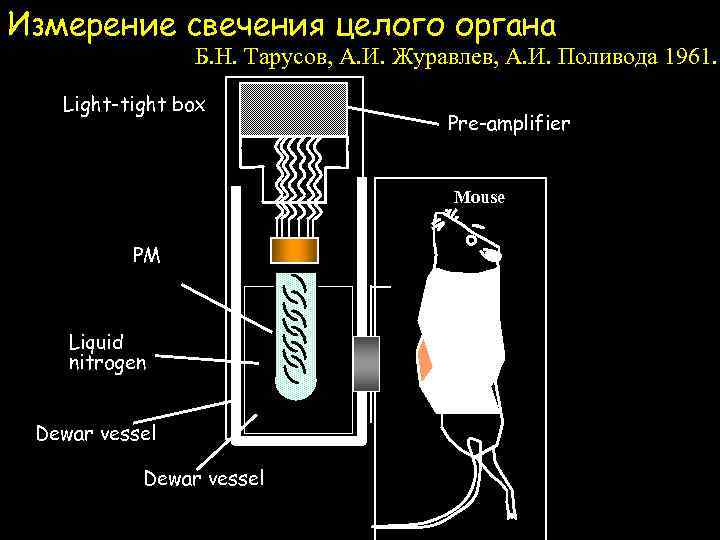 Измерение свечения целого органа Б. Н. Тарусов, А. И. Журавлев, А. И. Поливода 1961. Light-tight box Pre-amplifier Mouse PM Liquid nitrogen Dewar vessel
Измерение свечения целого органа Б. Н. Тарусов, А. И. Журавлев, А. И. Поливода 1961. Light-tight box Pre-amplifier Mouse PM Liquid nitrogen Dewar vessel
 Химические реакции, ответственные за сверхслабое свечение животных тканей Реакции активных форм кислорода HOOH ·OO¯ ·OH 1 O 2 Пероксид водорода Супероксид-радикал Радикал гидроксила Синглетный кислород Активные формы кислорода (АФК) Свободнорадикальное (= цепное, = перекисное) окисление липидов (= липопероксидация, = ПОЛ, = ЛПО). LOOH Гидропероксид LOO· Диоксил-радикал LO· Алкоксил радикал Реакции активных фором азота. ·NO Нитроксид ONOO¯ Пероксинитрит Активные формы липидов Активные формы азота
Химические реакции, ответственные за сверхслабое свечение животных тканей Реакции активных форм кислорода HOOH ·OO¯ ·OH 1 O 2 Пероксид водорода Супероксид-радикал Радикал гидроксила Синглетный кислород Активные формы кислорода (АФК) Свободнорадикальное (= цепное, = перекисное) окисление липидов (= липопероксидация, = ПОЛ, = ЛПО). LOOH Гидропероксид LOO· Диоксил-радикал LO· Алкоксил радикал Реакции активных фором азота. ·NO Нитроксид ONOO¯ Пероксинитрит Активные формы липидов Активные формы азота
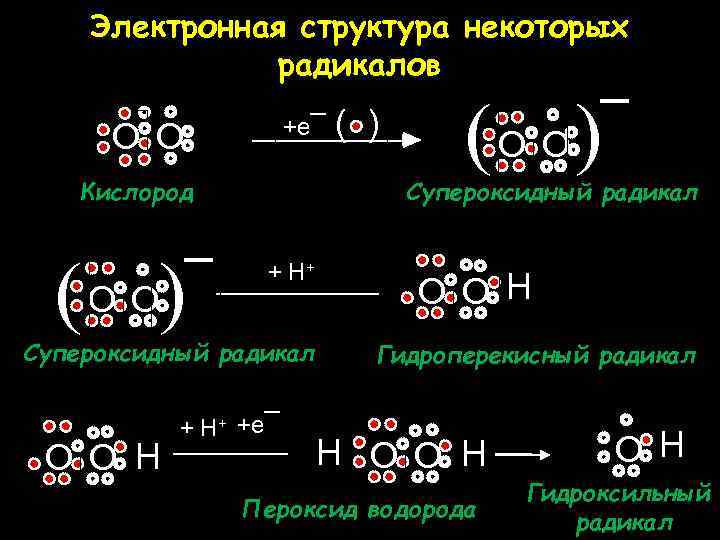 Электронная структура некоторых радикалов +e¯ O O Кислород ( ) O O ¯ ( ) ¯ O O Супероксидный радикал + H+ Супероксидный радикал O O H ( ) + H+ +e¯ O O H Гидроперекисный радикал H O O H Пероксид водорода O H Гидроксильный радикал
Электронная структура некоторых радикалов +e¯ O O Кислород ( ) O O ¯ ( ) ¯ O O Супероксидный радикал + H+ Супероксидный радикал O O H ( ) + H+ +e¯ O O H Гидроперекисный радикал H O O H Пероксид водорода O H Гидроксильный радикал
 Супероксидный радикал Основной источник супероксидных радикалов в нашем организме - клетки-фагоциты, к которым относятся гранулоциты и моноциты крови, и тканевые макрофаги. Фагоцит Встретив чужеродную частицу, например, бактерию, фагоцит прикрепляется к ней и начинает выделять активные формы кислорода, первая из которых супероксидный радикал. НАДФН + 2 О 2 НАДФ+ + 2( • О 2¯) Реакция катализируется ферментным комплексом —НАДФН оксидазой, который встроен в цитоплазматическую мембрану.
Супероксидный радикал Основной источник супероксидных радикалов в нашем организме - клетки-фагоциты, к которым относятся гранулоциты и моноциты крови, и тканевые макрофаги. Фагоцит Встретив чужеродную частицу, например, бактерию, фагоцит прикрепляется к ней и начинает выделять активные формы кислорода, первая из которых супероксидный радикал. НАДФН + 2 О 2 НАДФ+ + 2( • О 2¯) Реакция катализируется ферментным комплексом —НАДФН оксидазой, который встроен в цитоплазматическую мембрану.
 Метаболизм супероксидного радикала 1) 2 ·OO¯ + 2 H+ H 2 O 2 + 1 O 2 (Спонтанно) 2) 2 ·OO¯ + 2 H+ H 2 O 2 + 3 O 2 (Супероксиддисмутаза) 3) 1 O 2 3 O 2 + фотон (1268 нм) 4) H 2 O 2 + Cl¯ Cl. O¯ (Миелопероксидаза) 5) H 2 O 2 H 2 O + ½O 2 (Каталаза) 6) H 2 O 2 + ·OO¯ + H+ H 2 O + ·OH + 1 O 2 (Реакция Габер-Вейса) 7) H 2 O 2 + Fe 2+ HO¯ + Fe 3+ + ·OH (Реакция Фентона) 8) Cl. O¯ + Fe 2+ Cl¯ + Fe 3+ + ·OH
Метаболизм супероксидного радикала 1) 2 ·OO¯ + 2 H+ H 2 O 2 + 1 O 2 (Спонтанно) 2) 2 ·OO¯ + 2 H+ H 2 O 2 + 3 O 2 (Супероксиддисмутаза) 3) 1 O 2 3 O 2 + фотон (1268 нм) 4) H 2 O 2 + Cl¯ Cl. O¯ (Миелопероксидаза) 5) H 2 O 2 H 2 O + ½O 2 (Каталаза) 6) H 2 O 2 + ·OO¯ + H+ H 2 O + ·OH + 1 O 2 (Реакция Габер-Вейса) 7) H 2 O 2 + Fe 2+ HO¯ + Fe 3+ + ·OH (Реакция Фентона) 8) Cl. O¯ + Fe 2+ Cl¯ + Fe 3+ + ·OH
 Тестовый контроль к лекции № 5 Фамилия, имя ___________группа №_______ Задание Впишите слова Вопрос: Ответ: Задание Вопрос: Ответ: Впишите слова
Тестовый контроль к лекции № 5 Фамилия, имя ___________группа №_______ Задание Впишите слова Вопрос: Ответ: Задание Вопрос: Ответ: Впишите слова
 Тестовый контроль к лекции № 5 Фамилия, имя ___________группа №_______ Задание Впишите слова Вопрос: Ответ: Задание Вопрос: Ответ: Впишите слова
Тестовый контроль к лекции № 5 Фамилия, имя ___________группа №_______ Задание Впишите слова Вопрос: Ответ: Задание Вопрос: Ответ: Впишите слова
 Тестовый контроль к лекции № 5 Фамилия, имя ___________группа №_______ Задание Впишите слова Вопрос: Ответ: Задание Вопрос: Ответ: Впишите слова
Тестовый контроль к лекции № 5 Фамилия, имя ___________группа №_______ Задание Впишите слова Вопрос: Ответ: Задание Вопрос: Ответ: Впишите слова
 Тестовый контроль к лекции № 5 Фамилия, имя ___________группа №_______ Задание Впишите слова Вопрос: Ответ: Задание Вопрос: Ответ: Впишите формулу
Тестовый контроль к лекции № 5 Фамилия, имя ___________группа №_______ Задание Впишите слова Вопрос: Ответ: Задание Вопрос: Ответ: Впишите формулу


