Антибиотики 2.ppt
- Количество слайдов: 21

Характеристика микроорганизмов 1. Патогенность возбудителя 2. Резистентность к антибактериальному средству 3. Чувствительность к антибактериальному препарату

Патогенность – способность м/о вызывать инфекционное заболевание у человека В зависимости от степени патогенности различают: - патогенные (Shigella dysenteriae, Yersinia pestis и т. д. ) - условно – патогенные (клебсиеллы, протей, цитробактеры, серрации, энтеробактеры, уреаплазмы и т. д. ) - непатогенные (бифидобактерии, молочнокислые бактерии, непатогенные штаммы Е. coliи и др. )

Резистентность бактерий 1. Природная (генетическая) - это генетически обусловленное отсутствие чувствительности м/о к антибактериальным препаратам (АМП). Является причиной абсолютной неэффективности АМП Данный вид устойчивости м/о легко прогнозируется.

Резистентность бактерий 2. Приобретенная возникает в результате мутации отдельных штаммов бактерий и селекции устойчивых клонов или в результате внехромосомного (плазмидного) обмена генетической информацией между отдельными бактериальными клетками.

Приобретенная резистентность: - Первичная – до начала лечения АБП - Вторичная – на фоне лечения АБП Сложно прогнозировать. Эффективность АБП слабо предсказуема.

Приобретенная резистентность: ♦ Перекрестная – в пределах одной группы АМП: - полная - частичная ♦ Ассоциированная – между различными группами АМП

Механизмы формирования антибиотикорезистентности 1. Нарушение проницаемости клеточной стенки м/о для АМП - модификация пориновых каналов (для тетрациклина, аминогликозидов) 2. Ферментативная инактивация АМП продукция бактериями ферментов, разрушающих АМП (для бета-лактамных антибиотиков, макролидов, аминогликозидов, линкозамидов, хлорамфеникола)

Механизмы формирования антибиотикорезистентности Модификация мишени действия АМП клеточных структур (для беталактамов, гликопептидов, макролидов, хинолонов/фторхинолонов, сульфаниламидов) 4. Активное выведение АМП из микробной клетки - эффлюкс (для тетрациклина, макролидов, хинолонов) 5. Формирование метаболического «шунта» (сульфаниламиды) 3.

Категории чувствительности м/о ♦ Чувствительный: - рост возбудителей прекращается при терапевтических концентрациях лекарств в крови и др. тканях; - у микроорганизма нет механизмов резистентности к АМП (МПК соответствует терапевтической концентрации препарата в крови) - при лечении стандартными дозами АБП инфекций, вызванных этим возбудителем, отмечается

Категории чувствительности м/о ♦ Умеренно чувствительный - для угнетения роста микроорганизмов требуются максимальные дозы лекарственного препарата

Категории чувствительности м/о ♦ Резистентный или устойчивый: - бактериостатический эффект может быть достигнут только in vitro при высоких концентрациях ЛП, являющихся токсичными для человека. - м/о имеют механизмы резистентности к данному ЛП. - при лечении инфекции терапевтическими дозами клинического эффекта нет или эффект есть, но только от очень высоких доз АБП ( «убивая» микроорганизм,

Методы оценки чувствительности возбудителей: • Метод разведения - наименьшая концентрация антибиотика (in vitro), внесенного в агар или питательный бульон, способная вызвать подавление видимого роста микроорганизма • Диско-диффузионный метод - измерение зоны подавления роста микроорганизма на чашке Петри с агаром вокруг диска, содержащего определенное количество антибиотика. По размеру подавления зоны роста все штаммы м/о подразделяют на: - чувствительные, - умеренно- резистентные, - резистентные к данному антибиотику.

Современные проблемы антибиотикорезистентности в популяции Микроорганизмы Резистентность к АБП Str. pneumoniae Аминогликозиды, макролиды, тетрациклины, хлорамфеникол, ко-тримоксазол Str. pyogenes Макролиды, тетрациклины Haem. influenzaе Ампициллин, Ко-тримоксазол, тетрациклины, хлорамфеникол Neis. gonorr. Ампициллин, ципрофлоксацин. ко-тримоксазол Escherichia coli Ко-тримоксазол, амоксициллин, тетрациклин, Shigella spp. Хлорамфеникол, ко-тримоксазол, тетрациклин, ампициллин

Устойчивость в стационаре Микроорганизмы Резистентность Staphylococcus Оксациллин, в перспективе Ванкомицин Enterococcus Ампициллин, Гентамицин, в перспективе Ванкомицин Klebsiella, E. coli Цефалоспорины, Ps. aerugnosa Ципрофлоксацин Имипенем
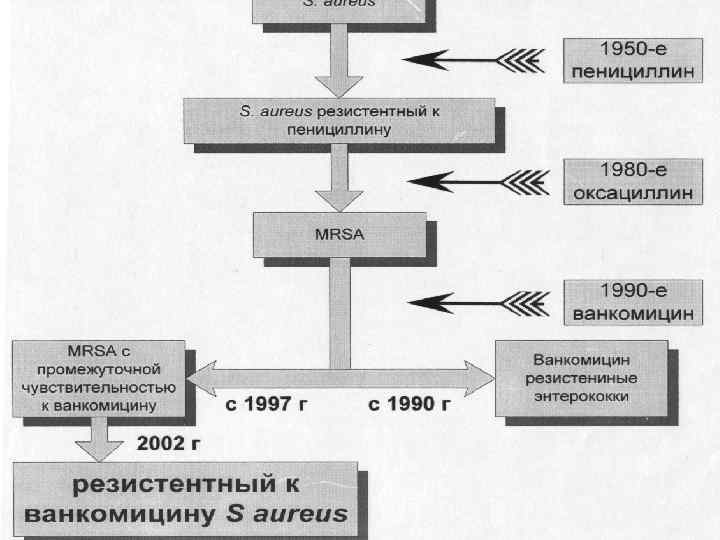

Staphylococcus aureus Аминогликозиды, тетрациклины, котримоксазол – Умеренно активны Фторхинолоны II поколения (ципрофлоксацин, офлоксацин) – Уступают «новым» (фторхинолонам III и IV поколений) Бета-лактамы – средства выбора – Оксациллин – Защищенные пенициллины – Цефалоспорины II

Streptococcus pneumoniae Высокая частота резистентности в России к коримоксазолу и тетрациклинам (>50%). Снижение активности макролидов, фторхинолонов II поколения. Высокая активность фторхинолонов III и IV поколений

Enterobacteriaceae Аминогликозиды, фторхинолоны II поколения высоко активны, эффективны Средства выбора – Защищенные пенициллины – Цефалоспорины III и IV поколений

Enterococcus обладают природной резистентностью к - аминогликозидам - цефалоспоринам - макролидам Большинство энтерококков сравнительно • чувствительны (устойчивы) к пенициллину, • ампициллину, ванкомицину (в обычных • дозах действуют лишь бактериостатически).

Enterococcus • E. faecium резистентен к большинству АБП, кроме гликопептидов (ванкомицин) и линезолида • большинство штаммов E. fecalis чувствительны к пенициллину и ампициллину

Pseudomonas aeruginosa • Степень активности АМП in vitro: меропенем>имипенем>цефтазидим>ципр офлоксацин=цефепим>>амикацин>тобр амицин>офлоксацин=цефоперазон=пип ерациллин/тазобактам>гентамицин Между карбапенемами (меропенем, имипенем) может отсутствовать перекрестная резистентность
Антибиотики 2.ppt