Лекция d-элементы (2).pptx
- Количество слайдов: 50

ХАРАКТЕРИСТИКА D-ЭЛЕМЕНТОВ

Из общего числа известных в настоящее время элементов в периодической таблице Менделеева 32 являются dэлементами. d-элементы появляются в 4 -ом периоде периодической системы. Эти элементы имеют на внешней энергетическом уровне 2 или 1 – S ē и различаются числом электронов на соседнем с внешним уровне. По мере увеличения порядкового номера у d-элементов происходит достройка уровня соседнего с внешним dэлектронами.

Все d-элементы являются металлами, степени окисления которых в соединениях различны. Их наибольшая степень окисления отвечает номеру группы, в которой расположен элемент (кроме Cu, у которого высшая степень окисления +2, Аu, у которого высшая степень окисления +3) Валентность d-элементов определяется как S-электронами внешнего уровня, так и d- электронами энергетического уровня предшествующего внешнему.

Высшие оксиды d-элементов с V по VIII группы обладают кислотными свойствами, низшие – основными, промежуточные - амфотерными. Так, оксид Mn (Mn. O) – основной, диоксид (Mn. O 2) – амфотерный, а триоксид Mn. O 3 и Mn 2 O 7 - кислотные оксиды.

Способность к кислотообразованию и степень диссоциации кислородных кислот у d-элементов увеличивается также как у S и p-элементов – слева направо и снизу вверх в периодической системе. У d-элементов имеются свободные d, S или p – орбитали. Число их может увеличиваться за счет спаривания одиночных электронов d-орбиталей. Катионы и атомы этих элементов могут являться акцепторами неподеленных e (электронных пар), чем и объясняется склонность d-элементов к комплексообразованию.

Для большинства d-элементов характерной особенностью является то, что их соединения окрашены. Эта особенность связана с тем, что возбуждение d-элементов при образовании соединений происходит благодаря поглощению квантов света видимой области спектра.

Элементы VI группы. Свойства хрома и его соединений.

Общая характеристика К VI группе относятся: Хром (Cr), элементы VI В группы Молибден (Mo), (побочная подгруппа). Вольфрам (W). Электронные формулы: Ø Cr - 1 S 22 p 63 S 23 p 64 S 13 d 5 - (провал электрона). Ø Mo [Kr] - 5 S 14 d 5 Ø W [Хе] - 6 S 25 d 4


Надо отметить, что энергия ионизации увеличивается сверху вниз. Вольфрам вследствие лантаноидного сжатия имеет атомный и ионный радиус близкий к молибдену. Поэтому молибден и вольфрам по своим свойствам ближе друг к другу, чем к хрому. Активность в подгруппе уменьшается от хрома к вольфраму в отличие от главных подгрупп. В соединениях Сr, Mo, W проявляют все степени окисления от 0 до +6.

Характерные степени окисления для хрома +3, в меньшей степени - +6. У Mo и W наиболее характерна высшая степень окисления +6. В пределах подгруппы наблюдается тенденция к снижению окислительной активности соединений со степенью окисления +6. Так, если Cr+6 O 3 - очень сильный окислитель, то Mo. O 3 уже слабый окислитель. Сr, Mo, W – белые блестящие металлы. Они очень тверды и тугоплавки.

Химически при комнатной температуре эти элементы мало реакционноспособны. В реакцию с O 2, галогенами, S, N, P, Si вступают только при нагревании. Концентрация HNO 3 быстро окисляет их поверхность и образовавшаяся пленка оксида защищает металл от дальнейшего её воздействия, т. е. происходит (пассивация) Me.

Надо отметить, что Сr растворяется в разбавленных растворах HCl, H 2 SO 4, а Mo и W – в горячей HNO 3 и «царской водке» .

Хром.

Хром был открыт в 1797 году Н. Вокеленом. Хром содержится в земной коре (0, 02%), в природе встречается главным образом в виде хромистого железняка Fe(Cr. O 2)2 (богатые месторождения на Урале, Казахстане).

При восстановлении хромита железа углем получают сплав железа с хромом – феррохром: Fe(Cr. O 2)2 + 4 C Fe + 2 Cr + 4 CO феррохром Для получения чистого хрома сначала получают Cr 2 O 3 (III), а затем восстанавливают его алюмотермическим способом: Cr 2 O 3 + 2 Al 2 Cr + Al 2 O 3

Хром как простое вещество это тугоплавкий металл, серо-стального цвета, ковок, тягуч, образует очень большое количество сплавов с различными металлами. При комнатной температуре хром стоек к воде и к воздуху. Разбавленные кислоты HCl и H 2 SO 4 растворяют его: Cr + 2 HCl Cr. Cl 2 + H 2 Cr + H 2 SO 4 Cr. SO 4 + H 2

HNO 3 быстро окисляет поверхность Cr и пассивирует его. Пленка оксида на поверхности хрома возникает в различных окислительных средах. Поэтому хром хорошо сопротивляется коррозии. Cr образует три оксида: Cr. O (II) – основного характера Cr 2 O 3 (III) – амфотерного характера Cr. O 3 (VI) – кислотный оксид Степени окисления проявляет +2, +3, +6 – устойчивые соединения.

Соединения Cr(II) можно получить: Cr + 2 HCl Cr. Cl 2 + H 2 Cr+2 неустойчивые в водной среде соединения и быстро окисляются кислородом воздуха в Cr+3: 4 Cr. Cl 2 + 4 HCl + O 2 4 Cr. Cl 3 + 2 H 2 O

Для Cr (II) характерен Cr(OH)2, который образуется: Cr. Cl 2 + 2 Na. OH Cr(OH)2 + 2 Na. Cl желт. цв. Cr(OH)2 взаимодействует только с кислотами и кислотными оксидами Cr(OH)2 + 2 HCl Cr. Cl 2 + 2 H 2 O Cr(OH)2 + SO 3 Cr. SO 4 + H 2 O
![Cr 2+ образует аквакомплексные соединения [Cr(H 2 O)6]2+, в состав которых входит ион гексааквахрома Cr 2+ образует аквакомплексные соединения [Cr(H 2 O)6]2+, в состав которых входит ион гексааквахрома](https://present5.com/presentation/82707496_126795232/image-21.jpg)
Cr 2+ образует аквакомплексные соединения [Cr(H 2 O)6]2+, в состав которых входит ион гексааквахрома (II), придающий раствору синюю окраску.

Соединения Cr (III). Одним из соединений хрома (III) является Cr 2 O 3 – оксид хрома (III) - тугоплавкое вещество зеленого цвета, применяется для приготовления клеевой и масляной красок служит для окраски стекла и фарфора. Cr 2 O 3 – амфотерный оксид. Получают: t (NH 4)Cr 2 O 7 Cr 2 O 3 + N 2 + 4 H 2 O t 2 Cr(OH)3 Cr 2 O 3 + 3 H 2 O

Следующее соединение, характерное для Cr(III) это Cr(OH)3 Получают: Cr. Cl 3 + 3 Na. OH Cr(OH)3 + 3 Na. Cl Cr(OH)3 – амфотерное основание, выпадает в виде осадка синевато-серого цвета.
![Cr(OH)3 растворяется в кислотах с образованием аквакатионных комплексов [Cr(H 2 O)6]3+ фиолетового цвета: Cr(OH)3 Cr(OH)3 растворяется в кислотах с образованием аквакатионных комплексов [Cr(H 2 O)6]3+ фиолетового цвета: Cr(OH)3](https://present5.com/presentation/82707496_126795232/image-24.jpg)
Cr(OH)3 растворяется в кислотах с образованием аквакатионных комплексов [Cr(H 2 O)6]3+ фиолетового цвета: Cr(OH)3 + 3 HCl + 3 H 2 O [Cr (H 2 O)6] Cl 3 и в щелочах с образованием гидроксохроматов зеленого цвета: Cr(OH)3 + 3 Na. OH Na 3[Cr(OH)6] Из этих реакций видно, что хром в комплексных соединениях имеет к. ч = 6

Хромиты, полученные при сплавлении Cr 2 O 3 (III) с оксидами щелочных металлов, щелочами представляют собой соли метахромистой кислоты: HCr. O 2 Na. Cr. O 2 Cr(OH)3 H 3 Cr. O 3 HCr. O 2 орто мета форма [Cr(H 2 O)6]3+ Cr 3+ - 4 S 03 d 3 4 p 4 s 4 d 3 d

Теперь посмотрим, а окрашены ли эти комлексы? d d d гибридизация d 2 Sp 3 внутриорбитальный комплекс, возможен переход d – электронов, комплекс окрашен.
![Окраска комплексов связана с изомерией – гидратная изомерия хрома: Ø [Cr(H 2 O)6]Cl 3 Окраска комплексов связана с изомерией – гидратная изомерия хрома: Ø [Cr(H 2 O)6]Cl 3](https://present5.com/presentation/82707496_126795232/image-27.jpg)
Окраска комплексов связана с изомерией – гидратная изомерия хрома: Ø [Cr(H 2 O)6]Cl 3 – сине-фиолетовая Ø [Cr(H 2 O)5 Cl]H 2 OCl 2 – светло-зеленая Ø [Cr(H 2 O)4 Cl 2]Cl(H 2 O)2 – темно-зеленая Дигидрат хлорид дихлоротетрааква хрома (III)

Для Cr(III) характерно образование солей с сильными кислотами Cr. Cl 3; Cr 2(SO 4)3. Из солей Cr(III) самой распространенной солью является хромокалиевые квасцы – КCr 2(SO 4)2*12 H 2 O – синефиолетовые кристаллы, используемые в кожевенной и текстильной промышленности. Эти соли Cr(III) подвергаются гидролизу по катиону.

Со слабыми кислотами Cr(III) солей не образует. При попытке получить в водном растворе обменной реакцией Cr 2(CO 3)3 вследствие гидролиза выделяется Cr(OH)3 в осадок. 2 Cr. Cl 3 + 3 Na 2 CO 3 + 3 H 2 O 2 Cr(OH)3 + 6 Na. Cl + 3 CO 2 Cr. Cl 3 Cr 3+ + 3 Cl- [Cr(H 2 O)6]3+ + H 2 O [Cr(H 2 O)5 OH]2+ + H 3 O+
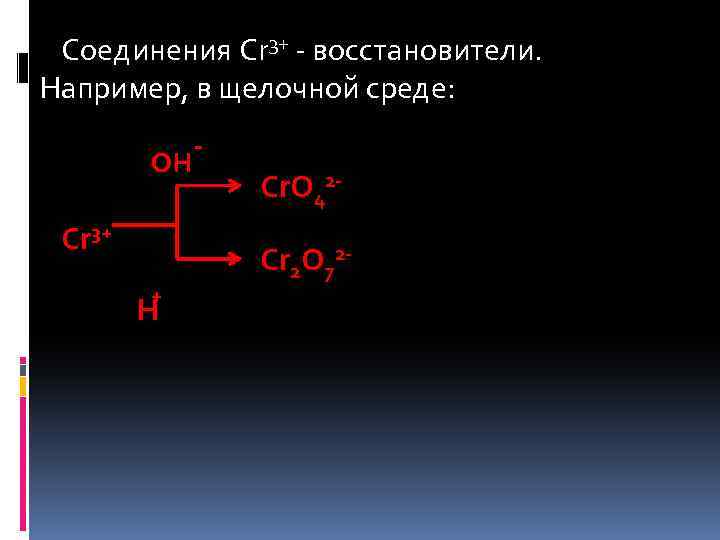
Соединения Cr 3+ - восстановители. Например, в щелочной среде: - OH Cr 3+ H Cr. O 42 Cr 2 O 72 -
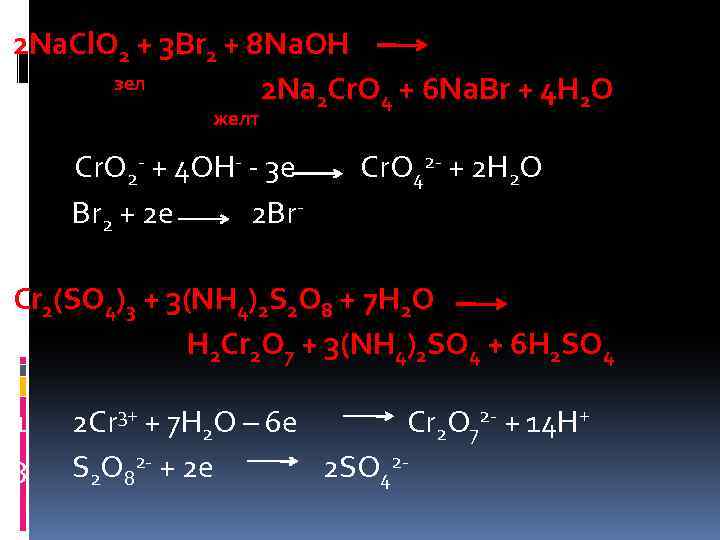
2 Na. Cl. O 2 + 3 Br 2 + 8 Na. OH зел 2 Na Cr. O + 6 Na. Br + 4 H O 2 4 2 желт 2 Cr. O 2 - + 4 OH- - 3 e Cr. O 42 - + 2 H 2 O 3 Br 2 + 2 e 2 Br. Cr 2(SO 4)3 + 3(NH 4)2 S 2 O 8 + 7 H 2 O H 2 Cr 2 O 7 + 3(NH 4)2 SO 4 + 6 H 2 SO 4 1 2 Cr 3+ + 7 H 2 O – 6 e Cr 2 O 72 - + 14 H+ 3 S 2 O 82 - + 2 e 2 SO 42 -

Соединения Cr (VI) Важнейшими соединениями Cr(VI) являются Cr. O 3 – оксид хрома (VI) – хромовый ангидрид – кристаллическое вещество темно-красного цвета и соли отвечающих его кислот: Ø H 2 Cr. O 4 – хромовая кислота Ø H 2 Cr 2 O 7 – двухромовая кислота Обе кислоты существуют только в водном растворе, но соли их достаточно стойки.

Соли хромовой кислоты – хроматы, двухромовой – дихроматы. Хроматы – желтого цвета, дихроматы – оранжевого. При подкислении раствора соли K 2 Cr. O 4 чисто желтая окраска раствора сменяется на оранжевую, вследствие перехода ионов Cr. O 42 - в ионы Cr 2 O 72 -. Из полученного раствора можно выделить соль K 2 Cr 2 O 7 в виде оранжево-красных кристаллов.

Переход выражается уравнением: 2 Cr. O 42 - + 2 H+ Cr 2 O 72 - + H 2 O Реакция обратима. Это значит, что при растворении дихроматов образуется хотя и незначительное кол-во H+ и Cr. O 42 -.

Если к раствору дихромата прибавить гидроксид, то OH- - ионы будут связывать находящиеся в растворе H+, равновесие смещается и в результате дихромат превращается в хромат Cr 2 O 72 - + 2 OH- 2 Cr. O 42 - + H 2 O Следовательно, хроматы устойчивы в щелочной среде, дихроматы – в кислой.

Хроматы щелочных металлов получаются путем окисления соединений Cr(III) в присутствии щелочи. Например, при действии брома на раствор хромита натрия (реакция выше) или сплавлением соединений Cr(III) с окислительными щелочными смесями: t Cr 2(SO 4)3 + 3 KNO 3 + 5 K 2 CO 3 зел 2 K Cr. O + 3 K SO + 3 KNO + 5 CO 2 4 2 2 желт

Хроматы щелочных металлов хорошо растворимые в воде соединения. Растворимость хроматов щелочноземельных металлов уменьшается. Хроматы и дихроматы – сильные окислители K 2 Cr 2 O 7(30 г) + H 2 SO 4 (1 л) – хромпик

В кислых и щелочных растворах соединения хрома (III) и Cr(VI) существуют в разных формах: кислая среда – Cr 3+ или Cr 2 O 72 щелочная среда – Cr. O 2 -, [Cr(OH)6]3 - или Cr. O 42 Поэтому взаимопревращение соединений Cr(III) и Cr(VI) протекает поразному в зависимости от реакции раствора

K 2 Cr 2 O 7 + 3 H 2 S + 4 H 2 SO 4 оранжевый Cr (SO ) + 3 S + K SO + 7 H O 2 4 3 2 4 2 зеленый 1 Cr 2 O 72 - + 14 H+ + 6 e 2 Cr 3++ + 7 H 2 O 3 H 2 S + 2 e S 0 + 2 H+ Cr 2 O 72 - + 14 H+ + 3 H 2 S 2 Cr 3+ + 7 H 2 O + 3 S 0 + 6 H+ Часто взаимодействие ионов Cl и Cl 2 O 7 принимают за окислительновосстановительную реакцию.

K 2 Cr 2 O 7 + 2 HCl 2 KCr. O 3 Cl + H 2 O оран. крист. хлорхромата калия K 2 Cr 2 O 7 + 6 HCl 2 KCl + 2 Cr. O 2 Cl 2 + 3 H 2 O хлористый хромил неполный хлорангидрид

Для хрома известны пероксосоединения: Cr. O 5 – пероксид хрома - неустойчивое соединение, хранят в эфире, яд. O O Cr O
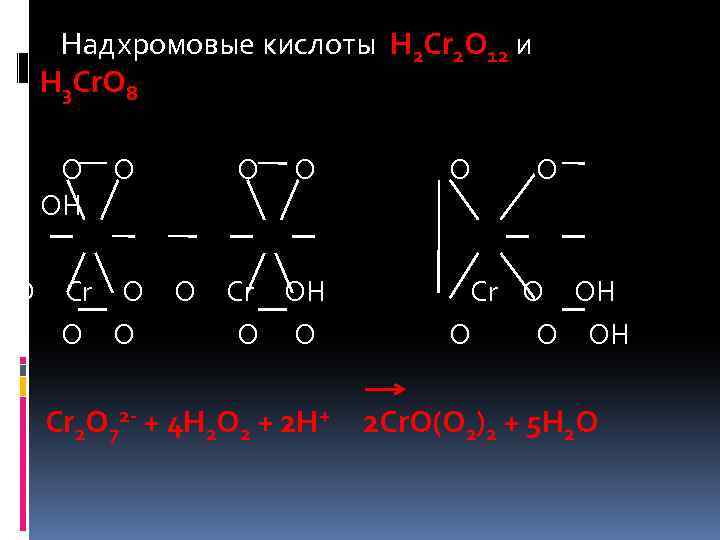
Надхромовые кислоты H 2 Cr 2 O 12 и H 3 Cr. O 8 O O O O OH O Cr OH Cr O OH O O O O OH Cr 2 O 72 - + 4 H 2 O 2 + 2 H+ 2 Cr. O(O 2)2 + 5 H 2 O

Cr. O 5 – неустойчивое соединение в воде, поэтому в реакционную смесь добавляют диэтиловый эфир или амиловый спирт. Cr. O 5 переходит в слой растворителя, что сильно повышает его устойчивость. Образование надхромовой кислоты является качественной реакцией на фармакопейные лекарственные препараты раствора перекиси водорода.

Биологическая роль хрома и молибдена.

Хром входит в состав крови, головного мозга, молока, фермента пепсина. При его недостатке замедляется рост животных, начинается заболевание глаз, нарушается углеводный обмен.

При недостаточном поступлении его с пищей, уменьшается чувствительность тканей к действию гормона поджелудочной железы-инсулину, ухудшаеся усвоение глюкозы, увеличивается концентрация липидов и атеросклеротических бляшек в аорте, уменьшается оплодотворяющая способность.

Хром применяется в сплавах для изготовления медицинских инструментов – хирургических ножей, скальпелей, для изготовления зубных коронок, игл, стерилизаторов. Дихроматы используются для получения некоторых ЛСК препаратов, например, бензойной кислоты, камфары. Дихроматометрия применяется для количественного определения лекарственных веществ, обладающих cвойствами восстановителей.

Фототурбидиметрия (использование реакции взаимодействия фосфорновольфрамовой кислоты с аминосоединениями с образованием дисперсной системы).

Молибден жизненно необходимый элемент, входит в состав 7 ферментов (ксантиндегидрогеназа, ксантиноксидаза, альдогидроксидаза и др. ) При дефиците молибдена возникает ксантинурия, при этом уменьшается содержание мочевой кислоты в сыворотке крови и моче. При избытке молибденоз, характеризующийся анемией, гипотонией, лейкопенией.

Лекция d-элементы (2).pptx