 Характеристические функции Термодинамические потенциалы
Характеристические функции Термодинамические потенциалы
 Характеристические функции. № Термодинамические потенциалы Энтальпия Энергия Гельмгольца Энергия Гиббса
Характеристические функции. № Термодинамические потенциалы Энтальпия Энергия Гельмгольца Энергия Гиббса
 Наибольшее значение имеют четыре термодинамических потенциала: 1) внутренняя энергия U(S, V), 2) энтальпия H(S, p) = U + p. V, 3) энергия Гельмгольца F(T, V) = U - TS, 4) энергия Гиббса G(T, p) = H - TS = F + p. V.
Наибольшее значение имеют четыре термодинамических потенциала: 1) внутренняя энергия U(S, V), 2) энтальпия H(S, p) = U + p. V, 3) энергия Гельмгольца F(T, V) = U - TS, 4) энергия Гиббса G(T, p) = H - TS = F + p. V.
 Потенци Естественные само- Условия ал переменные произво равновесия льные U S = const, V = d. U < 0 d. U = 0, d 2 U > 0 const H S = const, p = d. H < 0 d. H = 0, d 2 H > 0 const F T = const, V = d. F < 0 d. F = 0, d 2 F > 0 const G T = const, p = d. G < 0 d. G = 0, d 2 G > 0 const
Потенци Естественные само- Условия ал переменные произво равновесия льные U S = const, V = d. U < 0 d. U = 0, d 2 U > 0 const H S = const, p = d. H < 0 d. H = 0, d 2 H > 0 const F T = const, V = d. F < 0 d. F = 0, d 2 F > 0 const G T = const, p = d. G < 0 d. G = 0, d 2 G > 0 const
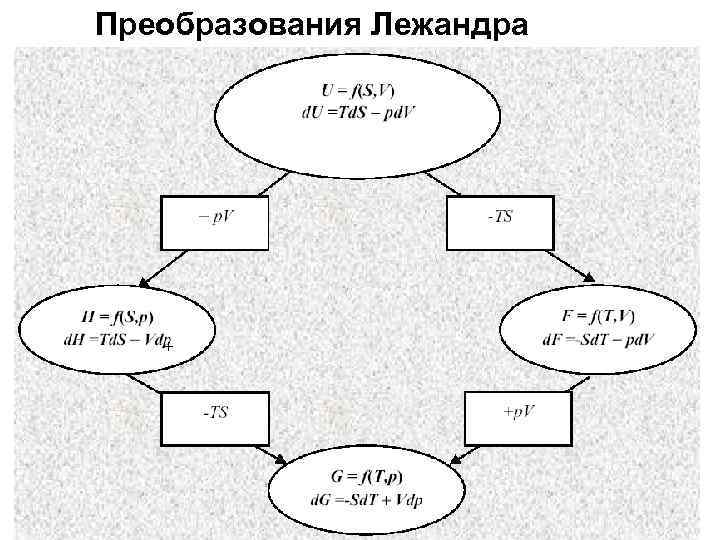 Преобразования Лежандра +
Преобразования Лежандра +
 При постоянстве естественных переменных характеристических функций (термодинамических потенциалов) их изменения обусловлены только химической природой системы и протекающих в ней реакций
При постоянстве естественных переменных характеристических функций (термодинамических потенциалов) их изменения обусловлены только химической природой системы и протекающих в ней реакций
 Определение химического потенциала
Определение химического потенциала
 xi – мольная доля mi (сi) – моляльная (молярная) к-ция pi – парциальное давление i-того компонента
xi – мольная доля mi (сi) – моляльная (молярная) к-ция pi – парциальное давление i-того компонента
 Произведение реакции (ПР)
Произведение реакции (ПР)
![>Выбор стандартного состояния: Все [Xi] = 1 Тогда, ln(ПР) = 0 >Выбор стандартного состояния: Все [Xi] = 1 Тогда, ln(ПР) = 0](https://present5.com/presentation/3/38046442_139922268.pdf-img/38046442_139922268.pdf-12.jpg) Выбор стандартного состояния: Все [Xi] = 1 Тогда, ln(ПР) = 0
Выбор стандартного состояния: Все [Xi] = 1 Тогда, ln(ПР) = 0
 II. Стандартная энергия реакции Гиббса (Стандартная)
II. Стандартная энергия реакции Гиббса (Стандартная)
 Состояние равновесия: r. G = 0 =K
Состояние равновесия: r. G = 0 =K
 Химическая переменная - a 1 A 1 + a 2 A 2 + … b 1 B 1 + b 2 B 2+ …
Химическая переменная - a 1 A 1 + a 2 A 2 + … b 1 B 1 + b 2 B 2+ …
 Фундаментальные уравнения Гиббса
Фундаментальные уравнения Гиббса










![Выбор стандартного состояния: Все [Xi] = 1 Тогда, ln(ПР) = 0 Выбор стандартного состояния: Все [Xi] = 1 Тогда, ln(ПР) = 0](https://present5.com/presentation/3/38046442_139922268.pdf-img/38046442_139922268.pdf-12.jpg)














![Выбор стандартного состояния: Все [Xi] = 1 Тогда, ln(ПР) = 0 Выбор стандартного состояния: Все [Xi] = 1 Тогда, ln(ПР) = 0](https://present5.com/presentation/3/38046442_139922268.pdf-img/38046442_139922268.pdf-12.jpg)



