Опыты Вода.Растворы..pptx
- Количество слайдов: 18



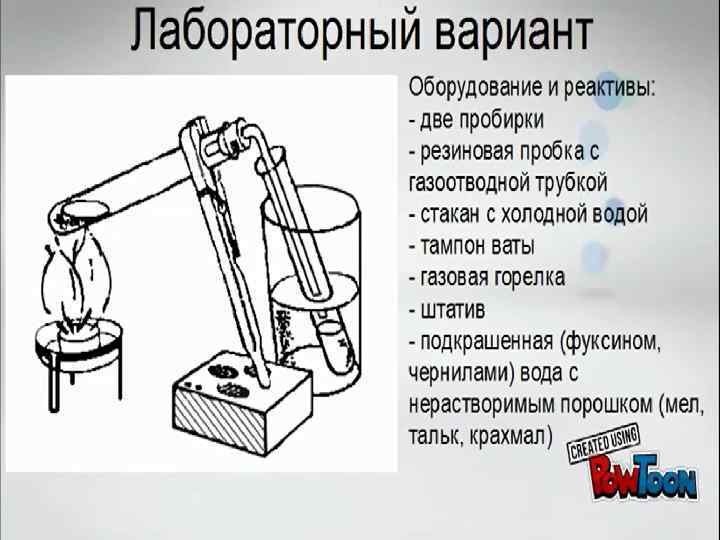




 Взаимодействие щелочных и щелочно-земельных металлов с водой I. Литий Оборудование: чашка Петри, лучинка. Реактивы: литий, вода, фенолфталеин. Ход работы: 1) Наливаем в простоквашницу воду, добавив фенолфталеин 2) Достаем литий из парафина, в котором он хранится; 3) Отрезаем скальпелем маленький кусочек лития; 4) Кладем его в воду, наблюдаем , что литий «бегает» по воде, так как его толкает выделяющийся водород. Кусочек лития не плавится. 2 Li+2 H 2 O=2 Li. OH+H 2↑ 5) Лучинкой поджигаем выделяющийся газ, наблюдаем пламя ярко-красного цвета.
Взаимодействие щелочных и щелочно-земельных металлов с водой I. Литий Оборудование: чашка Петри, лучинка. Реактивы: литий, вода, фенолфталеин. Ход работы: 1) Наливаем в простоквашницу воду, добавив фенолфталеин 2) Достаем литий из парафина, в котором он хранится; 3) Отрезаем скальпелем маленький кусочек лития; 4) Кладем его в воду, наблюдаем , что литий «бегает» по воде, так как его толкает выделяющийся водород. Кусочек лития не плавится. 2 Li+2 H 2 O=2 Li. OH+H 2↑ 5) Лучинкой поджигаем выделяющийся газ, наблюдаем пламя ярко-красного цвета.
 II. Натрий Оборудование: чашка Петри, пинцет, фильтровальная бумага. Ход работы: а) Приготовим дистиллированную воду и добавим к воде фенолфталеина. Фенолфталеин изменит окраску, когда в растворе появится щелочь. Счищаем оксидную пленку и опускаем натрий в воду. Металл бурно взаимодействует с водой. Выделяется газообразный водород. Фенолфталеин становится малиновым: в растворе образовалась щелочь - едкий натр. 2 Na + 2 H 2 O = 2 Na. OH + H 2 ↑ б) На поверхность воды положить кусочек фильтровальной бумаги и на нее кусочек металла. Происходит 2 процесса: 1) 2) 2 Na + 2 H 2 O = 2 Na. OH + H 2 ↑ 2 Na + O 2 = Na 2 O 2 + 2 H 2 O = 2 Na. OH + H 2 O 2 = H 2 O + O 2 ↑
II. Натрий Оборудование: чашка Петри, пинцет, фильтровальная бумага. Ход работы: а) Приготовим дистиллированную воду и добавим к воде фенолфталеина. Фенолфталеин изменит окраску, когда в растворе появится щелочь. Счищаем оксидную пленку и опускаем натрий в воду. Металл бурно взаимодействует с водой. Выделяется газообразный водород. Фенолфталеин становится малиновым: в растворе образовалась щелочь - едкий натр. 2 Na + 2 H 2 O = 2 Na. OH + H 2 ↑ б) На поверхность воды положить кусочек фильтровальной бумаги и на нее кусочек металла. Происходит 2 процесса: 1) 2) 2 Na + 2 H 2 O = 2 Na. OH + H 2 ↑ 2 Na + O 2 = Na 2 O 2 + 2 H 2 O = 2 Na. OH + H 2 O 2 = H 2 O + O 2 ↑
 III. Калий Оборудование: стакан, воронка. Реактивы: калий, вода, фенолфталеин. Ход работы: Стакан 0, 5 л заполнить на ¾ водой. Положить кусочек калия на поверхность воды и сразу же закрыть воронкой. Наблюдать фиолетовое пламя горящего калия. В конце реакции всегда происходит небольшой взрыв, поэтому нельзя снимать воронку до окончания реакции. Полученный раствор испытать фенолфталеином. 2 K+2 H 2 O = 2 KOH+H 2↑
III. Калий Оборудование: стакан, воронка. Реактивы: калий, вода, фенолфталеин. Ход работы: Стакан 0, 5 л заполнить на ¾ водой. Положить кусочек калия на поверхность воды и сразу же закрыть воронкой. Наблюдать фиолетовое пламя горящего калия. В конце реакции всегда происходит небольшой взрыв, поэтому нельзя снимать воронку до окончания реакции. Полученный раствор испытать фенолфталеином. 2 K+2 H 2 O = 2 KOH+H 2↑
 IV. Кальций Оборудование: фильтровальная бумага, напильник, марля, тигельные щипцы, цилиндр. Реактивы: кальций, вода. Ход работы: Кальций осушить фильтровальной бумагой и зачистить напильником. Завернуть кальций в марлю. Захватить тигельными щипцами и подвести под цилиндр заполненный водой. Са + 2 Н 2 О = Са(ОН)2 + Н 2 ↑
IV. Кальций Оборудование: фильтровальная бумага, напильник, марля, тигельные щипцы, цилиндр. Реактивы: кальций, вода. Ход работы: Кальций осушить фильтровальной бумагой и зачистить напильником. Завернуть кальций в марлю. Захватить тигельными щипцами и подвести под цилиндр заполненный водой. Са + 2 Н 2 О = Са(ОН)2 + Н 2 ↑
 V. Магний Оборудование: асбестовая сетка, пробирка, держатель, плитка, колба. Реактивы: вода, стружки магния Ход работы: а) На демонстрационный стол положить асбестовую сетку, на нее насыпать горку стружек магния. Приготовить пробирку с водой, закрепленной в держателе. Стружки магния поджечь. Когда магний хорошо разгорится, полить на него водой. Наблюдать образование белых «иголок» . Mg+2 H 2 O=Mg(OH) 2 ↓+H 2↑
V. Магний Оборудование: асбестовая сетка, пробирка, держатель, плитка, колба. Реактивы: вода, стружки магния Ход работы: а) На демонстрационный стол положить асбестовую сетку, на нее насыпать горку стружек магния. Приготовить пробирку с водой, закрепленной в держателе. Стружки магния поджечь. Когда магний хорошо разгорится, полить на него водой. Наблюдать образование белых «иголок» . Mg+2 H 2 O=Mg(OH) 2 ↓+H 2↑
 Магний Оборудование: асбестовая сетка, плитка, колба, ложечка. Реактивы: вода, порошок магния Ход работы: б)Асбестовую сетку положить на плитку, на нее поставить колбу с водой (плиту включить заранее, чтобы вода закипела). На ложечку поместить порошок магния, поджечь и внести в колбу. Держать ложечку над поверхностью воды, чуть касаясь воды.
Магний Оборудование: асбестовая сетка, плитка, колба, ложечка. Реактивы: вода, порошок магния Ход работы: б)Асбестовую сетку положить на плитку, на нее поставить колбу с водой (плиту включить заранее, чтобы вода закипела). На ложечку поместить порошок магния, поджечь и внести в колбу. Держать ложечку над поверхностью воды, чуть касаясь воды.
 Магний Оборудование: пробирка, тюльпанообразная воронка, 2 спиртовки, тарелка, штатив, картонная лопаточка. Реактивы: речной песок, порошок магния. Ход работы: в) В пробирку положить немного речного песка (1, 5 см) через тюльпанообразную воронку налить воду, чтобы смочить песок, вынуть резко воронку( не намочив края). Закрепить пробирку в лапке штатива над тарелкой с песком. С помощью картонной лопаточки поместить в пробирку магний. Нагреваем магний активно, а воду слегка. Когда магний раскалится, начинаем активно нагревать воду. Образующийся водород загорается. Mg + H 2 O = Mg. O + H 2↑
Магний Оборудование: пробирка, тюльпанообразная воронка, 2 спиртовки, тарелка, штатив, картонная лопаточка. Реактивы: речной песок, порошок магния. Ход работы: в) В пробирку положить немного речного песка (1, 5 см) через тюльпанообразную воронку налить воду, чтобы смочить песок, вынуть резко воронку( не намочив края). Закрепить пробирку в лапке штатива над тарелкой с песком. С помощью картонной лопаточки поместить в пробирку магний. Нагреваем магний активно, а воду слегка. Когда магний раскалится, начинаем активно нагревать воду. Образующийся водород загорается. Mg + H 2 O = Mg. O + H 2↑

 Опыт «Примораживание стакана» Оборудование: стакан, деревянная дощечка, стеклянная палочка. Реактивы: вода, нитрат аммония. Ход работы: В тонкостенный стаканчик объемом 50 мл с плоским (не вогнутым внутрь) дном наливают 1/3 воды и ставят его на деревянную дощечку. Под дно стаканчика наливают немного воды (d капли ≈ 2, 5 см), высыпают в стаканчик с налитой в него водой измельченный нитрат аммония и перемешивают стеклянной палочкой, придерживая стаканчик рукой, чтобы не сдвигать его с места.
Опыт «Примораживание стакана» Оборудование: стакан, деревянная дощечка, стеклянная палочка. Реактивы: вода, нитрат аммония. Ход работы: В тонкостенный стаканчик объемом 50 мл с плоским (не вогнутым внутрь) дном наливают 1/3 воды и ставят его на деревянную дощечку. Под дно стаканчика наливают немного воды (d капли ≈ 2, 5 см), высыпают в стаканчик с налитой в него водой измельченный нитрат аммония и перемешивают стеклянной палочкой, придерживая стаканчик рукой, чтобы не сдвигать его с места.
 Опыт «Закипание эфира при растворении гидроксида натрия» Оборудование: пробирка, газоотводная трубка, стакан, стеклянная палочка с резиновым наконечником. Реактивы: вода, серный эфир, гидроксид натрия. Ход работы: В пробирку, снабженную пробкой с газоотводной трубкой, изогнутой наливают 2— 3 мл серного эфира. В стакан емкостью 100 мл наливают 40— 50 мл воды и осторожно всыпают около одной чайной ложки едкого натра и взбалтывают стеклянной палочкой с надетым на конце куском резиновой трубки, чтобы случайно не пробить дно стакана. В образовавшийся горячий раствор опускают пробирку с эфиром и продолжают взбалтывание. Через некоторое время эфир закипает, и пары его можно зажечь у оттянутого конца стеклянной трубки.
Опыт «Закипание эфира при растворении гидроксида натрия» Оборудование: пробирка, газоотводная трубка, стакан, стеклянная палочка с резиновым наконечником. Реактивы: вода, серный эфир, гидроксид натрия. Ход работы: В пробирку, снабженную пробкой с газоотводной трубкой, изогнутой наливают 2— 3 мл серного эфира. В стакан емкостью 100 мл наливают 40— 50 мл воды и осторожно всыпают около одной чайной ложки едкого натра и взбалтывают стеклянной палочкой с надетым на конце куском резиновой трубки, чтобы случайно не пробить дно стакана. В образовавшийся горячий раствор опускают пробирку с эфиром и продолжают взбалтывание. Через некоторое время эфир закипает, и пары его можно зажечь у оттянутого конца стеклянной трубки.


