Лекция 1 (мол сп 2015).ppt
- Количество слайдов: 62
 Взаимодействие электромагнитного излучения Свет слева нет света свет падает нормально
Взаимодействие электромагнитного излучения Свет слева нет света свет падает нормально
 • Взаимодействие электромагнитного излучения – Типы взаимодействия • • • Поглощение Отражение Пропускание Рассеяние Преломление поглощение пропускание отражение рассеяние преломление – Каждое взаимодействие может раскрыть определенные свойства материи – При применении электромагнитного излучения различной частоты можно получать различную информацию
• Взаимодействие электромагнитного излучения – Типы взаимодействия • • • Поглощение Отражение Пропускание Рассеяние Преломление поглощение пропускание отражение рассеяние преломление – Каждое взаимодействие может раскрыть определенные свойства материи – При применении электромагнитного излучения различной частоты можно получать различную информацию
 Copyright © 2010 R. R. Dickerson & Z. Q. Li 3
Copyright © 2010 R. R. Dickerson & Z. Q. Li 3
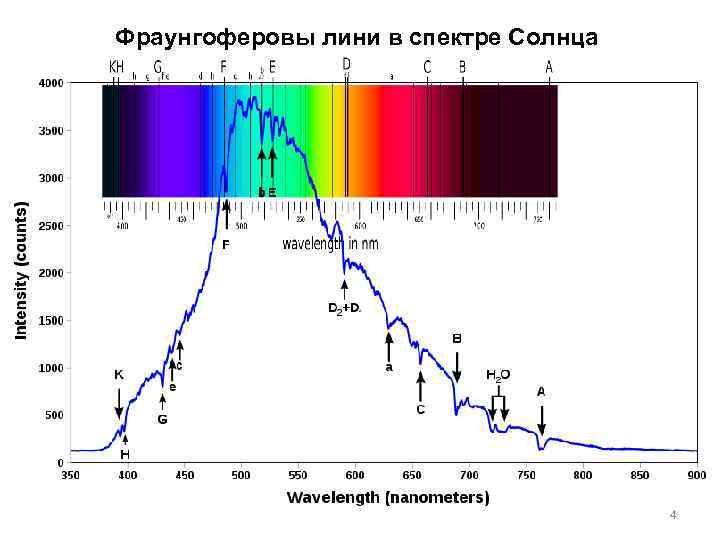 Фраунгоферовы лини в спектре Солнца 4
Фраунгоферовы лини в спектре Солнца 4
 5
5
 Copyright © 2010 R. R. Dickerson & Z. Q. Li 6
Copyright © 2010 R. R. Dickerson & Z. Q. Li 6
 Молекулярные спектры • Движение и энергия молекул – Молекулы колеблются и вращаются все время, два основных режима вибрации время • растяжение - изменение длины связи (высокие v) • изгиб - изменение угла связи (нижняя у) (другие возможные сложные типы растяжения и изгиба: ножницы / качалка / скручивания -Молекулы, как правило, находятся в основном состоянии (S 0) S (синглет) - два спин электронной пары имеют разное направление T (триплет) - два электронных спинов имеют одно и то же направление – После возбуждения молекул могут переходить на высокие E состояния (S 1, S 2, T 1 и т. д. ), которые связаны с определенными уровнями энергии – Переход от высоких состояний Е в низкие происходит засчет поглощения фотона; переход от низких до высоких состояний Е может привести к испускания фотонов v 4 v 3 v 2 v 1 S 2 S 1 T 1 v 4 v 3 v 2 v 1 S 0 v 4 v 3 v 2 v 1
Молекулярные спектры • Движение и энергия молекул – Молекулы колеблются и вращаются все время, два основных режима вибрации время • растяжение - изменение длины связи (высокие v) • изгиб - изменение угла связи (нижняя у) (другие возможные сложные типы растяжения и изгиба: ножницы / качалка / скручивания -Молекулы, как правило, находятся в основном состоянии (S 0) S (синглет) - два спин электронной пары имеют разное направление T (триплет) - два электронных спинов имеют одно и то же направление – После возбуждения молекул могут переходить на высокие E состояния (S 1, S 2, T 1 и т. д. ), которые связаны с определенными уровнями энергии – Переход от высоких состояний Е в низкие происходит засчет поглощения фотона; переход от низких до высоких состояний Е может привести к испускания фотонов v 4 v 3 v 2 v 1 S 2 S 1 T 1 v 4 v 3 v 2 v 1 S 0 v 4 v 3 v 2 v 1
 Классификация электромагнитного излучения
Классификация электромагнитного излучения
 Спектр электромагнитного излучения • Космические лучи • X-лучи Энергия • Ультрафиолетовый • Видимый • Инфракрасный • микроволны • Радио волны
Спектр электромагнитного излучения • Космические лучи • X-лучи Энергия • Ультрафиолетовый • Видимый • Инфракрасный • микроволны • Радио волны
 Спектр электромагнитного излучения Короткие длины волн ( ) Большие длины волн ( ) 400 nm 750 nm Видимый свет Высокие частоты ( ) Высокая энергия(E) Низкие частоты ( ) Низкая энергия (E)
Спектр электромагнитного излучения Короткие длины волн ( ) Большие длины волн ( ) 400 nm 750 nm Видимый свет Высокие частоты ( ) Высокая энергия(E) Низкие частоты ( ) Низкая энергия (E)
 Электромагнитное излучение V = Волновое число (cm-1) = Длина волны C = Скорость радиации (constant) = 3 x 1010 cm/sec. u = частота излучения (cycles/sec) Энергия фотона: h (константа Планка) = 6. 62 x 10 - (Erg sec) 27 C = u
Электромагнитное излучение V = Волновое число (cm-1) = Длина волны C = Скорость радиации (constant) = 3 x 1010 cm/sec. u = частота излучения (cycles/sec) Энергия фотона: h (константа Планка) = 6. 62 x 10 - (Erg sec) 27 C = u
 Spectral Properties, Application and Interactions of Electromagnetic Radiation Энергия Kcal/mol Electron volts, e. V 9. 4 x 107 4. 9 x 106 9. 4 x 103 9. 4 x 101 4. 9 x 102 4. 9 x 100 Волновое число V cm-1 3. 3 x 1010 3. 3 x 106 3. 3 x 104 Длина волны λ cm 3 x 10 -11 3 x 10 -7 3 x 10 -5 Частота υ Hz 1021 Тип Излучен ия Тип спектроскоп ии Gamma ray Гамма излучения 1017 X-ray 1015 Ультра фиолет 4. 9 x 10 -2 3. 3 x 102 3 x 10 -3 1013 9. 4 x 10 -3 4. 9 x 10 -4 3. 3 x 100 3 x 10 -1 1011 9. 4 x 10 -7 4. 9 x 10 -8 3. 3 x 10 -4 3 x 103 107 Инфрак расное электронные (внутренние оболочки) UV поглощение электронные( внешние оболочки) IR поглощение Микровол Поглощение микроволн ны Радио ядерные X-лучи поглощения Видимое 9. 4 x 10 -1 Тип Квантовых переходов Ядерный магнитный резонанс Молекулярные нык колебания вращения Магнитонавед енные спиновые
Spectral Properties, Application and Interactions of Electromagnetic Radiation Энергия Kcal/mol Electron volts, e. V 9. 4 x 107 4. 9 x 106 9. 4 x 103 9. 4 x 101 4. 9 x 102 4. 9 x 100 Волновое число V cm-1 3. 3 x 1010 3. 3 x 106 3. 3 x 104 Длина волны λ cm 3 x 10 -11 3 x 10 -7 3 x 10 -5 Частота υ Hz 1021 Тип Излучен ия Тип спектроскоп ии Gamma ray Гамма излучения 1017 X-ray 1015 Ультра фиолет 4. 9 x 10 -2 3. 3 x 102 3 x 10 -3 1013 9. 4 x 10 -3 4. 9 x 10 -4 3. 3 x 100 3 x 10 -1 1011 9. 4 x 10 -7 4. 9 x 10 -8 3. 3 x 10 -4 3 x 103 107 Инфрак расное электронные (внутренние оболочки) UV поглощение электронные( внешние оболочки) IR поглощение Микровол Поглощение микроволн ны Радио ядерные X-лучи поглощения Видимое 9. 4 x 10 -1 Тип Квантовых переходов Ядерный магнитный резонанс Молекулярные нык колебания вращения Магнитонавед енные спиновые
 Поглощение и излучение излучения Будем считать, что атом(или молекула) имеет два уровня, Ei и Ek E k Molecule in energy level Ei Ei Прямой излучательный переход между этими состояниями связан с фотоном с частотой ν: hν = ΔE = Ek – Ei Рассмотрим: Каковы возможные радиационные переходы? Какова вероятность такого перехода? Как измениться число фотонов при переходе?
Поглощение и излучение излучения Будем считать, что атом(или молекула) имеет два уровня, Ei и Ek E k Molecule in energy level Ei Ei Прямой излучательный переход между этими состояниями связан с фотоном с частотой ν: hν = ΔE = Ek – Ei Рассмотрим: Каковы возможные радиационные переходы? Какова вероятность такого перехода? Как измениться число фотонов при переходе?
 Поглощение Коэффициент Эйнштейна для поглощения B 12 • Спонтанный переход при котором атом или молекула поглощает фотон излучения • Поглощение фотона вызывает переход атома или молекулы в возбужденное состояние
Поглощение Коэффициент Эйнштейна для поглощения B 12 • Спонтанный переход при котором атом или молекула поглощает фотон излучения • Поглощение фотона вызывает переход атома или молекулы в возбужденное состояние
 Ek hν Ei «Идет» один фотон энергии hν Вероятность перехода: d. Pik/dt = Bik ρ(ν) d. Pik /dt вероятность поглощения молекулой фотонов в одну секунду Bik коэффициент Эйнштейна для вынужденного поглощения ρ(ν) спектральная плотность энергии (число фотонов частоты ν в единице объема )
Ek hν Ei «Идет» один фотон энергии hν Вероятность перехода: d. Pik/dt = Bik ρ(ν) d. Pik /dt вероятность поглощения молекулой фотонов в одну секунду Bik коэффициент Эйнштейна для вынужденного поглощения ρ(ν) спектральная плотность энергии (число фотонов частоты ν в единице объема )
 Спонтанное излучение • Статистический процесс- излучение изолированного атома или молекулы • Излучение 4π стеридиан Коэффициент Эйнштейна для спонтанного излучения A 21
Спонтанное излучение • Статистический процесс- излучение изолированного атома или молекулы • Излучение 4π стеридиан Коэффициент Эйнштейна для спонтанного излучения A 21
 Молекула с Ek спонтанно переходит на Ei излучая фотон в произвольном направлении Ek hν Ei Еще один фотон с энергией hν (произвольная фаза и направление) Вероятность перехода d. Pki/dt = Aki d. Pki /dt is вероятность излучения возбужденной молекулы в секунду Aki коэффициент Эйнштейна спонтанного излучения (или вероятность спонтанных переходов) Спонтанное излучение не зависит от присутствия других фотонов в среде
Молекула с Ek спонтанно переходит на Ei излучая фотон в произвольном направлении Ek hν Ei Еще один фотон с энергией hν (произвольная фаза и направление) Вероятность перехода d. Pki/dt = Aki d. Pki /dt is вероятность излучения возбужденной молекулы в секунду Aki коэффициент Эйнштейна спонтанного излучения (или вероятность спонтанных переходов) Спонтанное излучение не зависит от присутствия других фотонов в среде
 Стимулированное излучение Коэффициент Эйнштейна для вынужденного излучения Bul
Стимулированное излучение Коэффициент Эйнштейна для вынужденного излучения Bul
 Фотон соответствующей частоты вызывает переход от Ek hν к Ei Ek hν Ei Еще один фотон с энергией hν. Новый фотон имеет ту же частоту, фазу и направление как исходный фотон Вероятность перехода d. Pki/dt = Bki ρ(ν) d. Pki /dt есть вероятность в секунду возбужденной молекулы испускания фотона Bki является коэффициент Эйнштейна индуцированного излучения
Фотон соответствующей частоты вызывает переход от Ek hν к Ei Ek hν Ei Еще один фотон с энергией hν. Новый фотон имеет ту же частоту, фазу и направление как исходный фотон Вероятность перехода d. Pki/dt = Bki ρ(ν) d. Pki /dt есть вероятность в секунду возбужденной молекулы испускания фотона Bki является коэффициент Эйнштейна индуцированного излучения
 Соотношение между Bik и Bki: Коэффициенты Эйнштейна индуцированного поглощения и излучения непосредственно связаны через вырождение g. X, для каждого уровня х: Bik = (gk/gi) Bki В случае, когда каждый уровень имеет такое же вырождение (gi = gk), коэффициенты Эйнштейна индуцированного поглощения и испускания идентичны –Другими словами, вероятность индуцированного излучения является такой же, как индуцированного поглощения ВЫРОЖДЕНИЕ ЭНЕРГЕТИЧЕСКИХ УРОВНЕЙ — существование двух или более стационарных состояний квантовой системы (атома, молекулы) с одинаковыми значениями энергии.
Соотношение между Bik и Bki: Коэффициенты Эйнштейна индуцированного поглощения и излучения непосредственно связаны через вырождение g. X, для каждого уровня х: Bik = (gk/gi) Bki В случае, когда каждый уровень имеет такое же вырождение (gi = gk), коэффициенты Эйнштейна индуцированного поглощения и испускания идентичны –Другими словами, вероятность индуцированного излучения является такой же, как индуцированного поглощения ВЫРОЖДЕНИЕ ЭНЕРГЕТИЧЕСКИХ УРОВНЕЙ — существование двух или более стационарных состояний квантовой системы (атома, молекулы) с одинаковыми значениями энергии.


 Figure 21. 3
Figure 21. 3
 Figure 21. 4
Figure 21. 4


 Какие виды состояний? • электроннные UV-Vis • колебательные инфракрасные • Вращательные микроволны • Спин ядра радиочастоты
Какие виды состояний? • электроннные UV-Vis • колебательные инфракрасные • Вращательные микроволны • Спин ядра радиочастоты
 • Приближение Борна-Оппенгеймера является предположение, что электронное движение и движение ядер в молекуле может быть отделена. • Это приводит к тому, что молекулярные волновые функции, которые даны в терминах электронного позиций (ri) и ядерных позиций (Rj):
• Приближение Борна-Оппенгеймера является предположение, что электронное движение и движение ядер в молекуле может быть отделена. • Это приводит к тому, что молекулярные волновые функции, которые даны в терминах электронного позиций (ri) и ядерных позиций (Rj):
 Колебательные состояния • Колебательной моды также могут возбуждаться. • Тепловые колебательные движения • Iтакже, колебания в молекулах могут возникать под действием света светом. • Предположим, что два атома точечных масс связанных безмассовой пружиной совершают простые гармонические колебания
Колебательные состояния • Колебательной моды также могут возбуждаться. • Тепловые колебательные движения • Iтакже, колебания в молекулах могут возникать под действием света светом. • Предположим, что два атома точечных масс связанных безмассовой пружиной совершают простые гармонические колебания
 Колебательное движение: простой гармонический осциллятор • Простой гармонический осциллятор хорошо описывает как двухатомную , так и сложную молекулу
Колебательное движение: простой гармонический осциллятор • Простой гармонический осциллятор хорошо описывает как двухатомную , так и сложную молекулу
 Колебательные состояния Энергетические уровни квантовомеханического осциллятора Правило отбора для колебательного перехода: Dv = ± 1 Только для спектральной линии w ! отклонения от идеальной параболического потенциала позволяют другие переходы, называюмые обертонами, но они гораздо слабее,
Колебательные состояния Энергетические уровни квантовомеханического осциллятора Правило отбора для колебательного перехода: Dv = ± 1 Только для спектральной линии w ! отклонения от идеальной параболического потенциала позволяют другие переходы, называюмые обертонами, но они гораздо слабее,
 33 Department of Chemistry, KAIST
33 Department of Chemistry, KAIST
 CH 2 колебания Связь углерод- водород очень важна для химии жизни Симметричное растяжение Антисимметричное растяжение «ножницы» Раскачивание Wagging ( «виляние» ) скручивание
CH 2 колебания Связь углерод- водород очень важна для химии жизни Симметричное растяжение Антисимметричное растяжение «ножницы» Раскачивание Wagging ( «виляние» ) скручивание
 35 Колебательная спектроскопия Правило отбора
35 Колебательная спектроскопия Правило отбора
 36
36
 Вращательные состояния • Двухатомную молекулу можно рассматривать как два атома соединенные невысомым жестким стержнем (модель твердого ротатора). • В чисто вращательные системы, кинетическая энергия выражается через угловой момент L и инерции вращения I.
Вращательные состояния • Двухатомную молекулу можно рассматривать как два атома соединенные невысомым жестким стержнем (модель твердого ротатора). • В чисто вращательные системы, кинетическая энергия выражается через угловой момент L и инерции вращения I.
 re = r. A + r. B Кинетическая энергия вращения (Erot) где ω угловая скорость , dθ/dt
re = r. A + r. B Кинетическая энергия вращения (Erot) где ω угловая скорость , dθ/dt
 Кинетическая энергия вращения(Erot) Приведеная масса Момент инерции (сравним ) Используя угловой момент (сравним кинетическая энергия вращения становиться (сравним ) )
Кинетическая энергия вращения(Erot) Приведеная масса Момент инерции (сравним ) Используя угловой момент (сравним кинетическая энергия вращения становиться (сравним ) )
 40 Период вращения Для Krot = k. BT Для типичной молекулы при комнатной температуре (одна пикосекунда)
40 Период вращения Для Krot = k. BT Для типичной молекулы при комнатной температуре (одна пикосекунда)
 Квантование энергии вращения V=0 Циклическое граничное условие : Ψ(2π + θ) = Ψ(θ) Из решения уравнения Шредингера для вращательного движения, Энергия вращательных уровней Вращательные уровни энергии в волновых числах (cm-1)
Квантование энергии вращения V=0 Циклическое граничное условие : Ψ(2π + θ) = Ψ(θ) Из решения уравнения Шредингера для вращательного движения, Энергия вращательных уровней Вращательные уровни энергии в волновых числах (cm-1)
 Расстояние между соседними вращательными уровнями j и j-1, 42
Расстояние между соседними вращательными уровнями j и j-1, 42
 Вращательная спектроскопия (1) Постулат Бора (2) Правило отбора
Вращательная спектроскопия (1) Постулат Бора (2) Правило отбора
 44 От дальней инфракрасной области до микроволновой области спектра (микроволновая спектроскопия)
44 От дальней инфракрасной области до микроволновой области спектра (микроволновая спектроскопия)
 Комбинация колебания и вращения
Комбинация колебания и вращения
 Комбинация колебания и вращения q. DE увеличивается линейно с ℓ. • Многие переходы запрещены правилами отбора, которые требуют Dℓ = ± 1 and D n = ± 1
Комбинация колебания и вращения q. DE увеличивается линейно с ℓ. • Многие переходы запрещены правилами отбора, которые требуют Dℓ = ± 1 and D n = ± 1
 Комбинация колебаний и вращений • Спектр излучения (и поглощения) спектр меняется в зависимости от расстояния ℓ. • Чем выше начальный энергетический уровень, тем больше энергия фотона. • Колебательная энергия больше вращательной. Для диатомной молекулы эта разница энергий приводит к полосатой структуре. • Однако, интенсивность линий зависит от населенности состояний и колебательных правил отбора. Dn = 3 Dn = 2 Dn = 1 Длина волны → Dn = 0
Комбинация колебаний и вращений • Спектр излучения (и поглощения) спектр меняется в зависимости от расстояния ℓ. • Чем выше начальный энергетический уровень, тем больше энергия фотона. • Колебательная энергия больше вращательной. Для диатомной молекулы эта разница энергий приводит к полосатой структуре. • Однако, интенсивность линий зависит от населенности состояний и колебательных правил отбора. Dn = 3 Dn = 2 Dn = 1 Длина волны → Dn = 0
 Колебательно-вращательный спектр • В спектре поглощения HCl, расстояние между пиками могут быть использованы для расчета вращательных момента инерции. Отсутствует пик в центре, что соответствует запрещено D ℓ = 0 переход. ℓi- ℓf < 0 ℓi- ℓf > 0 ni- nf = 1
Колебательно-вращательный спектр • В спектре поглощения HCl, расстояние между пиками могут быть использованы для расчета вращательных момента инерции. Отсутствует пик в центре, что соответствует запрещено D ℓ = 0 переход. ℓi- ℓf < 0 ℓi- ℓf > 0 ni- nf = 1
 Частоты движений в атомах и молекулах • Электроны вибрируют в своем движении вокруг ядра • Высокая частота: ~1014 – 1017 колебаний в секунду. • Колебания ядер в молекулах по отношению друг к другу • промежуточная частота : ~1011 - 1013 колебаний в секунду. • Вращение ядер в молекулах • Низкая частота: ~109 – 1010 колебаний в секунду.
Частоты движений в атомах и молекулах • Электроны вибрируют в своем движении вокруг ядра • Высокая частота: ~1014 – 1017 колебаний в секунду. • Колебания ядер в молекулах по отношению друг к другу • промежуточная частота : ~1011 - 1013 колебаний в секунду. • Вращение ядер в молекулах • Низкая частота: ~109 – 1010 колебаний в секунду.
 50 «Включим» электронные энергетические уровни Etotal = Enuclear + Eelectron = Etrans + Evib + Erot + Eelectron = Etrans + Einternal
50 «Включим» электронные энергетические уровни Etotal = Enuclear + Eelectron = Etrans + Evib + Erot + Eelectron = Etrans + Einternal
 «Включим» электронные энергетические уровни • Энергетические уровни для типичной большой молекулы: E = Eelectonic + Evibrational + Erotational Низший колебательный и вращательный уровни этого электронного "многообразия" Возбужденный колебательны и вращательный уровни 1 возбужденное Электронное состояние Energy 2 возбужденное электронное состояние Переход Основное электронное состояние Есть много других осложнений, таких, как спин-орбитальное взаимодействие, спин ядра, и т. д. , которые расщепляют уровни. В результате, молекула имеет сложный спектр
«Включим» электронные энергетические уровни • Энергетические уровни для типичной большой молекулы: E = Eelectonic + Evibrational + Erotational Низший колебательный и вращательный уровни этого электронного "многообразия" Возбужденный колебательны и вращательный уровни 1 возбужденное Электронное состояние Energy 2 возбужденное электронное состояние Переход Основное электронное состояние Есть много других осложнений, таких, как спин-орбитальное взаимодействие, спин ядра, и т. д. , которые расщепляют уровни. В результате, молекула имеет сложный спектр

 Спектр поглощения молекулы V = колебательное квантовое число J =вращательное квантовое число
Спектр поглощения молекулы V = колебательное квантовое число J =вращательное квантовое число
 Формирование спектров
Формирование спектров
 Молекулярная спектроскопия • Электронные переходы: UV-visible • Колебательные переходы: IR • Вращательные переходы : E Электронные Колебательная Вращательная
Молекулярная спектроскопия • Электронные переходы: UV-visible • Колебательные переходы: IR • Вращательные переходы : E Электронные Колебательная Вращательная
 ЭНЕРГЕТИЧЕСКИЕ ПЕРЕХОДЫ МОЛЕКУЛЫ 1. Возбуждение молекулы: переход молекулы из основного (S 0) на один из возбужденных синглетных уровней по схеме: S 0 + hν→ S 1(vn) (процесс А) может произойти только в том случае, если энергия фотонов падающего излучения равна энергии перехода с уровня So на более высокий уровень или подуровень синглетного состояния.
ЭНЕРГЕТИЧЕСКИЕ ПЕРЕХОДЫ МОЛЕКУЛЫ 1. Возбуждение молекулы: переход молекулы из основного (S 0) на один из возбужденных синглетных уровней по схеме: S 0 + hν→ S 1(vn) (процесс А) может произойти только в том случае, если энергия фотонов падающего излучения равна энергии перехода с уровня So на более высокий уровень или подуровень синглетного состояния.
 2. Внутренняя конверсия: молекула очень быстро (~ 10 -13 с) переходит с колебательного подуровня vn(S 1) на основной возбужденный уровень S 1 с выделением избыточной энергии в форме тепла: vn(S 1) → S 1+ Q (процесс B)
2. Внутренняя конверсия: молекула очень быстро (~ 10 -13 с) переходит с колебательного подуровня vn(S 1) на основной возбужденный уровень S 1 с выделением избыточной энергии в форме тепла: vn(S 1) → S 1+ Q (процесс B)
 3. Молекула в возбужденном состоянии S 1 может расходовать оставшуюся энергию возбуждения по одному из трех механизмов: 3. 1. Колебательная релаксация: передать энергию в форме тепла при столкновении с другой химической частицей: S 1 → S 0 + Q (процесс С)
3. Молекула в возбужденном состоянии S 1 может расходовать оставшуюся энергию возбуждения по одному из трех механизмов: 3. 1. Колебательная релаксация: передать энергию в форме тепла при столкновении с другой химической частицей: S 1 → S 0 + Q (процесс С)
 3. 2. Флуоресценция: испустить энергию в виде кванта электромагнитного излучения: S 1 → S 0+ hν (процесс D)
3. 2. Флуоресценция: испустить энергию в виде кванта электромагнитного излучения: S 1 → S 0+ hν (процесс D)
 3. 3. Интеркомбинационная конверсия: перейти на какойлибо подуровень триплетного уровня, обладающий почти такой же энергией: S 1 → vn(T 1) + Q (процесс E)
3. 3. Интеркомбинационная конверсия: перейти на какойлибо подуровень триплетного уровня, обладающий почти такой же энергией: S 1 → vn(T 1) + Q (процесс E)
 3. 3. 1. Внутренняя конверсия: в свою очередь молекула из vn(T 1) переходит на основной возбужденный уровень T 1 с выделением тепла: vn(T 1) → T 1+ Q (процесс F)
3. 3. 1. Внутренняя конверсия: в свою очередь молекула из vn(T 1) переходит на основной возбужденный уровень T 1 с выделением тепла: vn(T 1) → T 1+ Q (процесс F)
 3. 3. 2. Колебательная релаксация: передать энергию в форме тепла при столкновении с другой химической частицей: T 1 → S 0 + Q (процесс G)
3. 3. 2. Колебательная релаксация: передать энергию в форме тепла при столкновении с другой химической частицей: T 1 → S 0 + Q (процесс G)
 3. 3. 3. Фосфоресценция: испустить энергию в виде кванта электромагнитного излучения: Т 1 → S 0+ hν (процесс H).
3. 3. 3. Фосфоресценция: испустить энергию в виде кванта электромагнитного излучения: Т 1 → S 0+ hν (процесс H).


