Sitdikova_Amina_bt_-_22.pptx
- Количество слайдов: 27
Выполнила: Ситдикова А. М. , БТ - 22
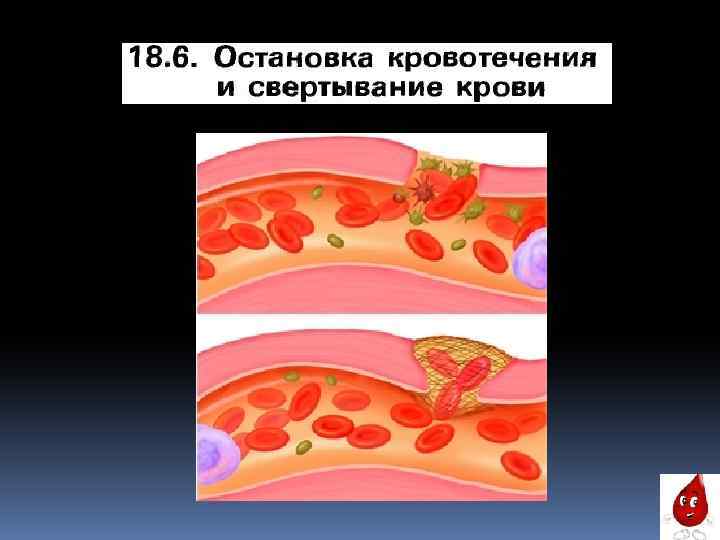

Гемостаз. Система гемостаза — это биологическая система в организме, функция которой заключается в сохранение жидкого состояния крови, остановке кровотечений при повреждениях стенок сосудов и растворении тромбов выполнивших свою функцию. Различают два основных механизма остановки кровотечения при повреждении сосудов, которые в зависимости от условий могут функционировать одновременно, с преобладанием одного из механизмов: * Первичный, или сосудисто-тромбоцитарный гемостаз, обусловленный спазмом сосудов и их механической закупоркой агрегатами тромбоцитов. На обнажившихся в результате повреждения стенки сосуда коллагеновых молекулах происходит адгезия (прилипание), активация и агрегация (склеивание между собой) тромбоцитов. При этом образуется так называемый «белый тромб» , т. е. тромб с преобладанием тромбоцитов. * Вторичный, или коагуляционный гемостаз (свертывание крови), запускается тканевым фактором из окружающих поврежденный сосуд тканей, и регулируемый многочисленными факторами свертывания крови. Он обеспечивает плотную закупорку поврежденного участка сосуда фибриновым сгустком – это так называемый «красный тромб» , т. к. образовавшаяся фибриновая сетка включает в себя клетки крови эритроциты.

Свёртывание крови – это важнейший этап работы системы гемостаза, отвечающей за остановку кровотечения при повреждении сосудистой системы организма. Совокупность взаимодействующих между собой весьма сложным образом различных факторов свёртывания крови образуют систему свёртывания крови. Свёртыванию крови предшествует стадия первичного сосудисто-тромбоцитарного гемостаза. Этот первичный гемостаз почти целиком обусловлен сужением сосудов и механической закупоркой агрегатами тромбоцитов места повреждения сосудистой стенки. Характерное время для первичного гемостаза у здорового человека составляет 1 -3 мин. Собственно свёртыванием крови (гемокоагуляция, плазменный гемостаз, вторичный гемостаз) называют сложный биологический процесс образования в крови нитей белка фибрина, который полимеризуется и образует тромбы, в результате чего кровь теряет текучесть, приобретая творожистую консистенцию. Свёртывание крови у здорового человека происходит локально, в месте образования первичной тромбоцитарной пробки. Характерное время образования фибринового сгустка – около 10 мин. Свертывание крови - ферментативный процесс. Фибриновый сгусток, полученный путём добавления тромбина в цельную кровь. Сканирующая электронная микроскопия.

Адгезия тромбоцитов (Platelet adhesion) - это прилипание тромбоцитов к компонентам субэндотелия (в частности, к коллагену ) или к чужеродной поверхности (например, к стеклу). Адгезия тромбоцитов к волокнам коллагена происходит в первые секунды после повреждения благодаря наличию на тромбоцитах рецепторов к коллагену — гликопротеида Ia/IIa, относящегося к семейству интегринов. Стабилизация образовавшегося соединения фактором фон Виллебранда не позволяет току крови смывать тромбоциты. Фактор фон Виллебранда образует связь между субэндотелиальными волокнами коллагена и другим рецептором тромбоцитов — гликопротеидом Ib/IX. В результате адгезии тромбоциты активируются и выбрасывают ряд активных веществ — как заранее запасенных в их гранулах (дегрануляция), так и образующихся при активации. Тромбоциты в крови Агрегация тромбоцитов (Platelet aggregation) — склеивание (слипание) тромбоцитов между собой под действием специфических стимуляторов. Реакция освобождения тромбоцитов приводит к выделению из них индукторов агрегации ( АДФ, серотонин, адреналин, нестабильные простагландины, тромбоксан А 2, тромбоцитоактивирующий фактор ). Наряду со стимуляторами, попадающими в кровоток из поврежденных тканей и других форменных элементов крови, они вызывают агрегацию других тромбоцитов, которые быстро покидают кровоток и оседают на уже адгезировавших и начавших агрегировать тромбоцитах. Агрегацию тромбоцитов определяют гликопротеины IIb/IIIа мембран тромбоцитов, которые взаимодействуют между собой при участии фибриногена.

Различают агрегацию: * обратимую; * необратимую. Обратимая агрегация – это скопление тромбоцитов у места повреждения и склеивание их между собой. Агрегация начинается почти одновременно с адгезией и обусловлена выделением поврежденной стенкой сосуда, а также тромбоцитами и эритроцитами биологически активных веществ (прежде всего АТФ и АДФ). В результате этого образуется рыхлая тромбоцитарная пробка, которая проницаема для плазмы крови. Необратимая агрегация – это агрегация кровяных пластинок, при которой они теряют свою структурность и сливаются в гомогенную массу, образуя пробку, непроницаемую для плазмы крови. Эта реакция происходит под действием тромбина, разрушающего мембрану тромбоцитов, что ведет к выходу из них биологически активных веществ: серотонина, гистамина, ферментов и факторов свертывания крови. Их выделение способствует вторичному спазму сосудов. Освобождение 3 тромбоцитарного фактора дает начало образованию тромбоцитарной протромбиназы, т. е. включению механизма коагуляционного гемостаза. На агрегатах тромбоцитов образуется небольшое количество нитей фибрина, в сетях которого задерживаются форменные элементы крови. В регуляции тромбоцитарного гемостаза важную роль играют производные арахидоновой кислоты, освобождаемой из мембранных фосфолипидов тромбоцитов и сосудистой стенки вследствии активации фосфолипаз. Под влиянием циклооксигеназы образуются простагландины, из них в тромбоцитах под влиянием тромбоксан-синтетазы образуется чрезвычайно мощный агрегирующий агент – тромбоксан-А 2. Продолжительность жизни тромбоксана, простациклина и других простагландинов несколько минут, но их значение в регуляции и патологии гемостаза весьма велико. Этот механизм является триггерным в реализации адгезивно-агрегационной функции тромбоцитов. Для осуществления этой функции кровяных пластинок необходим ряд плазменных кофакторов агрегации – ионы кальция и магния, фибриноген, альбумин и два белковых кофактора, обозначаемых как агрексоны A и B, фосфолипидный кофактор и др. В то же время парапротеины, криоглобулины и продукты фибринолиза ингибируют агрегацию
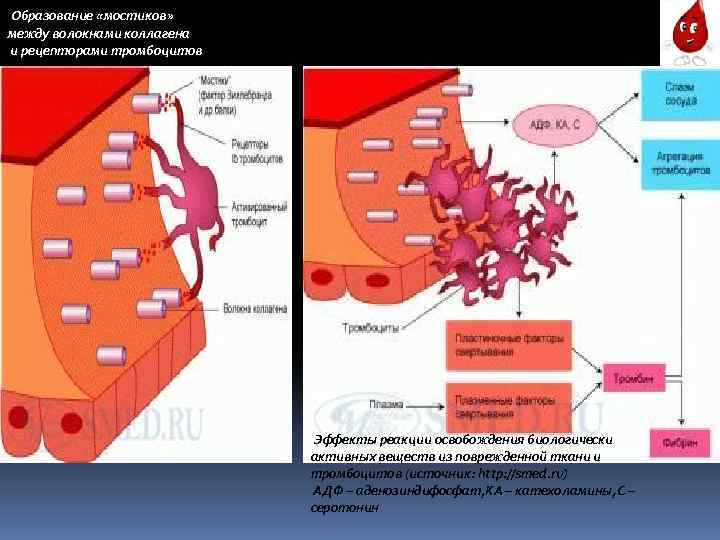
Образование «мостиков» между волокнами коллагена и рецепторами тромбоцитов Эффекты реакции освобождения биологически активных веществ из поврежденной ткани и тромбоцитов (источник: http: //smed. ru) АДФ – аденозиндифосфат, КА – катехоламины, С – серотонин
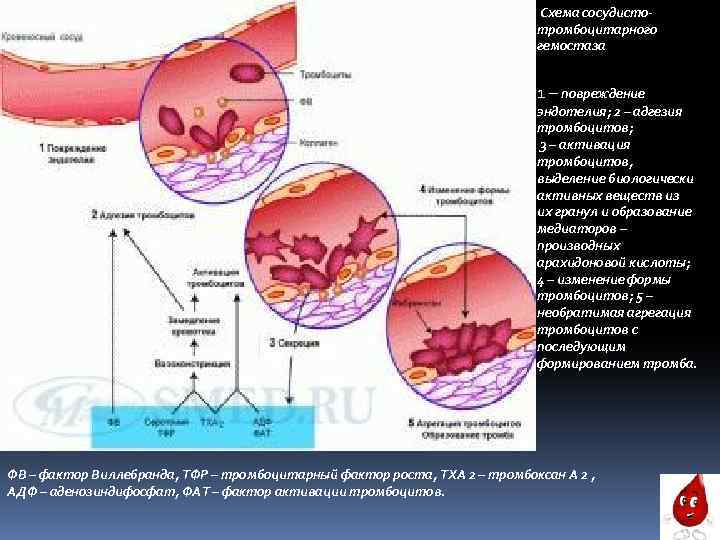
Схема сосудистотромбоцитарного гемостаза 1 – повреждение эндотелия; 2 – адгезия тромбоцитов; 3 – активация тромбоцитов, выделение биологически активных веществ из их гранул и образование медиаторов – производных арахидоновой кислоты; 4 – изменение формы тромбоцитов; 5 – необратимая агрегация тромбоцитов с последующим формированием тромба. ФВ – фактор Виллебранда, ТФР – тромбоцитарный фактор роста, TXA 2 – тромбоксан А 2 , АДФ – аденозиндифосфат, ФАТ – фактор активации тромбоцитов.
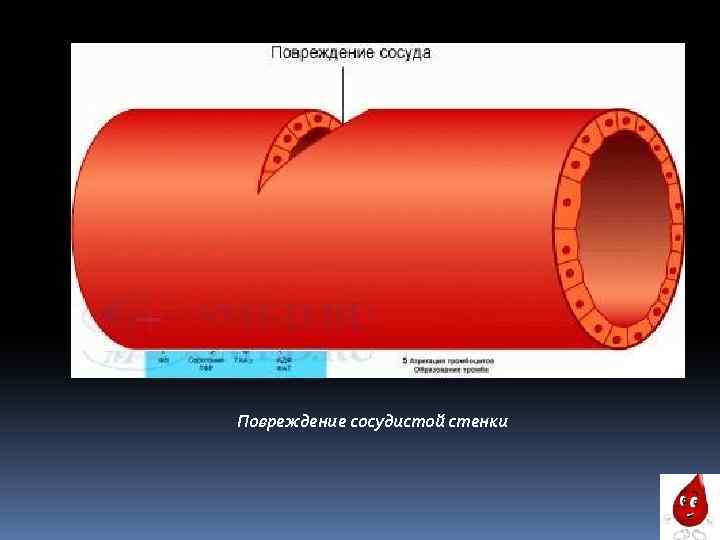
Повреждение сосудистой стенки
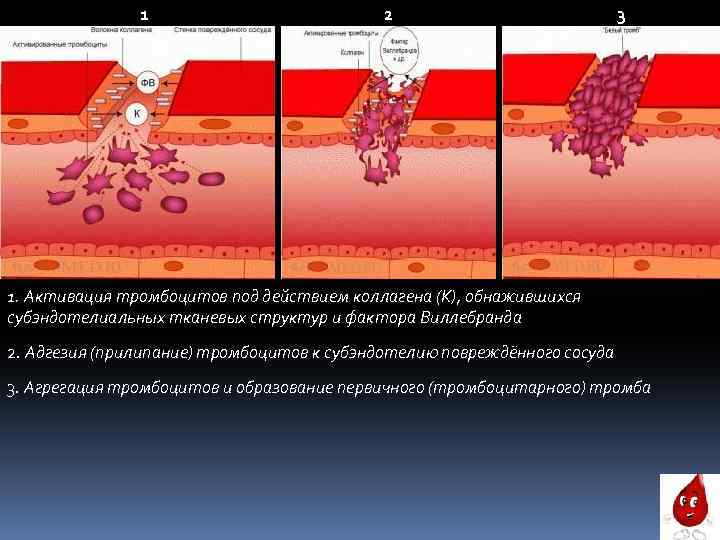
1 2 3 1. Активация тромбоцитов под действием коллагена (К), обнажившихся субэндотелиальных тканевых структур и фактора Виллебранда 2. Адгезия (прилипание) тромбоцитов к субэндотелию повреждённого сосуда 3. Агрегация тромбоцитов и образование первичного (тромбоцитарного) тромба
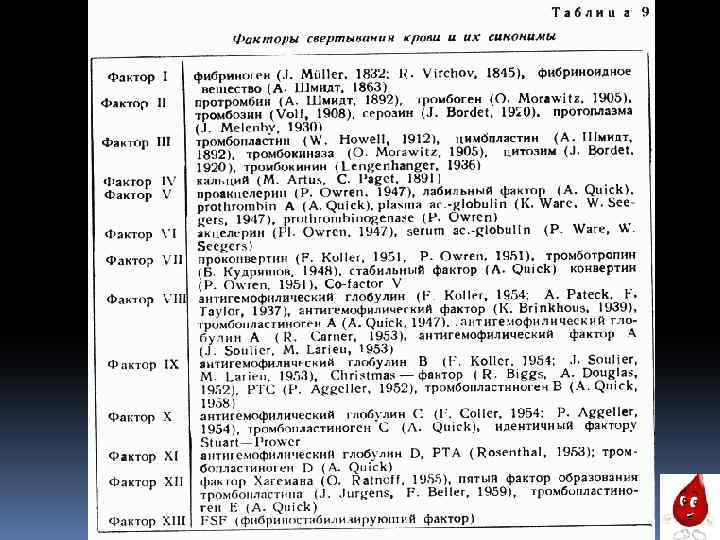

Важно знать, что: * Физиологическая роль сосудисто-тромбоцитарного звена гемостаза – это первичная остановка кровотечения путем формирования нестойкого первичного (тромбоцитарного) тромба. * Первичная остановка кровотечения в норме происходит за 2 -4 минуты. * Наиболее важными факторами, обеспечивающими первичный (сосудисто-тромбоцитарный) гемостаз, являются тромбоциты и фактор Виллебранда, способствующий их адгезии и агрегации. * Первичный гемостаз является первым этапом в остановке кровотечения и не способен обеспечить окончательную остановку кровотечения в сосудах среднего и крупного калибра. * Сосудисто-тромбоцитарный и коагуляционный гемостаз являются взаимосвязанными, но все же относительно независимыми процессами.
Красные и белые кровяные клетки
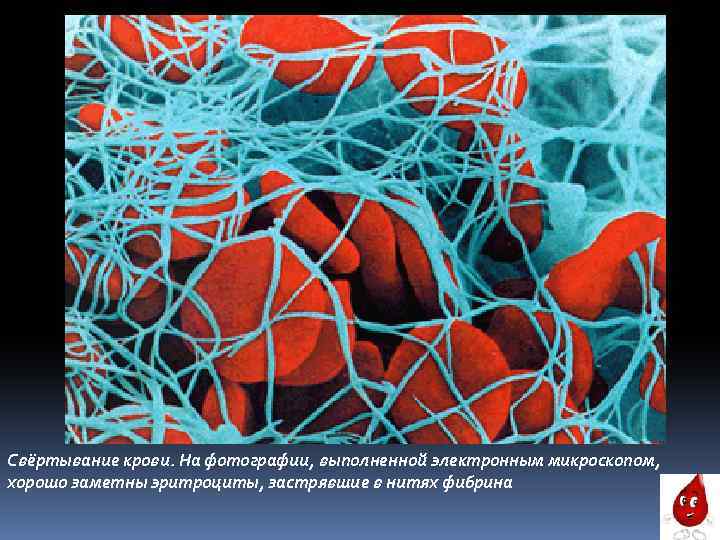
Свёртывание крови. На фотографии, выполненной электронным микроскопом, хорошо заметны эритроциты, застрявшие в нитях фибрина

Тромбин ( EC 3. 4. 21. 5 ) - сериновая протеиназа семейства трипсина - ключевой фермент свертывающей системы крови , который превращает фибриноген в фибрин - основу тромба, участвует в регуляции многих физиологических и патофизиологических процессов, таких как свертывание крови и противосвертывающие механизмы, тромбообразование и фибринолиз, регуляция сосудистого тонуса и процессов развития организма, а также в процессах воспаления, репарации тканей, атерогенеза, канцерогенеза и болезни Альцгеймера Активация свертывания крови и образование тромбина происходят при воспалении, заживлении ран, атерогенезе и других процессах, индуцируемых при повреждении эндотелия сосудов. Тромбин образуется из протромбина на заключительном этапе свертывания крови и превращает растворимый фибриноген в нерастворимый фибриновый сгусток, при этом реализуется высокоспецифическое взаимодействие участка фибриногена, содержащего фибринопептиды А и В, с отрицательно заряженным центром узнавания тромбина, удаленным от каталитического участка активного центра Фибрин (от лат. fibra — волокно) — высокомолекулярный, неглобулярный белок, образующийся из фибриногена плазмы крови под действием фермента тромбина; имеет форму гладких или поперечноисчерченных волокон, сгустки которых составляют основу тромба при свёртывании крови

Образуется фибрин в три стадии: * На первой стадии под действием тромбина от молекулы фибриногена отщепляются два пептида А (молекулярная масса около 2000) и два пептида Б (молекулярная масса около 2500) и образуется фибрин-мономер, построенный из двух идентичных субъединиц, соединённых дисульфидными связями. Каждая из субъединиц состоит из трёх неодинаковых полипептидных цепей, обозначаемых a, b, g. * На второй стадии фибрин-мономер самопроизвольно превращается в сгусток, называемый фибрин-агрегатом, или нестабилизированным фибрином. Агрегация фибрин-мономера (самосборка фибриновых волокон) включает переход молекулы из состояния глобулы в состояние фибриллы. В образовании фибрин-агрегата принимают участие водородные и электростатические связи и силы гидрофобного взаимодействия, которые могут быть ослаблены в концентрированных растворах мочевины и др. агентов, вызывающих денатурацию. Это приводит к восстановлению фибрин-мономера. Образование фибрин-агрегата ускоряется веществами, несущими положит, заряд (ионы кальция, протаминсульфат), и тормозится отрицательно заряженными соединениями (гепарин). * На третьей стадии фибрин-агрегат претерпевает изменения, обусловленные ферментативным воздействием фибринстабилизирующего фактора XIII а (или фибринолигазы). Под действием этого фактора образуются прочные ковалентные связи между g-, а также между aполипептидными цепями молекул фибрин-агрегата, в результате чего он стабилизируется в фибрин-полимер, нерастворимый в концентрированных растворах мочевины. При врождённой или приобретённой недостаточности в организме фактора XIII и при некоторых заболеваниях фибрин -агрегат не стабилизируется в фибрин-полимер, что сопровождается кровоточивостью. Фибрин получают путём промывки и высушивания кровяного сгустка. Из фибрина приготовляют стерильные губки и плёнки для остановки кровотечения из мелких сосудов при различных хирургических операциях.

Фибринолиз (от Фибрин и греч. lýsis – разложение, растворение) - процесс растворения тромбов и сгустков крови, неотъемлемая часть системы гемостаза, всегда сопровождающая процесс свертывания крови и культивирующаяся факторами, принимающими участие в данном процессе. Является важной защитной реакцией организма и предотвращает закупорку кровеносных сосудов сгустками фибрина. Также фибринолиз способствует реканализации сосудов после прекращения кровотечения. Включает в себя расщепление фибрина под воздействием плазмина, присутствующего в плазме крови в виде неактивного предшественника - плазминогена. Последний активируется одновременно с началом процесса свертывания крови. Фибринолиз, как и процесс свертывания крови, протекает по внешнему или внутреннему механизму. Внешний путь активации осуществляется при неотъемлемом участии тканевых активаторов, синтезирующихся преимущественно в эндотелии сосудов. К данным активаторам относят тканевый активатор плазминогена (ТАП) и урокиназу. Внутренний механизм активации осуществляется благодаря плазменным активаторам и активаторами форменных элементов крови — лейкоцитов, тромбоцитов и эритроцитов. Внутренний механизм активации разделяют на на Хагеман-зависимый и Хагеман-независимый. Хагеман-зависимый фибринолиз происходит под влиянием фактора XIIа свертывания крови, калликреина, которые вызывают превращение плазминогена в плазмин. Хагеман-независимый фибринолиз происходит наиболее быстро. Его основным назначением является очищение сосудистого русла от нестабилизированного фибрина, который образуется в процессе внутрисосудистого свертывания крови.
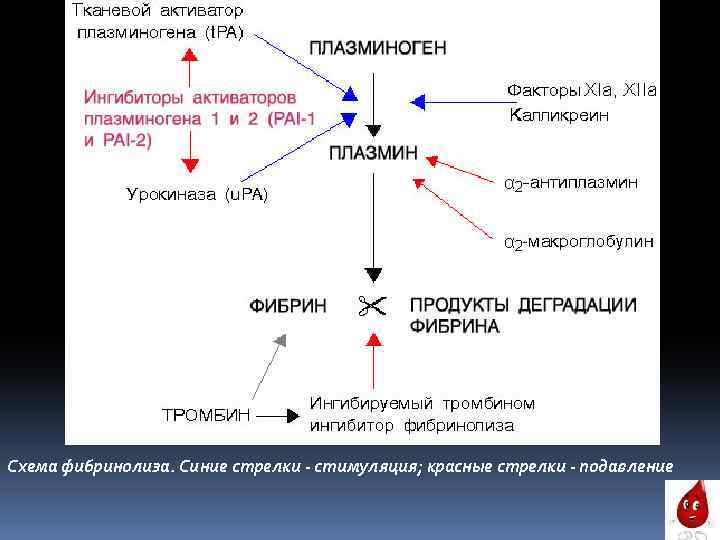
Схема фибринолиза. Синие стрелки - стимуляция; красные стрелки - подавление

Основные функции крови

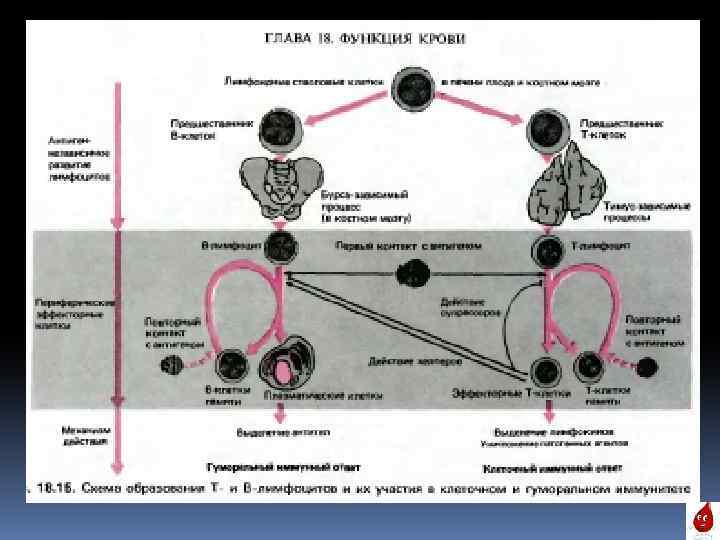
Защитная функция крови Иммунитет — невосприимчивость организма к возбудителям определенных заразных заболеваний или к определенным ядам. Существуют два механизма иммунитета: клеточный и гуморальный. Клеточный и плюральный иммунитет В клеточном иммунитете, или клеточной защите, участвуют лейкоциты и клетки ретикулоэндотелиальной системы. Лейкоциты обладают амебоидным движением, что позволяет им захватывать и переваривать чужеродные клетки и отмершие клетки данного организма. Поглощение и внутриклеточное переваривание микробов, чужеродных и отмерших клеток организма на называется фагоцитозом. Этот феномен открыл И. И. Мечников.

Различают следующие антитела, действующие на антигены: 1) антитоксины — нейтрализующие, обезвреживающие яды, токсины; 2) лизины — растворяющие, разрушающие микробы (бактериолизины), эритроциты (гемолизины); 3) преципитины — вызывающие осаждение белковых продуктов, образовавшихся из разрушенных микробов, или осаждение белковых растворов; 4) опсонины — подготавливающие микробы к перевариванию их фагоцитами путем прилипания к ним протеинов плазмы; 5) агглютинины — склеивающие микробы или чужеродные эритроциты.
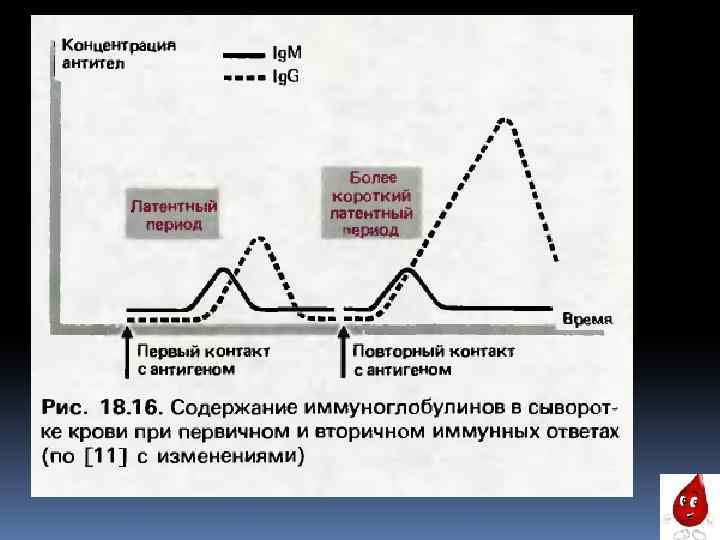
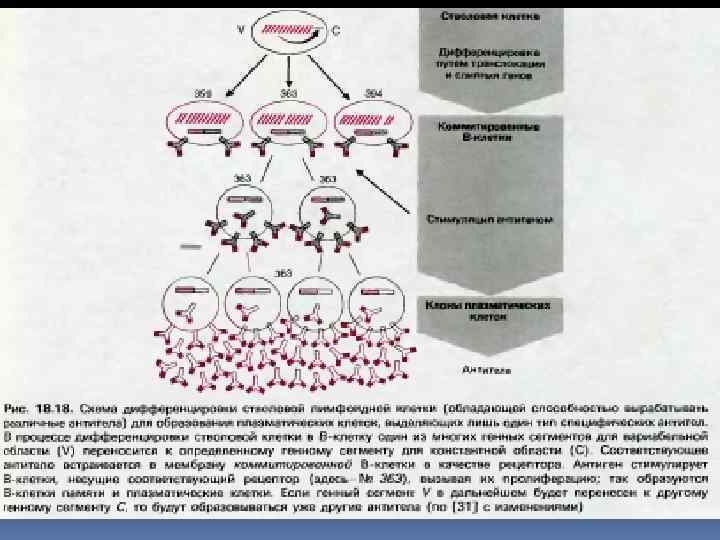
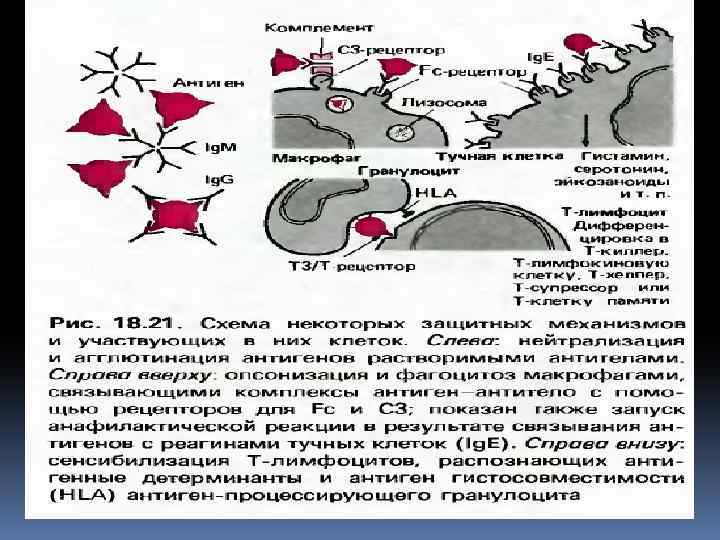

К защитным веществам относится и белковый компонент пропердин, содержащийся в плазме. У человека его количество составляет 0, 03% всех белков плазмы. При проникновении в клетки организма чужеродной нуклеиновой кислоты они выделяют полипептид — интерферон. Он угнетает размножение вирусов, подавляет генетическую информацию, содержащуюся в чужеродной нуклеиновой кислоте, и защищает организм от ее мутаций. Интерферон образуется во всех клетках, но особенно много продуцируют его лейкоциты и клетки ретикуло-эндотелиальной системы селезенки. Повышение температуры увеличивает, а понижение уменьшает его выделение. Он обладает видовой специфичностью. У здоровых людей он не обнаружен.

The end. Спасибо за Ваше внимание!! Астана, 2013 год.
Sitdikova_Amina_bt_-_22.pptx