 Выполнил студент 3 курса 9 группы ЛПФ Манандян Ашот
Выполнил студент 3 курса 9 группы ЛПФ Манандян Ашот
 Вирусы, бактерии, грибы и паразиты, проникающие в организм позвоночных, могут узнаваться иммунной системой и уничтожаться ею. По аналогичному механизму опознаются системой и устраняются трансформированные клетки организма, например опухолевые. Иммунная система в состоянии опознавать инородные тела, специфически реагировать на них и сохранять это событие в «памяти» . Упрощенная схема иммунного ответа :
Вирусы, бактерии, грибы и паразиты, проникающие в организм позвоночных, могут узнаваться иммунной системой и уничтожаться ею. По аналогичному механизму опознаются системой и устраняются трансформированные клетки организма, например опухолевые. Иммунная система в состоянии опознавать инородные тела, специфически реагировать на них и сохранять это событие в «памяти» . Упрощенная схема иммунного ответа :
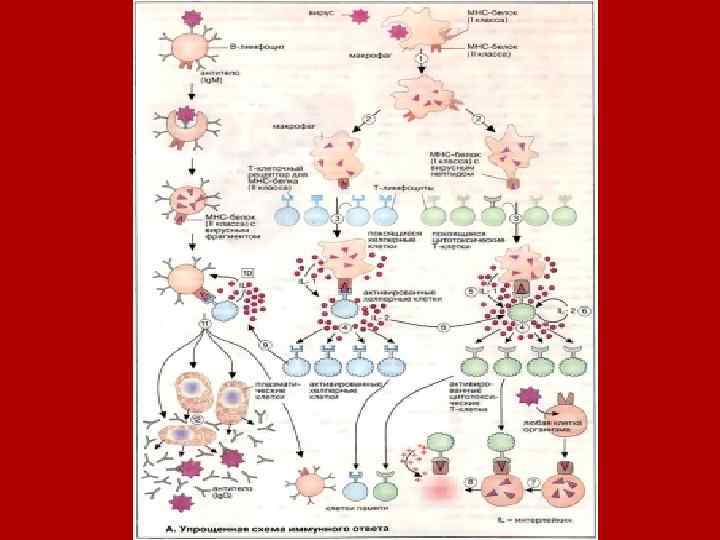
 Проникший в организм вирус эндоцитируется макрофагами и затем частично разрушается в эндоплазматическом ретикулуме (1). В результате образуются чужеродные фрагменты, которые экспонируются на клеточной поверхности макрофагов (2). Эти фрагменты «презентируются» специальной группой мембранных белков (белки ГКГС). Комплекс из вирусного фрагмента и белка главного комплекса гистосовместимости [ГКГС (МНС)] распознается и связывается Т клетками с помощью специфических (Т клеточных) рецепторов. Среди огромного числа Т клеток только немногие обладают подходящим рецептором (3), Связывание приводит к активации этих Т клеток и появлению их селективных копий (4, "клональная селекция"). В активации Т клеток участвуют различные гормоноподобные Сигнальные белки, интерлейкины [ИЛ (IL)]. Эти белки секретируются теми клетками иммунной системы, которые активируются при связывании с Т клетками. Так, активированные макрофаги с презентируемым вирусным фрагментом секретируют IL 1 (5), а Т клетки продуцируют IL 2 (6), который стимулирует их собственное клональное копирование и репликацию Т хелперных клеток. Клонированные и активированные Т клетки осуществляют различные функции в зависимости от их типа. Цитотоксические Т клетки (на схеме зеленого цвета) способны узнавать и связывать те клетки организма, которые инфицированы вирусами и на своих рецепторах ГКГС несут фрагменты вируса (7). Цитотоксические Т клетки секретируют перфорин — белок, который делает проницаемой мембрану связанной инфицированной клетки, что и приводит к ее лизису (8). Т Хелперы (на схеме голубого цвета), напротив, связываются с В клетками, которые презентируют на своей поверхности фрагменты вируса, связанные с белком ГКГС (9). Это ведет к селективному клонированию индивидуальных В клеток и их массированной пролиферации, Интерлейкин стимулирует (10) созревание В клеток — превращение в плазматические клетки (11), способные синтезировать и секретировать антитела (12). М
Проникший в организм вирус эндоцитируется макрофагами и затем частично разрушается в эндоплазматическом ретикулуме (1). В результате образуются чужеродные фрагменты, которые экспонируются на клеточной поверхности макрофагов (2). Эти фрагменты «презентируются» специальной группой мембранных белков (белки ГКГС). Комплекс из вирусного фрагмента и белка главного комплекса гистосовместимости [ГКГС (МНС)] распознается и связывается Т клетками с помощью специфических (Т клеточных) рецепторов. Среди огромного числа Т клеток только немногие обладают подходящим рецептором (3), Связывание приводит к активации этих Т клеток и появлению их селективных копий (4, "клональная селекция"). В активации Т клеток участвуют различные гормоноподобные Сигнальные белки, интерлейкины [ИЛ (IL)]. Эти белки секретируются теми клетками иммунной системы, которые активируются при связывании с Т клетками. Так, активированные макрофаги с презентируемым вирусным фрагментом секретируют IL 1 (5), а Т клетки продуцируют IL 2 (6), который стимулирует их собственное клональное копирование и репликацию Т хелперных клеток. Клонированные и активированные Т клетки осуществляют различные функции в зависимости от их типа. Цитотоксические Т клетки (на схеме зеленого цвета) способны узнавать и связывать те клетки организма, которые инфицированы вирусами и на своих рецепторах ГКГС несут фрагменты вируса (7). Цитотоксические Т клетки секретируют перфорин — белок, который делает проницаемой мембрану связанной инфицированной клетки, что и приводит к ее лизису (8). Т Хелперы (на схеме голубого цвета), напротив, связываются с В клетками, которые презентируют на своей поверхности фрагменты вируса, связанные с белком ГКГС (9). Это ведет к селективному клонированию индивидуальных В клеток и их массированной пролиферации, Интерлейкин стимулирует (10) созревание В клеток — превращение в плазматические клетки (11), способные синтезировать и секретировать антитела (12). М
 Ответ на структуру чужеродного вещества, антиген, осуществляемый клетками иммунной системы, лимфоцитами бывает различного типа. За клеточный иммунитет ответственны Т лимфоциты (Т клетки). Эти иммунные клетки названы так из за тимуса, в котором они подвергаются основным стадиям своей дифференциации (школа Т клеток). Активность Т клеток направлена против зараженной вирусом клетки организма, а также на защиту от грибов и паразитов. Т Клетки принимают активное участие в процессе отторжения чужеродной ткани и помогают в формировании гуморального иммунного ответа. По своей функции они делятся на цитотоксические Т клетки — Т киллеры (на схеме зеленого цвета) и клетки помощники — Т хелперы (на схеме голубого цвета). В свою очередь гуморальный иммунный ответ направлен на активацию В лимфоцитов (В клетки, на схеме светло коричневый цвет), которые созревают в костном мозге в отличие от Т клеток тимуса. В Клетки несут на своей поверхности антитела и выделяют их в плазму. Антитела обладают способностью специфически связывать соответствующие антигены. Связывание антител с антигенами — решающее звено в системе защиты организма от внеклеточных вирусов и бактерий. В результате такого связывания последние опознаются как инородные тела и в дальнейшем уничтожаются. "Память" иммунной системы представлена так называемыми "клетками памяти". Эти наиболее долгоживущие клетки существуют для каждого типа иммунных клеток.
Ответ на структуру чужеродного вещества, антиген, осуществляемый клетками иммунной системы, лимфоцитами бывает различного типа. За клеточный иммунитет ответственны Т лимфоциты (Т клетки). Эти иммунные клетки названы так из за тимуса, в котором они подвергаются основным стадиям своей дифференциации (школа Т клеток). Активность Т клеток направлена против зараженной вирусом клетки организма, а также на защиту от грибов и паразитов. Т Клетки принимают активное участие в процессе отторжения чужеродной ткани и помогают в формировании гуморального иммунного ответа. По своей функции они делятся на цитотоксические Т клетки — Т киллеры (на схеме зеленого цвета) и клетки помощники — Т хелперы (на схеме голубого цвета). В свою очередь гуморальный иммунный ответ направлен на активацию В лимфоцитов (В клетки, на схеме светло коричневый цвет), которые созревают в костном мозге в отличие от Т клеток тимуса. В Клетки несут на своей поверхности антитела и выделяют их в плазму. Антитела обладают способностью специфически связывать соответствующие антигены. Связывание антител с антигенами — решающее звено в системе защиты организма от внеклеточных вирусов и бактерий. В результате такого связывания последние опознаются как инородные тела и в дальнейшем уничтожаются. "Память" иммунной системы представлена так называемыми "клетками памяти". Эти наиболее долгоживущие клетки существуют для каждого типа иммунных клеток.
 Реакция антиген — антитело это специфическое взаимодействие антител с соответствующими антигенами, в результате которого образуются комплексы антиген — антитело (иммунные комплексы). Часто конечным результатом этой реакции является связывание токсинов, обездвиживание вирулентных бактерий, нейтрализация вирусов. Антигенсвязывающие центры молекулы антитела могут связывать несколько неродственных антигенов. Такие антигены обладают структурным сходством и носят название перекрестно реагирующих. Гомогенная популяция молекул антител может связывать различные молекулы с очень малым структурным сходством или вовсе несхожие. В этом случае говорят о мультиспецифическом связывании, которое объясняют образованием связей в различных участках внутри антигенсвязывающих центров
Реакция антиген — антитело это специфическое взаимодействие антител с соответствующими антигенами, в результате которого образуются комплексы антиген — антитело (иммунные комплексы). Часто конечным результатом этой реакции является связывание токсинов, обездвиживание вирулентных бактерий, нейтрализация вирусов. Антигенсвязывающие центры молекулы антитела могут связывать несколько неродственных антигенов. Такие антигены обладают структурным сходством и носят название перекрестно реагирующих. Гомогенная популяция молекул антител может связывать различные молекулы с очень малым структурным сходством или вовсе несхожие. В этом случае говорят о мультиспецифическом связывании, которое объясняют образованием связей в различных участках внутри антигенсвязывающих центров
 Реакция антиген — антитело протекает в две фазы, которые различаются между собой по механизму и скорости. Первая фаза — специфическое соединение активного центра антитела с соответствующими группами антигена или гаптена; вторая — неспецифическая фаза, следующая за первой, — визуально наблюдаемая реакция. При взаимодействии антител с простыми гаптенами вторая фаза, как правило, отсутствует. При некоторых условиях, например в отсутствие солей, первая фаза может осуществиться, а вторая — нет. Первая фаза протекает всегда быстро, а вторая иногда очень медленно. Соединение антигена с антителом обратимо; прочность соединения, называемая аффинитетом, может быть количественно измерена с помощью определения константы ассоциации. Существует также термин авидности антител, который употребляется для описания суммарной силы взаимодействия поливалентного антитела с полидетерминантным антигеном.
Реакция антиген — антитело протекает в две фазы, которые различаются между собой по механизму и скорости. Первая фаза — специфическое соединение активного центра антитела с соответствующими группами антигена или гаптена; вторая — неспецифическая фаза, следующая за первой, — визуально наблюдаемая реакция. При взаимодействии антител с простыми гаптенами вторая фаза, как правило, отсутствует. При некоторых условиях, например в отсутствие солей, первая фаза может осуществиться, а вторая — нет. Первая фаза протекает всегда быстро, а вторая иногда очень медленно. Соединение антигена с антителом обратимо; прочность соединения, называемая аффинитетом, может быть количественно измерена с помощью определения константы ассоциации. Существует также термин авидности антител, который употребляется для описания суммарной силы взаимодействия поливалентного антитела с полидетерминантным антигеном.
 При изучении механизма взаимодействия антител с антигеном с помощью спектрополяриметрии и других физико химических методов установлено, что в момент связывания антителом гаптена возникает конформационная перестройка молекулы антитела. При этом молекула антитела становится более устойчивой к действию различных денатурирующих агентов, а также и к гидролизу протеолитическими ферментами. Очевидно, в процессе связывания детерминантной группы антигена происходит адаптационная перестройка активного центра антитела. Взаимодействие антитела с молекулой антигена сопровождается, в свою очередь, изменениями пространственной структуры антигена. Так, метмиоглобин превращается в апомиоглобин в результате комплексообразования с антителом, направленным к апомиоглобину, а лишенная активности β галактозидаза — в активный фермент в результате реакции с антителами к активной форме β галактозидазы. Таким образом, при взаимодействии антигена с антителом оба соединения оказывают взаимное влияние на собственную пространственную конформацию. Возникающие конформационные изменения имеют обратимый характер. Извлеченные из иммунных комплексов антитела сохраняют антигенсвязывающую активность и не отличаются по химическим и физическим свойствам от нативных антител.
При изучении механизма взаимодействия антител с антигеном с помощью спектрополяриметрии и других физико химических методов установлено, что в момент связывания антителом гаптена возникает конформационная перестройка молекулы антитела. При этом молекула антитела становится более устойчивой к действию различных денатурирующих агентов, а также и к гидролизу протеолитическими ферментами. Очевидно, в процессе связывания детерминантной группы антигена происходит адаптационная перестройка активного центра антитела. Взаимодействие антитела с молекулой антигена сопровождается, в свою очередь, изменениями пространственной структуры антигена. Так, метмиоглобин превращается в апомиоглобин в результате комплексообразования с антителом, направленным к апомиоглобину, а лишенная активности β галактозидаза — в активный фермент в результате реакции с антителами к активной форме β галактозидазы. Таким образом, при взаимодействии антигена с антителом оба соединения оказывают взаимное влияние на собственную пространственную конформацию. Возникающие конформационные изменения имеют обратимый характер. Извлеченные из иммунных комплексов антитела сохраняют антигенсвязывающую активность и не отличаются по химическим и физическим свойствам от нативных антител.
 Характер реакций, протекающих во второй фазе А. — а. р. , определяется в значительной мере физическими свойствами антигена и проявляется в виде нескольких основных феноменов (агглютинации, нейтрализации токсинов и преципитации). Феномен агглютинации заключается в том, что микроорганизмы, животные клетки или другие корпускулярные антигенные частицы, находящиеся во взвеси, под влиянием антител склеиваются между собой. Реакция агглютинации нашла широкое применение для определения групп крови человека, резус фактора, количественного определения антител и антигенов. Реакция нейтрализации токсинов основана на свойствах антитоксинов (антител против токсинов), которые, соединяясь с соответствующими токсическими веществами, нейтрализуют их. Степень нейтрализации может быть учтена посредством введения восприимчивому животному смеси токсин — антитоксин. Количество антитоксина в иммунной сыворотке характеризуют тем количеством минимальных смертельных доз токсина, которое может быть нейтрализовано определенным количеством сыворотки. Реакцией нейтрализации пользуются для определения концентрации токсинов возбудителей дифтерии, столбняка и др. Для этого применяют стандартизированные антитоксические сыворотки. Феномен преципитации заключается в образовании нерастворимых комплексов антиген — антитело в результате соединения растворимого антигена со специфическими антителами и выпадании этого комплекса в осадок. Особый случай реакции преципитации — реакция иммунной флоккуляции, которая происходит только в относительно узком диапазоне концентраций антигена, а при незначительном избытке антител и антигена образуются растворимые комплексы. Реакцию преципитации используют для количественного определения антигенов и антител, концентрации иммуноглобулинов различных классов в крови людей, в судебно медицинской экспертизе для определения видовой принадлежности белков сыворотки крови в реакции Чистовича — Уленгута.
Характер реакций, протекающих во второй фазе А. — а. р. , определяется в значительной мере физическими свойствами антигена и проявляется в виде нескольких основных феноменов (агглютинации, нейтрализации токсинов и преципитации). Феномен агглютинации заключается в том, что микроорганизмы, животные клетки или другие корпускулярные антигенные частицы, находящиеся во взвеси, под влиянием антител склеиваются между собой. Реакция агглютинации нашла широкое применение для определения групп крови человека, резус фактора, количественного определения антител и антигенов. Реакция нейтрализации токсинов основана на свойствах антитоксинов (антител против токсинов), которые, соединяясь с соответствующими токсическими веществами, нейтрализуют их. Степень нейтрализации может быть учтена посредством введения восприимчивому животному смеси токсин — антитоксин. Количество антитоксина в иммунной сыворотке характеризуют тем количеством минимальных смертельных доз токсина, которое может быть нейтрализовано определенным количеством сыворотки. Реакцией нейтрализации пользуются для определения концентрации токсинов возбудителей дифтерии, столбняка и др. Для этого применяют стандартизированные антитоксические сыворотки. Феномен преципитации заключается в образовании нерастворимых комплексов антиген — антитело в результате соединения растворимого антигена со специфическими антителами и выпадании этого комплекса в осадок. Особый случай реакции преципитации — реакция иммунной флоккуляции, которая происходит только в относительно узком диапазоне концентраций антигена, а при незначительном избытке антител и антигена образуются растворимые комплексы. Реакцию преципитации используют для количественного определения антигенов и антител, концентрации иммуноглобулинов различных классов в крови людей, в судебно медицинской экспертизе для определения видовой принадлежности белков сыворотки крови в реакции Чистовича — Уленгута.
 Способность антител соединять антигенные частицы в крупные конгломераты (агглютинация бактерийных и других клеток, преципитация растворенных антигенов) обусловливается наличием по крайней мере двух активных центров в молекуле антитела. Одна специфическая группа соединяется с одной антигенной детерминантой, другая — с аналогичной детерминантой другой антигенной частицы. Двухвалентность антител обеспечивает возможность соединения неограниченного числа антигенных частиц в конгломераты. При различном числе антигенных детерминант на молекуле антигена характер структуры конгломератов комплекса антиген — антитело может быть разным. При избытке антигена или антител крупные конгломераты вообще не возникают вследствие заполнения реагирующих участков молекул избыточным количеством второго компонента.
Способность антител соединять антигенные частицы в крупные конгломераты (агглютинация бактерийных и других клеток, преципитация растворенных антигенов) обусловливается наличием по крайней мере двух активных центров в молекуле антитела. Одна специфическая группа соединяется с одной антигенной детерминантой, другая — с аналогичной детерминантой другой антигенной частицы. Двухвалентность антител обеспечивает возможность соединения неограниченного числа антигенных частиц в конгломераты. При различном числе антигенных детерминант на молекуле антигена характер структуры конгломератов комплекса антиген — антитело может быть разным. При избытке антигена или антител крупные конгломераты вообще не возникают вследствие заполнения реагирующих участков молекул избыточным количеством второго компонента.
 Первичный и вторичный иммунный ответ иммунная память. Иммунная система обладает двумя поистине удивительными свойствами: специфическим распознаванием и иммунной памятью. Под последней понимают способность развивать качественно и количественно более эффективный иммунный ответ при повторном контакте с тем же патогеном. Согласно этому различают первичный и вторичный иммунный ответ. Первичный иммунный ответ реализуется при первом контакте с незнакомым антигеном, а вторичный – при повторном. Вторичный иммунный ответ является более совершенным, так как осуществляется на качественно более высоком уровне из за наличия преформированных иммунных факторов, отражающих генетическую адаптацию к патогену (уже имеются готовые гены специфических иммуноглобулинов и антиген распознающих рецепторов Т клеток). Действительно, здоровые люди не болеют дважды многими инфекционными заболеваниями, так как при повторном заражении реализуется вторичный иммунный ответ, при котором отсутствует длительная воспалительная фаза, а в работу сразу же вступают иммунные факторы – специфические лимфоциты и антитела.
Первичный и вторичный иммунный ответ иммунная память. Иммунная система обладает двумя поистине удивительными свойствами: специфическим распознаванием и иммунной памятью. Под последней понимают способность развивать качественно и количественно более эффективный иммунный ответ при повторном контакте с тем же патогеном. Согласно этому различают первичный и вторичный иммунный ответ. Первичный иммунный ответ реализуется при первом контакте с незнакомым антигеном, а вторичный – при повторном. Вторичный иммунный ответ является более совершенным, так как осуществляется на качественно более высоком уровне из за наличия преформированных иммунных факторов, отражающих генетическую адаптацию к патогену (уже имеются готовые гены специфических иммуноглобулинов и антиген распознающих рецепторов Т клеток). Действительно, здоровые люди не болеют дважды многими инфекционными заболеваниями, так как при повторном заражении реализуется вторичный иммунный ответ, при котором отсутствует длительная воспалительная фаза, а в работу сразу же вступают иммунные факторы – специфические лимфоциты и антитела.
 Вторичный иммунный ответ характеризуется следующими признаками: • 1. Более ранним развитием, иногда – даже молниеносным. • 2. Меньшей дозой антигена, необходимой для достижения оптимального иммунного ответа. • 3. Увеличением силы и продолжительности иммунного ответа за счёт более интенсивной продукции цитокинов (Тh 1 или Th 2 профиля, в зависимости от природы патогена). • 4. Усилением клеточных иммунных реакций за счёт более интенсивного образования специфических Т хелперов 1 типа и цитотоксических Т лимфоцитов. • 5. Усилением образования антител за счёт формирования большего количества Т хелперов 2 типа и плазматических клеток. • 6. Повышением специфичности распознавания иммуногенных пептидов Т лимфоцитами за счёт увеличения аффинности их антиген специфических рецепторов. • 7. Повышением специфичности синтезируемых антител за счёт изначальной продукции Ig. G высокой аффинности/авидности. Следует отметить, что невозможность формирования эффективной иммунной памяти является одним из характерных симптомов иммунодефицитных заболеваний человека. Так, у пациентов с гипоиммуноглобулинемией наблюдается феномен множественных эпизодов т. н. детских инфекций, так как после перенесённых инфекционных болезней не формируется защитный титр антител. Больные с дефектами клеточного иммунитета также не формируют иммунную память на Т зависимые антигены, что проявляется отсутствием сероконверсии после инфекций и вакцинаций, однако общие концентрации иммуноглобулинов в их сыворотке крови могут быть нормальными.
Вторичный иммунный ответ характеризуется следующими признаками: • 1. Более ранним развитием, иногда – даже молниеносным. • 2. Меньшей дозой антигена, необходимой для достижения оптимального иммунного ответа. • 3. Увеличением силы и продолжительности иммунного ответа за счёт более интенсивной продукции цитокинов (Тh 1 или Th 2 профиля, в зависимости от природы патогена). • 4. Усилением клеточных иммунных реакций за счёт более интенсивного образования специфических Т хелперов 1 типа и цитотоксических Т лимфоцитов. • 5. Усилением образования антител за счёт формирования большего количества Т хелперов 2 типа и плазматических клеток. • 6. Повышением специфичности распознавания иммуногенных пептидов Т лимфоцитами за счёт увеличения аффинности их антиген специфических рецепторов. • 7. Повышением специфичности синтезируемых антител за счёт изначальной продукции Ig. G высокой аффинности/авидности. Следует отметить, что невозможность формирования эффективной иммунной памяти является одним из характерных симптомов иммунодефицитных заболеваний человека. Так, у пациентов с гипоиммуноглобулинемией наблюдается феномен множественных эпизодов т. н. детских инфекций, так как после перенесённых инфекционных болезней не формируется защитный титр антител. Больные с дефектами клеточного иммунитета также не формируют иммунную память на Т зависимые антигены, что проявляется отсутствием сероконверсии после инфекций и вакцинаций, однако общие концентрации иммуноглобулинов в их сыворотке крови могут быть нормальными.
 ИММУНОЛОГИЧЕСКАЯ ПАМЯТЬ способность иммунной системы организма после первого взаимодействия с антигеном специфически отвечать на его повторное введение. Наряду со специфичностью, И. п. — важнейшее свойство иммунного ответа. Позитивная И. п. проявляется как ускоренный и усиленный специфич. ответ на повторное введение антигена. При первичном гуморальном иммунном ответе после введения антигена проходит неск. дней (латентный период) до появления в крови антител. Затем наблюдается постепенное увеличение кол ва антител до максимума с последующим снижением. При вторичном ответе на ту же дозу антигена латентный период сокращается, кривая увеличения антител становится круче и выше, а её снижение происходит медленнее. В клеточном иммунитете И. п. проявляется ускоренным отторжением вторичного трансплантата и более интенсивной воспалительно нек ротич. реакцией на повторное внутрикож ное введение антигена. Позитивная И. п. к антигенным компонентам окружающей среды лежит в основе аллергич. заболеваний, а к резус антигену (возникает при резус несовместимой беременности)— в основе гемолитич. болезни новорождённых. Негативная И. п. — это естеств. и приобретённая иммунологич. толерантность, проявляющаяся ослабленным ответом или его полным отсутствием как на первое, так и на повторное введение антигена. Нарушение негативной И. п. к собств. антигенам организма является патогенетич. механизмом нек рых аутоиммунных заболеваний. Выработка негативной И. п. — наиб, перспективный приём преодоления гистонесовместимости при трансплантации органов и тканей. И. п. при ответе на разные антигены различна. Она может быть краткосрочной (дни, недели), долговременной (месяцы, годы) и пожизненной. Напр. , человек, иммунизированный столбнячным анатоксином или живой полиомиелитной вакциной, сохраняет И. п. св. 10 лет. И. п. представляет собой разновидность биол. памяти, принципиально отличающуюся от нейрологич. (мозговой) памяти по способу её введения, уровню хранения и объёму информации. Осн. носители И. п. — долгоживущие Т и В лимфоциты, к рые образуются при первичном иммунном ответе и продолжают циркулировать с кровью и лимфой в качестве специфич. предшественников антиген реактивных лимфоцитов. При вторичном ответе эти клетки размножаются, обеспечивая быстрое увеличение клона антителообразующих или антиген реактивных лимфоцитов данной специфичности. Из др. механизмов И. п. (кроме клеток памяти) определ. значение имеют иммунные комплексы, цитоф ильные антитела, а также блокирующие и антиидиотипич. антитела. И. п. можно перенести от иммунного донора неиммунному реципиенту, переливая живые лимфоциты или вводя лимфоцитарный экстракт, содержащий «фактор переноса» или иммунную РНК. Ввод информации в И. п. осуществляется антигеном, хотя информация об антигене к этому моменту уже существует в генетич. памяти, возникшей в филогенезе и в т. н. онтогенетич. памяти, появившись в эмбриогенезе при дифференцировке лимфоидных клеток. Информац. ёмкость И. п. — до 106— 107 бит на организм. У позвоночных включается более 100 бит в сутки. В филогенезе И. п. возникла одновременно с нейрологич. памятью. Полной ёмкости И. п. достигает у взрослых животных со зрелой иммунной системой (у новорождённых и старых особей она ослаблена).
ИММУНОЛОГИЧЕСКАЯ ПАМЯТЬ способность иммунной системы организма после первого взаимодействия с антигеном специфически отвечать на его повторное введение. Наряду со специфичностью, И. п. — важнейшее свойство иммунного ответа. Позитивная И. п. проявляется как ускоренный и усиленный специфич. ответ на повторное введение антигена. При первичном гуморальном иммунном ответе после введения антигена проходит неск. дней (латентный период) до появления в крови антител. Затем наблюдается постепенное увеличение кол ва антител до максимума с последующим снижением. При вторичном ответе на ту же дозу антигена латентный период сокращается, кривая увеличения антител становится круче и выше, а её снижение происходит медленнее. В клеточном иммунитете И. п. проявляется ускоренным отторжением вторичного трансплантата и более интенсивной воспалительно нек ротич. реакцией на повторное внутрикож ное введение антигена. Позитивная И. п. к антигенным компонентам окружающей среды лежит в основе аллергич. заболеваний, а к резус антигену (возникает при резус несовместимой беременности)— в основе гемолитич. болезни новорождённых. Негативная И. п. — это естеств. и приобретённая иммунологич. толерантность, проявляющаяся ослабленным ответом или его полным отсутствием как на первое, так и на повторное введение антигена. Нарушение негативной И. п. к собств. антигенам организма является патогенетич. механизмом нек рых аутоиммунных заболеваний. Выработка негативной И. п. — наиб, перспективный приём преодоления гистонесовместимости при трансплантации органов и тканей. И. п. при ответе на разные антигены различна. Она может быть краткосрочной (дни, недели), долговременной (месяцы, годы) и пожизненной. Напр. , человек, иммунизированный столбнячным анатоксином или живой полиомиелитной вакциной, сохраняет И. п. св. 10 лет. И. п. представляет собой разновидность биол. памяти, принципиально отличающуюся от нейрологич. (мозговой) памяти по способу её введения, уровню хранения и объёму информации. Осн. носители И. п. — долгоживущие Т и В лимфоциты, к рые образуются при первичном иммунном ответе и продолжают циркулировать с кровью и лимфой в качестве специфич. предшественников антиген реактивных лимфоцитов. При вторичном ответе эти клетки размножаются, обеспечивая быстрое увеличение клона антителообразующих или антиген реактивных лимфоцитов данной специфичности. Из др. механизмов И. п. (кроме клеток памяти) определ. значение имеют иммунные комплексы, цитоф ильные антитела, а также блокирующие и антиидиотипич. антитела. И. п. можно перенести от иммунного донора неиммунному реципиенту, переливая живые лимфоциты или вводя лимфоцитарный экстракт, содержащий «фактор переноса» или иммунную РНК. Ввод информации в И. п. осуществляется антигеном, хотя информация об антигене к этому моменту уже существует в генетич. памяти, возникшей в филогенезе и в т. н. онтогенетич. памяти, появившись в эмбриогенезе при дифференцировке лимфоидных клеток. Информац. ёмкость И. п. — до 106— 107 бит на организм. У позвоночных включается более 100 бит в сутки. В филогенезе И. п. возникла одновременно с нейрологич. памятью. Полной ёмкости И. п. достигает у взрослых животных со зрелой иммунной системой (у новорождённых и старых особей она ослаблена).
 Комплемент называют сложный комплекс белков, действующий совместно для удаления внеклеточных форм патогена; система активируется спонтанно определенными патогенами или комплексом антиген антитело. Активированные белки либо непосредственно разрушают патоген (киллерное действие), либо обеспечивают лучшее их поглощение фагоцитами ( опсонизирующее действие ); либо выполняют функцию хемотаксических факторов , привлекая в зону проникновения патогена клетки воспаления. Комплемент включает около 20 взаимодействующих компонентов: С 1 (комплекс из трех белков), С 2, СЗ, …, С 9, фактор В, фактор D и ряд регуляторных белков. Все эти компоненты — растворимые белки с мол. массой от 24 000 до 400 000, циркулирующие в крови и тканевой жидкости. Белки комплемента синтезируются в основном в печени и составляют приблизительно 5 % от всей глобулиновой фракции плазмы крови Комплекс белков комплемента формирует каскадные системы, обнаруженные в плазме крови. Для этих систем характерно формирование быстрого, многократно усиленного ответа на первичный сигнал за счет каскадного процесса. В этом случае продукт одной реакции служит катализатором последующей, что в конечном итоге приводит к лизису клетки или микроорганизма.
Комплемент называют сложный комплекс белков, действующий совместно для удаления внеклеточных форм патогена; система активируется спонтанно определенными патогенами или комплексом антиген антитело. Активированные белки либо непосредственно разрушают патоген (киллерное действие), либо обеспечивают лучшее их поглощение фагоцитами ( опсонизирующее действие ); либо выполняют функцию хемотаксических факторов , привлекая в зону проникновения патогена клетки воспаления. Комплемент включает около 20 взаимодействующих компонентов: С 1 (комплекс из трех белков), С 2, СЗ, …, С 9, фактор В, фактор D и ряд регуляторных белков. Все эти компоненты — растворимые белки с мол. массой от 24 000 до 400 000, циркулирующие в крови и тканевой жидкости. Белки комплемента синтезируются в основном в печени и составляют приблизительно 5 % от всей глобулиновой фракции плазмы крови Комплекс белков комплемента формирует каскадные системы, обнаруженные в плазме крови. Для этих систем характерно формирование быстрого, многократно усиленного ответа на первичный сигнал за счет каскадного процесса. В этом случае продукт одной реакции служит катализатором последующей, что в конечном итоге приводит к лизису клетки или микроорганизма.
 Пути активации комплемента Система комплемента работает как биохимический каскад реакций. Комплемент активируется тремя биохимическими путями: классическим, альтернативным и лектиновым путем. Все три пути активации производят разные варианты C 3 конвертазы (белка, расщепляющего С 3). Классический путь (он был открыт первым, но эволюционно является новым) требует антител для активации (специфический иммунный ответ, приобретённый иммунитет), в то время как альтернативный и лектиновый пути могут быть активизированы антигенами без присутствия антител (неспецифический иммунный ответ, врождённый иммунитет). Итог активации комплемента во всех трёх случаях одинаков: C 3 конвертаза гидролизует СЗ, создавая C 3 a и C 3 b и вызывая каскад дальнейшего гидролиза элементов системы комплемента и событий активации. В классическом пути для активации С 3 конвертазы необходимо образование комплекса С 4 b. C 2 a. Этот комплекс образуется при расщеплении С 2 и С 4 С 1 комплексом. С 1 комплекс, в свою очередь, для активации должен связаться с иммуноглобулинами класса М или G. C 3 b связывается с поверхностью болезнетворных микроорганизмов, что приводит к большей «заинтересованности» фагоцитов к связанным с СЗb клеткам (опсонизация). C 5 a — важный хемоаттрактант, помогающий привлекать в район активации системы комплемента новые иммунные клетки. И C 3 a, и C 5 a имеют анафилотоксическую активность, непосредственно вызывая дегрануляцию тучных клеток (как следствие — выделение медиаторов воспаления). C 5 b начинает формирование мембраноатакующих комплексов (МАК), состоящим из C 5 b, C 6, C 7, C 8 и полимерного C 9. МАК — цитолитический конечный продукт активации системы комплемента. МАК формирует трансмембранный канал, вызывающий осмотический лизис клетки мишени. Макрофаги поглощают помеченные системой комплемента болезнетворные микроорганизмы.
Пути активации комплемента Система комплемента работает как биохимический каскад реакций. Комплемент активируется тремя биохимическими путями: классическим, альтернативным и лектиновым путем. Все три пути активации производят разные варианты C 3 конвертазы (белка, расщепляющего С 3). Классический путь (он был открыт первым, но эволюционно является новым) требует антител для активации (специфический иммунный ответ, приобретённый иммунитет), в то время как альтернативный и лектиновый пути могут быть активизированы антигенами без присутствия антител (неспецифический иммунный ответ, врождённый иммунитет). Итог активации комплемента во всех трёх случаях одинаков: C 3 конвертаза гидролизует СЗ, создавая C 3 a и C 3 b и вызывая каскад дальнейшего гидролиза элементов системы комплемента и событий активации. В классическом пути для активации С 3 конвертазы необходимо образование комплекса С 4 b. C 2 a. Этот комплекс образуется при расщеплении С 2 и С 4 С 1 комплексом. С 1 комплекс, в свою очередь, для активации должен связаться с иммуноглобулинами класса М или G. C 3 b связывается с поверхностью болезнетворных микроорганизмов, что приводит к большей «заинтересованности» фагоцитов к связанным с СЗb клеткам (опсонизация). C 5 a — важный хемоаттрактант, помогающий привлекать в район активации системы комплемента новые иммунные клетки. И C 3 a, и C 5 a имеют анафилотоксическую активность, непосредственно вызывая дегрануляцию тучных клеток (как следствие — выделение медиаторов воспаления). C 5 b начинает формирование мембраноатакующих комплексов (МАК), состоящим из C 5 b, C 6, C 7, C 8 и полимерного C 9. МАК — цитолитический конечный продукт активации системы комплемента. МАК формирует трансмембранный канал, вызывающий осмотический лизис клетки мишени. Макрофаги поглощают помеченные системой комплемента болезнетворные микроорганизмы.
 Биологические функции • • • Опсонизирующая функция. Сразу вслед за активацией системы комплемента образуются опсонизирующие компоненты, которые покрывают патогенные организмы или иммунные комплексы, привлекая фагоцитов. Наличие на поверхности фагоцитирующих клеток рецептора к С 3 b усиливает их прикрепление к опсонизированным бактериям и активирует процесс поглощения. Такое более тесное прикрепление С 3 b связанных клеток или иммунных комплексов к фагоцитирующим клеткам получило название феномена иммунного прикрепления. Солюбилизация (т. е. растворение) иммунных комплексов (молекулой C 3 b). При недостаточности комплемента развивается иммунокомплексная патология (СКВ подобные состояния). [СКВ = системная красная волчанка] Участие в воспалительных реакциях. Активация системы комплемента приводит к выделению из тканевых базофилов (тучных клеток) и базофильных гранулоцитов крови биологически активных веществ (гистамина, серотонина, брадикинина), которые стимулируют воспалительную реакцию (медиаторов воспаления). Биологически активные компоненты, которые образуются при расщеплении С 3 и С 5, приводят к высвобождению вазоактивных аминов, таких как гистамин, из тканевых базофилов (тучных клеток) и базофильных гранулоцитов крови. В свою очередь это сопровождается расслаблением гладкой мускулатуры и сокращением клеток эндотелия капилляров, усилением сосудистой проницаемости. Фрагмент С 5 а и другие продукты активации комплемента содействуют хемотаксису, агрегации и дегрануляции нейтрофилов и образованию свободных радикалов кислорода. Введение С 5 а животным приводило к артериальной гипотонии, сужению легочных сосудов и повышению проницаемости сосудов из за повреждения эндотелия. Фукнции С 3 а: выступать в роли хемотаксического фактора, вызывая миграцию нейтрофилов по направлению к месту его высвобождения; индуцировать прикрепление нейтрофилов к эндотелию сосудов и друг к другу; активировать нейтрофилы, вызывая в них развитие респираторного взрыва и дегрануляцию; стимулировать продукцию нейтрофилами лейкотриенов. Цитотоксическая, или литическая функция. В конечной стадии активации системы комплемента образуется мембраноатакующий комплекс (МАК) из поздних компонентов комплемента, который атакует мембрану бактериальной или любой другой клетки и разрушает ее. Фактор С 3 е, образующийся при расщеплении фактора С 3 b, обладает способностью вызывать миграцию нейтрофилов из костного мозга, и в таком случае быть причиной лейкоцитоза.
Биологические функции • • • Опсонизирующая функция. Сразу вслед за активацией системы комплемента образуются опсонизирующие компоненты, которые покрывают патогенные организмы или иммунные комплексы, привлекая фагоцитов. Наличие на поверхности фагоцитирующих клеток рецептора к С 3 b усиливает их прикрепление к опсонизированным бактериям и активирует процесс поглощения. Такое более тесное прикрепление С 3 b связанных клеток или иммунных комплексов к фагоцитирующим клеткам получило название феномена иммунного прикрепления. Солюбилизация (т. е. растворение) иммунных комплексов (молекулой C 3 b). При недостаточности комплемента развивается иммунокомплексная патология (СКВ подобные состояния). [СКВ = системная красная волчанка] Участие в воспалительных реакциях. Активация системы комплемента приводит к выделению из тканевых базофилов (тучных клеток) и базофильных гранулоцитов крови биологически активных веществ (гистамина, серотонина, брадикинина), которые стимулируют воспалительную реакцию (медиаторов воспаления). Биологически активные компоненты, которые образуются при расщеплении С 3 и С 5, приводят к высвобождению вазоактивных аминов, таких как гистамин, из тканевых базофилов (тучных клеток) и базофильных гранулоцитов крови. В свою очередь это сопровождается расслаблением гладкой мускулатуры и сокращением клеток эндотелия капилляров, усилением сосудистой проницаемости. Фрагмент С 5 а и другие продукты активации комплемента содействуют хемотаксису, агрегации и дегрануляции нейтрофилов и образованию свободных радикалов кислорода. Введение С 5 а животным приводило к артериальной гипотонии, сужению легочных сосудов и повышению проницаемости сосудов из за повреждения эндотелия. Фукнции С 3 а: выступать в роли хемотаксического фактора, вызывая миграцию нейтрофилов по направлению к месту его высвобождения; индуцировать прикрепление нейтрофилов к эндотелию сосудов и друг к другу; активировать нейтрофилы, вызывая в них развитие респираторного взрыва и дегрануляцию; стимулировать продукцию нейтрофилами лейкотриенов. Цитотоксическая, или литическая функция. В конечной стадии активации системы комплемента образуется мембраноатакующий комплекс (МАК) из поздних компонентов комплемента, который атакует мембрану бактериальной или любой другой клетки и разрушает ее. Фактор С 3 е, образующийся при расщеплении фактора С 3 b, обладает способностью вызывать миграцию нейтрофилов из костного мозга, и в таком случае быть причиной лейкоцитоза.
 Первичные и вторичные иммунодефициты. Диагностика, лечение. Иммунодефициты — это нарушения нор мального иммунного статуса, обусловлен ные дефектом одного или нескольких механизмов иммунного ответа. Различают первичные, или врожденные (генетические), и вторичные, или приобре тенные, иммунодефициты.
Первичные и вторичные иммунодефициты. Диагностика, лечение. Иммунодефициты — это нарушения нор мального иммунного статуса, обусловлен ные дефектом одного или нескольких механизмов иммунного ответа. Различают первичные, или врожденные (генетические), и вторичные, или приобре тенные, иммунодефициты.
 Первичные, или врожденные, иммунодефициты. В качестве первичных иммунодефицитов выделяют такие состояния, при которых нарушение иммунных гуморальных и кле точных механизмов связано с генетическим блоком, т. е. генетически обусловлено неспо собностью организма реализовывать то или иное звено иммунологической реактивности. Расстройства иммунной системы могут затра гивать как основные специфические звенья в функционировании иммунной системы, так и факторы, определяющие неспецифическую резистентность. Возможны комбинирован ные и селективные варианты иммунных рас стройств. В зависимости от уровня и характера нарушений различают гуморальные, клеточ ные и комбинированные иммунодефициты. Врожденные иммунодефицитные синдро мы и заболевания представляют собой до вольно редкое явление. Причинами врожден ных иммунодефицитов могут быть удвоение хромосом, точечные мутации, дефект фер ментов обмена нуклеиновых кислот, генети чески обусловленные нарушения мембран, повреждения генома в эмбриональном пе риодеи др. Как правило, первичные имму нодефицита проявляются на ранних этапах постнатального периода и наследуются по аутосомно рецессивному типу. Проявляться первичные иммунодефициты могут в виде недостаточности фагоцитоза, системы комп лемента , гуморального иммунитета (В системы), клеточного иммунитета (Т системы) или же в виде комбинированной иммунологичес койнедостаточности.
Первичные, или врожденные, иммунодефициты. В качестве первичных иммунодефицитов выделяют такие состояния, при которых нарушение иммунных гуморальных и кле точных механизмов связано с генетическим блоком, т. е. генетически обусловлено неспо собностью организма реализовывать то или иное звено иммунологической реактивности. Расстройства иммунной системы могут затра гивать как основные специфические звенья в функционировании иммунной системы, так и факторы, определяющие неспецифическую резистентность. Возможны комбинирован ные и селективные варианты иммунных рас стройств. В зависимости от уровня и характера нарушений различают гуморальные, клеточ ные и комбинированные иммунодефициты. Врожденные иммунодефицитные синдро мы и заболевания представляют собой до вольно редкое явление. Причинами врожден ных иммунодефицитов могут быть удвоение хромосом, точечные мутации, дефект фер ментов обмена нуклеиновых кислот, генети чески обусловленные нарушения мембран, повреждения генома в эмбриональном пе риодеи др. Как правило, первичные имму нодефицита проявляются на ранних этапах постнатального периода и наследуются по аутосомно рецессивному типу. Проявляться первичные иммунодефициты могут в виде недостаточности фагоцитоза, системы комп лемента , гуморального иммунитета (В системы), клеточного иммунитета (Т системы) или же в виде комбинированной иммунологичес койнедостаточности.
 Вторичные, или приобретенные, иммунодефициты Вторичные иммунодефициты в отличие от первичных развиваются у лиц с нормально функционировавшей от рождения иммунной системой. Они формируются под воздействи ем окружающей среды на уровне фенотипа и обусловлены нарушением функции иммунной системы в результате различных заболеваний или неблагоприятных воздействий на орга низм. При вторичных иммунодефицитах могут поражаться Т и В системы иммунитета, фак торы еспецифической резистентности, воз можны также их сочетания. н Вторичные имму нодефицита встречаются значительно чаще, чем первичные. Вторичные иммунодефицита, как правило, преходящи и поддаются иммунокоррекции, т. е. восстановлению нормальной деятельности иммунной системы. Вторичные иммунодефицита могут быть: после перенесенных инфекций (особенно ви русных) и нвазий и (протозойные и гельминтозы); при ожоговой болезни; при уремии; при опухолях; при нарушении обмена веществ и истощении; при дисбиозах; при тяжелых травмах, обширных хирургических операци ях , особенно выполняемых под общим нар козом; при о блучении, действии химических веществ; при старении, а также медикамен тозные , связанные с приемом лекарств. По времени возникновения выделяют ан тенатальные (например, ненаследственные формы синдрома Ди. Джорджи), перинаталь ные (например, нейтропения новорожденного, вызванная изосенсибилизацией матери к антигенам нейтрофилов плода) и постнатальные вторичные иммунодефициты. По клиническому течению выделяют ком пенсированную, субкомпенсированную и декомпенсированную формы вторичных иммуноде фицитов. Компенсированная форма сопро вождается повышенной восприимчивостью организма к инфекционным агентам, вы зывающим оппортунистические инфекции. Субкомпенсированная форма характеризует ся склонностью к хронизации инфекционных процессов. Декомпенсированная форма про является в виде генерализованных инфекций, вызванных условно патогенными микробами (УПМ) и злокачественными новообразова ниями.
Вторичные, или приобретенные, иммунодефициты Вторичные иммунодефициты в отличие от первичных развиваются у лиц с нормально функционировавшей от рождения иммунной системой. Они формируются под воздействи ем окружающей среды на уровне фенотипа и обусловлены нарушением функции иммунной системы в результате различных заболеваний или неблагоприятных воздействий на орга низм. При вторичных иммунодефицитах могут поражаться Т и В системы иммунитета, фак торы еспецифической резистентности, воз можны также их сочетания. н Вторичные имму нодефицита встречаются значительно чаще, чем первичные. Вторичные иммунодефицита, как правило, преходящи и поддаются иммунокоррекции, т. е. восстановлению нормальной деятельности иммунной системы. Вторичные иммунодефицита могут быть: после перенесенных инфекций (особенно ви русных) и нвазий и (протозойные и гельминтозы); при ожоговой болезни; при уремии; при опухолях; при нарушении обмена веществ и истощении; при дисбиозах; при тяжелых травмах, обширных хирургических операци ях , особенно выполняемых под общим нар козом; при о блучении, действии химических веществ; при старении, а также медикамен тозные , связанные с приемом лекарств. По времени возникновения выделяют ан тенатальные (например, ненаследственные формы синдрома Ди. Джорджи), перинаталь ные (например, нейтропения новорожденного, вызванная изосенсибилизацией матери к антигенам нейтрофилов плода) и постнатальные вторичные иммунодефициты. По клиническому течению выделяют ком пенсированную, субкомпенсированную и декомпенсированную формы вторичных иммуноде фицитов. Компенсированная форма сопро вождается повышенной восприимчивостью организма к инфекционным агентам, вы зывающим оппортунистические инфекции. Субкомпенсированная форма характеризует ся склонностью к хронизации инфекционных процессов. Декомпенсированная форма про является в виде генерализованных инфекций, вызванных условно патогенными микробами (УПМ) и злокачественными новообразова ниями.
 Известно разделение вторичных иммунодефицитов на: Физиологические, новорожденные, пубертатного периода, беременности и лактации, старения, биоритмичности, экологические, сезонные, эндогенные интоксикации, радиационные, СВЧ, патологические, постинфекционные, стрессовые, регуляторно метаболические, медикаментозные, онкологические. Иммунодефициты, как первичные, так и особенно вторичные, широко распростране ны среди людей. Они являются причиной проявления многих болезней и патологичес ких состояний, поэтому требуют профилак тики и лечения с помощью иммунотропных препаратов. Диагностика и лечение. Диагноз имунодефицитов ставят на основании данных анамнеза, проявления клинических симптомов (наличия оппортунистической инфекции, аллергии, опухолей, пороки развития) и по результатам оценки иммунного статуса. При вторичных иммунодефицитах может страдать как В , так и Т система иммунитета, а также естественные факторы резистентности организма. Вторичные иммунодефициты преходящи и поддаются иммунокоррекции и лечению.
Известно разделение вторичных иммунодефицитов на: Физиологические, новорожденные, пубертатного периода, беременности и лактации, старения, биоритмичности, экологические, сезонные, эндогенные интоксикации, радиационные, СВЧ, патологические, постинфекционные, стрессовые, регуляторно метаболические, медикаментозные, онкологические. Иммунодефициты, как первичные, так и особенно вторичные, широко распростране ны среди людей. Они являются причиной проявления многих болезней и патологичес ких состояний, поэтому требуют профилак тики и лечения с помощью иммунотропных препаратов. Диагностика и лечение. Диагноз имунодефицитов ставят на основании данных анамнеза, проявления клинических симптомов (наличия оппортунистической инфекции, аллергии, опухолей, пороки развития) и по результатам оценки иммунного статуса. При вторичных иммунодефицитах может страдать как В , так и Т система иммунитета, а также естественные факторы резистентности организма. Вторичные иммунодефициты преходящи и поддаются иммунокоррекции и лечению.
 СПИД, ВИЧ Синдром приобретённого иммунного дефицита (СПИД, синдром приобретенного иммунодефицита, англ. AIDS) — состояние, развивающееся на фоне ВИЧ инфекции и характеризующееся падением числа CD 4+ лимфоцитов, множественными оппортунистическими инфекциями, неинфекционными и опухолевыми заболеваниями. ВИЧ передается при прямом контакте слизистых оболочек или крови с биологическими жидкостями, содержащими вирус, например, с кровью, спермой, секретом влагалища или с грудным молоком. ВИЧ инфекция не передается через слюну и слезы, а также бытовым путём. Передача ВИЧ может происходить при анальном, вагинальном или оральном сексе, переливании крови, использовании зараженных игл и шприцев; между матерью и ребёнком во время беременности, родов или при грудном вскармливании через указанные выше биологические жидкости. СПИД является терминальной стадией ВИЧ инфекции.
СПИД, ВИЧ Синдром приобретённого иммунного дефицита (СПИД, синдром приобретенного иммунодефицита, англ. AIDS) — состояние, развивающееся на фоне ВИЧ инфекции и характеризующееся падением числа CD 4+ лимфоцитов, множественными оппортунистическими инфекциями, неинфекционными и опухолевыми заболеваниями. ВИЧ передается при прямом контакте слизистых оболочек или крови с биологическими жидкостями, содержащими вирус, например, с кровью, спермой, секретом влагалища или с грудным молоком. ВИЧ инфекция не передается через слюну и слезы, а также бытовым путём. Передача ВИЧ может происходить при анальном, вагинальном или оральном сексе, переливании крови, использовании зараженных игл и шприцев; между матерью и ребёнком во время беременности, родов или при грудном вскармливании через указанные выше биологические жидкости. СПИД является терминальной стадией ВИЧ инфекции.
 Пути передачи ВИЧ-инфекции • Половой • Инъекционный и инструментальный — при использовании загрязнённых вирусом шприцев, игл, катетеров и т. п. — особенно актуальный и проблематичный в среде лиц, употребляющих инъекционные наркотики (наркомания). Вероятность передачи ВИЧ при использовании общих игл составляет 67 случаев на 10000 инъекций[25]: 21. Этот путь передачи обусловил повсеместное распространение одноразовых шприцев во второй половине XX века. [источник не указан 1115 дней] • Гемотрансфузионный (после переливания инфицированной крови или её компонентов — плазмы, тромбоцитарной, лейкоцитарной или эритроцитарной массы, концентратов крови, факторов свёртывания крови); • Перинатальный (антенатальный, трансплацентарный — от инфицированной матери; интранатальный — при прохождении ребёнка по инфицированным родовым путям матери); • Трансплантационный (пересадка инфицированных органов, костного мозга, искусственная инсеминация инфицированной спермой); • Молочный (заражение ребёнка инфицированным молоком матери); • Профессиональный и бытовой — заражение через повреждённые кожные покровы и слизистые оболочки людей, контактирующих с кровью или некоторыми секретами (слизью из влагалища, грудным молоком, отделяемым из ран, цереброспинальной жидкостью, содержимым трахеи, плевральной полости и др. ) больных ВИЧ инфекцией.
Пути передачи ВИЧ-инфекции • Половой • Инъекционный и инструментальный — при использовании загрязнённых вирусом шприцев, игл, катетеров и т. п. — особенно актуальный и проблематичный в среде лиц, употребляющих инъекционные наркотики (наркомания). Вероятность передачи ВИЧ при использовании общих игл составляет 67 случаев на 10000 инъекций[25]: 21. Этот путь передачи обусловил повсеместное распространение одноразовых шприцев во второй половине XX века. [источник не указан 1115 дней] • Гемотрансфузионный (после переливания инфицированной крови или её компонентов — плазмы, тромбоцитарной, лейкоцитарной или эритроцитарной массы, концентратов крови, факторов свёртывания крови); • Перинатальный (антенатальный, трансплацентарный — от инфицированной матери; интранатальный — при прохождении ребёнка по инфицированным родовым путям матери); • Трансплантационный (пересадка инфицированных органов, костного мозга, искусственная инсеминация инфицированной спермой); • Молочный (заражение ребёнка инфицированным молоком матери); • Профессиональный и бытовой — заражение через повреждённые кожные покровы и слизистые оболочки людей, контактирующих с кровью или некоторыми секретами (слизью из влагалища, грудным молоком, отделяемым из ран, цереброспинальной жидкостью, содержимым трахеи, плевральной полости и др. ) больных ВИЧ инфекцией.
 • • • Классификация ВИЧ-инфекции и СПИДа I — стадия инкубации II — стадия первичных проявлений А — острая лихорадочная фаза Б — бессимптомная фаза В — персистирующая генерализованная лимфаденопатия III — персистирующая генерализованная лимфаденопатия А — потеря массы тела менее 10 %, поверхностные грибковые, бактериальные, вирусные поражения кожи и слизистых оболочек, опоясывающий герпес, повторные фарингиты, синуситы Б — прогрессирующая потеря массы тела более 10 %, необъяснимая диарея или лихорадка более 1 месяца, повторные и/или стойкие бактериальные и протозойные поражения внутренних органов (без диссеминации) или глубокие поражения кожи и слизистых оболочек: повторный или диссеминированный опоясывающий лишай, локализованная саркома Капоши В — генерализованные бактериальные, грибковые, вирусные, протозойные и паразитарные заболевания, пневмоцистная пневмония, кандидоз пищевода, атипичный микобактериоз, внелёгочный туберкулёз, кахексия, диссеминированная саркома Капоши, поражения ЦНС различной этиологии IV — терминальная стадия
• • • Классификация ВИЧ-инфекции и СПИДа I — стадия инкубации II — стадия первичных проявлений А — острая лихорадочная фаза Б — бессимптомная фаза В — персистирующая генерализованная лимфаденопатия III — персистирующая генерализованная лимфаденопатия А — потеря массы тела менее 10 %, поверхностные грибковые, бактериальные, вирусные поражения кожи и слизистых оболочек, опоясывающий герпес, повторные фарингиты, синуситы Б — прогрессирующая потеря массы тела более 10 %, необъяснимая диарея или лихорадка более 1 месяца, повторные и/или стойкие бактериальные и протозойные поражения внутренних органов (без диссеминации) или глубокие поражения кожи и слизистых оболочек: повторный или диссеминированный опоясывающий лишай, локализованная саркома Капоши В — генерализованные бактериальные, грибковые, вирусные, протозойные и паразитарные заболевания, пневмоцистная пневмония, кандидоз пищевода, атипичный микобактериоз, внелёгочный туберкулёз, кахексия, диссеминированная саркома Капоши, поражения ЦНС различной этиологии IV — терминальная стадия
 Применение антигенов и антител с целью предупреждения, диагностики и лечения заболеваний. Для специфической профилактики и лечения инфекционных заболеваний большое значение имеют вакцины и иммунные сыворотки. Специфические иммунные сыворотки используют также как диагностические препараты при определении антигенной структуры возбудителя инфекционного заболевания.
Применение антигенов и антител с целью предупреждения, диагностики и лечения заболеваний. Для специфической профилактики и лечения инфекционных заболеваний большое значение имеют вакцины и иммунные сыворотки. Специфические иммунные сыворотки используют также как диагностические препараты при определении антигенной структуры возбудителя инфекционного заболевания.
 Вакцины. Препараты, введение которых предохраняет от заболевания. Содержат убитые микробы (корпускулярные вакцины), антигены микробов, полученные химическим путем (химические вакцины), или живые ослаб¬ленные микробы (аттенуированные вакцины). Препараты, приготовленные из токсинов, называют анатоксинами. Наилучший защитный эффект получают при введении вакцин, содержащих живые ослабленные микробы. • Живые аттенуированные вакцины содержат живые микробы, вирулентность которых ослаблена при сохранении их иммуногенных свойств (от франц. attenuer — ослаблять, смягчать). Для получения аттенуированных культур микробов используют различные методы. Микробы выращивают на питательных средах, неблагоприятных для их роста и размножения (вакцина Кальметта — Герена при туберкулезе), на микроорганизмы действуют различными физическими и химическими веществами, фагами, антибиотиками, последовательно несколько раз заражают невосприимчивых или маловосприимчивых животных. Некоторые аттенуированные вакцины приготовлены из маловирулентных штаммов микробов, выделенных в разное время у больных людей или животных: штамм EV — для чумной вакцины, штамм № 19 — при бруцеллезе, , штамм Мадрид К — при сыпном тифе. В настоящее время применяют вакцины из живых ослабленных микроорганизмов для профилактики туберкулеза (вакцина БЦЖ), бруцеллеза, туляремии, чумы, гриппа, оспы, полиомиелита. • Убитые вакцины получают, инактивируя микробную взвесь нагреванием, добавлением формалина, спирта, ацетона, облучая ее ультрафиолетовым светом или разрушая ультразвуком. • • Корпускулярные вакцины содержат цельные микробные клетки, убитые нагреванием или с помощью химических веществ. • Химические вакцины готовят путем разрушения микробных клеток с последующим извлечением из них различных антигенных фракций. • Корпускулярные и химические вакцины используют для профилактики брюшного тифа, паратифов, холеры, коклюша и других заболеваний. Однако они менее эффективны, чем вакцины, приготовленные из аттенуированных штаммов бактерий.
Вакцины. Препараты, введение которых предохраняет от заболевания. Содержат убитые микробы (корпускулярные вакцины), антигены микробов, полученные химическим путем (химические вакцины), или живые ослаб¬ленные микробы (аттенуированные вакцины). Препараты, приготовленные из токсинов, называют анатоксинами. Наилучший защитный эффект получают при введении вакцин, содержащих живые ослабленные микробы. • Живые аттенуированные вакцины содержат живые микробы, вирулентность которых ослаблена при сохранении их иммуногенных свойств (от франц. attenuer — ослаблять, смягчать). Для получения аттенуированных культур микробов используют различные методы. Микробы выращивают на питательных средах, неблагоприятных для их роста и размножения (вакцина Кальметта — Герена при туберкулезе), на микроорганизмы действуют различными физическими и химическими веществами, фагами, антибиотиками, последовательно несколько раз заражают невосприимчивых или маловосприимчивых животных. Некоторые аттенуированные вакцины приготовлены из маловирулентных штаммов микробов, выделенных в разное время у больных людей или животных: штамм EV — для чумной вакцины, штамм № 19 — при бруцеллезе, , штамм Мадрид К — при сыпном тифе. В настоящее время применяют вакцины из живых ослабленных микроорганизмов для профилактики туберкулеза (вакцина БЦЖ), бруцеллеза, туляремии, чумы, гриппа, оспы, полиомиелита. • Убитые вакцины получают, инактивируя микробную взвесь нагреванием, добавлением формалина, спирта, ацетона, облучая ее ультрафиолетовым светом или разрушая ультразвуком. • • Корпускулярные вакцины содержат цельные микробные клетки, убитые нагреванием или с помощью химических веществ. • Химические вакцины готовят путем разрушения микробных клеток с последующим извлечением из них различных антигенных фракций. • Корпускулярные и химические вакцины используют для профилактики брюшного тифа, паратифов, холеры, коклюша и других заболеваний. Однако они менее эффективны, чем вакцины, приготовленные из аттенуированных штаммов бактерий.
 Анатоксины. Препараты, полученные из обезвреженных экзотоксинов микробов. Впервые метод приготовления анатоксинов был предложен французским ученым Рамоном. Этот способ применяют и в настоящее время. К фильтрату бульонной культуры микробов, содержащему экзотоксин, добавляют формалин (0, 1— 0, 4% раствор) и выдерживают длительное время в термостате при 37°С. В результате экзотоксин теряет токсические свойства, но сохраняет иммуногенность и антигенность. Анатоксины получены из дифтерийного, столбнячного, ботулинического, стафилококкового экзотоксинов, а также из токсинов возбудителей газовой гангрены, яда некоторых змей и растений. При использовании анатоксинов в организме вырабатывается активный иммунитет (антитоксический). Широко используют для актирной иммунизации против дифтерии и столбняка дифтерийный и столбнячный анатоксины. Стафилококковый анатоксин используют и для лечения заболеваний стафилококковой этиологии. Дифтерийный и столбнячный анатоксины изготовляют в виде отдельных препаратов или комбинированных с другими вакцинами. Как правило, анатоксины выпускают сорбированными на геле гидрата окиси алюминия.
Анатоксины. Препараты, полученные из обезвреженных экзотоксинов микробов. Впервые метод приготовления анатоксинов был предложен французским ученым Рамоном. Этот способ применяют и в настоящее время. К фильтрату бульонной культуры микробов, содержащему экзотоксин, добавляют формалин (0, 1— 0, 4% раствор) и выдерживают длительное время в термостате при 37°С. В результате экзотоксин теряет токсические свойства, но сохраняет иммуногенность и антигенность. Анатоксины получены из дифтерийного, столбнячного, ботулинического, стафилококкового экзотоксинов, а также из токсинов возбудителей газовой гангрены, яда некоторых змей и растений. При использовании анатоксинов в организме вырабатывается активный иммунитет (антитоксический). Широко используют для актирной иммунизации против дифтерии и столбняка дифтерийный и столбнячный анатоксины. Стафилококковый анатоксин используют и для лечения заболеваний стафилококковой этиологии. Дифтерийный и столбнячный анатоксины изготовляют в виде отдельных препаратов или комбинированных с другими вакцинами. Как правило, анатоксины выпускают сорбированными на геле гидрата окиси алюминия.
 Сывороточные препараты. Специфические иммунные сыворотки содержат антитела (иммуноглобулины) к определенным видам микроорганизмов. Сывороточные препараты используют для лечения, так как введение в организм антител обеспечивает быстрое обеззараживание микробов и их токсинов. Иммунные сыворотки применяются также с диагностической целью для определения антигенного состава микроорганизма, выделенного от больного, что позволяет установить вид (тип) микроба. Сывороточные препараты используют и в профилактических целях для быстрого создания невосприимчивости у человека, контактировавшего с больным или с инфицированным материалом. Специфическую иммунную сыворотку вводят, например, детям, имеющим контакт с больными корью или инфекционным гепатитом (болезнь Боткина). При наличии раневых поверхностей вводят противостолбнячную и противогангренозные сыворотки. При введении сыворотки для профилактики столбняка или бешенства ее комбинируют с активной иммунизацией анатоксином или вакциной. Введение сыворотки в организм человека создает пассивный иммунитет.
Сывороточные препараты. Специфические иммунные сыворотки содержат антитела (иммуноглобулины) к определенным видам микроорганизмов. Сывороточные препараты используют для лечения, так как введение в организм антител обеспечивает быстрое обеззараживание микробов и их токсинов. Иммунные сыворотки применяются также с диагностической целью для определения антигенного состава микроорганизма, выделенного от больного, что позволяет установить вид (тип) микроба. Сывороточные препараты используют и в профилактических целях для быстрого создания невосприимчивости у человека, контактировавшего с больным или с инфицированным материалом. Специфическую иммунную сыворотку вводят, например, детям, имеющим контакт с больными корью или инфекционным гепатитом (болезнь Боткина). При наличии раневых поверхностей вводят противостолбнячную и противогангренозные сыворотки. При введении сыворотки для профилактики столбняка или бешенства ее комбинируют с активной иммунизацией анатоксином или вакциной. Введение сыворотки в организм человека создает пассивный иммунитет.
 Препараты для создания пассивного иммунитета. Различают сыворотки антитоксические, которые получают путем иммунизации животных анатоксинами или токсинами микробов, и антимикробные, полученные при многократной иммунизации животных бактериями, эндотоксинами, фильтратами бактерий. Наиболее эффективны антитоксические сыворотки, которые быстро обезвреживают экзотоксины в организме больного. Их применяют для лечения дифтерии, скарлатины, столбняка, ботулизма, газовой гангрены и заболеваний, вызванных стафилококками. Антимикробные сыворотки менее эффективны, поэтому их используют реже. Для получения иммунных антитоксических сывороток иммунизируют здоровое животное, обычно лошадь, токсинами анатоксинами по специально разработанной схеме. Когда через 10— 12 дней в крови животного обнаруживают достаточное количество антител, производят кровопускание и получают сыворотку, которую консервируют хлорофор¬мом (0, 75%) или фенолом (0, 5%). Контролируют стерильность сыворотки, ее прозрачность и т. д. Для получения Необходимого лечебного эффекта сыворотку приме¬няют в больших объемах (150— 250 мл). Сыворотки, как и вакцины, вводят чаще внутримышечно. Для десенсибилизации используют метод Безредки. Сывороточные препараты, полученные при иммунизации лошади, содержат, помимо специфических антител, чужеродные для человека белки. Поэтому при повторном введении таких сывороток могут возникать аллергические реакции типа анафилактического шока или сывороточной болезни. В связи с этим разработаны различные методы очистки и концентрации лечебных антитоксических сывороток. Основным из них, применяемым, является метод «Диаферм 3» , включающий ферментативный (пептический) гидролиз, позволяющий освободиться от неспецифических белков сыворотки.
Препараты для создания пассивного иммунитета. Различают сыворотки антитоксические, которые получают путем иммунизации животных анатоксинами или токсинами микробов, и антимикробные, полученные при многократной иммунизации животных бактериями, эндотоксинами, фильтратами бактерий. Наиболее эффективны антитоксические сыворотки, которые быстро обезвреживают экзотоксины в организме больного. Их применяют для лечения дифтерии, скарлатины, столбняка, ботулизма, газовой гангрены и заболеваний, вызванных стафилококками. Антимикробные сыворотки менее эффективны, поэтому их используют реже. Для получения иммунных антитоксических сывороток иммунизируют здоровое животное, обычно лошадь, токсинами анатоксинами по специально разработанной схеме. Когда через 10— 12 дней в крови животного обнаруживают достаточное количество антител, производят кровопускание и получают сыворотку, которую консервируют хлорофор¬мом (0, 75%) или фенолом (0, 5%). Контролируют стерильность сыворотки, ее прозрачность и т. д. Для получения Необходимого лечебного эффекта сыворотку приме¬няют в больших объемах (150— 250 мл). Сыворотки, как и вакцины, вводят чаще внутримышечно. Для десенсибилизации используют метод Безредки. Сывороточные препараты, полученные при иммунизации лошади, содержат, помимо специфических антител, чужеродные для человека белки. Поэтому при повторном введении таких сывороток могут возникать аллергические реакции типа анафилактического шока или сывороточной болезни. В связи с этим разработаны различные методы очистки и концентрации лечебных антитоксических сывороток. Основным из них, применяемым, является метод «Диаферм 3» , включающий ферментативный (пептический) гидролиз, позволяющий освободиться от неспецифических белков сыворотки.
 • • • Иммуноглобулины (гамма глобулины) представляю собой белковую фракцию сыворотки, с которой связан специфические функции антител. По эффективности гамма глобулин, выделенный из сыворотки крови человека намного превосходит иммунные сыворотки. Для получения гамма глобулина специально подобранных доноров иммунизируют гриппозным, коклюшным и другими антигенами. Для приготовления гамма глобулина используют два варианта метода Кона — предложенных Н. В. Холчевым (вариант А), и Н. А. Пономаревой и А. С. Нечаевой (вариант Б). Гамма глобулин получают также из плацентарной и абортной крови, экстрактов плаценты рожениц. . Диагностические сыворотки. Широко используются для определения антигенного состава возбудителей инфекционных заболеваний. Они позволяют окончательно определить вид (тип) микроба. В настоящее время вы¬пускают агглютинирующие, преципитирующие, вирус нейтрализующие, токсин нейтрализующие диагностические сыворотки. Агглютинирующие сыворотки используют для идентификации бактерий семейства кишечных (шигеллы, сальмонеллы, эшерихии), возбудителей дифтерии, бруцеллеза, лептоспироза и др. Они могут быть родовые, видовые, типовые, адсорбированные (монорецепторные) и неадсорбированные. Их готовят путем гипериммунизации животных, чаще кроликов, корпускулярным антигеном, который вводят внутривенно, реже внутрибрюшинно и подкожно в возрастающих количествах. Для получения больших количеств сывороток иммунизируют ослов, баранов, коз, лошадей. Существуют различные схемы иммунизации животных. После проверки титра антител животное обескровливают, сыворотку консервируют, добавляя 1— 2% перекристаллизованной борной кислоты или мертиолатом (1 : 1000). Нативные сыворотки (родовые и видовые) используют для идентификации микробов в развернутой реакции агглютинации в пробирках. Адсорбированные сыворотки, содержащие антитела к 2— 3 или более специфическим для данного вида антигенам (поливалентные), а также монорецепторные сыворотки, имеющие антитела только к одному антигену, используют для реакции агглютинации на стекле. Диагностические сыворотки выпускают в сухом или жидком виде. Срок годности жидких сывороток 1 год при хранении их в условиях температуры 4— 10°С. Сухие сыворотки хранят до 3 лет и больше при комнатной температуре. Преципитирующие сыворотки используют в реакции преципитации при экспертизе определения чужеродных белков, в диагностике сибирской язвы (реакция преципитации по Асколи), типирования стрептококков, вирусов оспы, полиомиелита. Их готовят гипериммунизацией кроликов вакцинными штаммами бактерий и комплексами антигенов. Вирус- и токсиннейтрализующие сыворотки — нативные и очищенные по методу «Диаферм 3» — применяют при идентификации вирусов полиомиелита, энцефалитов, Коксаки, ECHO; для определения типа ботулинического токсина и перфрингенстоксина. Их получают, иммунизируя кроликов, лошадей, ослов внутривенно, подкожно или внутримышечно чистыми антигенами, сорбированными на гидроокиси алюминия, или анатоксинами клостридий ботулинус и перфрингенс.
• • • Иммуноглобулины (гамма глобулины) представляю собой белковую фракцию сыворотки, с которой связан специфические функции антител. По эффективности гамма глобулин, выделенный из сыворотки крови человека намного превосходит иммунные сыворотки. Для получения гамма глобулина специально подобранных доноров иммунизируют гриппозным, коклюшным и другими антигенами. Для приготовления гамма глобулина используют два варианта метода Кона — предложенных Н. В. Холчевым (вариант А), и Н. А. Пономаревой и А. С. Нечаевой (вариант Б). Гамма глобулин получают также из плацентарной и абортной крови, экстрактов плаценты рожениц. . Диагностические сыворотки. Широко используются для определения антигенного состава возбудителей инфекционных заболеваний. Они позволяют окончательно определить вид (тип) микроба. В настоящее время вы¬пускают агглютинирующие, преципитирующие, вирус нейтрализующие, токсин нейтрализующие диагностические сыворотки. Агглютинирующие сыворотки используют для идентификации бактерий семейства кишечных (шигеллы, сальмонеллы, эшерихии), возбудителей дифтерии, бруцеллеза, лептоспироза и др. Они могут быть родовые, видовые, типовые, адсорбированные (монорецепторные) и неадсорбированные. Их готовят путем гипериммунизации животных, чаще кроликов, корпускулярным антигеном, который вводят внутривенно, реже внутрибрюшинно и подкожно в возрастающих количествах. Для получения больших количеств сывороток иммунизируют ослов, баранов, коз, лошадей. Существуют различные схемы иммунизации животных. После проверки титра антител животное обескровливают, сыворотку консервируют, добавляя 1— 2% перекристаллизованной борной кислоты или мертиолатом (1 : 1000). Нативные сыворотки (родовые и видовые) используют для идентификации микробов в развернутой реакции агглютинации в пробирках. Адсорбированные сыворотки, содержащие антитела к 2— 3 или более специфическим для данного вида антигенам (поливалентные), а также монорецепторные сыворотки, имеющие антитела только к одному антигену, используют для реакции агглютинации на стекле. Диагностические сыворотки выпускают в сухом или жидком виде. Срок годности жидких сывороток 1 год при хранении их в условиях температуры 4— 10°С. Сухие сыворотки хранят до 3 лет и больше при комнатной температуре. Преципитирующие сыворотки используют в реакции преципитации при экспертизе определения чужеродных белков, в диагностике сибирской язвы (реакция преципитации по Асколи), типирования стрептококков, вирусов оспы, полиомиелита. Их готовят гипериммунизацией кроликов вакцинными штаммами бактерий и комплексами антигенов. Вирус- и токсиннейтрализующие сыворотки — нативные и очищенные по методу «Диаферм 3» — применяют при идентификации вирусов полиомиелита, энцефалитов, Коксаки, ECHO; для определения типа ботулинического токсина и перфрингенстоксина. Их получают, иммунизируя кроликов, лошадей, ослов внутривенно, подкожно или внутримышечно чистыми антигенами, сорбированными на гидроокиси алюминия, или анатоксинами клостридий ботулинус и перфрингенс.


