 Выполнено: Федотовой Антониной Валериевной ГОУ школа 336 Невского района
Выполнено: Федотовой Антониной Валериевной ГОУ школа 336 Невского района
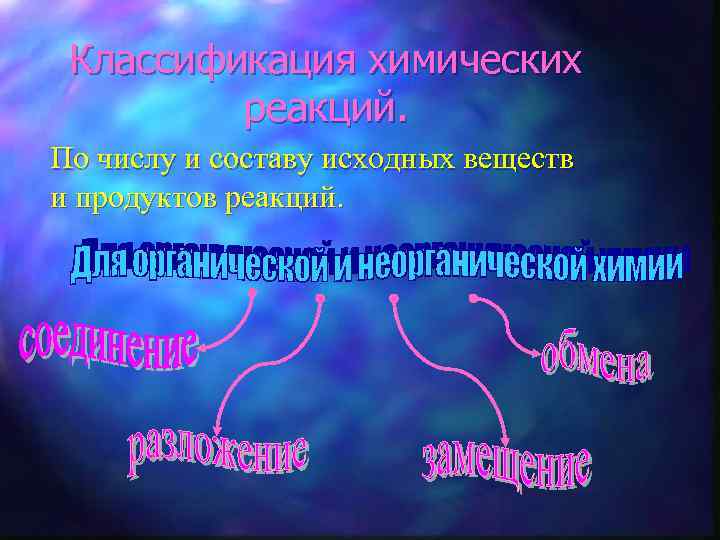 Классификация химических реакций. По числу и составу исходных веществ и продуктов реакций.
Классификация химических реакций. По числу и составу исходных веществ и продуктов реакций.
 Реакции соединения Это такие реакции, в которых из нескольких простых или сложных веществ образуется одно сложное вещество: 2 H 2+O 2 H 2+Cl 2 2 H 2 O 2 HCl
Реакции соединения Это такие реакции, в которых из нескольких простых или сложных веществ образуется одно сложное вещество: 2 H 2+O 2 H 2+Cl 2 2 H 2 O 2 HCl
 Реакции разложения Это реакции, в которых из одного сложного вещества получается несколько простых или сложных веществ: 2 KCl. O 3 2 KCl+3 O 2
Реакции разложения Это реакции, в которых из одного сложного вещества получается несколько простых или сложных веществ: 2 KCl. O 3 2 KCl+3 O 2
 Реакция замещения Это реакция между простым и cложным веществом, приводящая к образованию другого простого и сложного вещества: Zn+2 HCl Zn. Cl 2+H 2
Реакция замещения Это реакция между простым и cложным веществом, приводящая к образованию другого простого и сложного вещества: Zn+2 HCl Zn. Cl 2+H 2
 Реакция обмена Это реакция между двумя сложными веществами, приводящая к образованию других сложных веществ. Реакция обмена возможна только при условии образования в продуктах реакции нерастворимого вещества, газа или малодиссоциируемого вещества, например, воды: Ag. NO 3+HCl Ag. Cl +HNO 3
Реакция обмена Это реакция между двумя сложными веществами, приводящая к образованию других сложных веществ. Реакция обмена возможна только при условии образования в продуктах реакции нерастворимого вещества, газа или малодиссоциируемого вещества, например, воды: Ag. NO 3+HCl Ag. Cl +HNO 3
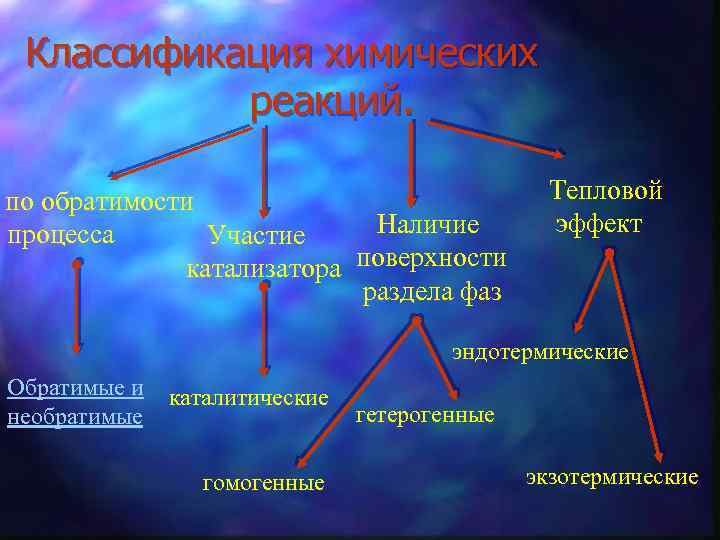 Классификация химических реакций. по обратимости Наличие процесса Участие катализатора поверхности раздела фаз Тепловой эффект эндотермические Обратимые и необратимые каталитические гомогенные гетерогенные экзотермические
Классификация химических реакций. по обратимости Наличие процесса Участие катализатора поверхности раздела фаз Тепловой эффект эндотермические Обратимые и необратимые каталитические гомогенные гетерогенные экзотермические
 Обратимые и необратимые реакции. Обратимые реакции -протекают во взаимно противоположных направлениях: N 2 + 3 H 2 2 NH 3 Необратимые реакции –протекают при одних и тех же условиях только в одном направлении: Ba. Cl 2+2 Ag. NO 3 Ba(NO 3)2+2 Ag. Cl
Обратимые и необратимые реакции. Обратимые реакции -протекают во взаимно противоположных направлениях: N 2 + 3 H 2 2 NH 3 Необратимые реакции –протекают при одних и тех же условиях только в одном направлении: Ba. Cl 2+2 Ag. NO 3 Ba(NO 3)2+2 Ag. Cl
 Каталитические реакции- протекают в присутствии катализатора: C 2 H 4+H 2 O H 2 SO 4 C 2 H 5 OH
Каталитические реакции- протекают в присутствии катализатора: C 2 H 4+H 2 O H 2 SO 4 C 2 H 5 OH
 Гомогенные и гетерогенные реакции. Гомогенные- протекают между веществами находящимися в одном агрегатном состоянии: Na. OH+HCl Na. Cl+H 2 Oж Ж Ж Гетерогенные- протекают между веществами находящимися в разном агрегатном состоянии: Mg+2 HCl Mg. Cl 2+H 2 ТВ Ж
Гомогенные и гетерогенные реакции. Гомогенные- протекают между веществами находящимися в одном агрегатном состоянии: Na. OH+HCl Na. Cl+H 2 Oж Ж Ж Гетерогенные- протекают между веществами находящимися в разном агрегатном состоянии: Mg+2 HCl Mg. Cl 2+H 2 ТВ Ж
 Экзотермические и эндотермические реакции. Эндотермические- протекают с выделением тепла: N 2+3 H 2 2 NH 3+Q Эндотермические- протекают с поглощением тепла: N 2+O 2 2 NO-Q
Экзотермические и эндотермические реакции. Эндотермические- протекают с выделением тепла: N 2+3 H 2 2 NH 3+Q Эндотермические- протекают с поглощением тепла: N 2+O 2 2 NO-Q
 Окислительновосстановительные реакции. В ходе окислительно-восстановительных реакций изменяются степени окисления элементов: 2 Fe 0 +3 Сu+2 Cl 2 -2 2 Fe+3 Cl 3 -1+3 Cu 0 Fe 0 -3 e Fe+3 восстановитель (окисление) Cu+2+2 e Cu 0 окислитель (восстановление)
Окислительновосстановительные реакции. В ходе окислительно-восстановительных реакций изменяются степени окисления элементов: 2 Fe 0 +3 Сu+2 Cl 2 -2 2 Fe+3 Cl 3 -1+3 Cu 0 Fe 0 -3 e Fe+3 восстановитель (окисление) Cu+2+2 e Cu 0 окислитель (восстановление)
 Спасибо за внимание
Спасибо за внимание