Выделение и очистка белков. Уровни структурной организации


Выделение и очистка белков. Уровни структурной организации белковой молекулы. Первичная структура

План лекции • Методы разрушения клеток и получения клеточных органелл • Методы избирательного осаждения белков • Хроматографические методы очистки • Критерии гомогенности полученных белков • Методы определения молекулярной массы • Представление об уровнях организации белковой молекулы • Определение первичной структуры белка

Различные методы разрушения клеток • А- гомогенизатор Поттера • Б- ножевой гомогенизатор (блендор Уорринга) • В-ультразвуковой дезинтегратор • Г- шаровая мельница • Д- френч-пресс
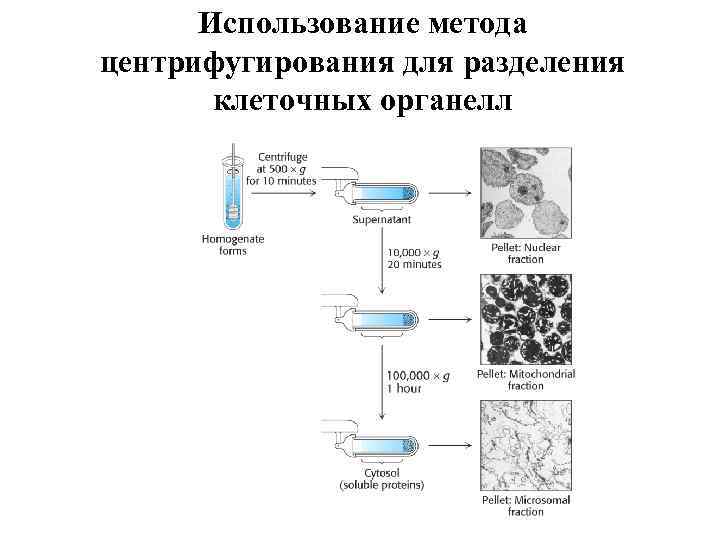
Использование метода центрифугирования для разделения клеточных органелл
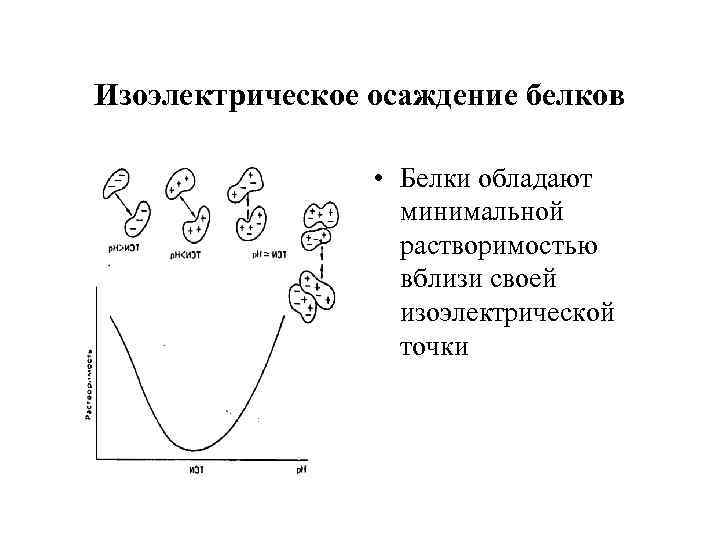
Изоэлектрическое осаждение белков • Белки обладают минимальной растворимостью вблизи своей изоэлектрической точки

Принципы, лежащие в основе высаливания белков

Принципы, лежащие в основе действия ионов ряда Гофмейстера • Космотропы (крупные анионы с высокой плотностью заряда) образуют прочные комплексы с молекулами воды и ослабляют водородные связи между молекулами воды. Вследствие этого гидратная оболочка вокруг молекул белка «разрыхляется» и растворимость белка уменьшается • Хаотропы (крупные анионы с низкой плотностью заряда) не способны разрушать образовывать прочные комплексы с молекулами воды и наоборот способствуют стабилизации водородных связей между молекулами воды, тем самым укрепляя и стабилизируя гидратную оболочку вокруг белка и увеличивают его растворимость
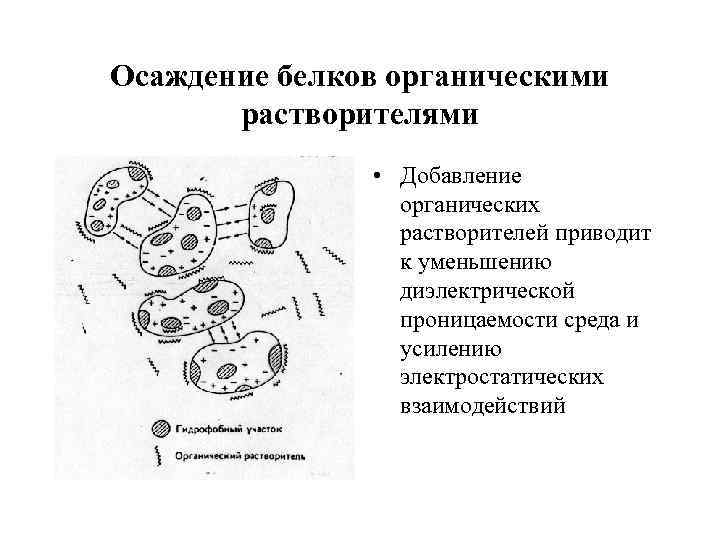
Осаждение белков органическими растворителями • Добавление органических растворителей приводит к уменьшению диэлектрической проницаемости среда и усилению электростатических взаимодействий

Использование диализа для удаления низкомолекулярных соединений

Использование колоночной хроматографии для разделения белков
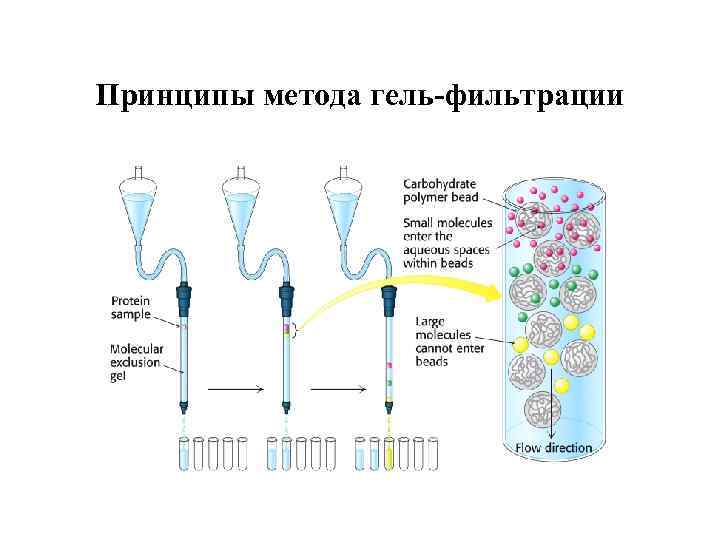
Принципы метода гель-фильтрации

Использование метода гель-фильтрации для разделения смеси белков
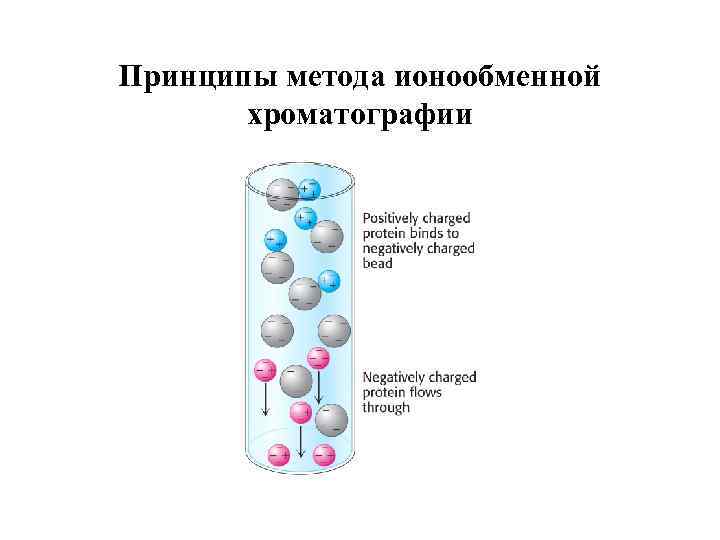
Принципы метода ионообменной хроматографии
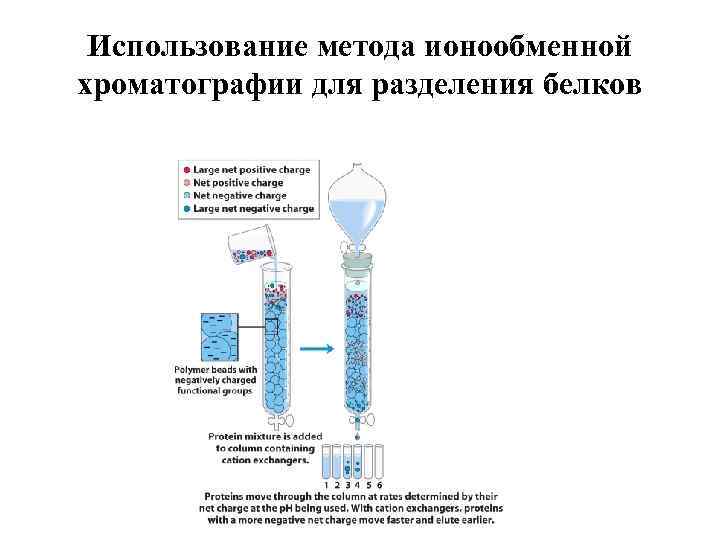
Использование метода ионообменной хроматографии для разделения белков

Катионо- и анионообменные носители

Кривые титрования сильных и слабых ионообменников
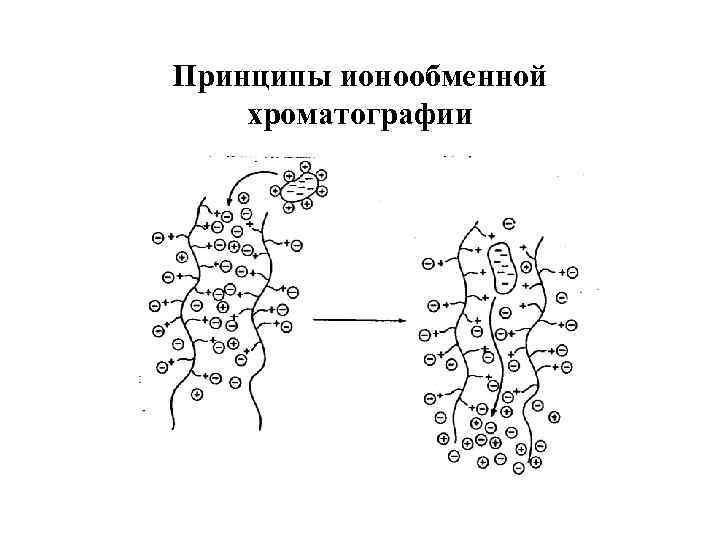
Принципы ионообменной хроматографии

Схема последовательных стадий проведения ионообменной хроматографии Зачерненными символами обозначены ионы белков, светлыми кружками обозначены противоины

Принципы метода хроматографии по сродству
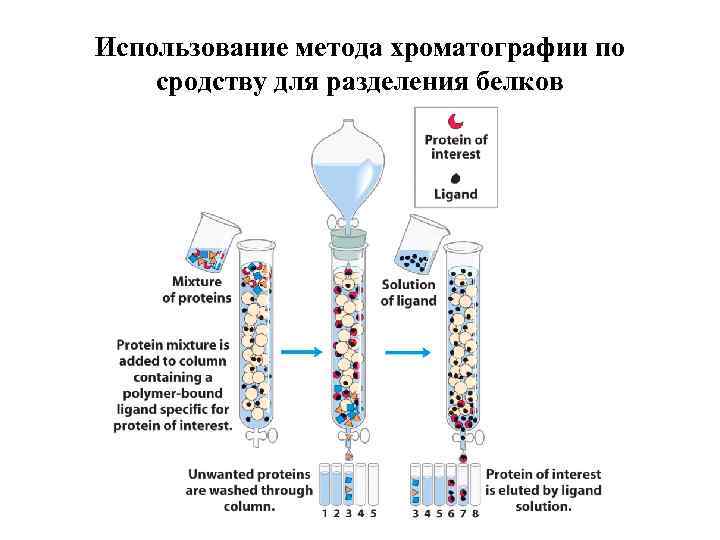
Использование метода хроматографии по сродству для разделения белков
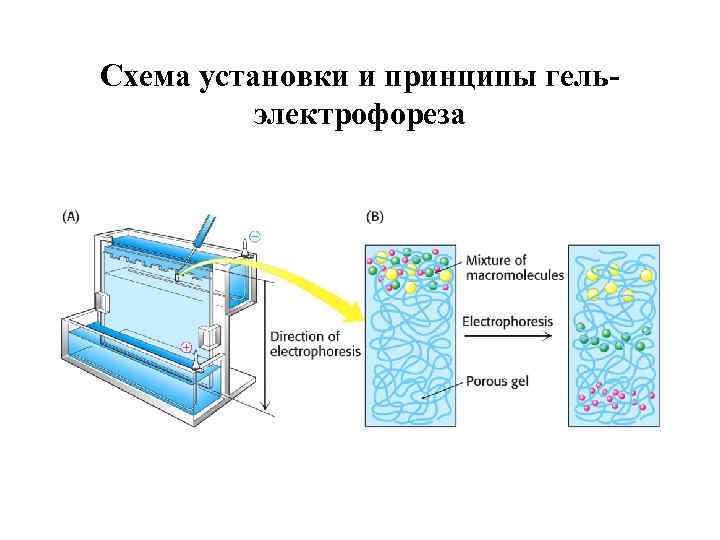
Схема установки и принципы гель- электрофореза
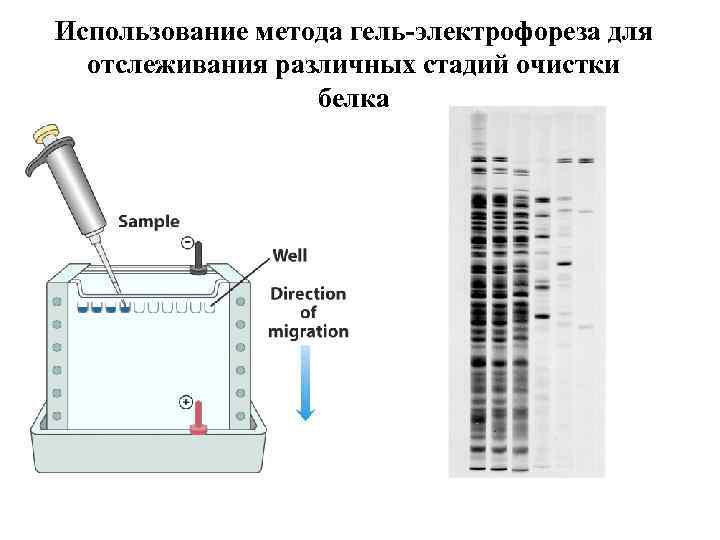
Использование метода гель-электрофореза для отслеживания различных стадий очистки белка

Фотография геля после электрофореза в полиакриламидном геле в присутствии додецилсульфата натрия

Использование метода электрофореза в полиакриламидном геле в присутствии додецилсульфата натрия для определения кажущейся молекулярной массы исследуемого белка
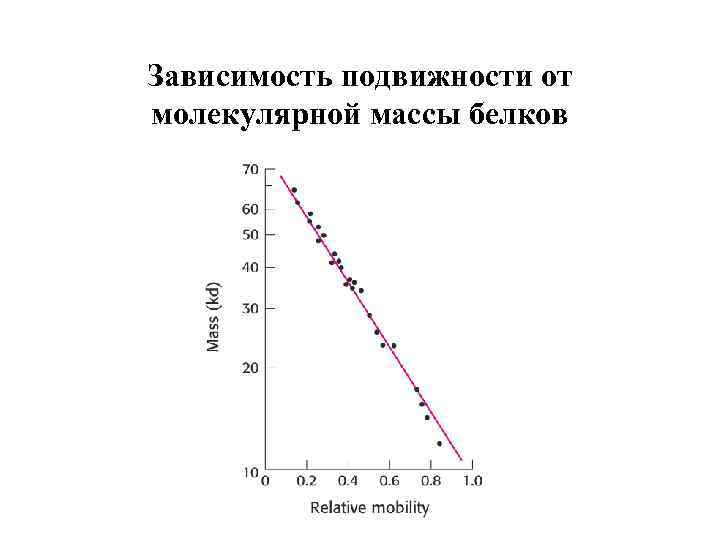
Зависимость подвижности от молекулярной массы белков

Принцип изоэлектрофокусирования

Использование метода изоэлектофокусирования для анализа белков

Использование метода двумерного электрофореза (изоэлектрофокусирование, SDS-электрофорез) для анализа сложных смесей белков

Двумерное разделение сложной смеси белков
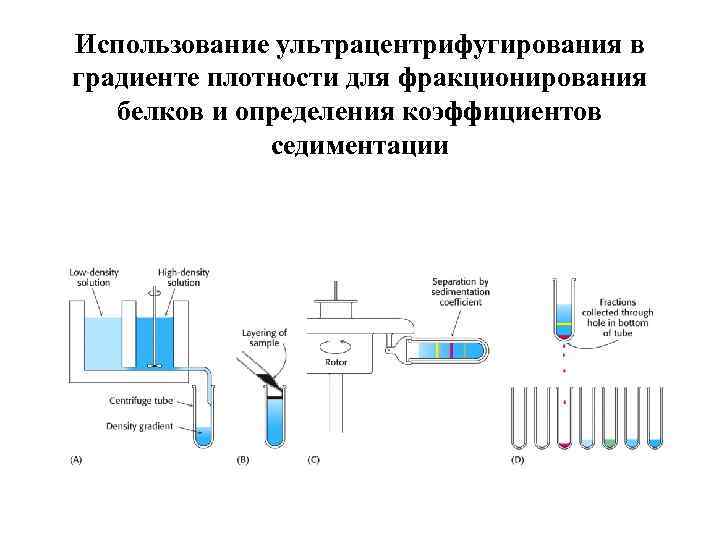
Использование ультрацентрифугирования в градиенте плотности для фракционирования белков и определения коэффициентов седиментации
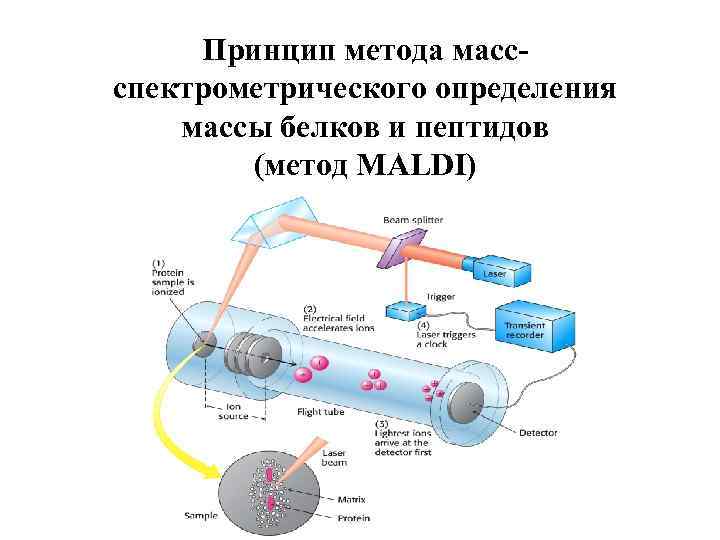
Принцип метода масс- спектрометрического определения массы белков и пептидов (метод MALDI)

Метод масс-спектроскопии (электроспрей)
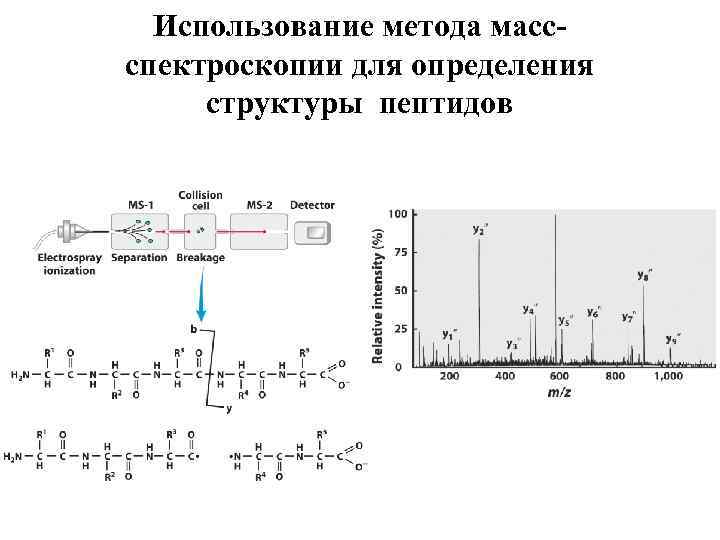
Использование метода масс- спектроскопии для определения структуры пептидов

Представление о четырех уровнях организации белковой молекулы

Дважды лауреат Нобелевской премии (1958, 1980) Фредерик Сенгер, первым установивший первичную структуру инсулина

Тактика определения первичной структуры белка

Энзиматические методы расщепления пептидных связей

Различные методы фрагментации полипептидной цепи

Стратегия определения первичной структуры белка

Основы метода Эдмановской деградации белка

Использование метода Эдмановской деградации для установления первичной структуры пептидов

Схема деградации пептидов по методу Эдмана

Схема деградации пептидов по методу Эдмана
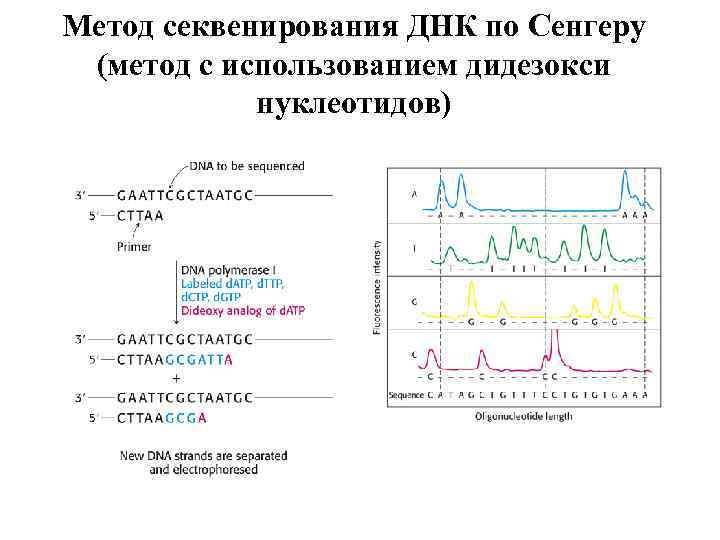
Метод секвенирования ДНК по Сенгеру (метод с использованием дидезокси нуклеотидов)

Представление о паралогах – белках-гомологах, экспрессируемых в одном и том же организме, и ортологах, белках- гомологах, экспрессируемых в разных видах

Представление о сходстве белков (ортологах и паралогах)

Сравнение первичных структур альфа- цепи гемоглобина и миоглобина человека

Для сравнения две структуры механически сдвинуты друг относительно друга

При введении пробелов (gap) количество совпадений возрастает с 22 -23 до 38 Параллельно с этим вводится определенный штраф за введение пробела любой длины (-25) и определенная «цена» за идентичность остатков (10). Общий показатель сходства (score) составит (38*10)- 25=355

Оценка вероятности случайного совпадения определяется путем сравнения с хаотическим набором тех же аминокислот

Таблица Blosum 62, позволяющая выявлять сходство (положительные значения) или существенные различия (отрицательные значения) в первичной структуре белков
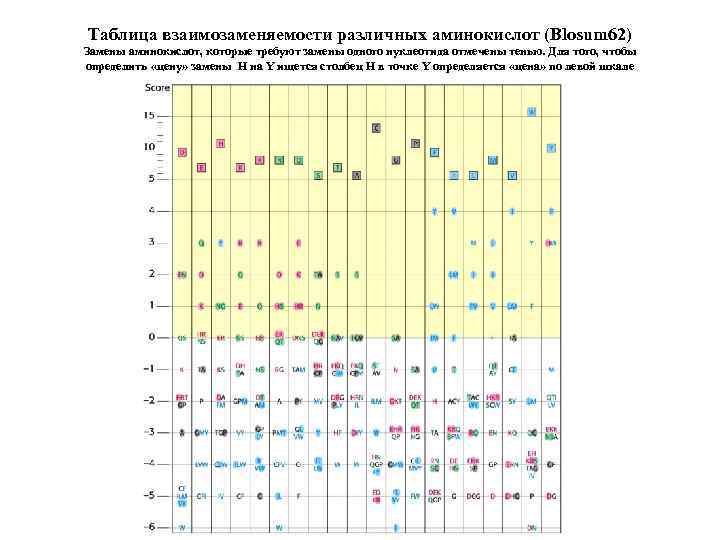
Таблица взаимозаменяемости различных аминокислот (Blosum 62) Замены аминокислот, которые требуют замены одного нуклеотида отмечены тенью. Для того, чтобы определить «цену» замены H на Y ищется столбец H в точке Y определяется «цена» по левой шкале

Заключительный этап сопоставления первичных структур с учетом как идентичных, так и гомологичных остатков

Эволюционное древо бактерий, построенное на основе сравнения первичных структур одного из белков (Gro. EL)

Четыре уровня организации структуры белка

Очистка гипотетического белка в ходе выделения

Сравнение первичных структур Hsp 70 E. coli и B. subtilis. Необходимость введения пробелов (gap)
2_Purif.ppt
- Количество слайдов: 57

