Вятский государственный университет Биологический


Вятский государственный университет Биологический факультет Кафедра микробиологии Дипломная работа на тему: Теоретическое и экспериментальное обоснование состава конъюгата коллоидного золота с антителами для разработки иммунохроматографической тест-системы, предназначенной для идентификации H. pylori Работу выполнила: Лежнина Ксения Евгеньевна Руководитель: д. м. н. , доцент Богачева Наталья Викторовна

Работа выполнена на кафедре микробиологии Вятского государственного университета 2
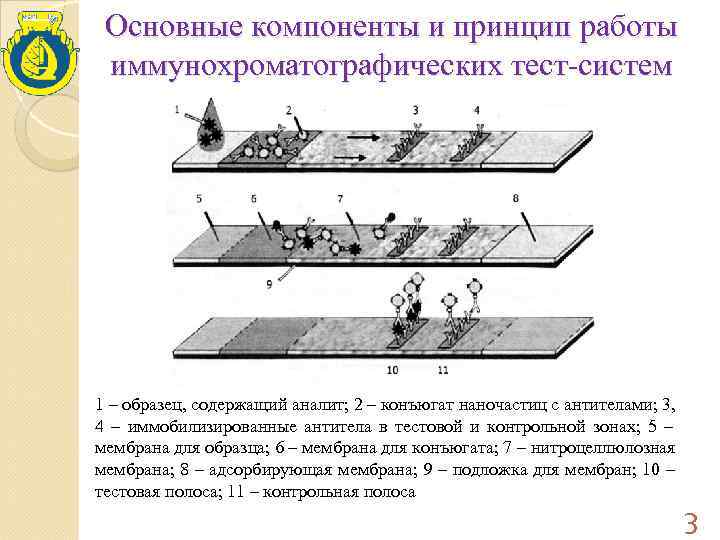
Основные компоненты и принцип работы иммунохроматографических тест-систем 1 – образец, содержащий аналит; 2 – конъюгат наночастиц с антителами; 3, 4 – иммобилизированные антитела в тестовой и контрольной зонах; 5 – мембрана для образца; 6 – мембрана для конъюгата; 7 – нитроцеллюлозная мембрана; 8 – адсорбирующая мембрана; 9 – подложка для мембран; 10 – тестовая полоса; 11 – контрольная полоса 3
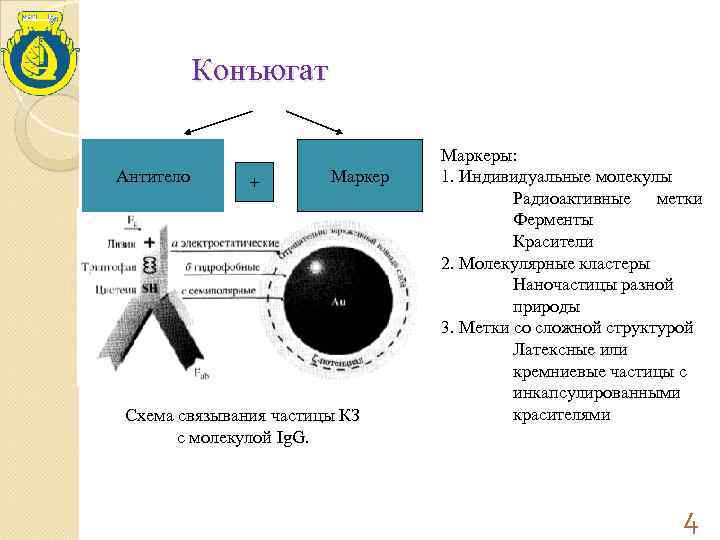
Конъюгат Маркеры: Антитело + Маркер 1. Индивидуальные молекулы Радиоактивные метки Ферменты Красители 2. Молекулярные кластеры Наночастицы разной природы 3. Метки со сложной структурой Латексные или кремниевые частицы с инкапсулированными Схема связывания частицы КЗ красителями с молекулой Ig. G. 4

Цель исследования – теоретическое и экспериментальное обоснование состава конъюгата коллоидного золота с антителами для разработки иммунохроматографической тест-системы, предназначенной для идентификации H. pylori 5

Задачи исследования: теоретически обосновать и экспериментально отработать методику приготовления наночастиц КЗ с диаметром 30 нм; с использованием метода электронной микроскопии и спектрофотометрии провести оценку полученных серий КЗ и выбрать кондиционные серии КЗ; провести оценку адсорбционной способности серий КЗ с Мк. Ат; теоретически и экспериментально обосновать состав конъюгата коллоидного золота с антителами для разработки иммунохроматографической тест-системы, предназначенной для идентификации H. pylori 6

Метод Френса К кипящему 0, 01 % водному раствору золотохлористоводородной кислоты добавляют 1% водный раствор цитрата натрия в объеме, зависящем от требуемого размера частиц. Схема реакции восстановления золотохлористоводородной кислоты с использованием цитрата натрия: 2 Au. Cl 3 + 3 Na 3 C 6 H 5 O 7 = 2 Au + 3 Na 2 C 5 H 4 O 5 + +3 CO 2 + Na. Cl + 3 HCl 7

Формула расчета объема цитрата натрия (V, мл), необходимого для получения определенного диаметра наночастиц КЗ (d, нм) в расчете на 100 мл золя 8
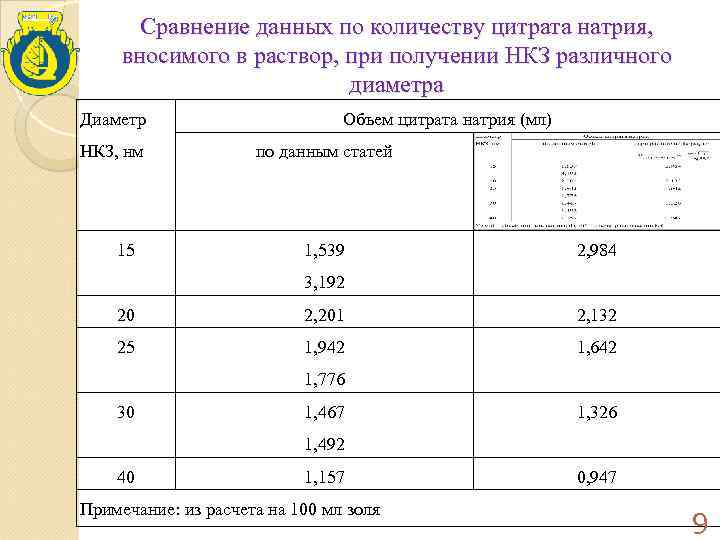
Сравнение данных по количеству цитрата натрия, вносимого в раствор, при получении НКЗ различного диаметра Диаметр Объем цитрата натрия (мл) НКЗ, нм по данным статей 15 1, 539 2, 984 3, 192 20 2, 201 2, 132 25 1, 942 1, 642 1, 776 30 1, 467 1, 326 1, 492 40 1, 157 0, 947 Примечание: из расчета на 100 мл золя 9
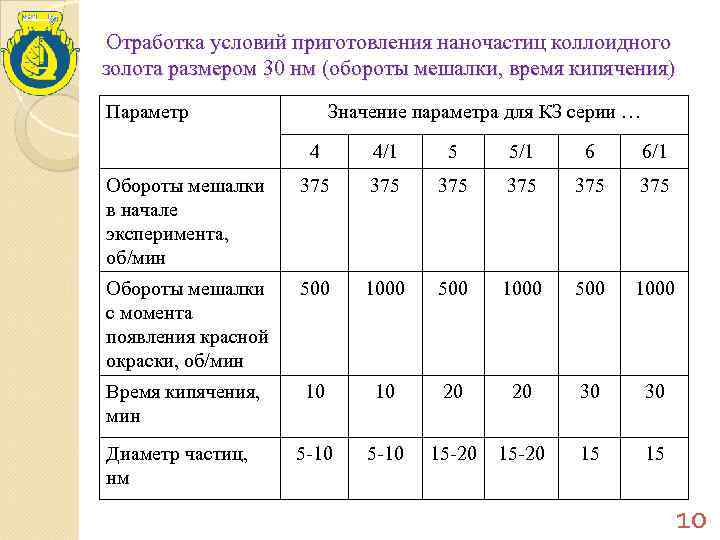
Отработка условий приготовления наночастиц коллоидного золота размером 30 нм (обороты мешалки, время кипячения) Параметр Значение параметра для КЗ серии … 4 4/1 5 5/1 6 6/1 Обороты мешалки 375 375 в начале эксперимента, об/мин Обороты мешалки 500 1000 500 1000 с момента появления красной окраски, об/мин Время кипячения, 10 20 20 30 мин Диаметр частиц, 5 -10 15 -20 15 нм 10
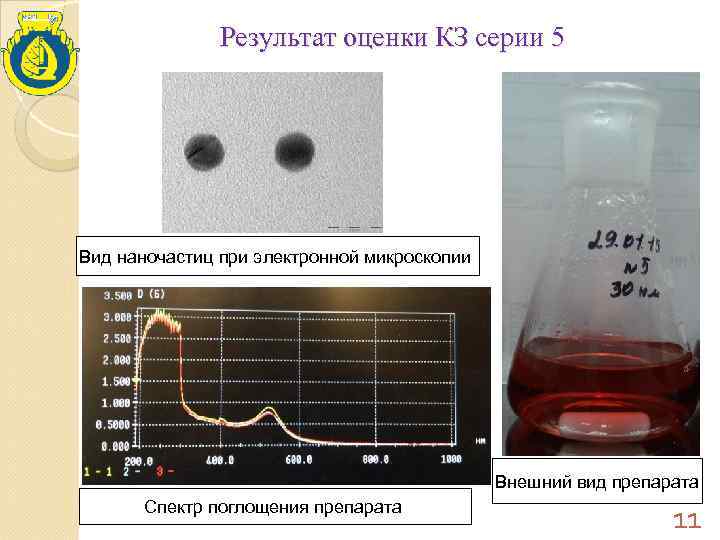
Результат оценки КЗ серии 5 Вид наночастиц при электронной микроскопии Внешний вид препарата Спектр поглощения препарата 11
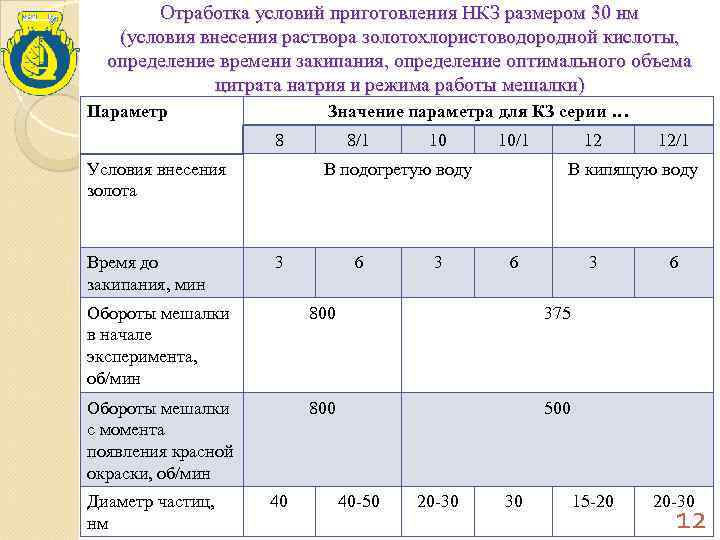
Отработка условий приготовления НКЗ размером 30 нм (условия внесения раствора золотохлористоводородной кислоты, определение времени закипания, определение оптимального объема цитрата натрия и режима работы мешалки) Параметр Значение параметра для КЗ серии … 8 8/1 10 10/1 12 12/1 Условия внесения В подогретую воду В кипящую воду золота Время до 3 6 закипания, мин Обороты мешалки 800 375 в начале эксперимента, об/мин Обороты мешалки 800 500 с момента появления красной окраски, об/мин Диаметр частиц, 40 -50 20 -30 15 -20 20 -30 нм 12
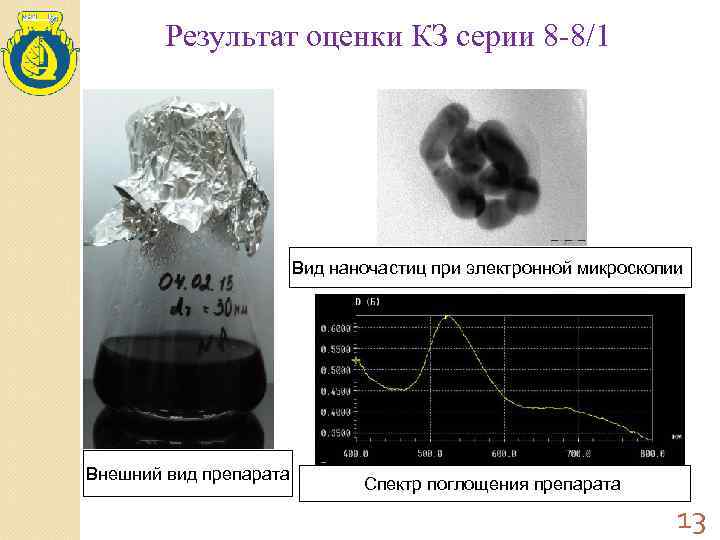
Результат оценки КЗ серии 8 -8/1 Вид наночастиц при электронной микроскопии Внешний вид препарата Спектр поглощения препарата 13
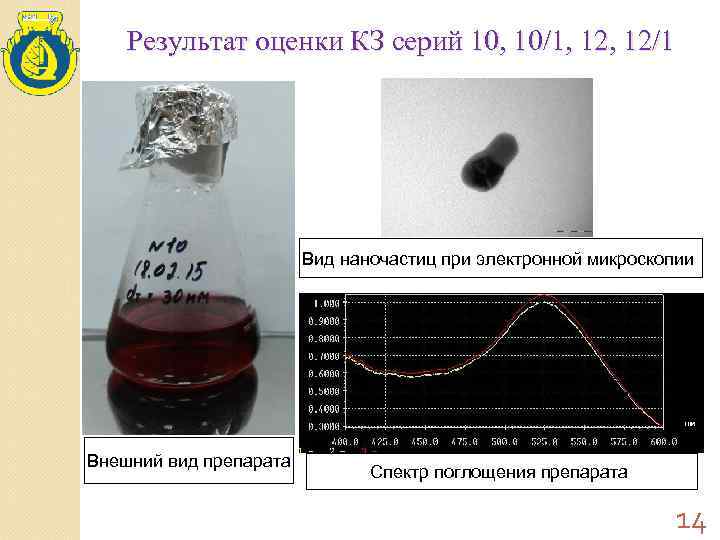
Результат оценки КЗ серий 10, 10/1, 12/1 Вид наночастиц при электронной микроскопии Внешний вид препарата Спектр поглощения препарата 14

Алгоритм приготовления наночастиц КЗ с размером частиц 30 нм 1. Приготовить 50 мл 1% раствора 5, 5 -водного цитрата натрия: 0, 69 г 5, 5 водного цитрата натрия растворить в 50 мл деионизированной воды. 2. Приготовить 10% раствор золохлористоводородной кислоты: (HAu. Cl 4· 3 H 2 O): к 1 г HAu. Cl 4 добавить 10 мл деионизированной воды. 3. В колбу Эрленмейера добавить 50 мл деионизированной воды и поместить магнитную мешалку. Надеть на колбу обратный холодильник, поставить колбу с содержимым на магнитную плитку и установить на плитке режим 375 об/мин и температуру 300◦С. 4. Через 6 мин внести 0, 058 мл 10% раствора КЗ, кипятить 2 мин. 5. Внести 0, 72 мл 1% раствора 5, 5 -водного цитрата натрия. 6. При изменении цвета раствора с синего на красный изменить режим на магнитной плитке на 500 об/мин и снизить температуру до 200 ◦С. 7. Кипятить раствор еще 20 мин. 8. Выключить магнитную плитку, снять обратный холодильник, остудить раствор при комнатной температуре и оставить до следующего дня с целью оценки на наличие осадка. Хранить в холодильнике при 4 ◦С. 15
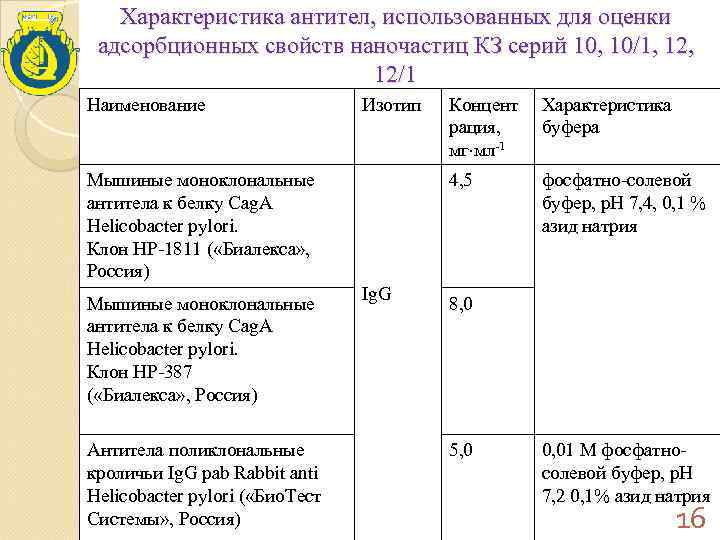
Характеристика антител, использованных для оценки адсорбционных свойств наночастиц КЗ серий 10, 10/1, 12, 12/1 Наименование Изотип Концент Характеристика рация, буфера мг мл-1 Мышиные моноклональные 4, 5 фосфатно-солевой антитела к белку Cag. A буфер, р. Н 7, 4, 0, 1 % Helicobacter pylori. азид натрия Клон HP-1811 ( «Биалекса» , Россия) Мышиные моноклональные Ig. G 8, 0 антитела к белку Cag. A Helicobacter pylori. Клон HP-387 ( «Биалекса» , Россия) Антитела поликлональные 5, 0 0, 01 М фосфатно- кроличьи Ig. G pab Rabbit anti солевой буфер, р. Н Helicobacter pylori ( «Био. Тест 7, 2 0, 1% азид натрия Системы» , Россия) 16

Методика постановки реакции по определению «золотого числа» Все серии КЗ доводили 0, 2 М К 2 CO 3 до р. Н 9, 5 ЕД. Во все лунки восьми горизонтальных рядов 96 -луночного круглодонного пиолистеролового планшета вносили 0, 005 М карбонатно-бикарбонатный буфер с p. H 9, 5 ЕД. В первые лунки планшета (А 1 -Н 1) вносили раствор Мк. Ат 1811. Титровали содержимое лунок А 1 -Н 1 слева направо с шагом два путем переноса 100 мкл раствора Мк. Ат из каждой предыдущей лунки в каждую последующую. В каждую лунку двух горизонтальных рядов (в 2 -х повторностях) вносили по 100 мкл КЗ. Содержимое лунок инкубировали 15 мин. По окончании инкубации в каждую лунку вносили 10%-ный раствор натрия хлорида. Конечная концентрация Na. Cl в каждой лунке при этом составила 1%. Содержимое лунок перемешивали. Инкубировали 10 мин. 17
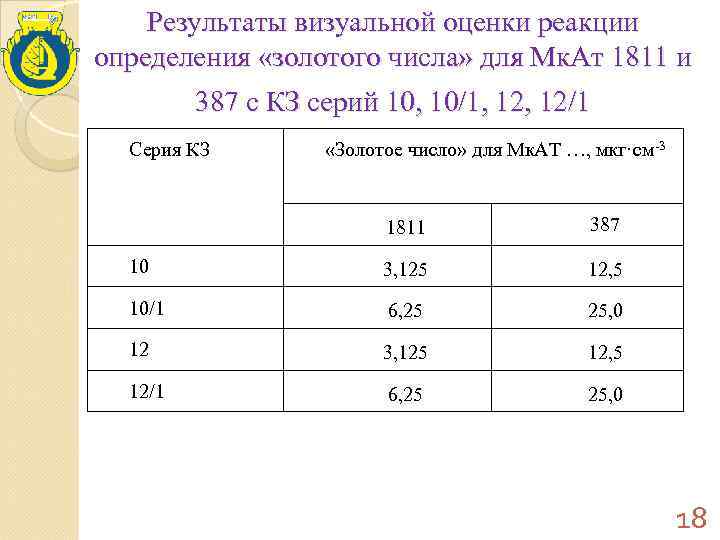
Результаты визуальной оценки реакции определения «золотого числа» для Мк. Ат 1811 и 387 с КЗ серий 10, 10/1, 12/1 Серия КЗ «Золотое число» для Мк. АТ …, мкг·см-3 1811 387 10 3, 125 12, 5 10/1 6, 25 25, 0 12 3, 125 12, 5 12/1 6, 25 25, 0 18
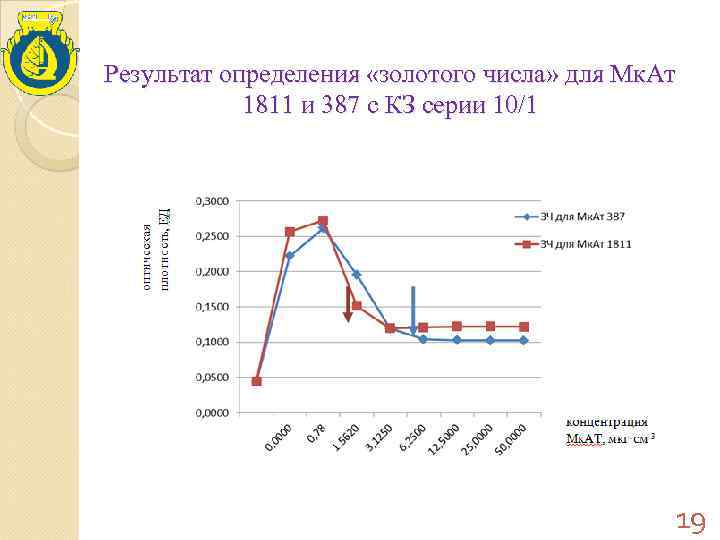
Результат определения «золотого числа» для Мк. Ат 1811 и 387 с КЗ серии 10/1 19
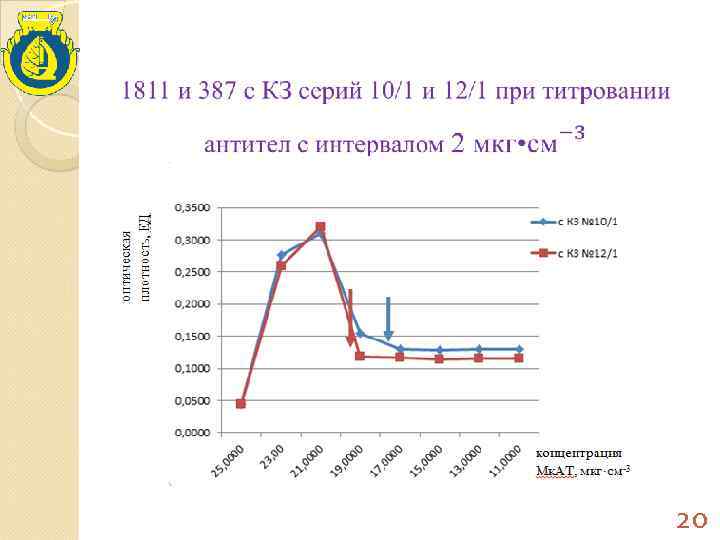
20

Характеристика препаратов КЗ серий 10/1 и 12/1 Показатель, ед. изм Значение показателя для КЗ серии … 10/1 12/1 Диаметр частиц КЗ ( d ср ) по данным 26, 7 30 электронной микроскопии, нм Форма Овальная, круглая Однородность Однородные Наличие конгломератов - Результаты спектрофотометрии: 1, 020 0, 867 оптическая плотность (ЕД), max пика поглощения; длина волны max пика поглощения при max при λ=526 max при λ=525 измерении в диапазоне λ=200 -600 нм Диаметр частиц КЗ (d ср ), определенный по 21 результатам спектрофотометрии, нм 30 20 -30

Выводы 1. Отработана методика приготовления наночастиц коллоидного золота с диаметром 30 нм. 2. Экспериментально получено 12 серий препарата коллоидного золота. 3. Проведена оценка полученных серий КЗ, кондиционными признаны серии 10, 10/1, 12/1 с размером частиц от 15 до 30 нм. 4. Определена адсорбционная способность указанных серий коллоидного золота с выбранными Мк. Ат к Сag белку H. pylori – клоны 1811 и 387. 5. Обоснован состав конъюгата коллоидного золота с антителами: серии коллоидного золота 10/1 и 12/1 и Мк. Ат к Сag белку H. pylori клон 387 с концентрацией, соответственно, 19, 5 мкг • см-3 и 23 мкг • см-3. 22

Практические предложения Использовать разработанную схему синтеза наночастиц коллоидного золота с размером 30 нм при изготовлении иммунохроматографических тест-систем для идентификации Helicobacter pylori; подготовить проект статьи для публикации в научно-практическом журнале. 23

Результаты работы опубликованы в виде тезисов на Всероссийской научной конференции «Наука – производство – технологии – экология» в апреле 2015 г. 24

Автор выражает глубокую благодарность дипломному руководителю д. м. н. Богачевой Наталье Викторовне, магистранту кафедры микробиологии Мокрецовой Ирине Михайловне 25
Лежнина.ppt
- Количество слайдов: 25

