Вводная лекция.pptx
- Количество слайдов: 43
 Вводная лекция Строение атома
Вводная лекция Строение атома
 История развития Дата Автор Открытие 400 г до н. э. Демокрит Термин «атом» 350 г до н. э. Аристотель «принципы природы» : холод – тепло – сухость – влажность 300 г н. э. Зосима 28 томов энциклопедии по химии 300 – 1500 гг. Алхимия Кислоты, щелочи, соли, спирт ~1530 г Теофраст Парацельс «цель химии в изготовлении лекарств» - элементов 1661 г Роберт Бойль Понятие «элемент» как составной части вещества 1785 г Антуан Лоран Лавуазье Классификация элементов по группам (свойствам). З-н сохранения масс реагирующих веществ
История развития Дата Автор Открытие 400 г до н. э. Демокрит Термин «атом» 350 г до н. э. Аристотель «принципы природы» : холод – тепло – сухость – влажность 300 г н. э. Зосима 28 томов энциклопедии по химии 300 – 1500 гг. Алхимия Кислоты, щелочи, соли, спирт ~1530 г Теофраст Парацельс «цель химии в изготовлении лекарств» - элементов 1661 г Роберт Бойль Понятие «элемент» как составной части вещества 1785 г Антуан Лоран Лавуазье Классификация элементов по группам (свойствам). З-н сохранения масс реагирующих веществ
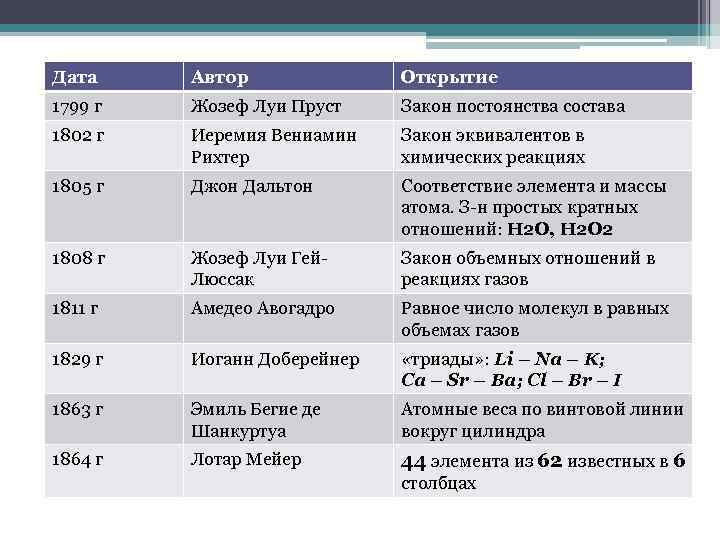 Дата Автор Открытие 1799 г Жозеф Луи Пруст Закон постоянства состава 1802 г Иеремия Вениамин Рихтер Закон эквивалентов в химических реакциях 1805 г Джон Дальтон Соответствие элемента и массы атома. З-н простых кратных отношений: Н 2 О, Н 2 О 2 1808 г Жозеф Луи Гей. Люссак Закон объемных отношений в реакциях газов 1811 г Амедео Авогадро Равное число молекул в равных объемах газов 1829 г Иоганн Доберейнер «триады» : Li – Na – K; Ca – Sr – Ba; Cl – Br – I 1863 г Эмиль Бегие де Шанкуртуа Атомные веса по винтовой линии вокруг цилиндра 1864 г Лотар Мейер 44 элемента из 62 известных в 6 столбцах
Дата Автор Открытие 1799 г Жозеф Луи Пруст Закон постоянства состава 1802 г Иеремия Вениамин Рихтер Закон эквивалентов в химических реакциях 1805 г Джон Дальтон Соответствие элемента и массы атома. З-н простых кратных отношений: Н 2 О, Н 2 О 2 1808 г Жозеф Луи Гей. Люссак Закон объемных отношений в реакциях газов 1811 г Амедео Авогадро Равное число молекул в равных объемах газов 1829 г Иоганн Доберейнер «триады» : Li – Na – K; Ca – Sr – Ba; Cl – Br – I 1863 г Эмиль Бегие де Шанкуртуа Атомные веса по винтовой линии вокруг цилиндра 1864 г Лотар Мейер 44 элемента из 62 известных в 6 столбцах
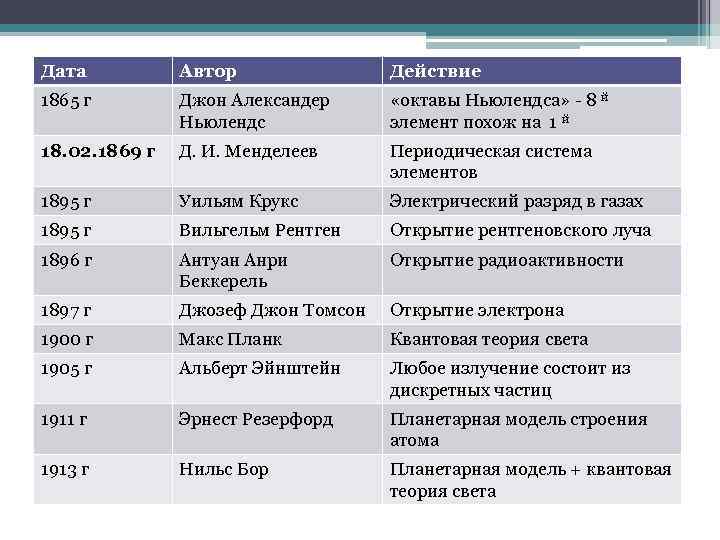 Дата Автор Действие 1865 г Джон Александер Ньюлендс «октавы Ньюлендса» - 8 й элемент похож на 1 й 18. 02. 1869 г Д. И. Менделеев Периодическая система элементов 1895 г Уильям Крукс Электрический разряд в газах 1895 г Вильгельм Рентген Открытие рентгеновского луча 1896 г Антуан Анри Беккерель Открытие радиоактивности 1897 г Джозеф Джон Томсон Открытие электрона 1900 г Макс Планк Квантовая теория света 1905 г Альберт Эйнштейн Любое излучение состоит из дискретных частиц 1911 г Эрнест Резерфорд Планетарная модель строения атома 1913 г Нильс Бор Планетарная модель + квантовая теория света
Дата Автор Действие 1865 г Джон Александер Ньюлендс «октавы Ньюлендса» - 8 й элемент похож на 1 й 18. 02. 1869 г Д. И. Менделеев Периодическая система элементов 1895 г Уильям Крукс Электрический разряд в газах 1895 г Вильгельм Рентген Открытие рентгеновского луча 1896 г Антуан Анри Беккерель Открытие радиоактивности 1897 г Джозеф Джон Томсон Открытие электрона 1900 г Макс Планк Квантовая теория света 1905 г Альберт Эйнштейн Любое излучение состоит из дискретных частиц 1911 г Эрнест Резерфорд Планетарная модель строения атома 1913 г Нильс Бор Планетарная модель + квантовая теория света
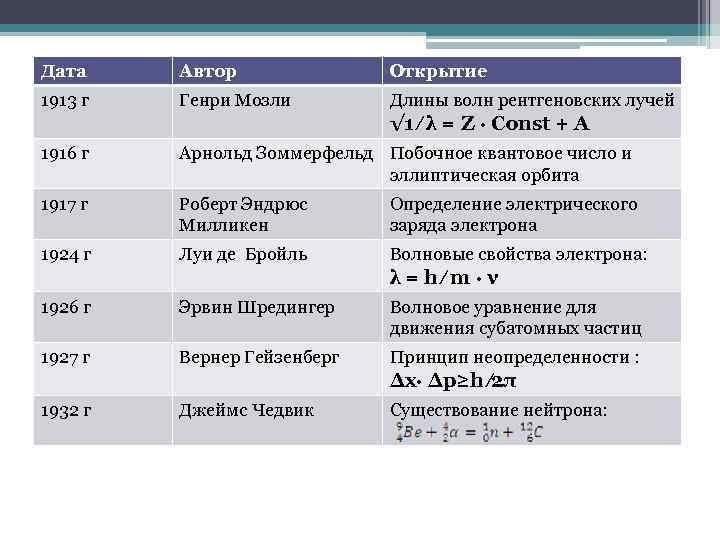 Дата Автор Открытие 1913 г Генри Мозли Длины волн рентгеновских лучей √ 1 ∕ λ = Z ∙ Const + A 1916 г Арнольд Зоммерфельд Побочное квантовое число и эллиптическая орбита 1917 г Роберт Эндрюс Милликен Определение электрического заряда электрона 1924 г Луи де Бройль Волновые свойства электрона: λ=h∕m∙ν 1926 г Эрвин Шредингер Волновое уравнение для движения субатомных частиц 1927 г Вернер Гейзенберг Принцип неопределенности : ∆x∙ ∆р≥h ∕ 2π 1932 г Джеймс Чедвик Существование нейтрона:
Дата Автор Открытие 1913 г Генри Мозли Длины волн рентгеновских лучей √ 1 ∕ λ = Z ∙ Const + A 1916 г Арнольд Зоммерфельд Побочное квантовое число и эллиптическая орбита 1917 г Роберт Эндрюс Милликен Определение электрического заряда электрона 1924 г Луи де Бройль Волновые свойства электрона: λ=h∕m∙ν 1926 г Эрвин Шредингер Волновое уравнение для движения субатомных частиц 1927 г Вернер Гейзенберг Принцип неопределенности : ∆x∙ ∆р≥h ∕ 2π 1932 г Джеймс Чедвик Существование нейтрона:
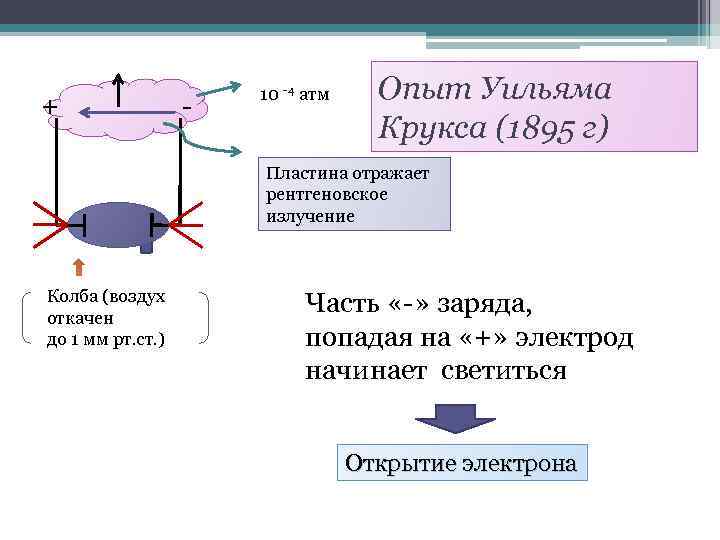 + - 10 -4 атм Опыт Уильяма Крукса (1895 г) Пластина отражает рентгеновское излучение Колба (воздух откачен до 1 мм рт. ст. ) Часть «-» заряда, попадая на «+» электрод начинает светиться Открытие электрона
+ - 10 -4 атм Опыт Уильяма Крукса (1895 г) Пластина отражает рентгеновское излучение Колба (воздух откачен до 1 мм рт. ст. ) Часть «-» заряда, попадая на «+» электрод начинает светиться Открытие электрона
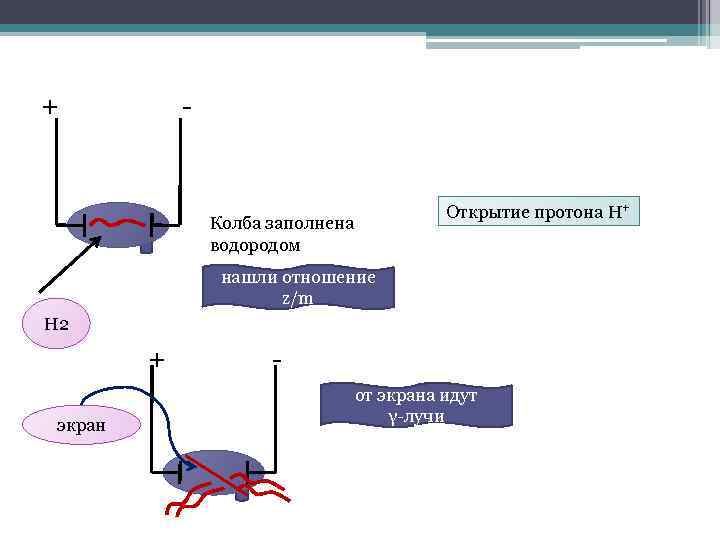 + - Открытие протона H+ Колба заполнена водородом нашли отношение z/m Н 2 + экран от экрана идут γ-лучи
+ - Открытие протона H+ Колба заполнена водородом нашли отношение z/m Н 2 + экран от экрана идут γ-лучи
 1896 г. – Беккерель Изучая радиоактивность, выделил : α-ядра 4 Не 2+ β-электроны γ-кванты Атом перестал быть неделим
1896 г. – Беккерель Изучая радиоактивность, выделил : α-ядра 4 Не 2+ β-электроны γ-кванты Атом перестал быть неделим
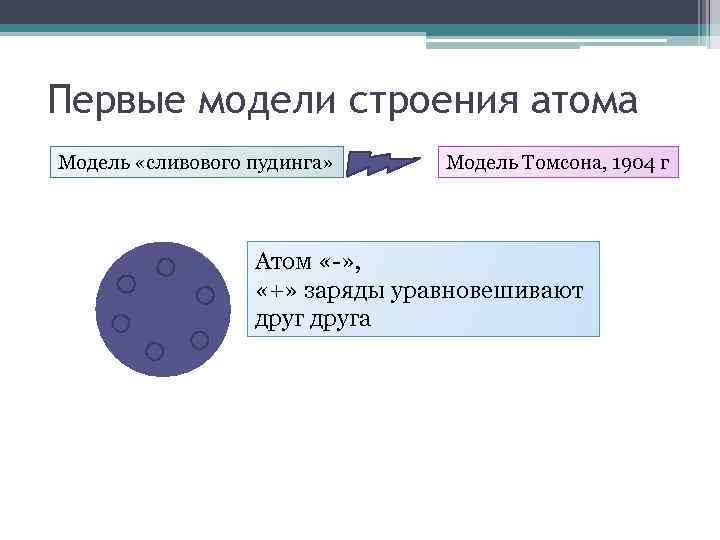 Первые модели строения атома Модель «сливового пудинга» Модель Томсона, 1904 г Атом «-» , «+» заряды уравновешивают друга
Первые модели строения атома Модель «сливового пудинга» Модель Томсона, 1904 г Атом «-» , «+» заряды уравновешивают друга
 Ядерная модель атома Резерфорда, 1911 г «+» заряженное ядро окружено облаком электронов
Ядерная модель атома Резерфорда, 1911 г «+» заряженное ядро окружено облаком электронов
 Планетарная модель атома, (Бор, 1911) Электроны движутся вокруг ядра по круговым орбитам Три постулата Бора: ØЭлектрон находится в атоме на стационарной орбите ØЭлектрон не излучает энергию ØЭнергия излучается при переходе электрона с одной орбиты на другую
Планетарная модель атома, (Бор, 1911) Электроны движутся вокруг ядра по круговым орбитам Три постулата Бора: ØЭлектрон находится в атоме на стационарной орбите ØЭлектрон не излучает энергию ØЭнергия излучается при переходе электрона с одной орбиты на другую
 Гипотезы о движении электронов • В. Гейзенберг (немецкий физик-теоретик)матричная механика. Электрон – частица • Э. Шрёдингер (австрийский физик-теоретик) – волновая механика. Электрон - волна Квантовомеханическая теория строения атома. Атом - система микрочастиц, не подчиняющихся законам классической механики.
Гипотезы о движении электронов • В. Гейзенберг (немецкий физик-теоретик)матричная механика. Электрон – частица • Э. Шрёдингер (австрийский физик-теоретик) – волновая механика. Электрон - волна Квантовомеханическая теория строения атома. Атом - система микрочастиц, не подчиняющихся законам классической механики.
 Квантование энергии электрона в атоме • Величины, принимающие определенные, дискретные значения (латинское "дискретус" - разделенный, прерывистый) – квантуются • В 1900 г. М. Планк (немецкий физик) изучавший тепловое излучение твердых тел. • Электромагнитное излучение испускается в виде отдельных порций квантов - энергии.
Квантование энергии электрона в атоме • Величины, принимающие определенные, дискретные значения (латинское "дискретус" - разделенный, прерывистый) – квантуются • В 1900 г. М. Планк (немецкий физик) изучавший тепловое излучение твердых тел. • Электромагнитное излучение испускается в виде отдельных порций квантов - энергии.
 1 квант энергии: ΔE - энергия кванта, Дж ΔE = hν, ν - частота, с-1 h - постоянная Планка (одна из фундаментальных постоянных природы), равная 6, 626· 10− 34 Дж·с. Кванты энергии - фотоны Квантование энергии позволило объяснить происхождение линейчатых атомных спектров, состоящих из набора линий, объединенных в линии
1 квант энергии: ΔE - энергия кванта, Дж ΔE = hν, ν - частота, с-1 h - постоянная Планка (одна из фундаментальных постоянных природы), равная 6, 626· 10− 34 Дж·с. Кванты энергии - фотоны Квантование энергии позволило объяснить происхождение линейчатых атомных спектров, состоящих из набора линий, объединенных в линии
 1885 г. - И. Я. Бальмер (швейцарский физик и математик) - длины волн, соответствующие определенным линиям в спектре атомов водорода, можно выразить как ряд целых чисел. 1 / λ = R(1 / n 12 − 1 / n 22), Предложенное уравнение, позднее модифицировано шведским физиком Ю. Р. Ридбергом λ - длина волны, см; R - постоянная Ридберга для атома водорода равная 1, 097373· 105 см− 1, n 1 и n 2 - целые числа, причем n 1 < n 2.
1885 г. - И. Я. Бальмер (швейцарский физик и математик) - длины волн, соответствующие определенным линиям в спектре атомов водорода, можно выразить как ряд целых чисел. 1 / λ = R(1 / n 12 − 1 / n 22), Предложенное уравнение, позднее модифицировано шведским физиком Ю. Р. Ридбергом λ - длина волны, см; R - постоянная Ридберга для атома водорода равная 1, 097373· 105 см− 1, n 1 и n 2 - целые числа, причем n 1 < n 2.
 Первая квантовая теория строения атома была предложена Н. Бором. v в изолированном атоме электроны двигаются по круговым стационарным орбитам, находясь на которых, они не излучают и не поглощают энергию. v Каждой такой орбите отвечает дискретное значение энергии. v Переход электрона из одного стационарного состояния в другое сопровождается излучением кванта электромагнитного излучения, частота которого равна v ν = ΔE / h, v где ΔE - разность энергий начального и конечного состояний электрона, v h - постоянная Планка.
Первая квантовая теория строения атома была предложена Н. Бором. v в изолированном атоме электроны двигаются по круговым стационарным орбитам, находясь на которых, они не излучают и не поглощают энергию. v Каждой такой орбите отвечает дискретное значение энергии. v Переход электрона из одного стационарного состояния в другое сопровождается излучением кванта электромагнитного излучения, частота которого равна v ν = ΔE / h, v где ΔE - разность энергий начального и конечного состояний электрона, v h - постоянная Планка.
 Важный принцип квантовой механики – дискретность электрона Электроны в атоме могут иметь лишь строго определенные значения энергии. Электронам - разрешен переход с одного уровня энергии на другой, - запрещены промежуточные состояния.
Важный принцип квантовой механики – дискретность электрона Электроны в атоме могут иметь лишь строго определенные значения энергии. Электронам - разрешен переход с одного уровня энергии на другой, - запрещены промежуточные состояния.
 Двойственная природа электрона • В механике рассматривается 2 вида движения: • движение тела с локализацией перемещающегося объекта в каждой точке траектории в определенный момент времени • движение волны, делокализованной в пространстве среды • Для микрообъектов такое разграничение движения невозможно. • Эту особенность движения называют корпускулярно-волновым дуализмом.
Двойственная природа электрона • В механике рассматривается 2 вида движения: • движение тела с локализацией перемещающегося объекта в каждой точке траектории в определенный момент времени • движение волны, делокализованной в пространстве среды • Для микрообъектов такое разграничение движения невозможно. • Эту особенность движения называют корпускулярно-волновым дуализмом.
 Корпускулярноволновой дуализм (КВД) способность микрочастицы, обладающей массой, размерами и зарядом, одновременно проявлять и свойства, характерные для волн, например, способность к дифракции. В зависимости от того, какие свойства частиц изучаются, они проявляют либо одни, либо другие свойства.
Корпускулярноволновой дуализм (КВД) способность микрочастицы, обладающей массой, размерами и зарядом, одновременно проявлять и свойства, характерные для волн, например, способность к дифракции. В зависимости от того, какие свойства частиц изучаются, они проявляют либо одни, либо другие свойства.
 А. Эйнштейн – автор идеи КВД предложил рассматривать кванты электромагнитного излучения - фотоны как движущиеся со скоростью света частицы, имеющие нулевую массу покоя. Их энергия равна E = mc 2 = hν = hc / λ, где m - масса фотона, ν - частота излучения, с - скорость света в вакууме, λ - длина волны. h - постоянная Планка,
А. Эйнштейн – автор идеи КВД предложил рассматривать кванты электромагнитного излучения - фотоны как движущиеся со скоростью света частицы, имеющие нулевую массу покоя. Их энергия равна E = mc 2 = hν = hc / λ, где m - масса фотона, ν - частота излучения, с - скорость света в вакууме, λ - длина волны. h - постоянная Планка,
 В 1924 г. французский физик Л. де Бройль корпускулярно-волновыми свойствами обладает не только фотон, но и любая другая частица, движущаяся со скоростью v. уравнение, связывающее скорость движения частицы с длиной волны производимого ей электромагнитного излучения где m - масса частицы, v - ее скорость, h - постоянная Планка; λ = h / mv, (уравнение де Бройля): величина λ получила название длины волны де -Бройля.
В 1924 г. французский физик Л. де Бройль корпускулярно-волновыми свойствами обладает не только фотон, но и любая другая частица, движущаяся со скоростью v. уравнение, связывающее скорость движения частицы с длиной волны производимого ей электромагнитного излучения где m - масса частицы, v - ее скорость, h - постоянная Планка; λ = h / mv, (уравнение де Бройля): величина λ получила название длины волны де -Бройля.
 Соотношение неопределенностей Гейзенберга ØΔp · Δ x ≥ h / 2π, Ø В 1927 г. немецкий физиктеоретик В. Гейзенберг сформулировал принцип неопределенности Ø принципиальная невозможность одновременно точно определить положение микрочастицы в пространстве и ее импульс: x Ø где Δpx = m Δvxx – неопределенность (ошибка в определении) импульса микрообъекта по координате х; Δx - неопределенность (ошибка в определении) положения микрообъекта по этой координате.
Соотношение неопределенностей Гейзенберга ØΔp · Δ x ≥ h / 2π, Ø В 1927 г. немецкий физиктеоретик В. Гейзенберг сформулировал принцип неопределенности Ø принципиальная невозможность одновременно точно определить положение микрочастицы в пространстве и ее импульс: x Ø где Δpx = m Δvxx – неопределенность (ошибка в определении) импульса микрообъекта по координате х; Δx - неопределенность (ошибка в определении) положения микрообъекта по этой координате.
 Выводы: v. Чем точнее определена скорость, тем меньше известно о местоположении частицы, и наоборот. v. Можно лишь говорить о вероятности обнаружить ее какой-то областях пространства. v. Поэтому для микрочастицы становится неприемлемым понятие о траектории движения, поскольку оно связано с конкретными координатами и импульсом частицы. v. Произошел переход от "орбит движения" электронов, введенных Бором, к понятию орбитали – области пространства, где вероятность пребывания электронов максимальна.
Выводы: v. Чем точнее определена скорость, тем меньше известно о местоположении частицы, и наоборот. v. Можно лишь говорить о вероятности обнаружить ее какой-то областях пространства. v. Поэтому для микрочастицы становится неприемлемым понятие о траектории движения, поскольку оно связано с конкретными координатами и импульсом частицы. v. Произошел переход от "орбит движения" электронов, введенных Бором, к понятию орбитали – области пространства, где вероятность пребывания электронов максимальна.
 Уравнение Шрёдингера Волновое уравнение (1926 г. ) - описание состояния электрона в атоме водорода. объединение математических выражений для колебательных процессов и уравнения де Бройля где Ψ - волновая функция (аналог Ψ характеризует движение амплитуды для волнового электрона в пространстве как движения в классической волнообразное возмущение; механике), x, y, z - координаты, E - полная энергия электрона, m - масса покоя электрона, Ep - потенциальная энергия h - постоянная Планка, электрона.
Уравнение Шрёдингера Волновое уравнение (1926 г. ) - описание состояния электрона в атоме водорода. объединение математических выражений для колебательных процессов и уравнения де Бройля где Ψ - волновая функция (аналог Ψ характеризует движение амплитуды для волнового электрона в пространстве как движения в классической волнообразное возмущение; механике), x, y, z - координаты, E - полная энергия электрона, m - масса покоя электрона, Ep - потенциальная энергия h - постоянная Планка, электрона.
 Решениями уравнения Шрёдингера являются волновые функции. Для одноэлектронной системы (атома водорода) выражение для потенциальной энергии электрона имеет простой вид: где e - заряд электрона, Ep = -e 2 / r r - расстояние от электрона до ядра. В этом случае уравнение Шрёдингера имеет точное решение.
Решениями уравнения Шрёдингера являются волновые функции. Для одноэлектронной системы (атома водорода) выражение для потенциальной энергии электрона имеет простой вид: где e - заряд электрона, Ep = -e 2 / r r - расстояние от электрона до ядра. В этом случае уравнение Шрёдингера имеет точное решение.
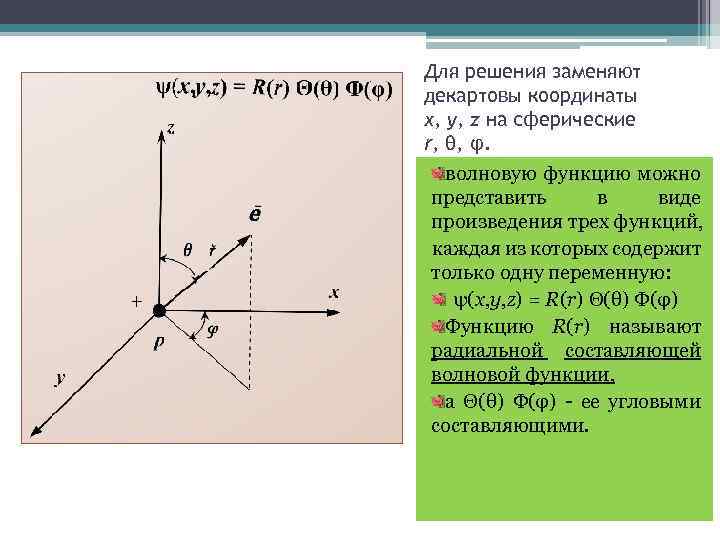 Для решения заменяют декартовы координаты x, y, z на сферические r, θ, φ. волновую функцию можно представить в виде произведения трех функций, каждая из которых содержит только одну переменную: ψ(x, y, z) = R(r) Θ(θ) Φ(φ) Функцию R(r) называют радиальной составляющей волновой функции, а Θ(θ) Φ(φ) - ее угловыми составляющими.
Для решения заменяют декартовы координаты x, y, z на сферические r, θ, φ. волновую функцию можно представить в виде произведения трех функций, каждая из которых содержит только одну переменную: ψ(x, y, z) = R(r) Θ(θ) Φ(φ) Функцию R(r) называют радиальной составляющей волновой функции, а Θ(θ) Φ(φ) - ее угловыми составляющими.
 Квантовые числа Øглавное n Øорбитальное l Øмагнитное ml ØФункция R(r) зависит от n и l ØФункция Θ(θ) - от l и ml ØФункция Φ(φ) - от ml.
Квантовые числа Øглавное n Øорбитальное l Øмагнитное ml ØФункция R(r) зависит от n и l ØФункция Θ(θ) - от l и ml ØФункция Φ(φ) - от ml.
 Атомная орбиталь - геометрический образ одноэлектронной волновой функции Орбиталь – область пространства вокруг ядра атома, в которой высока вероятность обнаружения электрона (обычно выбирают значение вероятности 90 -95%). Контуры атомной орбитали графическое отображение волновой функции, полученной при решении волнового уравнения для одного электрона.
Атомная орбиталь - геометрический образ одноэлектронной волновой функции Орбиталь – область пространства вокруг ядра атома, в которой высока вероятность обнаружения электрона (обычно выбирают значение вероятности 90 -95%). Контуры атомной орбитали графическое отображение волновой функции, полученной при решении волнового уравнения для одного электрона.
 Главное квантовое число n характеризует энергию атомной орбитали. принимает любые положительные целочисленные значения. Чем больше значение n, тем выше энергия и больше размер Каждому значению главного орбитали. квантового числа отвечает определенное значение энергии электрона. Уровни энергии с определенными значениями n иногда обозначают буквами K, L, M, N. . . (для n = 1, 2, 3, 4. . . ).
Главное квантовое число n характеризует энергию атомной орбитали. принимает любые положительные целочисленные значения. Чем больше значение n, тем выше энергия и больше размер Каждому значению главного орбитали. квантового числа отвечает определенное значение энергии электрона. Уровни энергии с определенными значениями n иногда обозначают буквами K, L, M, N. . . (для n = 1, 2, 3, 4. . . ).

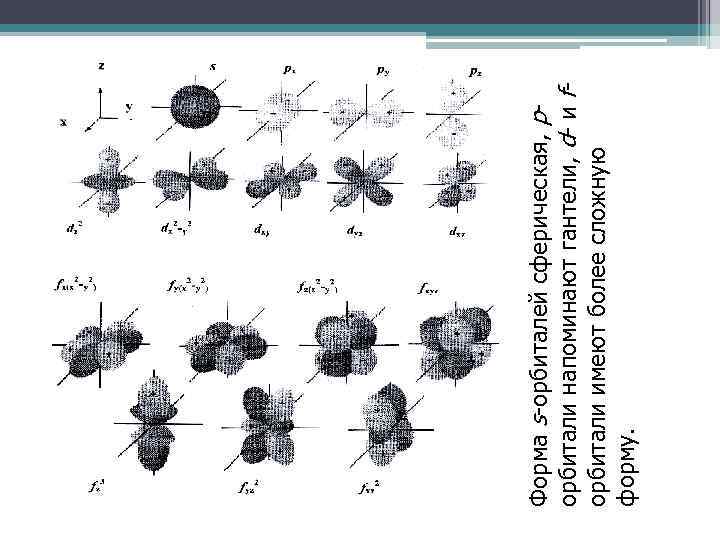 Форма s-орбиталей сферическая, pорбитали напоминают гантели, d- и fорбитали имеют более сложную форму.
Форма s-орбиталей сферическая, pорбитали напоминают гантели, d- и fорбитали имеют более сложную форму.
 Магнитное квантовое число ml Для каждого значения l отвечает за ориентацию атомных орбиталей в пространстве. магнитное квантовое число ml может принимать целочисленные значения от −l до +l (всего 2 l + 1 значений) Например, р-орбитали (l = 1) могут быть ориентированы тремя способами (ml = -1, 0, +1)
Магнитное квантовое число ml Для каждого значения l отвечает за ориентацию атомных орбиталей в пространстве. магнитное квантовое число ml может принимать целочисленные значения от −l до +l (всего 2 l + 1 значений) Например, р-орбитали (l = 1) могут быть ориентированы тремя способами (ml = -1, 0, +1)
 Электрон, занимающий определенную орбиталь ms – спин электрона - одно из свойств (наряду с массой и зарядом) этой элементарной частицы.
Электрон, занимающий определенную орбиталь ms – спин электрона - одно из свойств (наряду с массой и зарядом) этой элементарной частицы.
 Спин - собственный магнитный момент количества движения элементарной частицы. Спин электрона характеризуется спиновым квантовым числом ms, которое может быть равно +1/2 и − 1/2 Квантовые числа для электрона в атоме Главное квантовое число n Орбитальное квантовое число l Магнитное квантовое число ml Спиновое квантовое число ms
Спин - собственный магнитный момент количества движения элементарной частицы. Спин электрона характеризуется спиновым квантовым числом ms, которое может быть равно +1/2 и − 1/2 Квантовые числа для электрона в атоме Главное квантовое число n Орбитальное квантовое число l Магнитное квантовое число ml Спиновое квантовое число ms
 Совокупность состояний электрона в атоме с одним и тем же значением n называют энергетическим уровнем. Число уровней, на которых совпадает с номером периода, находятся электроны в основном состоянии атома, в котором располагается элемент Номера этих уровней обозначают цифрами: 1, 2, 3, . . . (реже - буквами K, L, M, . . . )
Совокупность состояний электрона в атоме с одним и тем же значением n называют энергетическим уровнем. Число уровней, на которых совпадает с номером периода, находятся электроны в основном состоянии атома, в котором располагается элемент Номера этих уровней обозначают цифрами: 1, 2, 3, . . . (реже - буквами K, L, M, . . . )
 Энергетический подуровень совокупность энергетических состояний электрона в атоме, характеризуется одними и теми же значениями квантовых чисел n и l Подуровни обозначают буквами: s, p, d, f. . . второй - два подуровня, Первый энергетический уровень имеет один подуровень, третий - три подуровня и так далее
Энергетический подуровень совокупность энергетических состояний электрона в атоме, характеризуется одними и теми же значениями квантовых чисел n и l Подуровни обозначают буквами: s, p, d, f. . . второй - два подуровня, Первый энергетический уровень имеет один подуровень, третий - три подуровня и так далее
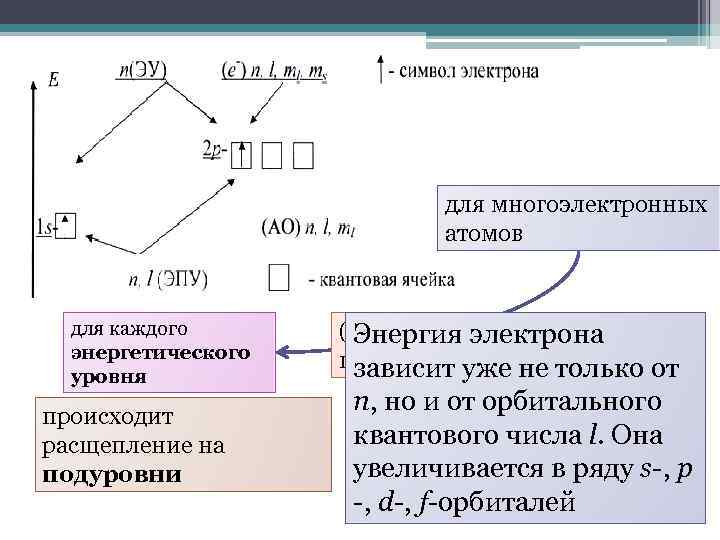 для многоэлектронных атомов для каждого энергетического уровня происходит расщепление на подуровни (при данном значении Энергия электрона главного квантового числа n) зависит уже не только от n, но и от орбитального квантового числа l. Она увеличивается в ряду s-, p -, d-, f-орбиталей
для многоэлектронных атомов для каждого энергетического уровня происходит расщепление на подуровни (при данном значении Энергия электрона главного квантового числа n) зависит уже не только от n, но и от орбитального квантового числа l. Она увеличивается в ряду s-, p -, d-, f-орбиталей
 Принцип минимума энергии определяет порядок заселения атомных орбиталей, имеющих различные энергии электроны занимают в первую очередь орбитали, имеющие наименьшую энергию Энергия подуровней растет в ряду: 1 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s < 4 f ≈ 5 d < 6 p < 7 s < 5 f ≈ 6 d. . .
Принцип минимума энергии определяет порядок заселения атомных орбиталей, имеющих различные энергии электроны занимают в первую очередь орбитали, имеющие наименьшую энергию Энергия подуровней растет в ряду: 1 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s < 4 f ≈ 5 d < 6 p < 7 s < 5 f ≈ 6 d. . .
 принцип запрета ограничивает число электронов, которые могут находиться на одной орбитали. На любой орбитали может находиться не более двух электронов Поэтому в атоме не должно быть двух электронов с одинаковыми четырьмя квантовыми числами (n, l, ms). в том случае, если они имеют противоположные спины (неодинаковые спиновые числа).
принцип запрета ограничивает число электронов, которые могут находиться на одной орбитали. На любой орбитали может находиться не более двух электронов Поэтому в атоме не должно быть двух электронов с одинаковыми четырьмя квантовыми числами (n, l, ms). в том случае, если они имеют противоположные спины (неодинаковые спиновые числа).
 Правило Гунда 1927 г. - на основе атомных спектров определяет порядок заселения электронами орбиталей, имеющих одинаковую энергию Последовательность заселения атомных орбиталей электронами
Правило Гунда 1927 г. - на основе атомных спектров определяет порядок заселения электронами орбиталей, имеющих одинаковую энергию Последовательность заселения атомных орбиталей электронами
 порядок заселения орбиталей электронами и построение электронной формулы любого элемента.
порядок заселения орбиталей электронами и построение электронной формулы любого элемента.
 Электронная конфигурация атома Электронная формула атома • Распределение электронов по орбиталям в основном (невозбужденном) состоянии атома и его ионов: • 1 s 22 p 63 s 23 p 6. . . Число электронов на орбиталях подуровня • указывается в верхнем индексе справа от буквы, • например 3 d 5 это 5 электронов на 3 d-подуровне.
Электронная конфигурация атома Электронная формула атома • Распределение электронов по орбиталям в основном (невозбужденном) состоянии атома и его ионов: • 1 s 22 p 63 s 23 p 6. . . Число электронов на орбиталях подуровня • указывается в верхнем индексе справа от буквы, • например 3 d 5 это 5 электронов на 3 d-подуровне.
![1 s 2 = [He] 1 s 22 p 6 = [Ne] 1 s 1 s 2 = [He] 1 s 22 p 6 = [Ne] 1 s](https://present5.com/presentation/157088600_437574200/image-43.jpg) 1 s 2 = [He] 1 s 22 p 6 = [Ne] 1 s 22 p 63 s 23 p 6 = [Ar] электронная формула атома хлора 1 s 22 p 63 s 23 p 5, или [Ne]3 s 23 p 5 За скобки вынесены валентные электроны, принимающие участие в образовании химических связей
1 s 2 = [He] 1 s 22 p 6 = [Ne] 1 s 22 p 63 s 23 p 6 = [Ar] электронная формула атома хлора 1 s 22 p 63 s 23 p 5, или [Ne]3 s 23 p 5 За скобки вынесены валентные электроны, принимающие участие в образовании химических связей


