Vvedenie_v_zelyonuyu_khimiyu-_ZR-2012.ppt
- Количество слайдов: 50
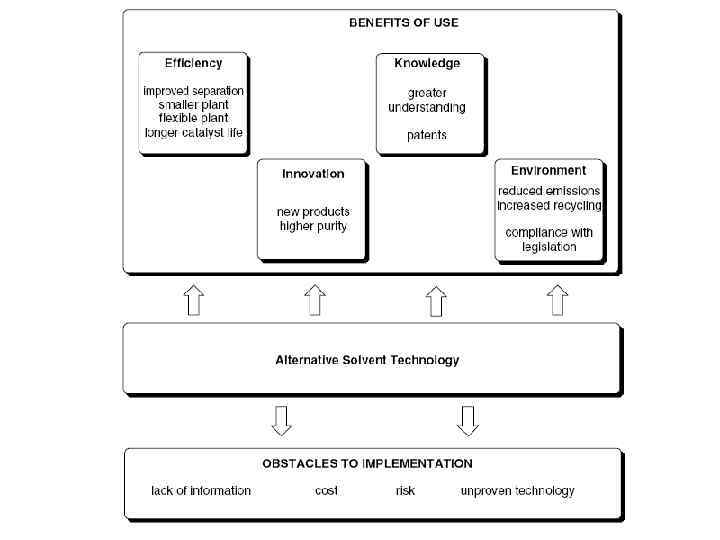
 Введение в «зелёную» химию «Зеленые» растворители
Введение в «зелёную» химию «Зеленые» растворители
 Предел мечтаний химика-синтетика Хочу, чтобы: • Реакция протекала в нужном направлении, • Был обеспечен максимальный выход продуктов реакции, • Реакция протекала с достаточной скоростью.
Предел мечтаний химика-синтетика Хочу, чтобы: • Реакция протекала в нужном направлении, • Был обеспечен максимальный выход продуктов реакции, • Реакция протекала с достаточной скоростью.
 Успех Определяется следующими факторами: • удачный выбор метода синтеза или аппаратурного оформления, • подбор катализатора, • оптимальный температурный режим, • чистота исходных реактивов, • некоторые тактические приемы • удачный выбор растворителя.
Успех Определяется следующими факторами: • удачный выбор метода синтеза или аппаратурного оформления, • подбор катализатора, • оптимальный температурный режим, • чистота исходных реактивов, • некоторые тактические приемы • удачный выбор растворителя.
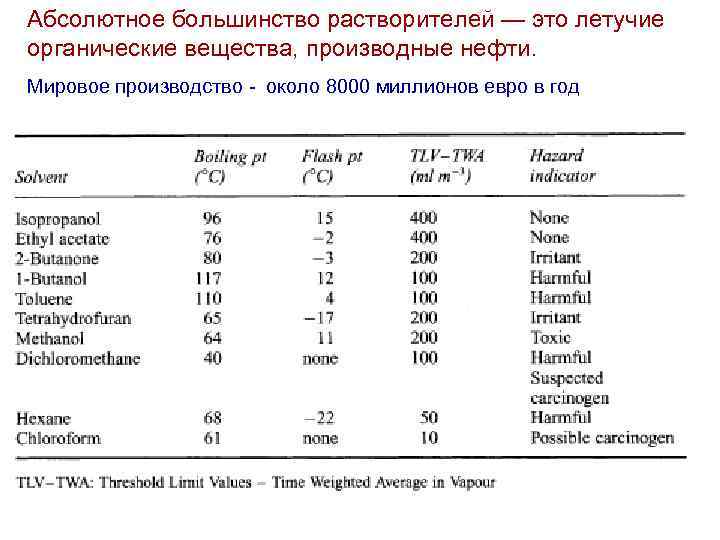 Абсолютное большинство растворителей — это летучие органические вещества, производные нефти. Мировое производство - около 8000 миллионов евро в год
Абсолютное большинство растворителей — это летучие органические вещества, производные нефти. Мировое производство - около 8000 миллионов евро в год
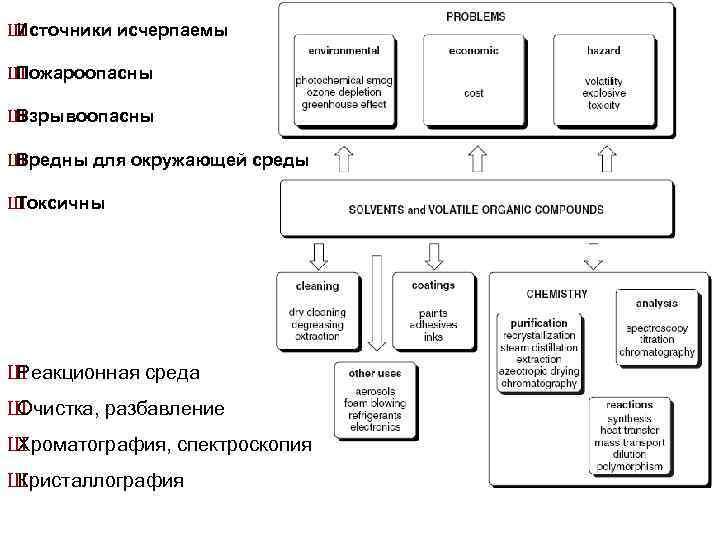 Ш Источники исчерпаемы Ш Пожароопасны Ш Взрывоопасны Ш Вредны для окружающей среды Ш Токсичны Ш Реакционная среда Ш Очистка, разбавление Ш Хроматография, спектроскопия Ш Кристаллография
Ш Источники исчерпаемы Ш Пожароопасны Ш Взрывоопасны Ш Вредны для окружающей среды Ш Токсичны Ш Реакционная среда Ш Очистка, разбавление Ш Хроматография, спектроскопия Ш Кристаллография
 Strategies of solvent replacement • Avoid or minimise solvents in first place • Use less toxic solvents • Use renewable solvents (not derived from petrochemicals) • Avoid VOC’s – solvents with high boiling points may be preferable as long as this does not lead to other complications.
Strategies of solvent replacement • Avoid or minimise solvents in first place • Use less toxic solvents • Use renewable solvents (not derived from petrochemicals) • Avoid VOC’s – solvents with high boiling points may be preferable as long as this does not lead to other complications.
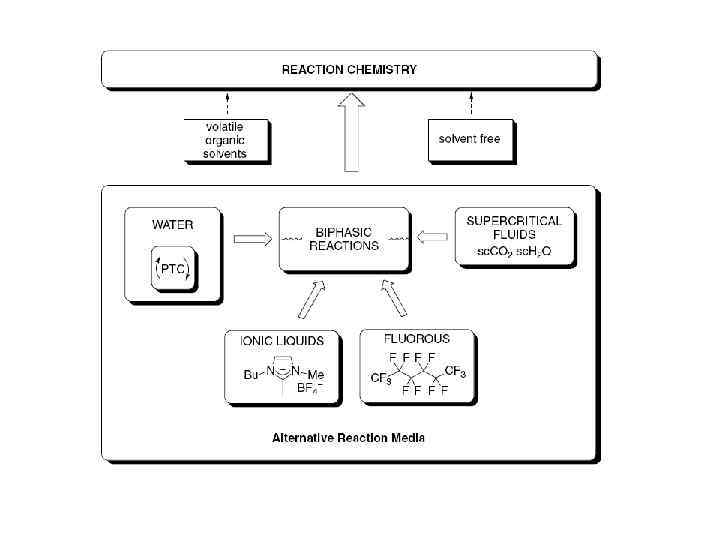
 Альтернативы Ш Проведение химических процессов без органических растворителей Ш Диметилкарбонат Ш Сверхкритические среды Ш Ионные жидкости Ш Фторированные бифазные растворители All have advantages and disadvantages which need to be considered when assessing suitability for replacement
Альтернативы Ш Проведение химических процессов без органических растворителей Ш Диметилкарбонат Ш Сверхкритические среды Ш Ионные жидкости Ш Фторированные бифазные растворители All have advantages and disadvantages which need to be considered when assessing suitability for replacement
 ‘Solventless’ chemistry • Has been around for many years • Provides one of the simplest solutions to the problem of solvents • Not many reactions amenable to solventless approach, particularly on large scale • Exothermic reactions can be dangerous on large scale – need close collaboration with chemical engineers to overcome such problems • Efficient mixing can be a problem, particularly when have solid reagents or products • Solvents still often required for extraction, separation and purification of products
‘Solventless’ chemistry • Has been around for many years • Provides one of the simplest solutions to the problem of solvents • Not many reactions amenable to solventless approach, particularly on large scale • Exothermic reactions can be dangerous on large scale – need close collaboration with chemical engineers to overcome such problems • Efficient mixing can be a problem, particularly when have solid reagents or products • Solvents still often required for extraction, separation and purification of products
 Проведение химических процессов без ОР • Реакции восстановления R 1, R 2 = Ph Условия проведения: твердофазная реакция, соотношение кетон : Na. BH 4 = 1: 10, комнатная температура, периодическое перемешивание и измельчение, 5 дней
Проведение химических процессов без ОР • Реакции восстановления R 1, R 2 = Ph Условия проведения: твердофазная реакция, соотношение кетон : Na. BH 4 = 1: 10, комнатная температура, периодическое перемешивание и измельчение, 5 дней
 Проведение химических процессов без ОР • Реакции окисления R 1, R 2 = Ph Условия проведения: твердофазная реакция, соотношение кетон : хлорпербензойная кислота = 1: 2, комнатная температура, перемешивание и измельчение 1 раз в день. Избыток пероксида удаляется с помощью 20% Na. HSO 4
Проведение химических процессов без ОР • Реакции окисления R 1, R 2 = Ph Условия проведения: твердофазная реакция, соотношение кетон : хлорпербензойная кислота = 1: 2, комнатная температура, перемешивание и измельчение 1 раз в день. Избыток пероксида удаляется с помощью 20% Na. HSO 4
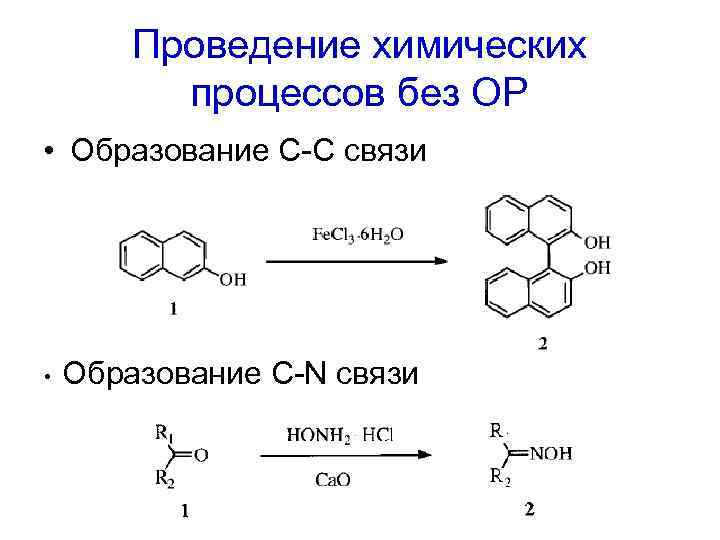 Проведение химических процессов без ОР • Образование С-С связи • Образование C-N связи
Проведение химических процессов без ОР • Образование С-С связи • Образование C-N связи
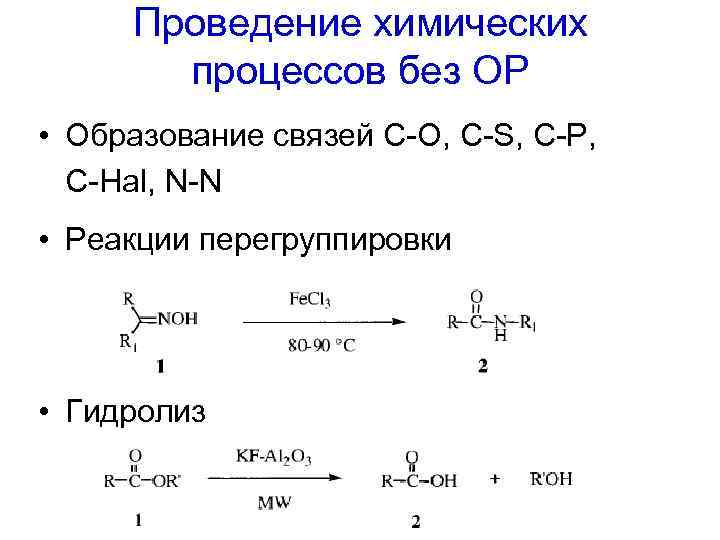 Проведение химических процессов без ОР • Образование связей С-О, C-S, C-P, C-Hal, N-N • Реакции перегруппировки • Гидролиз
Проведение химических процессов без ОР • Образование связей С-О, C-S, C-P, C-Hal, N-N • Реакции перегруппировки • Гидролиз
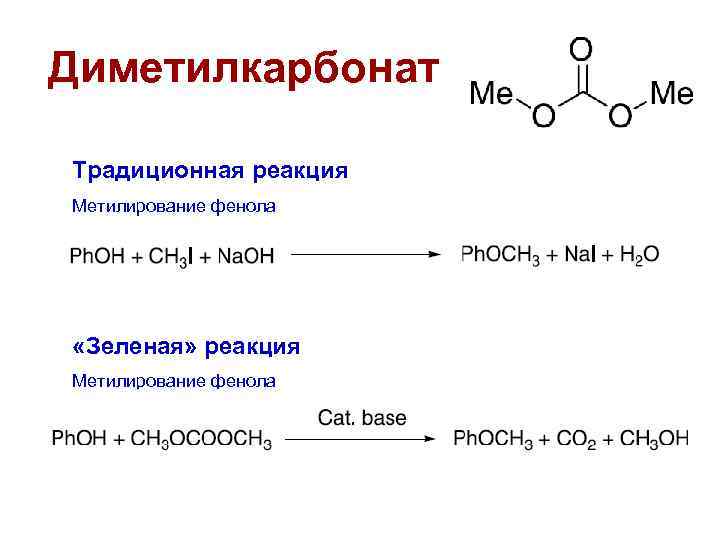 Диметилкарбонат Традиционная реакция Метилирование фенола «Зеленая» реакция Метилирование фенола
Диметилкарбонат Традиционная реакция Метилирование фенола «Зеленая» реакция Метилирование фенола
 Почему диметилкарбонат? • Биоразлагаемый (более 90%, в течение 28 дней, тест OECD 301 C) • Не оказывает влияния на рыб при концентрации 1000 мг/л (тест OECD 203) • Малотоксичен LD 50 при проглатывании 13, 8 г/кг LD 50 при вдыхании 140 мг/л • Не вызывает раздражения • Не обладает мутагенным действием • Простота получения
Почему диметилкарбонат? • Биоразлагаемый (более 90%, в течение 28 дней, тест OECD 301 C) • Не оказывает влияния на рыб при концентрации 1000 мг/л (тест OECD 203) • Малотоксичен LD 50 при проглатывании 13, 8 г/кг LD 50 при вдыхании 140 мг/л • Не вызывает раздражения • Не обладает мутагенным действием • Простота получения
 Получение ДМК Долгое время производился из фосгена и метанола. Нежелательный продукт – HCl. C cередины 80 -х годов получают путем окислительного карбонилирования метанола в присутствии кислорода по процессу, разработанному компанией Enichem (Италия). Бесфосгеновая схема запатентована в 1984 г. Преимущества процесса: • Дешевое и легкодоступное сырье • Высококачественный конечный продукт • Нетоксичные побочные продукты
Получение ДМК Долгое время производился из фосгена и метанола. Нежелательный продукт – HCl. C cередины 80 -х годов получают путем окислительного карбонилирования метанола в присутствии кислорода по процессу, разработанному компанией Enichem (Италия). Бесфосгеновая схема запатентована в 1984 г. Преимущества процесса: • Дешевое и легкодоступное сырье • Высококачественный конечный продукт • Нетоксичные побочные продукты
 Получение ДМК • Основной недостаток окислительного карбонилирования метанола - трудность выделения реакционного продукта из-за образования азеотропных смесей между водой и диметилкарбонатом и между диметилкарбонатом и метанолом. • Для получения чистого диметилкарбоната предложены перегонка под давлением, при которой ликвидируется азеотроп, или использование специальных мембран.
Получение ДМК • Основной недостаток окислительного карбонилирования метанола - трудность выделения реакционного продукта из-за образования азеотропных смесей между водой и диметилкарбонатом и между диметилкарбонатом и метанолом. • Для получения чистого диметилкарбоната предложены перегонка под давлением, при которой ликвидируется азеотроп, или использование специальных мембран.
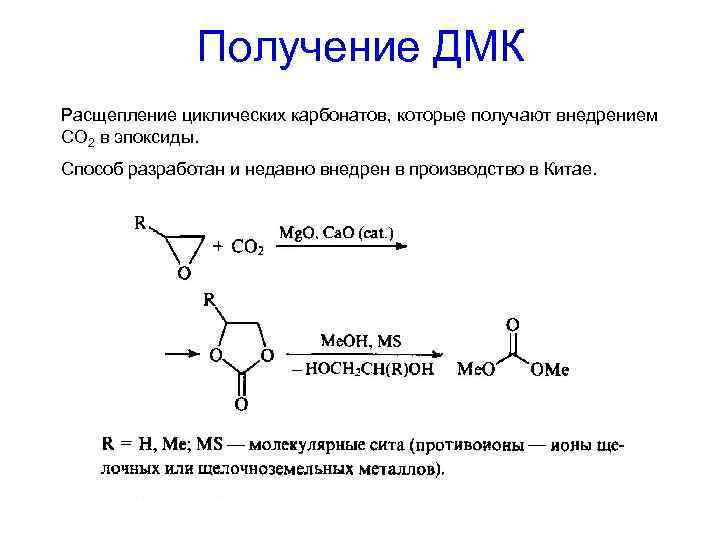 Получение ДМК Расщепление циклических карбонатов, которые получают внедрением СО 2 в эпоксиды. Способ разработан и недавно внедрен в производство в Китае.
Получение ДМК Расщепление циклических карбонатов, которые получают внедрением СО 2 в эпоксиды. Способ разработан и недавно внедрен в производство в Китае.
 ДМК как карбоксиметилирующий агент (заменитель фосгена) • Карбоксиметилирование аминов, которое имеет важное промышленное значение. • Образование карбаматов или уретанов (общая формула R'R''NCOOR ) Биологическая активность карбаматов обнаружена в 1923 году, когда впервые описана структура алкалоида эзерина (или физостигмина), содержавшегося в зернах Калабарских бобов. В 1929 году были синтезированы аналоги физостигмина. Изучение карбаминовых соединений началось в том же году, и сейчас известно более 1000 производных карбаминовой кислоты. Физостигма ядовитая или Калабарские бобы • Карбаматы – в фармацевтике и производстве средств защиты растений.
ДМК как карбоксиметилирующий агент (заменитель фосгена) • Карбоксиметилирование аминов, которое имеет важное промышленное значение. • Образование карбаматов или уретанов (общая формула R'R''NCOOR ) Биологическая активность карбаматов обнаружена в 1923 году, когда впервые описана структура алкалоида эзерина (или физостигмина), содержавшегося в зернах Калабарских бобов. В 1929 году были синтезированы аналоги физостигмина. Изучение карбаминовых соединений началось в том же году, и сейчас известно более 1000 производных карбаминовой кислоты. Физостигма ядовитая или Калабарские бобы • Карбаматы – в фармацевтике и производстве средств защиты растений.
 ДМК как карбоксиметилирующий агент (заменитель фосгена) • Карбоксиметилирование спиртов В общем случае реакция дает продукты переэтерификации
ДМК как карбоксиметилирующий агент (заменитель фосгена) • Карбоксиметилирование спиртов В общем случае реакция дает продукты переэтерификации
 ДМК как метилирующий агент (заменитель метилгалогенидов и метилсульфата) • Метилирование тиолов
ДМК как метилирующий агент (заменитель метилгалогенидов и метилсульфата) • Метилирование тиолов
 Другие области применения ДМК Присадка к бензину или дизельному топливу, может заменить метил-третбутиловый эфир. Способен уменьшать поверхностное натяжение фракций, кипящих в диапазоне дизельного топлива (ДТ с лучшим впрыскиванием и распылением).
Другие области применения ДМК Присадка к бензину или дизельному топливу, может заменить метил-третбутиловый эфир. Способен уменьшать поверхностное натяжение фракций, кипящих в диапазоне дизельного топлива (ДТ с лучшим впрыскиванием и распылением).
 Сверхкритические жидкости Сверхкритические флюиды (от англ. fluid - жидкость). Впервые сверхкритическое состояние вещества обнаружил Каньяр де ла Тур в 1822 году. Интерес возник в конце XIX века после экспериментов Т. Эндрюса.
Сверхкритические жидкости Сверхкритические флюиды (от англ. fluid - жидкость). Впервые сверхкритическое состояние вещества обнаружил Каньяр де ла Тур в 1822 году. Интерес возник в конце XIX века после экспериментов Т. Эндрюса.
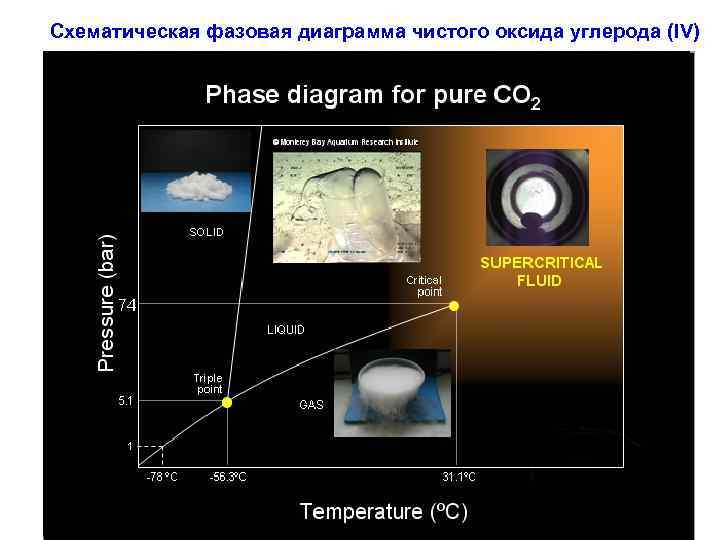 Схематическая фазовая диаграмма чистого оксида углерода (IV)
Схематическая фазовая диаграмма чистого оксида углерода (IV)
 Сверхкритическое состояние – это форма агрегатного состояния вещества, в которую способны переходить многие органические и неорганические вещества в условиях повышенного давления и температуры. Вещество в сверхкритическом состоянии представлено: свободными молекулами и многочисленными слабо связанными кластерами (от англ. сluster – рой, скопление) молекул.
Сверхкритическое состояние – это форма агрегатного состояния вещества, в которую способны переходить многие органические и неорганические вещества в условиях повышенного давления и температуры. Вещество в сверхкритическом состоянии представлено: свободными молекулами и многочисленными слабо связанными кластерами (от англ. сluster – рой, скопление) молекул.
 Особенности сверхкритического состояния Ш Расстояния между присутствующими в сверхкритической фазе частицами значительно больше, чем в жидкости, но намного меньше, чем в газах. Ш Внутри кластеров молекулы располагаются хаотично. Ш Энергия взаимодействия молекул в кластерах невелика. Ш Скорости, с которыми отдельные молекулы входят в кластеры и покидают их, очень высоки. Ш Исключительно низкая вязкость и одновременно высокая диффузионная способность сверхкритических сред, как у газов, и высокая плотность, как у жидкостей.
Особенности сверхкритического состояния Ш Расстояния между присутствующими в сверхкритической фазе частицами значительно больше, чем в жидкости, но намного меньше, чем в газах. Ш Внутри кластеров молекулы располагаются хаотично. Ш Энергия взаимодействия молекул в кластерах невелика. Ш Скорости, с которыми отдельные молекулы входят в кластеры и покидают их, очень высоки. Ш Исключительно низкая вязкость и одновременно высокая диффузионная способность сверхкритических сред, как у газов, и высокая плотность, как у жидкостей.
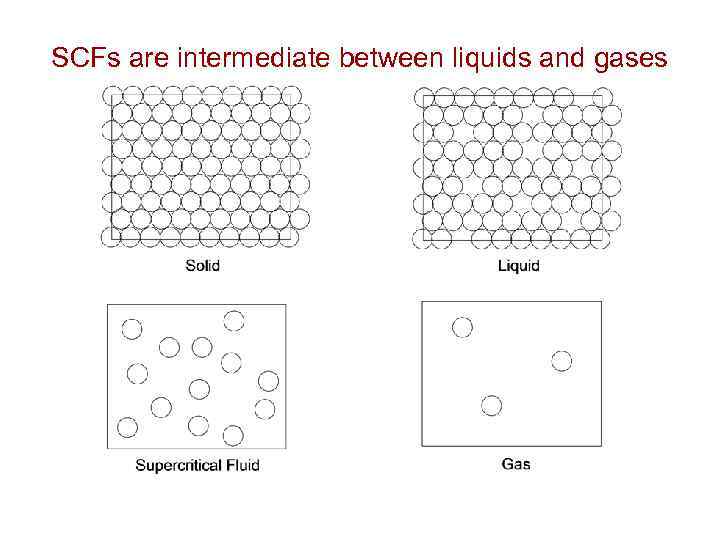 SCFs are intermediate between liquids and gases
SCFs are intermediate between liquids and gases
 Свойства сверхкритических жидкостей
Свойства сверхкритических жидкостей
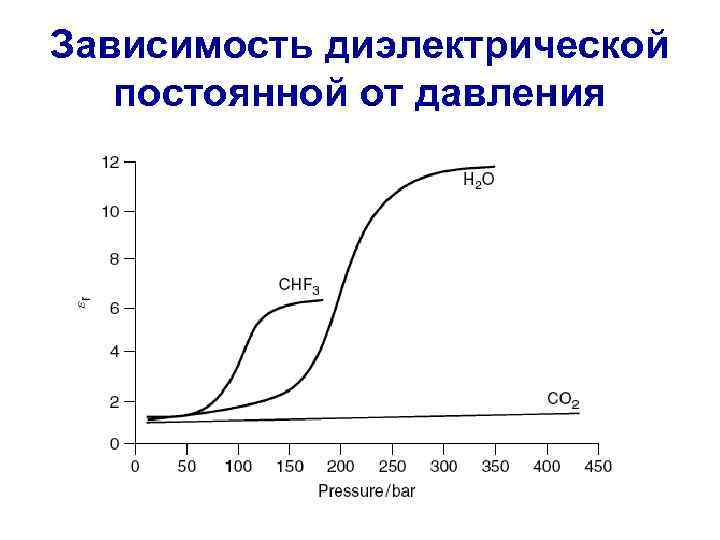 Зависимость диэлектрической постоянной от давления
Зависимость диэлектрической постоянной от давления
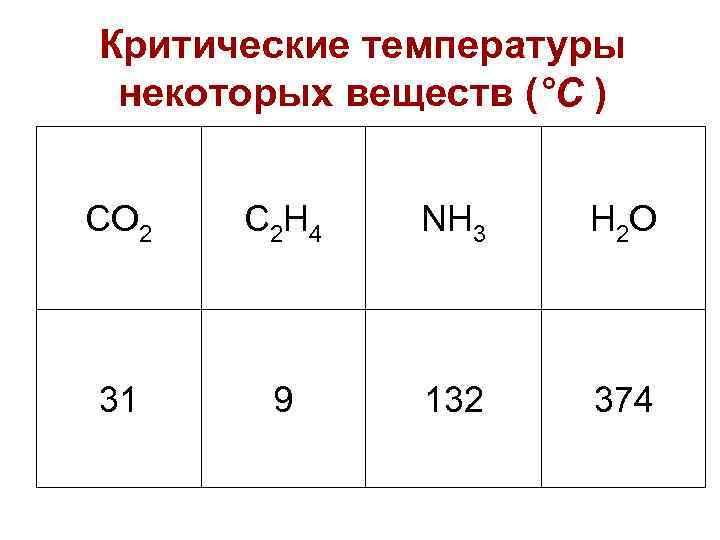 Критические температуры некоторых веществ (°С ) CO 2 C 2 H 4 NH 3 H 2 O 31 9 132 374
Критические температуры некоторых веществ (°С ) CO 2 C 2 H 4 NH 3 H 2 O 31 9 132 374
 ОСНОВНЫЕ ОБЛАСТИ ПРАКТИЧЕСКОГО ИСПОЛЬЗОВАНИЯ СВЕРХКРИТИЧЕСКИХ СРЕД • Экстракция веществ из различных материалов, продуктов или отходов производства. • Осуществление ценных, часто новых химических превращений.
ОСНОВНЫЕ ОБЛАСТИ ПРАКТИЧЕСКОГО ИСПОЛЬЗОВАНИЯ СВЕРХКРИТИЧЕСКИХ СРЕД • Экстракция веществ из различных материалов, продуктов или отходов производства. • Осуществление ценных, часто новых химических превращений.
 Сверхкритический оксид углерода (IV) (sc. CO 2) Преимущества Ш Не токсичен, не взрывоопасен Ш Инертен (возможна обратимая реакция с нуклеофилами (амины)) Ш Летуч, отсутствие отходов Ш Высокая растворимость легких газов (H 2, O 2 и др. ) Недостатки Ш Высокое давление Ш Дорогостоящее оборудование Ш Низкая растворимость полярных веществ
Сверхкритический оксид углерода (IV) (sc. CO 2) Преимущества Ш Не токсичен, не взрывоопасен Ш Инертен (возможна обратимая реакция с нуклеофилами (амины)) Ш Летуч, отсутствие отходов Ш Высокая растворимость легких газов (H 2, O 2 и др. ) Недостатки Ш Высокое давление Ш Дорогостоящее оборудование Ш Низкая растворимость полярных веществ
 Сверхкритический оксид углерода (IV) (sc. CO 2) ШСинтез органических веществ, в том числе комплексов металлов ШГидрирование и окисление ШРадикальная полимеризация фторсодержащих мономеров ШЭкстракция, в том числе из твердых веществ
Сверхкритический оксид углерода (IV) (sc. CO 2) ШСинтез органических веществ, в том числе комплексов металлов ШГидрирование и окисление ШРадикальная полимеризация фторсодержащих мономеров ШЭкстракция, в том числе из твердых веществ
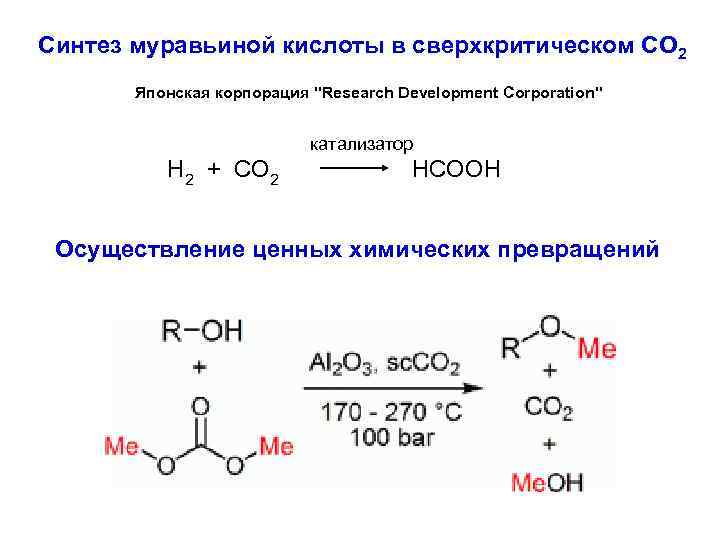 Синтез муравьиной кислоты в сверхкритическом CO 2 Японская корпорация "Research Development Corporation" Н 2 + СО 2 катализатор НСООН Осуществление ценных химических превращений
Синтез муравьиной кислоты в сверхкритическом CO 2 Японская корпорация "Research Development Corporation" Н 2 + СО 2 катализатор НСООН Осуществление ценных химических превращений
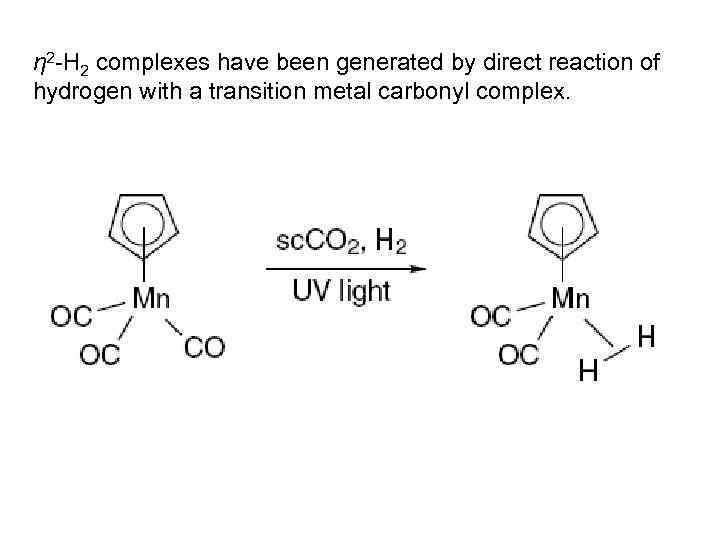 η 2 -H 2 complexes have been generated by direct reaction of hydrogen with a transition metal carbonyl complex.
η 2 -H 2 complexes have been generated by direct reaction of hydrogen with a transition metal carbonyl complex.
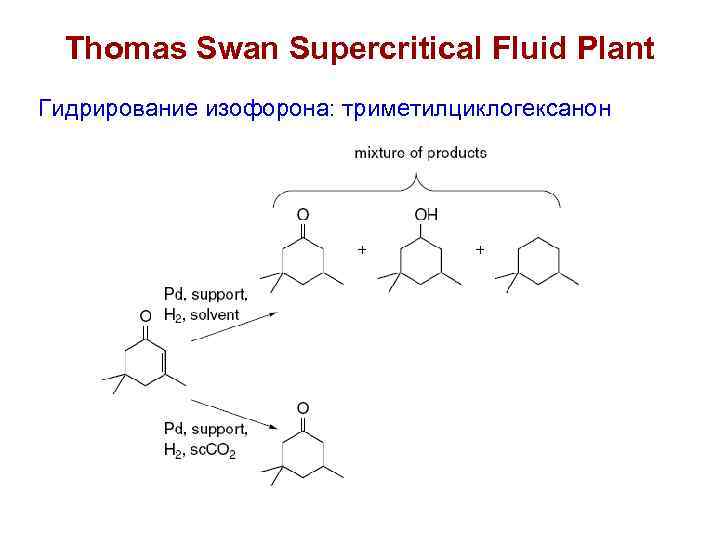 Thomas Swan Supercritical Fluid Plant Гидрирование изофорона: триметилциклогексанон
Thomas Swan Supercritical Fluid Plant Гидрирование изофорона: триметилциклогексанон
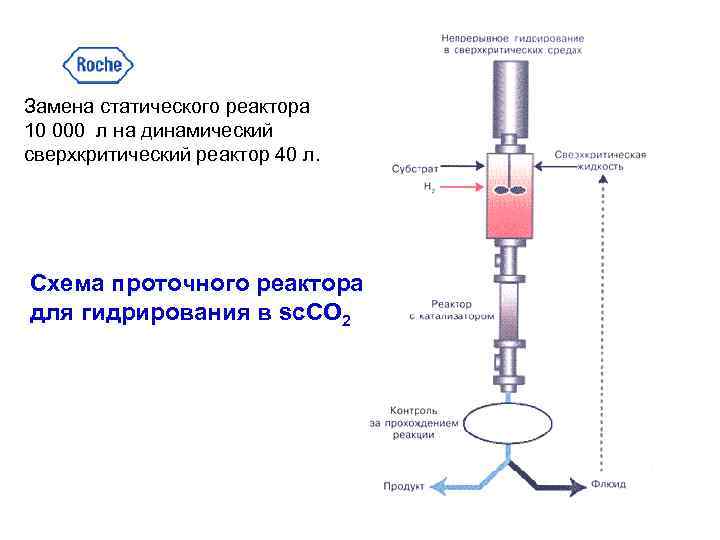 Замена статического реактора 10 000 л на динамический сверхкритический реактор 40 л. Схема проточного реактора для гидрирования в sc. CO 2
Замена статического реактора 10 000 л на динамический сверхкритический реактор 40 л. Схема проточного реактора для гидрирования в sc. CO 2
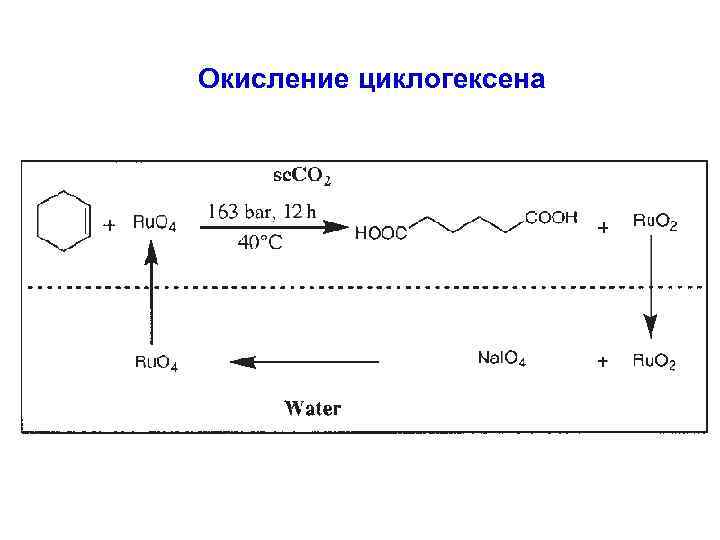 Окисление циклогексена
Окисление циклогексена
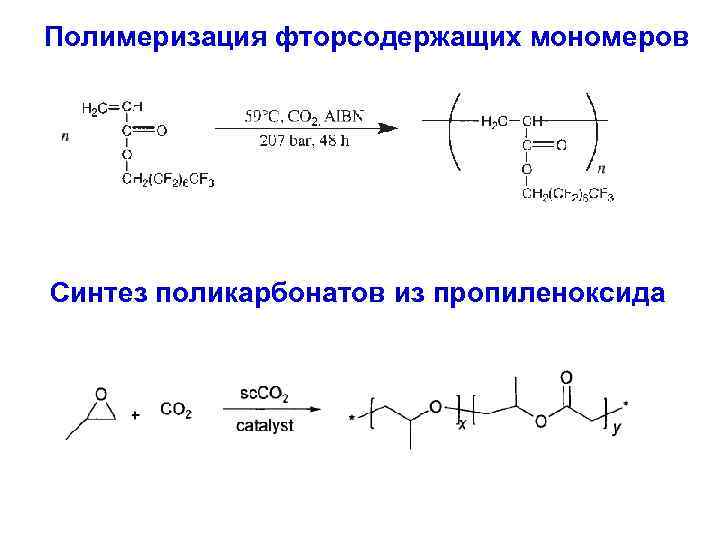 Полимеризация фторсодержащих мономеров Синтез поликарбонатов из пропиленоксида
Полимеризация фторсодержащих мономеров Синтез поликарбонатов из пропиленоксида
 Установка экстракции в СО 2
Установка экстракции в СО 2
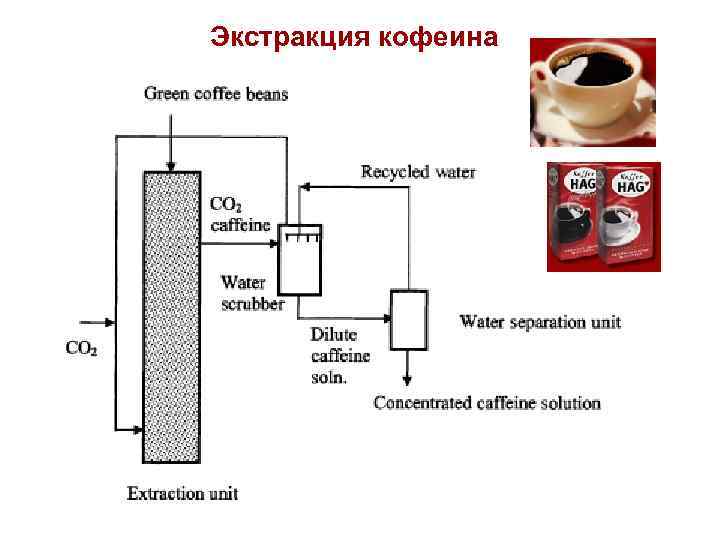 Экстракция кофеина
Экстракция кофеина
 Extraction using sc. CO 2 • Extraction of Hops for Brewing • Many other extraction processes – Spices – Essential oils and fragrances • Simple product isolation by evaporation, to 100% dryness. • No solvent residues or effluent
Extraction using sc. CO 2 • Extraction of Hops for Brewing • Many other extraction processes – Spices – Essential oils and fragrances • Simple product isolation by evaporation, to 100% dryness. • No solvent residues or effluent
 SCF Chromatography • Widely used – Gives superior resolution – Solvent power modified by pressure – Minimal evaporation required for preparative work – Easy product isolation – Negligible solvent waste
SCF Chromatography • Widely used – Gives superior resolution – Solvent power modified by pressure – Minimal evaporation required for preparative work – Easy product isolation – Negligible solvent waste
 Water as a reaction medium • One of the most obvious alternatives to VOCs. • Cheap, readily available, and plentiful • Useful for certain types of reaction but limited because of: – Low solubility of organic substrates – Compatibility with reagents • Clean up of aqueous waste difficult • Useful in biphasic processes in conjunction with other solvents
Water as a reaction medium • One of the most obvious alternatives to VOCs. • Cheap, readily available, and plentiful • Useful for certain types of reaction but limited because of: – Low solubility of organic substrates – Compatibility with reagents • Clean up of aqueous waste difficult • Useful in biphasic processes in conjunction with other solvents
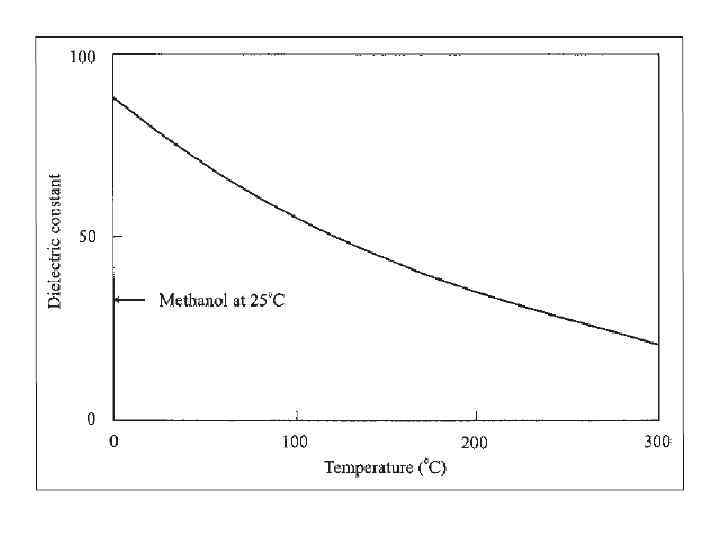
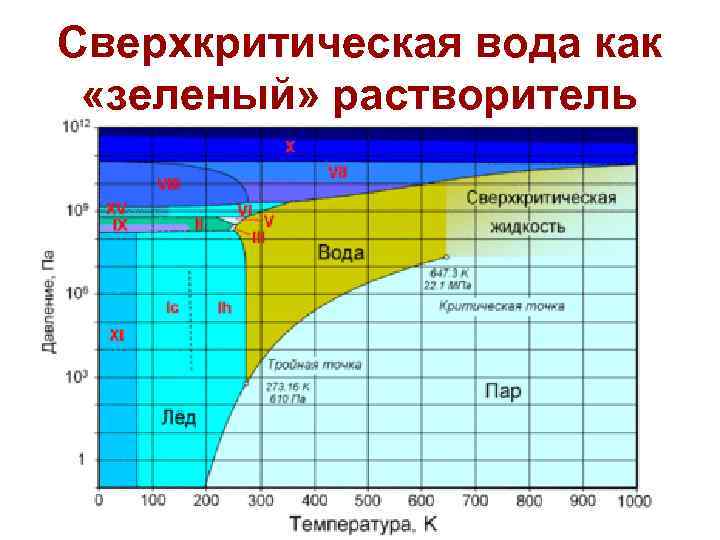 Сверхкритическая вода как «зеленый» растворитель
Сверхкритическая вода как «зеленый» растворитель
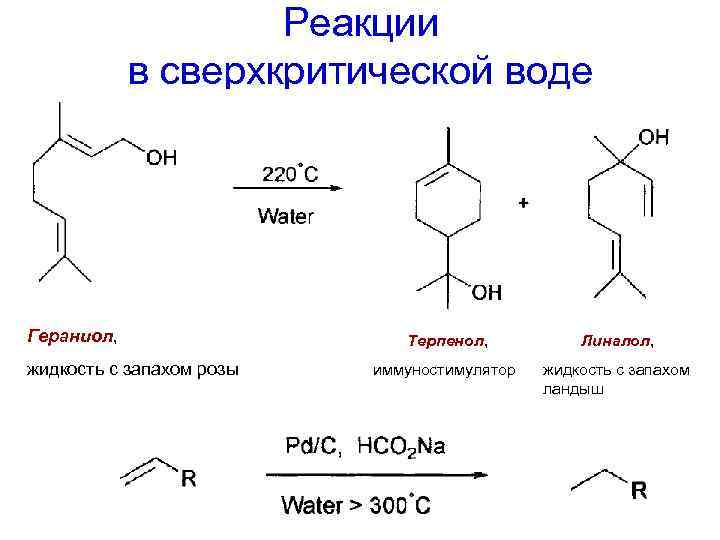 Реакции в сверхкритической воде Гераниол, жидкость с запахом розы Терпенол, иммуностимулятор Линалол, жидкость с запахом ландыш
Реакции в сверхкритической воде Гераниол, жидкость с запахом розы Терпенол, иммуностимулятор Линалол, жидкость с запахом ландыш
 Сверхкритические спирты • Конверсия триглицеридов в биодизельное топливо в сверхкритических спиртах. • Значения критических температур и критических давлений спиртов позволяет проводить реакцию в относительно мягких условиях с высокими скоростями. Обычно используется избыток спирта, продолжительность процесса 5 -40 минут. • В реакции не применяется катализатор, в результате упрощается выделение продукта.
Сверхкритические спирты • Конверсия триглицеридов в биодизельное топливо в сверхкритических спиртах. • Значения критических температур и критических давлений спиртов позволяет проводить реакцию в относительно мягких условиях с высокими скоростями. Обычно используется избыток спирта, продолжительность процесса 5 -40 минут. • В реакции не применяется катализатор, в результате упрощается выделение продукта.
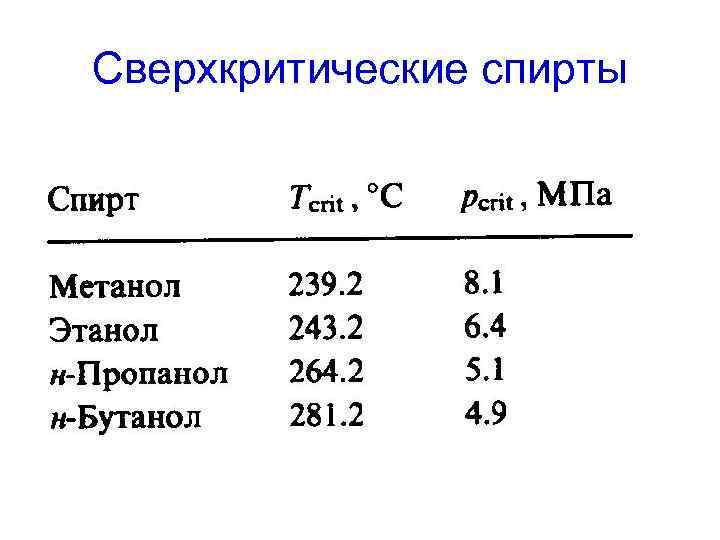 Сверхкритические спирты
Сверхкритические спирты