advanced TC.pptx
- Количество слайдов: 19
 Введение в Термохимию Химическое равновесие
Введение в Термохимию Химическое равновесие
 Меры энергии Внутренняя энергия системы (U) – сумма энергий взия молекул между собой, теплового движения, энергии взаимодействия нуклонов, движения электронов – функция состояния Теплота (Q) – энергия, передаваемая на микроскопическом уровне, в результате теплообмена Работа (W) – способ изменения энергии системы, засчет изменения внешних параметров (в основном механическая)
Меры энергии Внутренняя энергия системы (U) – сумма энергий взия молекул между собой, теплового движения, энергии взаимодействия нуклонов, движения электронов – функция состояния Теплота (Q) – энергия, передаваемая на микроскопическом уровне, в результате теплообмена Работа (W) – способ изменения энергии системы, засчет изменения внешних параметров (в основном механическая)
 Первый закон термодинамики. Энтальпия. d. U = δQ + d. Aвнешн ΔQp= ΔU+ ΔAсистемы = U 2 -U 1+p. V 2 -p. V 1 = (U 2+p. V 2) – (U 1+p. V 1) = H 2 – H 1 = ΔH Энтальпия H – энергия системы, которую она может отдать в виде тепла • В термохимии тепловой эффект Q = - ΔH • •
Первый закон термодинамики. Энтальпия. d. U = δQ + d. Aвнешн ΔQp= ΔU+ ΔAсистемы = U 2 -U 1+p. V 2 -p. V 1 = (U 2+p. V 2) – (U 1+p. V 1) = H 2 – H 1 = ΔH Энтальпия H – энергия системы, которую она может отдать в виде тепла • В термохимии тепловой эффект Q = - ΔH • •
 Такие разные энтальпии • Энтальпия реакции Δr. H (A+B=C - Δr. H) • Энтальпия образования Δf. H (A+B = C - Δf. H), A и B – простые, C – 1 моль • Энергия связи – (ABг = Aг + Вг - EAB) • Энергия ионизации (A = A+ + e- - Eion) • Сродство к электрону (A + е-= A- - Eср) • Энтальпии фазовых переходов
Такие разные энтальпии • Энтальпия реакции Δr. H (A+B=C - Δr. H) • Энтальпия образования Δf. H (A+B = C - Δf. H), A и B – простые, C – 1 моль • Энергия связи – (ABг = Aг + Вг - EAB) • Энергия ионизации (A = A+ + e- - Eion) • Сродство к электрону (A + е-= A- - Eср) • Энтальпии фазовых переходов
 Стандартизация • С. у. в ТД – давление в одну атмосферу. • Чаще всего используются значения энтальпии при 298 К (25 o. С) • У стабильных модификаций простых веществ при стандартных условиях энтальпия образования принята равной нулю(графит, красный фосфор)
Стандартизация • С. у. в ТД – давление в одну атмосферу. • Чаще всего используются значения энтальпии при 298 К (25 o. С) • У стабильных модификаций простых веществ при стандартных условиях энтальпия образования принята равной нулю(графит, красный фосфор)
 Закон Гесса • Тепловой эффект реакции зависит только от природы реагентов и продуктов, не зависит от пути её проведения(числа стадий) • C(графит)+O 2(г) = CO 2(г) – Δr. H 1 • C(графит) + 0. 5 O 2(г) = CO(г) – Δr. H 2 Δr. H 1=Δr. H 2 + Δr. H 3 • CO(г) + 0. 5 O 2(г) = CO 2(г) – Δr. H 3
Закон Гесса • Тепловой эффект реакции зависит только от природы реагентов и продуктов, не зависит от пути её проведения(числа стадий) • C(графит)+O 2(г) = CO 2(г) – Δr. H 1 • C(графит) + 0. 5 O 2(г) = CO(г) – Δr. H 2 Δr. H 1=Δr. H 2 + Δr. H 3 • CO(г) + 0. 5 O 2(г) = CO 2(г) – Δr. H 3
 Энтальпия реакции • Благодаря закону Гесса для реакции a. A+b. B = c. C + d. D Δr. H = cΔf. H(C) + dΔf. H(D) – aΔf. H(A) – bΔf. H(B)
Энтальпия реакции • Благодаря закону Гесса для реакции a. A+b. B = c. C + d. D Δr. H = cΔf. H(C) + dΔf. H(D) – aΔf. H(A) – bΔf. H(B)
 Энтропия • Энтропия (S) – мера беспорядка, хаоса системы, величина пропорциональная колву реализуемых микросостояний макросистемы (тоже функция состояния) • S=kln. W k=1. 38*10 -23 – константа Больцмана Энтропия присуща каждому веществу!(Даже простому) и всегда положительна.
Энтропия • Энтропия (S) – мера беспорядка, хаоса системы, величина пропорциональная колву реализуемых микросостояний макросистемы (тоже функция состояния) • S=kln. W k=1. 38*10 -23 – константа Больцмана Энтропия присуща каждому веществу!(Даже простому) и всегда положительна.
 Второй и третий законы • Энтропия изолированной системы не может уменьшаться. • Энтропия идеального бесконечного кристалла равна нулю (постулат Планка) • Изменение энтропии приближении к нулю также стремится к нулю
Второй и третий законы • Энтропия изолированной системы не может уменьшаться. • Энтропия идеального бесконечного кристалла равна нулю (постулат Планка) • Изменение энтропии приближении к нулю также стремится к нулю
 Расчет энтропий, энтальпий Δ
Расчет энтропий, энтальпий Δ
 Свободные энергии • Энергия Гельмгольца (F) – энергия, способная превратиться в полную работу F = U - TS • Энергия Гиббса (G) – энергия системы, способная превратится в полезную работу • G = H - TS • ΔG = ΔH – TΔS при изобарном и изотермическом процессе
Свободные энергии • Энергия Гельмгольца (F) – энергия, способная превратиться в полную работу F = U - TS • Энергия Гиббса (G) – энергия системы, способная превратится в полезную работу • G = H - TS • ΔG = ΔH – TΔS при изобарном и изотермическом процессе
 Возможность протекания реакций • Знак Δr. G 0 определяет возможность значительного протекания реакций (т. е. глубину протекания) • Δr. G 0 >0 – р-ия идет в очень слабой степени (самопроизвольно не протекает значительно) • Δr. G 0 =0 – р-ия идет как в прямом, так и в обратном направлении • Δr. G 0 <0 – р-ия идет почти нацело, до конца
Возможность протекания реакций • Знак Δr. G 0 определяет возможность значительного протекания реакций (т. е. глубину протекания) • Δr. G 0 >0 – р-ия идет в очень слабой степени (самопроизвольно не протекает значительно) • Δr. G 0 =0 – р-ия идет как в прямом, так и в обратном направлении • Δr. G 0 <0 – р-ия идет почти нацело, до конца
 Пример расчета • S(р)+O 2(г) = SO 2(г) • Δr. G 0298= ?
Пример расчета • S(р)+O 2(г) = SO 2(г) • Δr. G 0298= ?
 Равновесие • Химическое равновесие – состояние системы, при котором скорость прямой реакции равна скорости обратной. • A+B↔C+D
Равновесие • Химическое равновесие – состояние системы, при котором скорость прямой реакции равна скорости обратной. • A+B↔C+D
 Принцип Ле-Шателье • При изменении внешнего воздействия на систему, равновесие сместится в сторону той реакции, которая будет ослаблять это воздействие.
Принцип Ле-Шателье • При изменении внешнего воздействия на систему, равновесие сместится в сторону той реакции, которая будет ослаблять это воздействие.
 Константа равновесия • • m. A+n. B ↔ x. C+y. D K=(ax(C)*ay(D))/(am(A)*an(B)) Kp=(px(C)*py(D))/(pm(A)*pn(B)) – для газов Kc=(cx(C)*cy(D))/(cm(A)*cn(B)) – для растворов • 2 Hg. O(тв)=2 Hg(тв)+O 2(г) Kp=p(O 2) • Ba. SO 4(тв)=Ba 2+(р-р) + SO 42 -(р-р) Kc=c(Ba 2+)*c(SO 42 -)
Константа равновесия • • m. A+n. B ↔ x. C+y. D K=(ax(C)*ay(D))/(am(A)*an(B)) Kp=(px(C)*py(D))/(pm(A)*pn(B)) – для газов Kc=(cx(C)*cy(D))/(cm(A)*cn(B)) – для растворов • 2 Hg. O(тв)=2 Hg(тв)+O 2(г) Kp=p(O 2) • Ba. SO 4(тв)=Ba 2+(р-р) + SO 42 -(р-р) Kc=c(Ba 2+)*c(SO 42 -)
 Связь K и ΔG 0 • В равновесии ΔG 0=-RTln. Ke R=8, 314 Дж*моль-1*К-1 R=k*Na Ke=e(- ΔG 0/RT) Задача – рассчитать концентрацию ионов H+ в дистиллированной воде при 250 С. Δf. H 0298(H 2 O(ж))=-286 к. Дж/моль
Связь K и ΔG 0 • В равновесии ΔG 0=-RTln. Ke R=8, 314 Дж*моль-1*К-1 R=k*Na Ke=e(- ΔG 0/RT) Задача – рассчитать концентрацию ионов H+ в дистиллированной воде при 250 С. Δf. H 0298(H 2 O(ж))=-286 к. Дж/моль
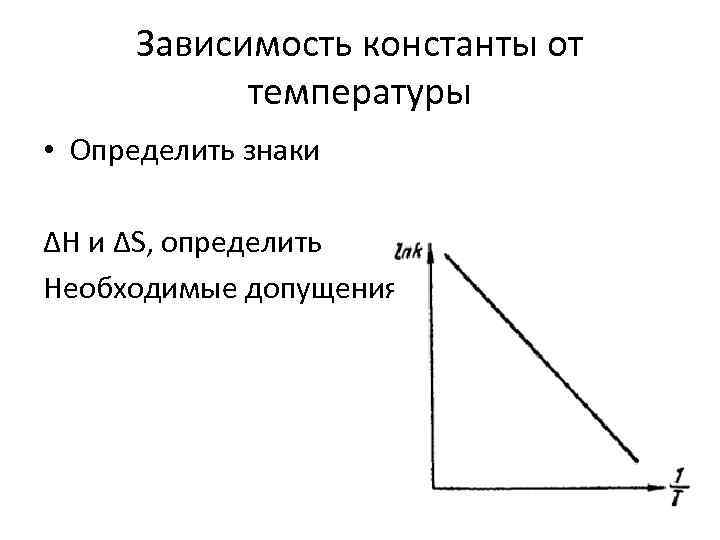 Зависимость константы от температуры • Определить знаки ΔH и ΔS, определить Необходимые допущения
Зависимость константы от температуры • Определить знаки ΔH и ΔS, определить Необходимые допущения
 Вне равновесия • ΔG = ΔG 0 + ? ? = RTlnϕ ϕ= ΔG = -RTln. Ke + RTlnϕ
Вне равновесия • ΔG = ΔG 0 + ? ? = RTlnϕ ϕ= ΔG = -RTln. Ke + RTlnϕ


