Vvedenie_v_onkologiyu_Lektsia_1.ppt
- Количество слайдов: 88
 Введение в онкологию Лекции № 1, 2
Введение в онкологию Лекции № 1, 2
 Онкология – (от греч. оncos – опухоль, logos – наука, слово) медико-биологическая наука, изучающая теоретические, экспериментальные и клинические аспекты онкогенеза у человека, животных, растений и разрабатывающая методы распознавания, лечения и профилактики опухолей. Медицинская онкология как наука сформировалась в XX в. на основе достижений экспериментальной медицины. В России представлена школой академика Н. Н. Блохина, основателя Всесоюзного онкологического научного центра АМН. Опухоли или новообразования – патологические разрастания тканей, состоящие из качественно изменившихся, утративших дифференцировку клеток организма, в условиях потери над ними иммунологического контроля.
Онкология – (от греч. оncos – опухоль, logos – наука, слово) медико-биологическая наука, изучающая теоретические, экспериментальные и клинические аспекты онкогенеза у человека, животных, растений и разрабатывающая методы распознавания, лечения и профилактики опухолей. Медицинская онкология как наука сформировалась в XX в. на основе достижений экспериментальной медицины. В России представлена школой академика Н. Н. Блохина, основателя Всесоюзного онкологического научного центра АМН. Опухоли или новообразования – патологические разрастания тканей, состоящие из качественно изменившихся, утративших дифференцировку клеток организма, в условиях потери над ними иммунологического контроля.
 Принципы организации онкологической службы в РФ Государственная система онкологической службы была создана в СССР в 1945 г. Началом ее организации явилось постановление Правительства СССР от 30. 04. 1945, которым предусматривалось создание в каждой области (республике) онкологического диспансера, в задачу которого входит лечение и учет онкологических больных. С 1953 года введен учет онкологических больных не только в онкодиспансерах, но и в лечебных учреждениях городских и районных ЛПУ благодаря созданию онкологических кабинетов. Современная структура онкологической службы в России выглядит следующим образом. Первичной организацией онкологической сети является онкологическое отделение при больнице и онкологический кабинет при поликлинике. Врач онкологического кабинета в методическом отношении подчиняется онкологическому диспансеру, а в административном – главному врачу своего лечебного учреждения.
Принципы организации онкологической службы в РФ Государственная система онкологической службы была создана в СССР в 1945 г. Началом ее организации явилось постановление Правительства СССР от 30. 04. 1945, которым предусматривалось создание в каждой области (республике) онкологического диспансера, в задачу которого входит лечение и учет онкологических больных. С 1953 года введен учет онкологических больных не только в онкодиспансерах, но и в лечебных учреждениях городских и районных ЛПУ благодаря созданию онкологических кабинетов. Современная структура онкологической службы в России выглядит следующим образом. Первичной организацией онкологической сети является онкологическое отделение при больнице и онкологический кабинет при поликлинике. Врач онкологического кабинета в методическом отношении подчиняется онкологическому диспансеру, а в административном – главному врачу своего лечебного учреждения.
 На онкологический кабинет возлагаются следующие задачи: 1. Организация учета и регистрация онкологических больных. 2. Диспансерное наблюдение за онкологическими больными, и лицами с предраковыми заболеваниями. 3. Организация профилактических осмотров. 4. Оказание квалифицированной консультативной помощи. 5. Проведение санитарно-просветительной работы. 6. Лечебная работа.
На онкологический кабинет возлагаются следующие задачи: 1. Организация учета и регистрация онкологических больных. 2. Диспансерное наблюдение за онкологическими больными, и лицами с предраковыми заболеваниями. 3. Организация профилактических осмотров. 4. Оказание квалифицированной консультативной помощи. 5. Проведение санитарно-просветительной работы. 6. Лечебная работа.
 Всех взятых под диспансерное наблюдение больных распределяют на клинические группы: группа Ia - больные с заболеванием, подозрительным на злокачественное новообразование; группа Iб - больные с предопухолевыми заболеваниями; группа II - больные злокачественными новообразованиями, подлежащие специальному лечению; группа IIа - больные злокачественными новообразованиями, подлежащие радикальному лечению; группа III - практически здоровые лица (после проведенного радикального лечения злокачественной опухоли); группа IV - больные с распространенными (запущенными) формами злокачественных новообразований, подлежащие паллиативному или симптоматическому лечению.
Всех взятых под диспансерное наблюдение больных распределяют на клинические группы: группа Ia - больные с заболеванием, подозрительным на злокачественное новообразование; группа Iб - больные с предопухолевыми заболеваниями; группа II - больные злокачественными новообразованиями, подлежащие специальному лечению; группа IIа - больные злокачественными новообразованиями, подлежащие радикальному лечению; группа III - практически здоровые лица (после проведенного радикального лечения злокачественной опухоли); группа IV - больные с распространенными (запущенными) формами злокачественных новообразований, подлежащие паллиативному или симптоматическому лечению.
 Онкологический диспансер (республиканский, краевой, областной, городской) является лечебно-профилактическим учреждением, обеспечивающим население квалифицированной и специализированной онкологической помощью, осуществляет организационно-методическое руководство лечебнопрофилактическими учреждениями по вопросам онкологии, обеспечивает специализацию и повышение квалификации врачей, среднего медицинского персонала в области диагностики и лечения больных злокачественными новообразованиями. В структуре онкологического диспансера предусмотрены следующие подразделения: стационар, поликлиника, лаборатория, организационно-методический кабинет, пансионат. В стационаре обязательно должны быть три отделения: хирургическое, гинекологическое, лучевой терапии (радиологическое). В поликлинике имеются следующие кабинеты: терапевтический, гинекологический, хирургический, урологический. Функционируют лаборатории: клиническая, биохимическая, цитологическая, бактериологическая, патогистологическая, радиоизотопная.
Онкологический диспансер (республиканский, краевой, областной, городской) является лечебно-профилактическим учреждением, обеспечивающим население квалифицированной и специализированной онкологической помощью, осуществляет организационно-методическое руководство лечебнопрофилактическими учреждениями по вопросам онкологии, обеспечивает специализацию и повышение квалификации врачей, среднего медицинского персонала в области диагностики и лечения больных злокачественными новообразованиями. В структуре онкологического диспансера предусмотрены следующие подразделения: стационар, поликлиника, лаборатория, организационно-методический кабинет, пансионат. В стационаре обязательно должны быть три отделения: хирургическое, гинекологическое, лучевой терапии (радиологическое). В поликлинике имеются следующие кабинеты: терапевтический, гинекологический, хирургический, урологический. Функционируют лаборатории: клиническая, биохимическая, цитологическая, бактериологическая, патогистологическая, радиоизотопная.
 Эпидемиология злокачественных опухолей -раздел онкологии, изучающий закономерности распространения злокачественных новообразований, а также, факторов, влияющих на их возникновение и объясняющих различия в частоте на отдельных территориях. Знание эпидемиологии рака позволяет разработать методы профилактики злокачественных новообразований. -Различают первичную и вторичную профилактику рака. Под первичной понимают меры по снижению заболеваемости ЗН. Целью вторичной профилактики является уменьшение смертности среди лиц, у которых выявлены злокачественные новообразования путем диспансеризации и своевременного лечения. Такие показатели как заболеваемость и смертность оценивают по количеству заболевших или умерших на 100 000 населения (т. н. обычный показатель заболеваемости или смертности, характеризующий фактическую частоту рака. Величина его зависит, в частности, от возрастного состава населения: чем старше возраст жителей региона, тем выше заболеваемость. У людей 60 -69 лет заболеваемость в 13 раз выше, чем у 39 -летних и в 75 раз выше, чем у лиц моложе 30 лет).
Эпидемиология злокачественных опухолей -раздел онкологии, изучающий закономерности распространения злокачественных новообразований, а также, факторов, влияющих на их возникновение и объясняющих различия в частоте на отдельных территориях. Знание эпидемиологии рака позволяет разработать методы профилактики злокачественных новообразований. -Различают первичную и вторичную профилактику рака. Под первичной понимают меры по снижению заболеваемости ЗН. Целью вторичной профилактики является уменьшение смертности среди лиц, у которых выявлены злокачественные новообразования путем диспансеризации и своевременного лечения. Такие показатели как заболеваемость и смертность оценивают по количеству заболевших или умерших на 100 000 населения (т. н. обычный показатель заболеваемости или смертности, характеризующий фактическую частоту рака. Величина его зависит, в частности, от возрастного состава населения: чем старше возраст жителей региона, тем выше заболеваемость. У людей 60 -69 лет заболеваемость в 13 раз выше, чем у 39 -летних и в 75 раз выше, чем у лиц моложе 30 лет).
 Сравнение заболеваемости в различных регионах осуществляется с помощью стандартизованных показателей, дающих возможность исключить влияние различий в возрастном составе населения.
Сравнение заболеваемости в различных регионах осуществляется с помощью стандартизованных показателей, дающих возможность исключить влияние различий в возрастном составе населения.
 1. Уровень заболеваемости характеризует частоту встречаемости рака. Более высокий в промышленно развитых городах, регионах, странах, там, где имеет место “постарение” населения. 2. Динамика заболеваемости характеризуется возрастанием или убыванием заболеваемости за промежуток времени (1 год, 5, 10 лет и т. д. ). 3. Структура заболеваемости характеризует спектр различных форм рака в популяции. Так, у мужчин наиболее частой локализацией рака являются легкие, затем с уменьшающейся частотой идут ободочная кишка, прямая кишка и предстательная железа. У женщин также чаще всего поражаются легкие, далее – молочные железы, ободочная и прямая кишка. Однако, в различных регионах, могут отмечаться расхождения в частоте встречаемости отдельных форм злокачественных новообразований. 4. Смертность от злокачественных новообразований в общей структуре смертности достаточно высока и занимает 3 место после таковой от сердечно-сосудистых заболеваний и от внешних причин (травмы, несчастные случаи). Динамика смертности от рака отдельных органов соответствует динамике заболеваемости и характеризуется неуклонным ростом во всем мире.
1. Уровень заболеваемости характеризует частоту встречаемости рака. Более высокий в промышленно развитых городах, регионах, странах, там, где имеет место “постарение” населения. 2. Динамика заболеваемости характеризуется возрастанием или убыванием заболеваемости за промежуток времени (1 год, 5, 10 лет и т. д. ). 3. Структура заболеваемости характеризует спектр различных форм рака в популяции. Так, у мужчин наиболее частой локализацией рака являются легкие, затем с уменьшающейся частотой идут ободочная кишка, прямая кишка и предстательная железа. У женщин также чаще всего поражаются легкие, далее – молочные железы, ободочная и прямая кишка. Однако, в различных регионах, могут отмечаться расхождения в частоте встречаемости отдельных форм злокачественных новообразований. 4. Смертность от злокачественных новообразований в общей структуре смертности достаточно высока и занимает 3 место после таковой от сердечно-сосудистых заболеваний и от внешних причин (травмы, несчастные случаи). Динамика смертности от рака отдельных органов соответствует динамике заболеваемости и характеризуется неуклонным ростом во всем мире.
 Этиология и патогенез опухолевых заболеваний В объяснении причин возникновения опухолей нет единой точки зрения. Считается, что большинство злокачественных опухолей является результатом воздействия факторов различной природы и их сочетаний. Такие факторы получили название канцерогенов (от cancer – рак, genu – род, происхождение).
Этиология и патогенез опухолевых заболеваний В объяснении причин возникновения опухолей нет единой точки зрения. Считается, что большинство злокачественных опухолей является результатом воздействия факторов различной природы и их сочетаний. Такие факторы получили название канцерогенов (от cancer – рак, genu – род, происхождение).
 Химические канцерогены были описаны одними из первых в качестве этиологического фактора рака. В 1775 г. английский хирург Персивал Потт (Percivall Pott) описал рак мошонки, часто встречавшийся у трубочистов. Последующие исследования, проводившиеся на протяжении ряда лет, показали, что углеводороды, выделенные из дегтя, являются канцерогенными веществами. С тех пор в качестве канцерогенов описаны многочисленные химические вещества, которые как у людей, так и у животных в эксперименте способны стимулировать появление новообразований. Т. н. ароматические амины способны вызывать опухоли мочевыводящих путей. Действие бензола ассоциируется с развитием острого лейкоза. Деготь, скипидар и креозот способны вызывать рак кожи, гортани и бронхов. Мезотелиома (злокачественная опухоль плевры) чаще встречается у лиц, подверженных асбестозу.
Химические канцерогены были описаны одними из первых в качестве этиологического фактора рака. В 1775 г. английский хирург Персивал Потт (Percivall Pott) описал рак мошонки, часто встречавшийся у трубочистов. Последующие исследования, проводившиеся на протяжении ряда лет, показали, что углеводороды, выделенные из дегтя, являются канцерогенными веществами. С тех пор в качестве канцерогенов описаны многочисленные химические вещества, которые как у людей, так и у животных в эксперименте способны стимулировать появление новообразований. Т. н. ароматические амины способны вызывать опухоли мочевыводящих путей. Действие бензола ассоциируется с развитием острого лейкоза. Деготь, скипидар и креозот способны вызывать рак кожи, гортани и бронхов. Мезотелиома (злокачественная опухоль плевры) чаще встречается у лиц, подверженных асбестозу.
 К основным физическим канцерогенным факторам относится ионизирующее излучение. У художников, расписывавших циферблаты солнечных часов красками, содержащими радий, и облизывавших кисточки, развивались злокачественные поражения костей. Рак щитовидной железы нередко связан с облучением в раннем детстве. Также, у выживших после атомной бомбардировки людей доказана более высокая, чем в популяции, частота лейкозов. Другим физическим канцерогенным фактором является ультрафиолетовое излучение. У фермеров и моряков из-за избыточного контакта с ультрафиолетовыми лучами гораздо чаще наблюдается рак кожи, как и у представителей белой расы, проживающих в тропической зоне. Механическое раздражение тканей также может рассматриваться как физический канцерогенный фактор. Результатом такого раздражения развитие меланомы при механической травме невусов.
К основным физическим канцерогенным факторам относится ионизирующее излучение. У художников, расписывавших циферблаты солнечных часов красками, содержащими радий, и облизывавших кисточки, развивались злокачественные поражения костей. Рак щитовидной железы нередко связан с облучением в раннем детстве. Также, у выживших после атомной бомбардировки людей доказана более высокая, чем в популяции, частота лейкозов. Другим физическим канцерогенным фактором является ультрафиолетовое излучение. У фермеров и моряков из-за избыточного контакта с ультрафиолетовыми лучами гораздо чаще наблюдается рак кожи, как и у представителей белой расы, проживающих в тропической зоне. Механическое раздражение тканей также может рассматриваться как физический канцерогенный фактор. Результатом такого раздражения развитие меланомы при механической травме невусов.
 Вирусы все чаще рассматривают как фактор канцерогенеза — особенно печеночноклеточного рака, Т-клеточного лимфолейкоза у взрослых, лимфомы Беркетта (Burkitt) и рака шейки матки. Изучение вирусов, вызывающих возникновение опухолей, привело к открытию онкогенов, которые, как было показано, индуцируют опухолевую трансформацию клетки. Концепция онкогенеза заключается в том, что клеточные онкогены являются нормальными генами, которые регулируют рост и дифференцировку клетки. Трансформирующие вирусы могут включаться в цепь ДНК рядом с онкогенами и вызывать молекулярные нарушения, делающие возможным патологический рост клеток, становящихся опухолевыми.
Вирусы все чаще рассматривают как фактор канцерогенеза — особенно печеночноклеточного рака, Т-клеточного лимфолейкоза у взрослых, лимфомы Беркетта (Burkitt) и рака шейки матки. Изучение вирусов, вызывающих возникновение опухолей, привело к открытию онкогенов, которые, как было показано, индуцируют опухолевую трансформацию клетки. Концепция онкогенеза заключается в том, что клеточные онкогены являются нормальными генами, которые регулируют рост и дифференцировку клетки. Трансформирующие вирусы могут включаться в цепь ДНК рядом с онкогенами и вызывать молекулярные нарушения, делающие возможным патологический рост клеток, становящихся опухолевыми.
 Наследственность играет важную роль в развитии рака. Рак толстой кишки у ряда членов одной семьи, так же как отмечающийся у кровных родственников рак молочной железы, с очевидностью указывают на роль генетических факторов в канцерогенезе. Также, было доказано доминантное наследование таких опухолей, как ретинобластома и полипоз ободочной кишки.
Наследственность играет важную роль в развитии рака. Рак толстой кишки у ряда членов одной семьи, так же как отмечающийся у кровных родственников рак молочной железы, с очевидностью указывают на роль генетических факторов в канцерогенезе. Также, было доказано доминантное наследование таких опухолей, как ретинобластома и полипоз ободочной кишки.
 Географические факторы также влияют на возникновение рака. Были найдены различия в частоте определенных типов рака в зависимости от расы и региона проживания. Так, рак желудка очень часто встречается у жителей Японии, Китая, Кореи и России, значительно реже в Северной Америке. Другими примерами различий в частоте заболеваемости раком в зависимости от географии региона являются низкая частота колоректального рака в Африке и рака предстательной и молочной желез в Японии.
Географические факторы также влияют на возникновение рака. Были найдены различия в частоте определенных типов рака в зависимости от расы и региона проживания. Так, рак желудка очень часто встречается у жителей Японии, Китая, Кореи и России, значительно реже в Северной Америке. Другими примерами различий в частоте заболеваемости раком в зависимости от географии региона являются низкая частота колоректального рака в Африке и рака предстательной и молочной желез в Японии.
 Миграция населения обычно сопровождается сдвигом структуры раковой заболеваемости в сторону, характерную для того региона, куда прибывают переселенцы. Так, японцы, переселившиеся в США, попадают в группу с низким риском развития у них рака желудка, а если они курильщики, то — с высоким риском развития рака легких.
Миграция населения обычно сопровождается сдвигом структуры раковой заболеваемости в сторону, характерную для того региона, куда прибывают переселенцы. Так, японцы, переселившиеся в США, попадают в группу с низким риском развития у них рака желудка, а если они курильщики, то — с высоким риском развития рака легких.
 К развитию рака имеют также отношение и социальноэкономические факторы. Так, частота рака желудка и шейки матки в 3 -4 раза выше у лиц с низким социально-экономическим статусом.
К развитию рака имеют также отношение и социальноэкономические факторы. Так, частота рака желудка и шейки матки в 3 -4 раза выше у лиц с низким социально-экономическим статусом.
 Вредные привычки имеют важное значение в возникновении опухолей. Так, курение – один из наиболее важных причинных факторов рака, с ним связывают около 30%(!) всех злокачественных новообразований. 70 -90% 50 -76% 20 -44% 30 -56% рака легкого и гортани; пищевода; ПЖЖ, мочевого пузыря. Люди, начавшие курить в подростковом возрасте, подвергаются значительно большему риску в среднем и пожилом, чем те, кто начал курить, будучи взрослым. Курение опасно и для пассивных курильщиков, в частности, риск рака легкого повышен у членов семьи курильщиков.
Вредные привычки имеют важное значение в возникновении опухолей. Так, курение – один из наиболее важных причинных факторов рака, с ним связывают около 30%(!) всех злокачественных новообразований. 70 -90% 50 -76% 20 -44% 30 -56% рака легкого и гортани; пищевода; ПЖЖ, мочевого пузыря. Люди, начавшие курить в подростковом возрасте, подвергаются значительно большему риску в среднем и пожилом, чем те, кто начал курить, будучи взрослым. Курение опасно и для пассивных курильщиков, в частности, риск рака легкого повышен у членов семьи курильщиков.
 Алкоголь в качестве хронического раздражителя способствует возникновению или ускорению развития рака, как растворитель жиров облегчает контакт канцерогенов с клетками. Повышает риск рака полости рта, глотки, гортани, пищевода, печени, прямой и ободочной кишки; токсическое воздействие возрастает в сочетании с курением.
Алкоголь в качестве хронического раздражителя способствует возникновению или ускорению развития рака, как растворитель жиров облегчает контакт канцерогенов с клетками. Повышает риск рака полости рта, глотки, гортани, пищевода, печени, прямой и ободочной кишки; токсическое воздействие возрастает в сочетании с курением.
 Факторы питания С характером питания прямо или косвенно связано возникновение рака органов желудочно-кишечного тракта, молочной и предстательной желез, рака легкого, яичников и тела матки. Наибольшее значение для человека имеет загрязнение пищи ПАУ (полициклическими ароматическими углеводородами) – бензпиреном, бензантраценом, нитрозаминами и их предшественниками, пестицидами и афлатоксинами. Эти канцерогены образуются в пище при кулинарной обработке жиров, при их пережаривании, перегревании, после обработки коптильным дымом мяса или рыбы, консервировании. Частое использование консервированных продуктов, копченостей и маринадов ведет к росту заболеваемости раком желудка. Такой же эффект оказывает избыток поваренной соли, недостаточное потребление фруктов и овощей, содержащих витамины А, С и Е. Недостаточное поступление с пищей клетчатки повышает риск развития рака толстой кишки. Чрезмерное употребление животных жиров способствует возникновению колоректального рака, рака ПЖЖ, рака молочной железы, тела матки.
Факторы питания С характером питания прямо или косвенно связано возникновение рака органов желудочно-кишечного тракта, молочной и предстательной желез, рака легкого, яичников и тела матки. Наибольшее значение для человека имеет загрязнение пищи ПАУ (полициклическими ароматическими углеводородами) – бензпиреном, бензантраценом, нитрозаминами и их предшественниками, пестицидами и афлатоксинами. Эти канцерогены образуются в пище при кулинарной обработке жиров, при их пережаривании, перегревании, после обработки коптильным дымом мяса или рыбы, консервировании. Частое использование консервированных продуктов, копченостей и маринадов ведет к росту заболеваемости раком желудка. Такой же эффект оказывает избыток поваренной соли, недостаточное потребление фруктов и овощей, содержащих витамины А, С и Е. Недостаточное поступление с пищей клетчатки повышает риск развития рака толстой кишки. Чрезмерное употребление животных жиров способствует возникновению колоректального рака, рака ПЖЖ, рака молочной железы, тела матки.
 Профессиональные вредности Считается, что доля профессионально обусловлен-ного рака составляет около 6% от общего числа ЗН. С профессиональными факторами связано значительное число рака мочевого пузыря (производство анилиновых красителей, резины), легкого (производство алюминия, добыча железной руды, асбеста) и т. д.
Профессиональные вредности Считается, что доля профессионально обусловлен-ного рака составляет около 6% от общего числа ЗН. С профессиональными факторами связано значительное число рака мочевого пузыря (производство анилиновых красителей, резины), легкого (производство алюминия, добыча железной руды, асбеста) и т. д.
 Стресс Имеются наблюдения о повышении частоты возникновения злокачественных опухолей при эмоциональной подавленности, неврозах, психотравмах.
Стресс Имеются наблюдения о повышении частоты возникновения злокачественных опухолей при эмоциональной подавленности, неврозах, психотравмах.
 Онкогенез - процесс превращения нормальных клеток в опухолевые (син. бластомогенез, канцерогенез). Включает ряд предопухолевых стадий и завершается опухолевой трансформацией. Механизм воздействия канцерогенов независимо от способа их проникновения связан с необратимым взаимодействием с нуклеиновыми кислотами клетки, вследствие чего возникает локальная ускоренная пролиферация незрелых клеточных элементов с наклонностью к инфильтративному росту. Такие процессы предшествуют возникновению рака и при длительном существовании сравнительно часто в него переходят, поэтому они и получили название предраковых. Нарушения структуры ткани, при которых микроскопически наблюдается патологическая пролиферация и структурный атипизм клеток, называют дисплазиями. Различают 3 степени дисплазии - легкую, умеренную и тяжелую, причем, чем более выражен атипизм клеток, тем выше степень дисплазии.
Онкогенез - процесс превращения нормальных клеток в опухолевые (син. бластомогенез, канцерогенез). Включает ряд предопухолевых стадий и завершается опухолевой трансформацией. Механизм воздействия канцерогенов независимо от способа их проникновения связан с необратимым взаимодействием с нуклеиновыми кислотами клетки, вследствие чего возникает локальная ускоренная пролиферация незрелых клеточных элементов с наклонностью к инфильтративному росту. Такие процессы предшествуют возникновению рака и при длительном существовании сравнительно часто в него переходят, поэтому они и получили название предраковых. Нарушения структуры ткани, при которых микроскопически наблюдается патологическая пролиферация и структурный атипизм клеток, называют дисплазиями. Различают 3 степени дисплазии - легкую, умеренную и тяжелую, причем, чем более выражен атипизм клеток, тем выше степень дисплазии.
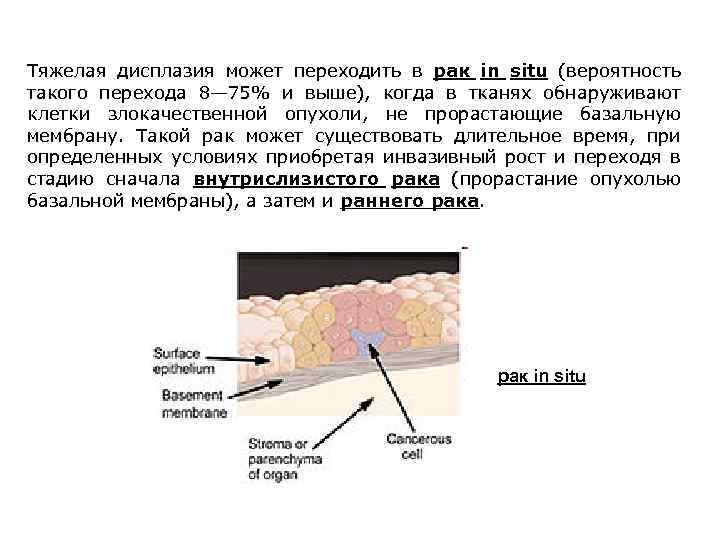 Тяжелая дисплазия может переходить в рак in situ (вероятность такого перехода 8— 75% и выше), когда в тканях обнаруживают клетки злокачественной опухоли, не прорастающие базальную мембрану. Такой рак может существовать длительное время, при определенных условиях приобретая инвазивный рост и переходя в стадию сначала внутрислизистого рака (прорастание опухолью базальной мембраны), а затем и раннего рака. рак in situ
Тяжелая дисплазия может переходить в рак in situ (вероятность такого перехода 8— 75% и выше), когда в тканях обнаруживают клетки злокачественной опухоли, не прорастающие базальную мембрану. Такой рак может существовать длительное время, при определенных условиях приобретая инвазивный рост и переходя в стадию сначала внутрислизистого рака (прорастание опухолью базальной мембраны), а затем и раннего рака. рак in situ
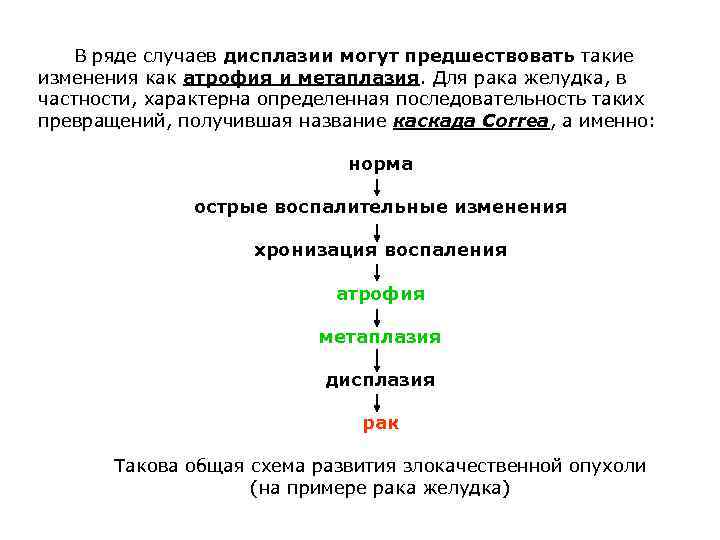 В ряде случаев дисплазии могут предшествовать такие изменения как атрофия и метаплазия. Для рака желудка, в частности, характерна определенная последовательность таких превращений, получившая название каскада Correa, а именно: норма острые воспалительные изменения хронизация воспаления атрофия метаплазия дисплазия рак Такова общая схема развития злокачественной опухоли (на примере рака желудка)
В ряде случаев дисплазии могут предшествовать такие изменения как атрофия и метаплазия. Для рака желудка, в частности, характерна определенная последовательность таких превращений, получившая название каскада Correa, а именно: норма острые воспалительные изменения хронизация воспаления атрофия метаплазия дисплазия рак Такова общая схема развития злокачественной опухоли (на примере рака желудка)
 Атрофия (от греч. atropheo) — голодаю, чахну), прижизненное уменьшение размеров органа или ткани организма животных и человека, сопровождающееся нарушением или прекращением функции. Применимо к слизистым оболочкам атрофия означает их истончение вследствие резкого уменьшения размеров клеток. Метаплазия (от греч. μετα- — приставка, обозначающая изменение и πλάσις — «образование, формирование» ) — стойкое замещение дифференцированных клеток одного типа дифференцированными клетками другого типа при сохранении основной видовой принадлежности ткани. Подругому можно определить ее как переход одного вида ткани в другой, родственный ей. Метаплазия чаще встречается в эпителии и соединительной ткани, реже - в других тканях.
Атрофия (от греч. atropheo) — голодаю, чахну), прижизненное уменьшение размеров органа или ткани организма животных и человека, сопровождающееся нарушением или прекращением функции. Применимо к слизистым оболочкам атрофия означает их истончение вследствие резкого уменьшения размеров клеток. Метаплазия (от греч. μετα- — приставка, обозначающая изменение и πλάσις — «образование, формирование» ) — стойкое замещение дифференцированных клеток одного типа дифференцированными клетками другого типа при сохранении основной видовой принадлежности ткани. Подругому можно определить ее как переход одного вида ткани в другой, родственный ей. Метаплазия чаще встречается в эпителии и соединительной ткани, реже - в других тканях.
 В зависимости от вероятности развития рака предраковые процессы делят на облигатные и факультативные. Облигатным предраком являются состояния, на фоне которых практически всегда возникает злокачественная опухоль (пример – ворсинчатые опухоли толстой кишки), факультативным – заболевания, при которых рак развивается относительно редко, но чаще, чем у здоровых лиц (пример - старческий гиперкератоз).
В зависимости от вероятности развития рака предраковые процессы делят на облигатные и факультативные. Облигатным предраком являются состояния, на фоне которых практически всегда возникает злокачественная опухоль (пример – ворсинчатые опухоли толстой кишки), факультативным – заболевания, при которых рак развивается относительно редко, но чаще, чем у здоровых лиц (пример - старческий гиперкератоз).
 Течение рака Раковые клетки в целом размножаются быстрее, чем нормальные клетки (исключая лейкоциты и клетки слизистой оболочки кишечника). По мере увеличения объема опухоли скорость размножения клеток снижается. Большинство опухолей существует в человеческом организме до момента их обнаружения клиническими методами от 1 года до 10 лет. Различают доклинический и клинический периоды опухолевого роста.
Течение рака Раковые клетки в целом размножаются быстрее, чем нормальные клетки (исключая лейкоциты и клетки слизистой оболочки кишечника). По мере увеличения объема опухоли скорость размножения клеток снижается. Большинство опухолей существует в человеческом организме до момента их обнаружения клиническими методами от 1 года до 10 лет. Различают доклинический и клинический периоды опухолевого роста.
 Под доклиническим периодом понимают длительный этап бессимптомного течения новообразования, когда опухоль может быть случайно обнаружена при проведении, например, профосмотра. На этот период приходится около ¾ общей продолжительности существования опухоли, ему соответствуют, как правило, 1 -я и 2 -я стадия ЗН.
Под доклиническим периодом понимают длительный этап бессимптомного течения новообразования, когда опухоль может быть случайно обнаружена при проведении, например, профосмотра. На этот период приходится около ¾ общей продолжительности существования опухоли, ему соответствуют, как правило, 1 -я и 2 -я стадия ЗН.
 Термин “ранний рак” впервые был предложен в 1956 г. R. Hess и характеризовал опухоль, не выходящую за пределы подслизистого слоя вне зависимости от поражения периорганных лимфоузлов. Распознавание опухоли на стадии раннего рака представляет собой очень важный момент, поскольку существенно влияет на прогноз. Так, например, 5 -летняя выживаемость после операций на желудке по поводу раннего рака составляет 70 -90%, в то время как на стадии прогрессии она опускается ниже 10% (!)
Термин “ранний рак” впервые был предложен в 1956 г. R. Hess и характеризовал опухоль, не выходящую за пределы подслизистого слоя вне зависимости от поражения периорганных лимфоузлов. Распознавание опухоли на стадии раннего рака представляет собой очень важный момент, поскольку существенно влияет на прогноз. Так, например, 5 -летняя выживаемость после операций на желудке по поводу раннего рака составляет 70 -90%, в то время как на стадии прогрессии она опускается ниже 10% (!)
 Клинический период характеризует стадию прогрессии злокачественного новообразования, когда возникает разнообразная симптоматика, что соответствует запущенным (3 -4) стадиям рака. Клиническая картина может быть специфичной или неспецифичной и проявляет себя определенными синдромами:
Клинический период характеризует стадию прогрессии злокачественного новообразования, когда возникает разнообразная симптоматика, что соответствует запущенным (3 -4) стадиям рака. Клиническая картина может быть специфичной или неспецифичной и проявляет себя определенными синдромами:
 1. Синдром обтурации. Наблюдается при опухолях большинства полых (трубчатых) или трубчатых структур некоторых паренхиматозных органов. Обусловлен постепенным сужением (либо сдавлением) просвета органа растущей опухолью. В различных органах феномен проявляется неодинаково.
1. Синдром обтурации. Наблюдается при опухолях большинства полых (трубчатых) или трубчатых структур некоторых паренхиматозных органов. Обусловлен постепенным сужением (либо сдавлением) просвета органа растущей опухолью. В различных органах феномен проявляется неодинаково.
 2. Синдром деструкции. Обусловлен распадом опухоли самопроизвольно, либо под воздействием механических факторов. Проявляется кровотечением, которое м. б. незначительным и не обнаруживаться визуально (оккультное кровотечение). Длительность может быть различной. При аррозии опухолью крупного сосуда может быть профузное кровотечение. При наличии даже однократных кровянистых выделений необходимо заподозрить ЗН и тщательно исследовать соответствующий орган!
2. Синдром деструкции. Обусловлен распадом опухоли самопроизвольно, либо под воздействием механических факторов. Проявляется кровотечением, которое м. б. незначительным и не обнаруживаться визуально (оккультное кровотечение). Длительность может быть различной. При аррозии опухолью крупного сосуда может быть профузное кровотечение. При наличии даже однократных кровянистых выделений необходимо заподозрить ЗН и тщательно исследовать соответствующий орган!
 3. Синдром компрессии. Проявляется таким симптомом как боль, возникающим вследствие увеличения размеров опухоли и прорастанием либо сдавлением нервных окончаний, стволов или сплетений. Развивается постепенно, усиливаясь с течением времени и приобретая постоянный характер, иногда становясь очень острой, а в поздних стадиях нестерпимой. Ведущий с-м при раке ПЖЖ, тела желудка, печени, опухолях почек, саркомах кости, реже – при раке легкого, пищевода и наружных органов.
3. Синдром компрессии. Проявляется таким симптомом как боль, возникающим вследствие увеличения размеров опухоли и прорастанием либо сдавлением нервных окончаний, стволов или сплетений. Развивается постепенно, усиливаясь с течением времени и приобретая постоянный характер, иногда становясь очень острой, а в поздних стадиях нестерпимой. Ведущий с-м при раке ПЖЖ, тела желудка, печени, опухолях почек, саркомах кости, реже – при раке легкого, пищевода и наружных органов.
 4. Интоксикационный синдром. Рост опухоли ведет к нарушению всех видов обмена, вызывая существенные сдвиги. Наиболее типичными симптомами являются общая слабость, похудание, снижение аппетита и нередко служат основанием для обращения к врачу. Данный синдром характерен для далеко зашедших стадий рака и наиболее выражен при раке желудка, ПЖЖ, печени. Практически может отсутствовать при опухолях матки, кожи и молочной железы.
4. Интоксикационный синдром. Рост опухоли ведет к нарушению всех видов обмена, вызывая существенные сдвиги. Наиболее типичными симптомами являются общая слабость, похудание, снижение аппетита и нередко служат основанием для обращения к врачу. Данный синдром характерен для далеко зашедших стадий рака и наиболее выражен при раке желудка, ПЖЖ, печени. Практически может отсутствовать при опухолях матки, кожи и молочной железы.
 5. Синдром “плюс-ткани”. Является наиболее достоверным признаком опухоли, выявляемым клинически либо с помощью инструментальных методов. Характерны такие признаки, как бугристость, безболезненность, плотная консистенция, смещаемость вместе с окружающими тканями (при прорастании опухолью глубоких тканевых структур, подвижность ее теряется).
5. Синдром “плюс-ткани”. Является наиболее достоверным признаком опухоли, выявляемым клинически либо с помощью инструментальных методов. Характерны такие признаки, как бугристость, безболезненность, плотная консистенция, смещаемость вместе с окружающими тканями (при прорастании опухолью глубоких тканевых структур, подвижность ее теряется).
 6. Синдром патологических выделений. Характерен для рака прямой кишки, матки, иногда – молочной железы, кожи. Отделяемое м. б. кровянистым, сукровичным, иметь примеси слизи или гноя.
6. Синдром патологических выделений. Характерен для рака прямой кишки, матки, иногда – молочной железы, кожи. Отделяемое м. б. кровянистым, сукровичным, иметь примеси слизи или гноя.
 7. Синдром нарушения специфических функций органа. Наиболее ярко выражен при опухолях эндокринной системы. При опухолях инсулярного аппарата ПЖЖ – гипо-(гипер)гликемия и нервные расстройства, при опухолях яичника – признаки вирилизации, при опухолях гипофиза – ожирение, признаки акромегалии и т. д.
7. Синдром нарушения специфических функций органа. Наиболее ярко выражен при опухолях эндокринной системы. При опухолях инсулярного аппарата ПЖЖ – гипо-(гипер)гликемия и нервные расстройства, при опухолях яичника – признаки вирилизации, при опухолях гипофиза – ожирение, признаки акромегалии и т. д.
 1. Паранеопластические синдромы. Клинические проявления, которые нельзя объяснить прямым влиянием опухоли или ее метастазов. При опухолях внутренних органов - тромбофлебиты, разнообразные кожные проявления, нарушения функции ССС, эндокринной, нервной систем и т. д. Обусловлены биохимическими сдвигами или результатами аутоиммунных реакций
1. Паранеопластические синдромы. Клинические проявления, которые нельзя объяснить прямым влиянием опухоли или ее метастазов. При опухолях внутренних органов - тромбофлебиты, разнообразные кожные проявления, нарушения функции ССС, эндокринной, нервной систем и т. д. Обусловлены биохимическими сдвигами или результатами аутоиммунных реакций
 С клинической и морфологической точек зрения принято различать доброкачественные и злокачественные новобразования (опухоли). Доброкачественные опухоли характеризуются: • медленным (годы) ростом; • экспансией (оттеснением) тканей; • наличием внешней капсулы, позволяющей отграничить опухоль от здоровой ткани; • отсутствуем метастазов. Злокачественные опухоли характеризуются: • быстрым (недели, месяцы) ростом; • инвазией (прорастанием) в окружающие ткани; • отсутствием внешней капсулы; • метастазированием
С клинической и морфологической точек зрения принято различать доброкачественные и злокачественные новобразования (опухоли). Доброкачественные опухоли характеризуются: • медленным (годы) ростом; • экспансией (оттеснением) тканей; • наличием внешней капсулы, позволяющей отграничить опухоль от здоровой ткани; • отсутствуем метастазов. Злокачественные опухоли характеризуются: • быстрым (недели, месяцы) ростом; • инвазией (прорастанием) в окружающие ткани; • отсутствием внешней капсулы; • метастазированием
 Классификация опухолей по гистологическому варианту включает следующие группы (упрощенный вариант): Эпителиальные опухоли 1. Доброкачественные или зрелые: • • Из железистого эпителия – аденома, фиброаденома, цистаденома Из покровного эпителия – папиллома 2. Злокачественные или незрелые (синоним – раки) • • Из железистого эпителия – аденокарцинома, слизистый (коллоидный) рак, солидный рак Из покровного эпителия – плоскоклеточный (ороговевающий или неороговевающий), базальноклеточный, переходноклеточный, недифференцированный (мелкоклеточный, полиморфноклеточный) Неэпителиальные опухоли (мезенхимального и нейроэктодермального происхождения) – зрелые и незрелые Опухоли из фиброзной ткани Опухоли из жировой ткани Опухоли из мышечной ткани Опухоли из кровеносных и лимфатических сосудов Опухоли синовиальных оболочек Опухоли мезотелиальной ткани Опухоли периферических нервов Опухоли симпатических ганглиев Тератомы Опухоли ЦНС: нейроэктодермальные и опухоли мозговых оболочек Опухоли APUD-системы (карциноиды)
Классификация опухолей по гистологическому варианту включает следующие группы (упрощенный вариант): Эпителиальные опухоли 1. Доброкачественные или зрелые: • • Из железистого эпителия – аденома, фиброаденома, цистаденома Из покровного эпителия – папиллома 2. Злокачественные или незрелые (синоним – раки) • • Из железистого эпителия – аденокарцинома, слизистый (коллоидный) рак, солидный рак Из покровного эпителия – плоскоклеточный (ороговевающий или неороговевающий), базальноклеточный, переходноклеточный, недифференцированный (мелкоклеточный, полиморфноклеточный) Неэпителиальные опухоли (мезенхимального и нейроэктодермального происхождения) – зрелые и незрелые Опухоли из фиброзной ткани Опухоли из жировой ткани Опухоли из мышечной ткани Опухоли из кровеносных и лимфатических сосудов Опухоли синовиальных оболочек Опухоли мезотелиальной ткани Опухоли периферических нервов Опухоли симпатических ганглиев Тератомы Опухоли ЦНС: нейроэктодермальные и опухоли мозговых оболочек Опухоли APUD-системы (карциноиды)
 Дополнительная классификация раков основана на соотношении паренхиматозного и стромального компонентов опухоли, в связи с чем различают: • медуллярный (мозговидный) рак, который характеризуется преобладанием паренхимы над стромой. Опухоль мягкая, напоминает ткань головного мозга; • простой, или вульгарный рак, который содержит примерно равное количество паренхимы и стромы; • скирр, или фиброзный рак, который отличается явным преобладанием стромы над паренхимой.
Дополнительная классификация раков основана на соотношении паренхиматозного и стромального компонентов опухоли, в связи с чем различают: • медуллярный (мозговидный) рак, который характеризуется преобладанием паренхимы над стромой. Опухоль мягкая, напоминает ткань головного мозга; • простой, или вульгарный рак, который содержит примерно равное количество паренхимы и стромы; • скирр, или фиброзный рак, который отличается явным преобладанием стромы над паренхимой.
 Метастаз (metha – перемещение, stasis – остановка) – группа клеток злокачественной опухоли, перенесенная в ткань здорового органа с током крови или лимфы и инициирующая в нем опухолевый рост. Соответственно, метастазирование может осуществляться лимфогенным и гематогенным путями. Характер метастазирования определяется рядом факторов – кровоснабжением и функцией органа, типом лимфо- и кровотока. Так, для гипернефромы характерно гематогенное метастазирование, для желудка – преимущественно лимфогенный тип метастазирования, в печень метастазирует большинство опухолей ЖКТ. Различают еще т. н. имплантационные метастазы, когда клетки ЗН могут внедряться в здоровую ткань при непосредственном контакте с ней.
Метастаз (metha – перемещение, stasis – остановка) – группа клеток злокачественной опухоли, перенесенная в ткань здорового органа с током крови или лимфы и инициирующая в нем опухолевый рост. Соответственно, метастазирование может осуществляться лимфогенным и гематогенным путями. Характер метастазирования определяется рядом факторов – кровоснабжением и функцией органа, типом лимфо- и кровотока. Так, для гипернефромы характерно гематогенное метастазирование, для желудка – преимущественно лимфогенный тип метастазирования, в печень метастазирует большинство опухолей ЖКТ. Различают еще т. н. имплантационные метастазы, когда клетки ЗН могут внедряться в здоровую ткань при непосредственном контакте с ней.
 Отдельную группу представляют т. н. карциноиды. Термин дословно означает “подобный раку” и был предложен 100 лет назад Oberndorfer с целью противопоставить аденокарциноме аналогичную по морфологическому строению, но доброкачественную по клиническому течению опухоль. Однако, сейчас установлены характерные различия между аденокарциномой и карциноидом, относящимся к нейроэндокринным опухолям, происходящим из клеток APUDсистемы. Частота встречаемости их крайне редка (0, 1 – 0, 5% по отношению ко всем опухолям человека). Чаще поражают легкие, реже – ЖКТ. Различают 3 типа, 2 и 3 типы часто дают метастазы, 1 практически не метастазирует. Карциноидный синдром чаще развивается при поражении легких и проявляется перепадами АД, тахикардией, бронхоспазмом, приливами жара, диареей и связан с выбросом в кровь гормонов и медиаторов, выделяемых опухолью. В настоящее время карциноидные опухоли отнесены к ЗН.
Отдельную группу представляют т. н. карциноиды. Термин дословно означает “подобный раку” и был предложен 100 лет назад Oberndorfer с целью противопоставить аденокарциноме аналогичную по морфологическому строению, но доброкачественную по клиническому течению опухоль. Однако, сейчас установлены характерные различия между аденокарциномой и карциноидом, относящимся к нейроэндокринным опухолям, происходящим из клеток APUDсистемы. Частота встречаемости их крайне редка (0, 1 – 0, 5% по отношению ко всем опухолям человека). Чаще поражают легкие, реже – ЖКТ. Различают 3 типа, 2 и 3 типы часто дают метастазы, 1 практически не метастазирует. Карциноидный синдром чаще развивается при поражении легких и проявляется перепадами АД, тахикардией, бронхоспазмом, приливами жара, диареей и связан с выбросом в кровь гормонов и медиаторов, выделяемых опухолью. В настоящее время карциноидные опухоли отнесены к ЗН.
 Внешний вид опухоли зависит от характера ее роста. Различают экзофитный и эндофитный рост опухоли. В случаях, когда новообразование имеет вид узла, выступающего в просвет полого органа, либо распространяющегося в толщу паренхиматозного, формируя в нем объемную структуру, такая опухоль называется экзофитной. В других случаях, когда раковые клетки распространяются преимущественно по стенке органа (например, вдоль бронхов, в подслизистом слое органа), при этом стенка или сам орган становятся толще и плотнее, а границы опухоли четко не определяются, характер роста называют инфильтративным, а опухоль – эндофитной. Инфильтративный (эндофитный) рак протекает более злокачественно, отличается ускоренным течением, ранним и бурным метастазированием, худшим прогнозом. Независимо от формы роста, раковая опухоль имеет склонность к распаду и изъязвлениям, что обусловлено недостаточным кровоснабжением центральных отделов новообразования и незрелостью (неполноценностью) покровного эпителия, который легко повреждается.
Внешний вид опухоли зависит от характера ее роста. Различают экзофитный и эндофитный рост опухоли. В случаях, когда новообразование имеет вид узла, выступающего в просвет полого органа, либо распространяющегося в толщу паренхиматозного, формируя в нем объемную структуру, такая опухоль называется экзофитной. В других случаях, когда раковые клетки распространяются преимущественно по стенке органа (например, вдоль бронхов, в подслизистом слое органа), при этом стенка или сам орган становятся толще и плотнее, а границы опухоли четко не определяются, характер роста называют инфильтративным, а опухоль – эндофитной. Инфильтративный (эндофитный) рак протекает более злокачественно, отличается ускоренным течением, ранним и бурным метастазированием, худшим прогнозом. Независимо от формы роста, раковая опухоль имеет склонность к распаду и изъязвлениям, что обусловлено недостаточным кровоснабжением центральных отделов новообразования и незрелостью (неполноценностью) покровного эпителия, который легко повреждается.
 Степень злокачественности (“агрессивности”) опухоли и, как следствие, интенсивность метастазирования определяется гистологической структурой ЗН. Гистологически различают: • высокодифференцированные • умереннодифференцированные • низкодифференцированные (недифференцированные) опухоли. Чем ниже степень дифференциации клеток, тем злокачественней опухоль. К недифференцированным относят, например, перстневидноклеточный рак желудка, мелкоклеточный рак легкого
Степень злокачественности (“агрессивности”) опухоли и, как следствие, интенсивность метастазирования определяется гистологической структурой ЗН. Гистологически различают: • высокодифференцированные • умереннодифференцированные • низкодифференцированные (недифференцированные) опухоли. Чем ниже степень дифференциации клеток, тем злокачественней опухоль. К недифференцированным относят, например, перстневидноклеточный рак желудка, мелкоклеточный рак легкого
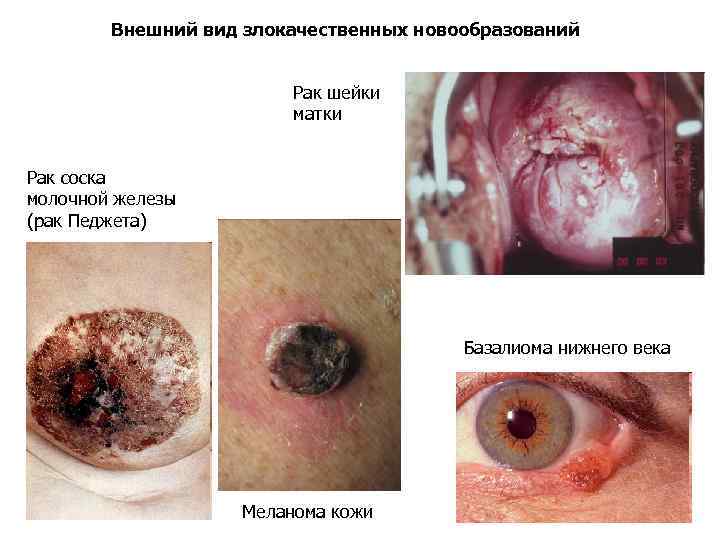 Внешний вид злокачественных новообразований Рак шейки матки Рак соска молочной железы (рак Педжета) Базалиома нижнего века Меланома кожи
Внешний вид злокачественных новообразований Рак шейки матки Рак соска молочной железы (рак Педжета) Базалиома нижнего века Меланома кожи
 Классификация ЗН по стадиям В зависимости от размеров, степени прорастания в окружающие ткани органов, метастазирования в лимфатические узлы и отдаленные органы в развитии злокачественных опухолей принято различать 4 стадии (классификация РОНЦ). 1. Опухоль до 2 см, ограничена одним или двумя слоями стенки органа без метастазов в регионарные лимфоузлы; 2. Опухоль от 2 до 5 см, без или с одиночными mts в регионарные лимфоузлы; 3. Опухоль прорастает все слои органа, а иногда в окружающие ткани, значительных размеров или опухоль с множественными mts в регионарные лимфоузлы; 4. Опухоль больших размеров, прорастающая на значительном протяжении в окружающие орган ткани, неподвижная, не удалимая хирургическим путем или опухоль любых размеров с отдаленными mts.
Классификация ЗН по стадиям В зависимости от размеров, степени прорастания в окружающие ткани органов, метастазирования в лимфатические узлы и отдаленные органы в развитии злокачественных опухолей принято различать 4 стадии (классификация РОНЦ). 1. Опухоль до 2 см, ограничена одним или двумя слоями стенки органа без метастазов в регионарные лимфоузлы; 2. Опухоль от 2 до 5 см, без или с одиночными mts в регионарные лимфоузлы; 3. Опухоль прорастает все слои органа, а иногда в окружающие ткани, значительных размеров или опухоль с множественными mts в регионарные лимфоузлы; 4. Опухоль больших размеров, прорастающая на значительном протяжении в окружающие орган ткани, неподвижная, не удалимая хирургическим путем или опухоль любых размеров с отдаленными mts.
 Международным противораковым союзом (IARC) в 1987 г. разработана унифицированная классификация злокачественных новообразований различных органов по т. н. системе TNM (Tumor-Nodus-Metastasis) (на примере рака толстой кишки) T – характеризует первичную опухоль. Tx – недостаточно данных для оценки T 0 – нет данных о наличии первичной опухоли Tis – carcinoma in situ T 1 – прорастает подслизистую оболочку T 2 – прорастает мышечную оболочку T 3 – прорастает субсерозную/адвентициальную оболочку T 4 – переходит на другие органы и структуры N – характеризует вовлечение в процесс регионарных лимфоузлов Nx – недостаточно данных для оценки N 0 – нет mts в регионарные лимфоузлы N 1 – 1 -3 mts в регионарные лимфоузлы N 2 – 4 или более mts в региональные узлы N 3 – mts в лимфоузлы крупных сосудистых стволов M – характеризует отдаленные метастазы Mx – недостаточно данных для оценки M 0 – отсутствуют M 1 – имеются
Международным противораковым союзом (IARC) в 1987 г. разработана унифицированная классификация злокачественных новообразований различных органов по т. н. системе TNM (Tumor-Nodus-Metastasis) (на примере рака толстой кишки) T – характеризует первичную опухоль. Tx – недостаточно данных для оценки T 0 – нет данных о наличии первичной опухоли Tis – carcinoma in situ T 1 – прорастает подслизистую оболочку T 2 – прорастает мышечную оболочку T 3 – прорастает субсерозную/адвентициальную оболочку T 4 – переходит на другие органы и структуры N – характеризует вовлечение в процесс регионарных лимфоузлов Nx – недостаточно данных для оценки N 0 – нет mts в регионарные лимфоузлы N 1 – 1 -3 mts в регионарные лимфоузлы N 2 – 4 или более mts в региональные узлы N 3 – mts в лимфоузлы крупных сосудистых стволов M – характеризует отдаленные метастазы Mx – недостаточно данных для оценки M 0 – отсутствуют M 1 – имеются
 Принципы диагностики злокачественных опухолей Своевременное распознавание ЗН является чрезвычайно сложной задачей и возможно только при наличии у врача постоянной онкологической настороженности. Немаловажное значение придается также современной технической оснащенности ЛПУ. Основной проблемой является позднее обращение больных, когда опухоль имеет, как правило, запущенную стадию.
Принципы диагностики злокачественных опухолей Своевременное распознавание ЗН является чрезвычайно сложной задачей и возможно только при наличии у врача постоянной онкологической настороженности. Немаловажное значение придается также современной технической оснащенности ЛПУ. Основной проблемой является позднее обращение больных, когда опухоль имеет, как правило, запущенную стадию.
 Процесс установления диагноза ЗН состоит из 4 этапов 1. Сбор и критическая оценка жалоб. Следует активно расспросить больного о наличии симптомов, поскольку они часто акцентируют внимание на одном-двух наиболее тревожащих их, упуская другие, менее выраженные, но, порой, весьма существенные для диагностики. 2. Выяснение динамики развития заболевания и условий, способствовавших его возникновению. Появление новых признаков, усиление прежних жалоб говорит о прогрессировании процесса.
Процесс установления диагноза ЗН состоит из 4 этапов 1. Сбор и критическая оценка жалоб. Следует активно расспросить больного о наличии симптомов, поскольку они часто акцентируют внимание на одном-двух наиболее тревожащих их, упуская другие, менее выраженные, но, порой, весьма существенные для диагностики. 2. Выяснение динамики развития заболевания и условий, способствовавших его возникновению. Появление новых признаков, усиление прежних жалоб говорит о прогрессировании процесса.
 3. Физикальное исследование больного, включающее осмотр и пальпацию пораженного органа и зон метастазирования. Не прибегая к специальным методам обследования можно осмотреть только опухоли наружных органов (кожи, губы, мягких тканей, полости рта и др. ). Рак молочной железы, лимогранулематоз, новообразования мягких тканей и костей обнаруживают при пальпации. ЗН выглядят плотными, неровными, мало и ли совершенно безболезненные, в той или иной мере фиксированы к окружающим тканям. Обязательным элементом объективного исследования онкологического больного является пальпация зон возможного метастазирования опухоли (лимфоузлов). Пораженные mts они увеличены в размерах, плотны и безболезненны, обычно не спаяны с окружающими тканями и легко смещаются. Плотная консистенция свидетельствует о замещении лимфоидной ткани клетками ЗН. 4. Дополнительное специальное обследование, направленное на объективизацию опухоли и получения материала для микроскопии клеточного состава ЗН. Это лабораторные и инструментальные методы, которые нередко они являются решающими для постановки диагноза.
3. Физикальное исследование больного, включающее осмотр и пальпацию пораженного органа и зон метастазирования. Не прибегая к специальным методам обследования можно осмотреть только опухоли наружных органов (кожи, губы, мягких тканей, полости рта и др. ). Рак молочной железы, лимогранулематоз, новообразования мягких тканей и костей обнаруживают при пальпации. ЗН выглядят плотными, неровными, мало и ли совершенно безболезненные, в той или иной мере фиксированы к окружающим тканям. Обязательным элементом объективного исследования онкологического больного является пальпация зон возможного метастазирования опухоли (лимфоузлов). Пораженные mts они увеличены в размерах, плотны и безболезненны, обычно не спаяны с окружающими тканями и легко смещаются. Плотная консистенция свидетельствует о замещении лимфоидной ткани клетками ЗН. 4. Дополнительное специальное обследование, направленное на объективизацию опухоли и получения материала для микроскопии клеточного состава ЗН. Это лабораторные и инструментальные методы, которые нередко они являются решающими для постановки диагноза.
 Лабораторные методы диагностики Наибольшее значение имеет исследование периферической крови, в котором наиболее постоянным признаком является ускорение СОЭ, несколько реже наблюдается анемия, умеренный лейкоцитоз или лейкопения, лимфопения. Изменения чаще обнаруживают при раке внутренних органов на поздних (3 -4) стадиях. Необходимо помнить, что эти признаки не являются специфичными, они могут быть изолированными (например, только гипохромная анемия или только ускорение СОЭ), кроме того, они могут характеризовать сопутствующий ЗН процесс Определенный интерес представляет иммунохроматографический высокоспецифичный тест, определяющий скрытую кровь в кале, однако, имеющий больше скрининговое значение в обнаружении колоректального рака, в меньшей степени рака верхних отделов ЖКТ. Особенностью теста является отсутствие необходимости специальной диеты. Исследования мокроты, мочи, кала, других экскретов имеют значение только (!) для распознавания рака соответствующих органов.
Лабораторные методы диагностики Наибольшее значение имеет исследование периферической крови, в котором наиболее постоянным признаком является ускорение СОЭ, несколько реже наблюдается анемия, умеренный лейкоцитоз или лейкопения, лимфопения. Изменения чаще обнаруживают при раке внутренних органов на поздних (3 -4) стадиях. Необходимо помнить, что эти признаки не являются специфичными, они могут быть изолированными (например, только гипохромная анемия или только ускорение СОЭ), кроме того, они могут характеризовать сопутствующий ЗН процесс Определенный интерес представляет иммунохроматографический высокоспецифичный тест, определяющий скрытую кровь в кале, однако, имеющий больше скрининговое значение в обнаружении колоректального рака, в меньшей степени рака верхних отделов ЖКТ. Особенностью теста является отсутствие необходимости специальной диеты. Исследования мокроты, мочи, кала, других экскретов имеют значение только (!) для распознавания рака соответствующих органов.
 Иммунологические тесты (определение уровня онкомаркеров) Онкомаркеры представляют собой специфические вещества, которые образуется в результате жизнедеятельности раковых (а иногда и нормальных) клеток и обычно обнаруживаются в крови и/или моче онкологических пациентов. Они чрезвычайно многообразны по своей структуре, хотя в большинстве случаев, являются пептидами или их производными. Характеризуются относительно низкой специфичностью. Оценка в Ед/мл или Нг/мл PSA (простата-специфический антиген) – рак предстательной железы; ά-фетопротеин – гепатоцеллюлярная карцинома. CA – 125 – рак яичников CEA (карциноэмбриональный антиген, КЭА) — характерен в норме для кишечника, печени и поджелудочной железы плода. Этот антиген был найден в целом ряде аденокарцином органов желудочно-кишечного тракта и поджелудочной железы, так же как в саркомах и лимфомах различных гистологических типов. Высокий уровень в крови КЭА обнаруживается у больных при целом ряде неопухолевых состояний – при алкогольном циррозе печени, панкреатите, холецистите, дивертикулите и язвенном колите, с другой стороны при раке он может быть повышен уже в запущенных стадиях. По этой причине тест на КЭА не используется как серологический метод для скрининговой диагностики рака из за низкой чувствительности и специфичности. Имеет большее значение в мониторинге динамики течения ЗН (метастазирования, рецидива). CA – 19 -9. Определяется с той же целью, что и CEA, часто перекрестно
Иммунологические тесты (определение уровня онкомаркеров) Онкомаркеры представляют собой специфические вещества, которые образуется в результате жизнедеятельности раковых (а иногда и нормальных) клеток и обычно обнаруживаются в крови и/или моче онкологических пациентов. Они чрезвычайно многообразны по своей структуре, хотя в большинстве случаев, являются пептидами или их производными. Характеризуются относительно низкой специфичностью. Оценка в Ед/мл или Нг/мл PSA (простата-специфический антиген) – рак предстательной железы; ά-фетопротеин – гепатоцеллюлярная карцинома. CA – 125 – рак яичников CEA (карциноэмбриональный антиген, КЭА) — характерен в норме для кишечника, печени и поджелудочной железы плода. Этот антиген был найден в целом ряде аденокарцином органов желудочно-кишечного тракта и поджелудочной железы, так же как в саркомах и лимфомах различных гистологических типов. Высокий уровень в крови КЭА обнаруживается у больных при целом ряде неопухолевых состояний – при алкогольном циррозе печени, панкреатите, холецистите, дивертикулите и язвенном колите, с другой стороны при раке он может быть повышен уже в запущенных стадиях. По этой причине тест на КЭА не используется как серологический метод для скрининговой диагностики рака из за низкой чувствительности и специфичности. Имеет большее значение в мониторинге динамики течения ЗН (метастазирования, рецидива). CA – 19 -9. Определяется с той же целью, что и CEA, часто перекрестно
 Морфологические исследования Цитологическое исследование. Производится микроскопирование мазков с использованием специальных красителей. Оцениваются клетки исследуемой ткани. Обращают внимание на увеличение размеров ядра, гиперхромию и др. признаки. Цитологическое исследование проводят при раке нижней губы, кожи, молочной железы, раке шейки матки, а, также, при проведении биопсии опухолевых образований в качестве скринингдиагностики (мазки-отпечатки) во время эндоскопических исследований. Также исследуется материал (пунктат) из наружных лимфатических узлов, узловых образований ЩЖ (при условии, если они превышают 1 см), молочной железы, селезенки, печени. Проводят с помощью обычного шприца без анестезии (спец. иглы используют для пункции селезенки и печени). Под м/а проводят пункцию грудины иглой Кассирского для получения пунктата костного мозга при подозрении на гемобластоз. Оценке подвергаются, также, центрифугаты бронхиальной жидкости, мочи, плеврального выпота на предмет обнаружения клеток ЗН
Морфологические исследования Цитологическое исследование. Производится микроскопирование мазков с использованием специальных красителей. Оцениваются клетки исследуемой ткани. Обращают внимание на увеличение размеров ядра, гиперхромию и др. признаки. Цитологическое исследование проводят при раке нижней губы, кожи, молочной железы, раке шейки матки, а, также, при проведении биопсии опухолевых образований в качестве скринингдиагностики (мазки-отпечатки) во время эндоскопических исследований. Также исследуется материал (пунктат) из наружных лимфатических узлов, узловых образований ЩЖ (при условии, если они превышают 1 см), молочной железы, селезенки, печени. Проводят с помощью обычного шприца без анестезии (спец. иглы используют для пункции селезенки и печени). Под м/а проводят пункцию грудины иглой Кассирского для получения пунктата костного мозга при подозрении на гемобластоз. Оценке подвергаются, также, центрифугаты бронхиальной жидкости, мочи, плеврального выпота на предмет обнаружения клеток ЗН
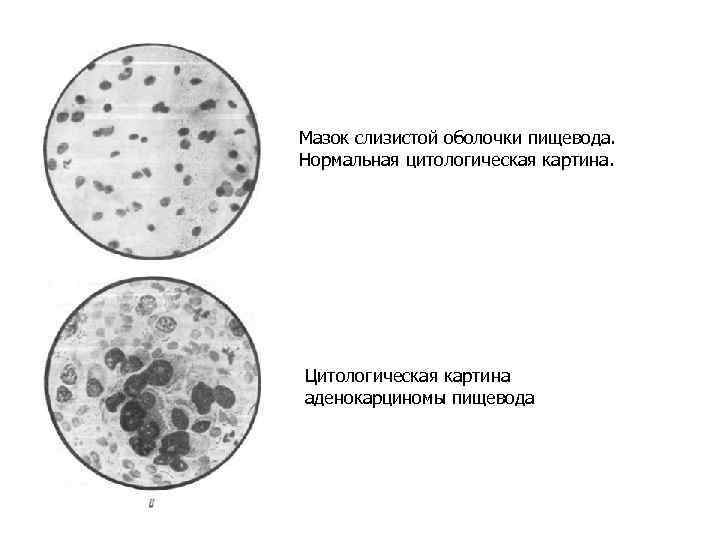 Мазок слизистой оболочки пищевода. Нормальная цитологическая картина. Цитологическая картина аденокарциномы пищевода
Мазок слизистой оболочки пищевода. Нормальная цитологическая картина. Цитологическая картина аденокарциномы пищевода
 Гистологическое исследование. Производится микроскопирование гистологических срезов, также, с использованием специальных красителей. Оценивается ткань опухоли, полученная либо при биопсии, либо при выполнении оперативного вмешательства (операционный материал). Позволяет установить окончательный диагноз ЗН, являясь завершающим этапом диагностического процесса. Рак (аденокарцинома) предстательной железы. Базальноклеточный рак кожи (базалиома).
Гистологическое исследование. Производится микроскопирование гистологических срезов, также, с использованием специальных красителей. Оценивается ткань опухоли, полученная либо при биопсии, либо при выполнении оперативного вмешательства (операционный материал). Позволяет установить окончательный диагноз ЗН, являясь завершающим этапом диагностического процесса. Рак (аденокарцинома) предстательной железы. Базальноклеточный рак кожи (базалиома).
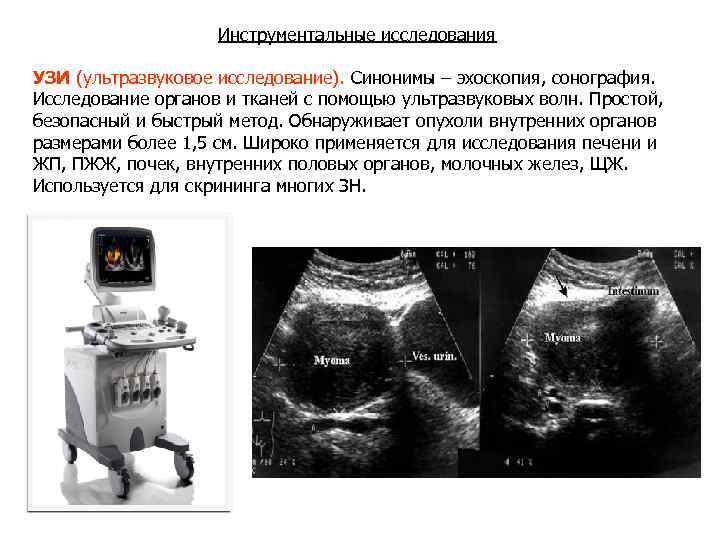 Инструментальные исследования УЗИ (ультразвуковое исследование). Синонимы – эхоскопия, сонография. Исследование органов и тканей с помощью ультразвуковых волн. Простой, безопасный и быстрый метод. Обнаруживает опухоли внутренних органов размерами более 1, 5 см. Широко применяется для исследования печени и ЖП, ПЖЖ, почек, внутренних половых органов, молочных желез, ЩЖ. Используется для скрининга многих ЗН.
Инструментальные исследования УЗИ (ультразвуковое исследование). Синонимы – эхоскопия, сонография. Исследование органов и тканей с помощью ультразвуковых волн. Простой, безопасный и быстрый метод. Обнаруживает опухоли внутренних органов размерами более 1, 5 см. Широко применяется для исследования печени и ЖП, ПЖЖ, почек, внутренних половых органов, молочных желез, ЩЖ. Используется для скрининга многих ЗН.
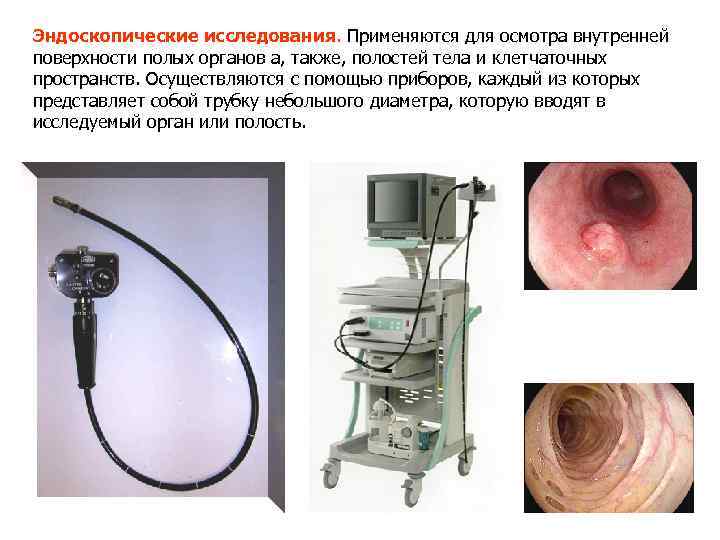 Эндоскопические исследования. Применяются для осмотра внутренней поверхности полых органов а, также, полостей тела и клетчаточных пространств. Осуществляются с помощью приборов, каждый из которых представляет собой трубку небольшого диаметра, которую вводят в исследуемый орган или полость.
Эндоскопические исследования. Применяются для осмотра внутренней поверхности полых органов а, также, полостей тела и клетчаточных пространств. Осуществляются с помощью приборов, каждый из которых представляет собой трубку небольшого диаметра, которую вводят в исследуемый орган или полость.
 Классификация эндоскопических методов исследования Исследования, выполняемые через естественные отверстия (per vias naturalis): • Эзофагогастродуоденоскопия • Ректосигмоколоноскопия (колоноскопия) а) ретороманоскопия (выполняемая жестким (ригидным) аппаратом) б) ректосигмоскопия (сигмоскопия) • Ларинготрахеобронхоскопия (выполняемая гибким и жестким бронхоскопом) • Дуоденоскопия Исследования, выполняемые через операционные отверстия (per operationem): • Лапароскопия • Торакоскопия • Медиастиноскопия Специальные исследования: • Эндоскопия с использованием красителей (хромоэндоскопия) • • • Капсульная эндоскопия Энтероскопия (одно- и двухбаллонная) Увеличительная (ZOOM-) эндоскопия Автофлуоресцентная эндоскопия Узкоспектральная эндоскопия (NBI – Narrow Band Image Endoscopy) Комбинированные исследования: • • Бронхография Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ) Ультразвуковая эндоскопия - эндосонография (EUS – Endoscopic Ultrasonography) Конфокальная эндомикроскопия
Классификация эндоскопических методов исследования Исследования, выполняемые через естественные отверстия (per vias naturalis): • Эзофагогастродуоденоскопия • Ректосигмоколоноскопия (колоноскопия) а) ретороманоскопия (выполняемая жестким (ригидным) аппаратом) б) ректосигмоскопия (сигмоскопия) • Ларинготрахеобронхоскопия (выполняемая гибким и жестким бронхоскопом) • Дуоденоскопия Исследования, выполняемые через операционные отверстия (per operationem): • Лапароскопия • Торакоскопия • Медиастиноскопия Специальные исследования: • Эндоскопия с использованием красителей (хромоэндоскопия) • • • Капсульная эндоскопия Энтероскопия (одно- и двухбаллонная) Увеличительная (ZOOM-) эндоскопия Автофлуоресцентная эндоскопия Узкоспектральная эндоскопия (NBI – Narrow Band Image Endoscopy) Комбинированные исследования: • • Бронхография Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ) Ультразвуковая эндоскопия - эндосонография (EUS – Endoscopic Ultrasonography) Конфокальная эндомикроскопия
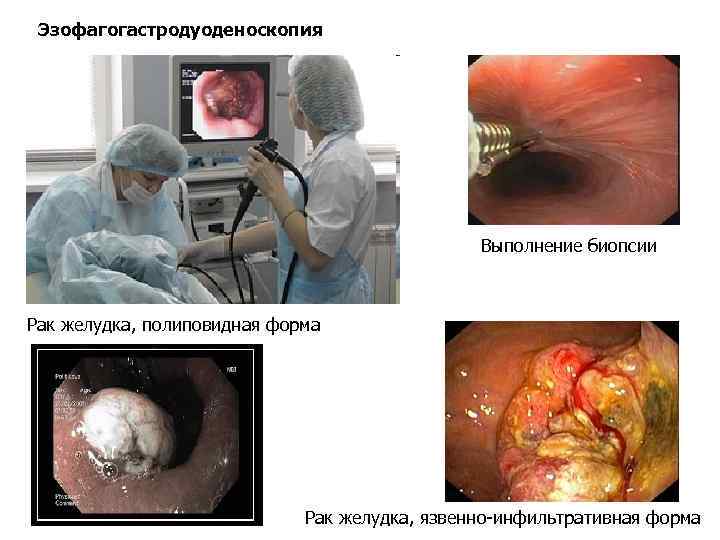 Эзофагогастродуоденоскопия Выполнение биопсии Рак желудка, полиповидная форма Рак желудка, язвенно-инфильтративная форма
Эзофагогастродуоденоскопия Выполнение биопсии Рак желудка, полиповидная форма Рак желудка, язвенно-инфильтративная форма
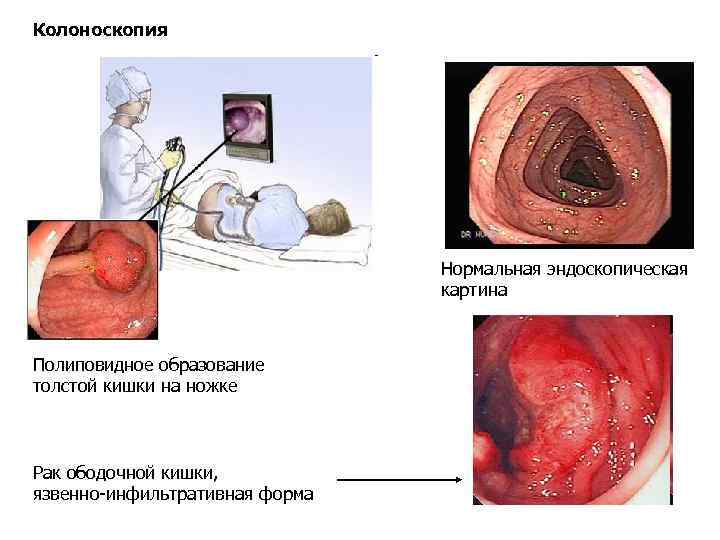 Колоноскопия Нормальная эндоскопическая картина Полиповидное образование толстой кишки на ножке Рак ободочной кишки, язвенно-инфильтративная форма
Колоноскопия Нормальная эндоскопическая картина Полиповидное образование толстой кишки на ножке Рак ободочной кишки, язвенно-инфильтративная форма
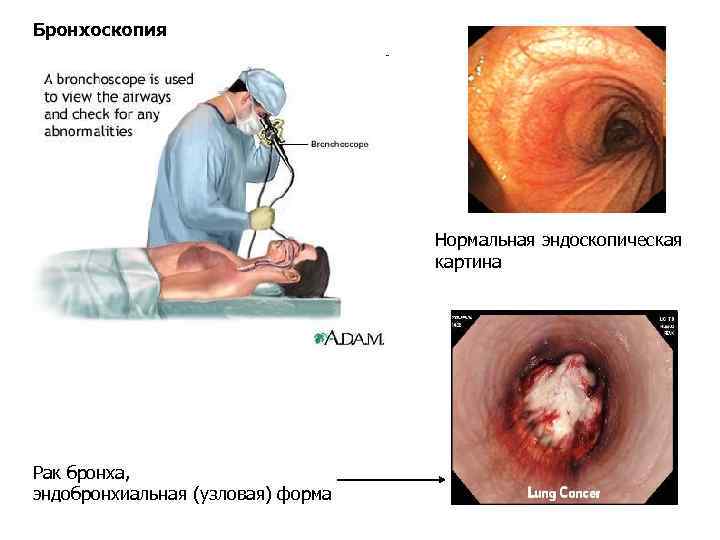 Бронхоскопия Нормальная эндоскопическая картина Рак бронха, эндобронхиальная (узловая) форма
Бронхоскопия Нормальная эндоскопическая картина Рак бронха, эндобронхиальная (узловая) форма
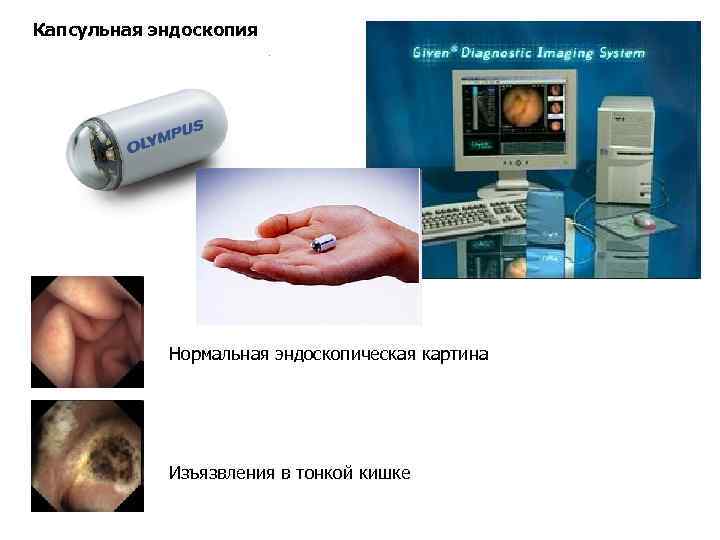 Капсульная эндоскопия Нормальная эндоскопическая картина Изъязвления в тонкой кишке
Капсульная эндоскопия Нормальная эндоскопическая картина Изъязвления в тонкой кишке
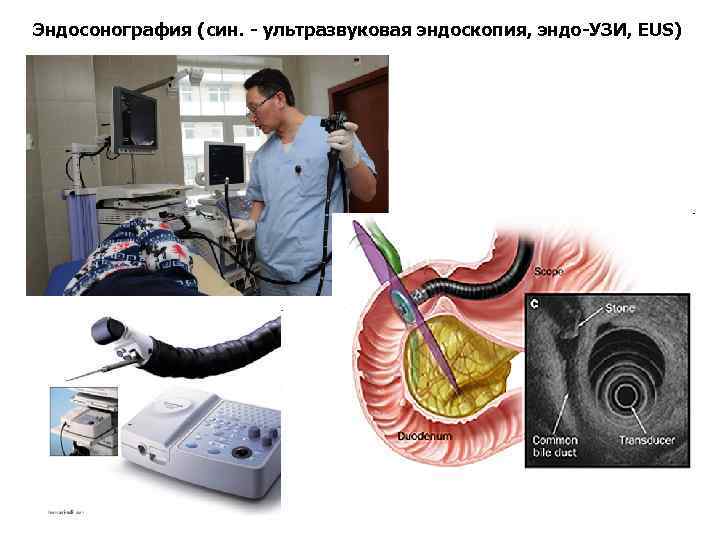 Эндосонография (син. - ультразвуковая эндоскопия, эндо-УЗИ, EUS)
Эндосонография (син. - ультразвуковая эндоскопия, эндо-УЗИ, EUS)
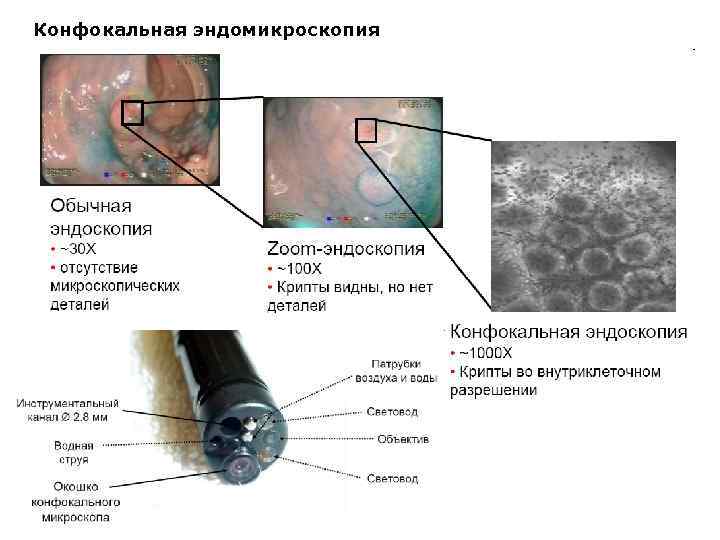 Конфокальная эндомикроскопия
Конфокальная эндомикроскопия
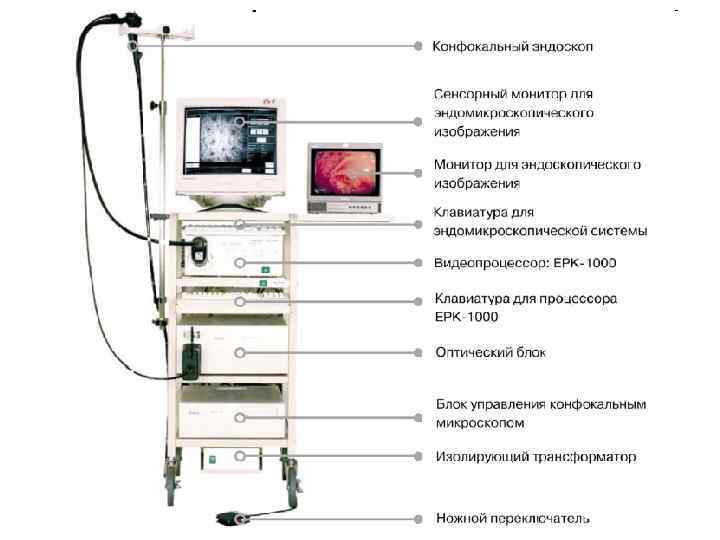
 Исследования, выполняемые с использованием устаревших аппаратов с волоконной оптикой имеют приставку “фибро” (например, фиброэзофаго-гастродуоденоскопия). Аппараты, не имеющие волоконной оптики, где преобразование изображения происходит с использованием электронных технологий, именуются видеоэндоскопами (все специальные исследования). Специальные и комбинированные исследования наряду с рутинными методиками существенно расширяют диагностические возможности в диагностике рака, особенно ранних его стадий, однако, остаются малодоступными и выполняются только в крупных специализированных центрах. Осмотр при эндоскопических исследованиях, как правило, дополняется биопсией, получением мазков с поверхности новообразований, а в некоторых случаях, еще и промывных вод. Проведение биопсии осуществляется с помощью специальных игл, щипцов, петель, щеток, кюреток и т. д. Полученный материал направляют на патоморфологическое исследование. Такой комплекс мероприятий называют комплексным.
Исследования, выполняемые с использованием устаревших аппаратов с волоконной оптикой имеют приставку “фибро” (например, фиброэзофаго-гастродуоденоскопия). Аппараты, не имеющие волоконной оптики, где преобразование изображения происходит с использованием электронных технологий, именуются видеоэндоскопами (все специальные исследования). Специальные и комбинированные исследования наряду с рутинными методиками существенно расширяют диагностические возможности в диагностике рака, особенно ранних его стадий, однако, остаются малодоступными и выполняются только в крупных специализированных центрах. Осмотр при эндоскопических исследованиях, как правило, дополняется биопсией, получением мазков с поверхности новообразований, а в некоторых случаях, еще и промывных вод. Проведение биопсии осуществляется с помощью специальных игл, щипцов, петель, щеток, кюреток и т. д. Полученный материал направляют на патоморфологическое исследование. Такой комплекс мероприятий называют комплексным.
 Рентгенологические исследования Позволяют обнаружить теневое изображение опухоли или вызванных ею изменения в органах. Такие исследования, как рентгенография легких, костей, маммография, проводятся без использования контрастных препаратов. Для обнаружения опухолей в органах, имеющих трубчатое строение, в них вводят контрастные вещества (сульфат бария), которые заполняя свободное пространство, обтекают новообразования, контурируя их. Незаполненный контрастным веществом участок называют дефектом наполнения, его очертания по форме и размерам соответствуют опухоли. Данный рентгенологический признак является ведущим в распознавании ЗН. Другими симптомами являются: - нарушение рельефа слизистой оболочки; - обрыв складок; - отсутствие перистальтики на участке поражения и деформация контуров органов.
Рентгенологические исследования Позволяют обнаружить теневое изображение опухоли или вызванных ею изменения в органах. Такие исследования, как рентгенография легких, костей, маммография, проводятся без использования контрастных препаратов. Для обнаружения опухолей в органах, имеющих трубчатое строение, в них вводят контрастные вещества (сульфат бария), которые заполняя свободное пространство, обтекают новообразования, контурируя их. Незаполненный контрастным веществом участок называют дефектом наполнения, его очертания по форме и размерам соответствуют опухоли. Данный рентгенологический признак является ведущим в распознавании ЗН. Другими симптомами являются: - нарушение рельефа слизистой оболочки; - обрыв складок; - отсутствие перистальтики на участке поражения и деформация контуров органов.
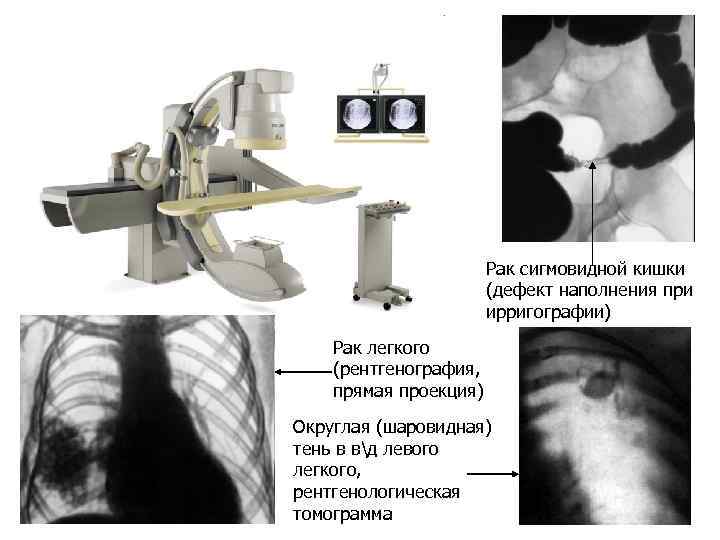 Рак сигмовидной кишки (дефект наполнения при ирригографии) Рак легкого (рентгенография, прямая проекция) Округлая (шаровидная) тень в вд левого легкого, рентгенологическая томограмма
Рак сигмовидной кишки (дефект наполнения при ирригографии) Рак легкого (рентгенография, прямая проекция) Округлая (шаровидная) тень в вд левого легкого, рентгенологическая томограмма
 Для оценки глубины залегания опухоли в легочной ткани и уточнения ее признаков используют Rtg-томографию. Сочетанными рентгено-эндоскопическими методами являются ЭРХПГ (позволяет обнаружить опухоли панкреатобилиарной зоны) и бронхография (опухоли трахеи и бронхов), которые постепенно вытесняются эндосонографией. Практически в настоящее время не проводятся Rtg-исследования с введением газа в исследуемые полости и клетчаточные пространства – пневмоперитонеум, ретропневмоперитонеум и пневмомедиастинум.
Для оценки глубины залегания опухоли в легочной ткани и уточнения ее признаков используют Rtg-томографию. Сочетанными рентгено-эндоскопическими методами являются ЭРХПГ (позволяет обнаружить опухоли панкреатобилиарной зоны) и бронхография (опухоли трахеи и бронхов), которые постепенно вытесняются эндосонографией. Практически в настоящее время не проводятся Rtg-исследования с введением газа в исследуемые полости и клетчаточные пространства – пневмоперитонеум, ретропневмоперитонеум и пневмомедиастинум.
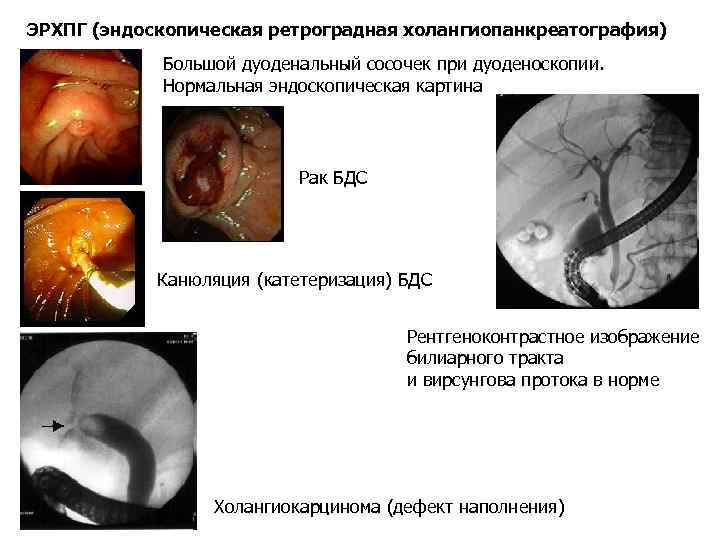 ЭРХПГ (эндоскопическая ретроградная холангиопанкреатография) Большой дуоденальный сосочек при дуоденоскопии. Нормальная эндоскопическая картина Рак БДС Канюляция (катетеризация) БДС Рентгеноконтрастное изображение билиарного тракта и вирсунгова протока в норме Холангиокарцинома (дефект наполнения)
ЭРХПГ (эндоскопическая ретроградная холангиопанкреатография) Большой дуоденальный сосочек при дуоденоскопии. Нормальная эндоскопическая картина Рак БДС Канюляция (катетеризация) БДС Рентгеноконтрастное изображение билиарного тракта и вирсунгова протока в норме Холангиокарцинома (дефект наполнения)
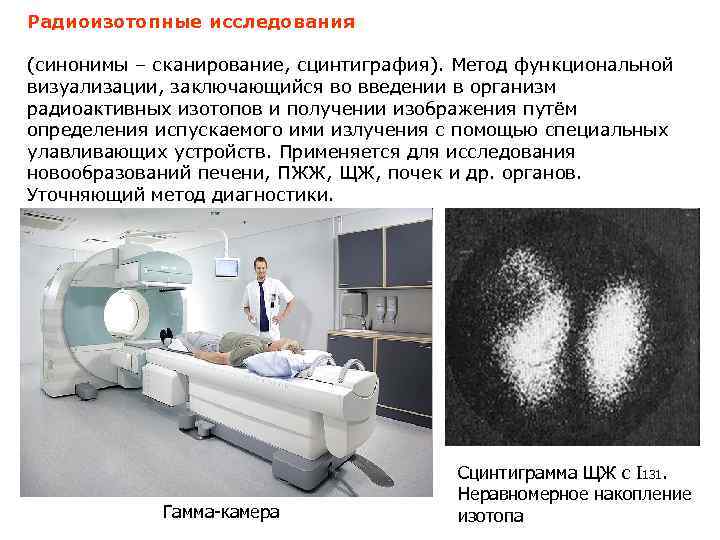 Радиоизотопные исследования (синонимы – сканирование, сцинтиграфия). Метод функциональной визуализации, заключающийся во введении в организм радиоактивных изотопов и получении изображения путём определения испускаемого ими излучения с помощью специальных улавливающих устройств. Применяется для исследования новообразований печени, ПЖЖ, ЩЖ, почек и др. органов. Уточняющий метод диагностики. Гамма-камера Сцинтиграмма ЩЖ с I 131. Неравномерное накопление изотопа
Радиоизотопные исследования (синонимы – сканирование, сцинтиграфия). Метод функциональной визуализации, заключающийся во введении в организм радиоактивных изотопов и получении изображения путём определения испускаемого ими излучения с помощью специальных улавливающих устройств. Применяется для исследования новообразований печени, ПЖЖ, ЩЖ, почек и др. органов. Уточняющий метод диагностики. Гамма-камера Сцинтиграмма ЩЖ с I 131. Неравномерное накопление изотопа
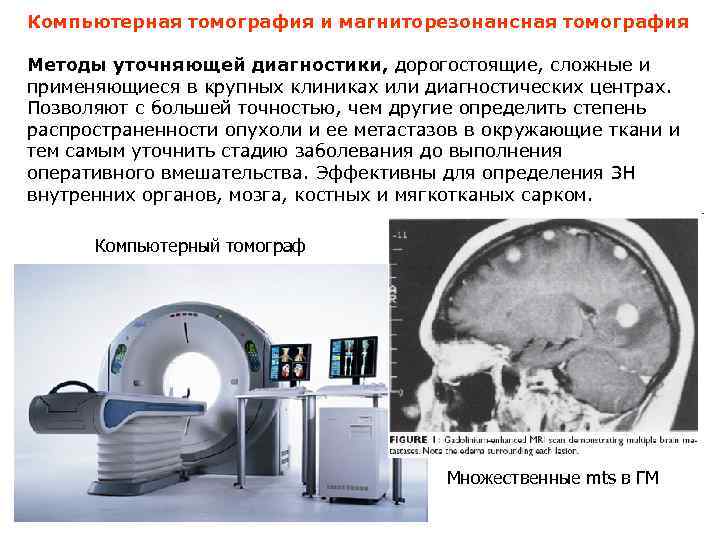 Компьютерная томография и магниторезонансная томография Методы уточняющей диагностики, дорогостоящие, сложные и применяющиеся в крупных клиниках или диагностических центрах. Позволяют с большей точностью, чем другие определить степень распространенности опухоли и ее метастазов в окружающие ткани и тем самым уточнить стадию заболевания до выполнения оперативного вмешательства. Эффективны для определения ЗН внутренних органов, мозга, костных и мягкотканых сарком. Компьютерный томограф Множественные mts в ГМ
Компьютерная томография и магниторезонансная томография Методы уточняющей диагностики, дорогостоящие, сложные и применяющиеся в крупных клиниках или диагностических центрах. Позволяют с большей точностью, чем другие определить степень распространенности опухоли и ее метастазов в окружающие ткани и тем самым уточнить стадию заболевания до выполнения оперативного вмешательства. Эффективны для определения ЗН внутренних органов, мозга, костных и мягкотканых сарком. Компьютерный томограф Множественные mts в ГМ
 Принципы лечения злокачественных опухолей Существует 3 основных метода лечения ЗН: • Хирургический • Лучевая терапия • Химиотерапия Они могут использоваться как самостоятельно, независимо друг от друга, так и в комбинации друг с другом. Сочетание 2 -х методов называется комбинированным, а 3 -х – комплексным лечением. Существует, также, т. н. симптоматическое лечение, направленное на ликвидацию наиболее тягостных симптомов (например, боли) и улучшения качества жизни больных, но не приносящее им излечения. К специальным методам лечения относят фотодинамическую терапию, применяемую при ранних стадиях рака желудка, кишечника, трахеобронхиального дерева, кожи, когда в организм вводится фотосенсибилизирующий агент, накапливающийся в ткани опухоли с последующим облучением ткани лучом лазера определенной длины волны. Происходящая фотохимическая реакция сопровождается гибелью клеток ЗН. Кроме того, при ранних формах рака желудка, пищевода, толстой кишки применяют внутрипросветные эндоскопические вмешательства, такие как эндоскопическая резекция слизистой оболочки (ЭРСО, EMR – Endoscopic Mucosal Resection) и эндоскопическая диссекция в подслизистом слое (ЭПД, ESD – Endoscopic Submucosal Dissection), которые могут выполняться как радикальные органосохраняющие малоинвазивные вмешательства
Принципы лечения злокачественных опухолей Существует 3 основных метода лечения ЗН: • Хирургический • Лучевая терапия • Химиотерапия Они могут использоваться как самостоятельно, независимо друг от друга, так и в комбинации друг с другом. Сочетание 2 -х методов называется комбинированным, а 3 -х – комплексным лечением. Существует, также, т. н. симптоматическое лечение, направленное на ликвидацию наиболее тягостных симптомов (например, боли) и улучшения качества жизни больных, но не приносящее им излечения. К специальным методам лечения относят фотодинамическую терапию, применяемую при ранних стадиях рака желудка, кишечника, трахеобронхиального дерева, кожи, когда в организм вводится фотосенсибилизирующий агент, накапливающийся в ткани опухоли с последующим облучением ткани лучом лазера определенной длины волны. Происходящая фотохимическая реакция сопровождается гибелью клеток ЗН. Кроме того, при ранних формах рака желудка, пищевода, толстой кишки применяют внутрипросветные эндоскопические вмешательства, такие как эндоскопическая резекция слизистой оболочки (ЭРСО, EMR – Endoscopic Mucosal Resection) и эндоскопическая диссекция в подслизистом слое (ЭПД, ESD – Endoscopic Submucosal Dissection), которые могут выполняться как радикальные органосохраняющие малоинвазивные вмешательства
 Оценку результатов лечения проводят, вычисляя процент 5 летних выздоровлений. По прошествии данного срока говорят об излечении от ЗН. Если опухоль рецидивирует в течение первых 3 лет, говорят о раннем рецидиве, если позже – о позднем рецидиве заболевания. Результаты лечения значительно лучше при опухолях наружных органов, а также, при I – II ст. рака внутренних органов. Рак in situ излечивается у 100% больных.
Оценку результатов лечения проводят, вычисляя процент 5 летних выздоровлений. По прошествии данного срока говорят об излечении от ЗН. Если опухоль рецидивирует в течение первых 3 лет, говорят о раннем рецидиве, если позже – о позднем рецидиве заболевания. Результаты лечения значительно лучше при опухолях наружных органов, а также, при I – II ст. рака внутренних органов. Рак in situ излечивается у 100% больных.
 Хирургическое лечение Различают радикальные и паллиативные хирургические вмешательства. Радикальными называются такие операции, при которых опухоль и ее метастазы удаляются полностью совместно с органом или частью его, регионарными лимфоузлами. Паллиативными считают вмешательства, при которых не происходит излечения больных, но преследуется задача ликвидации тягостных симптомов и осложнений (кишечная непроходимость, невозможность питаться при обтурации опухолью пищевода – наложение гастро (коло-)стомы, стентирование, кровотечение – остановка кровотечения и т. д. ) и продление жизни больных. В ряде случаев окончательное решение о возможности радикального лечения принимается хирургом во время оперативного вмешательства. При этом могут обнаруживаться неудалимые mts и прорастание опухолью окружающих жизненно важных органов, что делает невозможным радикальное вмешательство. В таких случаях операция ограничивается исключительно обследованием (осмотром) без проведения лечебных манипуляций и получила название эксплоративной.
Хирургическое лечение Различают радикальные и паллиативные хирургические вмешательства. Радикальными называются такие операции, при которых опухоль и ее метастазы удаляются полностью совместно с органом или частью его, регионарными лимфоузлами. Паллиативными считают вмешательства, при которых не происходит излечения больных, но преследуется задача ликвидации тягостных симптомов и осложнений (кишечная непроходимость, невозможность питаться при обтурации опухолью пищевода – наложение гастро (коло-)стомы, стентирование, кровотечение – остановка кровотечения и т. д. ) и продление жизни больных. В ряде случаев окончательное решение о возможности радикального лечения принимается хирургом во время оперативного вмешательства. При этом могут обнаруживаться неудалимые mts и прорастание опухолью окружающих жизненно важных органов, что делает невозможным радикальное вмешательство. В таких случаях операция ограничивается исключительно обследованием (осмотром) без проведения лечебных манипуляций и получила название эксплоративной.
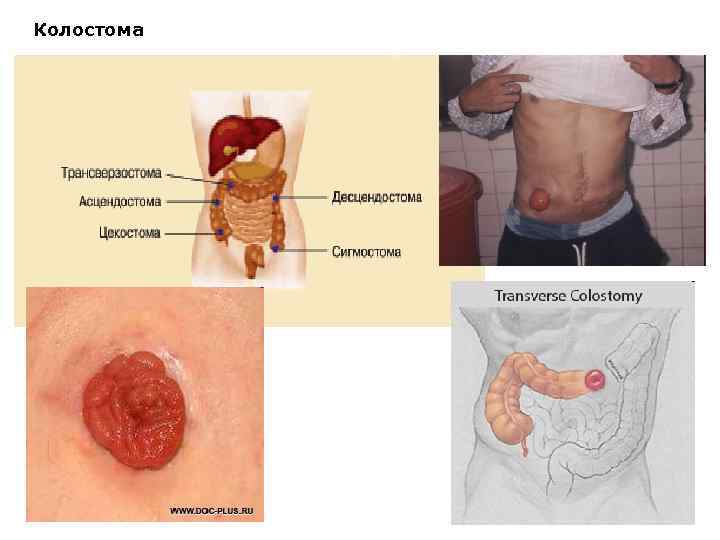 Колостома
Колостома
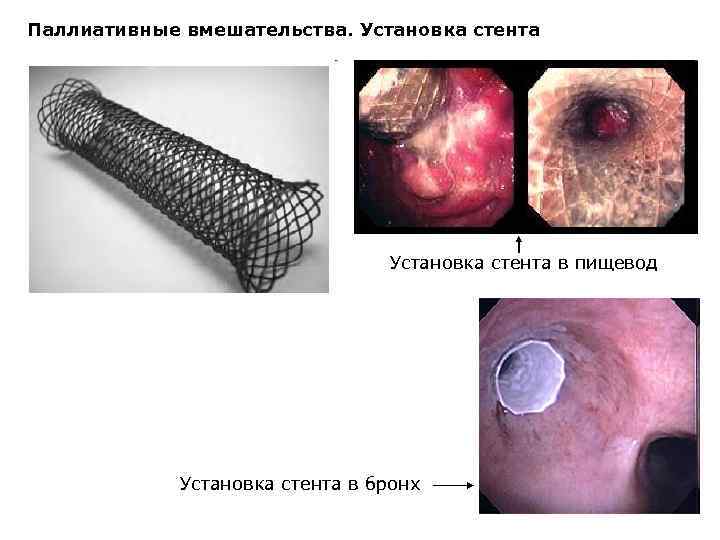 Паллиативные вмешательства. Установка стента в пищевод Установка стента в бронх
Паллиативные вмешательства. Установка стента в пищевод Установка стента в бронх
 Оперативные вмешательства, во время которых происходит удаление органа, пораженного опухолью целиком, называются экстирпацией (от лат. ex(s)tirpatio — удаление с корнем). Синонимом является ампутация. Чаще этот термин применяется в отношении удаляемой конечности, пораженной ЗН. В желудочно-кишечной хирургии применяется термин эктомия (гастрэктомия, гемиколэктомия). При этом оставшиеся органы или части их сшиваются друг с другом, с формированием искусственного соустья (анастомоза). Если орган, пораженный ЗН удаляется частично, то тогда используется термин резекция. При опухолях, локализованных в желудке, обычно удаляется ¾ органа (реже – больше – субтотальная резекция), при этом резекции могут быть проксимальными (с формированием искусственного гастроэзофагеального соустья) или дистальными (с формированием искусственного привратника). Во всех случаях, одновременно с удалением органа или его части, удаляются и периорганные лимфоузлы, являющимися коллекторами лимфоотока (лимфаденэктомия). Весь материал отправляется на патоморфологическое исследование, а с зон резекции берутся мазки для цитологического интраоперационного исследования на предмет обнаружения клеток ЗН
Оперативные вмешательства, во время которых происходит удаление органа, пораженного опухолью целиком, называются экстирпацией (от лат. ex(s)tirpatio — удаление с корнем). Синонимом является ампутация. Чаще этот термин применяется в отношении удаляемой конечности, пораженной ЗН. В желудочно-кишечной хирургии применяется термин эктомия (гастрэктомия, гемиколэктомия). При этом оставшиеся органы или части их сшиваются друг с другом, с формированием искусственного соустья (анастомоза). Если орган, пораженный ЗН удаляется частично, то тогда используется термин резекция. При опухолях, локализованных в желудке, обычно удаляется ¾ органа (реже – больше – субтотальная резекция), при этом резекции могут быть проксимальными (с формированием искусственного гастроэзофагеального соустья) или дистальными (с формированием искусственного привратника). Во всех случаях, одновременно с удалением органа или его части, удаляются и периорганные лимфоузлы, являющимися коллекторами лимфоотока (лимфаденэктомия). Весь материал отправляется на патоморфологическое исследование, а с зон резекции берутся мазки для цитологического интраоперационного исследования на предмет обнаружения клеток ЗН
 Резекция желудка (дистальная, принцип) Резекция желудка: А) – Бильрот –I Б) – Бильрот – II В) – Бильрот – II (с формированием соустья по Брауну) Вид гастроэнтероанастомоза при ЭГДС
Резекция желудка (дистальная, принцип) Резекция желудка: А) – Бильрот –I Б) – Бильрот – II В) – Бильрот – II (с формированием соустья по Брауну) Вид гастроэнтероанастомоза при ЭГДС
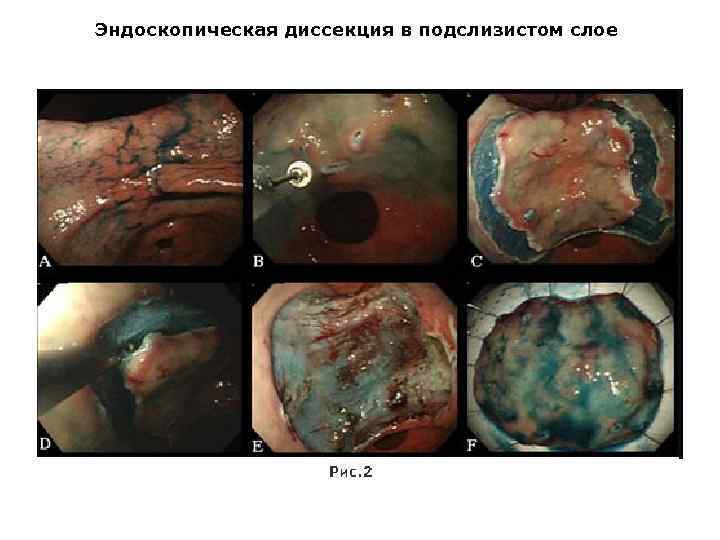 Эндоскопическая диссекция в подслизистом слое
Эндоскопическая диссекция в подслизистом слое
 Фотодинамическая терапия
Фотодинамическая терапия
 Лучевая терапия Применяется в лечении 55 -60% больных. Ее используют при ЗН наружных органов, раке легкого, гортани, верхних отделах пищевода, злокачественных лимфомах и др. ЗН. При раке ЖКТ лечение малоэффективно (требуются очень высокие дозы с проявлением выраженного токсического эффекта). Принцип заключается в воздействии на хромосомный аппарат клеток ЗН, в результате чего происходит их гибель. В ряде случаев в клетках происходит лишь торможение митозов на определенный период, после чего рост опухли возобновляется. В зависимости от расположения источника ионизирующего излучения различают дистанционное и контактное облучение. При дистанционном облучении источник находится на расстоянии от больного. При этом, если пациент и источник облучения на протяжении всего сеанса неподвижны, такое воздействие называют статичным. Если установка с источником излучения может перемещаться относительно очага поражения, то такой вариант воздействия называется ротационным. Применяются γ(гамма)-лучи, рентгеновские лучи, протоны, быстрые электроны При контактном способе источник ионизирующего излучения непосредственно соприкасается с опухолью. Для этого препарат накладывают на пораженный участок (аппликационный метод) или вводят в опухоль в виде радиоактивных игл (внутритканевая или брахитерапия). Используют γ-лучи
Лучевая терапия Применяется в лечении 55 -60% больных. Ее используют при ЗН наружных органов, раке легкого, гортани, верхних отделах пищевода, злокачественных лимфомах и др. ЗН. При раке ЖКТ лечение малоэффективно (требуются очень высокие дозы с проявлением выраженного токсического эффекта). Принцип заключается в воздействии на хромосомный аппарат клеток ЗН, в результате чего происходит их гибель. В ряде случаев в клетках происходит лишь торможение митозов на определенный период, после чего рост опухли возобновляется. В зависимости от расположения источника ионизирующего излучения различают дистанционное и контактное облучение. При дистанционном облучении источник находится на расстоянии от больного. При этом, если пациент и источник облучения на протяжении всего сеанса неподвижны, такое воздействие называют статичным. Если установка с источником излучения может перемещаться относительно очага поражения, то такой вариант воздействия называется ротационным. Применяются γ(гамма)-лучи, рентгеновские лучи, протоны, быстрые электроны При контактном способе источник ионизирующего излучения непосредственно соприкасается с опухолью. Для этого препарат накладывают на пораженный участок (аппликационный метод) или вводят в опухоль в виде радиоактивных игл (внутритканевая или брахитерапия). Используют γ-лучи
 Установка для лучевой терапии Иглы для γ-терапии
Установка для лучевой терапии Иглы для γ-терапии
 Химиотерапия Проводится, как правило, в виде комбинации препаратов (полихимиотерапия), а, также, в сочетании с лучевой терапией и хирургическим лечением. Основное действие химиопрепаратов связано с изменением обмена нуклеиновых кислот раковой клетки. Используется для паллиативного и радикального лечения ЗН при их распространенных формах. В качестве самостоятельного метода применяются только при высокочувствительных опухолях (лейкозы) в виде определенных схем. Химиотерапия, назначаемая перед оперативным лечением предназначается для перевода агрессивно протекающей опухоли в операбельное состояние. ХТ, применяемая после оперативного вмешательства получила название адъювантной целью которой является уничтожение оставшихся клеток ЗН с целью профилактики mts и рецидива. Такую ХТ проводят повторными курсами в течении длительного времени. Вследствие своей токсичности химиопрепараты вызывают побочные эффекты (тошнота, рвота, диарея, обратимая алопеция, изменения со стороны картины крови, периферические парестезии и др. ) Химиопрепараты вводят различными путями, чаще внутривенно.
Химиотерапия Проводится, как правило, в виде комбинации препаратов (полихимиотерапия), а, также, в сочетании с лучевой терапией и хирургическим лечением. Основное действие химиопрепаратов связано с изменением обмена нуклеиновых кислот раковой клетки. Используется для паллиативного и радикального лечения ЗН при их распространенных формах. В качестве самостоятельного метода применяются только при высокочувствительных опухолях (лейкозы) в виде определенных схем. Химиотерапия, назначаемая перед оперативным лечением предназначается для перевода агрессивно протекающей опухоли в операбельное состояние. ХТ, применяемая после оперативного вмешательства получила название адъювантной целью которой является уничтожение оставшихся клеток ЗН с целью профилактики mts и рецидива. Такую ХТ проводят повторными курсами в течении длительного времени. Вследствие своей токсичности химиопрепараты вызывают побочные эффекты (тошнота, рвота, диарея, обратимая алопеция, изменения со стороны картины крови, периферические парестезии и др. ) Химиопрепараты вводят различными путями, чаще внутривенно.
 Группы химиопрепаратов 1. Гормональные препараты. Применяются при опухолях, проявляющих гормональную зависимость (опухоли половых органов, молочной железы). Эстрогены, андрогены и их синтетические аналоги 2. Алкилирующие агенты. Чаще при опухолях системы крови. Сарколизин, циклофосфан. 3. Антиметаболиты. При опухолях ЖКТ, молочной железы (5 фторурацил), лейкозах (метатрексат, 6 -меркаптопурин) 4. Вещества растительного происхождения. При опухолях лимфатической системы (винкристин, винбластин), раке кожи (колхицин) 5. Противоопухолевые антибиотики. При опухолях системы крови, саркомах мягких тканей (блеомицин, митрамицин, адриамицин, даунорубимицин) 6. Прочие препараты. При раке мочевого пузыря (дибунол). Производные нитрозомочевины (БХНМ, ЦГНМ) – миеломная болезнь, болезнь Ходжкина, опухоли яичников, головного мозга, бронхопульмональный рак
Группы химиопрепаратов 1. Гормональные препараты. Применяются при опухолях, проявляющих гормональную зависимость (опухоли половых органов, молочной железы). Эстрогены, андрогены и их синтетические аналоги 2. Алкилирующие агенты. Чаще при опухолях системы крови. Сарколизин, циклофосфан. 3. Антиметаболиты. При опухолях ЖКТ, молочной железы (5 фторурацил), лейкозах (метатрексат, 6 -меркаптопурин) 4. Вещества растительного происхождения. При опухолях лимфатической системы (винкристин, винбластин), раке кожи (колхицин) 5. Противоопухолевые антибиотики. При опухолях системы крови, саркомах мягких тканей (блеомицин, митрамицин, адриамицин, даунорубимицин) 6. Прочие препараты. При раке мочевого пузыря (дибунол). Производные нитрозомочевины (БХНМ, ЦГНМ) – миеломная болезнь, болезнь Ходжкина, опухоли яичников, головного мозга, бронхопульмональный рак
 Деонтология в онкологии Необходимо максимально щадить психику больного, который находится в подавленном состоянии. Не рекомендуется сообщать ему о наличии онкологического заболевания, когда оно предполагается лишь гипотетически и больной недообследован. Однако, в случае явного подозрения на ЗН необходимо объяснить больному необходимость в детальном обследовании и предстоящем лечении, особенно, когда пациент недооценивает серьезность своего недуга. Нужно стараться избегать таких терминов как “рак”, “саркома”. Медработники не имеют право распространять сведения об онкологическом больном посторонним лицам, но родственников следует объективно информировать о характере заболевания и, по возможности, оставить надежду на благоприятный исход. Указывать предполагаемую продолжительность жизни больных с запущенными стадиями ЗН даже ориентировочно не следует. Конкретный ответ в такой ситуации тяжело воспринимается больными и родственниками, а ошибка в ту или иную сторону роняет авторитет медработника
Деонтология в онкологии Необходимо максимально щадить психику больного, который находится в подавленном состоянии. Не рекомендуется сообщать ему о наличии онкологического заболевания, когда оно предполагается лишь гипотетически и больной недообследован. Однако, в случае явного подозрения на ЗН необходимо объяснить больному необходимость в детальном обследовании и предстоящем лечении, особенно, когда пациент недооценивает серьезность своего недуга. Нужно стараться избегать таких терминов как “рак”, “саркома”. Медработники не имеют право распространять сведения об онкологическом больном посторонним лицам, но родственников следует объективно информировать о характере заболевания и, по возможности, оставить надежду на благоприятный исход. Указывать предполагаемую продолжительность жизни больных с запущенными стадиями ЗН даже ориентировочно не следует. Конкретный ответ в такой ситуации тяжело воспринимается больными и родственниками, а ошибка в ту или иную сторону роняет авторитет медработника


