стом 2.ppt
- Количество слайдов: 25

ВВЕДЕНИЕ В МЕТАБОЛИЗМ И БИОЭНЕРГЕТИКУ Часть 2 Тканевое дыхание и окислительное фосфорилирование
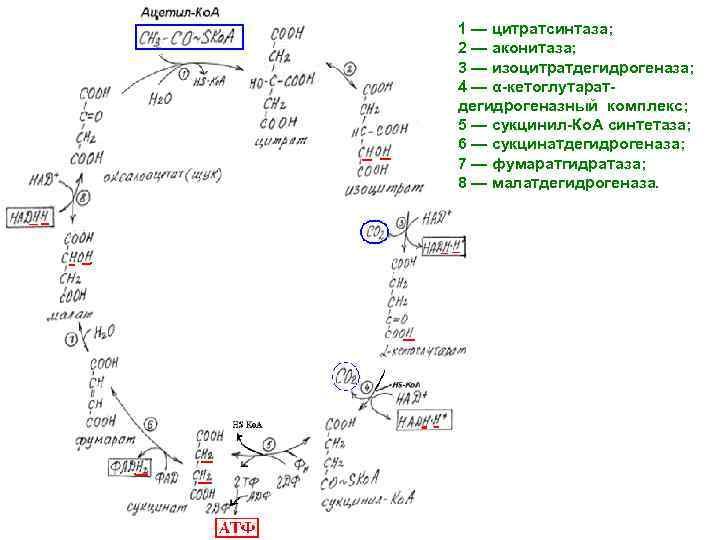
1 — цитратсинтаза; 2 — аконитаза; 3 — изоцитратдегидрогеназа; 4 — α-кетоглутаратдегидрогеназный комплекс; 5 — сукцинил-Ко. А синтетаза; 6 — сукцинатдегидрогеназа; 7 — фумаратгидратаза; 8 — малатдегидрогеназа.

Регуляция ЦТК Цитратсинтаза ингибируется АТФ, жирными кислотами. Изоцитрат. ДГ активируется АДФ, НАД+, ингибируется АТФ, НАДН·Н+.
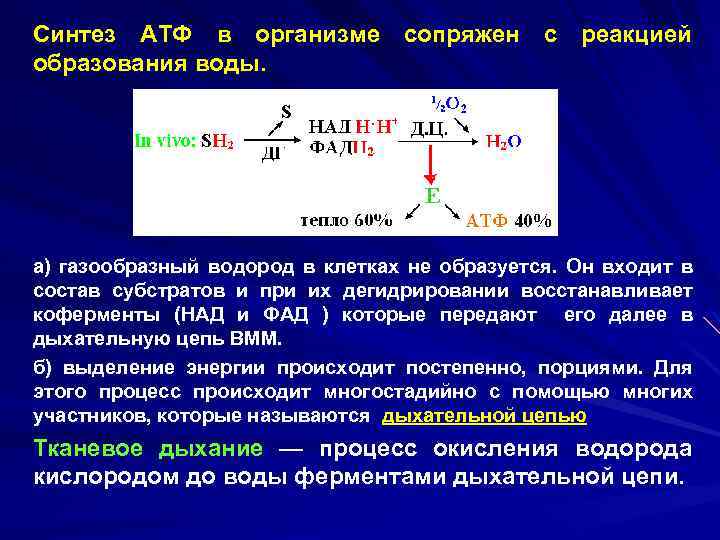
Синтез АТФ в организме сопряжен с реакцией образования воды. а) газообразный водород в клетках не образуется. Он входит в состав субстратов и при их дегидрировании восстанавливает коферменты (НАД и ФАД ) которые передают его далее в дыхательную цепь ВММ. б) выделение энергии происходит постепенно, порциями. Для этого процесс происходит многостадийно с помощью многих участников, которые называются дыхательной цепью Тканевое дыхание — процесс окисления водорода кислородом до воды ферментами дыхательной цепи.
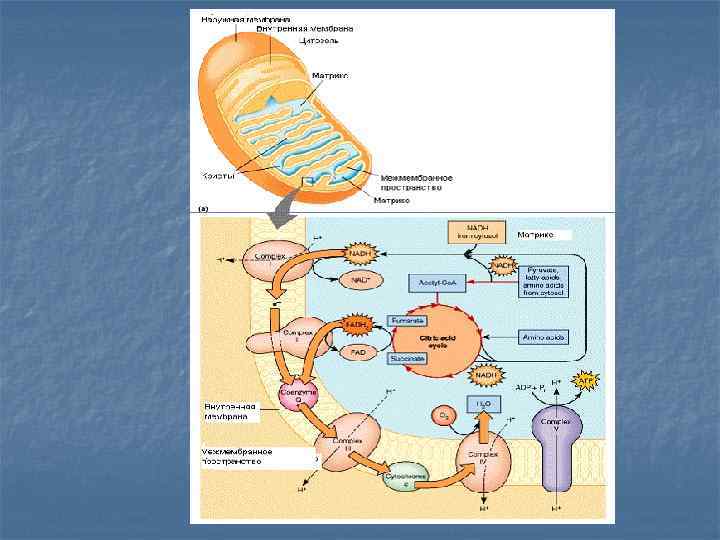

Дыхательная цепь — последовательность переносчиков электронов на кислород, локализованная во внутренней мембране митохондрий (ВММ). Роль таких переносчиков выполняют: активные формы витамина В 2 — ФМН и ФАД (присоединяют электроны и протоны); атомы железа и меди в составе цитохромов; цитохромы –это хромопротеины. Классы: цит. А, цит. В, цит. С (различаются по строению гема). Цит. А и А 3, цит. С и С 1. . Переносят только электроны: Fe 3+ + ē ↔ Fe 2+ Cu 2+ + ē ↔ Cu+ В → С 1 → С → А 3 железосерные белки (Fe. S-белки) – содержат негемовое железо; переносят только электроны; жирорастворимый переносчик электронов и протонов, свободно перемещающийся по мембране, — убихинол (Ко. Q).

Принцип построения дыхательной цепи Последовательность переносчиков способностью отдавать электроны стандартным восстановительным (редокс-потенциалом). определяется их окислителю, т. е. потенциалом Е 0' В дыхательной цепи все реакции направлены по термодинамической лестнице от компонента с самым отрицательным редокс-потенциалом НАДН (-0, 42 В) к кислороду, имеющему самый положительный редокспотенциал (+ 0, 82 В). Для синтеза 1 молекулы АТФ необходимо 32 к. Дж. Для этого достаточной является разность потенциалов между окислителем и восстановителем ≥ 0, 2 В. Б. Чанс установил что таких участков (где разность потенциалов ≥ 0, 2 В) в дыхательной цепи три. Эти участки были названы Б. Чансом пунктами сопряжения или фосфорилирования. Эти участки соответствуют I, III и IV комплексам.
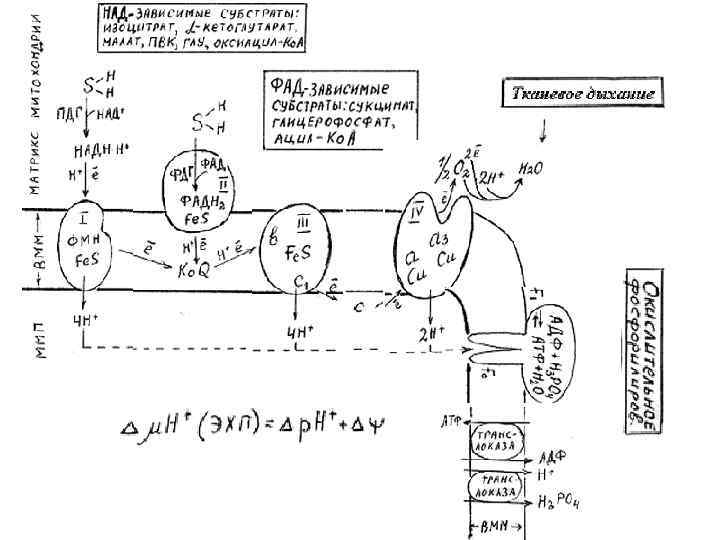

Связь между транспортом электронов по дыхательной цепи и синтезом АТФ: V комплекс внутренней мембраны митохондрий — фермент протонная АТФ-синтаза Эфраим Рэкер, 1961 г.

П. Митчелл сформулировал хемиоосмотическую теорию окислительного фосфорилирования (Нобелевская премия 1978 г. ). Постулаты хемиоосмотической теории: внутренняя митохондриальная мембрана (ВММ) непроницаема для ионов, в частности для Н+ и ОН-; за счет энергии транспорта электронов через I, III и IV комплексы дыхательной цепи из матрикса выкачиваются протоны; возникающий на мембране электрохимический потенциал (ЭХП) и есть промежуточная форма запасания энергии; возвращение (транслокация) протонов в матрикс митохондрии через протонный канал V комплекса за счет ЭХП является движущей силой синтеза АТФ.

Показали, что энергия движения протонов используется на изменения конформации активного центра АТФ-синтазы, что сопровождается синтезом АТФ, а затем ее высвобождением. L (свободная) – связывает лиганды. T (сжатая) – синтез АТФ О (открытая) – выход АТФ из активного центра. Образовавшаяся АТФ с помощью транслоказы перемещается в цитозоль; в ответ в матрикс митохондрии поступают АДФ и фосфат. Всего на процесс синтеза, высвобождения и выброса в цитозоль АТФ расходуется 4 протона: 3 протона – на изменение конформации АТФ-синтазы и 1 протон – на перенос в матрикс
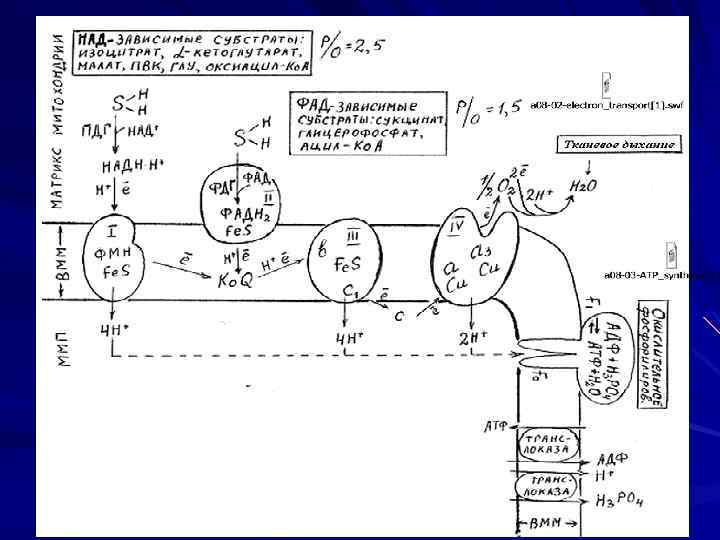

Коэффициент фосфорилирования (Р/О) – количество молекул неорганического фосфата, которое включается в АТФ в расчете на 1 атом кислорода. При окислении НАД-зависимых субстратов в ММП выбрасывается 10 протонов. Может быть синтезировано 2, 5 моль АТФ (10: 4), т. е. коэффициент фосфорилирования Р/О = 2, 5. При окислении ФАД-зависимых субстратов в ММП выбрасывается 6 протонов. Может быть синтезировано 1, 5 моль АТФ (6: 4), т. е. коэффициент фосфорилирования Р/О = 1, 5.
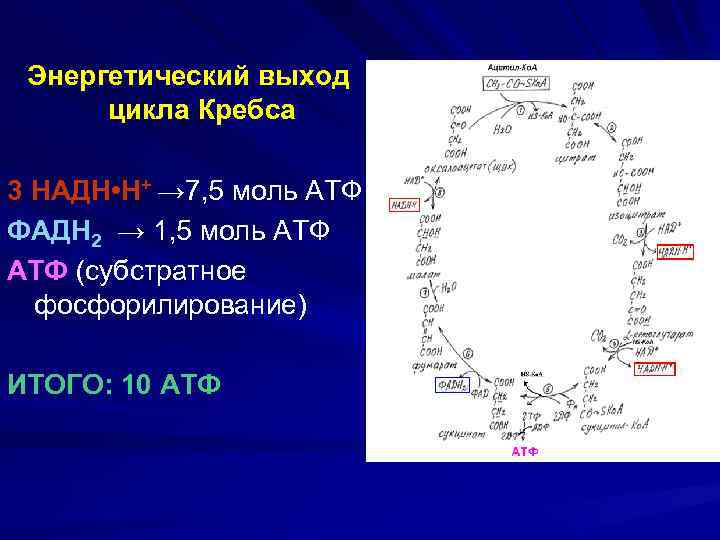
Энергетический выход цикла Кребса 3 HAДН • Н+ → 7, 5 моль АТФ ФАДН 2 → 1, 5 моль АТФ (субстратное фосфорилирование) ИТОГО: 10 АТФ

РЕГУЛЯЦИЯ РАБОТЫ ДЫХАТЕЛЬНОЙ ЦЕПИ энергетический заряд клетки – соотношение АТФ/АДФ является стимулятором дыхательной цепи АТФ – аллостерическим ингибитором. Дыхательный контроль – это увеличение поглощения кислорода митохондриями при добавлении АДФ Тканевое дыхание → ∆μН → Окислительное фосфорилирование

Гипоэнергетические состояния Причины: алиментарные (голодание, гиповитаминозы РР, В 2); гипоксические (нарушения доставки О 2 в клетки); митохондриальные (действие ингибиторов и разобщителей; митохондриальные болезни) - ингибиторы тканевого дыхания - ингибиторы окислительного фосфорилирования - разобщители тканевого дыхания и окислительного фосфорилирования
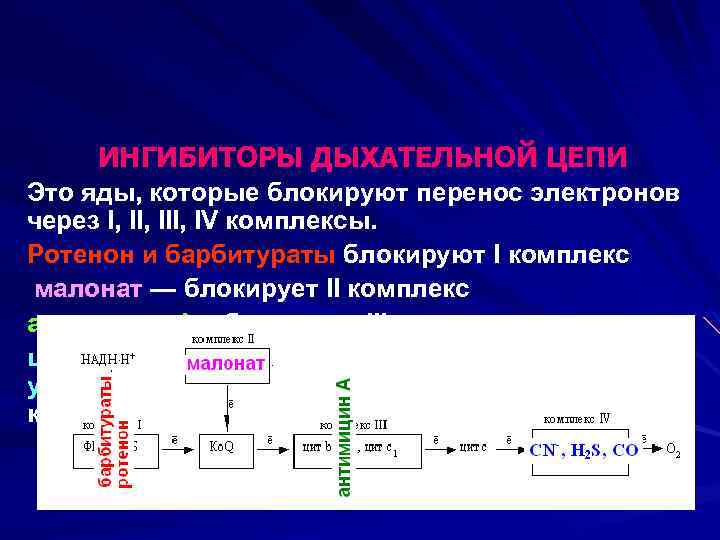
ИНГИБИТОРЫ ДЫХАТЕЛЬНОЙ ЦЕПИ Это яды, которые блокируют перенос электронов через I, III, IV комплексы. Ротенон и барбитураты блокируют I комплекс малонат — блокирует II комплекс антимицин А – блокирует III комплекс цианиды, сероводород, азид натрия, оксид азота, угарный газ блокируют перенос электронов на кислород (IV комплекс дыхательной цепи).
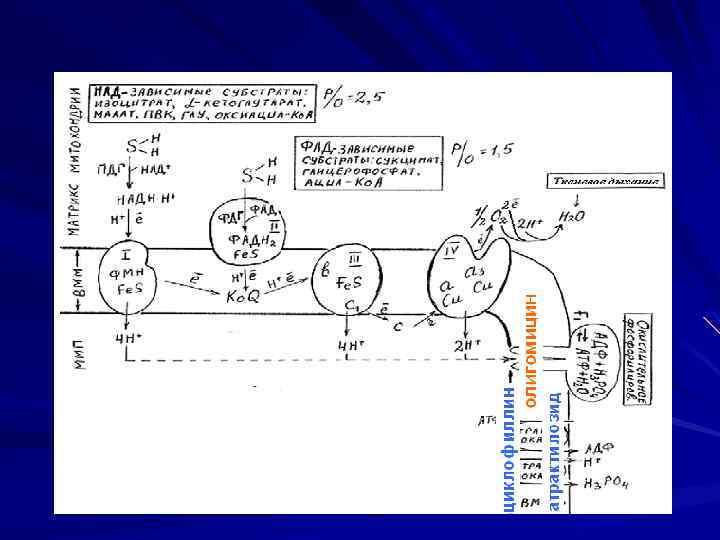
Ингибиторы окислительного фосфорилирования
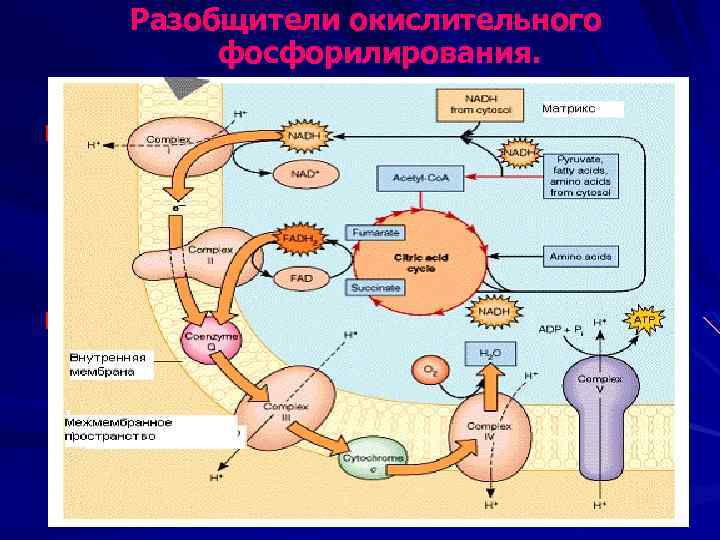
Разобщители окислительного фосфорилирования. Естественные разобщители Искусственные разобщители (продукты перекисного окисления липидов, жирные кислоты с длинной цепью, белки термогенины бурой жировой ткани, большие дозы йодсодержащих гормонов щитовидной железы); (дикумарол, динитрофенол, эфир, производные витамина К, некоторые антибиотики, анестетики).

ПУТИ УТИЛИЗАЦИИ КИСЛОРОДА КЛЕТКОЙ 1. Оксидазный путь (около 80 %) цитохромоксидаза ØПроисходит полное восстановление кислорода ØСубстрат не реагирует с кислородом непосредственно ØЭтот путь дает клетке энергию в виде АТФ Оксидазы (ФМН и ФАД-зависимые), которые катализируют реакции окисления веществ с образованием перекиси водорода
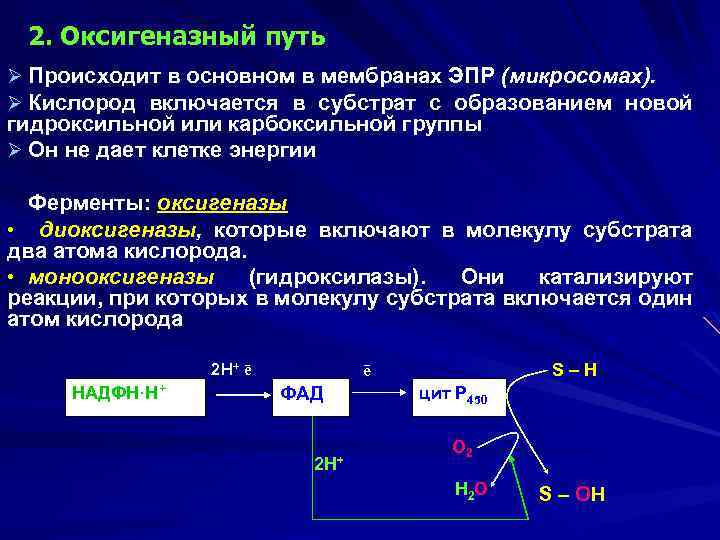
2. Оксигеназный путь Ø Происходит в основном в мембранах ЭПР (микросомах). Ø Кислород включается в субстрат с образованием новой гидроксильной или карбоксильной группы Ø Он не дает клетке энергии Ферменты: оксигеназы • диоксигеназы, которые включают в молекулу субстрата два атома кислорода. • монооксигеназы (гидроксилазы). Они катализируют реакции, при которых в молекулу субстрата включается один атом кислорода 2 Н+ ē НАДФН·Н+ S–H ē ФАД 2 Н+ цит Р 450 О 2 Н 2 О S – ОН

Роль оксигеназного пути: α- и ω-окисление жирных кислот, синтез ненасыщенных жирных кислот, стероидов. Синтез коллагена (гидроксилирование пролина и лизина). обезвреживание ксенобиотикков (лекарства, ядохимикаты, косметические препараты).

АКТИВНЫЕ ФОРМЫ КИСЛОРОДА Свободные радикалы кислорода, активные формы кислорода (АФК) - продукты неполного восстановления кислорода, агрессивные молекулы, содержащие неспаренные электроны, способные атаковать другие молекулы с целью забрать недостающий электрон. Полное восстановление кислорода до воды требует 4 -х электронов и катализируется цитохромоксидазой. О 2 + 4 е + 4 Н + → 2 Н 2 О Присоединение электронов происходит поэтапно и при этом образуются АФК. О 2 + е- → O 2 - (супероксидный радикал) O 2 - + 2 H + → H 2 O 2 H 2 O 2 + O 2 - → HO • (гидроперекисный радикал) HO • + е- + H+ → H 2 O

В живых клетках АФК образуются: §в реакциях окисления гемоглобина в метгемоглобин; §в реакциях, катализируемых оксидазами (пероксид водорода); §в процессе переноса е- по дыхательной цепи ( при передаче электронов с убихинона на цитохром с) §в процессе микросомного окисления (при передаче электрона с цит. Р 450); §при гипоксии (в митохондриях нарушается работа цитохромоксидазы, происходит утечка АФК); §при действии ионизирующей радиации и УФО.

ФЕРМЕНТАТИВНАЯ АНТИОКСИДАНТНАЯ ЗАЩИТА КЛЕТКИ ОТ АФК Супероксиддисмутаза (превращает супероксидные радикалы в менее токсичную перекись водорода); Каталаза (разлагает перекись водорода на воду и кислород); Система глутатиона: трипептид глутатион ( Г – SH), глутатионпероксидазу (ГП), глутатионредуктазу (ГР), НАДФН·Н+, селен.
стом 2.ppt