advanced AC-1 46.pptx
- Количество слайдов: 20
 Введение в аналитическую химию Титрование
Введение в аналитическую химию Титрование
 Раствор • Раствор – однофазная гомогенная система переменного состава, состоящая из двух и более компонентов и продуктов их взаимодействия • Растворитель – вещество, чье агрегатное состояние остается прежним при растворении • Растворяемое вещество – вещество, которое взаимодействует с растворителем, меняя или не меняя свое агрегатное состояние
Раствор • Раствор – однофазная гомогенная система переменного состава, состоящая из двух и более компонентов и продуктов их взаимодействия • Растворитель – вещество, чье агрегатное состояние остается прежним при растворении • Растворяемое вещество – вещество, которое взаимодействует с растворителем, меняя или не меняя свое агрегатное состояние
 Выражение количественного содержания вещества в растворе • Массовая доля ω(a) = m(a) / m(р-ра) • Молярная концентрация c(a)=ν(a) / V(р-ра) • Растворимость s(a)=m(a) / m(р-ля) • Моляльность y(a)=ν(a) / m(р-ля) (в кг!!!) • Мольная доля χ(a)=ν(a) / ν(всех) • Нормальность n(a)=M(a) / n. V(р-ра) • Титр T(a) = m(a)/V(р-ра)
Выражение количественного содержания вещества в растворе • Массовая доля ω(a) = m(a) / m(р-ра) • Молярная концентрация c(a)=ν(a) / V(р-ра) • Растворимость s(a)=m(a) / m(р-ля) • Моляльность y(a)=ν(a) / m(р-ля) (в кг!!!) • Мольная доля χ(a)=ν(a) / ν(всех) • Нормальность n(a)=M(a) / n. V(р-ра) • Титр T(a) = m(a)/V(р-ра)
 Реальное равновесие • Электростатические взаимодействия • Химические взаимодействия • Сольватационные
Реальное равновесие • Электростатические взаимодействия • Химические взаимодействия • Сольватационные
 Такие активные вещества • Реальные растворы отличаются от идеальных. Концетранционные переменные заменяются активностью a. • a. A+b. B=c. C+d. D
Такие активные вещества • Реальные растворы отличаются от идеальных. Концетранционные переменные заменяются активностью a. • a. A+b. B=c. C+d. D
 Закон действующих масс • В состоянии химического равновесия отношение произведения активностей продуктов реакции в степенях стехиометрических коэффициентов к произведению активностей реагентов есть величина постоянная при данной температуре, давлении и растворителе • Коэффициент активности
Закон действующих масс • В состоянии химического равновесия отношение произведения активностей продуктов реакции в степенях стехиометрических коэффициентов к произведению активностей реагентов есть величина постоянная при данной температуре, давлении и растворителе • Коэффициент активности
 Ионная сила • ИС – приближение, позволяющее рассчитывать активности на основе представлений об электростатических взаимодействиях • И коэффициент активности для воды A=0, 5
Ионная сила • ИС – приближение, позволяющее рассчитывать активности на основе представлений об электростатических взаимодействиях • И коэффициент активности для воды A=0, 5
 Кислотно-основное равновесие • Апротонные растворители (бензол, хлороформ) • Протофильные растворители (ацетон, трет-амины) • Амфипротные растворители (вода, спирты, кислоты)
Кислотно-основное равновесие • Апротонные растворители (бензол, хлороформ) • Протофильные растворители (ацетон, трет-амины) • Амфипротные растворители (вода, спирты, кислоты)
 Автопротолиз воды и p. H • • H 2 O + H 2 O = H 3 O+ + OHH 2 O = H+ + OHKw=[H+][OH-]=10 -14 при 250 С [H+]=[OH-]=10 -7 p. H= -lg[H+] = 7 p. OH= -lg[OH-]=7 p. H + p. OH = 14
Автопротолиз воды и p. H • • H 2 O + H 2 O = H 3 O+ + OHH 2 O = H+ + OHKw=[H+][OH-]=10 -14 при 250 С [H+]=[OH-]=10 -7 p. H= -lg[H+] = 7 p. OH= -lg[OH-]=7 p. H + p. OH = 14
 Диссоциация кислот или оснований • H 2 A = H+ + HA- Ka 1 = [H+][HA-]/[H 2 A] • HA- = H+ + A 2 - Ka 2 = [H+][A 2 -]/[HA-] • B(OH)2 = BOH+ + OH- Kb 1 = [OH-][BOH+]/[B(OH)2] • BOH+ = B 2+ + OH- Kb 2 = [OH-][B 2+]/[BOH+] • Рассчитать p. H 0. 1 М раствора уксусной кислоты (250 С) Ka = 1. 75*10 -5 • Рассчитать концентрацию ионов SO 42 - в 0. 1 М растворе H 2 SO 4. Ka 2 = 1. 2*10 -2
Диссоциация кислот или оснований • H 2 A = H+ + HA- Ka 1 = [H+][HA-]/[H 2 A] • HA- = H+ + A 2 - Ka 2 = [H+][A 2 -]/[HA-] • B(OH)2 = BOH+ + OH- Kb 1 = [OH-][BOH+]/[B(OH)2] • BOH+ = B 2+ + OH- Kb 2 = [OH-][B 2+]/[BOH+] • Рассчитать p. H 0. 1 М раствора уксусной кислоты (250 С) Ka = 1. 75*10 -5 • Рассчитать концентрацию ионов SO 42 - в 0. 1 М растворе H 2 SO 4. Ka 2 = 1. 2*10 -2
 Гидролиз • PO 43 - + H 2 O = HPO 42 - + OH • Kг=[HPO 42 -][OH-]/[PO 43 -][H 2 O] = • = ([HPO 42 -]/[H+][PO 43 -]) * ([H+][OH-]/[H 2 O]) = Kw/Ka 3 • NH 4+ + H 2 O = NH 3 + H 3 O+ • Kг = [NH 3][H+]/[H 2 O][NH 4+] = Kw/Kb
Гидролиз • PO 43 - + H 2 O = HPO 42 - + OH • Kг=[HPO 42 -][OH-]/[PO 43 -][H 2 O] = • = ([HPO 42 -]/[H+][PO 43 -]) * ([H+][OH-]/[H 2 O]) = Kw/Ka 3 • NH 4+ + H 2 O = NH 3 + H 3 O+ • Kг = [NH 3][H+]/[H 2 O][NH 4+] = Kw/Kb
 Буферные системы • с1 – концентрация кислоты, с2 - соли • HA = A- + H+ • Ka=[H+][A-]/[HA] • [H+] = Ka*[HA]/[A-] = Ka*c 1/c 2 • p. H = -lg[H+] = - lg. Ka – lg c 1/c 2 = p. Ka + lg c 2/c 1 • Рассчитать p. H системы CH 3 COOH/CH 3 COONa Ka = 1. 75*10 -5 ; V=100 мл; ν(CH 3 COOH)=10 ммоль; m(CH 3 COONa)= 10 г
Буферные системы • с1 – концентрация кислоты, с2 - соли • HA = A- + H+ • Ka=[H+][A-]/[HA] • [H+] = Ka*[HA]/[A-] = Ka*c 1/c 2 • p. H = -lg[H+] = - lg. Ka – lg c 1/c 2 = p. Ka + lg c 2/c 1 • Рассчитать p. H системы CH 3 COOH/CH 3 COONa Ka = 1. 75*10 -5 ; V=100 мл; ν(CH 3 COOH)=10 ммоль; m(CH 3 COONa)= 10 г
 Равновесие твердость-жидкость • Ag. Clтв = Ag+aq + Cl-aq • Произведение растворимости – константа равновесия реакции между твердым веществом в растворе и ионами на которые оно частично растворяется • ПР = [Ag+][Cl-] = 1, 77 * 10 -10 • Условие выпадения осадка - [Ag+][Cl-]>ПР
Равновесие твердость-жидкость • Ag. Clтв = Ag+aq + Cl-aq • Произведение растворимости – константа равновесия реакции между твердым веществом в растворе и ионами на которые оно частично растворяется • ПР = [Ag+][Cl-] = 1, 77 * 10 -10 • Условие выпадения осадка - [Ag+][Cl-]>ПР
 Титрование • Метод количественного анализа, основанный на строго стехиометрическом соотношении взаимодействующих веществ(одного с известной концентрацией) • Кислотно-основное • Окислительно-восстановительное • Комплексонометрия • Кондуктометрия
Титрование • Метод количественного анализа, основанный на строго стехиометрическом соотношении взаимодействующих веществ(одного с известной концентрацией) • Кислотно-основное • Окислительно-восстановительное • Комплексонометрия • Кондуктометрия
 Способы титрования • Прямое – к аликвоте исследуемого вещества добавляют титрант (порциями) • Обратное – добавляем заведомо избыток титранта, и титруем затем его непрореагировавший остаток • Заместительное – титруется не само вещество, а некоторый продукт его реакции с добавочным реагентом
Способы титрования • Прямое – к аликвоте исследуемого вещества добавляют титрант (порциями) • Обратное – добавляем заведомо избыток титранта, и титруем затем его непрореагировавший остаток • Заместительное – титруется не само вещество, а некоторый продукт его реакции с добавочным реагентом
 Основные индикаторы • Метиловый оранжевый: переход красныйоранжевый-желтый (p. H 3, 1 -4, 4) • Фенолфталеин: переход бесцветныймалиновый (8, 2) • Универсальный(смесь)
Основные индикаторы • Метиловый оранжевый: переход красныйоранжевый-желтый (p. H 3, 1 -4, 4) • Фенолфталеин: переход бесцветныймалиновый (8, 2) • Универсальный(смесь)
 Точка эквивалентности. Точка титрования • Точка эквивалентности – число эквивалентов добавляемого вещества равно числу эквивалентов исследуемого • cэкв 1 V 1=cэкв 2 V 2 • Точка титрования – момент цветового перехода • Вообще говоря, точка титрования и эквивалентности не одно и тоже!
Точка эквивалентности. Точка титрования • Точка эквивалентности – число эквивалентов добавляемого вещества равно числу эквивалентов исследуемого • cэкв 1 V 1=cэкв 2 V 2 • Точка титрования – момент цветового перехода • Вообще говоря, точка титрования и эквивалентности не одно и тоже!
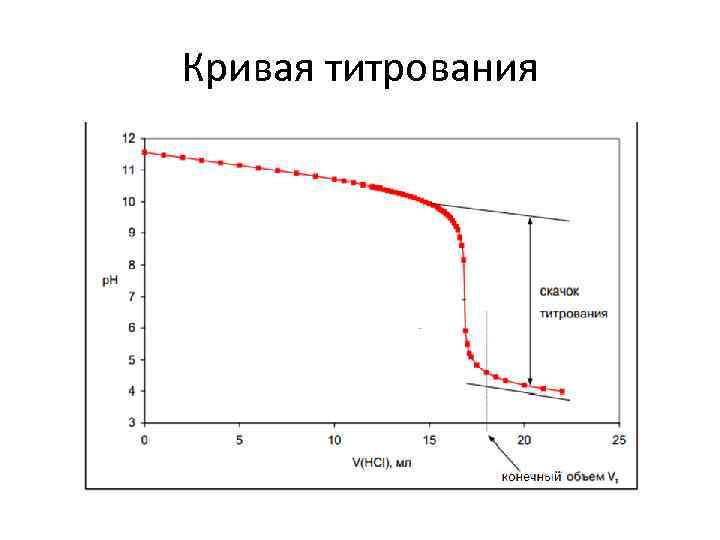 Кривая титрования
Кривая титрования
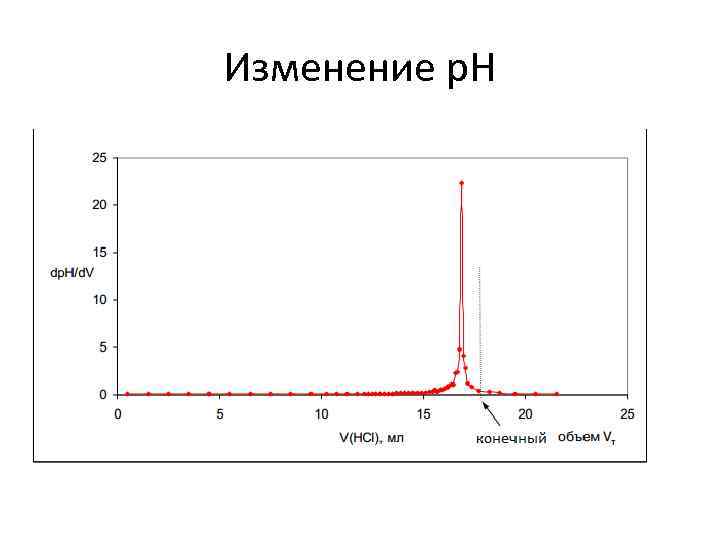 Изменение p. H
Изменение p. H
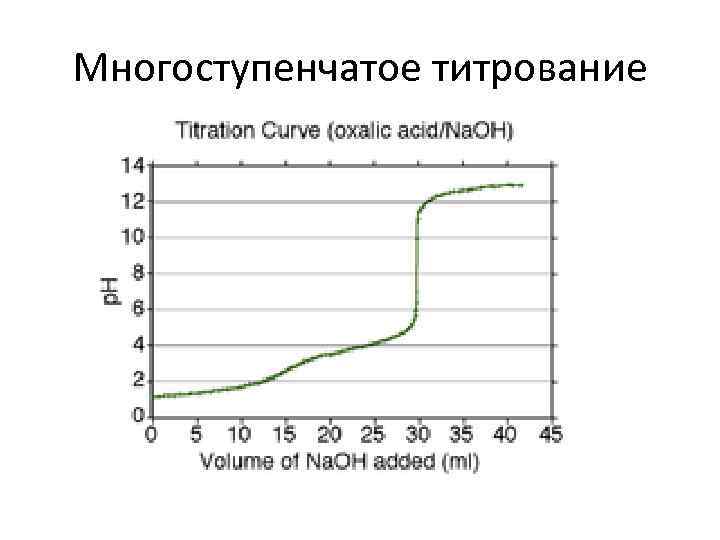 Многоступенчатое титрование
Многоступенчатое титрование


