общ. хим.1.1 Vvedenie_Predmet_khimii.ppt
- Количество слайдов: 19
 Введение. Предмет и основные понятия химии Лекция 1 по курсу «Общая химия»
Введение. Предмет и основные понятия химии Лекция 1 по курсу «Общая химия»
 Основная литература по курсу Н. Л. Глинка. Общая химия. Интегралпресс, 2006 Н. С. Ахметов. Общая и неорганическая химия. Высшая школа, 2001 Карапетьянц М. Х. Дракин С. И. Общая и неорганическая химия Химия, 1992 Неорганическая химия, т. 1. Физико-химические основы неорганической химии Под ред. Ю. Д. Третьякова Академия, 2004
Основная литература по курсу Н. Л. Глинка. Общая химия. Интегралпресс, 2006 Н. С. Ахметов. Общая и неорганическая химия. Высшая школа, 2001 Карапетьянц М. Х. Дракин С. И. Общая и неорганическая химия Химия, 1992 Неорганическая химия, т. 1. Физико-химические основы неорганической химии Под ред. Ю. Д. Третьякова Академия, 2004
 Литература к практикуму • Общая химия: введение в химический эксперимент: лаборатор. практикум / Е. Н. Мицкевич, Е. Б. Окаев. – Минск: БГПУ, 2008. • Синтезы неорганических веществ: лаборатор. практикум / Е. Н. Мицкевич, Е. Б. Окаев, С. Ю. Елисеев. – Минск: БГПУ, 2010. • Методы решения задач по общей химии: учеб. пособие / Е. И. Василевская, Т. В. Свиридова. – Минск : Вышэйш. шк. , 2007. • Большой химический справочник. / А. И. Волков, И. М. Жарский – Минск: Современная школа, 2005. • Краткий химический справочник / В. А. Рабинович, З. Я. Хавин – Л. : Химия, 1991.
Литература к практикуму • Общая химия: введение в химический эксперимент: лаборатор. практикум / Е. Н. Мицкевич, Е. Б. Окаев. – Минск: БГПУ, 2008. • Синтезы неорганических веществ: лаборатор. практикум / Е. Н. Мицкевич, Е. Б. Окаев, С. Ю. Елисеев. – Минск: БГПУ, 2010. • Методы решения задач по общей химии: учеб. пособие / Е. И. Василевская, Т. В. Свиридова. – Минск : Вышэйш. шк. , 2007. • Большой химический справочник. / А. И. Волков, И. М. Жарский – Минск: Современная школа, 2005. • Краткий химический справочник / В. А. Рабинович, З. Я. Хавин – Л. : Химия, 1991.
 Дополнительная литература • Химия в таблицах и схемах / Ф. Ф. Лахвич, О. М. Травникова. – Минск: Аверсэв, 2009. • Общая химия в формулах, определениях, схемах / И. Е. Шиманович, М. Л. Павлович, В. Ф. Тикавый, П. М. Малашко. – Минск: Университетское, 1996. • Современный курс общей химии: в 2 -х т. / К. Хаускрофт, Э. Констебл. – М. : Мир, 2002.
Дополнительная литература • Химия в таблицах и схемах / Ф. Ф. Лахвич, О. М. Травникова. – Минск: Аверсэв, 2009. • Общая химия в формулах, определениях, схемах / И. Е. Шиманович, М. Л. Павлович, В. Ф. Тикавый, П. М. Малашко. – Минск: Университетское, 1996. • Современный курс общей химии: в 2 -х т. / К. Хаускрофт, Э. Констебл. – М. : Мир, 2002.
 Что нужно иметь при себе на занятиях по химии • На лекциях: Периодическая система, ручка, конспект (или вместо них нетбук) • На лабораторных занятиях, кроме этого: • Обязательно: халат, полуобщую тетрадь для лабораторных, инженерный калькулятор, пособие (№ 1, 2 из списка) • Желательно: таблицу растворимости, ряд напряжений металлов, мыло, полотенце, тонкие резиновые перчатки
Что нужно иметь при себе на занятиях по химии • На лекциях: Периодическая система, ручка, конспект (или вместо них нетбук) • На лабораторных занятиях, кроме этого: • Обязательно: халат, полуобщую тетрадь для лабораторных, инженерный калькулятор, пособие (№ 1, 2 из списка) • Желательно: таблицу растворимости, ряд напряжений металлов, мыло, полотенце, тонкие резиновые перчатки
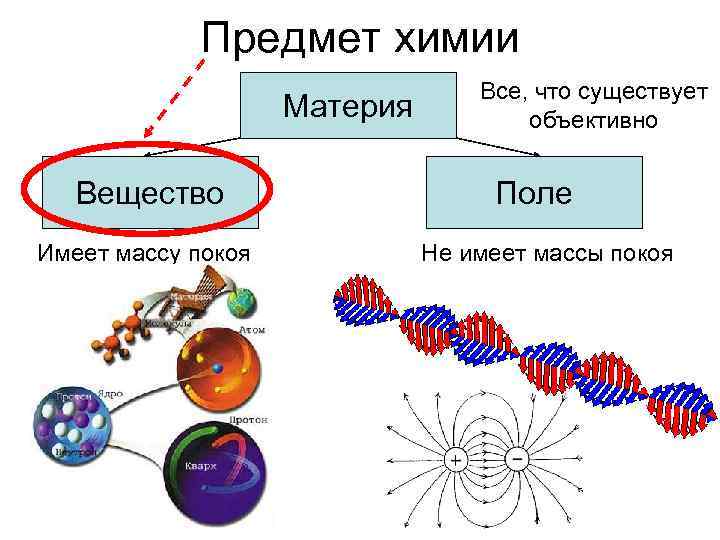 Предмет химии Материя Вещество Имеет массу покоя Все, что существует объективно Поле Не имеет массы покоя
Предмет химии Материя Вещество Имеет массу покоя Все, что существует объективно Поле Не имеет массы покоя
 Химическое вещество Устойчивая совокупность химических частиц, обладающая: • Определенным химическим составом (определенные химические частицы в заданном соотношении) • Определенной структурой (порядком взаимного расположения и соединения этих частиц) • Определенным набором физических и химических свойств СОСТАВ + СТРУКТУРА СВОЙСТВА
Химическое вещество Устойчивая совокупность химических частиц, обладающая: • Определенным химическим составом (определенные химические частицы в заданном соотношении) • Определенной структурой (порядком взаимного расположения и соединения этих частиц) • Определенным набором физических и химических свойств СОСТАВ + СТРУКТУРА СВОЙСТВА
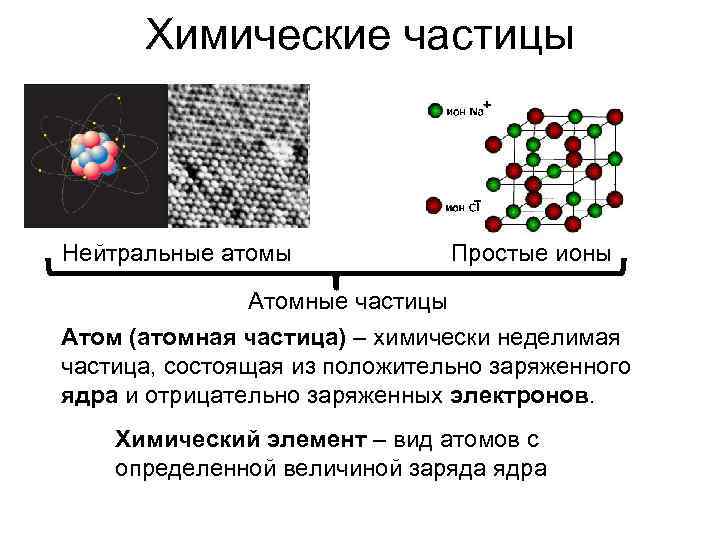 Химические частицы Нейтральные атомы Простые ионы Атомные частицы Атом (атомная частица) – химически неделимая частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов. Химический элемент – вид атомов с определенной величиной заряда ядра
Химические частицы Нейтральные атомы Простые ионы Атомные частицы Атом (атомная частица) – химически неделимая частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов. Химический элемент – вид атомов с определенной величиной заряда ядра
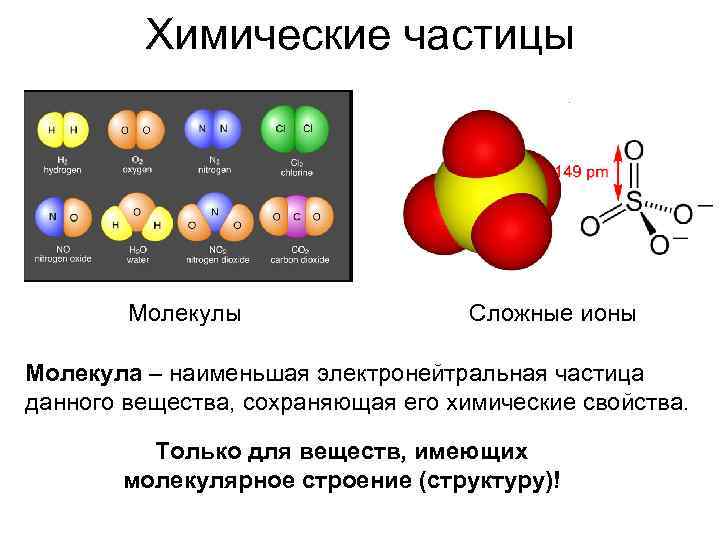 Химические частицы Молекулы Сложные ионы Молекула – наименьшая электронейтральная частица данного вещества, сохраняющая его химические свойства. Только для веществ, имеющих молекулярное строение (структуру)!
Химические частицы Молекулы Сложные ионы Молекула – наименьшая электронейтральная частица данного вещества, сохраняющая его химические свойства. Только для веществ, имеющих молекулярное строение (структуру)!
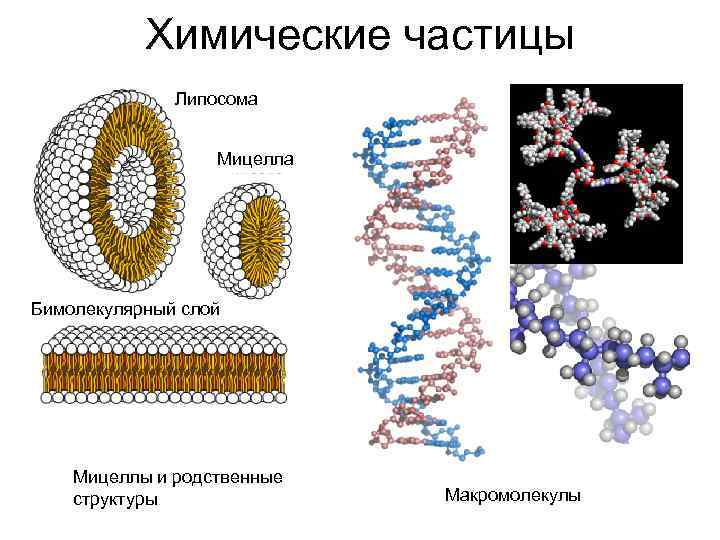 Химические частицы Липосома Мицелла Бимолекулярный слой Мицеллы и родственные структуры Макромолекулы
Химические частицы Липосома Мицелла Бимолекулярный слой Мицеллы и родственные структуры Макромолекулы
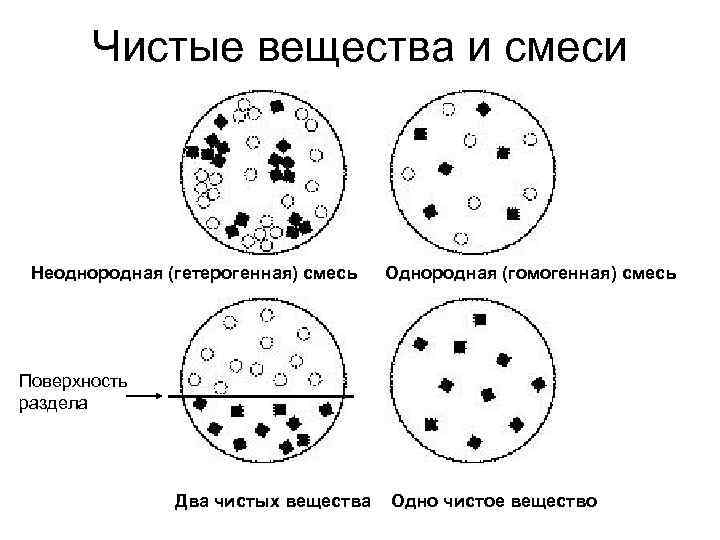 Чистые вещества и смеси Неоднородная (гетерогенная) смесь Однородная (гомогенная) смесь Поверхность раздела Два чистых вещества Одно чистое вещество
Чистые вещества и смеси Неоднородная (гетерогенная) смесь Однородная (гомогенная) смесь Поверхность раздела Два чистых вещества Одно чистое вещество
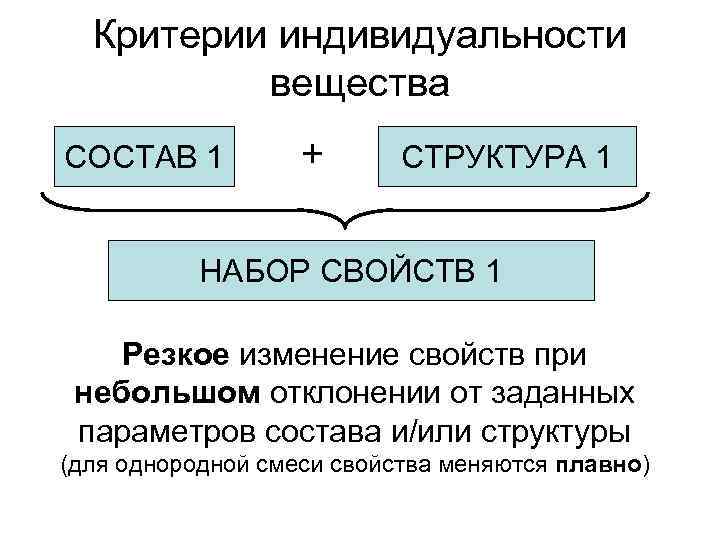 Критерии индивидуальности вещества СОСТАВ 1 + СТРУКТУРА 1 НАБОР СВОЙСТВ 1 Резкое изменение свойств при небольшом отклонении от заданных параметров состава и/или структуры (для однородной смеси свойства меняются плавно)
Критерии индивидуальности вещества СОСТАВ 1 + СТРУКТУРА 1 НАБОР СВОЙСТВ 1 Резкое изменение свойств при небольшом отклонении от заданных параметров состава и/или структуры (для однородной смеси свойства меняются плавно)
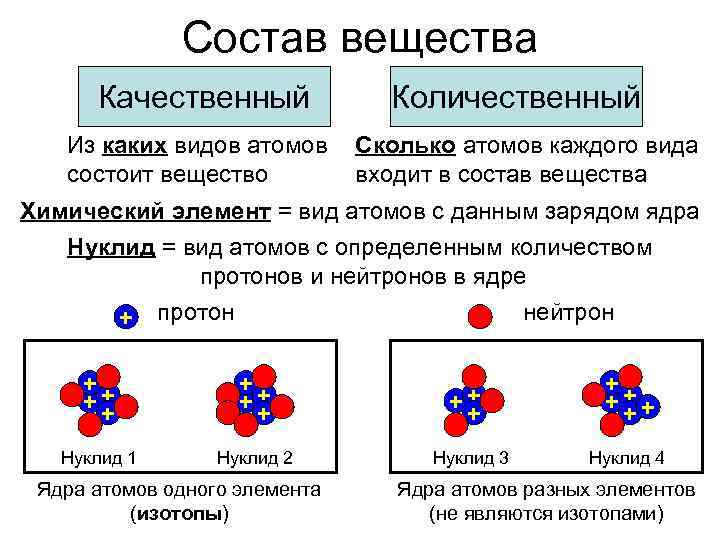 Состав вещества Качественный Количественный Из каких видов атомов Сколько атомов каждого вида состоит вещество входит в состав вещества Химический элемент = вид атомов с данным зарядом ядра Нуклид = вид атомов с определенным количеством протонов и нейтронов в ядре нейтрон + протон ++ ++ Нуклид 1 Нуклид 2 Ядра атомов одного элемента (изотопы) ++ + Нуклид 3 ++ +++ Нуклид 4 Ядра атомов разных элементов (не являются изотопами)
Состав вещества Качественный Количественный Из каких видов атомов Сколько атомов каждого вида состоит вещество входит в состав вещества Химический элемент = вид атомов с данным зарядом ядра Нуклид = вид атомов с определенным количеством протонов и нейтронов в ядре нейтрон + протон ++ ++ Нуклид 1 Нуклид 2 Ядра атомов одного элемента (изотопы) ++ + Нуклид 3 ++ +++ Нуклид 4 Ядра атомов разных элементов (не являются изотопами)
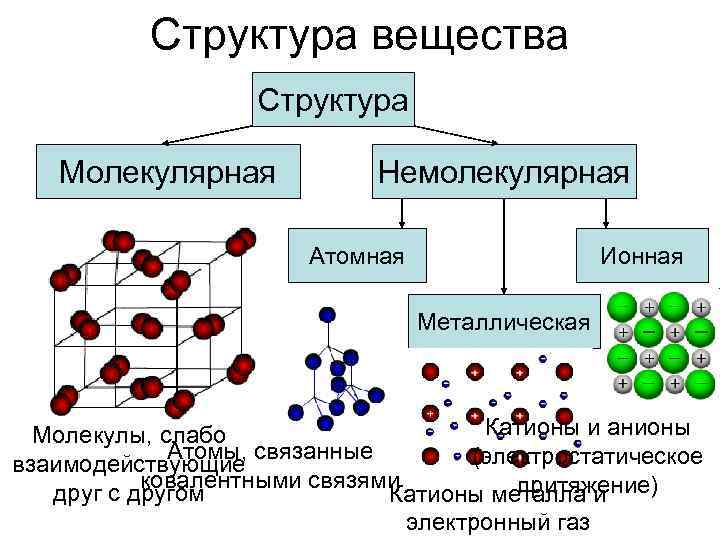 Структура вещества Структура Молекулярная Немолекулярная Атомная Ионная Металлическая Катионы и анионы Молекулы, слабо Атомы, связанные (электростатическое взаимодействующие ковалентными связями притяжение) друг с другом Катионы металла и электронный газ
Структура вещества Структура Молекулярная Немолекулярная Атомная Ионная Металлическая Катионы и анионы Молекулы, слабо Атомы, связанные (электростатическое взаимодействующие ковалентными связями притяжение) друг с другом Катионы металла и электронный газ
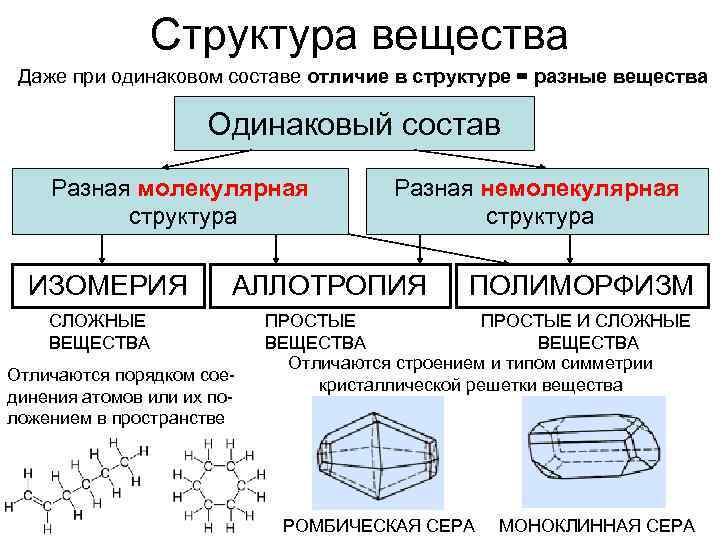 Структура вещества Даже при одинаковом составе отличие в структуре = разные вещества Одинаковый состав Разная молекулярная структура ИЗОМЕРИЯ Разная немолекулярная структура АЛЛОТРОПИЯ СЛОЖНЫЕ ВЕЩЕСТВА Отличаются порядком соединения атомов или их положением в пространстве ПОЛИМОРФИЗМ ПРОСТЫЕ И СЛОЖНЫЕ ВЕЩЕСТВА Отличаются строением и типом симметрии кристаллической решетки вещества РОМБИЧЕСКАЯ СЕРА МОНОКЛИННАЯ СЕРА
Структура вещества Даже при одинаковом составе отличие в структуре = разные вещества Одинаковый состав Разная молекулярная структура ИЗОМЕРИЯ Разная немолекулярная структура АЛЛОТРОПИЯ СЛОЖНЫЕ ВЕЩЕСТВА Отличаются порядком соединения атомов или их положением в пространстве ПОЛИМОРФИЗМ ПРОСТЫЕ И СЛОЖНЫЕ ВЕЩЕСТВА Отличаются строением и типом симметрии кристаллической решетки вещества РОМБИЧЕСКАЯ СЕРА МОНОКЛИННАЯ СЕРА
 Свойства вещества ФИЗИЧЕСКИЕ СВОЙСТВА Индивидуальность вещества сохраняется ХИМИЧЕСКИЕ СВОЙСТВА Образуется новое вещество (вещества) Характерны только для вещества в целом, но не для отдельных химических частиц Характерны как для вещества в целом, так и для отдельных химических частиц Температура плавления Температура кипения Показатель преломления Плотность и т. д. Химическое взаимодействие с веществами различных классов МОЖНО ЗАПИСАТЬ УРАВНЕНИЕ РЕАКЦИИ!
Свойства вещества ФИЗИЧЕСКИЕ СВОЙСТВА Индивидуальность вещества сохраняется ХИМИЧЕСКИЕ СВОЙСТВА Образуется новое вещество (вещества) Характерны только для вещества в целом, но не для отдельных химических частиц Характерны как для вещества в целом, так и для отдельных химических частиц Температура плавления Температура кипения Показатель преломления Плотность и т. д. Химическое взаимодействие с веществами различных классов МОЖНО ЗАПИСАТЬ УРАВНЕНИЕ РЕАКЦИИ!
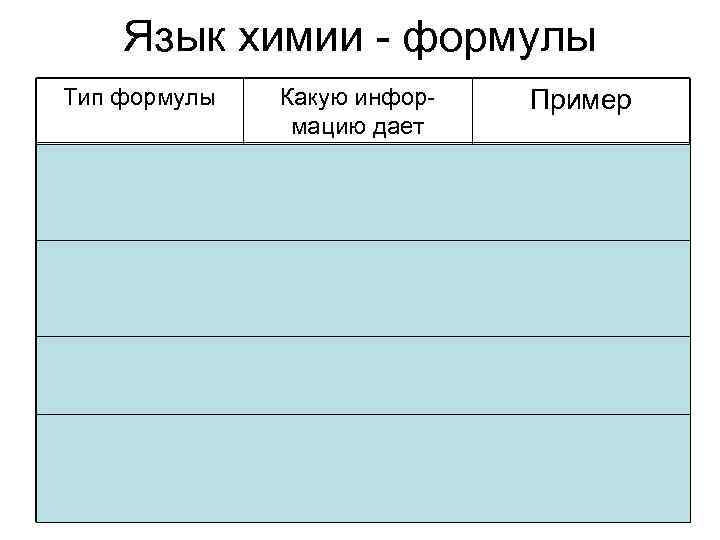 Язык химии - формулы Тип формулы Какую информацию дает Пример Простейшая (эмпирическая) Соотношение атомов разных элементов в составе вещества (ТОЛЬКО СОСТАВ) СH 2 Молекулярная +Точное количество атомов каждого элемента в составе молекулы (ТОЛЬКО СОСТАВ) C 4 H 8 Структурная +Порядок соединения атомов (СОСТАВ + СТРУКТУРА) CН 3–CH=CH–СН 3 Пространственная +Взаимное расположение атомов в пространстве (СОСТАВ + СТРУКТУРА)
Язык химии - формулы Тип формулы Какую информацию дает Пример Простейшая (эмпирическая) Соотношение атомов разных элементов в составе вещества (ТОЛЬКО СОСТАВ) СH 2 Молекулярная +Точное количество атомов каждого элемента в составе молекулы (ТОЛЬКО СОСТАВ) C 4 H 8 Структурная +Порядок соединения атомов (СОСТАВ + СТРУКТУРА) CН 3–CH=CH–СН 3 Пространственная +Взаимное расположение атомов в пространстве (СОСТАВ + СТРУКТУРА)
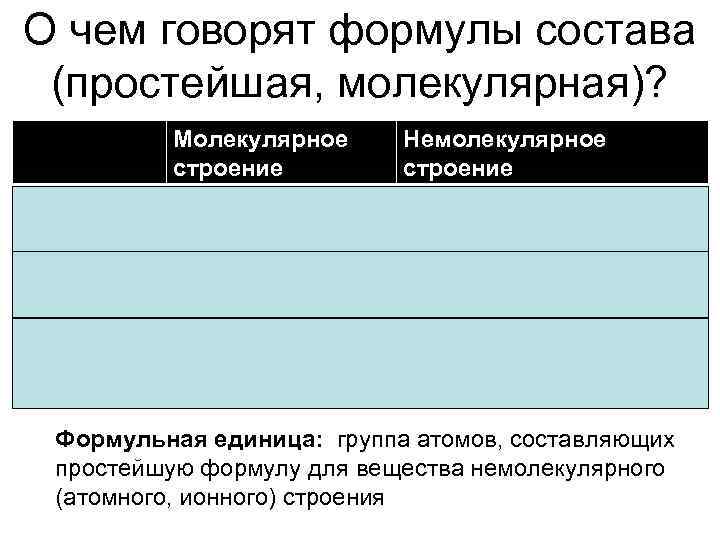 О чем говорят формулы состава (простейшая, молекулярная)? Тип формулы Молекулярное строение Молекулярная Немолекулярное строение Простейшая (эмпирическая) Что показывает Состав молекулы Соотношение элементов в формульной единице Пример H 2 SO 4: в молекуле Na 2 CO 3: в веществе на 2 2 атома H, 1 атома Na приходится 1 S, 4 атома O. атом C и 3 атома O. Формульная единица: группа атомов, составляющих простейшую формулу для вещества немолекулярного (атомного, ионного) строения
О чем говорят формулы состава (простейшая, молекулярная)? Тип формулы Молекулярное строение Молекулярная Немолекулярное строение Простейшая (эмпирическая) Что показывает Состав молекулы Соотношение элементов в формульной единице Пример H 2 SO 4: в молекуле Na 2 CO 3: в веществе на 2 2 атома H, 1 атома Na приходится 1 S, 4 атома O. атом C и 3 атома O. Формульная единица: группа атомов, составляющих простейшую формулу для вещества немолекулярного (атомного, ионного) строения
 Применимость формул • Простейшие – для большинства веществ немолекулярного строения • Молекулярные – в основном для неорганических веществ молекулярного строения • Структурные и пространственные – для большинства органических веществ (причина – изомерия!) Количество изомеров для данного состава C 7 H 16 C 14 H 30 C 20 H 42 9 1885 >366 000!
Применимость формул • Простейшие – для большинства веществ немолекулярного строения • Молекулярные – в основном для неорганических веществ молекулярного строения • Структурные и пространственные – для большинства органических веществ (причина – изомерия!) Количество изомеров для данного состава C 7 H 16 C 14 H 30 C 20 H 42 9 1885 >366 000!


