ЛК-1, Химия, 1 курс-2012.ppt
- Количество слайдов: 36
 Введение. Основные законы и понятия химии 13. 09. 2012
Введение. Основные законы и понятия химии 13. 09. 2012
 Темы для самостоятельного изучения 1. 2. 3. Метод валентных связей Зонная теория кристаллов. Металлические, ковалентные, ионные, молекулярные кристаллы. Растворы. Твердые, жидкие и газовые растворы. Способы выражения концентраций растворов. Рекомендуемая литература 1. Н. С. Ахметов. Общая и неорганическая химия. 7 -ое изд. -М. : Высшая школа. , 2006 -743 с. 2. Глинка Н. Л. Общая химия (любое издание).
Темы для самостоятельного изучения 1. 2. 3. Метод валентных связей Зонная теория кристаллов. Металлические, ковалентные, ионные, молекулярные кристаллы. Растворы. Твердые, жидкие и газовые растворы. Способы выражения концентраций растворов. Рекомендуемая литература 1. Н. С. Ахметов. Общая и неорганическая химия. 7 -ое изд. -М. : Высшая школа. , 2006 -743 с. 2. Глинка Н. Л. Общая химия (любое издание).
 Основные понятия химии
Основные понятия химии
 Основные понятия химии • Вещество – вид материи (или формы материи), дискретные частицы которой обладают конечной массой покоя, т. е. массой частиц в неподвижном состоянии. • К веществу относятся многие элементарные частицы (электроны, протоны, нейтроны и др. ), а также образованные из них ядра атомов, атомы, молекулы, ионы, кристаллы и др. • Скорость движения в пространстве частиц, представляющих вещество, не может достигать скорости света (с=3. 00· 108 м/с). • Всем частицам вещества, например, электронам, присущи не только корпускулярные, но и волновые свойства.
Основные понятия химии • Вещество – вид материи (или формы материи), дискретные частицы которой обладают конечной массой покоя, т. е. массой частиц в неподвижном состоянии. • К веществу относятся многие элементарные частицы (электроны, протоны, нейтроны и др. ), а также образованные из них ядра атомов, атомы, молекулы, ионы, кристаллы и др. • Скорость движения в пространстве частиц, представляющих вещество, не может достигать скорости света (с=3. 00· 108 м/с). • Всем частицам вещества, например, электронам, присущи не только корпускулярные, но и волновые свойства.
 Основные понятия химии • Поля формы материи, дискретные частицы (кванты) которых не имеют массы покоя. • Так, электромагнитным полям соответствуют дискретные частицы – фотоны, гравитационным полям – гравитоны (гипотетические частицы). • Масса покоя фотонов и гравитонов равна нулю, т. к. невозможно найти систему отсчета, в которой эти частицы покоятся. Их скорость равна скорости света. • Частицы поля и вещества находятся в неразрывной связи друг с другом. Например, электромагнитное поле осуществляет взаимодействие между электрически заряженными частицами.
Основные понятия химии • Поля формы материи, дискретные частицы (кванты) которых не имеют массы покоя. • Так, электромагнитным полям соответствуют дискретные частицы – фотоны, гравитационным полям – гравитоны (гипотетические частицы). • Масса покоя фотонов и гравитонов равна нулю, т. к. невозможно найти систему отсчета, в которой эти частицы покоятся. Их скорость равна скорости света. • Частицы поля и вещества находятся в неразрывной связи друг с другом. Например, электромагнитное поле осуществляет взаимодействие между электрически заряженными частицами.
 Основные понятия Вещество - это конкретный вид материи, обладающий определенными физическими и химическими свойствами, состав которого может быть выражен химической формулой Вещество-форма материи, в отличие от поля, обладающая, массой покоя Каждому веществу присущ набор специфических свойств — объективных характеристик, которые определяют индивидуальность конкретного вещества и тем самым позволяют отличить его от всех других веществ. К наиболее характерным физико-химическим свойствам относятся константы — плотность, температура плавления, температура кипения, термодинамические характеристики, параметры кристаллической структуры. К основным характеристикам вещества принадлежат его химические свойства.
Основные понятия Вещество - это конкретный вид материи, обладающий определенными физическими и химическими свойствами, состав которого может быть выражен химической формулой Вещество-форма материи, в отличие от поля, обладающая, массой покоя Каждому веществу присущ набор специфических свойств — объективных характеристик, которые определяют индивидуальность конкретного вещества и тем самым позволяют отличить его от всех других веществ. К наиболее характерным физико-химическим свойствам относятся константы — плотность, температура плавления, температура кипения, термодинамические характеристики, параметры кристаллической структуры. К основным характеристикам вещества принадлежат его химические свойства.
 Предмет и назначение химии
Предмет и назначение химии
 Основные понятия химии Химия – наука о веществах и их превращениях (химических реакциях), сопровождающихся изменением состава и структуры веществ. Химия – наука о превращениях веществ, связанных с изменением электронного окружения атомных ядер
Основные понятия химии Химия – наука о веществах и их превращениях (химических реакциях), сопровождающихся изменением состава и структуры веществ. Химия – наука о превращениях веществ, связанных с изменением электронного окружения атомных ядер
 Основные понятия химии Химический элемент– есть вещество, которое не может разлагаться при химических реакциях на более простые вещества. Их обозначают символами: H, N, O, S, Fe и т. д. Каждый элемент состоит из одного вида атомов, характеризующихся одинаковым зарядом ядра. Химические реакции не приводят к переходу одного элемента в другой. Такие превращения протекают в ходе ядерных реакций. Химические элементы входят в состав простых веществ и соединений. Химический элемент – совокупность атомов с одинаковым зарядом ядра.
Основные понятия химии Химический элемент– есть вещество, которое не может разлагаться при химических реакциях на более простые вещества. Их обозначают символами: H, N, O, S, Fe и т. д. Каждый элемент состоит из одного вида атомов, характеризующихся одинаковым зарядом ядра. Химические реакции не приводят к переходу одного элемента в другой. Такие превращения протекают в ходе ядерных реакций. Химические элементы входят в состав простых веществ и соединений. Химический элемент – совокупность атомов с одинаковым зарядом ядра.
 Основные понятия химии • Химический элемент (E) – совокупность атомов с определенным зарядом ядра Z, который равен числу содержащихся в ядре протонов. • Число Z определяет также порядковый номер элемента в периодической системе химических элементов.
Основные понятия химии • Химический элемент (E) – совокупность атомов с определенным зарядом ядра Z, который равен числу содержащихся в ядре протонов. • Число Z определяет также порядковый номер элемента в периодической системе химических элементов.
 Карточка химического элемента 1 — обозначение химического элемента. 2 — русское название. 3 — порядковый номер химического элемента, равный количеству протонов в атоме. 4 — атомная масса. 5 — распределение электронов по энергетическим уровням. 6 — электронная конфигурация.
Карточка химического элемента 1 — обозначение химического элемента. 2 — русское название. 3 — порядковый номер химического элемента, равный количеству протонов в атоме. 4 — атомная масса. 5 — распределение электронов по энергетическим уровням. 6 — электронная конфигурация.
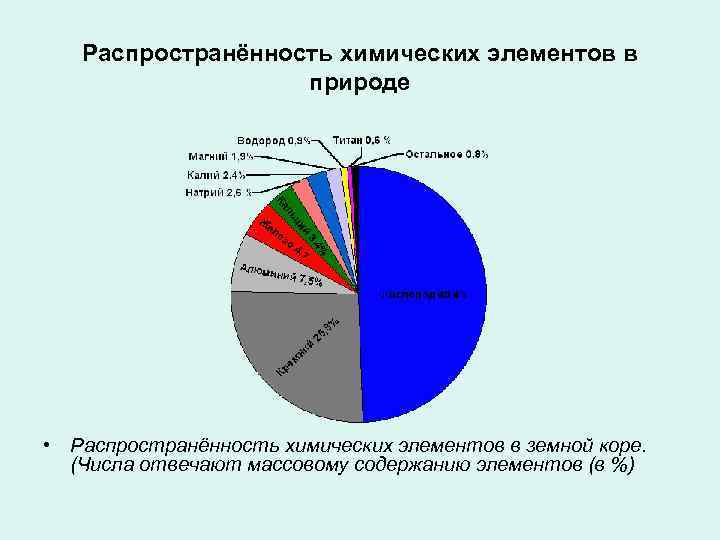 Распространённость химических элементов в природе • Распространённость химических элементов в земной коре. (Числа отвечают массовому содержанию элементов (в %)
Распространённость химических элементов в природе • Распространённость химических элементов в земной коре. (Числа отвечают массовому содержанию элементов (в %)
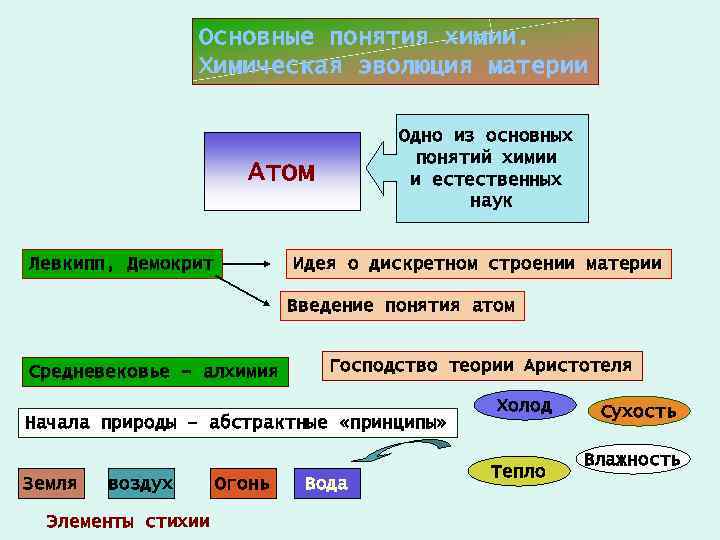 Основные понятия химии. Химическая эволюция материи Одно из основных понятий химии и естественных наук Атом Левкипп, Демокрит Идея о дискретном строении материи Введение понятия атом Средневековье - алхимия Господство теории Аристотеля Начала природы – абстрактные «принципы» Земля воздух Элементы стихии Огонь Вода Холод Тепло Сухость Влажность
Основные понятия химии. Химическая эволюция материи Одно из основных понятий химии и естественных наук Атом Левкипп, Демокрит Идея о дискретном строении материи Введение понятия атом Средневековье - алхимия Господство теории Аристотеля Начала природы – абстрактные «принципы» Земля воздух Элементы стихии Огонь Вода Холод Тепло Сухость Влажность
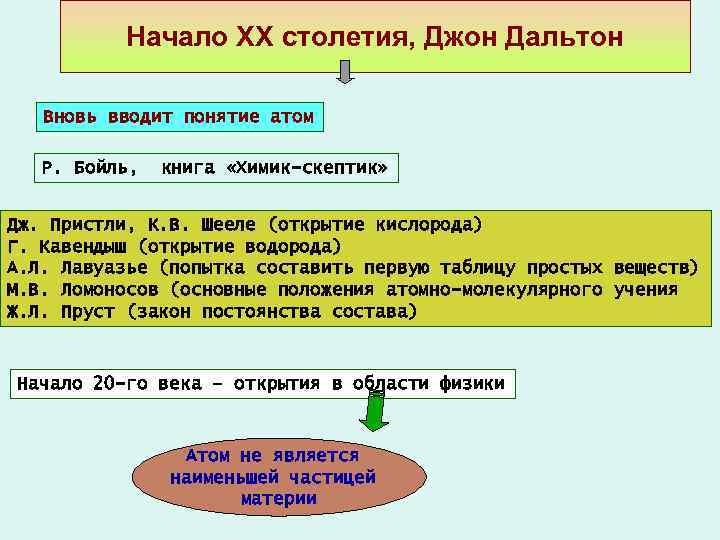 Начало XX столетия, Джон Дальтон Вновь вводит понятие атом Р. Бойль, книга «Химик-скептик» Дж. Пристли, К. В. Шееле (открытие кислорода) Г. Кавендыш (открытие водорода) А. Л. Лавуазье (попытка составить первую таблицу простых веществ) М. В. Ломоносов (основные положения атомно-молекулярного учения Ж. Л. Пруст (закон постоянства состава) Начало 20 -го века – открытия в области физики Атом не является наименьшей частицей материи
Начало XX столетия, Джон Дальтон Вновь вводит понятие атом Р. Бойль, книга «Химик-скептик» Дж. Пристли, К. В. Шееле (открытие кислорода) Г. Кавендыш (открытие водорода) А. Л. Лавуазье (попытка составить первую таблицу простых веществ) М. В. Ломоносов (основные положения атомно-молекулярного учения Ж. Л. Пруст (закон постоянства состава) Начало 20 -го века – открытия в области физики Атом не является наименьшей частицей материи
 Атомно-молекулярная теория (М. В. Ломоносов, 1741 г. ) 1. Все вещества состоят из молекул. Молекула – наименьшая частица вещества, обладающая всеми его свойствами. 2. Молекулы состоят из атомов. Атом - наименьшая частица химического элемента, сохраняющая все его свойства. Различным элементам соответствуют различные атомы. 3. Молекулы и атомы находятся в непрерывном движении; между ними существуют силы притяжения и отталкивания. 4. Молекулы простых веществ состоят из одинаковых атомов, молекулы сложных веществ- из различных атомов.
Атомно-молекулярная теория (М. В. Ломоносов, 1741 г. ) 1. Все вещества состоят из молекул. Молекула – наименьшая частица вещества, обладающая всеми его свойствами. 2. Молекулы состоят из атомов. Атом - наименьшая частица химического элемента, сохраняющая все его свойства. Различным элементам соответствуют различные атомы. 3. Молекулы и атомы находятся в непрерывном движении; между ними существуют силы притяжения и отталкивания. 4. Молекулы простых веществ состоят из одинаковых атомов, молекулы сложных веществ- из различных атомов.
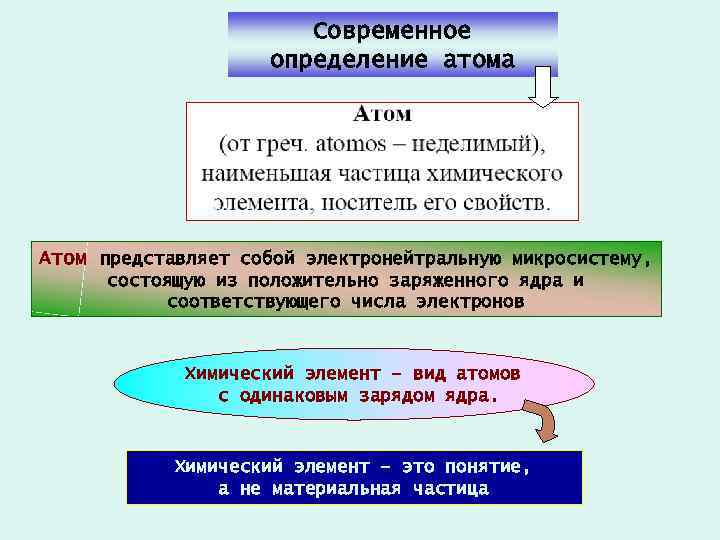 Современное определение атома Атом представляет собой электронейтральную микросистему, состоящую из положительно заряженного ядра и соответствующего числа электронов Химический элемент – вид атомов с одинаковым зарядом ядра. Химический элемент – это понятие, а не материальная частица
Современное определение атома Атом представляет собой электронейтральную микросистему, состоящую из положительно заряженного ядра и соответствующего числа электронов Химический элемент – вид атомов с одинаковым зарядом ядра. Химический элемент – это понятие, а не материальная частица
 Основные понятия химии • Атом- наименьшая химически не делимая частица элемента, сохраняющая его химические свойства. • Атом может существовать как в свободном состоянии ( «изолированный атом» ), так и в соединении с другими атомами, образуя молекулы (в том числе полимерные), ионы, радикалы, кристаллы.
Основные понятия химии • Атом- наименьшая химически не делимая частица элемента, сохраняющая его химические свойства. • Атом может существовать как в свободном состоянии ( «изолированный атом» ), так и в соединении с другими атомами, образуя молекулы (в том числе полимерные), ионы, радикалы, кристаллы.
 Основные понятия химии • Атом является наименьшей частицей химического элемента, носителем его свойств. • Молекула – нейтральная микрочас тица, образованная из двух или большего числа атомов и способная к самостоятельному существованию.
Основные понятия химии • Атом является наименьшей частицей химического элемента, носителем его свойств. • Молекула – нейтральная микрочас тица, образованная из двух или большего числа атомов и способная к самостоятельному существованию.
![Основные понятия Электрон [др. греч. ηλεκτρον – янтарь (хорошо электризуется при трении)] – стабильная Основные понятия Электрон [др. греч. ηλεκτρον – янтарь (хорошо электризуется при трении)] – стабильная](https://present5.com/presentation/3/31722805_129732594.pdf-img/31722805_129732594.pdf-19.jpg) Основные понятия Электрон [др. греч. ηλεκτρον – янтарь (хорошо электризуется при трении)] – стабильная элементарная частица, имеющая массу покоя, равную 9, 109 ⋅ 10– 31 кг = 5, 486 ⋅ 10– 4 а. е. м. , и несущая элементарный отрицательный заряд, равный 1, 6 ⋅ 10– 19 Кл. Заряд электрона принимают за – 1 и заряды всех остальных частиц выражают в этих единицах. Электроны входят в состав всех атомов Протон (греч. πρωτοσ – первый) – элементарная частица, являющаяся составной частью ядер атомов всех химических элементов, обладает массой покоя mp =1, 672 ⋅ 10– 27 кг = 1, 007 а. е. м. и элементарным положительным электрическим зарядом, равным по величине заряду электрона, т. е. 1, 6 ⋅ 10– 19 Кл. определяет порядковый номер химического элемента Число протонов в ядре Порядковый N элемента
Основные понятия Электрон [др. греч. ηλεκτρον – янтарь (хорошо электризуется при трении)] – стабильная элементарная частица, имеющая массу покоя, равную 9, 109 ⋅ 10– 31 кг = 5, 486 ⋅ 10– 4 а. е. м. , и несущая элементарный отрицательный заряд, равный 1, 6 ⋅ 10– 19 Кл. Заряд электрона принимают за – 1 и заряды всех остальных частиц выражают в этих единицах. Электроны входят в состав всех атомов Протон (греч. πρωτοσ – первый) – элементарная частица, являющаяся составной частью ядер атомов всех химических элементов, обладает массой покоя mp =1, 672 ⋅ 10– 27 кг = 1, 007 а. е. м. и элементарным положительным электрическим зарядом, равным по величине заряду электрона, т. е. 1, 6 ⋅ 10– 19 Кл. определяет порядковый номер химического элемента Число протонов в ядре Порядковый N элемента
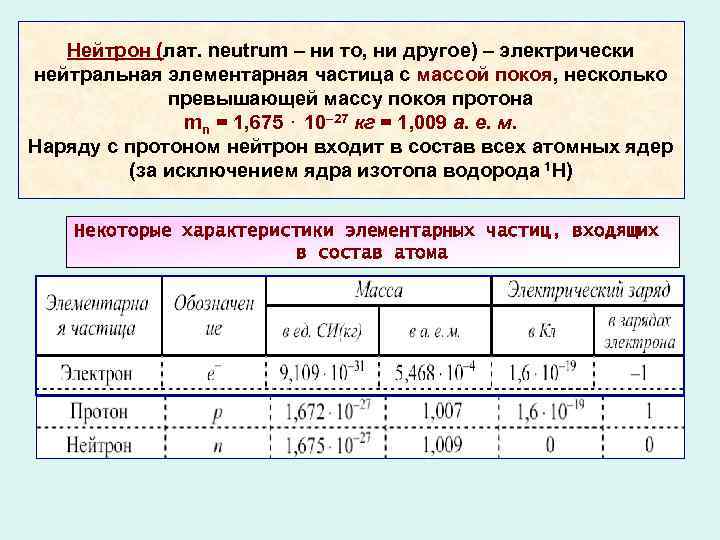 Нейтрон (лат. neutrum – ни то, ни другое) – электрически нейтральная элементарная частица с массой покоя, несколько превышающей массу покоя протона mn = 1, 675 ⋅ 10– 27 кг = 1, 009 а. е. м. Наряду с протоном нейтрон входит в состав всех атомных ядер (за исключением ядра изотопа водорода 1 Н) Некоторые характеристики элементарных частиц, входящих в состав атома
Нейтрон (лат. neutrum – ни то, ни другое) – электрически нейтральная элементарная частица с массой покоя, несколько превышающей массу покоя протона mn = 1, 675 ⋅ 10– 27 кг = 1, 009 а. е. м. Наряду с протоном нейтрон входит в состав всех атомных ядер (за исключением ядра изотопа водорода 1 Н) Некоторые характеристики элементарных частиц, входящих в состав атома
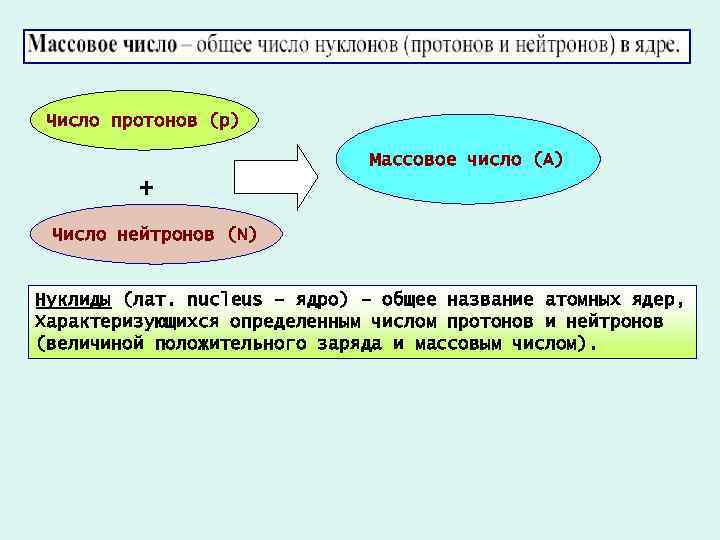 Число протонов (р) Массовое число (А) + Число нейтронов (N) Нуклиды (лат. nucleus – ядро) – общее название атомных ядер, Характеризующихся определенным числом протонов и нейтронов (величиной положительного заряда и массовым числом).
Число протонов (р) Массовое число (А) + Число нейтронов (N) Нуклиды (лат. nucleus – ядро) – общее название атомных ядер, Характеризующихся определенным числом протонов и нейтронов (величиной положительного заряда и массовым числом).
 Основные понятия химии Простые вещества – состоят из химически связанных атомов одного химического элемента. Некоторые химические элементы способны образовывать по нескольку простых веществ, различающихся строением и свойствами. Например, для серы известны простые вещества, построенные из молекул S 8, S 6 и др. Соединения (сложные вещества) , которые являются результатом химического соединения атомов двух или более элементов. Многие соединения составлены из молекул. Состав молекул выражается химическими формулами.
Основные понятия химии Простые вещества – состоят из химически связанных атомов одного химического элемента. Некоторые химические элементы способны образовывать по нескольку простых веществ, различающихся строением и свойствами. Например, для серы известны простые вещества, построенные из молекул S 8, S 6 и др. Соединения (сложные вещества) , которые являются результатом химического соединения атомов двух или более элементов. Многие соединения составлены из молекул. Состав молекул выражается химическими формулами.
 Основные понятия химии Изотопы (греч. ισοζ – одинаковый + τοποζ – место) – нуклиды, имеющие одинаковое число протонов, но различающиеся массовыми числами Изотопы – нуклиды, занимающие одно и то же место в Периодической системе, т. е. атомы одного и того же химического элемента. Например: 2211 Na, 2311 Na , 2411 Na – изотопы натрия.
Основные понятия химии Изотопы (греч. ισοζ – одинаковый + τοποζ – место) – нуклиды, имеющие одинаковое число протонов, но различающиеся массовыми числами Изотопы – нуклиды, занимающие одно и то же место в Периодической системе, т. е. атомы одного и того же химического элемента. Например: 2211 Na, 2311 Na , 2411 Na – изотопы натрия.
 Изобары (греч. ιζο – равный + βαροσ – вес) – нуклиды, имеющие одинаковые массовые числа, но различное число протонов (т. е. относящиеся к различным химическим элементам), например, 90 Sr, 90 Y, 90 Zr. Изотоны – нуклиды с одинаковым числом нейтронов. 1811 г. А. Авогадро, понятие молекулы в 1860 г. , Карлсруэ (Германия), первый международный съезд химиков молекула стала пониматься как мельчайшая частица вещества, участвующая в его химических превращениях Молекула (уменьшительное от лат. moles – масса) – это наименьшая частица вещества, определяющая его свойства. Состоит из атомов одного или нескольких химических элементов и существует как единая система атомных ядер и электронов.
Изобары (греч. ιζο – равный + βαροσ – вес) – нуклиды, имеющие одинаковые массовые числа, но различное число протонов (т. е. относящиеся к различным химическим элементам), например, 90 Sr, 90 Y, 90 Zr. Изотоны – нуклиды с одинаковым числом нейтронов. 1811 г. А. Авогадро, понятие молекулы в 1860 г. , Карлсруэ (Германия), первый международный съезд химиков молекула стала пониматься как мельчайшая частица вещества, участвующая в его химических превращениях Молекула (уменьшительное от лат. moles – масса) – это наименьшая частица вещества, определяющая его свойства. Состоит из атомов одного или нескольких химических элементов и существует как единая система атомных ядер и электронов.
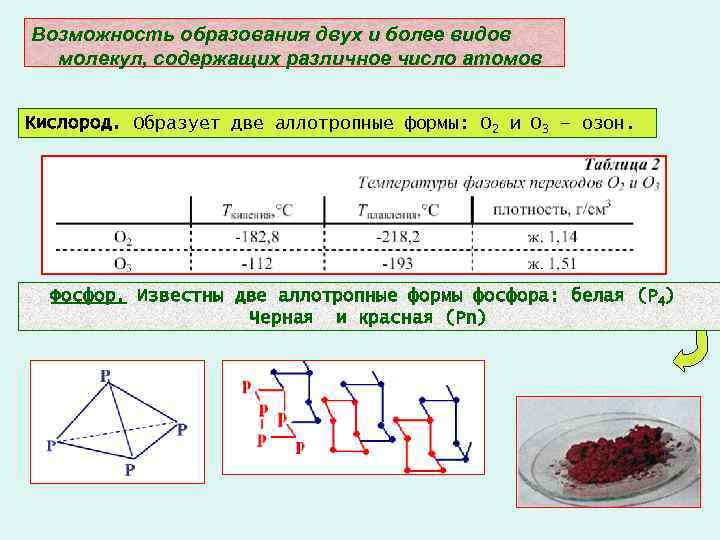 Возможность образования двух и более видов молекул, содержащих различное число атомов Кислород. Образует две аллотропные формы: O 2 и O 3 – озон. Фосфор. Известны две аллотропные формы фосфора: белая (Р 4) Черная и красная (Рn)
Возможность образования двух и более видов молекул, содержащих различное число атомов Кислород. Образует две аллотропные формы: O 2 и O 3 – озон. Фосфор. Известны две аллотропные формы фосфора: белая (Р 4) Черная и красная (Рn)
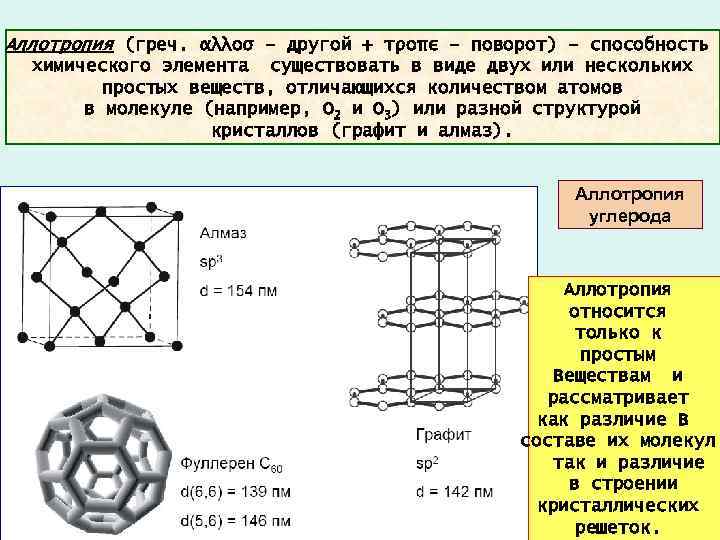 Аллотрoпия (греч. αλλοσ – другой + τροπε – поворот) – способность химического элемента существовать в виде двух или нескольких простых веществ, отличающихся количеством атомов в молекуле (например, O 2 и O 3) или разной структурой кристаллов (графит и алмаз). Аллотропия углерода Аллотропия относится только к простым Веществам и рассматривает как различие В составе их молекул, так и различие в строении кристаллических решеток.
Аллотрoпия (греч. αλλοσ – другой + τροπε – поворот) – способность химического элемента существовать в виде двух или нескольких простых веществ, отличающихся количеством атомов в молекуле (например, O 2 и O 3) или разной структурой кристаллов (графит и алмаз). Аллотропия углерода Аллотропия относится только к простым Веществам и рассматривает как различие В составе их молекул, так и различие в строении кристаллических решеток.
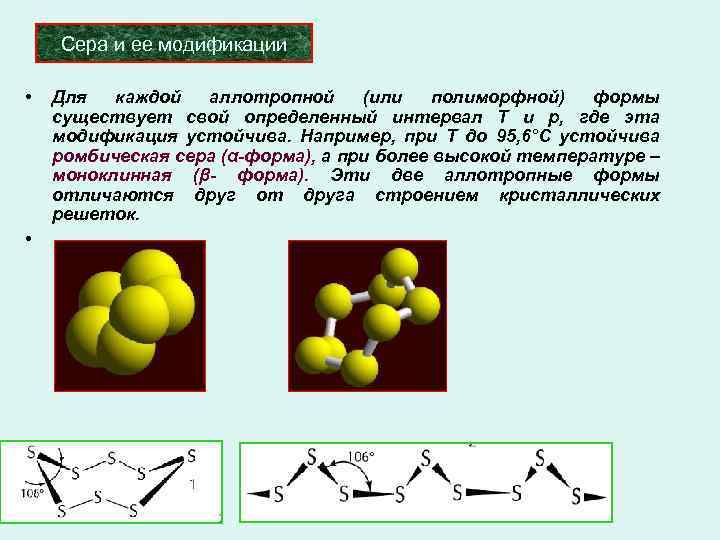 Сера и ее модификации • Для каждой аллотропной (или полиморфной) формы существует свой определенный интервал Т и р, где эта модификация устойчива. Например, при Т до 95, 6°С устойчива ромбическая сера (α-форма), а при более высокой температуре – моноклинная (β- форма). Эти две аллотропные формы отличаются друг от друга строением кристаллических решеток. •
Сера и ее модификации • Для каждой аллотропной (или полиморфной) формы существует свой определенный интервал Т и р, где эта модификация устойчива. Например, при Т до 95, 6°С устойчива ромбическая сера (α-форма), а при более высокой температуре – моноклинная (β- форма). Эти две аллотропные формы отличаются друг от друга строением кристаллических решеток. •
 Изоморфизм (греч. ιζο – равный, подобный + μορϕε – форма) – способность сходных по составу веществ образовывать смешанные кристаллы, в которых близкие по размеру атомы, ионы или атомные группировки случайным образом замещают друга. Например В кристаллах алюмокалиевых квасцов KAl(SO 4)2 ⋅ 12 H 2 O ионы калия могут быть замещены ионами рубидия или аммония, а ионы Al 3+ ионами Cr 3+ или Fe 3+ К+ изоморфны Rb+ или NH 4+, а Al 3+ изоморфны Cr 3+ или Fe 3+
Изоморфизм (греч. ιζο – равный, подобный + μορϕε – форма) – способность сходных по составу веществ образовывать смешанные кристаллы, в которых близкие по размеру атомы, ионы или атомные группировки случайным образом замещают друга. Например В кристаллах алюмокалиевых квасцов KAl(SO 4)2 ⋅ 12 H 2 O ионы калия могут быть замещены ионами рубидия или аммония, а ионы Al 3+ ионами Cr 3+ или Fe 3+ К+ изоморфны Rb+ или NH 4+, а Al 3+ изоморфны Cr 3+ или Fe 3+
 Количественные соотношения в химии • для выражения масс атомов и молекул используют единицу измерения – атомную единицу массы (а. е. м. ). За атомную единицу массы принята 1 / 12 массы нуклида углерода 12 C. Масса нуклида в единицах СИ = 1, 9927 ⋅ 10– 26 кг. Относительная атомная масса Ar (устаревший термин – атомный вес) – масса атома, выраженная в атомных единицах массы (а. е. м. ). За относительную атомную массу элемента принимают среднее значение относительной атомной массы природной смеси его изотопов с учетом их содержания в земных условиях. Именно эти значения и приведены в Периодической системе.
Количественные соотношения в химии • для выражения масс атомов и молекул используют единицу измерения – атомную единицу массы (а. е. м. ). За атомную единицу массы принята 1 / 12 массы нуклида углерода 12 C. Масса нуклида в единицах СИ = 1, 9927 ⋅ 10– 26 кг. Относительная атомная масса Ar (устаревший термин – атомный вес) – масса атома, выраженная в атомных единицах массы (а. е. м. ). За относительную атомную массу элемента принимают среднее значение относительной атомной массы природной смеси его изотопов с учетом их содержания в земных условиях. Именно эти значения и приведены в Периодической системе.
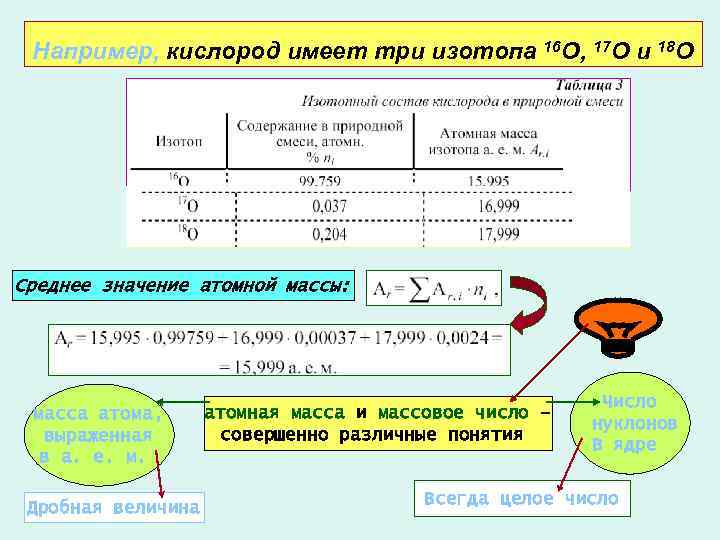 Например, кислород имеет три изотопа 16 O, 17 O и 18 O Среднее значение атомной массы: масса атома, выраженная в а. е. м. Дробная величина атомная масса и массовое число – совершенно различные понятия Число нуклонов В ядре Всегда целое число
Например, кислород имеет три изотопа 16 O, 17 O и 18 O Среднее значение атомной массы: масса атома, выраженная в а. е. м. Дробная величина атомная масса и массовое число – совершенно различные понятия Число нуклонов В ядре Всегда целое число
 Молекулярная масса – масса молекулы, выраженная в а. е. м. Моль (ν)– единица измерения количества вещества. 1 моль – это такое количество вещества, в котором содержится столько же структурных единиц (атомов, молекул, ионов, радикалов), сколько атомов содержится в 0, 012 кг изотопа углерода 12 C, а именно – NA = 6, 022 ⋅ 1023 моль– 1 Молярная масса вещества (М) равна отношению массы этого вещества (m) к его количеству (ν) , выражается в г/моль
Молекулярная масса – масса молекулы, выраженная в а. е. м. Моль (ν)– единица измерения количества вещества. 1 моль – это такое количество вещества, в котором содержится столько же структурных единиц (атомов, молекул, ионов, радикалов), сколько атомов содержится в 0, 012 кг изотопа углерода 12 C, а именно – NA = 6, 022 ⋅ 1023 моль– 1 Молярная масса вещества (М) равна отношению массы этого вещества (m) к его количеству (ν) , выражается в г/моль
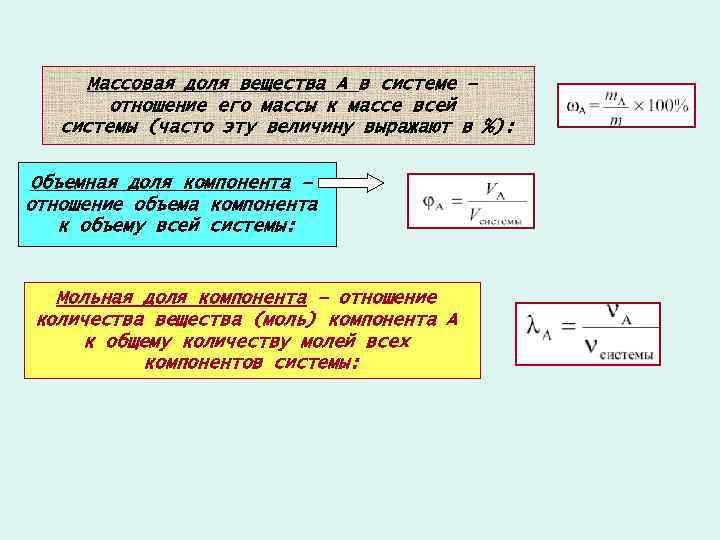 Массовая доля вещества A в системе – отношение его массы к массе всей системы (часто эту величину выражают в %): Объемная доля компонента – отношение объема компонента к объему всей системы: Мольная доля компонента – отношение количества вещества (моль) компонента A к общему количеству молей всех компонентов системы:
Массовая доля вещества A в системе – отношение его массы к массе всей системы (часто эту величину выражают в %): Объемная доля компонента – отношение объема компонента к объему всей системы: Мольная доля компонента – отношение количества вещества (моль) компонента A к общему количеству молей всех компонентов системы:
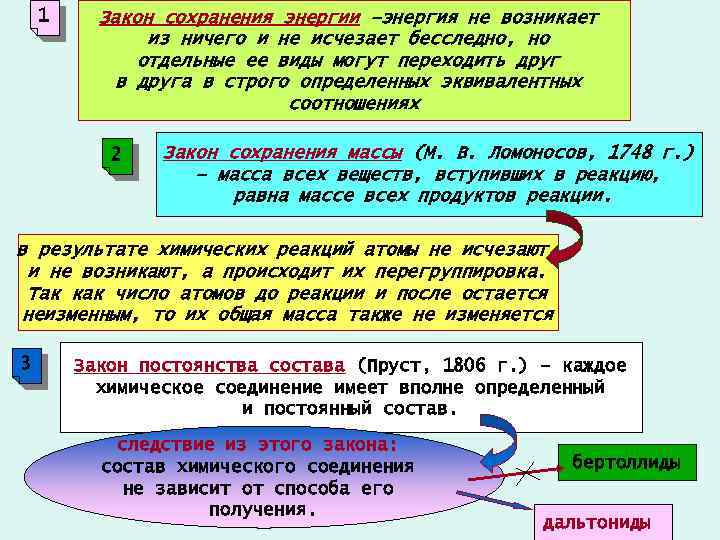 1 Закон сохранения энергии –энергия не возникает из ничего и не исчезает бесследно, но отдельные ее виды могут переходить друг в друга в строго определенных эквивалентных соотношениях 2 Закон сохранения массы (М. В. Ломоносов, 1748 г. ) – масса всех веществ, вступивших в реакцию, равна массе всех продуктов реакции. в результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка. Так как число атомов до реакции и после остается неизменным, то их общая масса также не изменяется 3 Закон постоянства состава (Пруст, 1806 г. ) – каждое химическое соединение имеет вполне определенный и постоянный состав. следствие из этого закона: состав химического соединения не зависит от способа его получения. бертоллиды дальтониды
1 Закон сохранения энергии –энергия не возникает из ничего и не исчезает бесследно, но отдельные ее виды могут переходить друг в друга в строго определенных эквивалентных соотношениях 2 Закон сохранения массы (М. В. Ломоносов, 1748 г. ) – масса всех веществ, вступивших в реакцию, равна массе всех продуктов реакции. в результате химических реакций атомы не исчезают и не возникают, а происходит их перегруппировка. Так как число атомов до реакции и после остается неизменным, то их общая масса также не изменяется 3 Закон постоянства состава (Пруст, 1806 г. ) – каждое химическое соединение имеет вполне определенный и постоянный состав. следствие из этого закона: состав химического соединения не зависит от способа его получения. бертоллиды дальтониды
 4 Закон кратных отношений (Дальтон) – если два элемента обр-ют между собой несколько соединений, то массовые количества одного элемента, соединяющиеся с одним и тем же массовым кол-вом другого, относятся между собой как небольшие целые числа. 5 Закон Авогадро (1811 г. ) – в равных объемах различных идеальных газов при одинаковых условиях (Т и р) содержится одинаковое число молекул. Следствия из закона Авогадро 1 1 моль любого идеального газа при одинаковых условиях (Т и Р) занимает один и тот же объем 2 Плотности идеальных газов при одинаковых условиях (Т и Р) прямо пропорциональны их молярным массам:
4 Закон кратных отношений (Дальтон) – если два элемента обр-ют между собой несколько соединений, то массовые количества одного элемента, соединяющиеся с одним и тем же массовым кол-вом другого, относятся между собой как небольшие целые числа. 5 Закон Авогадро (1811 г. ) – в равных объемах различных идеальных газов при одинаковых условиях (Т и р) содержится одинаковое число молекул. Следствия из закона Авогадро 1 1 моль любого идеального газа при одинаковых условиях (Т и Р) занимает один и тот же объем 2 Плотности идеальных газов при одинаковых условиях (Т и Р) прямо пропорциональны их молярным массам:
 Для газов вводят понятие относительной плотности одного газа по другому. DA(X) – относительная плотность газа Х по газу А:
Для газов вводят понятие относительной плотности одного газа по другому. DA(X) – относительная плотность газа Х по газу А:
 Закон Авогадро ди Кваренья (1811 г. ) • В равных объемах различных газов при одинаковых условиях (температура, давление и т. д. ) содержится одинаковое число молекул. • • • Закон справедлив только для газообразных веществ. Следствия. 1. Одно и то же число молекул различных газов при одинаковых условиях занимает одинаковые объемы. 2. При нормальных условиях (0°C = 273°К , 1 атм = 101, 3 к. Па) 1 моль любого газа занимает объем 22, 4 л. Пример 1. Какой объем водорода при н. у. выделится при растворении 4, 8 г магния в избытке соляной кислоты? Решение. Mg + 2 HCl Mg. Cl 2 + H 2 При растворении 24 г (1 моль) магния в HCl выделилось 22, 4 л (1 моль) водорода; при растворении 4, 8 г магния –– Х л водорода. X = (4, 8 x 22, 4) / 24 = 4, 48 л водорода • • •
Закон Авогадро ди Кваренья (1811 г. ) • В равных объемах различных газов при одинаковых условиях (температура, давление и т. д. ) содержится одинаковое число молекул. • • • Закон справедлив только для газообразных веществ. Следствия. 1. Одно и то же число молекул различных газов при одинаковых условиях занимает одинаковые объемы. 2. При нормальных условиях (0°C = 273°К , 1 атм = 101, 3 к. Па) 1 моль любого газа занимает объем 22, 4 л. Пример 1. Какой объем водорода при н. у. выделится при растворении 4, 8 г магния в избытке соляной кислоты? Решение. Mg + 2 HCl Mg. Cl 2 + H 2 При растворении 24 г (1 моль) магния в HCl выделилось 22, 4 л (1 моль) водорода; при растворении 4, 8 г магния –– Х л водорода. X = (4, 8 x 22, 4) / 24 = 4, 48 л водорода • • •


