Лекция 6 Второй закон термодинамики..ppt
- Количество слайдов: 13
 Второй закон термодинамики • Термины. самопроизвольные ≠ неравновесные самопроизвольные ≠ равновесные несамопроизвольные ≠ неравновесные самопроизвольные ≠ необратимые ≠ неравновесные
Второй закон термодинамики • Термины. самопроизвольные ≠ неравновесные самопроизвольные ≠ равновесные несамопроизвольные ≠ неравновесные самопроизвольные ≠ необратимые ≠ неравновесные
 Свойства равновесных процессов 1. Бесконечно малая разность действующих и противодействующих сил. 2. Бесконечно медленное течение процесса, связанное с бесконечно малой разностью действующих сил и бесконечно большим числом промежуточных состояний. 3. Абсолютные значения работ прямого и обратного процессов одинаковы. 4. Изменение внешней силы на бесконечно малую величину меняет направление процесса на обратный. 5. Пути прямого и обратного процессов совпадают.
Свойства равновесных процессов 1. Бесконечно малая разность действующих и противодействующих сил. 2. Бесконечно медленное течение процесса, связанное с бесконечно малой разностью действующих сил и бесконечно большим числом промежуточных состояний. 3. Абсолютные значения работ прямого и обратного процессов одинаковы. 4. Изменение внешней силы на бесконечно малую величину меняет направление процесса на обратный. 5. Пути прямого и обратного процессов совпадают.
 Самопроизвольные процессы - превращение ("диссипация") механической работы во внутреннюю энергию тела из-за трения, -диффузия в газах и жидкостях, -перемешивание газа. . . + KMn. O 4 = K aq + Mn. O 4 -aq
Самопроизвольные процессы - превращение ("диссипация") механической работы во внутреннюю энергию тела из-за трения, -диффузия в газах и жидкостях, -перемешивание газа. . . + KMn. O 4 = K aq + Mn. O 4 -aq
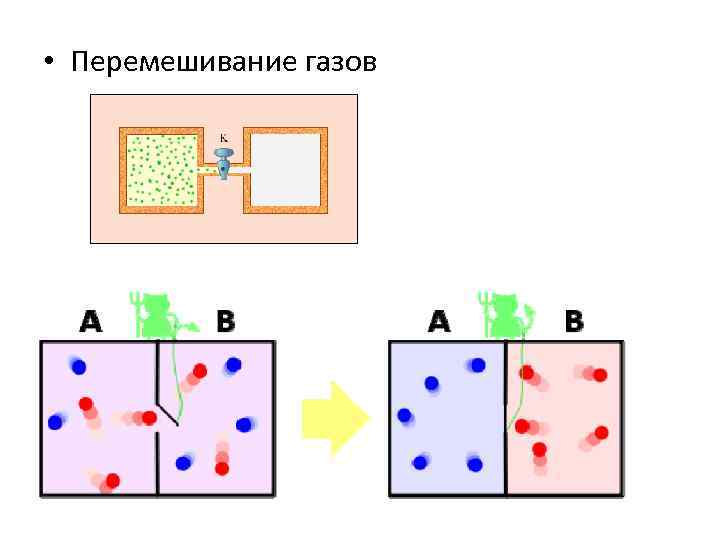 • Перемешивание газов
• Перемешивание газов
 Формулировки второго закона т. д. В циклически действующей тепловой машине невозможен процесс, единственным результатом которого было бы преобразование в механическую работу всего количества теплоты, полученного от единственного теплового резервуара (Кельвин) Невозможен процесс, единственным результатом которого была бы передача энергии путем теплообмена от тела с низкой температурой к телу с более высокой температурой (Клаузиус)
Формулировки второго закона т. д. В циклически действующей тепловой машине невозможен процесс, единственным результатом которого было бы преобразование в механическую работу всего количества теплоты, полученного от единственного теплового резервуара (Кельвин) Невозможен процесс, единственным результатом которого была бы передача энергии путем теплообмена от тела с низкой температурой к телу с более высокой температурой (Клаузиус)
 Формулировки второго закона т. д. 1. Существует некоторое экстенсивное свойство системы S, называемое энтропией, изменение которого следующим образом связано с поглощаемой теплотой и температурой: d. S > δQ/T (самопроизвольный процесс) d. S = δQ/T (равновесный процесс), d. S < δQ/T (несамопроизвольный процесс).
Формулировки второго закона т. д. 1. Существует некоторое экстенсивное свойство системы S, называемое энтропией, изменение которого следующим образом связано с поглощаемой теплотой и температурой: d. S > δQ/T (самопроизвольный процесс) d. S = δQ/T (равновесный процесс), d. S < δQ/T (несамопроизвольный процесс).
 Энтропия-это. . . 1. Тепловая координата, фактор емкости, подобно объему (A=pΔV) 2. Мера вероятности состояния системы 3. Функция состояния системы, позволяющая определить направление протекания процессов в системе. 4. Произведение TS является мерой связанной энергии системы, которая ни при каких условиях не превращается в работу.
Энтропия-это. . . 1. Тепловая координата, фактор емкости, подобно объему (A=pΔV) 2. Мера вероятности состояния системы 3. Функция состояния системы, позволяющая определить направление протекания процессов в системе. 4. Произведение TS является мерой связанной энергии системы, которая ни при каких условиях не превращается в работу.
 Направление процессов в физико – химических системах Энтальпийные и энтропийные факторы, обуславливающие самопроизвольность протекания физико-химических процессов – стремление к уменьшению энтальпии (ΔH < 0) и стремление к увеличению энтропии (ΔS > 0). 1. H<0 и S>0 - самопроизвольная: Cтв. +O 2(г)=2 CO(г) 2. H>0 и S<0 - НЕсамопроизвольная: 3 O 2(г)=2 O 3(г) (эл. разряд) 3. H>0 и S>0 - при высоких T: Cu 2 Oтв. =4 Cuтв. +O 2(г) 4. H<0 и S<0 - при низких T: 2 NO 2 (г)=N 2 O 4 (г)
Направление процессов в физико – химических системах Энтальпийные и энтропийные факторы, обуславливающие самопроизвольность протекания физико-химических процессов – стремление к уменьшению энтальпии (ΔH < 0) и стремление к увеличению энтропии (ΔS > 0). 1. H<0 и S>0 - самопроизвольная: Cтв. +O 2(г)=2 CO(г) 2. H>0 и S<0 - НЕсамопроизвольная: 3 O 2(г)=2 O 3(г) (эл. разряд) 3. H>0 и S>0 - при высоких T: Cu 2 Oтв. =4 Cuтв. +O 2(г) 4. H<0 и S<0 - при низких T: 2 NO 2 (г)=N 2 O 4 (г)
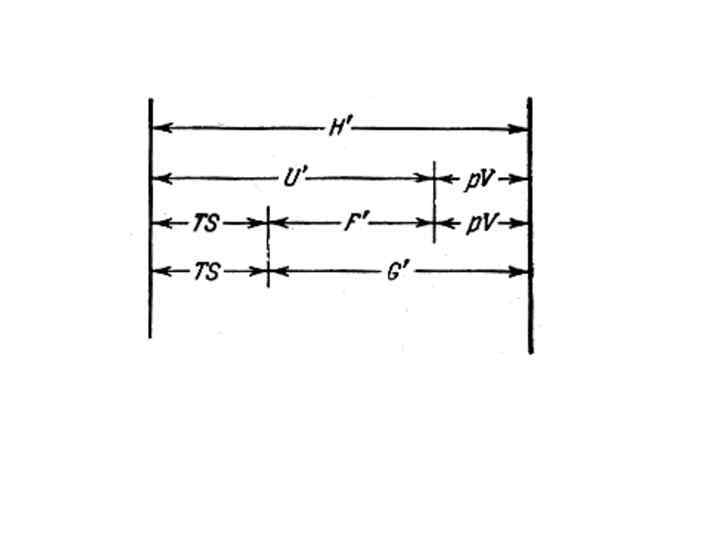
 Характеристические функции Характеристическая функция - функция состояния системы, посредством которой (или ее производных) могут быть выражены в явной форме термодинамические свойства системы 1. U, H=U+p. V (комбинация!), S, . . . ? 2. Изохорно-изотермический потенциал = изохорный потенциал = энергия Гельмгольца (V=const, T=const) F ≡ U – TS. При T=const, V=const , Aрасш. =0: -Ахимич. = U - T S = (U - TS) = F
Характеристические функции Характеристическая функция - функция состояния системы, посредством которой (или ее производных) могут быть выражены в явной форме термодинамические свойства системы 1. U, H=U+p. V (комбинация!), S, . . . ? 2. Изохорно-изотермический потенциал = изохорный потенциал = энергия Гельмгольца (V=const, T=const) F ≡ U – TS. При T=const, V=const , Aрасш. =0: -Ахимич. = U - T S = (U - TS) = F
 3. Изобарно-изотермический потенциал = изобарный потенциал = энергия Гиббса (p=const, T=const) G ≡ H - TS = U + p. V - TS G = F + p V F (если V const) G= H-T S -Ахимич. = U+p V-T S = (U+p. V-TS) Величина G характеризует ту часть изменения внутренней энергии ( Н) , которая может быть превращена в полезную работу.
3. Изобарно-изотермический потенциал = изобарный потенциал = энергия Гиббса (p=const, T=const) G ≡ H - TS = U + p. V - TS G = F + p V F (если V const) G= H-T S -Ахимич. = U+p V-T S = (U+p. V-TS) Величина G характеризует ту часть изменения внутренней энергии ( Н) , которая может быть превращена в полезную работу.
 Критерий протекания процесса F = U - T S (V=const, T=const) Самопроизвольный процесс или равновесие: S ≥ Q/T = U/T → T· S ≥ U или F≤ 0. F ≤ 0 (T=const, V=const) F < 0 - самопроизвольный процесс F = 0 – равновесие G ≤ 0 (T=const, p=const) < 0 - самопроизвольный процесс = 0 - равновесие
Критерий протекания процесса F = U - T S (V=const, T=const) Самопроизвольный процесс или равновесие: S ≥ Q/T = U/T → T· S ≥ U или F≤ 0. F ≤ 0 (T=const, V=const) F < 0 - самопроизвольный процесс F = 0 – равновесие G ≤ 0 (T=const, p=const) < 0 - самопроизвольный процесс = 0 - равновесие
 Принцип смещения равновесий Если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий, определяющих положение равновесия, то в системе усилится то из направлений процесса, течение которого ослабляет влияние произведенного воздействия, и положение равновесия сместится в том же направлении. –Принцип Ле Шателье
Принцип смещения равновесий Если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий, определяющих положение равновесия, то в системе усилится то из направлений процесса, течение которого ослабляет влияние произведенного воздействия, и положение равновесия сместится в том же направлении. –Принцип Ле Шателье