Lecture 3-4 Второй закон.ppt
- Количество слайдов: 69
 ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ
ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ
 Самопроизвольные процессы (1) Процессы, которые совершаются в системе без вмешательства со стороны окружающей среды называются самопроизвольными. В этих процессах всегда уменьшается внутренняя энергия системы. Энергия передается в окружающую среду в виде теплоты или работы. В самопроизвольном процессе работа превращается в теплоту 2/1/2018 2
Самопроизвольные процессы (1) Процессы, которые совершаются в системе без вмешательства со стороны окружающей среды называются самопроизвольными. В этих процессах всегда уменьшается внутренняя энергия системы. Энергия передается в окружающую среду в виде теплоты или работы. В самопроизвольном процессе работа превращается в теплоту 2/1/2018 2
 Самопроизвольные процессы (2) Самопроизвольные процессы Эндотермические процессы тоже могут быть самопроизвольными. Они производят работу за счет теплоты окружающей среды 2/1/2018 3
Самопроизвольные процессы (2) Самопроизвольные процессы Эндотермические процессы тоже могут быть самопроизвольными. Они производят работу за счет теплоты окружающей среды 2/1/2018 3
 Несамопроизвольные процессы Процессы, которые не могут совершаться в системе без вмешательства со стороны окружающей среды называются несамопроизвольными. Для этих процессов необходима передача энергии из окружающей среды в виде теплоты или работы 2/1/2018 4
Несамопроизвольные процессы Процессы, которые не могут совершаться в системе без вмешательства со стороны окружающей среды называются несамопроизвольными. Для этих процессов необходима передача энергии из окружающей среды в виде теплоты или работы 2/1/2018 4
 Обратимые процессы Если после протекания процесса систему и окружающую среду можно вернуть в прежнее состояние то процессы называются обратимыми. Пример: расширение газа в сосуде без трения. Работа, совершаемая при обратимом процессе – максимальная. 2/1/2018 5
Обратимые процессы Если после протекания процесса систему и окружающую среду можно вернуть в прежнее состояние то процессы называются обратимыми. Пример: расширение газа в сосуде без трения. Работа, совершаемая при обратимом процессе – максимальная. 2/1/2018 5
 Необратимые процессы (1) Необратимые процессы В условиях трения для перехода в прежнее состояние необходимо затратить работу, которая приведет к изменению энергии окружающей среду и процесс будет необратимым. 2/1/2018 6
Необратимые процессы (1) Необратимые процессы В условиях трения для перехода в прежнее состояние необходимо затратить работу, которая приведет к изменению энергии окружающей среду и процесс будет необратимым. 2/1/2018 6
 Необратимые процессы (2) Во всех необратимых процессах происходит превращение работы в теплоту. Во всех необратимых процессах происходит выравнивание термодинамических параметров (Т, Р). Система переходит в состояние равновесия. 7 2/1/2018
Необратимые процессы (2) Во всех необратимых процессах происходит превращение работы в теплоту. Во всех необратимых процессах происходит выравнивание термодинамических параметров (Т, Р). Система переходит в состояние равновесия. 7 2/1/2018
 Необратимые процессы (3) Пример: рассеяние энергии в окружающую среду в виде теплового движения (хаотичное рассеяние энергии) 2/1/2018 8
Необратимые процессы (3) Пример: рассеяние энергии в окружающую среду в виде теплового движения (хаотичное рассеяние энергии) 2/1/2018 8
 Второй закон термодинамики Определение 1 Невозможно проведение процесса, в котором вся теплота поглощенная из окружающей среды полностью превращается в работу (вечный двигатель второго рода). (Оствальд) 2/1/2018 Источник тепла Поток энергии теплота двигатель работа 9
Второй закон термодинамики Определение 1 Невозможно проведение процесса, в котором вся теплота поглощенная из окружающей среды полностью превращается в работу (вечный двигатель второго рода). (Оствальд) 2/1/2018 Источник тепла Поток энергии теплота двигатель работа 9
 Второй закон термодинамики Определение 2 Невозможно протекание самопроизвольного процесса, в котором теплота превращается в работу. Только превращение работы в теплоту может быть единственным результатом самопроизвольного процесса. (Томсон) 2/1/2018 10
Второй закон термодинамики Определение 2 Невозможно протекание самопроизвольного процесса, в котором теплота превращается в работу. Только превращение работы в теплоту может быть единственным результатом самопроизвольного процесса. (Томсон) 2/1/2018 10
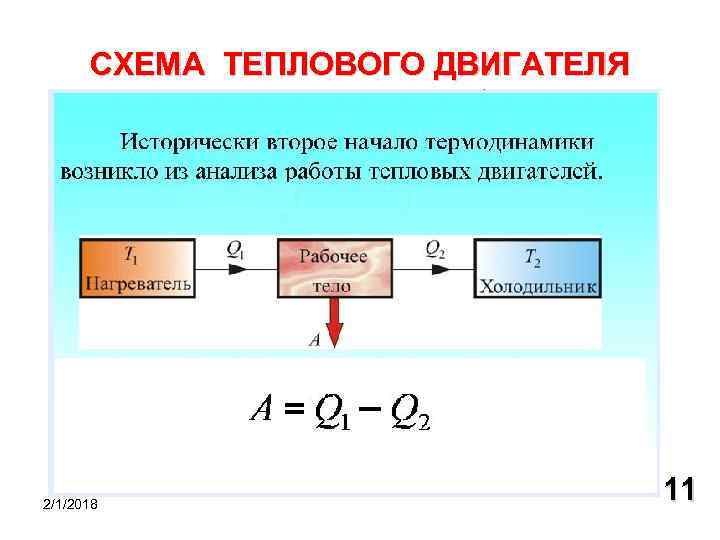 СХЕМА ТЕПЛОВОГО ДВИГАТЕЛЯ 2/1/2018 11
СХЕМА ТЕПЛОВОГО ДВИГАТЕЛЯ 2/1/2018 11
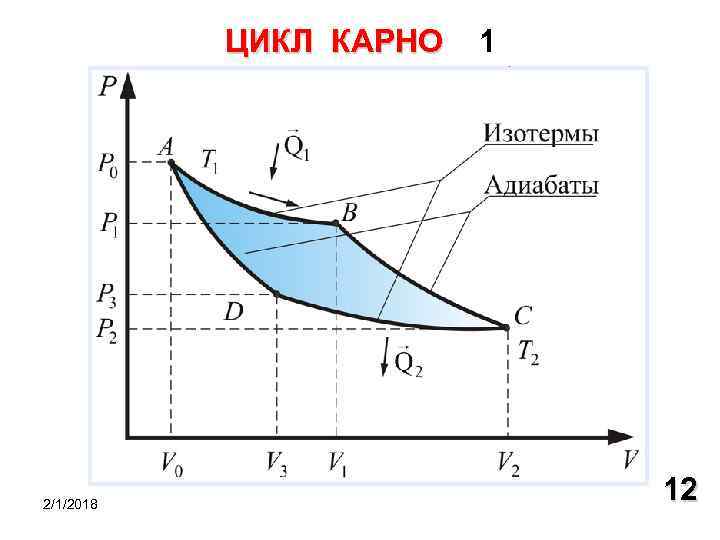 ЦИКЛ КАРНО 2/1/2018 1 12
ЦИКЛ КАРНО 2/1/2018 1 12
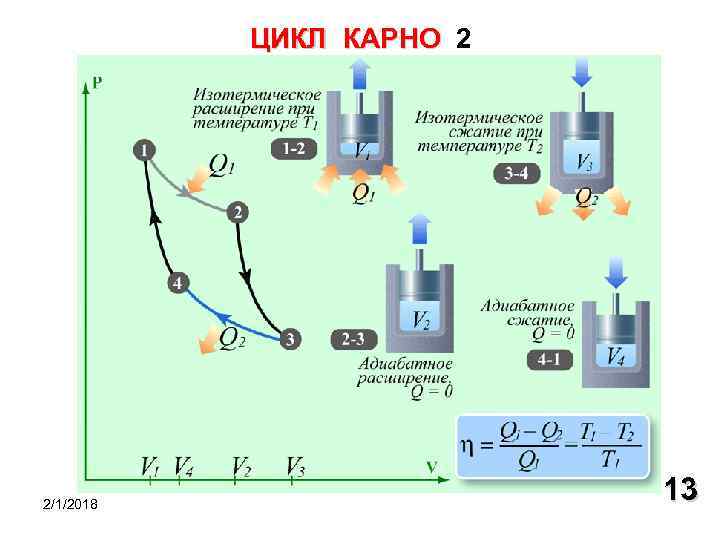 ЦИКЛ КАРНО 2/1/2018 13
ЦИКЛ КАРНО 2/1/2018 13
 КПД ИДЕАЛЬНОГО ТЕПЛОВОГО ДВИГАТЕЛЯ 2/1/2018 14
КПД ИДЕАЛЬНОГО ТЕПЛОВОГО ДВИГАТЕЛЯ 2/1/2018 14
 Энтропия – это мера беспорядка в системе. Во втором законе термодинамики энтропия используется для определения самопроизвольных процессов. Самопроизвольный процесс всегда сопровождается рассеянием энергии в окружающую среду и повышением энтропии. 2/1/2018 15
Энтропия – это мера беспорядка в системе. Во втором законе термодинамики энтропия используется для определения самопроизвольных процессов. Самопроизвольный процесс всегда сопровождается рассеянием энергии в окружающую среду и повышением энтропии. 2/1/2018 15
 Термодинамическое определение энтропии В результате физического или химического процесса всегда происходит изменение энтропии. обр 2/1/2018 16
Термодинамическое определение энтропии В результате физического или химического процесса всегда происходит изменение энтропии. обр 2/1/2018 16
 Изменение энтропии показывает какое количество энергии беспорядочно рассеивается в окружающую среду в виде теплоты (при определенной температуре). 2/1/2018 17
Изменение энтропии показывает какое количество энергии беспорядочно рассеивается в окружающую среду в виде теплоты (при определенной температуре). 2/1/2018 17
 Изменение энтропии в необратимых и обратимых процессах 1 Энтропия является критерием возможности и направленности протекания процессов. Энтропия является критерием состояния термодинамического равновесия. В обратимом (равновесном) процессе: ΔS = 0 2/1/2018 18
Изменение энтропии в необратимых и обратимых процессах 1 Энтропия является критерием возможности и направленности протекания процессов. Энтропия является критерием состояния термодинамического равновесия. В обратимом (равновесном) процессе: ΔS = 0 2/1/2018 18
 Изменение энтропии в необратимых и обратимых процессах 2 Энтропия в изолированной системе, при протекании самопроизвольного процесса всегда возрастает. Необратимый процесс является самопроизвольным и поэтому приводит к увеличению энтропии. ΔS 0 2/1/2018 19
Изменение энтропии в необратимых и обратимых процессах 2 Энтропия в изолированной системе, при протекании самопроизвольного процесса всегда возрастает. Необратимый процесс является самопроизвольным и поэтому приводит к увеличению энтропии. ΔS 0 2/1/2018 19
 Неравенство Клаузиуса (1) Энтропия является критерием самопроизвольного изменения в системе: 2/1/2018 20
Неравенство Клаузиуса (1) Энтропия является критерием самопроизвольного изменения в системе: 2/1/2018 20
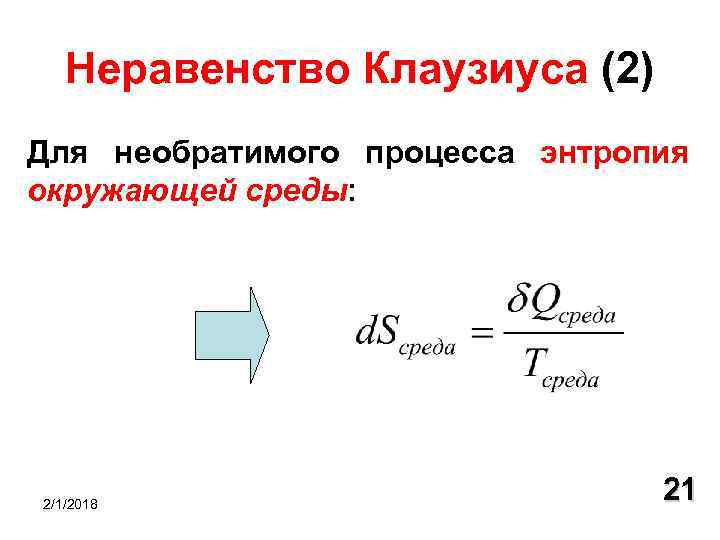 Неравенство Клаузиуса (2) Для необратимого процесса энтропия окружающей среды: 2/1/2018 21
Неравенство Клаузиуса (2) Для необратимого процесса энтропия окружающей среды: 2/1/2018 21
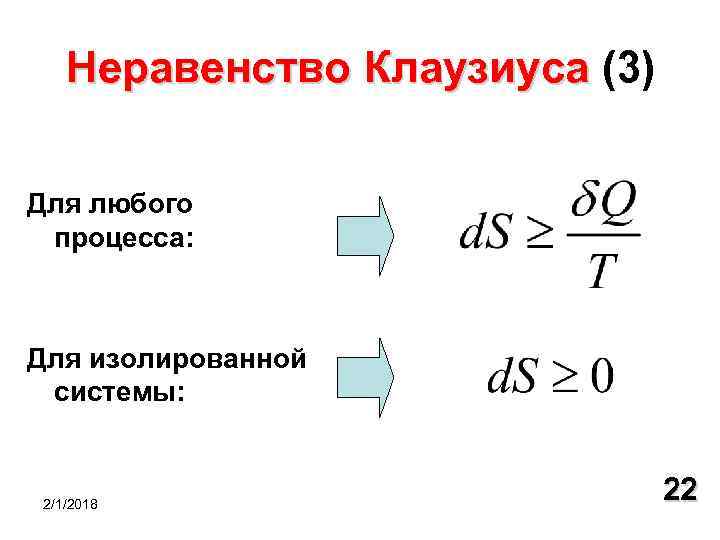 Неравенство Клаузиуса (3) Клаузиуса Для любого процесса: Для изолированной системы: 2/1/2018 22
Неравенство Клаузиуса (3) Клаузиуса Для любого процесса: Для изолированной системы: 2/1/2018 22
 Применение неравенства Клаузиуса (1) Пример 1. Неравновесный адиабатический процесс Для любого самопроизвольного процесса энтропия возрастает. Теплота не передается в окружающую среду 2/1/2018 23
Применение неравенства Клаузиуса (1) Пример 1. Неравновесный адиабатический процесс Для любого самопроизвольного процесса энтропия возрастает. Теплота не передается в окружающую среду 2/1/2018 23
 Применение неравенства Клаузиуса (2) Пример 2. Необратимый изотермический процесс (Т = const) если газ расширяется самопроизвольно в вакуум: 2/1/2018 24
Применение неравенства Клаузиуса (2) Пример 2. Необратимый изотермический процесс (Т = const) если газ расширяется самопроизвольно в вакуум: 2/1/2018 24
 Применение неравенства Клаузиуса (3) 2/1/2018 25
Применение неравенства Клаузиуса (3) 2/1/2018 25
 2/1/2018 26
2/1/2018 26
 ФОРМУЛИРОВКИ ВТОРОГО ЗАКОНА ТЕРМОДИНАМИКИ (1) ТЕРМОДИНАМИКИ 2/1/2018 27
ФОРМУЛИРОВКИ ВТОРОГО ЗАКОНА ТЕРМОДИНАМИКИ (1) ТЕРМОДИНАМИКИ 2/1/2018 27
 ФОРМУЛИРОВКИ ВТОРОГО ЗАКОНА ТЕРМОДИНАМИКИ (2, 3) ТЕРМОДИНАМИКИ 2/1/2018 28
ФОРМУЛИРОВКИ ВТОРОГО ЗАКОНА ТЕРМОДИНАМИКИ (2, 3) ТЕРМОДИНАМИКИ 2/1/2018 28
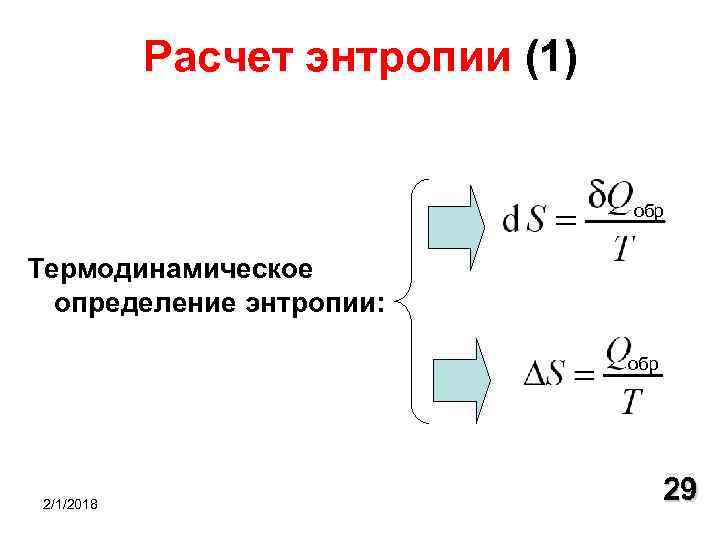 Расчет энтропии (1) обр Термодинамическое определение энтропии: обр 2/1/2018 29
Расчет энтропии (1) обр Термодинамическое определение энтропии: обр 2/1/2018 29
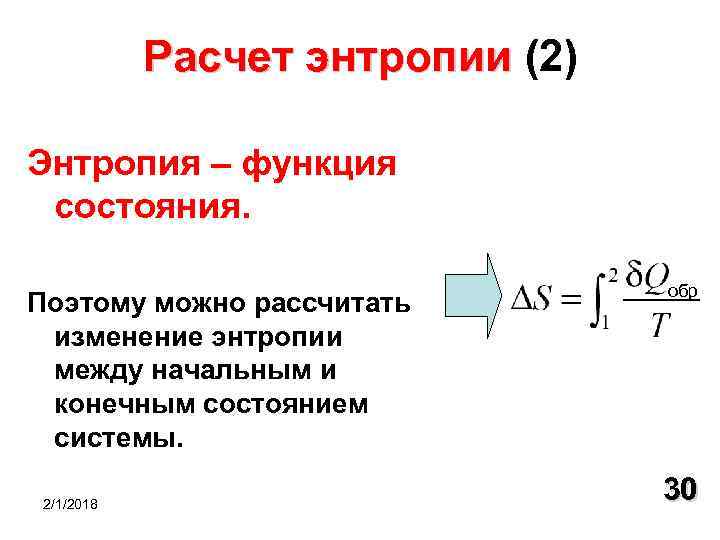 Расчет энтропии (2) Расчет энтропии Энтропия – функция состояния. Поэтому можно рассчитать изменение энтропии между начальным и конечным состоянием системы. 2/1/2018 обр 30
Расчет энтропии (2) Расчет энтропии Энтропия – функция состояния. Поэтому можно рассчитать изменение энтропии между начальным и конечным состоянием системы. 2/1/2018 обр 30
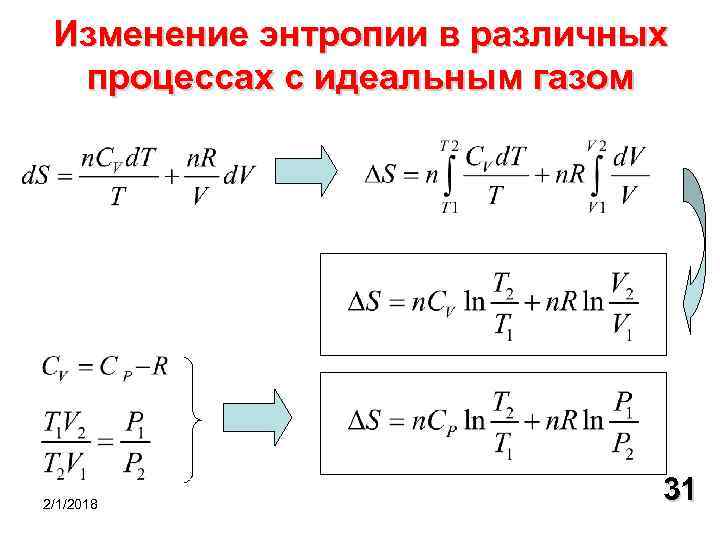 Изменение энтропии в различных процессах с идеальным газом 2/1/2018 31
Изменение энтропии в различных процессах с идеальным газом 2/1/2018 31
 Изменение энтропии в изотермическом процессе (1) изотермическом процессе 2/1/2018 32
Изменение энтропии в изотермическом процессе (1) изотермическом процессе 2/1/2018 32
 Изменение энтропии в изотермическом процессе (2) изотермическом процессе или так как 2/1/2018 33
Изменение энтропии в изотермическом процессе (2) изотермическом процессе или так как 2/1/2018 33
 Изменение энтропии в изохорном процессе 2/1/2018 34
Изменение энтропии в изохорном процессе 2/1/2018 34
 Изменение энтропии в изобарном процессе 2/1/2018 35
Изменение энтропии в изобарном процессе 2/1/2018 35
 Изменение энтропии в адиабатическом процессе 2/1/2018 36
Изменение энтропии в адиабатическом процессе 2/1/2018 36
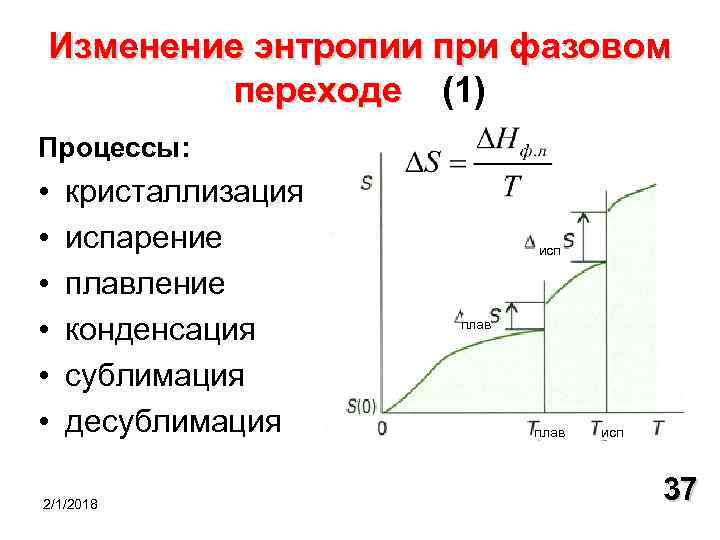 Изменение энтропии при фазовом переходе (1) переходе Процессы: • • • кристаллизация испарение плавление конденсация сублимация десублимация 2/1/2018 исп плав исп 37
Изменение энтропии при фазовом переходе (1) переходе Процессы: • • • кристаллизация испарение плавление конденсация сублимация десублимация 2/1/2018 исп плав исп 37
 Изменение энтропии при фазовом переходе (2) При постоянном давлении: Изменение молярной энтропии: 2/1/2018 38
Изменение энтропии при фазовом переходе (2) При постоянном давлении: Изменение молярной энтропии: 2/1/2018 38
 Изменение энтропии при фазовом переходе (3) Эндотермические процессы: - плавление - испарение - возгонка (сублимация) 2/1/2018 39
Изменение энтропии при фазовом переходе (3) Эндотермические процессы: - плавление - испарение - возгонка (сублимация) 2/1/2018 39
 Изменение энтропии при фазовых переходах (4) Экзотермические процессы: - кристаллизация - конденсация - десублимация 2/1/2018 40
Изменение энтропии при фазовых переходах (4) Экзотермические процессы: - кристаллизация - конденсация - десублимация 2/1/2018 40
 Правило Трутона Mолярная энтропия испарения разных веществ при нормальной температуре кипения является постоянной величиной и равняется константе Трутона: 2/1/2018 41
Правило Трутона Mолярная энтропия испарения разных веществ при нормальной температуре кипения является постоянной величиной и равняется константе Трутона: 2/1/2018 41
 Изменение энтропии при диффузии газов (1) диффузии газов Диффузия – это самопроизвольный необратимый процесс 2/1/2018 42
Изменение энтропии при диффузии газов (1) диффузии газов Диффузия – это самопроизвольный необратимый процесс 2/1/2018 42
 Изменение энтропии при диффузии газов (2) диффузии газов 2/1/2018 43
Изменение энтропии при диффузии газов (2) диффузии газов 2/1/2018 43
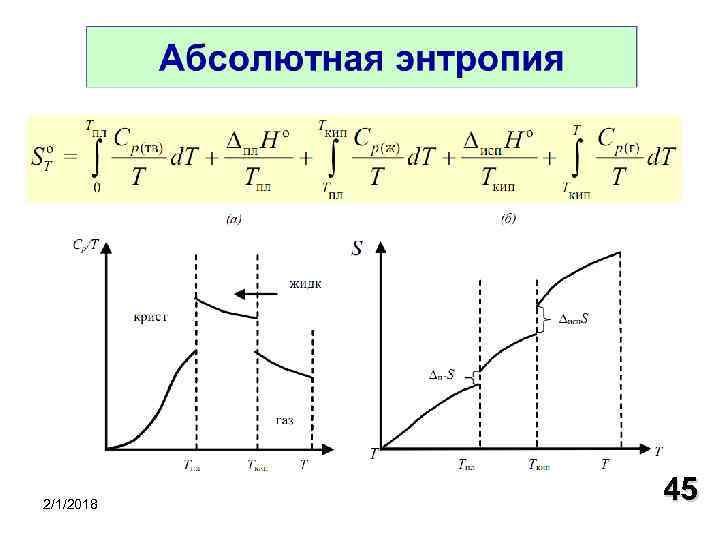
 ТРЕТЬЕ НАЧАЛО ТЕРМОДИНАМИКИ АБСОЛЮТНАЯ ЭНТРОПИЯ Вальтер Фридрих Герман Нернст При абсолютном нуле (Т = 0 К) все идеальные кристаллы имеют одинаковую энтропию, равную нулю. 2/1/2018 44
ТРЕТЬЕ НАЧАЛО ТЕРМОДИНАМИКИ АБСОЛЮТНАЯ ЭНТРОПИЯ Вальтер Фридрих Герман Нернст При абсолютном нуле (Т = 0 К) все идеальные кристаллы имеют одинаковую энтропию, равную нулю. 2/1/2018 44
 2/1/2018 45
2/1/2018 45
 Энтропия химической реакции Стандартная энтропия химической реакции ΔS° это разность между суммой молярных энтропий продуктов и реагентов в стандартном состоянии (с учетом стехиометрических коэффициентов): продукты 2/1/2018 реагенты 46
Энтропия химической реакции Стандартная энтропия химической реакции ΔS° это разность между суммой молярных энтропий продуктов и реагентов в стандартном состоянии (с учетом стехиометрических коэффициентов): продукты 2/1/2018 реагенты 46
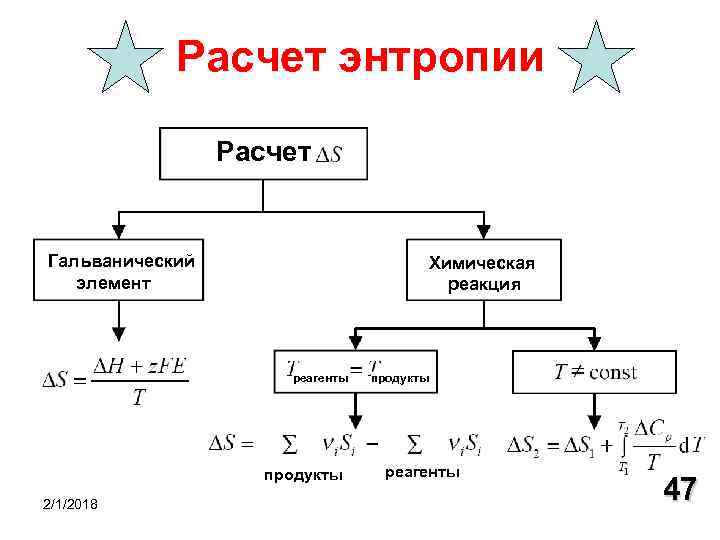 Расчет энтропии Расчет Гальванический Химическая реакция элемент реагенты продукты 2/1/2018 продукты реагенты 47
Расчет энтропии Расчет Гальванический Химическая реакция элемент реагенты продукты 2/1/2018 продукты реагенты 47
 ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ (1) Уравнение объединенного первого ( Q= d. U – А) и второго (Td. S Q) законов термодинамики: Td. S d. U – А C учетом полной работы А = -pd. V+ А' Td. S d. U + pd. V– А' 2/1/2018 48
ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ (1) Уравнение объединенного первого ( Q= d. U – А) и второго (Td. S Q) законов термодинамики: Td. S d. U – А C учетом полной работы А = -pd. V+ А' Td. S d. U + pd. V– А' 2/1/2018 48
 ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ (2) Для обратимых процессов максимальная полезная работа А max = d. U – Td. S + pd. V При V, S = const А max = d. U 2/1/2018 или А max = U 49
ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ (2) Для обратимых процессов максимальная полезная работа А max = d. U – Td. S + pd. V При V, S = const А max = d. U 2/1/2018 или А max = U 49
 ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ (3) При p, S = const А max = d. U + pd. V = d(U + p. V) = d. H или А max = Н При V, T = const максимальная полезная работа А max = d. U – Td. S = d(U – TS) 2/1/2018 50
ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ (3) При p, S = const А max = d. U + pd. V = d(U + p. V) = d. H или А max = Н При V, T = const максимальная полезная работа А max = d. U – Td. S = d(U – TS) 2/1/2018 50
 ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ (4) FV, T = UV, T – (Т S)V, T или UV, T = FV, T + (Т S) V, T 2/1/2018 51
ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ (4) FV, T = UV, T – (Т S)V, T или UV, T = FV, T + (Т S) V, T 2/1/2018 51
 АНАЛИЗ УРАВНЕНИЯ UV, T = FV, T + (Т S)V, T F – свободная энергия, расходуется на совершение работы, T S – связанная энергия, она рассеивается в виде теплоты. С этой точки зрения энтропия является мерой рассеивания (диссипации) энергии. 2/1/2018 52
АНАЛИЗ УРАВНЕНИЯ UV, T = FV, T + (Т S)V, T F – свободная энергия, расходуется на совершение работы, T S – связанная энергия, она рассеивается в виде теплоты. С этой точки зрения энтропия является мерой рассеивания (диссипации) энергии. 2/1/2018 52
 ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ (5) Величина (U – TS) называется изохорноизотермическим (сокращенно изохорным) потенциалом, или энергией Гельмгольца. F U – TS А max = d. F или А max = F, при V, Т = const убыль изохорного потенциала равна максимальной полезной работе процесса. 2/1/2018 53
ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ (5) Величина (U – TS) называется изохорноизотермическим (сокращенно изохорным) потенциалом, или энергией Гельмгольца. F U – TS А max = d. F или А max = F, при V, Т = const убыль изохорного потенциала равна максимальной полезной работе процесса. 2/1/2018 53
 Дифференцирование уравнения F = U – TS дает d. F = d. U – Td. S – Sd. T Тогда с учетом уравнения Td. S = d. U + pd. V – А max получаем d. F = ( А max – pd. V) – Sd. T = Аmax – Sd. T 2/1/2018 54
Дифференцирование уравнения F = U – TS дает d. F = d. U – Td. S – Sd. T Тогда с учетом уравнения Td. S = d. U + pd. V – А max получаем d. F = ( А max – pd. V) – Sd. T = Аmax – Sd. T 2/1/2018 54
 при T = const F = (Аmax)Т В обратимом изотермическом процессе убыль изохорного потенциала равна максимальной работе, производимой системой в этом процессе. 2/1/2018 55
при T = const F = (Аmax)Т В обратимом изотермическом процессе убыль изохорного потенциала равна максимальной работе, производимой системой в этом процессе. 2/1/2018 55
 ИЗОБАРНО-ИЗОТЕРМИЧЕСКИЙ ПОТЕНЦИАЛ ИЛИ ЭНЕРГИЯ ГИББСА, G (1) ИЛИ ЭНЕРГИЯ ГИББСА При p, T = const из уравнения Td. S = d. U + pd. V – А max следует А max = d(U + p. V – TS) G U + p. V – TS 2/1/2018 56
ИЗОБАРНО-ИЗОТЕРМИЧЕСКИЙ ПОТЕНЦИАЛ ИЛИ ЭНЕРГИЯ ГИББСА, G (1) ИЛИ ЭНЕРГИЯ ГИББСА При p, T = const из уравнения Td. S = d. U + pd. V – А max следует А max = d(U + p. V – TS) G U + p. V – TS 2/1/2018 56
 ИЗОБАРНО-ИЗОТЕРМИЧЕСКИЙ ПОТЕНЦИАЛ ИЛИ ЭНЕРГИЯ ГИББСА, G ИЛИ ЭНЕРГИЯ ГИББСА (2) При p, T = const убыль изобарно-изотермического потенциала равна максимальной полезной работе процесса А max = d. G и G = А max Gp, T = Нp, T – (Т S)p, T или 2/1/2018 Н = (А max)p, T + (Т S)p, T 57
ИЗОБАРНО-ИЗОТЕРМИЧЕСКИЙ ПОТЕНЦИАЛ ИЛИ ЭНЕРГИЯ ГИББСА, G ИЛИ ЭНЕРГИЯ ГИББСА (2) При p, T = const убыль изобарно-изотермического потенциала равна максимальной полезной работе процесса А max = d. G и G = А max Gp, T = Нp, T – (Т S)p, T или 2/1/2018 Н = (А max)p, T + (Т S)p, T 57
 УРАВНЕНИЯ ОБЪЕДИНЕННОГО ПЕРВОГО И ВТОРОГО ЗАКОНОВ ТЕРМОДИНАМИКИ d. U = Td. S – pd. V + А max d. H = Td. S + Vdp + А max d. F = – Sd. T – pd. V + А max d. G = – Sd. T + Vdp + А max U(S, V), U(S, p), F(T, V), G(T, p) – термодинамические потенциалы. 2/1/2018 58
УРАВНЕНИЯ ОБЪЕДИНЕННОГО ПЕРВОГО И ВТОРОГО ЗАКОНОВ ТЕРМОДИНАМИКИ d. U = Td. S – pd. V + А max d. H = Td. S + Vdp + А max d. F = – Sd. T – pd. V + А max d. G = – Sd. T + Vdp + А max U(S, V), U(S, p), F(T, V), G(T, p) – термодинамические потенциалы. 2/1/2018 58
 ИЗМЕНЕНИЕ ТЕРМОДИНАМИЧЕСКИХ ПОТЕНЦИАЛОВ КАК КРИТЕРИЙ НАПРАВЛЕНИЯ ПРОЦЕССОВ И РАВНОВЕСИЯ Так как изменения U, H, F, G не зависят от пути процесса, а работа в необратимом процессе меньше, чем в процессе обратимом, то в общем случае Фх, у А , где Фх, у обозначает любой термодинамический потенциал U(S, V); H(S, p); F(T, V); G(T, p) 2/1/2018 59
ИЗМЕНЕНИЕ ТЕРМОДИНАМИЧЕСКИХ ПОТЕНЦИАЛОВ КАК КРИТЕРИЙ НАПРАВЛЕНИЯ ПРОЦЕССОВ И РАВНОВЕСИЯ Так как изменения U, H, F, G не зависят от пути процесса, а работа в необратимом процессе меньше, чем в процессе обратимом, то в общем случае Фх, у А , где Фх, у обозначает любой термодинамический потенциал U(S, V); H(S, p); F(T, V); G(T, p) 2/1/2018 59
 КРИТЕРИЙ НАПРАВЛЕНИЯ ПРОЦЕССОВ Если система находится только под действием внешнего давления, т. е. может совершать только механическую работу, то А = 0 и Фх, у < 0, т. е. в любом самопроизвольном процессе термодинамический потенциал уменьшается. 2/1/2018 60
КРИТЕРИЙ НАПРАВЛЕНИЯ ПРОЦЕССОВ Если система находится только под действием внешнего давления, т. е. может совершать только механическую работу, то А = 0 и Фх, у < 0, т. е. в любом самопроизвольном процессе термодинамический потенциал уменьшается. 2/1/2018 60
 КРИТЕРИЙ РАВНОВЕСИЯ В СИСТЕМЕ Термодинамический потенциал, убывая по мере прохождения процесса, в момент равновесия достигает минимума. Следовательно, признаком равновесия в системе служит равенство d. Фх, у = 0 или Фх, у = 0, Все возможные процессы в системе описываются соотношением d. Фх, у 0 или Фх, у 0 2/1/2018 61
КРИТЕРИЙ РАВНОВЕСИЯ В СИСТЕМЕ Термодинамический потенциал, убывая по мере прохождения процесса, в момент равновесия достигает минимума. Следовательно, признаком равновесия в системе служит равенство d. Фх, у = 0 или Фх, у = 0, Все возможные процессы в системе описываются соотношением d. Фх, у 0 или Фх, у 0 2/1/2018 61
 ХАРАКТЕРИСТИЧЕСКИЕ ФУНКЦИИ (1) 1) Изменение внутренней энергии d. U = Td. S – pd. V При условии S = const или V = const имеем ( U/ V)S = – р и ( U/ S)V = Т 2) Изменение энтальпии d. H = Td. S + Vdp При постоянных S или p ( H/ p)S = V и ( H/ S)p = Т 2/1/2018 62
ХАРАКТЕРИСТИЧЕСКИЕ ФУНКЦИИ (1) 1) Изменение внутренней энергии d. U = Td. S – pd. V При условии S = const или V = const имеем ( U/ V)S = – р и ( U/ S)V = Т 2) Изменение энтальпии d. H = Td. S + Vdp При постоянных S или p ( H/ p)S = V и ( H/ S)p = Т 2/1/2018 62
 ХАРАКТЕРИСТИЧЕСКИЕ ФУНКЦИИ (2) 3) Изменение изохорного потенциала d. F = – Sd. T – pd. V При постоянных T или V ( F/ V)T = – р и ( F/ T)V = – S 4) Изменение изобарного потенциала d. G = –Sd. T + Vdp При постоянных T или p ( G/ p)T = V 2/1/2018 и ( G/ T)p = – S 63
ХАРАКТЕРИСТИЧЕСКИЕ ФУНКЦИИ (2) 3) Изменение изохорного потенциала d. F = – Sd. T – pd. V При постоянных T или V ( F/ V)T = – р и ( F/ T)V = – S 4) Изменение изобарного потенциала d. G = –Sd. T + Vdp При постоянных T или p ( G/ p)T = V 2/1/2018 и ( G/ T)p = – S 63
 УРАВНЕНИЯ МАКСИМАЛЬНОЙ РАБОТЫ (УРАВНЕНИЯ ГИББСА – ГЕЛЬМГОЛЬЦА) (1) Связь между максимальной полезной работой равновесного процесса и теплотой того же процесса, протекающего неравновесно. F = U – Т S ( F/ Т)V = – S F = U + Т( F/ Т)V 2/1/2018 64
УРАВНЕНИЯ МАКСИМАЛЬНОЙ РАБОТЫ (УРАВНЕНИЯ ГИББСА – ГЕЛЬМГОЛЬЦА) (1) Связь между максимальной полезной работой равновесного процесса и теплотой того же процесса, протекающего неравновесно. F = U – Т S ( F/ Т)V = – S F = U + Т( F/ Т)V 2/1/2018 64
 УРАВНЕНИЯ МАКСИМАЛЬНОЙ РАБОТЫ (УРАВНЕНИЯ ГИББСА – ГЕЛЬМГОЛЬЦА) (2) Так как F = A max, а U = QV, то: A max = QV + Т( A max/ Т)V 2/1/2018 65
УРАВНЕНИЯ МАКСИМАЛЬНОЙ РАБОТЫ (УРАВНЕНИЯ ГИББСА – ГЕЛЬМГОЛЬЦА) (2) Так как F = A max, а U = QV, то: A max = QV + Т( A max/ Т)V 2/1/2018 65
 УРАВНЕНИЯ МАКСИМАЛЬНОЙ РАБОТЫ (УРАВНЕНИЯ ГИББСА – ГЕЛЬМГОЛЬЦА) (3) Для изобарного потенциала G = Н + Т( G/ Т)p, или A max = Qp + Т( A max/ Т)p 2/1/2018 66
УРАВНЕНИЯ МАКСИМАЛЬНОЙ РАБОТЫ (УРАВНЕНИЯ ГИББСА – ГЕЛЬМГОЛЬЦА) (3) Для изобарного потенциала G = Н + Т( G/ Т)p, или A max = Qp + Т( A max/ Т)p 2/1/2018 66
 ХИМИЧЕСКИЙ ПОТЕНЦИАЛ (1) U = f(V, S, n 1, n 2, . . . , nk) 2/1/2018 67
ХИМИЧЕСКИЙ ПОТЕНЦИАЛ (1) U = f(V, S, n 1, n 2, . . . , nk) 2/1/2018 67
 ХИМИЧЕСКИЙ ПОТЕНЦИАЛ (2) d. U = Td. S – pd. V + Величина ( U/ ni)S, V, n, т. е. приращение внутренней энергии данной фазы системы при увеличении массы данного вещества на единицу, если объем, энтропия и массы всех остальных веществ остаются постоянными, называется химическим потенциалом і i-го компонента. 2/1/2018 68
ХИМИЧЕСКИЙ ПОТЕНЦИАЛ (2) d. U = Td. S – pd. V + Величина ( U/ ni)S, V, n, т. е. приращение внутренней энергии данной фазы системы при увеличении массы данного вещества на единицу, если объем, энтропия и массы всех остальных веществ остаются постоянными, называется химическим потенциалом і i-го компонента. 2/1/2018 68
 2/1/2018 69
2/1/2018 69


