Глобэкология 08 Второе начало Введение.ppt
- Количество слайдов: 19

ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ Нулевое начало убеждает нас в целесообразности введения такого свойства системы, которое позволило бы определить, находится ли данная система в тепловом равновесии с любой другой системой, если эти системы приведены в контакт. Для количественных описаний требуется ввести понятие — температура. Первое начало утверждает целесообразность введения еще одного понятия, называемого энергией. Энергия сообщает нам, в какие состояния может перейти система, если сообщить ей теплоту или совершить над ней работу. Энергия системы — это свойство, позволяющее решить вопрос, может ли система достигнуть того или иного состояния из заданного начального состояния. Системы могут обладать еще одним свойством, которое должно показать уже не просто возможность достижения системой нового состояния из заданного, а будет сразу указывать на возможность спонтанного достижения системой того или иного конечного состояния. Такое свойство существует и называется энтропией системы. С ее помощью можно придать количественный смысл такому понятию, как спонтанность (самопроизвольность).

Во втором начале термодинамики энергия уже рассматривается как вполне определенный объект, и речь идет лишь о ее диссипации (рассеянии). Основное различие между процессами взаимного перехода теплоты и работы заключается в том, что работа предполагает упорядоченное движение, тогда как теплота — неупорядоченное. Природа признает эквивалентность теплоты и работы, но требует «контрибуции» всегда, когда теплота преобразуется в работу. Это своеобразный фундаментальный «налог» : Для самопроизвольных процессов в природе существует фундаментальная асимметрия, т. е. однонаправленность таких процессов. Хотя полное количество энергии сохраняется в любом процессе, распределение между различными формами энергии изменяется необратимым образом. Существование любого организма является наглядной демонстрацией однонаправленных процессов.

Необходимо понять, как возникает упорядоченное движение из неупорядоченного и что при этом теряется. Для этого нужно максимально упростить ситуацию и начать рассмотрение не с организмов, а с неодушевленных предметов или всем известного процесса, допускающего наглядное и полное количественное рассмотрение. Имеено на этом основании мы и проведем анализ работы тепловой машины. Для этого необходимо проанализировать термодинамические циклы, т. е. круговые процессы, осуществляемые термодинамической системой. Циклы представляют собой сочетания различных термодинамических процессов: изотермических, адиабатических, изобарических и изохорических. Устройство, осуществляющее любой термодинамический цикл — тепловая машина, существенно отличается от механизмов , которые возвращают в виде работы потенциальную энергию, полученную ими из внешнего мира. Функционирование тепловых машин сопряжено с материальными изменениями состояний, включающими преобразование механических свойств системы, расширение и увеличение объема. Это подлинный процесс преобразования, а не только передачи движения. Создание тепловой машины базируется на том факте, что нагревание приводит к увеличению объема и, как следствие этого, может быть совершена работа.
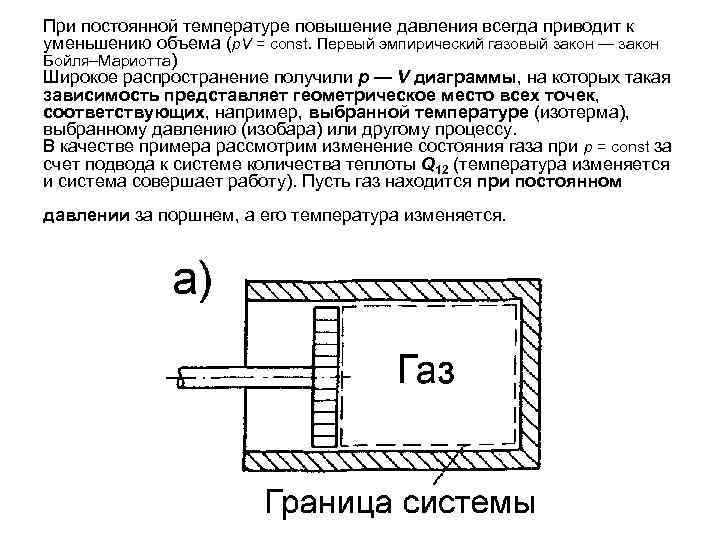
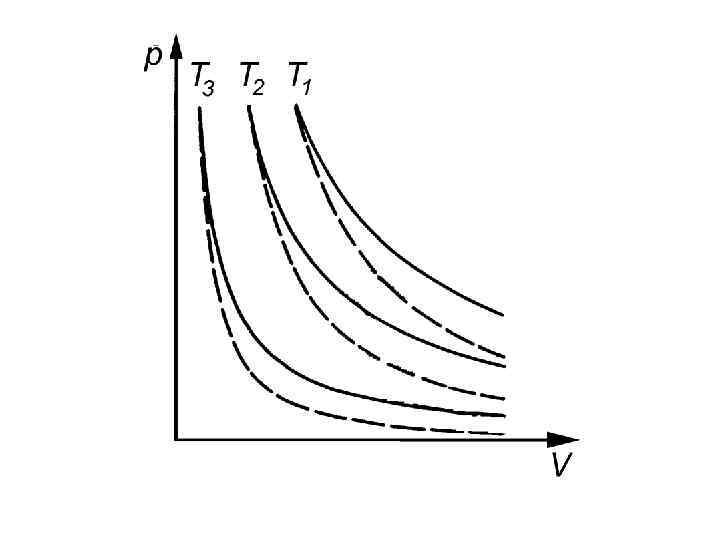
При постоянной температуре повышение давления всегда приводит к уменьшению объема (p. V = const. Первый эмпирический газовый закон — закон Бойля–Мариотта) Широкое распространение получили p — V диаграммы, на которых такая зависимость представляет геометрическое место всех точек, соответствующих, например, выбранной температуре (изотерма), выбранному давлению (изобара) или другому процессу. В качестве примера рассмотрим изменение состояния газа при p = const за счет подвода к системе количества теплоты Q 12 (температура изменяется и система совершает работу). Пусть газ находится при постоянном давлении за поршнем, а его температура изменяется.
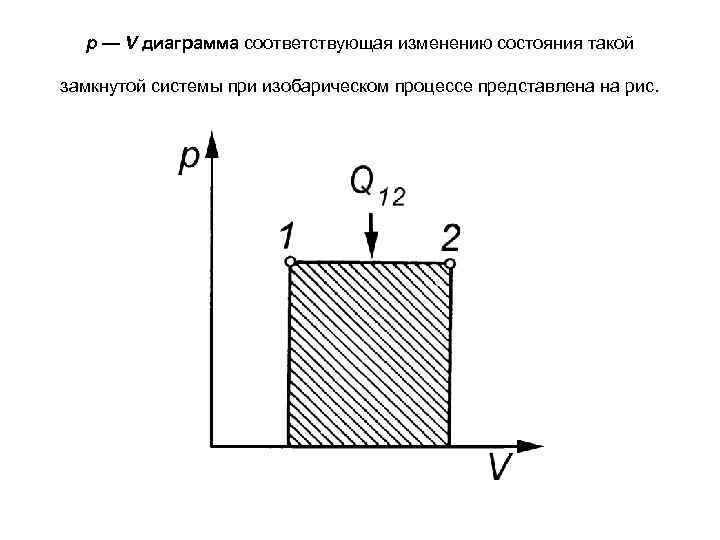
p — V диаграмма соответствующая изменению состояния такой замкнутой системы при изобарическом процессе представлена на рис.

В этом простейшем случае, когда давление остается постоянным в процессе изменения объема, работа равна произведению давления на изменение объема (Vкон – V нач) = ΔV. A = pd. V = p(Vкон – V нач) = pΔV. Площадь, ограниченная любой замкнутой кривой в координатах p, V, равна результирующей величине работы, совершенной системой или средой в течение всего цикла. (Термодинамический цикл — это круговой процесс, осуществляемый термодинамической системой. Изучаемые в термодинамике циклы представляют собой сочетания различных термодинамических процессов, и в первую очередь изотермических, адиабатических, изобарических и изохорических). Работа газа всегда записывается в виде интеграла: A = pd. V. Если изменение состояния системы (цикл) происходит по часовой стрелке, то площадь представляет работу, совершенную системой над средой (система является тепловой машиной), и работа считается положительной A > 0. В противоположном случае — работу среды над системой — A < 0 (система является холодильной машиной (или тепловым насосом)).
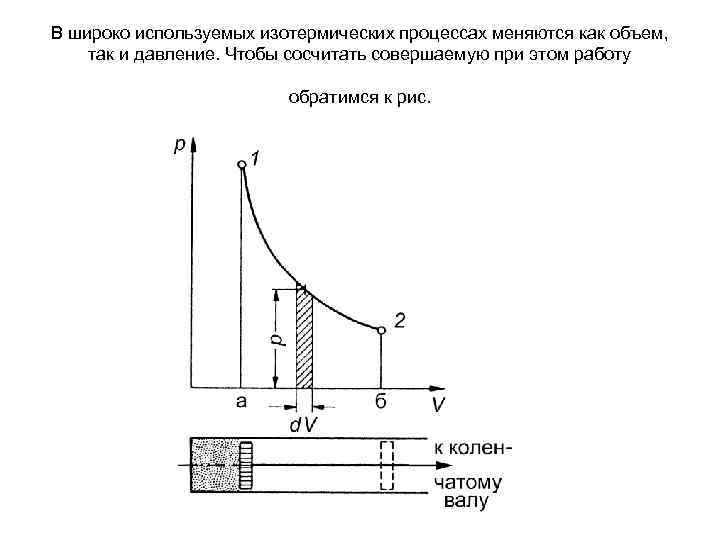
В широко используемых изотермических процессах меняются как объем, так и давление. Чтобы сосчитать совершаемую при этом работу обратимся к рис.
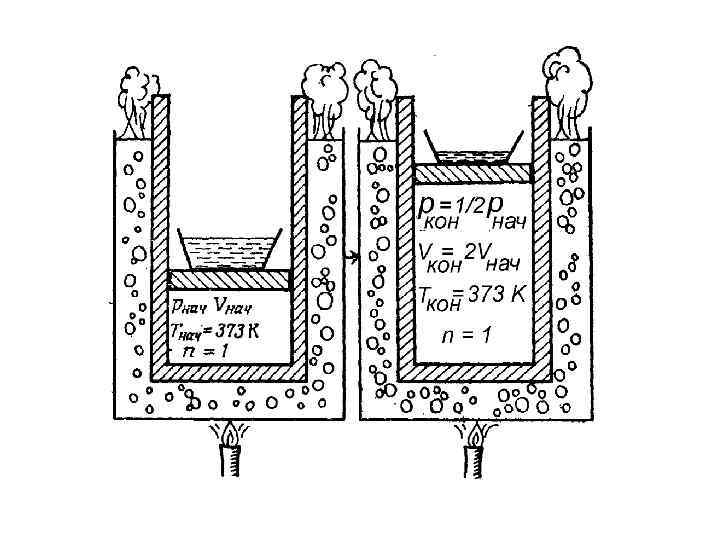

Расширение газа заставляет поршень, перемещаясь из положения а в положение б, вращать коленчатый вал. Бесконечно малое увеличение объема — d. V, занимаемого газом, приводит к бесконечно малому смещению поршня вправо и совершению работы δA = p·d. V. Суммарная работа А равна площади ограниченной кривой а 12 б. Внутренняя энергия при изотермическом процессе не изменяется. Следовательно, в состояниях 1 и 2 она одинакова, и вся теплота Q 1, подводенная к машине от нагревателя, затрачена на совершение работы. Если давление выразить через объем с помощью (p. V = nk. T), то работа при изотермическом процессе записывается в виде: A = Q 1 = pd. V = n. RT 1 ln (V 2/V 1).

Тепловая машина производит движение, а не является пассивным устройством. После того, как машина, получив какое-то количество теплоты, произвела движение, ее необходимо возвратить в начальное состояние. Процессом, компенсирующим происшедшие изменения, является охлаждение системы до начальных значений температуры и возвращение ее к исходным значениям давления и объема. Двигатель должен осуществлять преобразование теплоты в работу неопределенно долго, и поэтому устройство должно периодически возвращаться в исходное состояние. (Живой организм не является тепловой машиной, и нельзя, скажем, с помощью анализа термодинамических циклов объяснять его функционирование или эффективность, однако для анализа фунционирования экосистем ряд результатов теории тепловых машин находит непосредственное применение)

Большой вклад в понимание того, как возникает упорядоченное движение из неупорядоченного и что при этом теряется, внес С. Карно (1824 г. ), предложив для анализа использовать цикл, который получил название цикла Карно. Первый этап (такт) цикла Карно — рабочий. Он связан с поглощением теплоты, расширением и, как следствие, производством работы. Если сразу обратно, то в каждом таком цикле работу пришлось бы совершать «потребителю» . Чтобы термодинамический цикл стал полезным, необходимо понизить давление внутри цилиндра так, чтобы на стадии сжатия требовалась меньшая работа по обратному вдвиганию поршня. В цикле Карно это достигается с помощью включения в цикл адиабатического процесса. С помощью адиабатического расширения мы можем перейти от изотермического процесса, происходящего при температуре Т 1, к изотермическому процессу, происходящему при температуре Т 2.
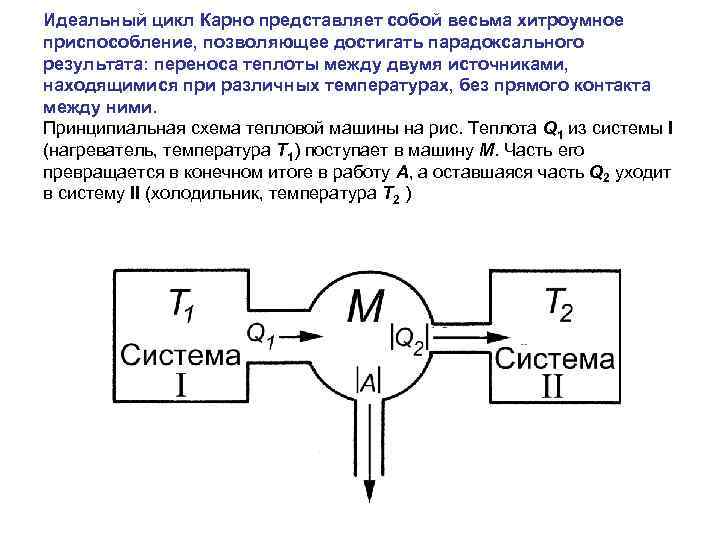
Идеальный цикл Карно представляет собой весьма хитроумное приспособление, позволяющее достигать парадоксального результата: переноса теплоты между двумя источниками, находящимися при различных температурах, без прямого контакта между ними. Принципиальная схема тепловой машины на рис. Теплота Q 1 из системы I (нагреватель, температура T 1) поступает в машину М. Часть его превращается в конечном итоге в работу А, а оставшаяся часть Q 2 уходит в систему II (холодильник, температура Т 2 )
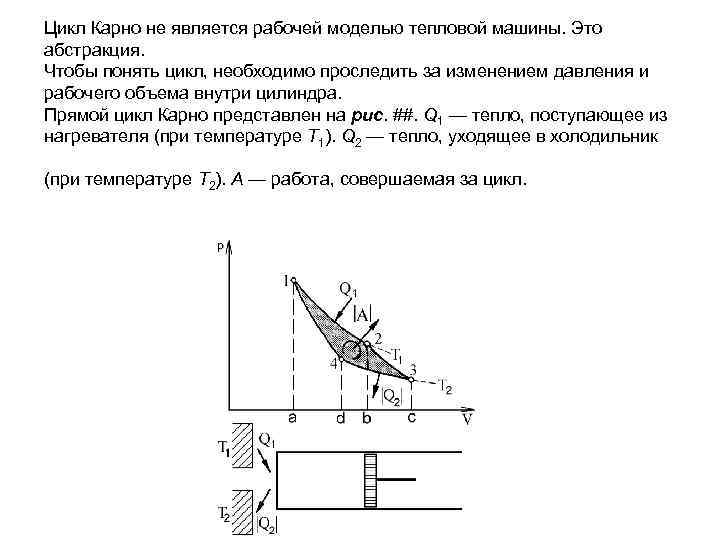
Цикл Карно не является рабочей моделью тепловой машины. Это абстракция. Чтобы понять цикл, необходимо проследить за изменением давления и рабочего объема внутри цилиндра. Прямой цикл Карно представлен на рис. ##. Q 1 — тепло, поступающее из нагревателя (при температуре T 1). Q 2 — тепло, уходящее в холодильник (при температуре Т 2). А — работа, совершаемая за цикл.

Используются два режима: изотермический и адиабатический (температура газа изменяется). В случае адиабатического процесса, при учете ограничения объема газа объемом цилиндра, давление газа изменяется быстрее, чем в изотермическом случае, как при сжатии, так и при расширении. При расширении — газ еще и охлаждается. На каждой из двух изотермических стадий цикла Карно система находится в контакте или с нагревателем при температуре T 1, или с холодильником при температуре T 2. Находясь в контакте с горячим источником, система поглощает теплоту Q 1 и расширяется (переходит из состояния 1 в состояние 2). Находясь в контакте с холодильником, система теряет теплоту Q 2 и сжимается (переходит из состояния 3 в состояние 4). Эти стадии связаны между собой двумя адиабатическими стадиями, на которых система изолирована от источников. Теплота не поступает в систему и не покидает ее, но температура системы или повышается в результате сжатия, или понижается в результате расширения. Адиабатические процессы продолжаются до тех пор, пока система не перейдет от температуры одного источника к температуре другого. Существенное различие между адиабатическими и изотермическими процессами состоит в том, что адиабатический процесс оказывается вполне обратимым.

При изотермическом сжатии теплота уходит через стенки цилиндра. Для «вытекания» теплоты из цилиндра достаточно, чтобы температура в окружающем пространстве была ниже, чем в цилиндре. При необратимых процессах возникают какие-нибудь другие формы энергии, или энергия уходит в окружающую среду, и мы не можем ее использовать. При обратимых процессах этих потерь нет, и они всегда дают максимально возможную работу. Для идеализированного цикла мы можем считать, что оба резервуара, между которыми происходит обмен теплотой, являются огромными, а перепад температур между ними бесконечно малый. При таких условиях оба изотермических такта также обратимы, и, следовательно, в процессе Карно производится максимально возможная работа.

Согласно рассуждениям Карно, «падение теплородной субстанции» , обусловленное разностью температур, аналогично падению воды с более высокого уровня на низкий. В обоих случаях работа определяется перепадом между «источником» и «стоком» температур — для теплорода и высот — для воды. Однако Карно нигде явным образом не утверждал, что количество теплоты (т. е. теплорода), отданное холодильнику, равно количеству теплоты, отобранной от нагревателя. Наиболее важные выводы Карно оказались правильными.

То, что в каждой тепловой машине должен быть свой холодильник, которому на определенной стадии цикла необходимо отдавать часть энергии (рассеивать энергию), по существу и составило базу для последующего введения второго начала термодинамики. Зная величину количества теплоты Q 1, изъятого от нагревателя, находящегося при температуре T 1, мы всегда можем для обратимого процесса сосчитать работу, совершаемую при наличии холодильника с температурой T 2. Результат совершенно не зависит от свойств рабочего вещества. Работа, совершаемая обратимой тепловой машиной, — это универсальная функция, не зависящая от свойств вещества! Этот принцип — то реальное правило, которое можно вывести из классической термодинамики. Конкретизируем закон, определяющий работу, как функцию Q 1, T 1 и T 2.

Внутренняя энергия при обратимом круговом процессе не изменяется. В пределах каждой из изотерм на рис. ##: 1– 2 (ab) и 3– 4 (cd) она остается постоянной и, следовательно, Q = A. Во время каждого из двух изотермических тактов вся тепловая энергия — Q 1 и Q 2 — переходит в работу A 1 и A 2, которую легко сосчитать A = Q 1 = n. RT 1 ln (V 2/V 1). . При адиабатических процессах, во время которых температура идеального газа изменяется от T 1 до T 2 и обратно, отношения объемов рабочего газа — V 2/V 1 и V 4/V 3 равны. Коль скоро это так, то между передаваемым (получаемым) количеством теплоты и температурой, при которой это происходит, имеет место очень простое соотношение: │Q 1│/T 1 = │Q 2│/T 2= │S│. () Если ввести для Q/T особое название, то можно сказать, что в обратимых процессах поглощается столько же Q/T, сколько и выделяется. Это очень удобное при всевозможных расчетах отношение стали обозначать буквой S, и оно получило название энтропия, а отношение бесконечно малого изменения количества теплоты к температуре, при которой это происходит, — Q/T стали называть приведенным количеством теплоты.
Глобэкология 08 Второе начало Введение.ppt