 Второе начало термодинамики и его приложения в химии и биохимиия
Второе начало термодинамики и его приложения в химии и биохимиия
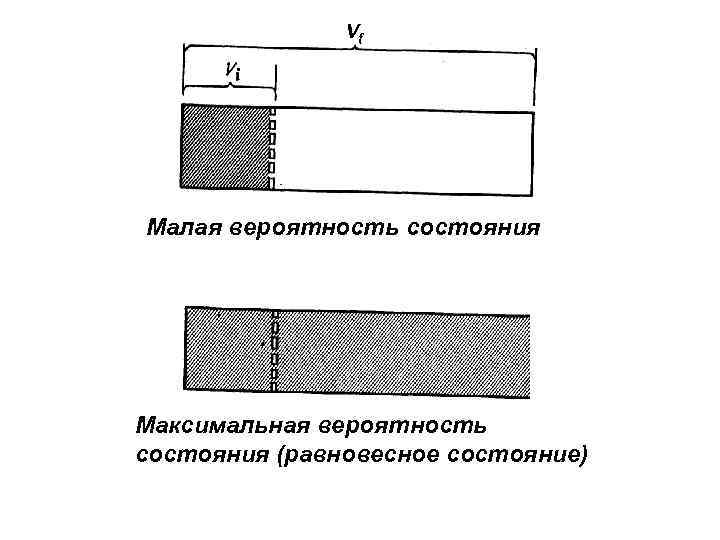 Vf Малая вероятность состояния Максимальная вероятность состояния (равновесное состояние)
Vf Малая вероятность состояния Максимальная вероятность состояния (равновесное состояние)
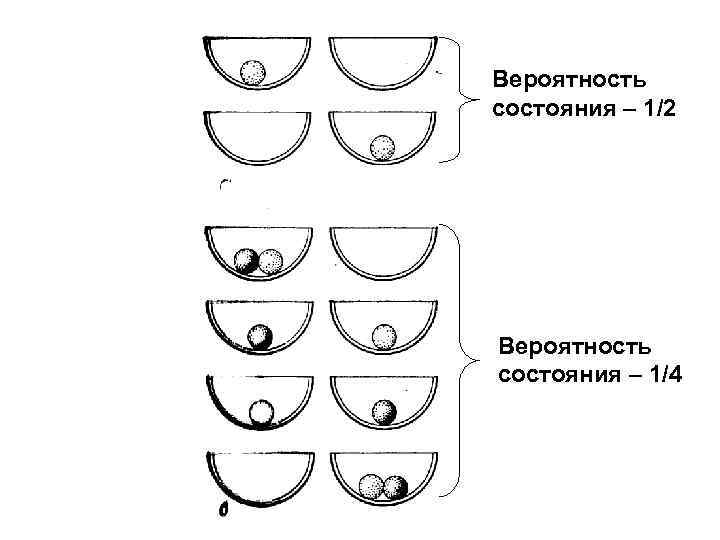 Вероятность состояния – 1/2 Вероятность состояния – 1/4
Вероятность состояния – 1/2 Вероятность состояния – 1/4
 Простая пропорциональность S~W~VN Получается, что некое свойство S пропорционально количеству вещества, которое находится в показателе степени !? Выход S(V) = kln. W(V) N 2 N, W W 2, S(2 N) = 2 S(N) = 2 kln. W
Простая пропорциональность S~W~VN Получается, что некое свойство S пропорционально количеству вещества, которое находится в показателе степени !? Выход S(V) = kln. W(V) N 2 N, W W 2, S(2 N) = 2 S(N) = 2 kln. W
 Изменение энтропии идеального газа при изотермическом расширении от объема Vi до Vf
Изменение энтропии идеального газа при изотермическом расширении от объема Vi до Vf
 Термодинамическое представление энтропии
Термодинамическое представление энтропии
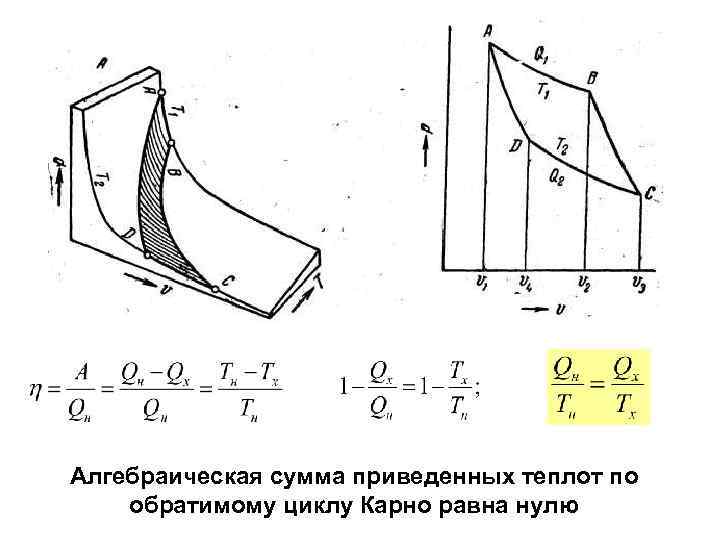 Алгебраическая сумма приведенных теплот по обратимому циклу Карно равна нулю
Алгебраическая сумма приведенных теплот по обратимому циклу Карно равна нулю
 Неравенство Клаузиуса
Неравенство Клаузиуса
 Смешение идеальных газов при постоянных температуре и давлении Парадокс Гиббса ?
Смешение идеальных газов при постоянных температуре и давлении Парадокс Гиббса ?
 Характеристические функции. № Термодинамические потенциалы Энтальпия Энергия Гельмгольца Энергия Гиббса
Характеристические функции. № Термодинамические потенциалы Энтальпия Энергия Гельмгольца Энергия Гиббса
 Фундаментальные уравнения Гиббса № 2
Фундаментальные уравнения Гиббса № 2
 Соотношения Максвелла № 3
Соотношения Максвелла № 3
 № 5
№ 5
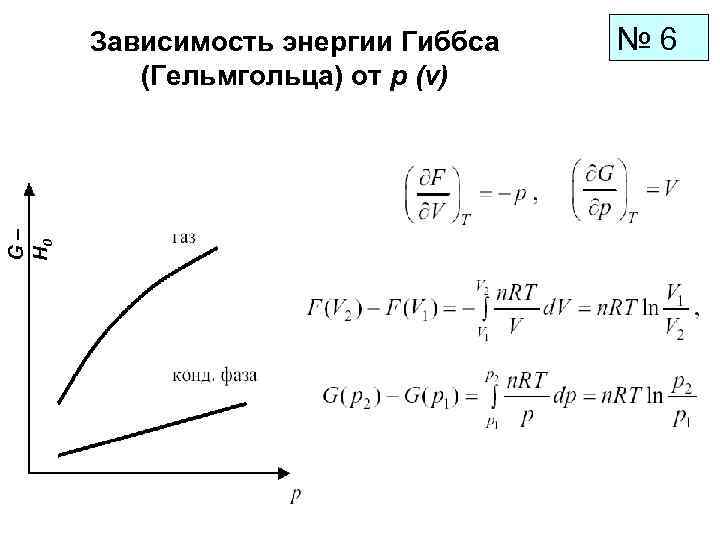 Зависимость энергии Гиббса № 6 (Гельмгольца) от р (v) G– H 0
Зависимость энергии Гиббса № 6 (Гельмгольца) от р (v) G– H 0
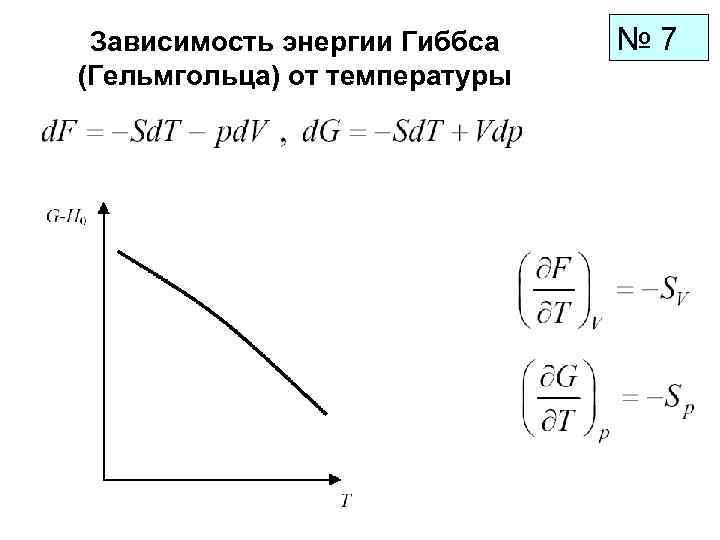 Зависимость энергии Гиббса № 7 (Гельмгольца) от температуры
Зависимость энергии Гиббса № 7 (Гельмгольца) от температуры
 II. Стандартная энергия № 8 реакции Гиббса (Стандартная)
II. Стандартная энергия № 8 реакции Гиббса (Стандартная)
 № 9 III. Стандартные приведенные потенциалы
№ 9 III. Стандартные приведенные потенциалы
 № 10
№ 10
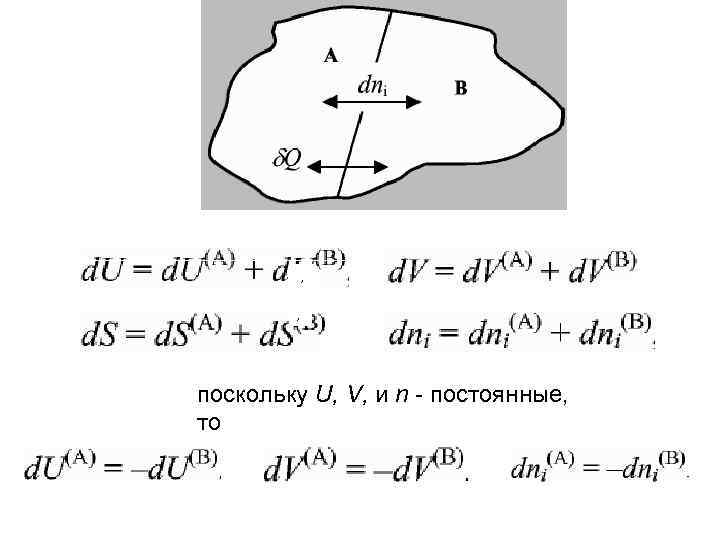 , , поскольку U, V, и n - постоянные, то
, , поскольку U, V, и n - постоянные, то







































