Вторичная структура белков.pptx
- Количество слайдов: 8
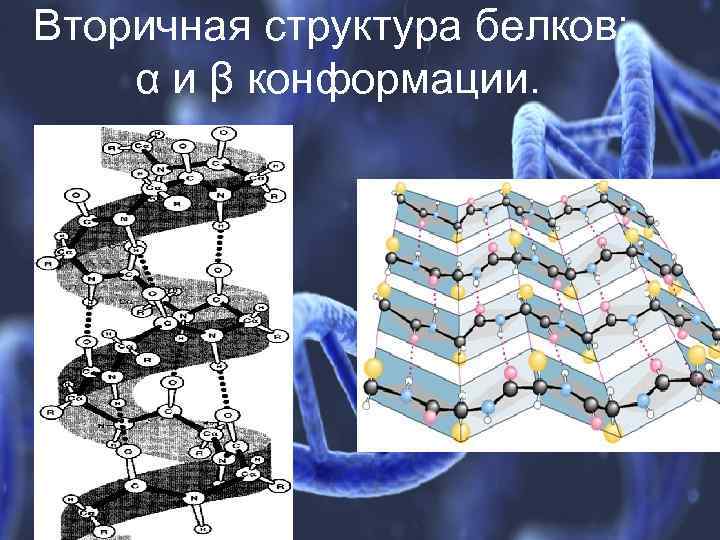
Вторичная структура белков: α и β конформации.

Вторичная структура белка ● ● Вторичная структура белка – это способ конфигурации полипептидной цепи (свертывание скручивание, упаковка) в спиральную или другую конформацию Существует 2 основные вторичные структуры белка α-спираль и βконформации

α спираль ● ● характеризуется предельно плотной упаковкой полипептидной цепи, так что внутренее пространство воображаемого цилиндра вокруг которого закручивается спираль заполнено На каждый виток (шаг) спирали приходится 3, 6 аминокислотных остатка, шаг спирали (расстояние вдоль оси) равен 0, 54 нм, угол подъема спирали 2 через 5 витков спирали (18 аминокислотных остатков) структурная конфигурация полипептидно цепи повторяется, таким образом, период идентичности равен 2, 7 нм.
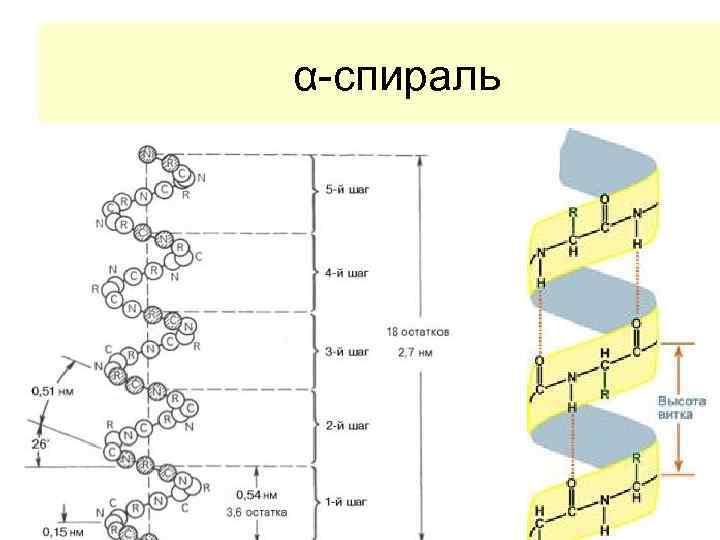
α-спираль
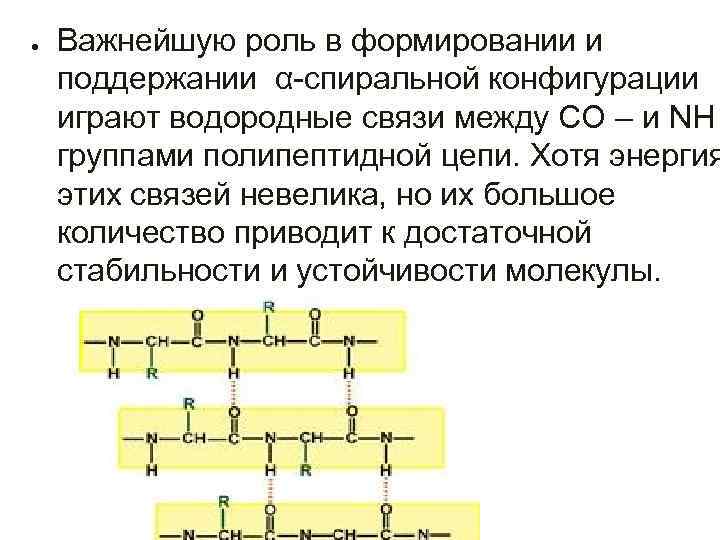
● Важнейшую роль в формировании и поддержании α-спиральной конфигурации играют водородные связи между СО – и NH группами полипептидной цепи. Хотя энергия этих связей невелика, но их большое количество приводит к достаточной стабильности и устойчивости молекулы.

β-конформации ● ● две или более линейные полипептидные цепи, расположенные параллельно или, чаще, антипараллельно, прочно связываются межцепочечными водородными связями между NH-и СОгруппами соседних цепей, образуя структур типа складчатого слоя Подобные структуры в массовом количеств представлены в волокнистых белках, например, в фиброине шелка.
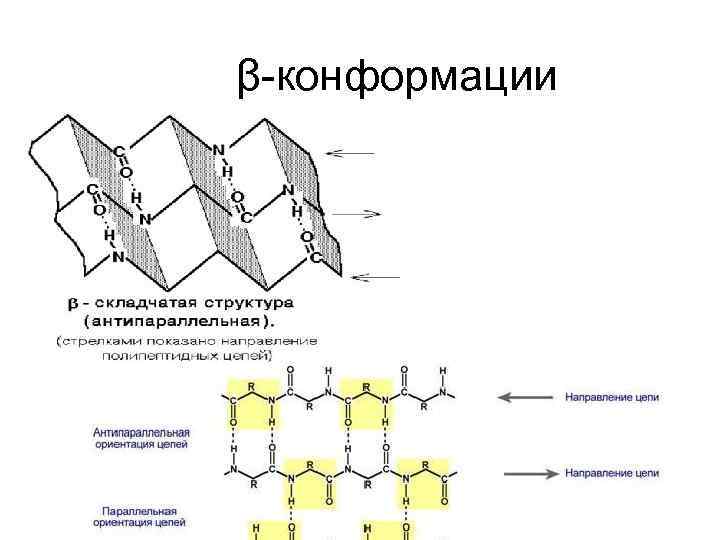
β-конформации

Способоность к образованию водородных связей, являющихся движущей силой при возникновении α-спирали и β-структуры, присуща разным аминокислотам в неравной степени. Вычленяют группу спиралеобразующих аминокислот: ала, глу, глн, лей, лиз, мет, гис. И бетта-образующие вал, иле, тре, тир, фен. Гли, сер, асп, асн и про имеют отношение к преимущественному возникновению неупорядоченных
Вторичная структура белков.pptx