65675dccf14b363b767056fb39eab609.ppt
- Количество слайдов: 15
 Всеукраинская конференция «Український шлях до міжнародних стандартів. Стандартизація та сертифікація лікарських засобів та виробів медичного призначення» 16 октября 2008 г. , г. Киев Гармонизация процедур сертификации производства лекарственных средств Подпружников Ю. В. , д. ф. н. , профессор кафедры управления качеством НФа. У
Всеукраинская конференция «Український шлях до міжнародних стандартів. Стандартизація та сертифікація лікарських засобів та виробів медичного призначення» 16 октября 2008 г. , г. Киев Гармонизация процедур сертификации производства лекарственных средств Подпружников Ю. В. , д. ф. н. , профессор кафедры управления качеством НФа. У
 Гармонизация процедур сертификации производства лекарственных средств Рассматриваемые вопросы: Сертификация лекарственных средств для международной торговли в Украине и в мире Сертификация производств на соответствие требованиям GMP Проблемы на пути гармонизации и предложения по их решению
Гармонизация процедур сертификации производства лекарственных средств Рассматриваемые вопросы: Сертификация лекарственных средств для международной торговли в Украине и в мире Сертификация производств на соответствие требованиям GMP Проблемы на пути гармонизации и предложения по их решению
 Гармонизация процедур сертификации производства лекарственных средств Сертификация лекарственных средств в мире: WHO TRS № 823, 1992, p. p. 92 -104 пер. в кн. под ред. В. А. Усенко, А. Л. Спасокукоцкий «Лицензирование Европейском Союзе: фармацевтический сектор» . К. : «Морион» , с. 273 -289. Украина: Сертификация ЛС для международной торговли: Порядок проведення сертифікації лікарських засобів для міжнародної торгівлі. Наказ МОЗ N 9 від
Гармонизация процедур сертификации производства лекарственных средств Сертификация лекарственных средств в мире: WHO TRS № 823, 1992, p. p. 92 -104 пер. в кн. под ред. В. А. Усенко, А. Л. Спасокукоцкий «Лицензирование Европейском Союзе: фармацевтический сектор» . К. : «Морион» , с. 273 -289. Украина: Сертификация ЛС для международной торговли: Порядок проведення сертифікації лікарських засобів для міжнародної торгівлі. Наказ МОЗ N 9 від
 Гармонизация процедур сертификации производства лекарственных средств v «Сертифікація - процедура, за допомогою якої визнаний в установленому порядку орган документально засвідчує відповідність продукції, систем якості, систем управління якістю, . . . встановленим Законодавством вимогам; » v «Підтвердження відповідності - видача документа (. . . сертифікат відповідності) на основі рішення, яке приймається після проведення відповідних (необхідних) процедур оцінки відповідності, що довели виконання встановлених вимог; »
Гармонизация процедур сертификации производства лекарственных средств v «Сертифікація - процедура, за допомогою якої визнаний в установленому порядку орган документально засвідчує відповідність продукції, систем якості, систем управління якістю, . . . встановленим Законодавством вимогам; » v «Підтвердження відповідності - видача документа (. . . сертифікат відповідності) на основі рішення, яке приймається після проведення відповідних (необхідних) процедур оцінки відповідності, що довели виконання встановлених вимог; »
 Гармонизация процедур сертификации производства лекарственных средств Сертификация лекарственных средств для международной торговле по системе ВОЗ. Участниками системы являются 143 страны мира, из стран СНГ – Армения (с 1992 г) и Россия (с 1999 г).
Гармонизация процедур сертификации производства лекарственных средств Сертификация лекарственных средств для международной торговле по системе ВОЗ. Участниками системы являются 143 страны мира, из стран СНГ – Армения (с 1992 г) и Россия (с 1999 г).
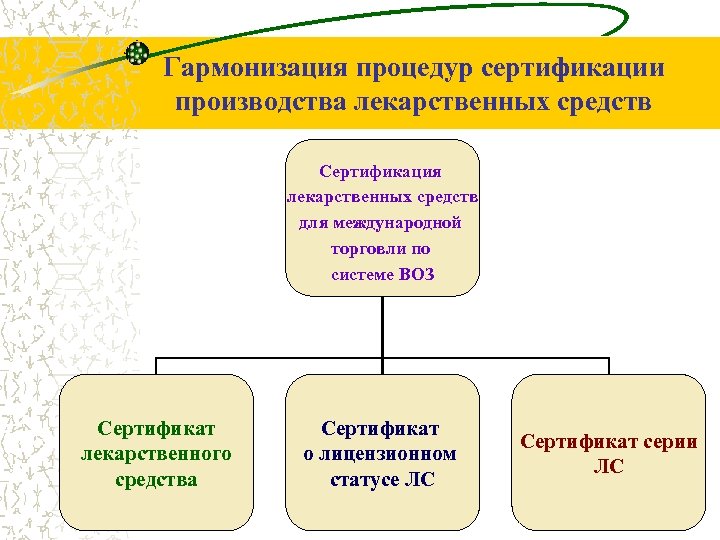 Гармонизация процедур сертификации производства лекарственных средств Сертификация лекарственных средств для международной торговли по системе ВОЗ Сертификат лекарственного средства Сертификат о лицензионном статусе ЛС Сертификат серии ЛС
Гармонизация процедур сертификации производства лекарственных средств Сертификация лекарственных средств для международной торговли по системе ВОЗ Сертификат лекарственного средства Сертификат о лицензионном статусе ЛС Сертификат серии ЛС
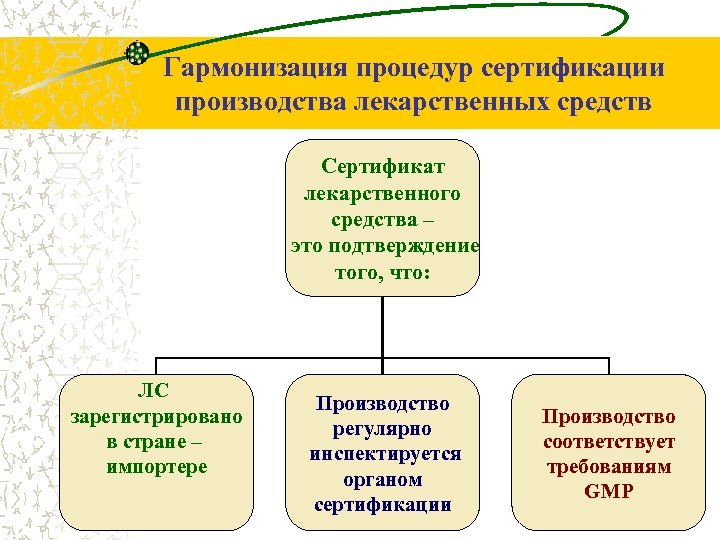 Гармонизация процедур сертификации производства лекарственных средств Сертификат лекарственного средства – это подтверждение того, что: ЛС зарегистрировано в стране – импортере Производство регулярно инспектируется органом сертификации Производство cоответствует требованиям GMP
Гармонизация процедур сертификации производства лекарственных средств Сертификат лекарственного средства – это подтверждение того, что: ЛС зарегистрировано в стране – импортере Производство регулярно инспектируется органом сертификации Производство cоответствует требованиям GMP
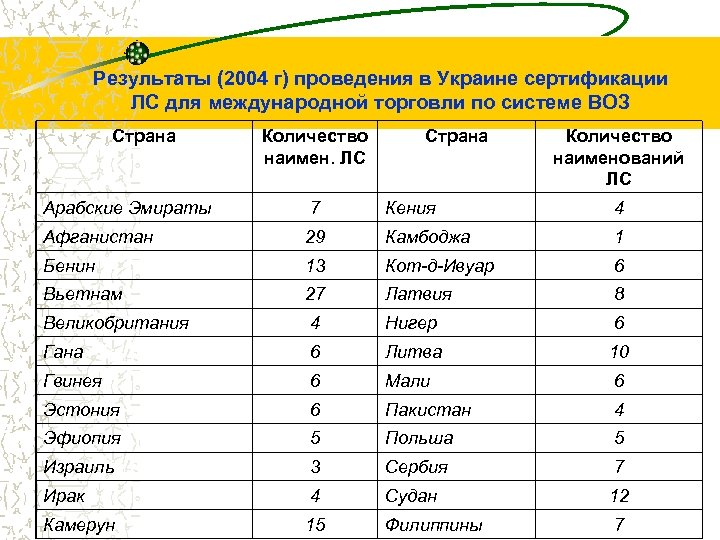 Результаты (2004 г) проведения в Украине сертификации ЛС для международной торговли по системе ВОЗ Страна Количество наимен. ЛС Страна Количество наименований ЛС Арабские Эмираты 7 Кения 4 Афганистан 29 Камбоджа 1 Бенин 13 Кот-д-Ивуар 6 Вьетнам 27 Латвия 8 Великобритания 4 Нигер 6 Гана 6 Литва 10 Гвинея 6 Мали 6 Эстония 6 Пакистан 4 Эфиопия 5 Польша 5 Израиль 3 Сербия 7 Ирак 4 Судан 12 Камерун 15 Филиппины 7
Результаты (2004 г) проведения в Украине сертификации ЛС для международной торговли по системе ВОЗ Страна Количество наимен. ЛС Страна Количество наименований ЛС Арабские Эмираты 7 Кения 4 Афганистан 29 Камбоджа 1 Бенин 13 Кот-д-Ивуар 6 Вьетнам 27 Латвия 8 Великобритания 4 Нигер 6 Гана 6 Литва 10 Гвинея 6 Мали 6 Эстония 6 Пакистан 4 Эфиопия 5 Польша 5 Израиль 3 Сербия 7 Ирак 4 Судан 12 Камерун 15 Филиппины 7
 Гармонизация процедур сертификации производства лекарственных средств Проблемы и несоответствия УКРАИНСКОЙ процедуры сертификации ЛС системе ВОЗ: (Порядок проведення сертифікації лікарських засобів для міжнародної торгівлі. Наказ МОЗ N 9 від 14. 01. 2004) ü Сертификатом ЛС подтверждается не то, что производство соответствует требованиям GMP, а то, что оно соответствует требованиям к производству ЛС, действующим в Украине (в настоящее время это не одно и то же – Ю. В. П. )
Гармонизация процедур сертификации производства лекарственных средств Проблемы и несоответствия УКРАИНСКОЙ процедуры сертификации ЛС системе ВОЗ: (Порядок проведення сертифікації лікарських засобів для міжнародної торгівлі. Наказ МОЗ N 9 від 14. 01. 2004) ü Сертификатом ЛС подтверждается не то, что производство соответствует требованиям GMP, а то, что оно соответствует требованиям к производству ЛС, действующим в Украине (в настоящее время это не одно и то же – Ю. В. П. )
 Гармонизация процедур сертификации производства лекарственных средств Сертификация производств ЛС в ЕС на их соответствие требованиям GMP ü Требования GMP устанавливаются Директовой ЕС (в настоящее время – Директива 2004/93), подробные требования – подзаконными Руководствами (Vol. 4 Eudralex) ü Требования GMP являются обязательными лицензионными требованиями
Гармонизация процедур сертификации производства лекарственных средств Сертификация производств ЛС в ЕС на их соответствие требованиям GMP ü Требования GMP устанавливаются Директовой ЕС (в настоящее время – Директива 2004/93), подробные требования – подзаконными Руководствами (Vol. 4 Eudralex) ü Требования GMP являются обязательными лицензионными требованиями
 Процедура сертификации производства ЛС в Украине на соответствие требованиям GMP Процедура сертификации (приказ МЗ Украины № 381 от 30. 10. 2002 № 391, с изменениями) Получение заявления Подготовка к инспектированию План проведения инспекции Инспектирование Составление отчета Принятие решения Выводы
Процедура сертификации производства ЛС в Украине на соответствие требованиям GMP Процедура сертификации (приказ МЗ Украины № 381 от 30. 10. 2002 № 391, с изменениями) Получение заявления Подготовка к инспектированию План проведения инспекции Инспектирование Составление отчета Принятие решения Выводы
 Гармонизация процедур сертификации производства лекарственных средств Проблемы и несоответствия УКРАИНСКОЙ процедуры сертификации производств ЛС: ü Требования GMP не являются обязательными для производства ЛС; ü Требования GMP в Украине не актуализированы, поэтому не соответствуют GMP ЕС; ü Процедуры сертификации и проверки лицензионных условий – разные
Гармонизация процедур сертификации производства лекарственных средств Проблемы и несоответствия УКРАИНСКОЙ процедуры сертификации производств ЛС: ü Требования GMP не являются обязательными для производства ЛС; ü Требования GMP в Украине не актуализированы, поэтому не соответствуют GMP ЕС; ü Процедуры сертификации и проверки лицензионных условий – разные
 Гармонизация процедур сертификации производства лекарственных средств Предложения по устранению несоответствий: ü Ввести GMP в Закон как обязательные для производства ЛС требования, до этого – ввести эти требования в лицензионные условия; ü Актуализировать требования GMP в Украине для обеспечения их эквивалентности GMP ЕС; ü Внести изменения в процедуры контроля лицензионных условий с использованием методологии PIC/S (градация несоответствий и т. д). ü При процедуре сертификации исключить
Гармонизация процедур сертификации производства лекарственных средств Предложения по устранению несоответствий: ü Ввести GMP в Закон как обязательные для производства ЛС требования, до этого – ввести эти требования в лицензионные условия; ü Актуализировать требования GMP в Украине для обеспечения их эквивалентности GMP ЕС; ü Внести изменения в процедуры контроля лицензионных условий с использованием методологии PIC/S (градация несоответствий и т. д). ü При процедуре сертификации исключить
 Гармонизация процедур сертификации производства лекарственных средств БЛАГОДАРЮ ЗА ВНИМАНИЕ!!!
Гармонизация процедур сертификации производства лекарственных средств БЛАГОДАРЮ ЗА ВНИМАНИЕ!!!
 Гармонизация процедур сертификации производства лекарственных средств ПРИГЛАШАЮ К ДИСКУССИИ!
Гармонизация процедур сертификации производства лекарственных средств ПРИГЛАШАЮ К ДИСКУССИИ!


