dc3512cd3222b6b8e6c572b8d4970a16.ppt
- Количество слайдов: 58
 ВСЕРОССИЙСКАЯ НАУЧНО-ПРАКТИЧЕСКАЯ КОНФЕРЕНЦИЯ АСПЕКТЫ ПРИМЕНЕНИЯ ТЕХНОЛОГИЙ ЯДЕРНОЙ МЕДИЦИНЫ В ХИРУРГИЧЕСКОЙ ПРАКТИКЕ У ДЕТЕЙ И ВЗРОСЛЫХ 17 СЕНТЯБРЯ 2015 ТАРГЕТНАЯ ТЕРАПИЯ ДРЩЖ: современное состояние вопроса и перспективы ИСАЕВ ПАВЕЛ АНАТОЛЬЕВИЧ Д. М. Н. ВЕДУЩИЙ НАУЧНЫЙ СОТРУДНИК МРНЦ им. А. Ф. ЦЫБА
ВСЕРОССИЙСКАЯ НАУЧНО-ПРАКТИЧЕСКАЯ КОНФЕРЕНЦИЯ АСПЕКТЫ ПРИМЕНЕНИЯ ТЕХНОЛОГИЙ ЯДЕРНОЙ МЕДИЦИНЫ В ХИРУРГИЧЕСКОЙ ПРАКТИКЕ У ДЕТЕЙ И ВЗРОСЛЫХ 17 СЕНТЯБРЯ 2015 ТАРГЕТНАЯ ТЕРАПИЯ ДРЩЖ: современное состояние вопроса и перспективы ИСАЕВ ПАВЕЛ АНАТОЛЬЕВИЧ Д. М. Н. ВЕДУЩИЙ НАУЧНЫЙ СОТРУДНИК МРНЦ им. А. Ф. ЦЫБА
 СТАТИСТИЧЕСКИЕ ДАННЫЕ ДРЩЖ МИРОВАЯ СТАТИСТИКА ДРЩЖ: ~1% от диагностируемых злокачественных опухолей во всем мире ~213, 179 новых случаев в 20081 ~35, 383 смертей в 20081 Значительный прирост заболеваемости за последние 10 лет2, 3 Российские данные за 2012 год 4: Заболеваемость раком щитовидной железы составила 9825 человек С впервые в жизни установленным диагнозом рака щитовидной железы выявлено 1436 человек Смертность от рака щитовидной железы составила 1164 человек 1. IARC_Globocan_Stat_2013[5 B]; 2. American Cancer Society. Thyroid cancer. Available at: http: //www. cancer. org/acs/groups/cid/documents/webcontent/003144 -pdf. Updated January 17, 2013. Accessed May 29, 2013; 3. Wartofsky L. Increasing world incidence of thyroid cancer: increased detection or higher radiation exposure? Hormones (Athens). 2010; 9(2): 103 -108. 4. ЗЛОКАЧЕСТВЕННЫЕ НОВООБРАЗОВАНИЯ В РОССИИ В 2012 ГОДУ (ЗАБОЛЕВАЕМОСТЬ И СМЕРТНОСТЬ). Под редакцией А. Д. КАПРИНА, В. В. СТАРИНСКОГО, Г. В. ПЕТРОВОЙ, Москва 2014
СТАТИСТИЧЕСКИЕ ДАННЫЕ ДРЩЖ МИРОВАЯ СТАТИСТИКА ДРЩЖ: ~1% от диагностируемых злокачественных опухолей во всем мире ~213, 179 новых случаев в 20081 ~35, 383 смертей в 20081 Значительный прирост заболеваемости за последние 10 лет2, 3 Российские данные за 2012 год 4: Заболеваемость раком щитовидной железы составила 9825 человек С впервые в жизни установленным диагнозом рака щитовидной железы выявлено 1436 человек Смертность от рака щитовидной железы составила 1164 человек 1. IARC_Globocan_Stat_2013[5 B]; 2. American Cancer Society. Thyroid cancer. Available at: http: //www. cancer. org/acs/groups/cid/documents/webcontent/003144 -pdf. Updated January 17, 2013. Accessed May 29, 2013; 3. Wartofsky L. Increasing world incidence of thyroid cancer: increased detection or higher radiation exposure? Hormones (Athens). 2010; 9(2): 103 -108. 4. ЗЛОКАЧЕСТВЕННЫЕ НОВООБРАЗОВАНИЯ В РОССИИ В 2012 ГОДУ (ЗАБОЛЕВАЕМОСТЬ И СМЕРТНОСТЬ). Под редакцией А. Д. КАПРИНА, В. В. СТАРИНСКОГО, Г. В. ПЕТРОВОЙ, Москва 2014
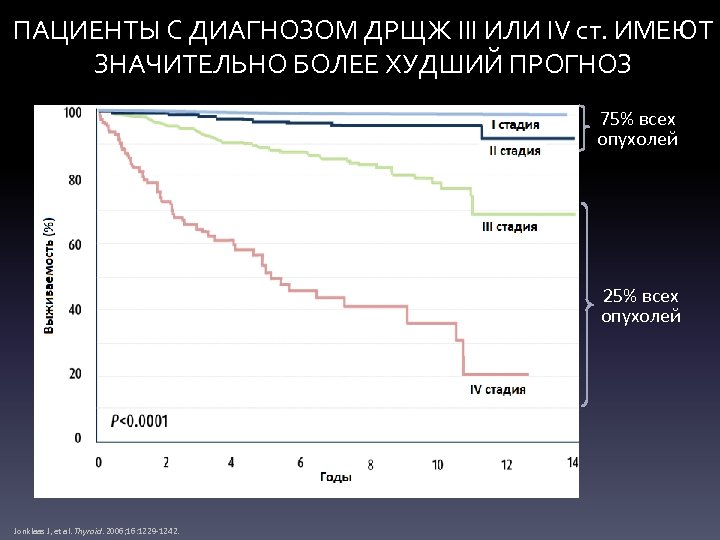 ПАЦИЕНТЫ С ДИАГНОЗОМ ДРЩЖ III ИЛИ IV ст. ИМЕЮТ ЗНАЧИТЕЛЬНО БОЛЕЕ ХУДШИЙ ПРОГНОЗ 75% всех опухолей 25% всех опухолей Jonklaas J, et al. Thyroid. 2006; 16: 1229 -1242.
ПАЦИЕНТЫ С ДИАГНОЗОМ ДРЩЖ III ИЛИ IV ст. ИМЕЮТ ЗНАЧИТЕЛЬНО БОЛЕЕ ХУДШИЙ ПРОГНОЗ 75% всех опухолей 25% всех опухолей Jonklaas J, et al. Thyroid. 2006; 16: 1229 -1242.
 СИСТЕМНОЕ ЛЕЧЕНИЕ МЕТАСТАТИЧЕСКОГО ДРЩЖ РЕФРАКТЕРНОГО К ТЕРАПИИ 131 I Циклофосфамид 600 мг/м 2 в/в 1 раз в 2 недели, 3 дозы курс. Доксорубицин 50 -60 мг/м 2 в/в, день 1; Блеомицин 30 в/в, в 1, 2, 3, дни. Повторные циклы через 3 недели. на мг Доксорубицин 40 -60 мг/м 2 в/в, 1 и 4 дни; Винкристин 1, 2 -1, 5 в/в, день. Повторные циклы каждые 3 недели. мг/м 2 Доксорубицин 70 мг/м 2 в/в, день 1; Блеомицин 15 мг в/в , 1 -5 дни; Винкристин 1, 4 мг/м 2 в/в, 1 и 8 дни. Циклы повторяют с интервалом 3 недели. А. М. Гарин, А. В. Хлебнов «Справочник практической химиотерапии опухолей» . Москва 1995. с. 274
СИСТЕМНОЕ ЛЕЧЕНИЕ МЕТАСТАТИЧЕСКОГО ДРЩЖ РЕФРАКТЕРНОГО К ТЕРАПИИ 131 I Циклофосфамид 600 мг/м 2 в/в 1 раз в 2 недели, 3 дозы курс. Доксорубицин 50 -60 мг/м 2 в/в, день 1; Блеомицин 30 в/в, в 1, 2, 3, дни. Повторные циклы через 3 недели. на мг Доксорубицин 40 -60 мг/м 2 в/в, 1 и 4 дни; Винкристин 1, 2 -1, 5 в/в, день. Повторные циклы каждые 3 недели. мг/м 2 Доксорубицин 70 мг/м 2 в/в, день 1; Блеомицин 15 мг в/в , 1 -5 дни; Винкристин 1, 4 мг/м 2 в/в, 1 и 8 дни. Циклы повторяют с интервалом 3 недели. А. М. Гарин, А. В. Хлебнов «Справочник практической химиотерапии опухолей» . Москва 1995. с. 274
 ВЫЖИВАЕМОСТЬ ПАЦИЕНТОВ С ДРЩЖ РЕФРАКТЕРНОГО К ТЕРАПИИ 131 I 1. 0 1 0. 9 Группа 1 Изначально накапливающие I 131 , терапия с полным ответом (контроль методами визуализации) • Возраст < 40 years • Чаще высокодифференцированные формы • Малые размеры метастазов 127 пациентов Выживаемость (%) 0. 8 0. 7 0. 6 168 пациентов 0. 5 0. 4 0. 3 132 пациента 0. 2 3 0. 1 0. 0 Группа 2 Изначально накапливающие I 131 , но прогрессирующие 2 0 5 10 15 20 25 30 Годы после выявления метастазов Durante C, et al. J Clin Endocrinol Metab. 2006; 91(8): 2892– 2899. 35 40 Группа 3 Изначально рефрактерные к I 131
ВЫЖИВАЕМОСТЬ ПАЦИЕНТОВ С ДРЩЖ РЕФРАКТЕРНОГО К ТЕРАПИИ 131 I 1. 0 1 0. 9 Группа 1 Изначально накапливающие I 131 , терапия с полным ответом (контроль методами визуализации) • Возраст < 40 years • Чаще высокодифференцированные формы • Малые размеры метастазов 127 пациентов Выживаемость (%) 0. 8 0. 7 0. 6 168 пациентов 0. 5 0. 4 0. 3 132 пациента 0. 2 3 0. 1 0. 0 Группа 2 Изначально накапливающие I 131 , но прогрессирующие 2 0 5 10 15 20 25 30 Годы после выявления метастазов Durante C, et al. J Clin Endocrinol Metab. 2006; 91(8): 2892– 2899. 35 40 Группа 3 Изначально рефрактерные к I 131
 ФАКТОРЫ ПРОГНОЗА ЗАБОЛЕВАНИЯ • ОТРАЖАЮТ ОСОБЕННОСТИ БИОЛОГИЧЕСКОГО ТЕЧЕНИЯ (АГРЕССИВНОСТЬ, ИНДОЛЕНТНЫЕ) • НЕ ЗАВИСЯТ ОТ ЛЕЧЕНИЯ • «НАДО ЛЕЧИТЬ» И «КОГДА ЛЕЧИТЬ» ФАКТОРЫ ПРЕДСКАЗЫВАЮЩИЕ ЭФФЕКТИВНОСТЬ ТЕРАПИИ • ТЕЧЕНИЕ БОЛЕЗНИ В ЗАВИСИМОСТИ ОТ ЛЕЧЕНИЯ • РЕЗУЛЬТАТЫ ЛЕЧЕНИЯ • «ЧЕМ ЛЕЧИТЬ»
ФАКТОРЫ ПРОГНОЗА ЗАБОЛЕВАНИЯ • ОТРАЖАЮТ ОСОБЕННОСТИ БИОЛОГИЧЕСКОГО ТЕЧЕНИЯ (АГРЕССИВНОСТЬ, ИНДОЛЕНТНЫЕ) • НЕ ЗАВИСЯТ ОТ ЛЕЧЕНИЯ • «НАДО ЛЕЧИТЬ» И «КОГДА ЛЕЧИТЬ» ФАКТОРЫ ПРЕДСКАЗЫВАЮЩИЕ ЭФФЕКТИВНОСТЬ ТЕРАПИИ • ТЕЧЕНИЕ БОЛЕЗНИ В ЗАВИСИМОСТИ ОТ ЛЕЧЕНИЯ • РЕЗУЛЬТАТЫ ЛЕЧЕНИЯ • «ЧЕМ ЛЕЧИТЬ»
 ДРЩЖ – ГЕТЕРОГЕННОЕ ЗАБОЛЕВАНИЕ ГИСТОЛОГИЧЕСКИЙ ВАРИАНТ • ПРЩЖ • ФРЩЖ Fagin JA, 2004 Nikiforova MN et al. , 2003 ОТКЛОННЕНИЕ НА МОЛЕКУЛЯРНОМ УРОВНЕ ВСТРЕЧАЕМОСТЬ • MAP (МИТОГЕН-АКТИВИРУЕМЫЙ БЕЛОК КИНАЗНОГО КАСКАДА ) • PTC, RET/PTC • RAS • BRAF • 80 % • • RAS PPAR-гамма-PAX 8 • 5 -30 % • 10 % • 44% • 20 -35 % • 30%
ДРЩЖ – ГЕТЕРОГЕННОЕ ЗАБОЛЕВАНИЕ ГИСТОЛОГИЧЕСКИЙ ВАРИАНТ • ПРЩЖ • ФРЩЖ Fagin JA, 2004 Nikiforova MN et al. , 2003 ОТКЛОННЕНИЕ НА МОЛЕКУЛЯРНОМ УРОВНЕ ВСТРЕЧАЕМОСТЬ • MAP (МИТОГЕН-АКТИВИРУЕМЫЙ БЕЛОК КИНАЗНОГО КАСКАДА ) • PTC, RET/PTC • RAS • BRAF • 80 % • • RAS PPAR-гамма-PAX 8 • 5 -30 % • 10 % • 44% • 20 -35 % • 30%
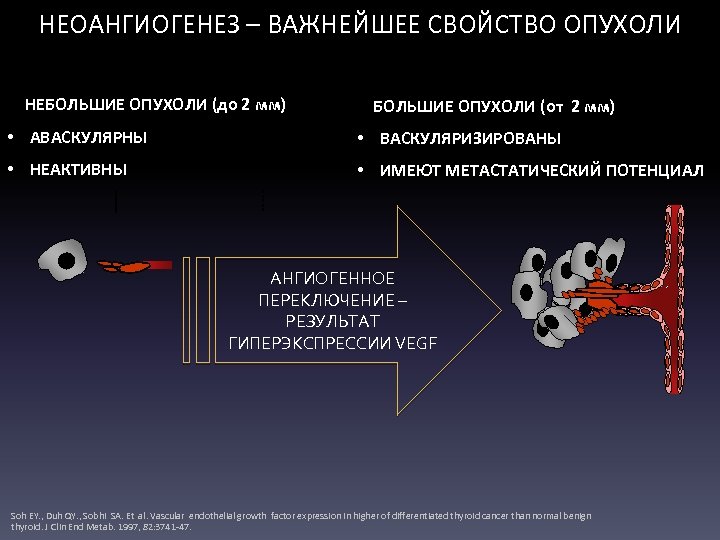 НЕОАНГИОГЕНЕЗ – ВАЖНЕЙШЕЕ СВОЙСТВО ОПУХОЛИ НЕБОЛЬШИЕ ОПУХОЛИ (до 2 мм) БОЛЬШИЕ ОПУХОЛИ (от 2 мм) • АВАСКУЛЯРНЫ • ВАСКУЛЯРИЗИРОВАНЫ • НЕАКТИВНЫ • ИМЕЮТ МЕТАСТАТИЧЕСКИЙ ПОТЕНЦИАЛ АНГИОГЕННОЕ ПЕРЕКЛЮЧЕНИЕ – РЕЗУЛЬТАТ ГИПЕРЭКСПРЕССИИ VEGF Soh EY. , Duh QY. , Sobhi SA. Et al. Vascular endothelial growth factor expression in higher of differentiated thyroid cancer than normal benign thyroid. J Clin End Metab. 1997, 82: 3741 -47.
НЕОАНГИОГЕНЕЗ – ВАЖНЕЙШЕЕ СВОЙСТВО ОПУХОЛИ НЕБОЛЬШИЕ ОПУХОЛИ (до 2 мм) БОЛЬШИЕ ОПУХОЛИ (от 2 мм) • АВАСКУЛЯРНЫ • ВАСКУЛЯРИЗИРОВАНЫ • НЕАКТИВНЫ • ИМЕЮТ МЕТАСТАТИЧЕСКИЙ ПОТЕНЦИАЛ АНГИОГЕННОЕ ПЕРЕКЛЮЧЕНИЕ – РЕЗУЛЬТАТ ГИПЕРЭКСПРЕССИИ VEGF Soh EY. , Duh QY. , Sobhi SA. Et al. Vascular endothelial growth factor expression in higher of differentiated thyroid cancer than normal benign thyroid. J Clin End Metab. 1997, 82: 3741 -47.
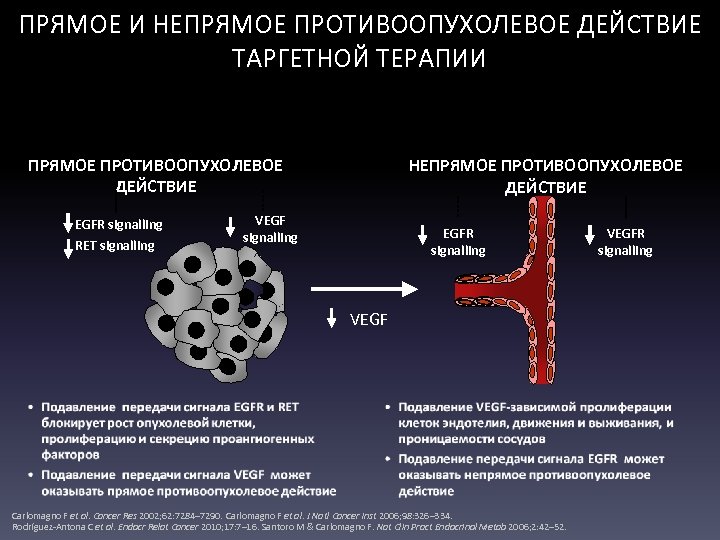 ПРЯМОЕ И НЕПРЯМОЕ ПРОТИВООПУХОЛЕВОЕ ДЕЙСТВИЕ ТАРГЕТНОЙ ТЕРАПИИ ПРЯМОЕ ПРОТИВООПУХОЛЕВОЕ ДЕЙСТВИЕ EGFR signalling RET signalling НЕПРЯМОЕ ПРОТИВООПУХОЛЕВОЕ ДЕЙСТВИЕ VEGF signalling EGFR signalling VEGF Carlomagno F et al. Cancer Res 2002; 62: 7284– 7290. Carlomagno F et al. J Natl Cancer Inst 2006; 98: 326– 334. Rodríguez-Antona C et al. Endocr Relat Cancer 2010; 17: 7– 16. Santoro M & Carlomagno F. Nat Clin Pract Endocrinol Metab 2006; 2: 42– 52. VEGFR signalling
ПРЯМОЕ И НЕПРЯМОЕ ПРОТИВООПУХОЛЕВОЕ ДЕЙСТВИЕ ТАРГЕТНОЙ ТЕРАПИИ ПРЯМОЕ ПРОТИВООПУХОЛЕВОЕ ДЕЙСТВИЕ EGFR signalling RET signalling НЕПРЯМОЕ ПРОТИВООПУХОЛЕВОЕ ДЕЙСТВИЕ VEGF signalling EGFR signalling VEGF Carlomagno F et al. Cancer Res 2002; 62: 7284– 7290. Carlomagno F et al. J Natl Cancer Inst 2006; 98: 326– 334. Rodríguez-Antona C et al. Endocr Relat Cancer 2010; 17: 7– 16. Santoro M & Carlomagno F. Nat Clin Pract Endocrinol Metab 2006; 2: 42– 52. VEGFR signalling
 МУЛЬТИКИНАЗНЫЕ ИНГИБИТОРЫ Препарат Целевые тирозин-киназные рецепторы Axitinib VEGFR 1 -3, PDGFR, c-Kit Cabozantinib (XL 184) HGFR, VEGFR 2, RET Gefitinib EGFR Imatinib Bcr-Abl, PDGFR, c-Fms, c-Kit, RET Lenvatinib (Е 7080) VEGFR 1 -3, FGFR 1 -4, RET, c-Kit, PDGFR Motesanib VEGFR 1 -3, PDGFR, c-Kit, RET Pazopanib VEGFR, PDGFR, c-Kit Sorafenib VEGFR 1 -3, PDGFR, RET, RAF, c-Kit Sunitinib VEGFR 1 -3, PDGFR, c-Kit, RET, CSF 1 R, FLT 3 Vandetanib VEGFR 2 -3, RET, EGFR 1. Cohen EE et al. J Clin Oncol 2008; 26: 4708– 4713. 2. NCT 00704730. 3. Pennell NA et al, Thyroid. 2008 Mar; 18(3): 317 -23, 4. de. Groot JW et al, J Clin Endoc Metab. 2007 Sep; 92(9): 3466 -9. Epub 2007 Jun 19 5. NCT 00784303. 6. Schlumberger M, et al J Clin Oncol 2009; 27: 3794– 3801. 7. Keith C Bible et al, The Lancet Oncology, Vol 11, Issue 10, Pages 962 - 972, October 2010. 8. Lam ET, et al. J Clin Oncol 2010; 28: 2323– 2330. 9. J. A. De Souza et al, J Clin Oncol 28: 15 s, 2010 (suppl; abstr 5504). 10. Wells et al, J Clin Oncol 28: 15 s, 2010 (suppl; abstr 5503).
МУЛЬТИКИНАЗНЫЕ ИНГИБИТОРЫ Препарат Целевые тирозин-киназные рецепторы Axitinib VEGFR 1 -3, PDGFR, c-Kit Cabozantinib (XL 184) HGFR, VEGFR 2, RET Gefitinib EGFR Imatinib Bcr-Abl, PDGFR, c-Fms, c-Kit, RET Lenvatinib (Е 7080) VEGFR 1 -3, FGFR 1 -4, RET, c-Kit, PDGFR Motesanib VEGFR 1 -3, PDGFR, c-Kit, RET Pazopanib VEGFR, PDGFR, c-Kit Sorafenib VEGFR 1 -3, PDGFR, RET, RAF, c-Kit Sunitinib VEGFR 1 -3, PDGFR, c-Kit, RET, CSF 1 R, FLT 3 Vandetanib VEGFR 2 -3, RET, EGFR 1. Cohen EE et al. J Clin Oncol 2008; 26: 4708– 4713. 2. NCT 00704730. 3. Pennell NA et al, Thyroid. 2008 Mar; 18(3): 317 -23, 4. de. Groot JW et al, J Clin Endoc Metab. 2007 Sep; 92(9): 3466 -9. Epub 2007 Jun 19 5. NCT 00784303. 6. Schlumberger M, et al J Clin Oncol 2009; 27: 3794– 3801. 7. Keith C Bible et al, The Lancet Oncology, Vol 11, Issue 10, Pages 962 - 972, October 2010. 8. Lam ET, et al. J Clin Oncol 2010; 28: 2323– 2330. 9. J. A. De Souza et al, J Clin Oncol 28: 15 s, 2010 (suppl; abstr 5504). 10. Wells et al, J Clin Oncol 28: 15 s, 2010 (suppl; abstr 5503).
 МУЛЬТИКИНАЗНЫЕ ИНГИБИТОРЫ (обзор клинических исследований) Лекарство Vandetanib Sorafenib Болезнь Фаза III МРЩЖ ДРЩЖ Cabozantinib МРЩЖ Pazopanib ДРЩЖ Motesanib МРЩЖ и ДРЩЖ Axitinib МРЩЖ и ДРЩЖ Sunitinib МРЩЖ и ДРЩЖ Lenvantinib ДРЩЖ ЗАВЕРШЕНЫ Clinical. Trials. gov НАБОР ПРОДОЛЖАЕТСЯ
МУЛЬТИКИНАЗНЫЕ ИНГИБИТОРЫ (обзор клинических исследований) Лекарство Vandetanib Sorafenib Болезнь Фаза III МРЩЖ ДРЩЖ Cabozantinib МРЩЖ Pazopanib ДРЩЖ Motesanib МРЩЖ и ДРЩЖ Axitinib МРЩЖ и ДРЩЖ Sunitinib МРЩЖ и ДРЩЖ Lenvantinib ДРЩЖ ЗАВЕРШЕНЫ Clinical. Trials. gov НАБОР ПРОДОЛЖАЕТСЯ
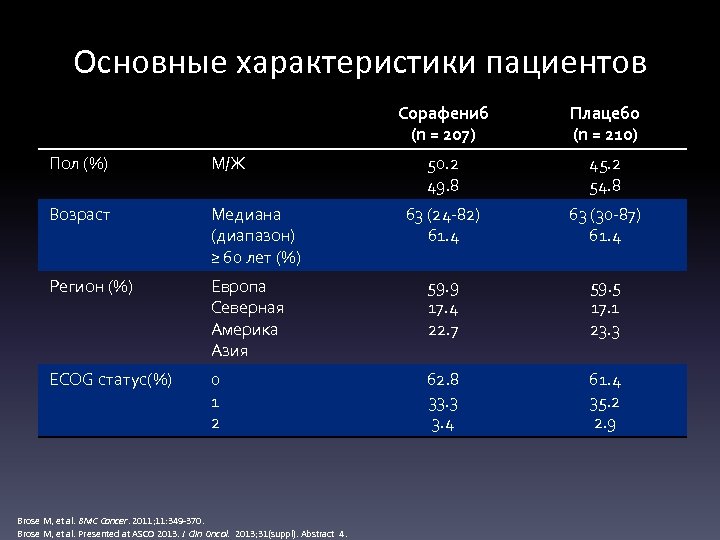 Основные характеристики пациентов Сорафениб (n = 207) Плацебо (n = 210) 50. 2 49. 8 45. 2 54. 8 63 (24 -82) 61. 4 63 (30 -87) 61. 4 Пол (%) М/Ж Возраст Медиана (диапазон) ≥ 60 лет (%) Регион (%) Европа Северная Америка Азия 59. 9 17. 4 22. 7 59. 5 17. 1 23. 3 ECOG статус(%) 0 1 2 62. 8 33. 3 3. 4 61. 4 35. 2 2. 9 Brose M, et al. BMC Cancer. 2011; 11: 349 -370. Brose M, et al. Presented at ASCO 2013. J Clin Oncol. 2013; 31(suppl). Abstract 4.
Основные характеристики пациентов Сорафениб (n = 207) Плацебо (n = 210) 50. 2 49. 8 45. 2 54. 8 63 (24 -82) 61. 4 63 (30 -87) 61. 4 Пол (%) М/Ж Возраст Медиана (диапазон) ≥ 60 лет (%) Регион (%) Европа Северная Америка Азия 59. 9 17. 4 22. 7 59. 5 17. 1 23. 3 ECOG статус(%) 0 1 2 62. 8 33. 3 3. 4 61. 4 35. 2 2. 9 Brose M, et al. BMC Cancer. 2011; 11: 349 -370. Brose M, et al. Presented at ASCO 2013. J Clin Oncol. 2013; 31(suppl). Abstract 4.
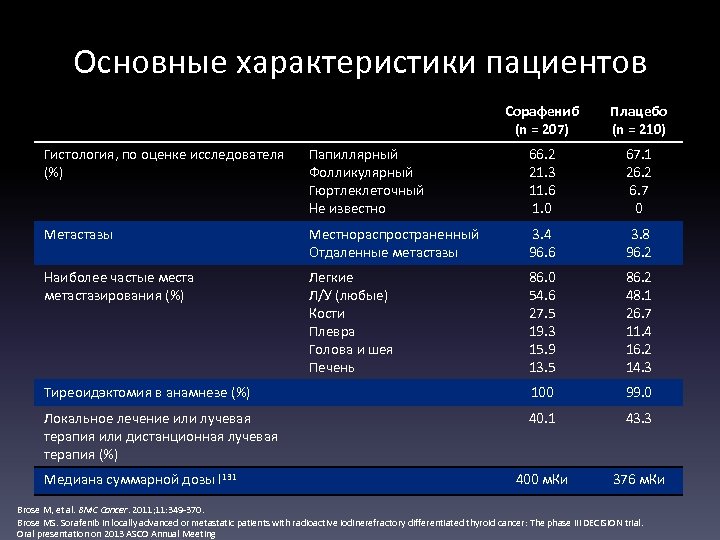 Основные характеристики пациентов Сорафениб (n = 207) Плацебо (n = 210) Гистология, по оценке исследователя (%) Папиллярный Фолликулярный Гюртлеклеточный Не известно 66. 2 21. 3 11. 6 1. 0 67. 1 26. 2 6. 7 0 Метастазы Местнораспространенный Отдаленные метастазы 3. 4 96. 6 3. 8 96. 2 Наиболее частые места метастазирования (%) Легкие Л/У (любые) Кости Плевра Голова и шея Печень 86. 0 54. 6 27. 5 19. 3 15. 9 13. 5 86. 2 48. 1 26. 7 11. 4 16. 2 14. 3 Тиреоидэктомия в анамнезе (%) 100 99. 0 Локальное лечение или лучевая терапия или дистанционная лучевая терапия (%) 40. 1 43. 3 400 м. Ки 376 м. Ки Медиана суммарной дозы I 131 Brose M, et al. BMC Cancer. 2011; 11: 349 -370. Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting
Основные характеристики пациентов Сорафениб (n = 207) Плацебо (n = 210) Гистология, по оценке исследователя (%) Папиллярный Фолликулярный Гюртлеклеточный Не известно 66. 2 21. 3 11. 6 1. 0 67. 1 26. 2 6. 7 0 Метастазы Местнораспространенный Отдаленные метастазы 3. 4 96. 6 3. 8 96. 2 Наиболее частые места метастазирования (%) Легкие Л/У (любые) Кости Плевра Голова и шея Печень 86. 0 54. 6 27. 5 19. 3 15. 9 13. 5 86. 2 48. 1 26. 7 11. 4 16. 2 14. 3 Тиреоидэктомия в анамнезе (%) 100 99. 0 Локальное лечение или лучевая терапия или дистанционная лучевая терапия (%) 40. 1 43. 3 400 м. Ки 376 м. Ки Медиана суммарной дозы I 131 Brose M, et al. BMC Cancer. 2011; 11: 349 -370. Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting
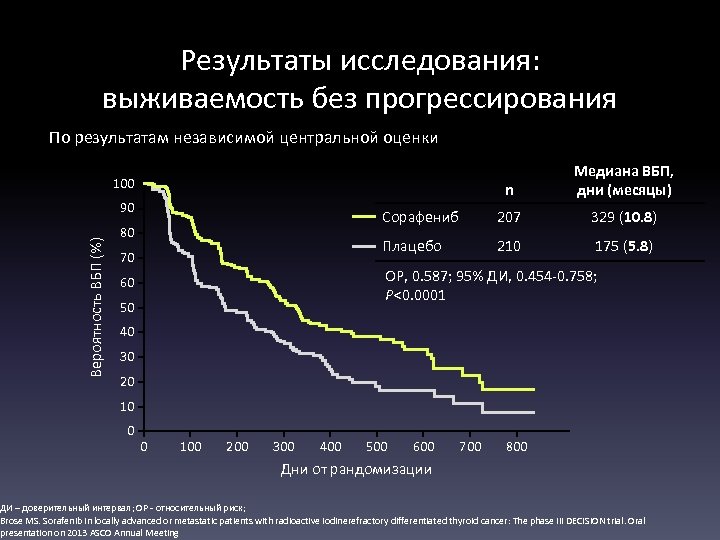 Результаты исследования: выживаемость без прогрессирования По результатам независимой центральной оценки n Медиана ВБП, дни (месяцы) Сорафениб 207 329 (10. 8) Плацебо 210 175 (5. 8) 100 Вероятность ВБП (%) 90 80 70 ОР, 0. 587; 95% ДИ, 0. 454 -0. 758; P<0. 0001 60 50 40 30 20 10 0 0 100 200 300 400 500 600 700 800 Дни от рандомизации ДИ – доверительный интервал; ОР - относительный риск; Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting
Результаты исследования: выживаемость без прогрессирования По результатам независимой центральной оценки n Медиана ВБП, дни (месяцы) Сорафениб 207 329 (10. 8) Плацебо 210 175 (5. 8) 100 Вероятность ВБП (%) 90 80 70 ОР, 0. 587; 95% ДИ, 0. 454 -0. 758; P<0. 0001 60 50 40 30 20 10 0 0 100 200 300 400 500 600 700 800 Дни от рандомизации ДИ – доверительный интервал; ОР - относительный риск; Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting
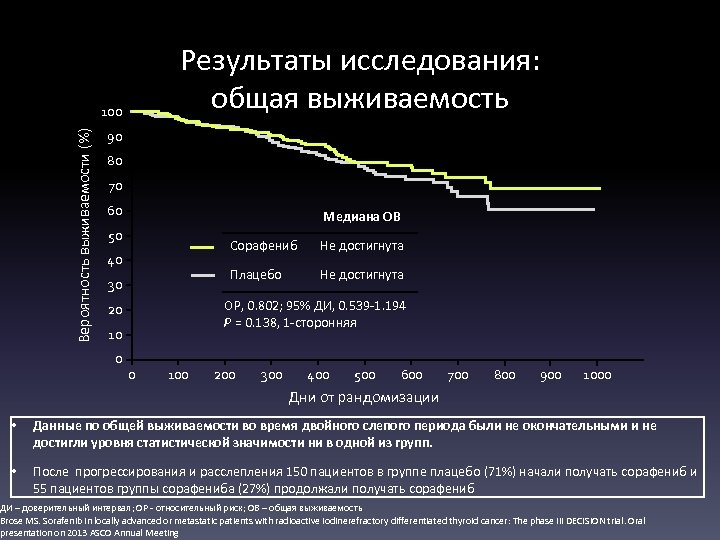 Результаты исследования: общая выживаемость Вероятность выживаемости (%) 100 90 80 70 60 Медиана ОВ 50 Сорафениб Плацебо 40 30 Не достигнута ОР, 0. 802; 95% ДИ, 0. 539 -1. 194 P = 0. 138, 1 -сторонняя 20 10 0 Не достигнута 0 100 200 300 400 500 600 700 800 900 1000 Дни от рандомизации • Данные по общей выживаемости во время двойного слепого периода были не окончательными и не достигли уровня статистической значимости ни в одной из групп. • После прогрессирования и расслепления 150 пациентов в группе плацебо (71%) начали получать сорафениб и 55 пациентов группы сорафениба (27%) продолжали получать сорафениб ДИ – доверительный интервал; ОР - относительный риск; ОВ – общая выживаемость Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting
Результаты исследования: общая выживаемость Вероятность выживаемости (%) 100 90 80 70 60 Медиана ОВ 50 Сорафениб Плацебо 40 30 Не достигнута ОР, 0. 802; 95% ДИ, 0. 539 -1. 194 P = 0. 138, 1 -сторонняя 20 10 0 Не достигнута 0 100 200 300 400 500 600 700 800 900 1000 Дни от рандомизации • Данные по общей выживаемости во время двойного слепого периода были не окончательными и не достигли уровня статистической значимости ни в одной из групп. • После прогрессирования и расслепления 150 пациентов в группе плацебо (71%) начали получать сорафениб и 55 пациентов группы сорафениба (27%) продолжали получать сорафениб ДИ – доверительный интервал; ОР - относительный риск; ОВ – общая выживаемость Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting
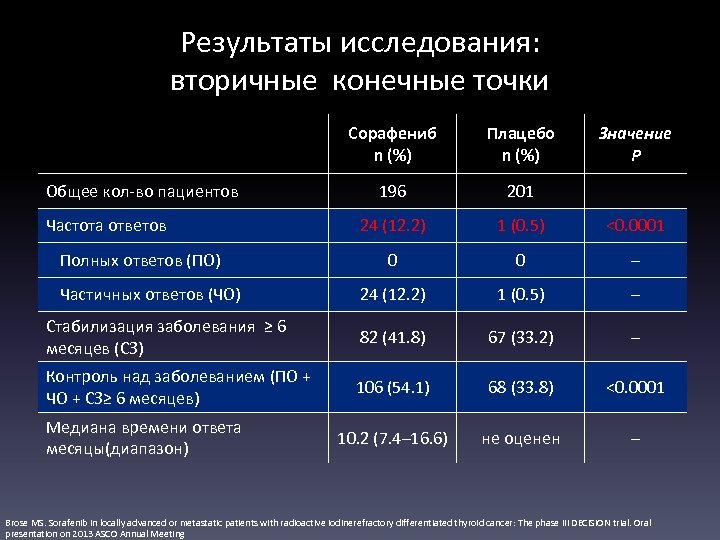 Результаты исследования: вторичные конечные точки Сорафениб n (%) Плацебо n (%) 196 201 24 (12. 2) 1 (0. 5) <0. 0001 0 0 – 24 (12. 2) 1 (0. 5) – Стабилизация заболевания ≥ 6 месяцев (СЗ) 82 (41. 8) 67 (33. 2) – Контроль над заболеванием (ПО + ЧО + СЗ≥ 6 месяцев) 106 (54. 1) 68 (33. 8) <0. 0001 10. 2 (7. 4– 16. 6) не оценен – Общее кол-во пациентов Частота ответов Полных ответов (ПО) Частичных ответов (ЧО) Медиана времени ответа месяцы(диапазон) Значение P Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting
Результаты исследования: вторичные конечные точки Сорафениб n (%) Плацебо n (%) 196 201 24 (12. 2) 1 (0. 5) <0. 0001 0 0 – 24 (12. 2) 1 (0. 5) – Стабилизация заболевания ≥ 6 месяцев (СЗ) 82 (41. 8) 67 (33. 2) – Контроль над заболеванием (ПО + ЧО + СЗ≥ 6 месяцев) 106 (54. 1) 68 (33. 8) <0. 0001 10. 2 (7. 4– 16. 6) не оценен – Общее кол-во пациентов Частота ответов Полных ответов (ПО) Частичных ответов (ЧО) Медиана времени ответа месяцы(диапазон) Значение P Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting
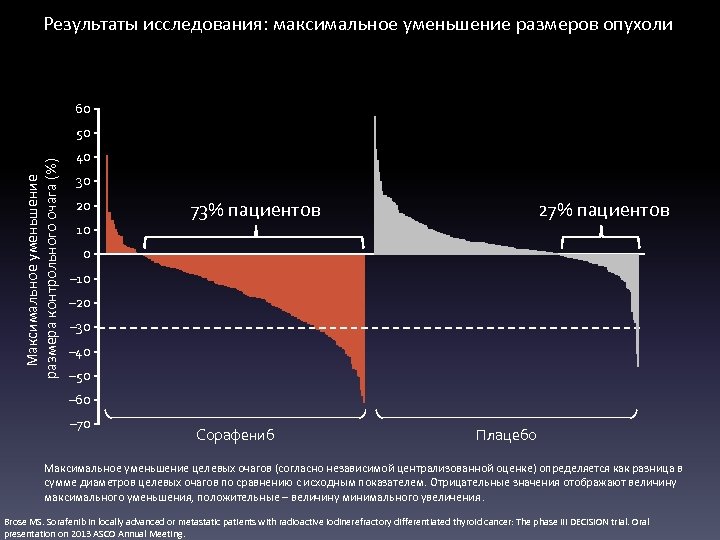 Результаты исследования: максимальное уменьшение размеров опухоли 60 Максимальное уменьшение размера контрольного очага (%) 50 40 30 20 10 73% пациентов 27% пациентов 0 – 10 – 20 – 30 – 40 – 50 – 60 – 70 Сорафениб Плацебо Максимальное уменьшение целевых очагов (согласно независимой централизованной оценке) определяется как разница в сумме диаметров целевых очагов по сравнению с исходным показателем. Отрицательные значения отображают величину максимального уменьшения, положительные – величину минимального увеличения. Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting.
Результаты исследования: максимальное уменьшение размеров опухоли 60 Максимальное уменьшение размера контрольного очага (%) 50 40 30 20 10 73% пациентов 27% пациентов 0 – 10 – 20 – 30 – 40 – 50 – 60 – 70 Сорафениб Плацебо Максимальное уменьшение целевых очагов (согласно независимой централизованной оценке) определяется как разница в сумме диаметров целевых очагов по сравнению с исходным показателем. Отрицательные значения отображают величину максимального уменьшения, положительные – величину минимального увеличения. Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting.
 Профиль безопасности препарата сорафенибом • Препарат Нексавар, как правило, хорошо переносился и имеет предсказуемым и корректируемым профилем нежелательных явлений • В большинстве случаев наблюдались нежелательные явления 1 -й или 2 -й степени • К наиболее распространенным нежелательным явлениям (любой степени) в группе препарата сорафениб относились: – – диарея – алопеция – • ладонно-подошвенная кожная реакция сыпь/шелушение кожи Лечение препаратом Нексавар продолжают до тех пор, пока сохраняется клиническая эффективность препарата, или до появления его неприемлемого токсического действия Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting.
Профиль безопасности препарата сорафенибом • Препарат Нексавар, как правило, хорошо переносился и имеет предсказуемым и корректируемым профилем нежелательных явлений • В большинстве случаев наблюдались нежелательные явления 1 -й или 2 -й степени • К наиболее распространенным нежелательным явлениям (любой степени) в группе препарата сорафениб относились: – – диарея – алопеция – • ладонно-подошвенная кожная реакция сыпь/шелушение кожи Лечение препаратом Нексавар продолжают до тех пор, пока сохраняется клиническая эффективность препарата, или до появления его неприемлемого токсического действия Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting.
 Наиболее частые нежелательные явления при терапии сорафенибом Нежелательные явления* (%) Сорафениб (n = 207) Любая ст. Ст. 3/4 Плацебо (n = 209) Любая ст. Ст. 3/4 Ладонно-подошвенная кожная реакция 76. 3 20. 3 9. 6 0 Диарея 68. 6 5. 8 15. 3 1. 0 Алопеция 67. 1 0 7. 7 0 Сыпь/шелушение 50. 2 4. 8 11. 5 0 Слабость 49. 8 5. 8 25. 4 1. 4 Потеря веса 46. 9 5. 8 13. 9 1. 0 Гипертензия 40. 6 9. 7 12. 4 Metabolic – lab (other) 35. 7 0 16. 7 0 Анорексия 31. 9 2. 4 4. 8 0 Мукозит ротовой полости 23. 2 1. 0 3. 3 0 Зуд 21. 3 1. 0 10. 5 0 Тошнота 20. 8 0 11. 5 0 Гипокальцемия 18. 8 9. 2 4. 8 1. 4 *в ослепленный период согласно National Cancer Institute Common Terminology Criteria for Adverse Events (NCI CTCAE) version 3. 0. Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting.
Наиболее частые нежелательные явления при терапии сорафенибом Нежелательные явления* (%) Сорафениб (n = 207) Любая ст. Ст. 3/4 Плацебо (n = 209) Любая ст. Ст. 3/4 Ладонно-подошвенная кожная реакция 76. 3 20. 3 9. 6 0 Диарея 68. 6 5. 8 15. 3 1. 0 Алопеция 67. 1 0 7. 7 0 Сыпь/шелушение 50. 2 4. 8 11. 5 0 Слабость 49. 8 5. 8 25. 4 1. 4 Потеря веса 46. 9 5. 8 13. 9 1. 0 Гипертензия 40. 6 9. 7 12. 4 Metabolic – lab (other) 35. 7 0 16. 7 0 Анорексия 31. 9 2. 4 4. 8 0 Мукозит ротовой полости 23. 2 1. 0 3. 3 0 Зуд 21. 3 1. 0 10. 5 0 Тошнота 20. 8 0 11. 5 0 Гипокальцемия 18. 8 9. 2 4. 8 1. 4 *в ослепленный период согласно National Cancer Institute Common Terminology Criteria for Adverse Events (NCI CTCAE) version 3. 0. Brose MS. Sorafenib in locally advanced or metastatic patients with radioactive iodinerefractory differentiated thyroid cancer: The phase III DECISION trial. Oral presentation on 2013 ASCO Annual Meeting.
 БОЛЬНАЯ , 1977 г. р. ДИАГНОЗ: ФОЛЛИКУЛЯРНЫЙ РАК ЩИТОВИДНОЙ ЖЕЛЕЗЫ, МЕТАСТАЗЫ В ЛИМФАТИЧЕСКИЕ УЗЛЫ ШЕИ, ЛЕГКИЕ, КОСТИ СКЕЛЕТА. Из “An. morbi”: 11. 03. 2011 ТИРЕОИДЭКТОМИЯ, ЛИМФОДИССЕКЦИЯ ЦЕНТРАЛЬНОЙ КЛЕТЧАТКИ ШЕИ, УДАЛЕНИЕ РЕТРОСТЕРНАЛЬНОЙ КЛЕТЧАТКИ, ФАСЦИАЛЬНОФУТЛЯРНОЕ ИССЕЧЕНИЕ КЛЕТЧАТКИ ШЕИ СПРАВА. № 40621031: НЕИНКАПСУЛИРОВАННЫЙ ФОЛЛИКУЛЯРНЫЙ РАК С ОБШИРНЫМИ УЧАСТКАМИ ДЕСМОПЛАСТИЧЕСКИГРАНУЛЕМАТОЗНОЙ РЕАКЦИЕЙ; ФОН – НОРМАЛЬНАЯ ТКАНЬ ЩИТОВИДНОЙ ЖЕЛЕЗЫ С УЧАСТКАМИ СКЛЕРОЗА. В 26 Л/У ОПУХОЛЕВОГО РОСТА НЕ ОБНАРУЖЕНО.
БОЛЬНАЯ , 1977 г. р. ДИАГНОЗ: ФОЛЛИКУЛЯРНЫЙ РАК ЩИТОВИДНОЙ ЖЕЛЕЗЫ, МЕТАСТАЗЫ В ЛИМФАТИЧЕСКИЕ УЗЛЫ ШЕИ, ЛЕГКИЕ, КОСТИ СКЕЛЕТА. Из “An. morbi”: 11. 03. 2011 ТИРЕОИДЭКТОМИЯ, ЛИМФОДИССЕКЦИЯ ЦЕНТРАЛЬНОЙ КЛЕТЧАТКИ ШЕИ, УДАЛЕНИЕ РЕТРОСТЕРНАЛЬНОЙ КЛЕТЧАТКИ, ФАСЦИАЛЬНОФУТЛЯРНОЕ ИССЕЧЕНИЕ КЛЕТЧАТКИ ШЕИ СПРАВА. № 40621031: НЕИНКАПСУЛИРОВАННЫЙ ФОЛЛИКУЛЯРНЫЙ РАК С ОБШИРНЫМИ УЧАСТКАМИ ДЕСМОПЛАСТИЧЕСКИГРАНУЛЕМАТОЗНОЙ РЕАКЦИЕЙ; ФОН – НОРМАЛЬНАЯ ТКАНЬ ЩИТОВИДНОЙ ЖЕЛЕЗЫ С УЧАСТКАМИ СКЛЕРОЗА. В 26 Л/У ОПУХОЛЕВОГО РОСТА НЕ ОБНАРУЖЕНО.
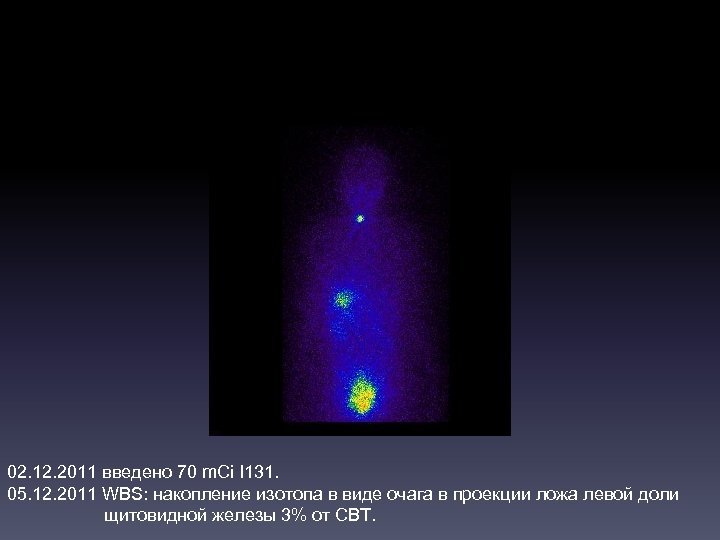 02. 12. 2011 введено 70 m. Ci I 131. 05. 12. 2011 WBS: накопление изотопа в виде очага в проекции ложа левой доли щитовидной железы 3% от СВТ.
02. 12. 2011 введено 70 m. Ci I 131. 05. 12. 2011 WBS: накопление изотопа в виде очага в проекции ложа левой доли щитовидной железы 3% от СВТ.
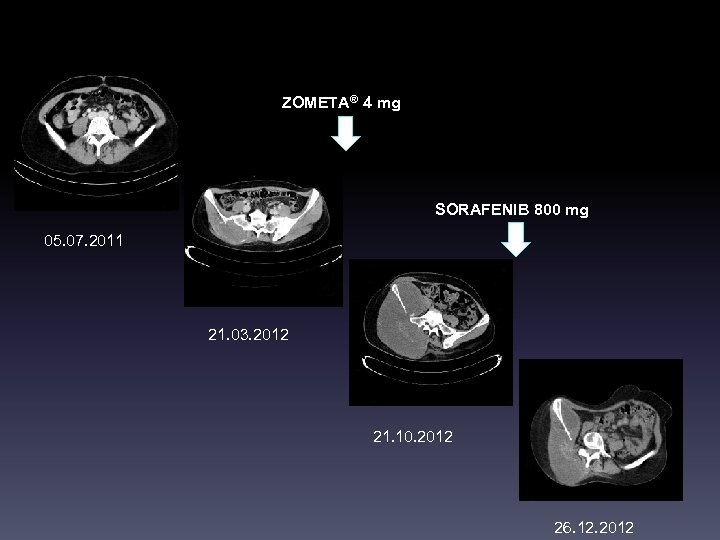 ZOMETA® 4 mg SORAFENIB 800 mg 05. 07. 2011 21. 03. 2012 21. 10. 2012 26. 12. 2012
ZOMETA® 4 mg SORAFENIB 800 mg 05. 07. 2011 21. 03. 2012 21. 10. 2012 26. 12. 2012
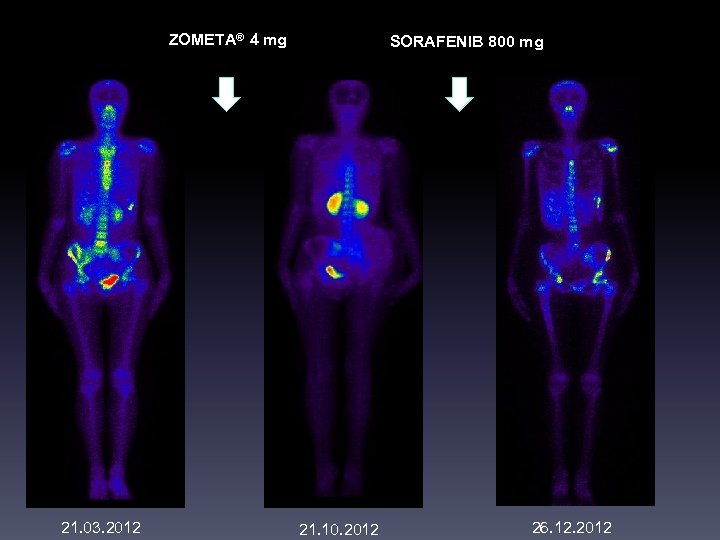 ZOMETA® 4 mg 21. 03. 2012 SORAFENIB 800 mg 21. 10. 2012 26. 12. 2012
ZOMETA® 4 mg 21. 03. 2012 SORAFENIB 800 mg 21. 10. 2012 26. 12. 2012
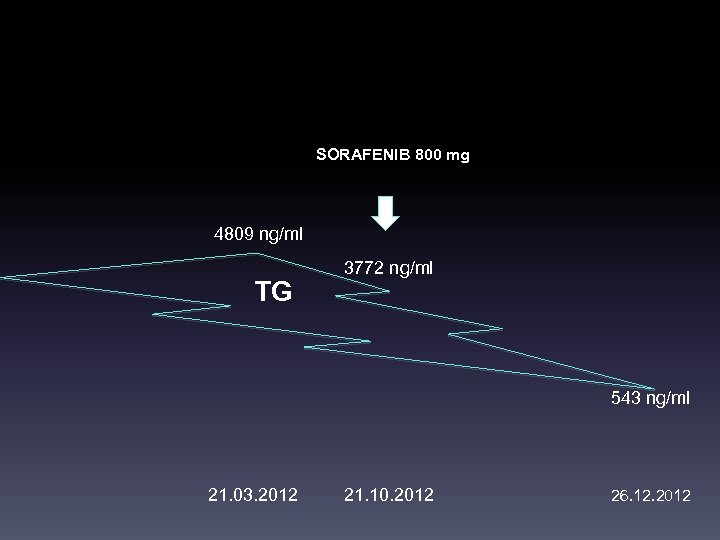 SORAFENIB 800 mg 4809 ng/ml TG 3772 ng/ml 543 ng/ml 21. 03. 2012 21. 10. 2012 26. 12. 2012
SORAFENIB 800 mg 4809 ng/ml TG 3772 ng/ml 543 ng/ml 21. 03. 2012 21. 10. 2012 26. 12. 2012
 Демографические данные пациентов Ленватиниб (n=261) Плацебо (n=131) 64. 0 (27, 89) 61. 0 (21, 81) ≤ 65 лет, n (%) 155 (59. 4) 81 (61. 8) >65 лет, n (%) 106 (40. 6) 50 (38. 2) Мужчины 125 (47. 9) 75 (57. 3) Женщины 136 (52. 1) 56 (42. 7) Европа 131 (50. 2) 64 (48. 9) Северная Америка 77 (29. 5) 39 (29. 8) Другойa 53 (20. 3) 28 (21. 4) Европеоидная 208 (79. 7) 103 (78. 6) Негроидная 4 (1. 5) 4 (3. 1) Азиатская 46 (17. 6) 24 (18. 3) Другая 3 (1. 2) 0 Латиноамериканцы 10 (3. 8) 9 (6. 9) Не латиноамериканцы 251 (96. 2) 122 (93. 1) Медиана возраста, годы (диапазон) Пол, n (%) Регион, n (%) Раса, n (%) Этническое происхождение, n (%) a. Включает Бразилию, Чили, Республику Корея, Российскую Федерацию и Таиланд. 25
Демографические данные пациентов Ленватиниб (n=261) Плацебо (n=131) 64. 0 (27, 89) 61. 0 (21, 81) ≤ 65 лет, n (%) 155 (59. 4) 81 (61. 8) >65 лет, n (%) 106 (40. 6) 50 (38. 2) Мужчины 125 (47. 9) 75 (57. 3) Женщины 136 (52. 1) 56 (42. 7) Европа 131 (50. 2) 64 (48. 9) Северная Америка 77 (29. 5) 39 (29. 8) Другойa 53 (20. 3) 28 (21. 4) Европеоидная 208 (79. 7) 103 (78. 6) Негроидная 4 (1. 5) 4 (3. 1) Азиатская 46 (17. 6) 24 (18. 3) Другая 3 (1. 2) 0 Латиноамериканцы 10 (3. 8) 9 (6. 9) Не латиноамериканцы 251 (96. 2) 122 (93. 1) Медиана возраста, годы (диапазон) Пол, n (%) Регион, n (%) Раса, n (%) Этническое происхождение, n (%) a. Включает Бразилию, Чили, Республику Корея, Российскую Федерацию и Таиланд. 25
 Параметры пациентов Ленватиниб (n=261) Плацебо (n=131) 73. 3 (33, 155) 74. 0 (31, 165) 0 144 (55. 2) 68 (51. 9) 1 104 (39. 8) 61 (46. 6) 2 12 (4. 6) 2 (1. 5) 3 1 (0. 4) 0 0 195 (74. 7) 104 (79. 4) 1 66 (25. 3) 27 (20. 6) 220 (84. 3) 63 (48. 1) ≤ 0. 5 мк. МЕ/мл 226 (86. 6) 120 (91. 6) >0. 5– 2. 0 мк. МЕ/мл 25 (9. 6) 10 (7. 6) >2. 0– 5. 5 мк. МЕ/мл 10 (3. 8) 1 (0. 8) Масса, кг, медиана (диапазон) Общее состояние по шкале ECOG, n (%) Предшествующая таргетная терапия, направленная на VEGF, n (%)a ≥ 1 сопутствующего гипотензивного средства Исходный уровень ТТГ, n (%) a. Различие 26 в частоте предшествующей таргетной терапии, направленной на VEGF, было не значимым (P = 0. 305).
Параметры пациентов Ленватиниб (n=261) Плацебо (n=131) 73. 3 (33, 155) 74. 0 (31, 165) 0 144 (55. 2) 68 (51. 9) 1 104 (39. 8) 61 (46. 6) 2 12 (4. 6) 2 (1. 5) 3 1 (0. 4) 0 0 195 (74. 7) 104 (79. 4) 1 66 (25. 3) 27 (20. 6) 220 (84. 3) 63 (48. 1) ≤ 0. 5 мк. МЕ/мл 226 (86. 6) 120 (91. 6) >0. 5– 2. 0 мк. МЕ/мл 25 (9. 6) 10 (7. 6) >2. 0– 5. 5 мк. МЕ/мл 10 (3. 8) 1 (0. 8) Масса, кг, медиана (диапазон) Общее состояние по шкале ECOG, n (%) Предшествующая таргетная терапия, направленная на VEGF, n (%)a ≥ 1 сопутствующего гипотензивного средства Исходный уровень ТТГ, n (%) a. Различие 26 в частоте предшествующей таргетной терапии, направленной на VEGF, было не значимым (P = 0. 305).
 Параметры заболевания n (%) Папиллярный 141 (54. 0) 71 (54. 2) 92 (35. 2) 41 (31. 3) Низко дифференцированный 28 (10. 7) 19 (14. 5) Все локализации 257 (98. 5) 131 (100) Легких 226 (86. 6) 123 (93. 9) Лимфатические узлы 138 (52. 9) 64 (48. 9) Костиb 104 (39. 8) 48 (36. 6) Плевры 46 (17. 6) 18 (13. 7) Печени 43 (16. 5) 28 (21. 4) Головного мозгаc Метастатическое поражение Плацебо (n=131) Фолликулярный Гистологияa Ленватиниб (n=261) 9 (3. 4) 7 (5. 3) 66. 0 (0. 4, 573. 6) 73. 9 (6. 0, 484. 8) 0. 7 (0. 2, 12. 5) 1. 1 (0. 2, 13. 6) Время с момента первичной диагностики до рандомизации, месяцы, медиана (диапазон) Время с самого последнего прогрессирования заболевания до рандомизации, месяцы, медиана (диапазон) a. Оценка исследователем. (%) пациентов с метастазами только в кости было 12 в группе с ленватинибом (4. 6%) и 3 в плацебо группе (2. 3%). 27 c. Пациенты считались подходящими для участия в исследовании, если ранее получали лечение по поводу метастазов в головной мозг и были в стабильном состоянии без использования стероидов. bn
Параметры заболевания n (%) Папиллярный 141 (54. 0) 71 (54. 2) 92 (35. 2) 41 (31. 3) Низко дифференцированный 28 (10. 7) 19 (14. 5) Все локализации 257 (98. 5) 131 (100) Легких 226 (86. 6) 123 (93. 9) Лимфатические узлы 138 (52. 9) 64 (48. 9) Костиb 104 (39. 8) 48 (36. 6) Плевры 46 (17. 6) 18 (13. 7) Печени 43 (16. 5) 28 (21. 4) Головного мозгаc Метастатическое поражение Плацебо (n=131) Фолликулярный Гистологияa Ленватиниб (n=261) 9 (3. 4) 7 (5. 3) 66. 0 (0. 4, 573. 6) 73. 9 (6. 0, 484. 8) 0. 7 (0. 2, 12. 5) 1. 1 (0. 2, 13. 6) Время с момента первичной диагностики до рандомизации, месяцы, медиана (диапазон) Время с самого последнего прогрессирования заболевания до рандомизации, месяцы, медиана (диапазон) a. Оценка исследователем. (%) пациентов с метастазами только в кости было 12 в группе с ленватинибом (4. 6%) и 3 в плацебо группе (2. 3%). 27 c. Пациенты считались подходящими для участия в исследовании, если ранее получали лечение по поводу метастазов в головной мозг и были в стабильном состоянии без использования стероидов. bn
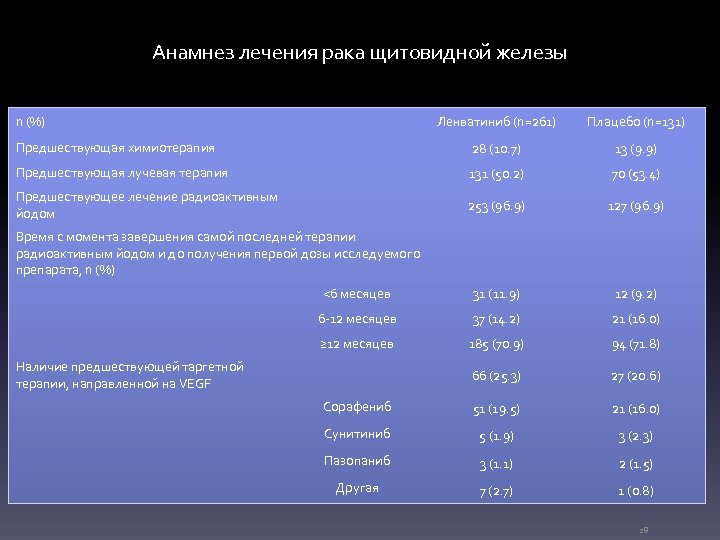 Анамнез лечения рака щитовидной железы n (%) Ленватиниб (n=261) Плацебо (n=131) Предшествующая химиотерапия 28 (10. 7) 13 (9. 9) Предшествующая лучевая терапия 131 (50. 2) 70 (53. 4) Предшествующее лечение радиоактивным йодом 253 (96. 9) 127 (96. 9) <6 месяцев 31 (11. 9) 12 (9. 2) 6 -12 месяцев 37 (14. 2) 21 (16. 0) ≥ 12 месяцев 185 (70. 9) 94 (71. 8) 66 (25. 3) 27 (20. 6) Сорафениб 51 (19. 5) 21 (16. 0) Сунитиниб 5 (1. 9) 3 (2. 3) Пазопаниб 3 (1. 1) 2 (1. 5) Другая 7 (2. 7) 1 (0. 8) Время с момента завершения самой последней терапии радиоактивным йодом и до получения первой дозы исследуемого препарата, n (%) Наличие предшествующей таргетной терапии, направленной на VEGF 28
Анамнез лечения рака щитовидной железы n (%) Ленватиниб (n=261) Плацебо (n=131) Предшествующая химиотерапия 28 (10. 7) 13 (9. 9) Предшествующая лучевая терапия 131 (50. 2) 70 (53. 4) Предшествующее лечение радиоактивным йодом 253 (96. 9) 127 (96. 9) <6 месяцев 31 (11. 9) 12 (9. 2) 6 -12 месяцев 37 (14. 2) 21 (16. 0) ≥ 12 месяцев 185 (70. 9) 94 (71. 8) 66 (25. 3) 27 (20. 6) Сорафениб 51 (19. 5) 21 (16. 0) Сунитиниб 5 (1. 9) 3 (2. 3) Пазопаниб 3 (1. 1) 2 (1. 5) Другая 7 (2. 7) 1 (0. 8) Время с момента завершения самой последней терапии радиоактивным йодом и до получения первой дозы исследуемого препарата, n (%) Наличие предшествующей таргетной терапии, направленной на VEGF 28
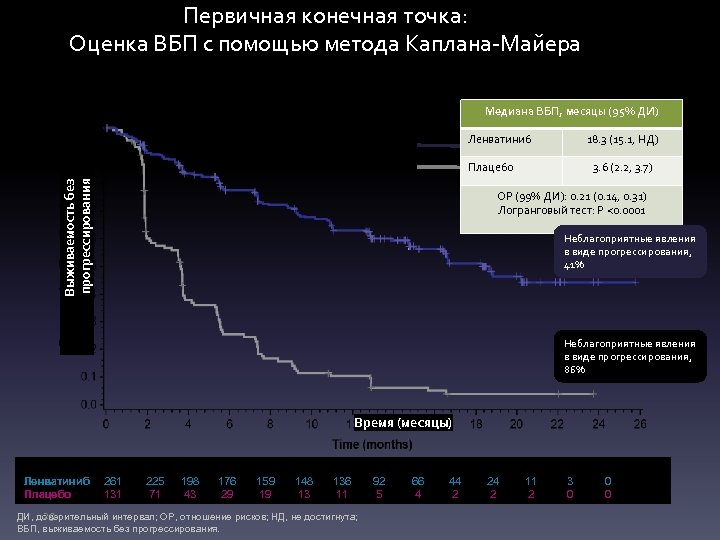 Первичная конечная точка: Оценка ВБП с помощью метода Каплана-Майера Медиана ВБП, месяцы (95% ДИ) Ленватиниб 18. 3 (15. 1, НД) Выживаемость без прогрессирования Плацебо 3. 6 (2. 2, 3. 7) ОР (99% ДИ): 0. 21 (0. 14, 0. 31) Логранговый тест: P <0. 0001 Неблагоприятные явления в виде прогрессирования, 41% Неблагоприятные явления в виде прогрессирования, 86% Время (месяцы) Количество пациентов, подверженных риску Ленватиниб 261 225 198 176 Плацебо 131 71 43 29 159 19 148 13 136 11 29 ДИ, доверительный интервал; ОР, отношение рисков; НД, не достигнута; ВБП, выживаемость без прогрессирования. 92 5 66 4 44 2 24 2 11 2 3 0 0 0
Первичная конечная точка: Оценка ВБП с помощью метода Каплана-Майера Медиана ВБП, месяцы (95% ДИ) Ленватиниб 18. 3 (15. 1, НД) Выживаемость без прогрессирования Плацебо 3. 6 (2. 2, 3. 7) ОР (99% ДИ): 0. 21 (0. 14, 0. 31) Логранговый тест: P <0. 0001 Неблагоприятные явления в виде прогрессирования, 41% Неблагоприятные явления в виде прогрессирования, 86% Время (месяцы) Количество пациентов, подверженных риску Ленватиниб 261 225 198 176 Плацебо 131 71 43 29 159 19 148 13 136 11 29 ДИ, доверительный интервал; ОР, отношение рисков; НД, не достигнута; ВБП, выживаемость без прогрессирования. 92 5 66 4 44 2 24 2 11 2 3 0 0 0
 Частота объективного ответа: независимая оценка n (%) Ленватиниб (n=261) 169 (64. 8) Частота объективного ответа 95% ДИ Плацебо (n=131) 2 (1. 5) 59. 0– 70. 5 0. 0– 3. 6 Р-значение <0. 0001 ПР 4 (1. 5) 0 ЧР 165 (63. 2) 2 (1. 5) СЗ 60 (23. 0) 71 (54. 2) СЗ ≥ 23 недель 40 (15. 3) 39 (29. 8) ПЗ 18 (6. 9) 52 (39. 7) Не поддается оценке/неизвестна 14 (5. 4) 6 (4. 6) 229 (87. 7) 73 (55. 7) 83. 8– 91. 7 47. 2– 64. 2 Частота контроля заболевания 95% ДИ Р-значение Частота клинического ответа <0. 0001 209 (80. 1) 95% ДИ Р-значение 41 (31. 3) 75. 2– 84. 9 23. 4– 39. 2 <0. 0001 Медиана времени до ответа на ленватиниб: 2. 0 месяца (диапазон, 1. 9– 3. 5 месяцев) Медиана продолжительности ответа на ленватиниб: НД (95% ДИ, 16. 8–НД) ПР, полный регресс; ПЗ, прогрессирование заболевания, ЧР, частичный регресс; СЗ, cтабилизация заболевания 30
Частота объективного ответа: независимая оценка n (%) Ленватиниб (n=261) 169 (64. 8) Частота объективного ответа 95% ДИ Плацебо (n=131) 2 (1. 5) 59. 0– 70. 5 0. 0– 3. 6 Р-значение <0. 0001 ПР 4 (1. 5) 0 ЧР 165 (63. 2) 2 (1. 5) СЗ 60 (23. 0) 71 (54. 2) СЗ ≥ 23 недель 40 (15. 3) 39 (29. 8) ПЗ 18 (6. 9) 52 (39. 7) Не поддается оценке/неизвестна 14 (5. 4) 6 (4. 6) 229 (87. 7) 73 (55. 7) 83. 8– 91. 7 47. 2– 64. 2 Частота контроля заболевания 95% ДИ Р-значение Частота клинического ответа <0. 0001 209 (80. 1) 95% ДИ Р-значение 41 (31. 3) 75. 2– 84. 9 23. 4– 39. 2 <0. 0001 Медиана времени до ответа на ленватиниб: 2. 0 месяца (диапазон, 1. 9– 3. 5 месяцев) Медиана продолжительности ответа на ленватиниб: НД (95% ДИ, 16. 8–НД) ПР, полный регресс; ПЗ, прогрессирование заболевания, ЧР, частичный регресс; СЗ, cтабилизация заболевания 30
 Максимальное процентное изменение размера изучаемого очага относительно исходного уровня: Ленватиниб Процентное изменение относительно исходного уровня при минимальном размере Лечебная группа: Ленватиниб Изменение медианы размера опухоли (диапазон): -52% (-100%, +30) Наилучший объективный (общий) ответ (n=245) ПО (n=4) ЧО (n=165) СЗ (n=60) ПЗ (n=16) ПО, полный ответ; ПЗ, прогрессирование заболевания; ЧО, частичный ответ; СЗ, cтабильное заболевание. Schlumberger M et al. NEJM 2015; 372: 621 -30. 31
Максимальное процентное изменение размера изучаемого очага относительно исходного уровня: Ленватиниб Процентное изменение относительно исходного уровня при минимальном размере Лечебная группа: Ленватиниб Изменение медианы размера опухоли (диапазон): -52% (-100%, +30) Наилучший объективный (общий) ответ (n=245) ПО (n=4) ЧО (n=165) СЗ (n=60) ПЗ (n=16) ПО, полный ответ; ПЗ, прогрессирование заболевания; ЧО, частичный ответ; СЗ, cтабильное заболевание. Schlumberger M et al. NEJM 2015; 372: 621 -30. 31
 Подгрупповой анализ 32
Подгрупповой анализ 32
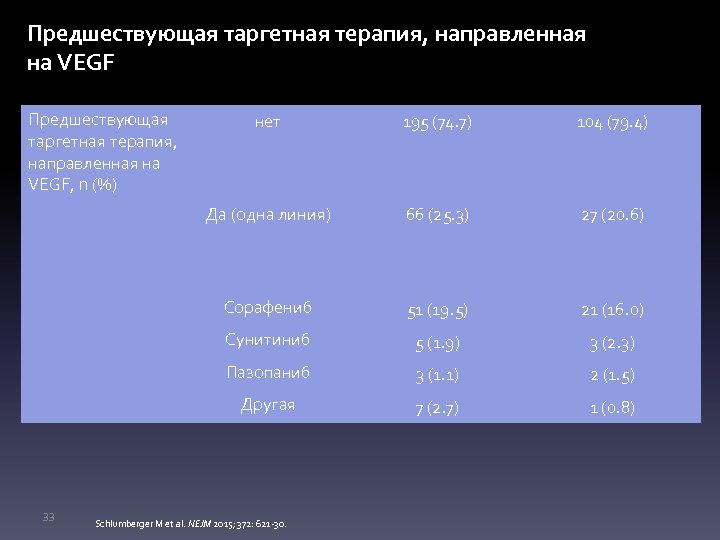 Предшествующая таргетная терапия, направленная на VEGF, n (%) 195 (74. 7) 104 (79. 4) Да (одна линия) 66 (25. 3) 27 (20. 6) Сорафениб 51 (19. 5) 21 (16. 0) Сунитиниб 5 (1. 9) 3 (2. 3) Пазопаниб 3 (1. 1) 2 (1. 5) Другая 33 нет 7 (2. 7) 1 (0. 8) Schlumberger M et al. NEJM 2015; 372: 621 -30.
Предшествующая таргетная терапия, направленная на VEGF, n (%) 195 (74. 7) 104 (79. 4) Да (одна линия) 66 (25. 3) 27 (20. 6) Сорафениб 51 (19. 5) 21 (16. 0) Сунитиниб 5 (1. 9) 3 (2. 3) Пазопаниб 3 (1. 1) 2 (1. 5) Другая 33 нет 7 (2. 7) 1 (0. 8) Schlumberger M et al. NEJM 2015; 372: 621 -30.
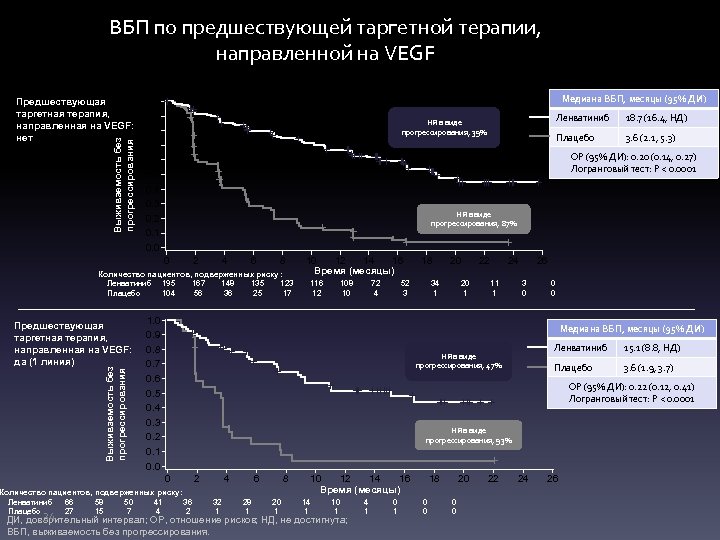 ВБП по предшествующей таргетной терапии, направленной на VEGF Выживаемость без прогрессирования Предшествующая таргетная терапия, направленная на VEGF: нет Медиана ВБП, месяцы (95% ДИ) 1. 0 0. 9 0. 8 0. 7 0. 6 0. 5 0. 4 0. 3 0. 2 0. 1 0. 0 Плацебо 3. 6 (2. 1, 5. 3) НЯ в виде прогрессирования, 87% 2 4 6 8 Количество пациентов, подверженных риску: Ленватиниб 195 167 148 135 123 Плацебо 104 56 36 25 17 Выживаемость без прогрессирования 18. 7 (16. 4, НД) ОР (95% ДИ): 0. 20 (0. 14, 0. 27) Логранговый тест: P < 0. 0001 0 Предшествующая таргетная терапия, направленная на VEGF: да (1 линия) Ленватиниб НЯ в виде прогрессирования, 39% 10 12 14 16 Время (месяцы) 116 12 108 10 72 4 18 52 3 1. 0 0. 9 0. 8 0. 7 0. 6 0. 5 0. 4 0. 3 0. 2 0. 1 0. 0 20 34 1 20 1 22 24 11 1 26 3 0 0 0 Медиана ВБП, месяцы (95% ДИ) Ленватиниб 15. 1 (8. 8, НД) Плацебо НЯ в виде прогрессирования, 47% 3. 6 (1. 9, 3. 7) ОР (95% ДИ): 0. 22 (0. 12, 0. 41) Логранговый тест: P < 0. 0001 НЯ в виде прогрессирования, 93% 0 2 Количество пациентов, подверженных риску: Ленватиниб 66 58 50 41 36 Плацебо 27 15 7 4 2 4 32 6 28 8 20 10 12 14 16 Время (месяцы) 14 10 1 1 1 34 ДИ, доверительный интервал; ОР, отношение рисков; НД, не достигнута; ВБП, выживаемость без прогрессирования. 4 1 0 1 18 0 0 20 0 0 22 24 26
ВБП по предшествующей таргетной терапии, направленной на VEGF Выживаемость без прогрессирования Предшествующая таргетная терапия, направленная на VEGF: нет Медиана ВБП, месяцы (95% ДИ) 1. 0 0. 9 0. 8 0. 7 0. 6 0. 5 0. 4 0. 3 0. 2 0. 1 0. 0 Плацебо 3. 6 (2. 1, 5. 3) НЯ в виде прогрессирования, 87% 2 4 6 8 Количество пациентов, подверженных риску: Ленватиниб 195 167 148 135 123 Плацебо 104 56 36 25 17 Выживаемость без прогрессирования 18. 7 (16. 4, НД) ОР (95% ДИ): 0. 20 (0. 14, 0. 27) Логранговый тест: P < 0. 0001 0 Предшествующая таргетная терапия, направленная на VEGF: да (1 линия) Ленватиниб НЯ в виде прогрессирования, 39% 10 12 14 16 Время (месяцы) 116 12 108 10 72 4 18 52 3 1. 0 0. 9 0. 8 0. 7 0. 6 0. 5 0. 4 0. 3 0. 2 0. 1 0. 0 20 34 1 20 1 22 24 11 1 26 3 0 0 0 Медиана ВБП, месяцы (95% ДИ) Ленватиниб 15. 1 (8. 8, НД) Плацебо НЯ в виде прогрессирования, 47% 3. 6 (1. 9, 3. 7) ОР (95% ДИ): 0. 22 (0. 12, 0. 41) Логранговый тест: P < 0. 0001 НЯ в виде прогрессирования, 93% 0 2 Количество пациентов, подверженных риску: Ленватиниб 66 58 50 41 36 Плацебо 27 15 7 4 2 4 32 6 28 8 20 10 12 14 16 Время (месяцы) 14 10 1 1 1 34 ДИ, доверительный интервал; ОР, отношение рисков; НД, не достигнута; ВБП, выживаемость без прогрессирования. 4 1 0 1 18 0 0 20 0 0 22 24 26
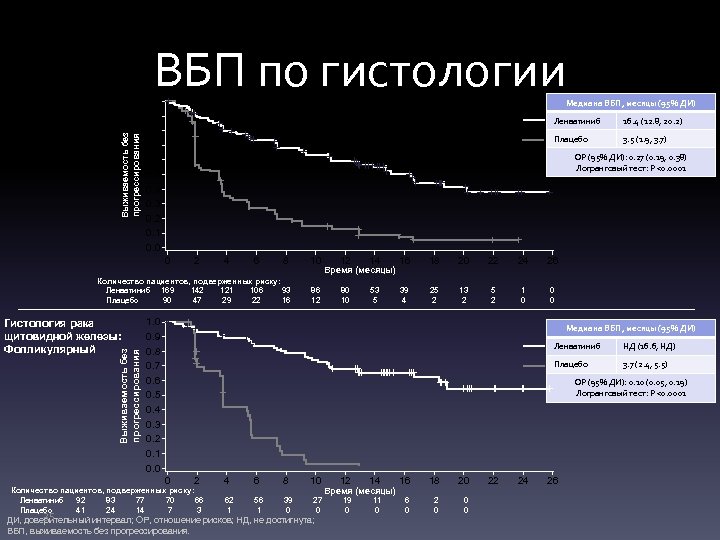 Выживаемость без прогрессирования Гистология рака щитовидной железы: Папиллярный ВБП по гистологии 1. 0 0. 9 0. 8 0. 7 0. 6 0. 5 0. 4 0. 3 0. 2 0. 1 0. 0 Медиана ВБП, месяцы (95% ДИ) Ленватиниб Плацебо 8 10 Количество пациентов, подверженных риску: Ленватиниб 169 142 121 106 93 Плацебо 90 47 29 22 16 86 12 Выживаемость без прогрессирования 3. 5 (1. 9, 3. 7) ОР (95% ДИ): 0. 27 (0. 19, 0. 38) Логранговый тест: P <0. 0001 0 Гистология рака щитовидной железы: Фолликулярный 16. 4 (12. 8, 20. 2) 2 4 6 12 14 16 18 20 22 24 26 80 10 53 5 39 4 25 2 13 2 5 2 1 0 0 0 Время (месяцы) 1. 0 0. 9 0. 8 0. 7 0. 6 0. 5 0. 4 0. 3 0. 2 0. 1 0. 0 Медиана ВБП, месяцы (95% ДИ) Ленватиниб НД (16. 6, НД) Плацебо 3. 7 (2. 4, 5. 5) ОР (95% ДИ): 0. 10 (0. 05, 0. 19) Логранговый тест: P <0. 0001 0 2 Количество пациентов, подверженных риску: Ленватиниб 92 83 77 70 66 Плацебо 41 24 14 7 3 4 6 8 10 62 1 56 1 39 0 27 0 35 ДИ, доверительный интервал; ОР, отношение рисков; НД, не достигнута; ВБП, выживаемость без прогрессирования. 12 14 16 18 20 19 0 11 0 6 0 2 0 0 0 Время (месяцы) 22 24 26
Выживаемость без прогрессирования Гистология рака щитовидной железы: Папиллярный ВБП по гистологии 1. 0 0. 9 0. 8 0. 7 0. 6 0. 5 0. 4 0. 3 0. 2 0. 1 0. 0 Медиана ВБП, месяцы (95% ДИ) Ленватиниб Плацебо 8 10 Количество пациентов, подверженных риску: Ленватиниб 169 142 121 106 93 Плацебо 90 47 29 22 16 86 12 Выживаемость без прогрессирования 3. 5 (1. 9, 3. 7) ОР (95% ДИ): 0. 27 (0. 19, 0. 38) Логранговый тест: P <0. 0001 0 Гистология рака щитовидной железы: Фолликулярный 16. 4 (12. 8, 20. 2) 2 4 6 12 14 16 18 20 22 24 26 80 10 53 5 39 4 25 2 13 2 5 2 1 0 0 0 Время (месяцы) 1. 0 0. 9 0. 8 0. 7 0. 6 0. 5 0. 4 0. 3 0. 2 0. 1 0. 0 Медиана ВБП, месяцы (95% ДИ) Ленватиниб НД (16. 6, НД) Плацебо 3. 7 (2. 4, 5. 5) ОР (95% ДИ): 0. 10 (0. 05, 0. 19) Логранговый тест: P <0. 0001 0 2 Количество пациентов, подверженных риску: Ленватиниб 92 83 77 70 66 Плацебо 41 24 14 7 3 4 6 8 10 62 1 56 1 39 0 27 0 35 ДИ, доверительный интервал; ОР, отношение рисков; НД, не достигнута; ВБП, выживаемость без прогрессирования. 12 14 16 18 20 19 0 11 0 6 0 2 0 0 0 Время (месяцы) 22 24 26
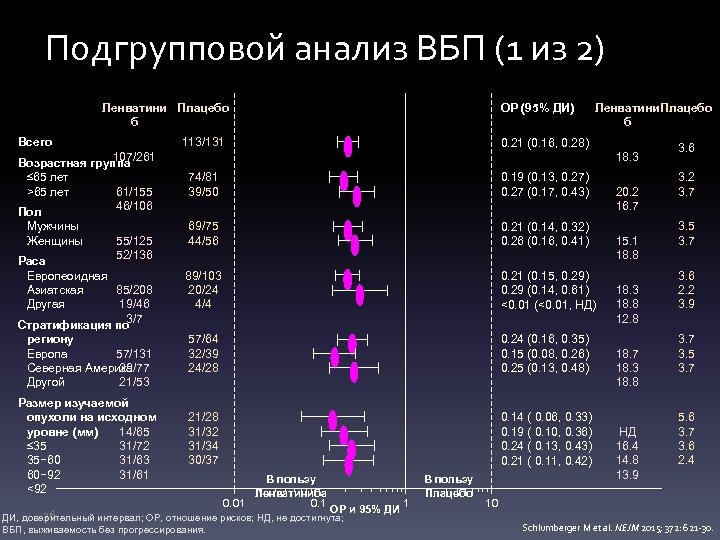 Подгрупповой анализ ВБП (1 из 2) Пациенты, достигшие ВБП/N Ленватини Плацебо б Всего 113/131 107/261 Возрастная группа ≤ 65 лет >65 лет 61/155 46/106 Пол Мужчины Женщины ОР (95% ДИ) 55/125 52/136 Раса Европеоидная 85/208 Азиатская 19/46 Другая 3/7 Стратификация по региону 57/131 Европа 29/77 Северная Америка 21/53 Другой Размер изучаемой опухоли на исходном 14/65 уровне (мм) 31/72 ≤ 35 31/63 35− 60 31/61 60− 92 <92 Медиана (месяцы) Ленватини Плацебо б 0. 21 (0. 16, 0. 28) 18. 3 74/81 39/50 0. 19 (0. 13, 0. 27) 0. 27 (0. 17, 0. 43) 69/75 44/56 0. 21 (0. 14, 0. 32) 0. 26 (0. 16, 0. 41) 89/103 20/24 4/4 0. 21 (0. 15, 0. 29) 0. 29 (0. 14, 0. 61) <0. 01 (<0. 01, НД) 57/64 32/39 24/28 0. 24 (0. 16, 0. 35) 0. 15 (0. 08, 0. 26) 0. 25 (0. 13, 0. 48) 21/28 31/32 31/34 30/37 0. 14 ( 0. 06, 0. 33) 0. 19 ( 0. 10, 0. 36) 0. 24 ( 0. 13, 0. 43) 0. 21 ( 0. 11, 0. 42) В пользу Ленватиниба 0. 01 0. 1 ОР и 95% ДИ 36 ДИ, доверительный интервал; ОР, отношение рисков; НД, не достигнута; ВБП, выживаемость без прогрессирования. 1 В пользу Плацебо 20. 2 16. 7 15. 1 18. 8 18. 3 18. 8 12. 8 18. 7 18. 3 18. 8 НД 16. 4 14. 8 13. 9 3. 6 3. 2 3. 7 3. 5 3. 7 3. 6 2. 2 3. 9 3. 7 3. 5 3. 7 5. 6 3. 7 3. 6 2. 4 10 Schlumberger M et al. NEJM 2015; 372: 621 -30.
Подгрупповой анализ ВБП (1 из 2) Пациенты, достигшие ВБП/N Ленватини Плацебо б Всего 113/131 107/261 Возрастная группа ≤ 65 лет >65 лет 61/155 46/106 Пол Мужчины Женщины ОР (95% ДИ) 55/125 52/136 Раса Европеоидная 85/208 Азиатская 19/46 Другая 3/7 Стратификация по региону 57/131 Европа 29/77 Северная Америка 21/53 Другой Размер изучаемой опухоли на исходном 14/65 уровне (мм) 31/72 ≤ 35 31/63 35− 60 31/61 60− 92 <92 Медиана (месяцы) Ленватини Плацебо б 0. 21 (0. 16, 0. 28) 18. 3 74/81 39/50 0. 19 (0. 13, 0. 27) 0. 27 (0. 17, 0. 43) 69/75 44/56 0. 21 (0. 14, 0. 32) 0. 26 (0. 16, 0. 41) 89/103 20/24 4/4 0. 21 (0. 15, 0. 29) 0. 29 (0. 14, 0. 61) <0. 01 (<0. 01, НД) 57/64 32/39 24/28 0. 24 (0. 16, 0. 35) 0. 15 (0. 08, 0. 26) 0. 25 (0. 13, 0. 48) 21/28 31/32 31/34 30/37 0. 14 ( 0. 06, 0. 33) 0. 19 ( 0. 10, 0. 36) 0. 24 ( 0. 13, 0. 43) 0. 21 ( 0. 11, 0. 42) В пользу Ленватиниба 0. 01 0. 1 ОР и 95% ДИ 36 ДИ, доверительный интервал; ОР, отношение рисков; НД, не достигнута; ВБП, выживаемость без прогрессирования. 1 В пользу Плацебо 20. 2 16. 7 15. 1 18. 8 18. 3 18. 8 12. 8 18. 7 18. 3 18. 8 НД 16. 4 14. 8 13. 9 3. 6 3. 2 3. 7 3. 5 3. 7 3. 6 2. 2 3. 9 3. 7 3. 5 3. 7 5. 6 3. 7 3. 6 2. 4 10 Schlumberger M et al. NEJM 2015; 372: 621 -30.
 Подгрупповой анализ ВБП (2 из 2) Пациенты, достигшие ВБП/N ОР (95% ДИ) Ленватин Плацебо Предшествующее лечениеиб 88/104 VEGF 25/27 76/195 0 31/66 1 18/19 Гистология 57/68 14/28 Низко дифференцированный 3/3 57/133 Папиллярный 35/41 4/8 Папиллярный неизвестный 32/92 Фолликулярный Исходный уровень ТТГ 91/226 (мк. МЕ/л) 11/25 ≤ 0. 5 5/10 >0. 5 – 2. 0 >2. 0 – 5. 5 60/157 Метастазы в кости 47/104 Нет Есть 104/249 Метастазы только в кости 3/12 Нет Есть 17/35 Метастазы в легких 90/226 Нет Есть 0. 20 (0. 14, 0. 27) 0. 22 (0. 12, 0. 41) 0. 21 ( 0. 08, 0. 56) 0. 29 ( 0. 19, 0. 43) 0. 39 ( 0. 03, 4. 44) 0. 10 (0. 05, 0. 19) 105/120 7/10 1/1 0. 20 (0. 14, 0. 27) 0. 35 (0. 09, 1. 39) <0. 01 (<0. 01, НД) 74/83 39/48 0. 18 ( 0. 12, 0. 27) 0. 26 ( 0. 16, 0. 42) 110/128 3/3 0. 21 ( 0. 16, 0. 28) 0. 65 ( 0. 11, 4. 07) 8/8 105/123 0. 21 ( 0. 07, 0. 66) 0. 21 ( 0. 15, 0. 29) В пользу Ленватиниба 0. 01 0. 1 ОР и 95% ДИ 1 37 ДИ, доверительный интервал; ОР, отношение рисков; НД, не достигнута; ВБП, выживаемость без прогрессирования. Медиана (месяцы) Ленватин Плацебо иб В пользу Плацебо 18. 7 15. 1 14. 8 16. 6 10. 9 НД 18. 7 15. 1 НД 20. 2 14. 8 18. 3 НД 14. 8 18. 7 3. 6 2. 1 3. 5 9. 0 3. 7 3. 6 5. 4 1. 9 3. 7 2. 1 3. 6 7. 4 2. 3 3. 6 10 Schlumberger M et al. NEJM 2015; 372: 621 -30.
Подгрупповой анализ ВБП (2 из 2) Пациенты, достигшие ВБП/N ОР (95% ДИ) Ленватин Плацебо Предшествующее лечениеиб 88/104 VEGF 25/27 76/195 0 31/66 1 18/19 Гистология 57/68 14/28 Низко дифференцированный 3/3 57/133 Папиллярный 35/41 4/8 Папиллярный неизвестный 32/92 Фолликулярный Исходный уровень ТТГ 91/226 (мк. МЕ/л) 11/25 ≤ 0. 5 5/10 >0. 5 – 2. 0 >2. 0 – 5. 5 60/157 Метастазы в кости 47/104 Нет Есть 104/249 Метастазы только в кости 3/12 Нет Есть 17/35 Метастазы в легких 90/226 Нет Есть 0. 20 (0. 14, 0. 27) 0. 22 (0. 12, 0. 41) 0. 21 ( 0. 08, 0. 56) 0. 29 ( 0. 19, 0. 43) 0. 39 ( 0. 03, 4. 44) 0. 10 (0. 05, 0. 19) 105/120 7/10 1/1 0. 20 (0. 14, 0. 27) 0. 35 (0. 09, 1. 39) <0. 01 (<0. 01, НД) 74/83 39/48 0. 18 ( 0. 12, 0. 27) 0. 26 ( 0. 16, 0. 42) 110/128 3/3 0. 21 ( 0. 16, 0. 28) 0. 65 ( 0. 11, 4. 07) 8/8 105/123 0. 21 ( 0. 07, 0. 66) 0. 21 ( 0. 15, 0. 29) В пользу Ленватиниба 0. 01 0. 1 ОР и 95% ДИ 1 37 ДИ, доверительный интервал; ОР, отношение рисков; НД, не достигнута; ВБП, выживаемость без прогрессирования. Медиана (месяцы) Ленватин Плацебо иб В пользу Плацебо 18. 7 15. 1 14. 8 16. 6 10. 9 НД 18. 7 15. 1 НД 20. 2 14. 8 18. 3 НД 14. 8 18. 7 3. 6 2. 1 3. 5 9. 0 3. 7 3. 6 5. 4 1. 9 3. 7 2. 1 3. 6 7. 4 2. 3 3. 6 10 Schlumberger M et al. NEJM 2015; 372: 621 -30.
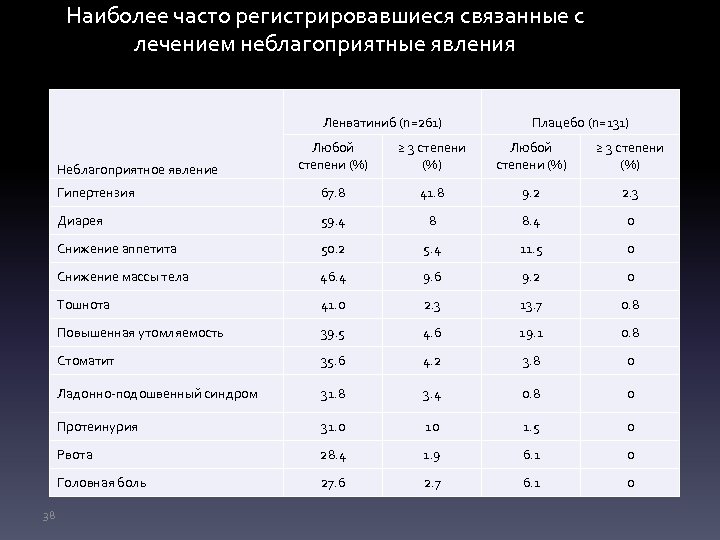 Наиболее часто регистрировавшиеся связанные с лечением неблагоприятные явления Ленватиниб (n=261) Плацебо (n=131) Любой степени (%) ≥ 3 степени (%) Гипертензия 67. 8 41. 8 9. 2 2. 3 Диарея 59. 4 8 8. 4 0 Снижение аппетита 50. 2 5. 4 11. 5 0 Снижение массы тела 46. 4 9. 6 9. 2 0 Тошнота 41. 0 2. 3 13. 7 0. 8 Повышенная утомляемость 39. 5 4. 6 19. 1 0. 8 Стоматит 35. 6 4. 2 3. 8 0 Ладонно-подошвенный синдром 31. 8 3. 4 0. 8 0 Протеинурия 31. 0 10 1. 5 0 Рвота 28. 4 1. 9 6. 1 0 Головная боль 27. 6 2. 7 6. 1 0 Неблагоприятное явление 38
Наиболее часто регистрировавшиеся связанные с лечением неблагоприятные явления Ленватиниб (n=261) Плацебо (n=131) Любой степени (%) ≥ 3 степени (%) Гипертензия 67. 8 41. 8 9. 2 2. 3 Диарея 59. 4 8 8. 4 0 Снижение аппетита 50. 2 5. 4 11. 5 0 Снижение массы тела 46. 4 9. 6 9. 2 0 Тошнота 41. 0 2. 3 13. 7 0. 8 Повышенная утомляемость 39. 5 4. 6 19. 1 0. 8 Стоматит 35. 6 4. 2 3. 8 0 Ладонно-подошвенный синдром 31. 8 3. 4 0. 8 0 Протеинурия 31. 0 10 1. 5 0 Рвота 28. 4 1. 9 6. 1 0 Головная боль 27. 6 2. 7 6. 1 0 Неблагоприятное явление 38
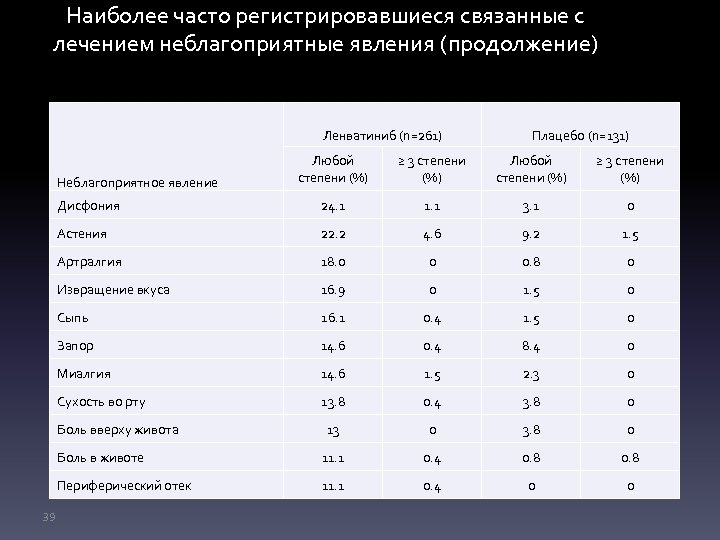 Наиболее часто регистрировавшиеся связанные с лечением неблагоприятные явления (продолжение) Ленватиниб (n=261) Плацебо (n=131) Любой степени (%) ≥ 3 степени (%) Дисфония 24. 1 1. 1 3. 1 0 Астения 22. 2 4. 6 9. 2 1. 5 Артралгия 18. 0 0 0. 8 0 Извращение вкуса 16. 9 0 1. 5 0 Сыпь 16. 1 0. 4 1. 5 0 Запор 14. 6 0. 4 8. 4 0 Миалгия 14. 6 1. 5 2. 3 0 Сухость во рту 13. 8 0. 4 3. 8 0 13 0 3. 8 0 Боль в животе 11. 1 0. 4 0. 8 Периферический отек 11. 1 0. 4 0 0 Неблагоприятное явление Боль вверху живота 39
Наиболее часто регистрировавшиеся связанные с лечением неблагоприятные явления (продолжение) Ленватиниб (n=261) Плацебо (n=131) Любой степени (%) ≥ 3 степени (%) Дисфония 24. 1 1. 1 3. 1 0 Астения 22. 2 4. 6 9. 2 1. 5 Артралгия 18. 0 0 0. 8 0 Извращение вкуса 16. 9 0 1. 5 0 Сыпь 16. 1 0. 4 1. 5 0 Запор 14. 6 0. 4 8. 4 0 Миалгия 14. 6 1. 5 2. 3 0 Сухость во рту 13. 8 0. 4 3. 8 0 13 0 3. 8 0 Боль в животе 11. 1 0. 4 0. 8 Периферический отек 11. 1 0. 4 0 0 Неблагоприятное явление Боль вверху живота 39
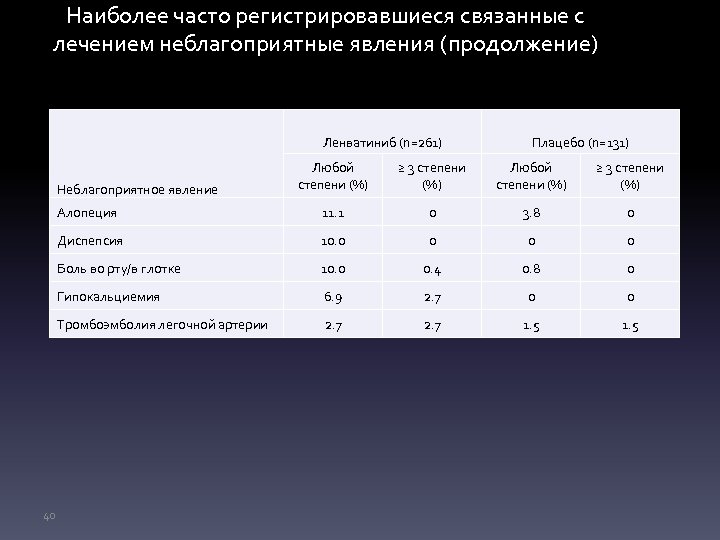 Наиболее часто регистрировавшиеся связанные с лечением неблагоприятные явления (продолжение) Ленватиниб (n=261) Плацебо (n=131) Любой степени (%) ≥ 3 степени (%) Алопеция 11. 1 0 3. 8 0 Диспепсия 10. 0 0 Боль во рту/в глотке 10. 0 0. 4 0. 8 0 Гипокальциемия 6. 9 2. 7 0 0 Тромбоэмболия легочной артерии 2. 7 1. 5 Неблагоприятное явление 40
Наиболее часто регистрировавшиеся связанные с лечением неблагоприятные явления (продолжение) Ленватиниб (n=261) Плацебо (n=131) Любой степени (%) ≥ 3 степени (%) Алопеция 11. 1 0 3. 8 0 Диспепсия 10. 0 0 Боль во рту/в глотке 10. 0 0. 4 0. 8 0 Гипокальциемия 6. 9 2. 7 0 0 Тромбоэмболия легочной артерии 2. 7 1. 5 Неблагоприятное явление 40
 Больной К. , 1964 г. р. , Жалобы: на кашель, одышку, слабость. v. В декабре 2009 года обнаружил асимметрию шеи. В марте 2010 года появились боли, осмотрен отоларингологом, назначена противовоспалительная терапия, боли купировались, однако асимметрия шеи осталась. v. При дополнительном обследовании выявлена узловая патология щитовидной железы. Выполнена пункционная биопсия лимфоузлов шеи и объемных образований щитовидной железы. Цитологическое заключение № 440 - 42 от 20. 04. 2010 фолликулярный рак щитовидной железы. v 25. 05. 2010 выполнена операция - модифицирванная радикальная шейная диссекция (уровни I-VI), тиреоидэктомия. Гистологическое исследование № 3896 от 28. 05. 2010 фолликулярный рак щитовидной железы с тотальным замещением ткани железы, прорастанием капсулы щитовидной железы в окружающие ткани. В регионарных лимфоузлах метастазы аналогичного рака.
Больной К. , 1964 г. р. , Жалобы: на кашель, одышку, слабость. v. В декабре 2009 года обнаружил асимметрию шеи. В марте 2010 года появились боли, осмотрен отоларингологом, назначена противовоспалительная терапия, боли купировались, однако асимметрия шеи осталась. v. При дополнительном обследовании выявлена узловая патология щитовидной железы. Выполнена пункционная биопсия лимфоузлов шеи и объемных образований щитовидной железы. Цитологическое заключение № 440 - 42 от 20. 04. 2010 фолликулярный рак щитовидной железы. v 25. 05. 2010 выполнена операция - модифицирванная радикальная шейная диссекция (уровни I-VI), тиреоидэктомия. Гистологическое исследование № 3896 от 28. 05. 2010 фолликулярный рак щитовидной железы с тотальным замещением ткани железы, прорастанием капсулы щитовидной железы в окружающие ткани. В регионарных лимфоузлах метастазы аналогичного рака.
 Больной К. , 1964 г. р. , v. В 2010 - 11 проведено четыре курса радиойодтерапии (12 ГБк) и селективная шейная диссекция (уровни III-VI), трахеостомия. v. При очередном обследовании в мае 2012 году выявлен продолженный рост метастазов РЩЖ в передне-верхнем средостении и в легких. • По условиям протокола в исследование включались пациенты прогрессирующие на фоне терапии радиоактивным йодом (131 I), фактом прогрессирования было принято считать рост имеющихся метастатических очагов и/или появление новых. v. В августе 2012 года включен в клиническое исследование E 7080 -G 000 -303, группа «препарат» Lenvantinib 24 мг/день (ежедневно).
Больной К. , 1964 г. р. , v. В 2010 - 11 проведено четыре курса радиойодтерапии (12 ГБк) и селективная шейная диссекция (уровни III-VI), трахеостомия. v. При очередном обследовании в мае 2012 году выявлен продолженный рост метастазов РЩЖ в передне-верхнем средостении и в легких. • По условиям протокола в исследование включались пациенты прогрессирующие на фоне терапии радиоактивным йодом (131 I), фактом прогрессирования было принято считать рост имеющихся метастатических очагов и/или появление новых. v. В августе 2012 года включен в клиническое исследование E 7080 -G 000 -303, группа «препарат» Lenvantinib 24 мг/день (ежедневно).
 Больной К. , 1964 г. р. , Нежелательные явления. v. Гипотиреоз 21. 08. 2013 TSG 9. 63 (0. 34 – 5. 60 m. IU/L). Диапазон TSG от 5. 46 – 56. 06 m. IU/L. v. Тошнота, рвота, диарея с 16. 07. 2013 – интермитирующий характер. v. Снижение массы тела со 111 кг (08. 2012) до 67 кг (23. 09. 2013) – в н. в. 81 кг. v. Утомляемость с 12. 01. 2015 – интермитирующий характер. v 15. 06. 2015 на ЭКГ зафиксирована синусовая брадикардия. ЧСС 47 уд в 1 мин. A-V блокада II степени по типу Мобитц II (с периодикой Самойлова-Венкебаха). Неспецифические изменения передней стенки левого желудочка (депрессия STI, II, элевация STv 1 -v 2). Осмотрен кардиологом. В плановом порядке установлен ЭКС
Больной К. , 1964 г. р. , Нежелательные явления. v. Гипотиреоз 21. 08. 2013 TSG 9. 63 (0. 34 – 5. 60 m. IU/L). Диапазон TSG от 5. 46 – 56. 06 m. IU/L. v. Тошнота, рвота, диарея с 16. 07. 2013 – интермитирующий характер. v. Снижение массы тела со 111 кг (08. 2012) до 67 кг (23. 09. 2013) – в н. в. 81 кг. v. Утомляемость с 12. 01. 2015 – интермитирующий характер. v 15. 06. 2015 на ЭКГ зафиксирована синусовая брадикардия. ЧСС 47 уд в 1 мин. A-V блокада II степени по типу Мобитц II (с периодикой Самойлова-Венкебаха). Неспецифические изменения передней стенки левого желудочка (депрессия STI, II, элевация STv 1 -v 2). Осмотрен кардиологом. В плановом порядке установлен ЭКС
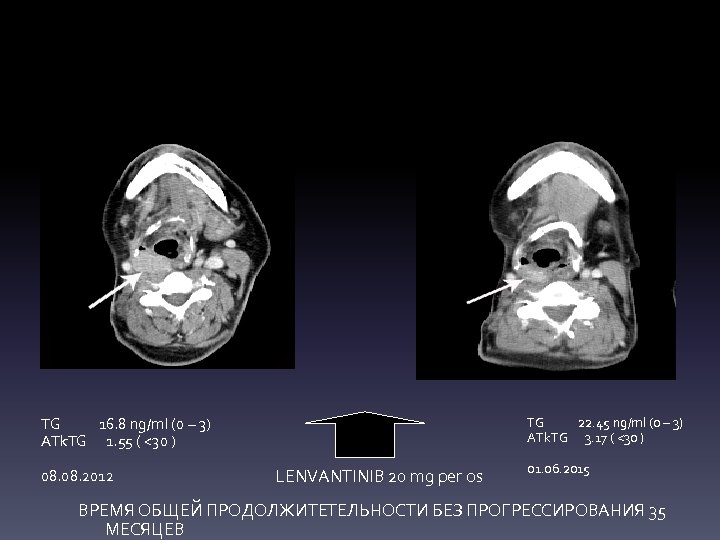 TG 16. 8 ng/ml (0 – 3) ATk. TG 1. 55 ( <30 ) 08. 2012 TG 22. 45 ng/ml (0 – 3) ATk. TG 3. 17 ( <30 ) LENVANTINIB 20 mg per os 01. 06. 2015 ВРЕМЯ ОБЩЕЙ ПРОДОЛЖИТЕТЕЛЬНОСТИ БЕЗ ПРОГРЕССИРОВАНИЯ 35 МЕСЯЦЕВ
TG 16. 8 ng/ml (0 – 3) ATk. TG 1. 55 ( <30 ) 08. 2012 TG 22. 45 ng/ml (0 – 3) ATk. TG 3. 17 ( <30 ) LENVANTINIB 20 mg per os 01. 06. 2015 ВРЕМЯ ОБЩЕЙ ПРОДОЛЖИТЕТЕЛЬНОСТИ БЕЗ ПРОГРЕССИРОВАНИЯ 35 МЕСЯЦЕВ
 Больная Л. , 1964 г. р. , Жалобы: на наличие опухолевого конгломерата шеи слева. v. Патология выявлена при пальпации эндокринологом, как узловой зоб, рекомендовано оперативное лечение. В мае 1989 года выполнена операция - гемитиреоидэктомия справа. Гистологическое исследование: коллоидный зоб. v. В 08. 06. 2006 операция – гемитиреоидэктомия слева, селективная шейная диссекция (уровень VI). Гистологическое исследование: папиллярный рак щитовидной железы, в регионарных лимфоузлах метастазы рака аналогичного строения. v. При очередном обследовании в августе 2007 года выявлен продолженный рост метастазов ПРЩЖ в лимфоузлах шеи слева. 26. 09. 07 операция – радикальная шейная диссекция (уровни I-V). Гистологическое исследование № 36329 папиллярный рак щитовидной железы фолликулярного строения, врастающий в стенку яремной вены, отдельно- комплексы папиллярного рака располагаются в жировой ткани.
Больная Л. , 1964 г. р. , Жалобы: на наличие опухолевого конгломерата шеи слева. v. Патология выявлена при пальпации эндокринологом, как узловой зоб, рекомендовано оперативное лечение. В мае 1989 года выполнена операция - гемитиреоидэктомия справа. Гистологическое исследование: коллоидный зоб. v. В 08. 06. 2006 операция – гемитиреоидэктомия слева, селективная шейная диссекция (уровень VI). Гистологическое исследование: папиллярный рак щитовидной железы, в регионарных лимфоузлах метастазы рака аналогичного строения. v. При очередном обследовании в августе 2007 года выявлен продолженный рост метастазов ПРЩЖ в лимфоузлах шеи слева. 26. 09. 07 операция – радикальная шейная диссекция (уровни I-V). Гистологическое исследование № 36329 папиллярный рак щитовидной железы фолликулярного строения, врастающий в стенку яремной вены, отдельно- комплексы папиллярного рака располагаются в жировой ткани.
 Больная Л. , 1964 г. р. , v. В октябре 2007 года проведен курс ДЛТ на область шеи СОД 52 Гр. v 18. 02. 2008 проведен курс радиойодтерапии (3 ГБк). WBS: на шее слева 37% v. В мае 2009 года при СКТ выявлены метастазы ПРЩЖ в лимфоузлах шеи слева и в левом легком. v 11. 03. 2010 проведен курс радиойодтерапии (3 ГБк). WBS: на шее слева 6%, диффузное накопление в проекции легких справа 11%, слева 9%. v 23. 09. 2010 проведен курс радиойодтерапии (4 ГБк). WBS: на шее слева 5%, диффузное накопление в проекции легких 16%. v 01. 04. 2011 проведен курс радиойодтерапии (3 ГБк). WBS: на шее слева 6%, диффузное накопление в проекции легких 12%. v 08. 07. 2011 проведен курс радиойодтерапии (3 ГБк). WBS: на шее слева 6%, диффузное накопление в проекции легких 10%.
Больная Л. , 1964 г. р. , v. В октябре 2007 года проведен курс ДЛТ на область шеи СОД 52 Гр. v 18. 02. 2008 проведен курс радиойодтерапии (3 ГБк). WBS: на шее слева 37% v. В мае 2009 года при СКТ выявлены метастазы ПРЩЖ в лимфоузлах шеи слева и в левом легком. v 11. 03. 2010 проведен курс радиойодтерапии (3 ГБк). WBS: на шее слева 6%, диффузное накопление в проекции легких справа 11%, слева 9%. v 23. 09. 2010 проведен курс радиойодтерапии (4 ГБк). WBS: на шее слева 5%, диффузное накопление в проекции легких 16%. v 01. 04. 2011 проведен курс радиойодтерапии (3 ГБк). WBS: на шее слева 6%, диффузное накопление в проекции легких 12%. v 08. 07. 2011 проведен курс радиойодтерапии (3 ГБк). WBS: на шее слева 6%, диффузное накопление в проекции легких 10%.
 Больная Л. , 1964 г. р. , v 12. 01. 2012 проведен курс радиойодтерапии (3 ГБк). WBS: на шее слева 32%, диффузное накопление в проекции легких 7%. v 18. 04. 2012 в области послеоперационного рубца на шее и в левой надключичной области наблюдается продолженный рост опухоли, рекомендована ПХТ. v. По данным СКТ 22. 08. 2012 на шее в ложе удаленной щитовидной железы определяется дополнительное мягкотканное образование, занимающее над и подключичные области, распространяется в передне-верхнее средостение, на мягкие ткани передней грудной стенки, разрушает грудинный конец ключицы, 106*87 мм. Метастатическое поражение легких и лимфатического узла малой грудной мышцы слева. v. С 30. 08. 2012 включена в клиническое исследование E 7080 -G 000 -303, группа «препарат» Lenvantinib 24 мг/день (ежедневно).
Больная Л. , 1964 г. р. , v 12. 01. 2012 проведен курс радиойодтерапии (3 ГБк). WBS: на шее слева 32%, диффузное накопление в проекции легких 7%. v 18. 04. 2012 в области послеоперационного рубца на шее и в левой надключичной области наблюдается продолженный рост опухоли, рекомендована ПХТ. v. По данным СКТ 22. 08. 2012 на шее в ложе удаленной щитовидной железы определяется дополнительное мягкотканное образование, занимающее над и подключичные области, распространяется в передне-верхнее средостение, на мягкие ткани передней грудной стенки, разрушает грудинный конец ключицы, 106*87 мм. Метастатическое поражение легких и лимфатического узла малой грудной мышцы слева. v. С 30. 08. 2012 включена в клиническое исследование E 7080 -G 000 -303, группа «препарат» Lenvantinib 24 мг/день (ежедневно).
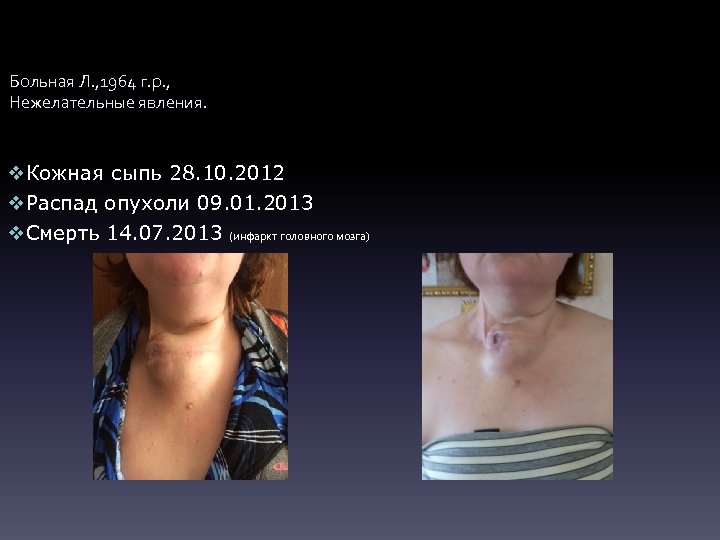 Больная Л. , 1964 г. р. , Нежелательные явления. v. Кожная сыпь 28. 10. 2012 v. Распад опухоли 09. 01. 2013 v. Смерть 14. 07. 2013 (инфаркт головного мозга)
Больная Л. , 1964 г. р. , Нежелательные явления. v. Кожная сыпь 28. 10. 2012 v. Распад опухоли 09. 01. 2013 v. Смерть 14. 07. 2013 (инфаркт головного мозга)
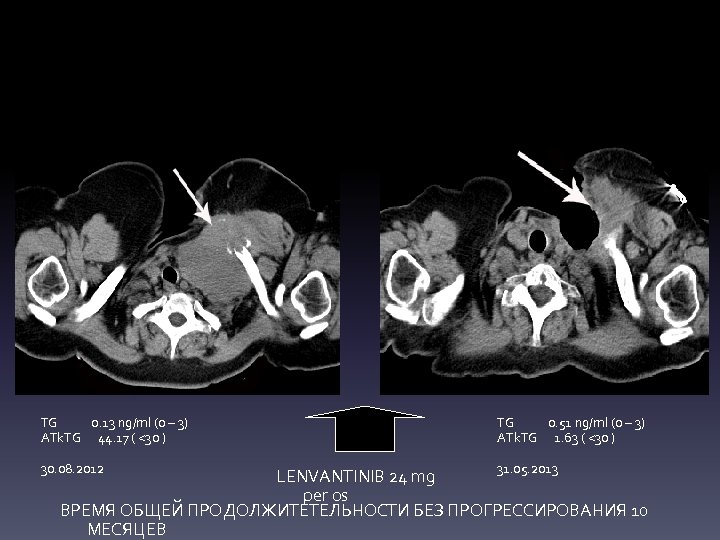 TG 0. 13 ng/ml (0 – 3) ATk. TG 44. 17 ( <30 ) 30. 08. 2012 TG 0. 51 ng/ml (0 – 3) ATk. TG 1. 63 ( <30 ) 31. 05. 2013 LENVANTINIB 24 mg per os ВРЕМЯ ОБЩЕЙ ПРОДОЛЖИТЕТЕЛЬНОСТИ БЕЗ ПРОГРЕССИРОВАНИЯ 10 МЕСЯЦЕВ
TG 0. 13 ng/ml (0 – 3) ATk. TG 44. 17 ( <30 ) 30. 08. 2012 TG 0. 51 ng/ml (0 – 3) ATk. TG 1. 63 ( <30 ) 31. 05. 2013 LENVANTINIB 24 mg per os ВРЕМЯ ОБЩЕЙ ПРОДОЛЖИТЕТЕЛЬНОСТИ БЕЗ ПРОГРЕССИРОВАНИЯ 10 МЕСЯЦЕВ
 ® КАПРЕЛСА Вандетаниб • Вандетаниб: – Ингибитор тирозинкиназы с активностью относительно VEGFR (преимущественно VEGFR-2) и EGFR, а также протоонкогена RET. Принимается внутрь F N O Br IC 50 (μM) N N VEGFR-2 (KDR) 0. 04 VEGFR-3 (Flt-4) N O Киназа 0. 11 RET 0. 13 EGFR 0. 50 VEGFR-1 (Flt-1), PDGFR-β, Tie 2, FGFR 1 >1 VEGFR - рецептор сосудистого эндотелиального фактора роста RET - REarranged during Transfection Carlomagno F et al. Cancer Res 2002; 62: 7284– 7290
® КАПРЕЛСА Вандетаниб • Вандетаниб: – Ингибитор тирозинкиназы с активностью относительно VEGFR (преимущественно VEGFR-2) и EGFR, а также протоонкогена RET. Принимается внутрь F N O Br IC 50 (μM) N N VEGFR-2 (KDR) 0. 04 VEGFR-3 (Flt-4) N O Киназа 0. 11 RET 0. 13 EGFR 0. 50 VEGFR-1 (Flt-1), PDGFR-β, Tie 2, FGFR 1 >1 VEGFR - рецептор сосудистого эндотелиального фактора роста RET - REarranged during Transfection Carlomagno F et al. Cancer Res 2002; 62: 7284– 7290

 Наиболее частые нежелательные явления 3+ степени (частота >2% в каждой группе) КАПРЕЛСА® 300 мг (n=231) Плацебо (n=99) Диарея 25 (11%) 2 (2%) Гипертензия 20 (9%) 1 (1%) Удлинение QT на ЭКГ 18 (8%) 1 (1%) Утомляемость 13 (6%) 1 (1%) Снижение аппетита 10 (4%) 0 Сыпь 8 (3%) 1 (1%) Астения 6 (3%) 1 (1%) Одышка 4 (2%) 3 (3%) Боли в спине 1 (0. 4%) 3 (3%) 0 2 (2%) Обморок Wells SA, Jr. et al. J Clin Oncol 2012; 30: 134– 141
Наиболее частые нежелательные явления 3+ степени (частота >2% в каждой группе) КАПРЕЛСА® 300 мг (n=231) Плацебо (n=99) Диарея 25 (11%) 2 (2%) Гипертензия 20 (9%) 1 (1%) Удлинение QT на ЭКГ 18 (8%) 1 (1%) Утомляемость 13 (6%) 1 (1%) Снижение аппетита 10 (4%) 0 Сыпь 8 (3%) 1 (1%) Астения 6 (3%) 1 (1%) Одышка 4 (2%) 3 (3%) Боли в спине 1 (0. 4%) 3 (3%) 0 2 (2%) Обморок Wells SA, Jr. et al. J Clin Oncol 2012; 30: 134– 141
 Побочные эффекты мультикиназных ингибиторов Препарат Axitinib 1 Cabozantinib 2 Lenvatinib 3 Motesanib 4 Pazopanib 5 Sorafenib 6 Sunitinib 7 Vandetanib 8 Возможные побочные эффекты Слабость, диарея, тошнота, анорексия, гипертензия, стоматит, потеря веса, головная боль Ладонно-подошвенная эритродизестезия, мукозиты, повышение уровней АСТ, АЛТ, липаз Гипертензия, слабость, диарея, потеря веса, анорексия, протеинурия Диарея, слабость, гипертензия, анорексия, гипотироз Слабость, кожная и волосяная пигментация, диарея, тошнота Диарея, боль в полости рта, ладонно-подошвенная эритродизестезия, алопеция, гипертензия, мышечная боль или заклинивание, цитопения Слабость, нейтропения, ладонно-подошвенная эритродизестезия, диарея, лейкопения Фотосенситивная кожная сыпь, удлинение QT-интервала, диарея, тошнота, гипертензия, лейкопения 1. Cohen EE et al. J Clin Oncol 2008; 26: 4708– 4713. 2. NCT 00704730. 3. NCT 00784303. 4. Schlumberger M, et al J Clin Oncol 2009; 27: 3794– 3801. 5. Keith C Bible et al, The Lancet Oncology, Volume 11, Issue 10 , Pages 962 - 972, October 2010. 6. Lam ET, et al. J Clin Oncol 2010; 28: 2323– 2330. 7. J. A. De Souza et al, J Clin Oncol 28: 15 s, 2010 (suppl; abstr 5504). 8. Wells et al, J Clin Oncol 28: 15 s, 2010 (suppl; abstr 5503).
Побочные эффекты мультикиназных ингибиторов Препарат Axitinib 1 Cabozantinib 2 Lenvatinib 3 Motesanib 4 Pazopanib 5 Sorafenib 6 Sunitinib 7 Vandetanib 8 Возможные побочные эффекты Слабость, диарея, тошнота, анорексия, гипертензия, стоматит, потеря веса, головная боль Ладонно-подошвенная эритродизестезия, мукозиты, повышение уровней АСТ, АЛТ, липаз Гипертензия, слабость, диарея, потеря веса, анорексия, протеинурия Диарея, слабость, гипертензия, анорексия, гипотироз Слабость, кожная и волосяная пигментация, диарея, тошнота Диарея, боль в полости рта, ладонно-подошвенная эритродизестезия, алопеция, гипертензия, мышечная боль или заклинивание, цитопения Слабость, нейтропения, ладонно-подошвенная эритродизестезия, диарея, лейкопения Фотосенситивная кожная сыпь, удлинение QT-интервала, диарея, тошнота, гипертензия, лейкопения 1. Cohen EE et al. J Clin Oncol 2008; 26: 4708– 4713. 2. NCT 00704730. 3. NCT 00784303. 4. Schlumberger M, et al J Clin Oncol 2009; 27: 3794– 3801. 5. Keith C Bible et al, The Lancet Oncology, Volume 11, Issue 10 , Pages 962 - 972, October 2010. 6. Lam ET, et al. J Clin Oncol 2010; 28: 2323– 2330. 7. J. A. De Souza et al, J Clin Oncol 28: 15 s, 2010 (suppl; abstr 5504). 8. Wells et al, J Clin Oncol 28: 15 s, 2010 (suppl; abstr 5503).
 КЛИНИЧЕСКИЙ СЛУЧАЙ v. Диагноз: Папиллярный рак щитовидной железы. p. T 4 a. N 1 b. M 1. Клин. стадия IV C. v. Оперативное лечение: 07. 06. 2007 резекция правой доли щитовидной железы. v. Рецидив рака в культе правой доли щитовидной железы. v. Комбинированное лечение: операция 04. 06. 2010 тиреоидэктомия, селективная шейная диссекция (уровень VI). 08. 07. 2010 радиойодтерапия (3 ГБк). v. Продолженный рост рака в регионарных лимфоузлах. v. Комбинированное лечение: операция 29. 12. 2011 селективная шейная диссекция (уровни III-V). 23. 01. 2012 радиойодтерапия (3 ГБк). v. Продолженный рост рака в регионарных лимфоузлах. v. Оперативное лечение 04. 2012 селективная шейная диссекция (уровни I, II, V). v. Продолженный рост рака в ложе удаленной щитовидной железы, в S 5 сегменте правого легкого. v. Комбинированное лечение: 25. 01. 2013 удаление рецидивной опухоли ложа щитовидной железы, селективная шейная диссекция (уровень VI). 01. 04. 2013 проведен курс радиоиодтерапии (3 ГБк).
КЛИНИЧЕСКИЙ СЛУЧАЙ v. Диагноз: Папиллярный рак щитовидной железы. p. T 4 a. N 1 b. M 1. Клин. стадия IV C. v. Оперативное лечение: 07. 06. 2007 резекция правой доли щитовидной железы. v. Рецидив рака в культе правой доли щитовидной железы. v. Комбинированное лечение: операция 04. 06. 2010 тиреоидэктомия, селективная шейная диссекция (уровень VI). 08. 07. 2010 радиойодтерапия (3 ГБк). v. Продолженный рост рака в регионарных лимфоузлах. v. Комбинированное лечение: операция 29. 12. 2011 селективная шейная диссекция (уровни III-V). 23. 01. 2012 радиойодтерапия (3 ГБк). v. Продолженный рост рака в регионарных лимфоузлах. v. Оперативное лечение 04. 2012 селективная шейная диссекция (уровни I, II, V). v. Продолженный рост рака в ложе удаленной щитовидной железы, в S 5 сегменте правого легкого. v. Комбинированное лечение: 25. 01. 2013 удаление рецидивной опухоли ложа щитовидной железы, селективная шейная диссекция (уровень VI). 01. 04. 2013 проведен курс радиоиодтерапии (3 ГБк).
 Больная Б. , 1949 г. р. v. Продолженный рост рака в регионарных лимфоузлах. v. Комбинированное лечение: операция 19. 06. 2013 селективная шейная диссекция (уровни I, III). 07. 10. 2013 радиойодтерапия (3 ГБк). v. Продолженный рост рака в коже шеи, регионарных лимфоузлах, в легких. v 15. 06. 2014 системная лекарственная терапия мультикиназным ингибитором: Капрелса 300 mg/день. v 09. 2014 дальнейшее увеличение количества и размеров «таргетных очагов» , угроза кровотечения из рецидивной опухоли шеи. v. Комбинированное лечение: операция 22. 09. 2014 удаление рецидивной опухоли шеи. Системная лекарственная терапия мультикиназным ингибитором: Нексавар 800 mg/день. v. Прогрессирование заболевания – дальнейшее увеличение количества и размеров «таргетных очагов» . Лучевое лечение с 16. 02. 2015 по 06. 03. 2015 на область шеи справа и слева СОД 47 Гр. С 16. 04. 2015 проводится системная лекарственная терапия мультикиназным ингибитором: Ленвантиниб 24 mg/день. Стабилизация опухолевого процесса.
Больная Б. , 1949 г. р. v. Продолженный рост рака в регионарных лимфоузлах. v. Комбинированное лечение: операция 19. 06. 2013 селективная шейная диссекция (уровни I, III). 07. 10. 2013 радиойодтерапия (3 ГБк). v. Продолженный рост рака в коже шеи, регионарных лимфоузлах, в легких. v 15. 06. 2014 системная лекарственная терапия мультикиназным ингибитором: Капрелса 300 mg/день. v 09. 2014 дальнейшее увеличение количества и размеров «таргетных очагов» , угроза кровотечения из рецидивной опухоли шеи. v. Комбинированное лечение: операция 22. 09. 2014 удаление рецидивной опухоли шеи. Системная лекарственная терапия мультикиназным ингибитором: Нексавар 800 mg/день. v. Прогрессирование заболевания – дальнейшее увеличение количества и размеров «таргетных очагов» . Лучевое лечение с 16. 02. 2015 по 06. 03. 2015 на область шеи справа и слева СОД 47 Гр. С 16. 04. 2015 проводится системная лекарственная терапия мультикиназным ингибитором: Ленвантиниб 24 mg/день. Стабилизация опухолевого процесса.
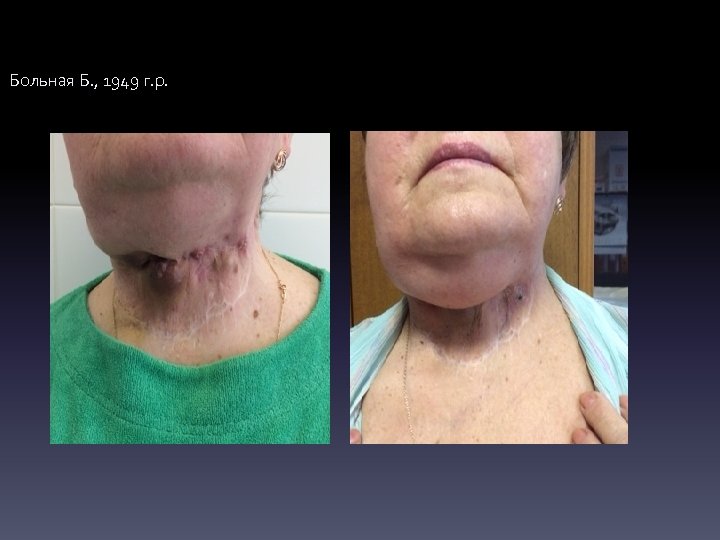 Больная Б. , 1949 г. р.
Больная Б. , 1949 г. р.
 ЗАКЛЮЧЕНИЕ: v. НОВЫЕ ТАРГЕТНЫЕ ПРЕПАРАТЫ – ИЗМЕНЕНИЕ ПОСТОЯННОЙ КЛИНИЧЕСКОЙ ПРАКТИКИ. v. НЕОБХОДИМ ПОИСК ПРЕДЕКТИВНЫХ МАРКЕРОВ. v. НУЖНЫ КОМБИНИРОВАННЫЕ СТРАТЕГИИ.
ЗАКЛЮЧЕНИЕ: v. НОВЫЕ ТАРГЕТНЫЕ ПРЕПАРАТЫ – ИЗМЕНЕНИЕ ПОСТОЯННОЙ КЛИНИЧЕСКОЙ ПРАКТИКИ. v. НЕОБХОДИМ ПОИСК ПРЕДЕКТИВНЫХ МАРКЕРОВ. v. НУЖНЫ КОМБИНИРОВАННЫЕ СТРАТЕГИИ.
 СПАСИБО ЗА ВНИМАНИЕ!
СПАСИБО ЗА ВНИМАНИЕ!


