Lek_rikket_khlamidii_mikoplazmy.ppt
- Количество слайдов: 92

Возбудители трансмиссивных бактериальных инфекций (риккетсии). Патогенные хламидии и микоплазмы ЛЕКЦИЯ 1

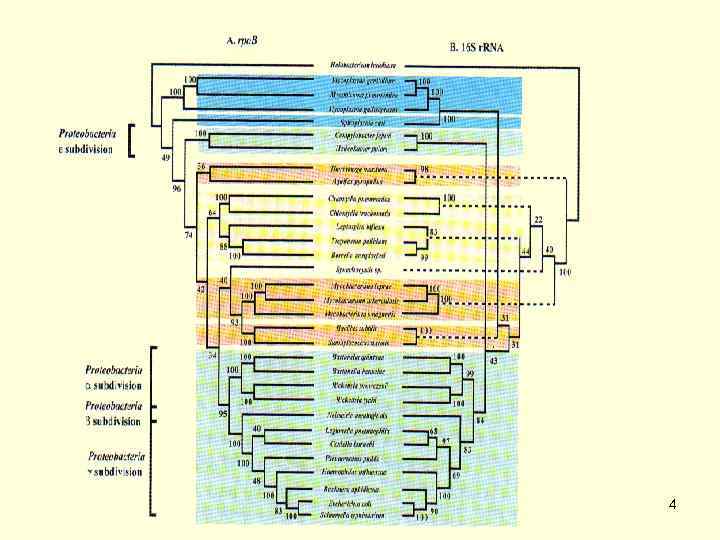
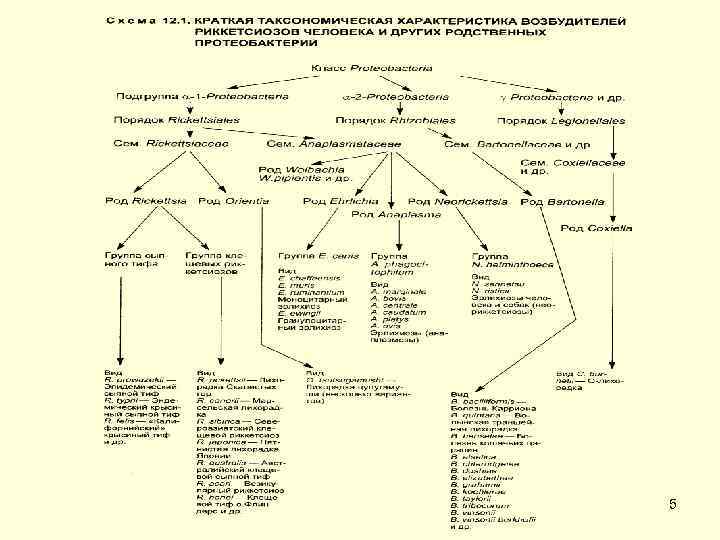
Термин "риккетсии", введенный H. da Rocha Lima (1916) в честь американского исследователя H. T. Ricketts, описавшего возбудителя лихорадки Скалистых гор, объединяет обширную группу грамотрицательных микроорганизмов, тесно связанных в своей жизнедеятельности с членистоногими. Риккетсии имеют ряд общих свойств а) они являются облигатными внутриклеточными паразитами; б) в отличие от подавляющего большинства бактерий риккетсии не способны к росту на питательных средах; в) их биология связана с паразитизмом у членистоногих (клещи, вши, блохи); г) они имеют ряд особенностей в строении, размножении, биохимических, генетических и иммунобиологических характеристиках; д) вызываемые риккетсиями заболевания (риккетсиозы) характеризуются своеобразием клиники и эпидемиологии; е) требуют специализированных методов изучения (риккетсиологических). Таксономия Порядок Rickettsiales класса Proteobacteria домена Bacteria объединяет α 1 протеобактерии двух родов семейства Rickettsiaceae (рода Rickettsia и Orientia) и четырех родов вновь организованного семейства Anaplasmataceae (рода Anaplasma, Ehrlichia, Neorickettsia, Wolbachia). 2

3
4
5

Основные виды и подгруппы рода Rickettsia ГРУППА КЛЕЩЕВЫХ ПЯТНИСТЫХ ЛИХОРАДОК A. R. rickettsii подгруппа 1. R. conorii 2. R. rickettsii 3. R. sibirica 4. R. africae 5. R. slovaca 6. R. japonica 7. R. heilongjiangensis 8. R. honei 9. R. parkeri B. R. massiliae подгруппа 10. R. massiliae 11. R. rhipicephali 12. R. montanensis 13. R. aeschlimannii 14. R. helvetica ПРЕДКОВАЯ ГРУППА D. R. canadensis подгруппа 18. R. canadensis 19. R. tarasevichiae 20. R. bellii C. R. akari подгруппа 15. R. akari 16. R. australis 17. R. felis ГРУППА СЫПНОГО ТИФА E. R. prowazekii подгруппа 21. R. prowazekii 22. R. typhi 6

Микроэкология возбудителей, круг хозяев и естественного обитания • • • Экологической микронишей представителей рода Rickettsia служит цитоплазма, для ряда из них (риккетсии группы КПЛ) и ядро эукариотической клетки, где они размножаются свободно, без окружения паразитофорной вакуолью. Экологические особенности риккетсий обусловлены их облигатным внутриклеточным паразитизмом с широким кругом филогенетически далеко отстоящих друг от друга хозяев – кровососущих членистоногих (клещей, вшей, блох) и их теплокровных прокормителей – грызунов, насекомоядных, сумчатых, копытных и других млекопитающих и птиц. Риккетсии имеют широкий диапазон патогенности и могут быть разделены по этому признаку на три группы классические патогены, новые патогены и симбионты эукариотических клеток, преимущественно насекомых. 7
8

Морфологические и тинкториальные свойства • Риккетсии мелкие плеоморфные микроорганизмы от кокковидных до палочковидных, иногда нитевидные. • Размножение риккетсий происходит бинарным делением вегетативных форм. • Жгутиков и капсул нет, но на электронных микрофотографиях клеток виден внешний слой аморфного материала. • Риккетсии грамотрицательные микроорганизмы, плохо окрашиваются обычными анилиновыми красителями. Удерживают основной фуксин. • Наиболее часто применяют модификацию окраски по П. Ф. Здродовскому, рекомендовавшему использование карболового фуксина. При этом риккетсии окрашиваются в ярко розовый или рубиново красный цвет, цитоплазма клеток в голубой цвет, ядра в синий. Риккетсии имеют сходное с классическими грамотрицательными бактериями строение клетки. У них выявлены волосовидные придатки (фимбрии). Подвижность риккетсий связывают с наличием «актиновых хвостов» . У ряда видов риккетсий отмечают наличие вегетативных и покоящихся форм. 9

Антигенное строение риккетсий • Основными антигенными комплексами риккетсий являются группоспецифический (отличающийся у риккетсий групп КПЛ и СТ) термостабильный липополисахаридный комплекс (ЛПС) и два протективных поверхностных белка r. Omp. A и r. Omp. B. • Токсические субстанции риккетсий являются термолабильными белками, неотделимы от их клеток, инактивируются формалином. Патогенные виды риккетсий синтезируют гемолизины, вызывающие гемолиз эритроцитов различных видов животных. 10

Культуральные особенности • Размножаются в клетках позвоночных и членистоногих, в эпидермальных клетках, выстилающих желточный мешок развивающегося куриного эмбриона. • Хороший рост получен in vitro в клетках куриного эмбриона и в некоторых стационарных линиях клеток млекопитающих (Vero, Hep 2). бразуют бляшки на фибробластах куриного эмбриона. • Температурный оптимум роста от 32 до 35˚ С (выше – для группы СТ, ниже – для группы КПЛ). • Для экспериментального воспроизведения инфекции и выделения штаммов патогенных риккетсий с успехом применяют различные виды чувствительных к определенным видам риккетсий животных, чаще морских свинок самцов (часто при внутрибрюшинном заражении возникает скротальный феномен – воспалительная реакция tunica vaginalis яичек) и хомячков. 11

Физиологические особенности • Риккетсии имеют осмотически активную клеточную мембрану, содержащую специфические переносчики для транспорта субстратов. • Наличие системы транспорта АТФ АДФ и собственного синтеза АТФ при окислении глютаминовой кислоты указывает на два типа использования риккетсиями АТФ. • При размножении риккетсии получают АТФ от клетки хозяина, в ее присутствии ингибируется цитратсинтаза – ключевой фермент цикла Кребса, что сопровождается снижением катаболизма глютаминовой кислоты. • При выходе риккетсий из клеток в условиях дефицита АТФ активность цитратсинтазы усиливается, что ведет к активации цикла Кребса и генерации эндогенной риккетсиальной АТФ. 12

Патогенность известных к настоящему времени риккетсий риккетсии группы КПЛ классические патогены 1. Rickettsia rickettsii 2. Rickettsia conorii 3. Rickettsia sibirica 4. Rickettsia australis 5. Rickettsia japonica 6. Rickettsia akari новые патогены (оппортунисты) 1. Rickettsia slovaca 2. Rickettsia helvetica 3. Rickettsia honei 4. Rickettsia africae 5. R. mongolotimonae 6. Rickettsia aeschlimannii 7. Rickettsia heilongjiangii 8. Rickettsia felis с неизвестной патогенностью 1. Rickettsia amblyommii 2. Rickettsia cooleyi 3. Rickettsia massiliae 4. Rickettsia montanensis 5. Rickettsia moreli 6. Rickettsia peacockii 7. Rickettsia parkeri 8. Rickettsia rhipicephali 9. Rickettsia sp. A 167 10. Rickettsia sp. AT 1 11. Rickettsia sp. Bar 29 12. Rickettsia raoultii 13. Rickettsia sp. IM 1 14. Rickettsia sp. IRS 4 15. Rickettsia sp. IRS 3 16. Rickettsia sp. RAv 1 17. Rickettsia sp. S 46. Rickettsia hulinii риккетсии гр. СТ классические патогены 1. Rickettsia prowazekii 2. Rickettsia typhi не классифицированные риккетсии новые патогены 1. R. canadensis симбионты эукариотических клеток членистоногих 1. Rickettsia amblyommii 2. Rickettsia bellii 3. Rickettsia cooleyi 4. Rickettsia peacockii 5. Rickettsia moreli 6. Rickettsia sp. ‘Digas & Belikov 1999’ 7. Rickettsia sp. ‘La Copita’ 8. Rickettsia sp. ‘midichlorii’ 9. Rickettsia sp. California 2 10. Rickettsia sp. Ir. R/Munich 11. Rickettsia sp. MOAa 12. Rickettsia sp. WB 8 2 симбионты других эукариотических клеток 1. male killing Rickettsia from Adalia bipunctata 2. male killing Rickettsia from Adalia decempunctata 3. papaya bunchy top disease rickettsia 4. Rickettsia sp. PAR (pea aphid rickettsia) 5. Rickettsia endosymbiont of Hemicrepsis marginata 6. Rickettsia endosymbiont of Torix tagoi 13

Факторы патогенности • У риккетсий описана микрокапсула, с наличием которой связывают так называемый механизм “реактивации” риккетсий (восстановления вирулентности штаммов). • Во взаимодействии риккетсий с эукариотическими клетками придается значение фосфолипазе А 2 и адгезинам риккетсий, которыми являются поверхностные белки r. Omp. A (имеют значение преимущественно для риккетсий группы КПЛ) и Omp. B (для риккетсий группы СТ и ориенций), а также активной подвижности патогенных риккетсий, связанной с наличием актиновых хвостов. • Риккетсии имеют субстанции, обладающие токсическими свойствами, в том числе липополисахарид, фосфолипидные фракции, специфический набор жирных кислот, однако токсичность риккетсий и их пирогенное действие связано преимущественно с поражением риккетсиями эндотелиальных клеток сосудистого русла. • Риккетсии обладают гемолитическими свойствами в отношении эритроцитов кролика и барана, гемагглютинином. • Риккетсии имеют также аллергенные субстанции, входящие в состав растворимых антигенных фракций. 14

Ориенции и лихорадка цуцугамуши • • • Orientia – отдельный род семейства Rickettsiaceae, который по ранее существовавшей таксономии входил в род Rickettsia на правах (серо)группы. В последние годы установлено, что ориенции имеют ряд отличий от представителей рода Rickettsia. Эти плеоморфные грамотрицательные микроорганизмы имеют форму коротких палочек, часто – диплобацилл. Характерно околоядерное расположение в цитоплазме эукариотических клеток. В связи с малой устойчивостью отдают фуксин принятых в риккетсиологии методах окраски (Здродовского, Маккиавелло, Романовского Гимзы). Наиболее пригоден метод Гименеса, при котором ориенции окрашены в темно розовый цвет и дифференцируются малахитовым зеленым от окружающих тканей. Наружная мембрана Orientia tsutsugamushi толще внутренней, в отличие от риккетсий. У ориенций отсутствует липополисахарид и пептидогликан и их основные компоненты, такие как муреиновые кислоты, глюкозамин, жирные кислоты, 2 кето 3 деоксиоктоновая кислота. Отсутствие пептидогликана объясняет нестойкость ориенций, а также их очень высокую устойчивость к пенициллину. 15

Основные свойства ориенций • • • Отмечена выраженная генетическая и антигенная гетерогенность возбудителя, наличие трех основных типов – Gilliam, Karp, Kato. Антигенная гетерогенность в наибольшей степени связана с вариабельностью доминантного поверхностного белка 56 КД. Ориенции имеют видоспецифический и типоспецифические антигены. Протективный иммунитет формируется преимущественно к типоспецифическому антигену, нестойкий и непродолжительный, вследствие чего могут быть повторные заболевания. Ориенции не имеют антигенных связей с риккетсиями групп СТ и КПЛ. Имеют общие антигенные детерминанты с Proteus mirabilis OXK. Анализ оснований ДНК выявил молекулярный % Г+Ц у ориенций в диапазоне 28, 1 30, 5%, что эквивалентно риккетсиям группы СТ. По данным пульс гелевого электрофореза ориенции имеют циркулярную хромосому размерами в два раза большую, чем у представителей рода Rickettsia. Это находит свое отражение и в большей длине ориенций и их двукратном объеме в сравнении с риккетсиями. Возбудитель передается человеку в результате присасывания личинок краснотелковых клещей (Trombididae) и вызывает лихорадку цуцугамуши. 16

Coxiella burnetii и лихорадка Ку • • • Coxiella burnetii (возбудитель лихорадки Ку) относят к гамма протеобактериям. Является облигатным фаголизосомальным паразитом эукариотических клеток, не размножается на питательных средах. C. burnetii культивируют в куриных эмбрионах, культурах клеток, в биопробах на различных лабораторных животных. Выделяют фазовые вариации коксиелл, аналогично R и S формам бактерий. Возбудитель в фазе 1 и фазе 2 отличается по вирулентности, строению, иммуногенности и другим свойствам. В естественных условиях возбудитель находится в фазе 1, при культивировании в куриных эмбрионах возбудитель переходит в фазу 2, утрачивая поверхностные структуры и вирулентность. Коксиеллы мельче риккетсий, способны образовывать инфраформы (менее 40 нм). Для лабораторной диагностики применяют РСК и РНИФ с антигенами 1 и 2 фазы, ИФА. Для выявления возбудителя применяют экспресс методы – МФА, ИФА. У больных с острой формой лихорадки Ку преобладают антитела к антигену фазы 2, при формировании хронического течения выявляют антитела преимущественно к антигену фазы 1. 17

Эколого эпидемиологические особенности коксиелл • • • Лихорадка Ку зооноз сельскохозяйственных животных с длительным и самостоятельным характером существования очагов (как при бруцеллезе). Характеризуется множественностью источников (прежде всего пуховые козы, овцы, крупный рогатый скот, меньше птицы) и факторов передачи инфекции (молоко, мясо, шкуры, вода, солома, пыль и др. ). Возбудитель в большом количестве содержится в плаценте и выделяется при родах (окоте, отеле) с околоплодной жидкостью, с молоком, с экскрементами животных. Коксиеллами инфицируется шерсть и пух животных, среда их обитания. Возбудитель обладает очень высокой устойчивостью во внешней среде. Ведущее значение имеют аспирационный и контактный пути передачи, меньшее алиментарный. Возбудитель характеризуется высокой экологической пластичностью и широким кругом позвоночных и беспозвоночных хозяев (сельскохозяйственные и дикие животные, иксодовые клещи). 18

Иммунитет при риккетсиозах • У переболевших риккетсиозами лиц развивается стойкий антитоксический и антибактериальный иммунитет, при сыпном тифе он может быть нестерильным. При риккетсиозах группы КПЛ после перенесенной инфекции создается стойкий иммунитет не только к данному виду риккетсий, но и к другим возбудителям группы КПЛ. • При лихорадке цуцугамуши, в связи с выраженной гетерогенностью генетических и антигенных свойств возбудителя, иммунитет типоспецифический, нестойкий. • При риккетсиозах группы КПЛ и СТ, лихорадке цуцугамуши доказано наличие стертых и бессимптомных форм инфекции, связанных как с гетерогенностью возбудителей, так и неодинаковой резистентностью населения, в том числе наличием популяционного иммунитета. • В развитии специфической невосприимчивости ведущее значение имеет клеточный иммунитет в виде гиперчувствительности замедленного типа. 19

Эпидемиология риккетсиозов • • • Риккетсиозы группы КПЛ – классические природно очаговые, передаваемые клещами, облигатно трансмиссивные инфекции. В России в настоящее время регистрируют заболевания двумя риккетсиозами группы КПЛ клещевым риккетсиозом (КР) и Астраханской пятнистой лихорадкой (АПЛ). Вероятная эволюция риккетсий группы СТ направлена от клещевых риккетсиозов – через блошиные и гамазовые к антропонозу, передаваемому вшами. Эпидемический сыпной тиф представляет антропоноз. Платяная вошь является лишь переносчиком с несовершенной адаптацией к R. prowazekii и не может сохранять этого возбудителя в своей популяции без участия сыпнотифозного больного (носителя). В организме вшей (преимущественно платяных) риккетсии размножаются в эпителиальных клетках кишечника с набуханием и отслоением инфицированных клеток вплоть до нарушения анатомической целостности пищеварительного тракта, что закономерно приводит к гибели переносчика. В слюнных железах и слюне вшей риккетсий не содержится. Заражение человека происходит путем втирания инфицированных экскрементов вшей преимущественно при расчесах. В современных условиях отмечают преимущественно болезнь Брилля Цинссера – рецидивный сыпной тиф у ранее переболевших (длительная персистенция возбудителя в организме хозяина). 20

21

Микробиологическая диагностика риккетсиозов • Лабораторная диагностика сыпного тифа и других риккетсиозов включает выделение возбудителя, определение его антигенов и ДНК, выявление антител к риккетсиям соответствующих видов, чаще осуществляется с использованием серологических (РСК, РНГА, РНИФ, ИФА) и молекулярно генетических (ПЦР, определение нуклеотидных последовательностей фрагментов генов) методов. • Эффективно риккетсиологическое обследование снятых с человека переносчиков классическими (выделение возбудителя) и экспресс (метод флюоресцирующих антител, ИФА, РНГА с иммуноглобулиновыми диагностикумами для выявления антигенов риккетсий групп СТ и КПЛ) методами. • В последние годы выявлен ряд новых риккетсий, не культивируемых на традиционных риккетсиологических моделях (лабораторные животные, куриные эмбрионы). • Для их культивирования использована клещевая экспериментальная модель (воспроизведение естественного цикла развития иксодид) и длительно культивируемые линии клеток млекопитающих (Vero, Hep 2) и клещей. 22
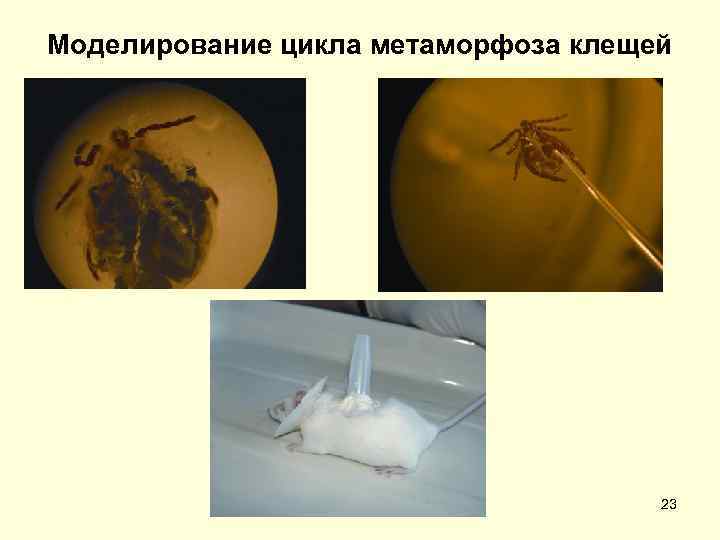
Моделирование цикла метаморфоза клещей 23
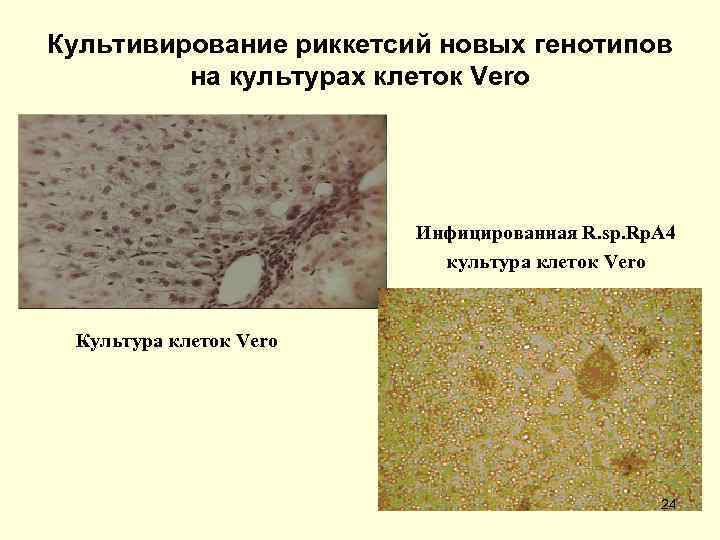
Культивирование риккетсий новых генотипов на культурах клеток Vero Инфицированная R. sp. Rp. A 4 культура клеток Vero Культура клеток Vero 24
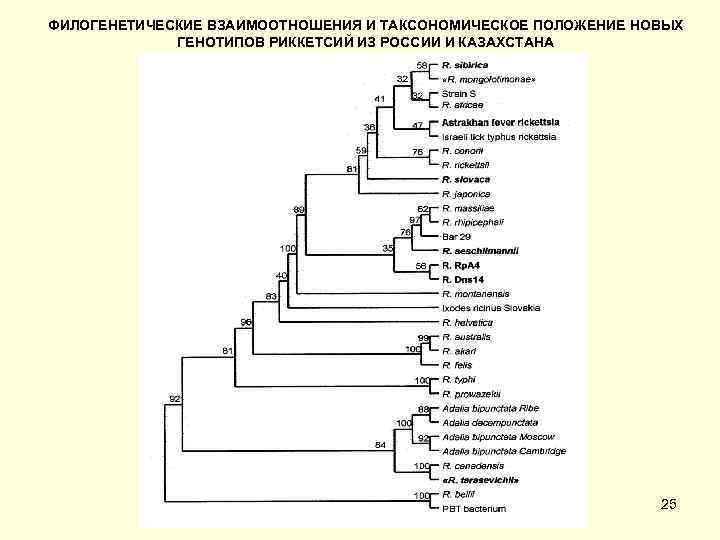
ФИЛОГЕНЕТИЧЕСКИЕ ВЗАИМООТНОШЕНИЯ И ТАКСОНОМИЧЕСКОЕ ПОЛОЖЕНИЕ НОВЫХ ГЕНОТИПОВ РИККЕТСИЙ ИЗ РОССИИ И КАЗАХСТАНА 25
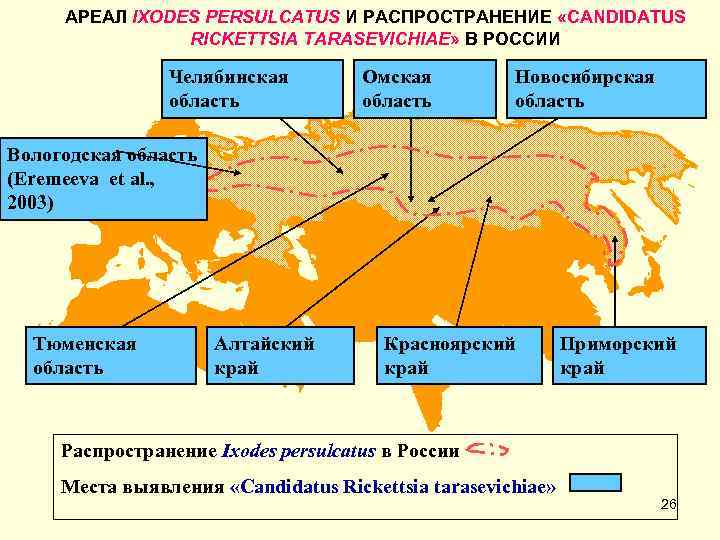
АРЕАЛ IXODES PERSULCATUS И РАСПРОСТРАНЕНИЕ «CANDIDATUS RICKETTSIA TARASEVICHIAE» В РОССИИ Челябинская область Омская область Новосибирская область Вологодская область (Eremeeva et al. , 2003) Тюменская область Алтайский край Красноярский край Приморский край Распространение Ixodes persulcatus в России Места выявления «Candidatus Rickettsia tarasevichiae» 26

Определение чувствительности к антибиотикам • • • С учетом внутриклеточного цикла жизни риккетсий для определения их антибиотикочувствительности используют лабораторных животных, развивающиеся куриные эмбрионы и клеточные культуры. Отмечена чувствительность риккетсий к тетрациклинам, хлорамфениколу, из макролидов – к джозамицину и кларитромицину. Все изученные виды оказались чувствительными к фторхинолонам (офлаксоцину, перфоксацину, спарфлоксацину, ципрофлоксацину). Риккетсии группы СТ более чувствительны к эритромицину, чем риккетсии группы КПЛ. Риккетсии группы СТ и большинство исследованных риккетсий группы КПЛ чувствительны к рифампицину, кроме филогенетического кластера R. massiliae, что свидетельствует об таксономическом значимости этого признака. Их резистентность к рифампицину связана с дивергенцией в этой подгруппе гена, кодирующего РНК – полимеразу. 27

Лечение и профилактика • • • Наиболее эффективными средствами антибиотикотерапии риккетсиозов и лихорадки цуцугамуши являются препараты группы тетрациклинов и фторхинолонов. В лечении лихорадки Ку, равно как и риккетсиозов групп СТ и КПЛ назначают преимущественно доксициклин, обладающий наилучшими фармакокинетическими характеристиками в отношении этих внутриклеточных микроорганизмов. Назначение тетрациклина или доксициклина в общетерапевтических дозах (2, 0 г тетрациклина или 200 мг доксициклина в 2 капсулах в сутки для взрослого) при острых формах риккетсиозов и лихорадки цуцугамуши является эффективным и позволяет нормализовать температуру и улучшить состояние больного в течение 36 – 96 часов с начала лечения. В связи с возможностью длительной персистенции риккетсий и ориенций лечение необходимо продолжать 2 3 дня после нормализации температуры. Разработана и применяется живая сыпнотифозная вакцина. Однако наибольшее значение применительно к СТ имеет борьба с педикулезом, своевременное лабораторное обследование на сыпной тиф длительно лихорадящих больных, особенно из категорий риска (завшивленные, бездомные, беженцы и др. ). Применительно к риккетсиозам группы КПЛ и лихорадке цуцугамуши применяют противоклещевые обработки территорий, меры личной защиты от нападения и присасывания клещей, возможно 28 превентивное назначение антибиотиков.
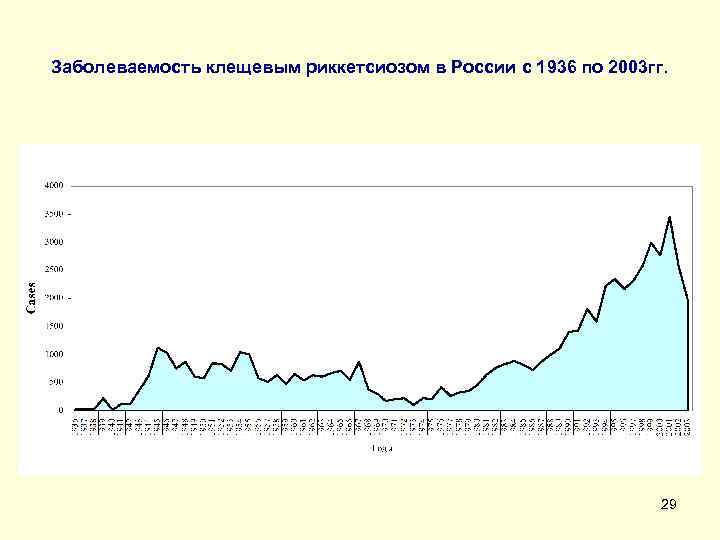
Заболеваемость клещевым риккетсиозом в России с 1936 по 2003 гг. 29
30

ХЛАМИДИИ (семейство Chlamydiaceae) • • Облигатные внутриклеточные паразиты, вызывают заболевания человека, животных и птиц (от греч. chlamyda мантия, в пораженных клетках образуют включения, окруженные оболочкой мантию). Таксономическое положение. Порядок Chlamydiales, семейство Chlamydaceae, род Chlamydia. Заболевания у человека и животных вызывают С. trachomatis, С. psittaci, С. рneumoniae. Патогенные только для животных С. ресогит, С. abortus, C. felis. Согласно последней классификации, семейство Chlamydaceae предложено разделять на два рода: род Chlamydia (вид С. Trachomatis) род Chlamidophila (включены виды С. psittaci и С. Pneumoniae). • • • Морфологические свойства. Хламидии это мелкие грам бактерии овоидной формы. Нет спор, не имеют жгутиков и капсулы. Отличие строения клеточной стенки: представляет собой двухслойную мембрану, которая не содержит (или в небольшом количестве) N ацетилмурамовую кислоту (основной компонент пептидогликана). Ригидность клеточной стенке придают пептиды, перекрестно сшитые пептидными мостиками. Имеются гликолипиды, аналогичные Л ПС грам бактерий. 31
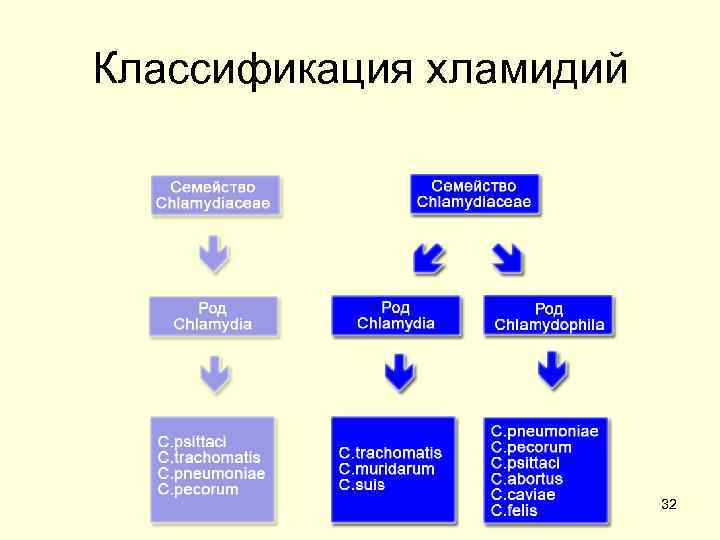
Классификация хламидий 32

Chlamydia trachomatis • Группа трахомы – серовары A, B, Ba, C – серовары D, Da, E, F, G, H, I, Ia, J, K • Группа венерической лимфогранулёмы (LGW) – серовары L 1, L 2 a, L 3 33

Антигенное строение хламидий 34

• Основной метод выявления хламидий окраска по Романовскому Гимзе (Р Г). • Полиморфны, что связано с особенностями их репродукции. Уникальный цикл развития чередование двух форм существования элементарных и ретикулярных (или инициальных) телец. • • • Элементарные тельца мелкие (размер 0, 2 0, 3 мкм) метаболически неактивные инфекционные частицы, расположенные вне клетки. Имеют толстую оболочку, состоящую из внутрен ней и наружной мембран (определяет устойчивость к неблагоприятным условиям окружающей среды). По Р Г окращиваются в красный цвет. Внутри клеток элементарные тельца трансформируются в ретикулярные тельца. • • • Ретикулярные тельца вегетативная форма хламидий. Имеют овоидную форму и крупнее элементарных телец в несколько раз. Располагаются внутриклеточно около ядра и окрашиваются по Р Г в голубой или фиолетовый цвет. Их инфекционность по сравнению с элементарными крайне мала. Репродукция хламидий. Размножение происходит преимущественно эпителиальных в клетках. Элементарные тельца индуцируют фагоцитоз и захватываются клеткой мишенью, попадая в нее путем эндоцитоза. После поглощения оказываются внутри фагосомы и блокируют ее слияние с лизосомами. Благодаря этому элементарные тельца «избегают» контакта с лизосомальными ферментами и размножаются внутри фагосомы. 35

• • • Внутри клеток элементарные тельца трансформируются в ретикулярные, которые многократно делятся бинарным делением, затем уплотняются и превращаются в элементарные тельца. В конце цикла они занимают большую часть клетки хозяина. Растягивая стенку вакуоли, разрывают ее, а затем и плазматическую мембрану клетки. Цикл развития хламидий 24 48 ч и завершается гибелью клетки хозяина, выходом элементарных телец, которые инфицируют соседние интактные клетки и цикл повторяется. • • Культивирование. Размножаются только в живых клетках. Они не способны ак кумулировать и использовать энергию (энергетические паразиты). Культивируют в желточном мешке куриных эмбрионов, в организ ме чувствительных животных, культуре кле ток типа He. La, Нер 2. Оптимальная t 350 С. Перед заражением культуры клеток облучают или об рабатывают циклогексамидом, что позволяет хламидиям легче усваивать АТФ. С. Trachomatis (возбудитель венерической лимфогранулемы)отличается высокой вирулентностью легче культивируется, не требуя даже предварительной подготовки культур клеток. 36

• • • Ферментативная активность. Небольшой набор ферментов. Ферментируют пировиноградную кислоту, синтезируют некоторые липиды. Хламидии не способны синтезировать высокоэнергетические соединения. Вне клеток хозяина их метаболические функции сведены до минимума. Обеспечение метаболитами за счет жизнедеятельности клеток хозяина. Некоторые метаболиты (изолейцин) – ингибиторы их роста, обеспечивают латентное течение хламидиоза. Антигенная структура. АГ трех типов: родоспецифический термостабильный липополисахарид (гликолипид), в клеточной стенке (выявляют РСК); видоспецифический АГ белковой природы, расположенный более поверхностно в наружной мембране. (обнаруживают РИФ); вариантоспецифический антиген белковой природы. • • • Кроме того, С. trachomatis и С. psittaci располагают типоспецифическими антигенами, (мембранные пептиды). Факторы патогенности. Адгезивные свойства связаны с белками наружной мембраны (только у элементарных телец). Эндотоксин (ЛПС). Возможно, выделение экзотоксина (внутривенное введение вызывает гибель мышей). Белки наружной мембраны ан тифагоцитарныйфактор, подавляет слияние фагосомы с лизосомой. Белок теплового шока (от англ. heat-shock protein - HSP), вызывает аутоиммунные реакции. 37

• • Резистентность к факторам внешней среды высокая. Устойчивы к низким температурам (не теряют активность при 50. . . 70 °С), высушиванию (возбудитель орнитоза сохраняется в подстилке гнезда птиц нескольких месяцев). Чувствительны к нагреванию и дезинфектантами. Эпидемиология, патогенез, клиника. Хламидии вызывают – хламидиозы. Антропонозы вызываются С. trachomatis и С. Pneumoniae. Зооантропонозная С. psittaci (орнитоз от человека человеку не передается. Поражают только животных С. ресогит, С. abortus, C. felis. Хламидии обладают эпителиотропностью различных органов. • • • Размножение приводит к разрушению эпителия и образованию язв, которые заживают с образованием рубцов и спаек. Рубцовые изменения роговицы при трахоме приводят к слепоте. Воспаление органов малого таза при урогенитальном хламидиозе ведет к бесплодию. Возбудитель может попадать в кровь, паренхиматозные органы, фиксироваться в лимфоидной ткани (при венерическом лимфогранулематоза и орнитозе). Латентное существованию или персистенция вызывают иммунную и аллергическую перестройку организма (синдром Рейтера). Отличительной особенностью является их способность накапливать гликоген в виде различного рода включений. 18 сероваров разделяют на «глазные» , «генитальные» и «хламидий венерической 38 лимфогранулемы» .

Клинические проявления 30% • Слизисто-гнойный цевицит • Гнойные выделения из влагалища • Межменструальные кровотечения • Дизурия • Боль в нижней части живота • Хронические боли в области малого таза € 75% • Выделения из уретры • Дизурия • Признаки эпидидимита или простатита €+ • Аноректальные выделения и дискомфорт • Конъюнктивит • Артралгии 39

• Серовары А, В, Ва и С называют «глазными» вызывают трахому. • Серовары от D до К «гениталъные» причина урогенитального хламидиоза (негоно кокковыйуретрит) и его экстрагениталъных ос ложнений ( • болезнь Рейтера). Серовары L 1, L 2 a, L 3 «хламидии венеричес кой лимфогранулемы» или паховый лимфогранулематоз. ВОЗБУДИТЕЛЬ ТРАХОМЫ С. trachomatis (греч. «trachys» означает «шероховатый, неровный» , при трахоме поверхность конъюнктивы выглядит • бугристой в результате гранулематозного воспаления). Провачек и Л. Хальберштедтер открыли (1907 г. ) в клетках роговицы больного (тельца Хальберштедтера – Провачека) и доказали контагиозность трахомы, экспериментально заразив орангутангов материалом из соскоба конъюнктивы больного человека. • • Эпидемиология. Трахома антропонозная инфекция. Контактно бытовой путь передачи. Высокая восприимчивость, особенно в детском возрасте (семейные очаги болезни). Трахома отличается эндемичностью. Встречается в Азии, Африки, Центральной и Южной Америки в странах с низким уровнем санитарной культуры и гигиены. Более 400 млн человек заражены трахомой, из них 10 20 млн страдают частичной или полной потерей зрения. В Росси спорадические, завозные случаи трахомы. Патогенез и клиника. Возбудитель, обладая эпителиотропностью, поражает слизистую оболочку глаз. Проникает в эпителий конъюнктивы и роговицы, размножается, разрушая клетки. Развивается фолликулярный кератоконъюнктивит (чаще двусторонний) с появлением лимфоидных фолликулов ( «трахоматозных гранулем» в 40 субэпителиальной ткани глаз).
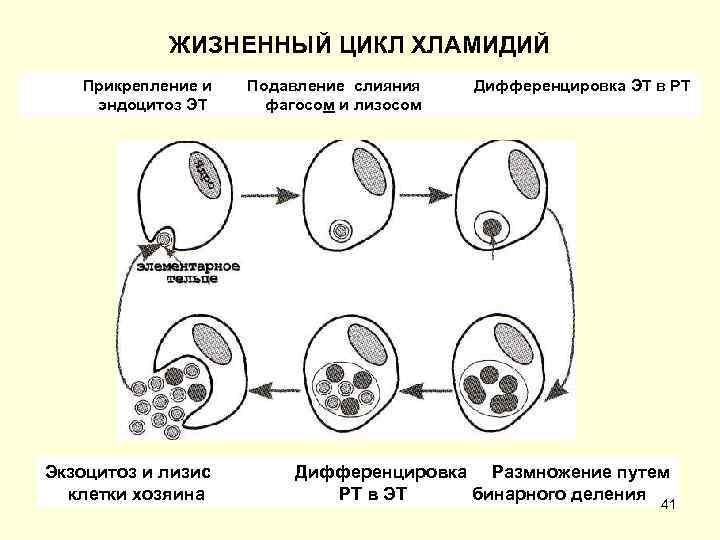
ЖИЗНЕННЫЙ ЦИКЛ ХЛАМИДИЙ Прикрепление и эндоцитоз ЭТ Экзоцитоз и лизис клетки хозяина Подавление слияния фагосом и лизосом Дифференцировка ЭТ в РТ Дифференцировка Размножение путем РТ в ЭТ бинарного деления 41
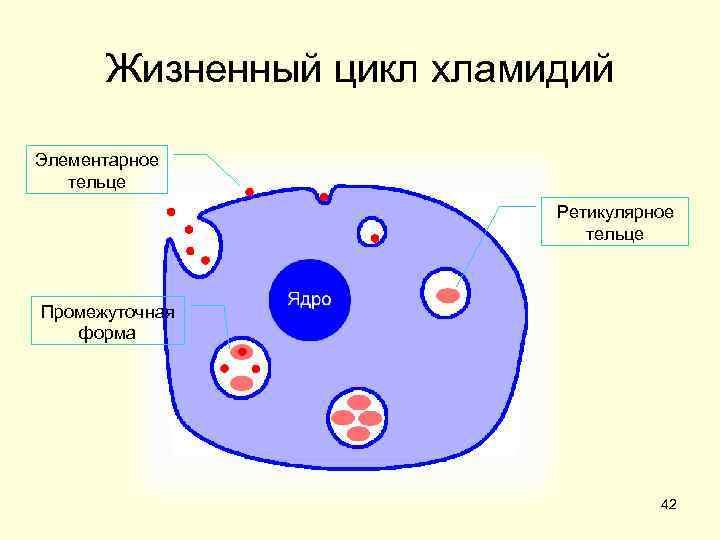
Жизненный цикл хламидий Элементарное тельце Ретикулярное тельце Промежуточная форма 42

Урогенитальный хламидиоз Клинические формы уретрит эпидидимит простатит орхит проктит фарингит конъюнктивит. . . уретрит цервицит эндометрит сальпингит оофорит пельвиоперитонит аппендицит холецистит. . . 43

Урогенитальный хламидиоз Последствия (резидуальная фаза) ухудшение фертильности хронические артриты болезнь Рейтера. . . бесплодие внематочная беременность спаечная болезнь кишечника хронические артриты болезнь Рейтера. . . 44

• • В запущен ных случаях вся конъюнктива глаза усеяна зернышками, прилегающими друг к другу в виде «вареное саго» . Начавшись в раннем детстве, заболевание прогрессирует на протяжении многих лет, пре кращается лишь после образования рубцовой соединительной ткани, что приводит к слепоте. Реинфекция с более тяжелым течением. Часто присоединяется вторичная инфекция (вторичный иммунодефицит при трахоме). Иммунитет. После перенесенного заболевания не вырабатывается. • • Микробиологическая диагностика. Исследование соскоба с конъюнктивы. В пораженных клетках при окраске по Р Г обнаруживают цитоплазматические включения фиолетового цвета с красным центром, расположенные около ядра тельца Хальберштедтера Провачека. Выявление хламидииного АГ в РИФ и ИФА. Культивирование хламидии трахомы на куриных эмбрионах или культуре клеток. Серологический метод малоинформативен Лечение. Антибиотики (тетрациклин), иммуностимуляторы (интерферон). Специфическая профилактика. Не разработана. 45

• • ВОЗБУДИТЕЛЬ УРОГЕНИТАЛЬНОГО ХЛАМИДИОЗА С. trachomatis Эпидемиология. Урогенитальный хламиди оз антропонозная инфекция. Источник больные люди, наиболее опасны женщины (бессимптомное течение отмечается в 70— 80%). Хламидии не представляют нормальную микрофлору, их обнаружение доказательство хронического бессимптомного течения хламидиоза. Заражение через слизистые оболочки половых путей. Возможно контактно бытовое инфицирование через предметы семейный хламидиоз (белье, мочалка). Новорожденные зара жаются при прохождении через родовые пути (хламидиоз глаз, отиты, атипичные пневмонии хламидийной этиологии). • • • Возможна трансплацентарная передача процессе внутриутробного развития (неонатальная патология врожденный хламидиоз). Генитальные серовары C. trachomatis могут попасть на слизистую глаз также при купании кератоконъюнктивит ( «хламидиоз бассейнов» ). Хламидийный конъюнктивит является односторонним процессом «паратрахома» . Восприимчивость высокая. 6 9% мужчин, 12 15% женщин в мире заражены хламидиями. Патогенез и клиника. Входные ворота слизистые оболочки половых органов. Патологический процесс через 5 30 дней после заражения. У женщин пер воначально поражается шейка матки. У мужчин первично инфицируется эпителий уретры. 46

• Урогенитальный хламидиоз (называют «негонококковый уретрит» ) у больных отмечаются симптомы, напоминающие гонорею: зуд, выделения, боль при мочеиспускании. Однако эти признаки менее выражены, чем при гонорее. • Далее развивается восходящая инфекция. У женщин про является развитием цервицита, уретрита, эндометрита, сальпингита. • У мужчин возникает эпидидимит или простатит. Воспалительный процесс в органах малого таза приводит к образованию спаек и рубцов. • Следствием является развитие непроходимости маточных труб у женщин, семенных протоков у мужчин. 47

Методы диагностики хламидиозов • Микроскопический – световая микроскопия – прямая РИФ (ПИФ) • Культуральный – культуры клеток (Mc. Coy) • ДНК - диагностика – полимеразная цепная реакция (PCR) – Гибридизационный анализ • Иммунологические (поиск антигена) – ИФА – Иммунохроматография • Серодиагностика – ИФА – точечный ИФА 48

Световая микроскопия • Окраска р-ром Люголя (йодофильные включения) • Окраска по Романовскому-Гимза (тельца Гальбершедтера. Провачека) Чувствительность – 10 -12% 49
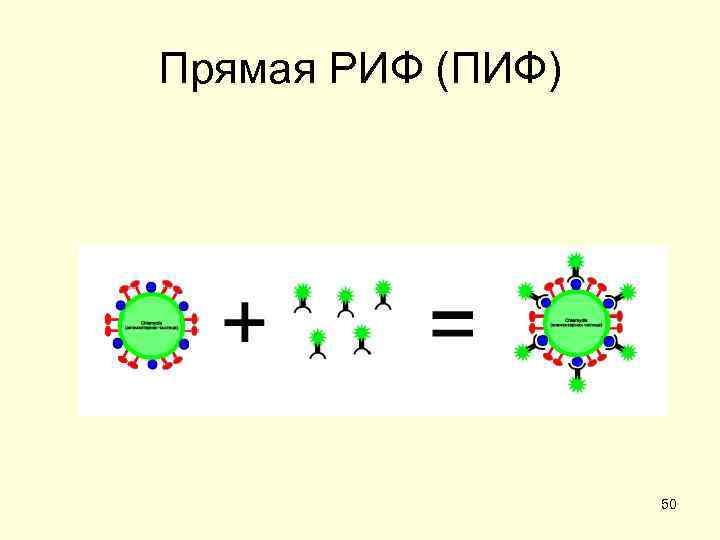
Прямая РИФ (ПИФ) 50
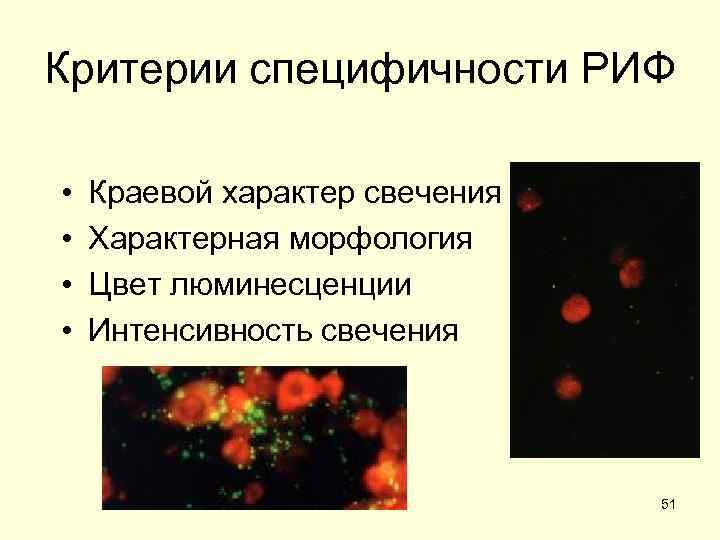
Критерии специфичности РИФ • • Краевой характер свечения Характерная морфология Цвет люминесценции Интенсивность свечения 51

Культуральный метод • Чувствительность – 40 -85% • Преимущества – Высокая специфичность – Определение чувствительности к антибиотикам • Недостатки – Высокая трудоемкость – Высокая стоимость – Продолжительность исследования 52

Этапы культурального метода • • Обработка клеток ДЕАЕ-декстраном Заражение клеток Центрифугирование клеток и отмывка Внесение ростовой среды с циклогексимидом • Инкубация • Детекция хламидий в ПИФ или ПЦР Общая продолжительность исследования » 7 дней 53

Достоинства ПЦР • • Универсальность Чувствительность Специфичность Технологичность 54

Выявление антигенов • Иммуноферментный метод • Иммунохроматография 55

Иммуноферментный анализ • Векто. Хлами-Антиген • Pathfinder Сhlamydia ELISA Bio-Rad • … Чувствительность 20 -85% 56
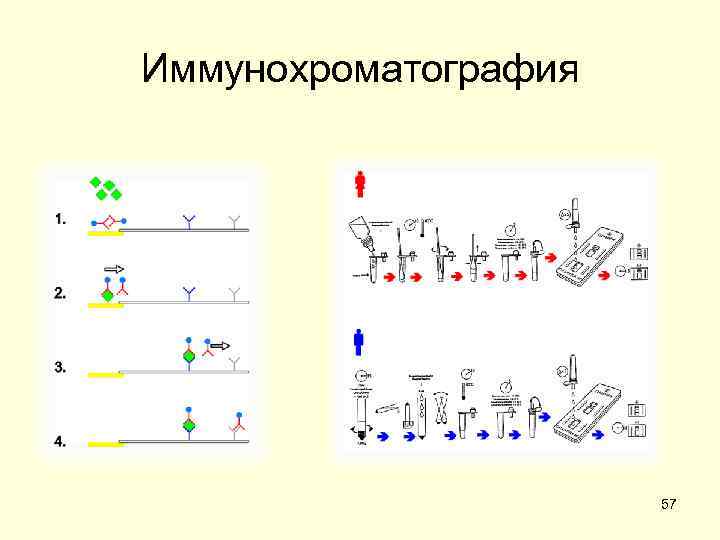
Иммунохроматография 57

Иммунохроматография € Чувствительность 77, 8% 93, 8% Специфичность 97, 5% 99, 8% Достоверность «+» 86, 6% 98, 4% Достоверность «-» 95, 4% 99, 2% Сравнение с культуральным методом 58
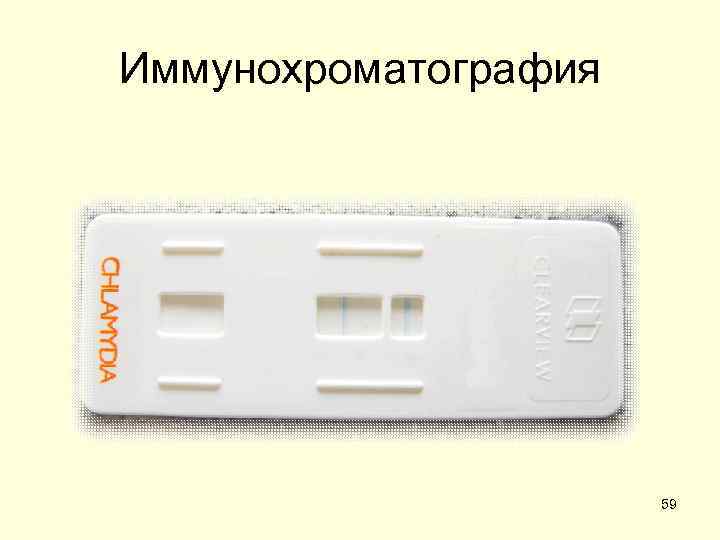
Иммунохроматография 59

Серодиагностика • Иммуноферментный анализ • Точечный ИФА • Непрямая микро иммунопероксидазная реакция • Непрямая реакция иммунолюминесценции 60
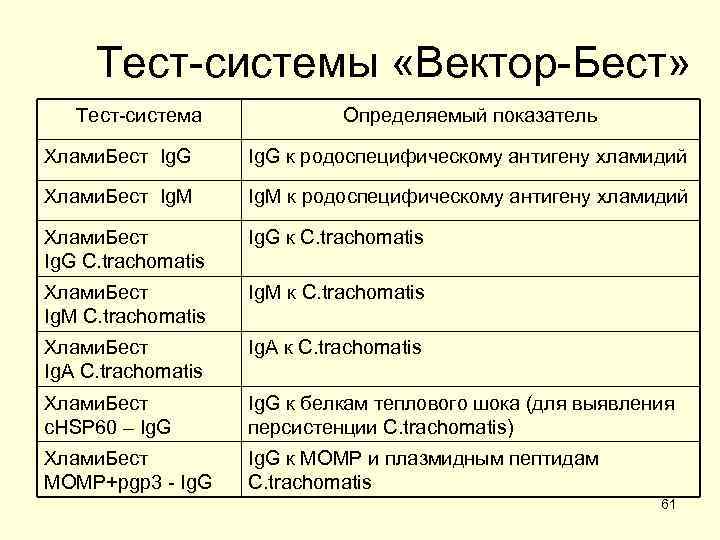
Тест-системы «Вектор-Бест» Тест-система Определяемый показатель Хлами. Бест Ig. G к родоспецифическому антигену хламидий Хлами. Бест Ig. M к родоспецифическому антигену хламидий Хлами. Бест Ig. G С. trachomatis Ig. G к С. trachomatis Хлами. Бест Ig. M С. trachomatis Ig. M к С. trachomatis Хлами. Бест Ig. A С. trachomatis Ig. A к С. trachomatis Хлами. Бест c. HSP 60 – Ig. G к белкам теплового шока (для выявления персистенции С. trachomatis) Хлами. Бест MOMP+pgp 3 - Ig. G к MOMP и плазмидным пептидам С. trachomatis 61

Immuno. Comb Orgenics • • • Ig. A, Ig. G полная комплектация наборов (мини лаборатория); для постановки реакции и ее учета не требуется приборное обеспечение; практичность (позволяет исследовать любое число проб - от 1 до 36); быстрота получения результатов (45 - 90 мин. ); • • стабильность (срок хранения >9 месяцев); простота в работе (не требует специальной квалификации); надежность (наличие внутреннего контроля); возможность исследования сыворотки или плазмы. 62
Immuno. Comb Orgenics 63
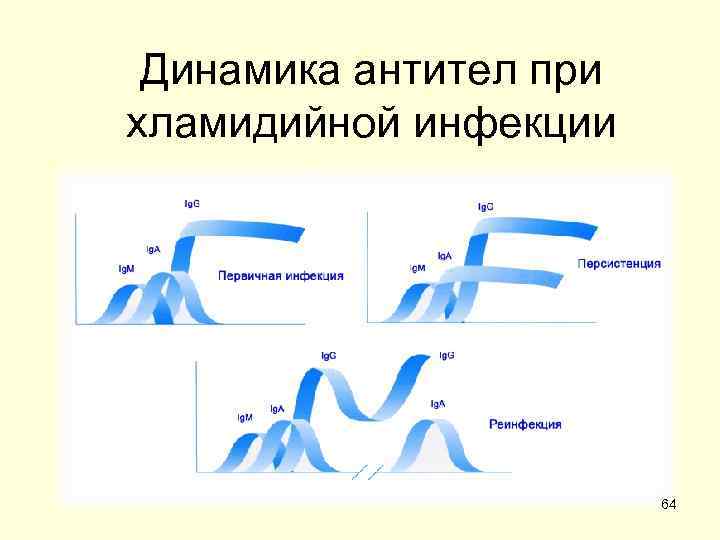
Динамика антител при хламидийной инфекции 64

65
66

67

68

69

70
71

Факторы вирулентности • Структурные факторы: адгезины, микрокапсула – обеспечивает адгезию и защищает от фагоцитоза. Эндотоксины – ЛПС. • Ферменты агрессии: фосфолипаза А, аминопептидазы – гидролизует фосфолипиды мембраны клетки; нейраминидаза – взаимодействует с поверхностными структурами клетки, содержащими сиаловые кислоты, разрушает клеточные мембраны и межклеточные взаимодействия; протеазы – вызывают дегрануляцию клеток; ДНК-азы, РНК-азы. 72

• Эпидемиология. Основной путь передачи – половой. Показатель инфицированности в разных странах – 10 -50%. • Клинические проявления. Инфицируются органы мочеполовой системы, вызывая деструктивновоспалительные процессы с выраженными микроциркуляторными нарушениями. • У мужчин возбудитель колонизирует уретру и крайнюю плоть с развитием уретрита и простатита. • У женщин – вагинозы, реже уретриты, цервициты, сальпингиты, эндометриты, аднекситы, параовариальные абсцессы. У беременных – преждевременные роды, внутриутробное заражение плода, послеродовой сепсис. 73

• Резистентность. Низкая, чувствительны к обычным антисептикам и дезинфектантам. • Иммунитет. Не выражен, характерны случаи повторного заражения. Фагоцитоз незавершенный. В цитоплазме нейтрофилов жизнеспособен. Дефицит компонентов комплемента создает условия для персистенции. Протективную функцию выполняют SIg. A, гуморальные Ат всех классов и специфически сенсибилизированные лимфоциты. 74

75

76

77

78

79

80

81

82

83

84

85

86

87

88

89

90

91

Лечение и профилактика • Лечение: Микоплазмы чувствительны к фторхинолонам, макролидам, цефалоспоринам, азалидам, тетрациклинам. Исчезновение клинической симптоматики часто не означает полного уничтожения возбудителя. • Профилактика. Специфическая отсутствует. Неспецифическая направлена на ликвидацию источника инфекции, на разрыв механизма и путей передачи, на повышение невосприимчивости коллектива к инфекции. 92
Lek_rikket_khlamidii_mikoplazmy.ppt