INFLAMMATIO, DEMONSTRATION FOR LECTURE 1.ppt
- Количество слайдов: 191
 ВОСПАЛЕНИЕ INFLAMMATIO PHLOGOSIS
ВОСПАЛЕНИЕ INFLAMMATIO PHLOGOSIS
 Определение типового ПАТОЛОГИЧЕСКОГО процесса в (1) озникающий и сохраняющийся в ходе эволюции (2) СТЕРЕОТИПНЫЙ (имеющий типичные черты у животных разного вида вне зависимости от причины) (3)УНИВЕРСАЛЬНЫЙ (встречающийся в структуре разных нозологических форм) (4) АУТОХТОННЫЙ, ЭКВИФИНАЛЬНЫЙ (саморазвивающийся до «своей конечной цели» )
Определение типового ПАТОЛОГИЧЕСКОГО процесса в (1) озникающий и сохраняющийся в ходе эволюции (2) СТЕРЕОТИПНЫЙ (имеющий типичные черты у животных разного вида вне зависимости от причины) (3)УНИВЕРСАЛЬНЫЙ (встречающийся в структуре разных нозологических форм) (4) АУТОХТОННЫЙ, ЭКВИФИНАЛЬНЫЙ (саморазвивающийся до «своей конечной цели» )
 ВОСПАЛЕНИЕ (КРАТКОЕ ОПРЕДЕЛЕНИЕ) МЕСТНЫЙ ОТВЕТ НА ПОВРЕЖДЕНИЕ В ВАСКУЛЯРИЗОВАННЫХ ОБЛАСТЯХ.
ВОСПАЛЕНИЕ (КРАТКОЕ ОПРЕДЕЛЕНИЕ) МЕСТНЫЙ ОТВЕТ НА ПОВРЕЖДЕНИЕ В ВАСКУЛЯРИЗОВАННЫХ ОБЛАСТЯХ.
 ГИППОКРАТ (V – IV век до н. э. ) Болезнь - результат "дискразии" (неправильного смешения соков): избыток соков в отдельном месте приводит к развитию воспаления.
ГИППОКРАТ (V – IV век до н. э. ) Болезнь - результат "дискразии" (неправильного смешения соков): избыток соков в отдельном месте приводит к развитию воспаления.
 Для Гиппократа ВОСПАЛЕНИЕ и БОЛЕЗНЬ - понятия тождественные; воспаление - это форма, в которой протекает болезнь.
Для Гиппократа ВОСПАЛЕНИЕ и БОЛЕЗНЬ - понятия тождественные; воспаление - это форма, в которой протекает болезнь.
 Уже во времена Гиппократа было известно о расширении сосудов после повреждения: «Ubi stimulus, ibi fluxus» .
Уже во времена Гиппократа было известно о расширении сосудов после повреждения: «Ubi stimulus, ibi fluxus» .
 ЦЕЛЬС ( I век н. э. ) выделил 4 основных феноменологических признака ВОСПАЛЕНИЯ: «Notae vero inflammationis sunt quator, rubor et tumor, cum calore et dolore» Гален добавил к этим четырем признакам пятый - "functio laesa".
ЦЕЛЬС ( I век н. э. ) выделил 4 основных феноменологических признака ВОСПАЛЕНИЯ: «Notae vero inflammationis sunt quator, rubor et tumor, cum calore et dolore» Гален добавил к этим четырем признакам пятый - "functio laesa".
 JOHN HUNTER (1728 – 1793) Шотландский хирург - один из основоположников экспериментального направления в патологии - моделировал и наблюдал течение ВОСПАЛЕНИЯ. Изучал развитие новых сосудов, повышение температуры, образование струпа. Первым заключил: ВОСПАЛЕНИЕ - не болезнь, а неспецифический ответ на любое повреждение, полезный для его «владельца» .
JOHN HUNTER (1728 – 1793) Шотландский хирург - один из основоположников экспериментального направления в патологии - моделировал и наблюдал течение ВОСПАЛЕНИЯ. Изучал развитие новых сосудов, повышение температуры, образование струпа. Первым заключил: ВОСПАЛЕНИЕ - не болезнь, а неспецифический ответ на любое повреждение, полезный для его «владельца» .
 Суть ВОСПАЛЕНИЯ - местное расширение сосудов (и артерий, и вен). Конечная цель ВОСПАЛЕНИЯ - восстановление естественной функции соответствующих частей.
Суть ВОСПАЛЕНИЯ - местное расширение сосудов (и артерий, и вен). Конечная цель ВОСПАЛЕНИЯ - восстановление естественной функции соответствующих частей.
 XVIII – первая половина XIXвв. В XVIII - первой половине XIX веков изучение ВОСПАЛЕНИЯ проходит в направлении исследования сосудистой реакции. Вильсон (1801), Томсон (1809), Гастингс (1818) указали на ускорение кровообращения в воспаленной части (ускорение вначале и замедление - в конце).
XVIII – первая половина XIXвв. В XVIII - первой половине XIX веков изучение ВОСПАЛЕНИЯ проходит в направлении исследования сосудистой реакции. Вильсон (1801), Томсон (1809), Гастингс (1818) указали на ускорение кровообращения в воспаленной части (ускорение вначале и замедление - в конце).
 В 1826 г. Жандрен наблюдал выход кровяных шариков из капилляров, когда замедление кровотока доходит до стаза. Эти кровяные шарики образуют гной.
В 1826 г. Жандрен наблюдал выход кровяных шариков из капилляров, когда замедление кровотока доходит до стаза. Эти кровяные шарики образуют гной.
 Паралитическая теория воспаления (Генле и Шиллинг, 1846) Сигнал о повреждении по чувствительным нервам достигает ЦНС, ответ осуществляется через раздражение вазомоторов, антагонистический паралич сосудистой стенки, расстройство кровообращения и питания развитие ВОСПАЛЕНИЯ.
Паралитическая теория воспаления (Генле и Шиллинг, 1846) Сигнал о повреждении по чувствительным нервам достигает ЦНС, ответ осуществляется через раздражение вазомоторов, антагонистический паралич сосудистой стенки, расстройство кровообращения и питания развитие ВОСПАЛЕНИЯ.
 ОСНОВНЫЕ ТЕОРИИ ВОСПАЛЕНИЯ ♥ Нутритивная (аттракционная) (Rudolf VIRHOW, 1853 -56) ♥ Биологическая (фагоцитарная) (И. И. Мечников, 1882 - 83) ♥ Физико – химическая (Hunter SCHADE, 1923) ♥ Сосудистая (Julius COHNHEIM, 1867) ♥ Медиаторная (V. MENKIN, 1938, 40, 48)
ОСНОВНЫЕ ТЕОРИИ ВОСПАЛЕНИЯ ♥ Нутритивная (аттракционная) (Rudolf VIRHOW, 1853 -56) ♥ Биологическая (фагоцитарная) (И. И. Мечников, 1882 - 83) ♥ Физико – химическая (Hunter SCHADE, 1923) ♥ Сосудистая (Julius COHNHEIM, 1867) ♥ Медиаторная (V. MENKIN, 1938, 40, 48)
 ТЕОРИЯ VIRHOW’а «Нутритивная, аттракционная» (Rudolf VIRHOW, 1853 -56) первая научная теория воспаления, в которой, основное внимание автора сосредоточено на изменениях в клетках.
ТЕОРИЯ VIRHOW’а «Нутритивная, аттракционная» (Rudolf VIRHOW, 1853 -56) первая научная теория воспаления, в которой, основное внимание автора сосредоточено на изменениях в клетках.
 В ответ на действие флогогена изменения в тканях могут быть пассивными (дегенерация, некроз) и активными (прогрессивные гипертрофии, гиперплазии и регенерация).
В ответ на действие флогогена изменения в тканях могут быть пассивными (дегенерация, некроз) и активными (прогрессивные гипертрофии, гиперплазии и регенерация).
 Флогоген обусловливает аттракцию клетками "питательного материала" ("нутритивное раздражение").
Флогоген обусловливает аттракцию клетками "питательного материала" ("нутритивное раздражение").
 Клетки, претерпевшие «нутритивное раздражение» , а затем и окружающие их клетки, увеличиваются в объеме, делятся, образуют большое количество недифференцированных клеток ( «бластема» ),
Клетки, претерпевшие «нутритивное раздражение» , а затем и окружающие их клетки, увеличиваются в объеме, делятся, образуют большое количество недифференцированных клеток ( «бластема» ),
 которые далее превращаются в соединительнотканные элементы или в другие виды тканей.
которые далее превращаются в соединительнотканные элементы или в другие виды тканей.
 ТЕОРИЯ COHNHEIM’a «Сосудистая» (J. Cohnheim, 1867) Главный момент в ВОСПАЛЕНИИ - сосудистая реакция и выход лейкоцитов из сосуда. J. Cohnheim писал: « Я могу определенно доказать, что только одна сосудистая стенка определяет весь ход событий» .
ТЕОРИЯ COHNHEIM’a «Сосудистая» (J. Cohnheim, 1867) Главный момент в ВОСПАЛЕНИИ - сосудистая реакция и выход лейкоцитов из сосуда. J. Cohnheim писал: « Я могу определенно доказать, что только одна сосудистая стенка определяет весь ход событий» .
 J. Cohnheim показал, что после перерезки и разрушения спинного мозга у лягушки можно получить обычную воспалительную реакцию, чем de facto определил роль нервной системы в развитии воспаления.
J. Cohnheim показал, что после перерезки и разрушения спинного мозга у лягушки можно получить обычную воспалительную реакцию, чем de facto определил роль нервной системы в развитии воспаления.
 Причина воспаления в «опыте Конхайма» – подсыхание на воздухе извлеченной и расправленной над отверстием дощечки брыжейки лягушки.
Причина воспаления в «опыте Конхайма» – подсыхание на воздухе извлеченной и расправленной над отверстием дощечки брыжейки лягушки.
 Cohnheim описал сосудистые реакции, сменяющие одна другую в ответ на повреждение: артериальную гиперемию, смешанную гиперемию, венозную гиперемию, стаз.
Cohnheim описал сосудистые реакции, сменяющие одна другую в ответ на повреждение: артериальную гиперемию, смешанную гиперемию, венозную гиперемию, стаз.
 А также – феномен краевого стояния (маргинации) лейкоцитов и феномен их эмиграции из сосудистого русла.
А также – феномен краевого стояния (маргинации) лейкоцитов и феномен их эмиграции из сосудистого русла.
 ТЕОРИЯ МЕЧНИКОВА «Фагоцитарная» И. И. Мечников первым применил Сравнительный метод в патологии ВОСПАЛЕНИЕ имеет место только у животных и в полном объеме проявляется начиная с рыб.
ТЕОРИЯ МЕЧНИКОВА «Фагоцитарная» И. И. Мечников первым применил Сравнительный метод в патологии ВОСПАЛЕНИЕ имеет место только у животных и в полном объеме проявляется начиная с рыб.
 В ходе ВОСПАЛЕНИЯ фагоциты выходят из сосудистого русла в очаг ВОСПАЛЕНИЯ. Именно фагоцитарная реакция есть "primum movens" [первичный источник] ВОСПАЛЕНИЯ. Все остальное в Воспалении - суть аксессуары, облегчающие приток фагоцитов к месту повреждения.
В ходе ВОСПАЛЕНИЯ фагоциты выходят из сосудистого русла в очаг ВОСПАЛЕНИЯ. Именно фагоцитарная реакция есть "primum movens" [первичный источник] ВОСПАЛЕНИЯ. Все остальное в Воспалении - суть аксессуары, облегчающие приток фагоцитов к месту повреждения.
 Воспаление – защитный ТПП, поскольку фагоцитоз приводит к ликвидации флогогена.
Воспаление – защитный ТПП, поскольку фагоцитоз приводит к ликвидации флогогена.
 Рисунки из книги И. И. Мечникова «Сравнительная патология воспаления» (1893) А. Четыре лейкоцита лягушки, поглотившие сибиреязвенные бациллы. Некоторые бациллы остались живыми и не окрасились. Другие погибли, и в них проник краситель везувин. Б. Сибиреязвенные бациллы, окрашенные везувином, в цитоплазме лейкоцита лягушки. В, Г Чужеродный предмет(окрашен) в теле личинки морской звезды окружен фагоцитами образовавшими в результате слияния многоядерный плазмодий. На рис Г плазмодий показан при большом увеличении. Д. Мезенхимальные фагоциты вокруг чужеродного предмета а теле личинки морской звезды.
Рисунки из книги И. И. Мечникова «Сравнительная патология воспаления» (1893) А. Четыре лейкоцита лягушки, поглотившие сибиреязвенные бациллы. Некоторые бациллы остались живыми и не окрасились. Другие погибли, и в них проник краситель везувин. Б. Сибиреязвенные бациллы, окрашенные везувином, в цитоплазме лейкоцита лягушки. В, Г Чужеродный предмет(окрашен) в теле личинки морской звезды окружен фагоцитами образовавшими в результате слияния многоядерный плазмодий. На рис Г плазмодий показан при большом увеличении. Д. Мезенхимальные фагоциты вокруг чужеродного предмета а теле личинки морской звезды.
 ТЕОРИЯ SCHADE «Физико – химическая» (Gunter Schade, 1923) В ответ на действие флогогена начинается сильное повышение местного метаболизма – «пожар обмена» , ходе которого в высокомолекулярные продукты распадаются на вещества с меньшим содержанием атомов.
ТЕОРИЯ SCHADE «Физико – химическая» (Gunter Schade, 1923) В ответ на действие флогогена начинается сильное повышение местного метаболизма – «пожар обмена» , ходе которого в высокомолекулярные продукты распадаются на вещества с меньшим содержанием атомов.
 возрастание числа частиц и повышение осмотического давления внутри будущего очага ВОСПАЛЕНИЯ обусловливают tumor,
возрастание числа частиц и повышение осмотического давления внутри будущего очага ВОСПАЛЕНИЯ обусловливают tumor,
 высвобождение большого количества тепла обусловливает calor ,
высвобождение большого количества тепла обусловливает calor ,
 накопление большого количества метаболитов и возникновение Н - гиперионии и ацидоза.
накопление большого количества метаболитов и возникновение Н - гиперионии и ацидоза.
 Ацидоз – основа аутохтонности. Ацидоз вызывает расширение сосудов rubor , раздражает рецепторы dolor.
Ацидоз – основа аутохтонности. Ацидоз вызывает расширение сосудов rubor , раздражает рецепторы dolor.
 Отечная жидкость сдавливает нервы и сосуды замедление кровотока и стаз. Ацидоз в очаге В развитие дегенеративных изменений в клетках: * мутное набухание, * зернистое и жировое перерождение.
Отечная жидкость сдавливает нервы и сосуды замедление кровотока и стаз. Ацидоз в очаге В развитие дегенеративных изменений в клетках: * мутное набухание, * зернистое и жировое перерождение.
 PMN, имеющие малый удельный вес, при замедлении кровотока отбрасываются на периферию прилипают к сосудистой стенке
PMN, имеющие малый удельный вес, при замедлении кровотока отбрасываются на периферию прилипают к сосудистой стенке
 проникают через нее и направляются в фокус ВОСПАЛЕНИЯ по градиенту изменения поверхностного натяжения. Эти нарушения - стимул раздражения соединительной ткани.
проникают через нее и направляются в фокус ВОСПАЛЕНИЯ по градиенту изменения поверхностного натяжения. Эти нарушения - стимул раздражения соединительной ткани.
 ТЕОРИЯ MENKIN’a «МЕДИАТОРНАЯ» (Valy Menkin, 1938, 40, 48) Химически разделил фракции выпота, содержащие факторы, способные спровоцировать различные компоненты воспаления и выделил некоторые аттрактанты, способные воспроизвести всю феноменологию Воспаления (около 25 веществ).
ТЕОРИЯ MENKIN’a «МЕДИАТОРНАЯ» (Valy Menkin, 1938, 40, 48) Химически разделил фракции выпота, содержащие факторы, способные спровоцировать различные компоненты воспаления и выделил некоторые аттрактанты, способные воспроизвести всю феноменологию Воспаления (около 25 веществ).
 ПИРЕКСИН повышение температуры НЕКРОЗИН некроз ЭКССУДИН экссудация
ПИРЕКСИН повышение температуры НЕКРОЗИН некроз ЭКССУДИН экссудация
 ЛЕЙКОТАКСИН = полипептидный фактор проницаемости Эмиграция лейкоцитов ЛЕЙКОПЕНИЧЕСКИЙ ФАКТОР лейкопения ФАКТОР ПРОЛИФЕРАЦИИ пролиферация
ЛЕЙКОТАКСИН = полипептидный фактор проницаемости Эмиграция лейкоцитов ЛЕЙКОПЕНИЧЕСКИЙ ФАКТОР лейкопения ФАКТОР ПРОЛИФЕРАЦИИ пролиферация
 Задержка повреждающего агента ("фиксация") определяется: повышенным выходом фибриногена, образованием сетки фибрина и тромбов, закупоривающих просвет отводящих лимфатических сосудов.
Задержка повреждающего агента ("фиксация") определяется: повышенным выходом фибриногена, образованием сетки фибрина и тромбов, закупоривающих просвет отводящих лимфатических сосудов.
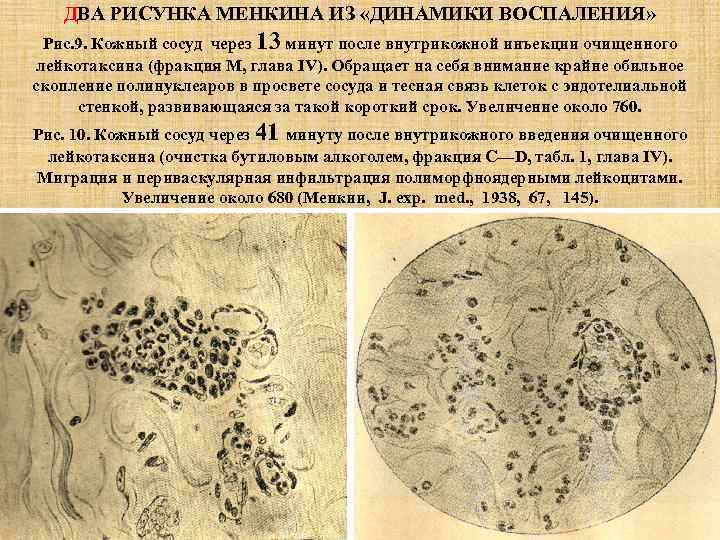 ДВА РИСУНКА МЕНКИНА ИЗ «ДИНАМИКИ ВОСПАЛЕНИЯ» Рис. 9. Кожный сосуд через 13 минут после внутрикожной инъекции очищенного лейкотаксина (фракция М, глава IV). Обращает на себя внимание крайне обильное скопление полинуклеаров в просвете сосуда и тесная связь клеток с эндотелиальной стенкой, развивающаяся за такой короткий срок. Увеличение около 760. Рис. 10. Кожный сосуд через 41 минуту после внутрикожного введения очищенного лейкотаксина (очистка бутиловым алкоголем, фракция С—D, табл. 1, глава IV). Миграция и периваскулярная инфильтрация полиморфноядерными лейкоцитами. Увеличение около 680 (Менкии, J. exp. med. , 1938, 67, 145).
ДВА РИСУНКА МЕНКИНА ИЗ «ДИНАМИКИ ВОСПАЛЕНИЯ» Рис. 9. Кожный сосуд через 13 минут после внутрикожной инъекции очищенного лейкотаксина (фракция М, глава IV). Обращает на себя внимание крайне обильное скопление полинуклеаров в просвете сосуда и тесная связь клеток с эндотелиальной стенкой, развивающаяся за такой короткий срок. Увеличение около 760. Рис. 10. Кожный сосуд через 41 минуту после внутрикожного введения очищенного лейкотаксина (очистка бутиловым алкоголем, фракция С—D, табл. 1, глава IV). Миграция и периваскулярная инфильтрация полиморфноядерными лейкоцитами. Увеличение около 680 (Менкии, J. exp. med. , 1938, 67, 145).
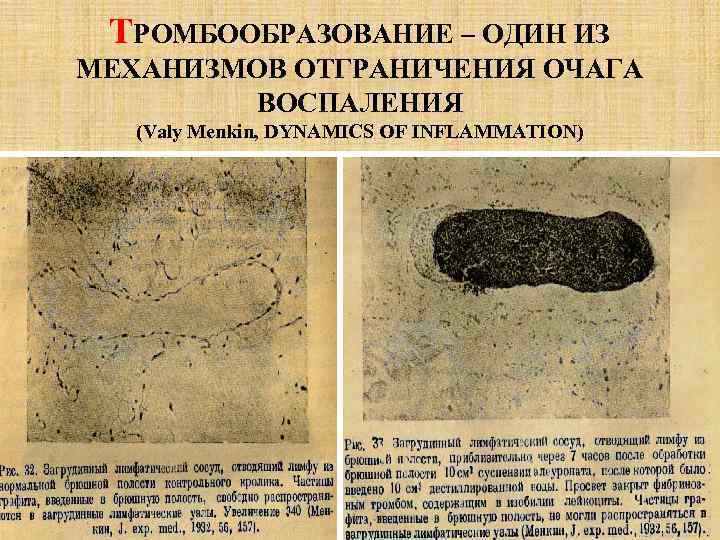 ТРОМБООБРАЗОВАНИЕ – ОДИН ИЗ МЕХАНИЗМОВ ОТГРАНИЧЕНИЯ ОЧАГА ВОСПАЛЕНИЯ (Valy Menkin, DYNAMICS OF INFLAMMATION)
ТРОМБООБРАЗОВАНИЕ – ОДИН ИЗ МЕХАНИЗМОВ ОТГРАНИЧЕНИЯ ОЧАГА ВОСПАЛЕНИЯ (Valy Menkin, DYNAMICS OF INFLAMMATION)
 Первыми в очаг ВОСПАЛЕНИЯ мигрируют PMN. Их миграция связана с освобождением из пораженных тканей ЛЕЙКОТАКСИНА, обусловливающего и хемотаксис, и повышенную проницаемость.
Первыми в очаг ВОСПАЛЕНИЯ мигрируют PMN. Их миграция связана с освобождением из пораженных тканей ЛЕЙКОТАКСИНА, обусловливающего и хемотаксис, и повышенную проницаемость.
 PMN постепенно вытесняются из очага MN. Макрофаги способны выдержать снижение р. Н до 6. 9 и 6. 8, тогда как дальнейшее снижение р. Н является гибельным для всех типов лейкоцитов, которые гибнут, обусловливая развитие нагноения.
PMN постепенно вытесняются из очага MN. Макрофаги способны выдержать снижение р. Н до 6. 9 и 6. 8, тогда как дальнейшее снижение р. Н является гибельным для всех типов лейкоцитов, которые гибнут, обусловливая развитие нагноения.
 Очаг В. обособлен от организма: имеет собственный обмен, свою концентрацию водородных ионов, свое модифицированное кровообращение.
Очаг В. обособлен от организма: имеет собственный обмен, свою концентрацию водородных ионов, свое модифицированное кровообращение.
 По Менкину: ВОСПАЛЕНИЕ - экстраординарный комплексный механизм, направленный на задержание или уничтожение химического или бактериального возбудителя, приводящий в конечном счете к организации и регенерации пораженной ткани.
По Менкину: ВОСПАЛЕНИЕ - экстраординарный комплексный механизм, направленный на задержание или уничтожение химического или бактериального возбудителя, приводящий в конечном счете к организации и регенерации пораженной ткани.
 Алексис Каррель (1873 - 1944, Нобелевская премия 1912 г. за сосудистый шов) в 1910 -12 гг. начал культивирование тканей. Обнаружил, что fbl сердца цыпленка живут в культуре только при добавлении сока насиженного яйца. Он назвал стимуляторы, полученные из сока без которых культура гибнет, трефоны.
Алексис Каррель (1873 - 1944, Нобелевская премия 1912 г. за сосудистый шов) в 1910 -12 гг. начал культивирование тканей. Обнаружил, что fbl сердца цыпленка живут в культуре только при добавлении сока насиженного яйца. Он назвал стимуляторы, полученные из сока без которых культура гибнет, трефоны.
 В 1922 г. он открыл трефоны в составе воспалительного экссудата и показал, что трефоны воспалительного экссудата гораздо сильнее способствуют росту культуры.
В 1922 г. он открыл трефоны в составе воспалительного экссудата и показал, что трефоны воспалительного экссудата гораздо сильнее способствуют росту культуры.
 Так было доказано, что стимуляторы пролиферации безвариантно присутствуют в воспалительном экссудате.
Так было доказано, что стимуляторы пролиферации безвариантно присутствуют в воспалительном экссудате.
 Christian de Duve, Кристиан де Дюв, (р. 1917, бельгийский биохимик и цитолог, Нобелевский лауреат 1974 г за открытие лизосом) в 1951 г. описал лизосомы и пероксисомы, и показал важную роль лизосом и пероксисом в ходе развития воспаления.
Christian de Duve, Кристиан де Дюв, (р. 1917, бельгийский биохимик и цитолог, Нобелевский лауреат 1974 г за открытие лизосом) в 1951 г. описал лизосомы и пероксисомы, и показал важную роль лизосом и пероксисом в ходе развития воспаления.
 В 50 -70 е гг ХХ века учение о воспалении обогатилось представлениями о роли медиаторов фосфолипидной природы.
В 50 -70 е гг ХХ века учение о воспалении обогатилось представлениями о роли медиаторов фосфолипидной природы.
 В 80 е гг ХХ века научные интересы концентрируются на изучении медиаторов пептидной природы (интерлейкины, нейропептиды).
В 80 е гг ХХ века научные интересы концентрируются на изучении медиаторов пептидной природы (интерлейкины, нейропептиды).
 И, наконец, представления о молекулах адгезии клеток (МАК) и роли МАК при самых разнообразных формах межклеточных взаимодействий при воспалении.
И, наконец, представления о молекулах адгезии клеток (МАК) и роли МАК при самых разнообразных формах межклеточных взаимодействий при воспалении.
 Современный этап учения о воспалении характеризуется сближением учения о воспалении с учением об иммунитете.
Современный этап учения о воспалении характеризуется сближением учения о воспалении с учением об иммунитете.
 Если В. – ТПП, неспецифически обеспечивающий отграничение и репарацию на месте повреждения, то иммунный ответ - специфическая нейтрализация и создание иммунитета на случай повторной инфекции тем же патогеном.
Если В. – ТПП, неспецифически обеспечивающий отграничение и репарацию на месте повреждения, то иммунный ответ - специфическая нейтрализация и создание иммунитета на случай повторной инфекции тем же патогеном.
 Система TNF Два фактора: альфа (кахектин) и бета (лимфотоксин) Два рецептора: TNFR – alfa и TNFR beta (рецепторы для TNF обнаружены на всех соматических клетках за исключением эритроцитов) Два естественных ингибитора: TNF BP I и TNF BP II (proteolytically processed extracellular domains of TNF –alfa and TNF –beta, respectively)
Система TNF Два фактора: альфа (кахектин) и бета (лимфотоксин) Два рецептора: TNFR – alfa и TNFR beta (рецепторы для TNF обнаружены на всех соматических клетках за исключением эритроцитов) Два естественных ингибитора: TNF BP I и TNF BP II (proteolytically processed extracellular domains of TNF –alfa and TNF –beta, respectively)
 Триггеры и ингибиторы cистемы TNF «Триггеры» образования TNF: INF; IL-1, 2; GM-CSF; Иммунные комплексы Действуя на макрофаги, триггеры вызывают выделение TNF –alfa, действуя на лимфоциты, - выделение TNF- beta.
Триггеры и ингибиторы cистемы TNF «Триггеры» образования TNF: INF; IL-1, 2; GM-CSF; Иммунные комплексы Действуя на макрофаги, триггеры вызывают выделение TNF –alfa, действуя на лимфоциты, - выделение TNF- beta.
 «Ингибиторы» продукции TNF: IL 6, TNF beta, Vit. D 3, Дексаметазон, Циклоспорин А
«Ингибиторы» продукции TNF: IL 6, TNF beta, Vit. D 3, Дексаметазон, Циклоспорин А
 «ДВА ЛИЦА» В ЭФФЕКТАХ TNF Местные (паракринные) иммунный ответ, антибактериальный и антивирусный, стимуляция образования медиаторов воспаления,
«ДВА ЛИЦА» В ЭФФЕКТАХ TNF Местные (паракринные) иммунный ответ, антибактериальный и антивирусный, стимуляция образования медиаторов воспаления,
 стимуляция образования МАК, стимуляция пролиферации, антиопухолевая активность, образование гранулом
стимуляция образования МАК, стимуляция пролиферации, антиопухолевая активность, образование гранулом
 Системные (токсические) кахексия, альтерация тканей, тромбогеморрагический синдром
Системные (токсические) кахексия, альтерация тканей, тромбогеморрагический синдром
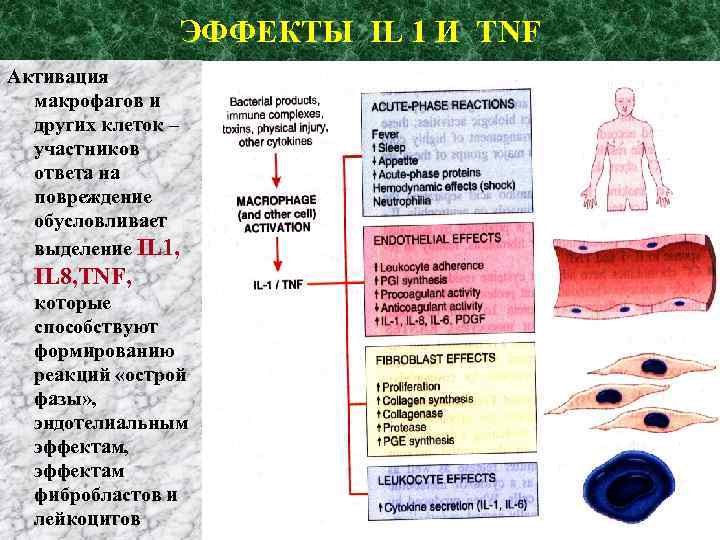 ЭФФЕКТЫ IL 1 И TNF Активация макрофагов и других клеток – участников ответа на повреждение обусловливает выделение IL 1, IL 8, TNF, которые способствуют формированию реакций «острой фазы» , эндотелиальным эффектам, эффектам фибробластов и лейкоцитов
ЭФФЕКТЫ IL 1 И TNF Активация макрофагов и других клеток – участников ответа на повреждение обусловливает выделение IL 1, IL 8, TNF, которые способствуют формированию реакций «острой фазы» , эндотелиальным эффектам, эффектам фибробластов и лейкоцитов
 ГЛАВНЫЕ ЭФФЕКТЫ IL 1/TNF В ВОСПАЛЕНИИ На “реакции острой фазы”: лихорадка, сонливость, угнетение аппетита,
ГЛАВНЫЕ ЭФФЕКТЫ IL 1/TNF В ВОСПАЛЕНИИ На “реакции острой фазы”: лихорадка, сонливость, угнетение аппетита,
 нейтрофилия, стимуляция синтеза белков острой фазы, гемодинамические системные эффекты (шок).
нейтрофилия, стимуляция синтеза белков острой фазы, гемодинамические системные эффекты (шок).
 На эндотелий: стимуляция синтеза МАК, стимуляция синтеза PG I, стимуляция синтеза ФАТ, M-CSF
На эндотелий: стимуляция синтеза МАК, стимуляция синтеза PG I, стимуляция синтеза ФАТ, M-CSF
 стимуляция прокоагулянтной активности, торможение антикоагулянтной активности, стимуляция синтеза IL 1, стимуляция синтеза GM-CSF, G-CSF, M-CSF
стимуляция прокоагулянтной активности, торможение антикоагулянтной активности, стимуляция синтеза IL 1, стимуляция синтеза GM-CSF, G-CSF, M-CSF
 На фибробласты: cтимуляция пролиферации, синтеза коллагеназы,
На фибробласты: cтимуляция пролиферации, синтеза коллагеназы,
 синтеза протеаз, синтеза PG E. На лимфоциты: активация лимфоцитов к производству IL-2
синтеза протеаз, синтеза PG E. На лимфоциты: активация лимфоцитов к производству IL-2
 На гранулоциты: стимуляция синтеза МАК, стимуляция миграции в поврежденную ткань и образования гранулоцитами токсичных соединений кислорода, разрушающих бактерии (прайминг)
На гранулоциты: стимуляция синтеза МАК, стимуляция миграции в поврежденную ткань и образования гранулоцитами токсичных соединений кислорода, разрушающих бактерии (прайминг)
 БЕЛКОВЫЕ ФАКТОРЫ, УЧАСТВУЮЩИЕ И В ВОСПАЛЕНИИ, И В ИММУННОМ ОТВЕТЕ Семейство Представители Интерфероны Альфа-, бета-, гамма TNF Альфа (кахектин), Бета (лимфотоксин) Интерлейкины 1 альфа, бета, 2, 3, 4, 5, 6
БЕЛКОВЫЕ ФАКТОРЫ, УЧАСТВУЮЩИЕ И В ВОСПАЛЕНИИ, И В ИММУННОМ ОТВЕТЕ Семейство Представители Интерфероны Альфа-, бета-, гамма TNF Альфа (кахектин), Бета (лимфотоксин) Интерлейкины 1 альфа, бета, 2, 3, 4, 5, 6
 Семейство Представители Колониистимулирующие G-CSF, M-CSF, GM-CSF, Факторы (CSF) EPO Факторы роста Эпидермальный (EGF) Фибробластов (FGF, КИСЛЫЙ И ОСНОВНЫЙ) Инсулиноподобный (IGF 1, 2) Нервов Тромбоцитарный (PDGF) Трансформирующий (TGF)
Семейство Представители Колониистимулирующие G-CSF, M-CSF, GM-CSF, Факторы (CSF) EPO Факторы роста Эпидермальный (EGF) Фибробластов (FGF, КИСЛЫЙ И ОСНОВНЫЙ) Инсулиноподобный (IGF 1, 2) Нервов Тромбоцитарный (PDGF) Трансформирующий (TGF)
 определение воспаления ТПП, развивающийся в ответ на местное повреждение, протекающий аутохтонно, проявляющийся триединством развития во времени АЛЬТЕРАЦИИ, ЭКССУДАЦИИ, ПРОЛИФЕРАЦИИ;
определение воспаления ТПП, развивающийся в ответ на местное повреждение, протекающий аутохтонно, проявляющийся триединством развития во времени АЛЬТЕРАЦИИ, ЭКССУДАЦИИ, ПРОЛИФЕРАЦИИ;
 направленный на локализацию и уничтожение агента, вызвавшего повреждение, и на репарацию дефекта. Наблюдается только в васкуляризованных органах. Феноменологически характеризуется как "Calor, tumor, rubor, dolor et functio leasa”.
направленный на локализацию и уничтожение агента, вызвавшего повреждение, и на репарацию дефекта. Наблюдается только в васкуляризованных органах. Феноменологически характеризуется как "Calor, tumor, rubor, dolor et functio leasa”.
 INFLAMMATIO, PHLOGOSIS ВОСПАЛЕНИЕ – ТРИЕДИНСТВО АЛЬТЕРАЦИИ, ЭКССУДАЦИИ И ПРОЛИФЕРАЦИИ АЛЬТЕРАЦИЯ ЭКССУДАЦИЯ ПРОЛИФЕРАЦИЯ
INFLAMMATIO, PHLOGOSIS ВОСПАЛЕНИЕ – ТРИЕДИНСТВО АЛЬТЕРАЦИИ, ЭКССУДАЦИИ И ПРОЛИФЕРАЦИИ АЛЬТЕРАЦИЯ ЭКССУДАЦИЯ ПРОЛИФЕРАЦИЯ
 ВАРИАНТЫ ПОВРЕЖДЕНИЯ ТРАВМА ИНФЕКЦИЯ ИММУНОЛОГИЧЕСКОЕ ПОВРЕЖДЕНИЕ
ВАРИАНТЫ ПОВРЕЖДЕНИЯ ТРАВМА ИНФЕКЦИЯ ИММУНОЛОГИЧЕСКОЕ ПОВРЕЖДЕНИЕ
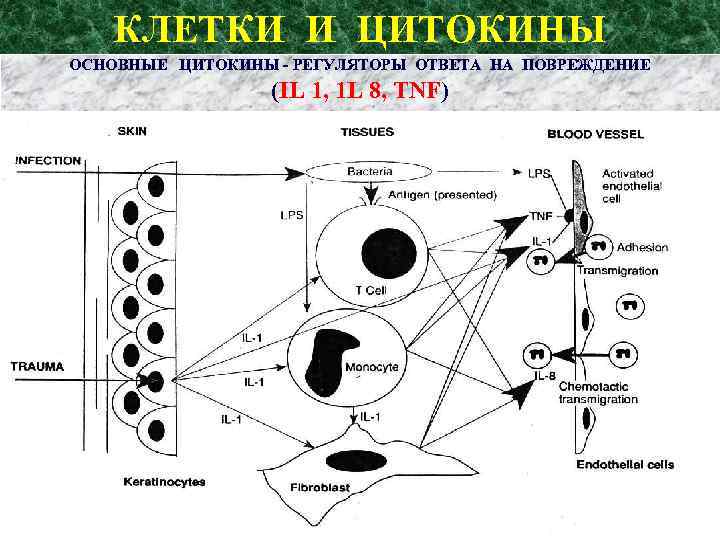 КЛЕТКИ И ЦИТОКИНЫ ОСНОВНЫЕ ЦИТОКИНЫ - РЕГУЛЯТОРЫ ОТВЕТА НА ПОВРЕЖДЕНИЕ (IL 1, 1 L 8, TNF)
КЛЕТКИ И ЦИТОКИНЫ ОСНОВНЫЕ ЦИТОКИНЫ - РЕГУЛЯТОРЫ ОТВЕТА НА ПОВРЕЖДЕНИЕ (IL 1, 1 L 8, TNF)
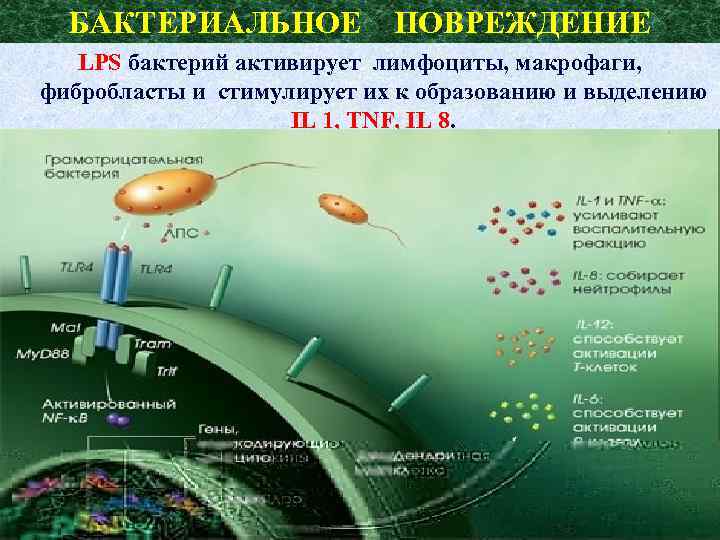 БАКТЕРИАЛЬНОЕ ПОВРЕЖДЕНИЕ LPS бактерий активирует лимфоциты, макрофаги, фибробласты и стимулирует их к образованию и выделению IL 1, TNF, IL 8.
БАКТЕРИАЛЬНОЕ ПОВРЕЖДЕНИЕ LPS бактерий активирует лимфоциты, макрофаги, фибробласты и стимулирует их к образованию и выделению IL 1, TNF, IL 8.
 АЛЬТЕРАТИВНЫЙ КОМПОНЕНТ
АЛЬТЕРАТИВНЫЙ КОМПОНЕНТ
 Флогоген альтерация первичная альтерация вторичная активные кислородные и кислород-галогеновые радикалы NO C 5 – C 9 ферменты лизосом TNF Катионные антибиотические белки Лактоферрин Некроз Некробиоз Дистрофии Апоптоз IL 1, IL 8, TNF Клеточные механизмы самоповреждения: Фагоцитоз КОЦ АЗКЦ
Флогоген альтерация первичная альтерация вторичная активные кислородные и кислород-галогеновые радикалы NO C 5 – C 9 ферменты лизосом TNF Катионные антибиотические белки Лактоферрин Некроз Некробиоз Дистрофии Апоптоз IL 1, IL 8, TNF Клеточные механизмы самоповреждения: Фагоцитоз КОЦ АЗКЦ
 АЛЬТЕРАТИВНЫЕ ИЗМЕНЕНИЯ В КЛЕТКЕ Альтерация как результат ишемии. Патогенез повреждения ПМ.
АЛЬТЕРАТИВНЫЕ ИЗМЕНЕНИЯ В КЛЕТКЕ Альтерация как результат ишемии. Патогенез повреждения ПМ.
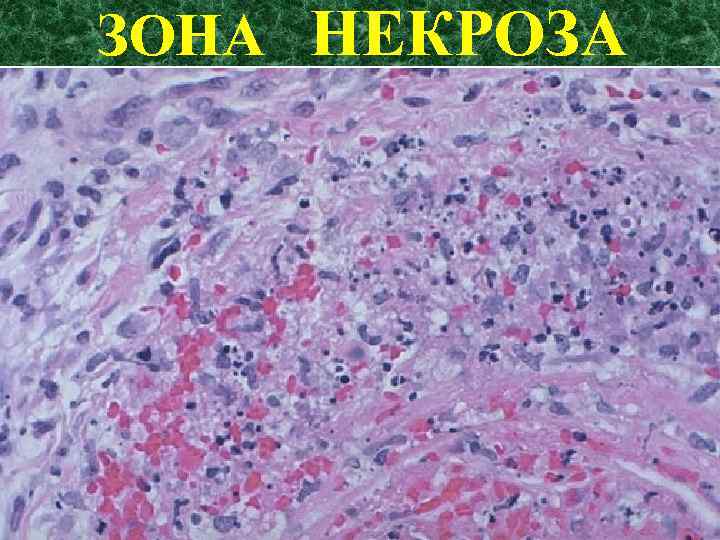 ЗОНА НЕКРОЗА (ОСТРОЕ ВОСПАЛЕНИЕ)
ЗОНА НЕКРОЗА (ОСТРОЕ ВОСПАЛЕНИЕ)
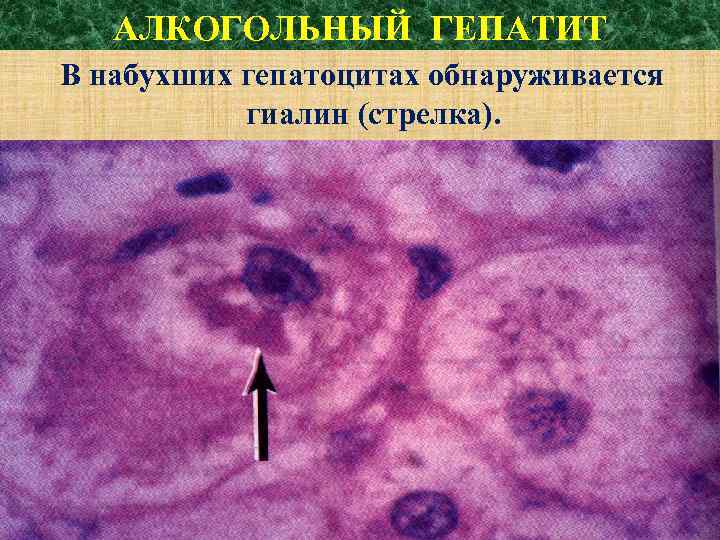 АЛКОГОЛЬНЫЙ ГЕПАТИТ В набухших гепатоцитах обнаруживается гиалин (стрелка).
АЛКОГОЛЬНЫЙ ГЕПАТИТ В набухших гепатоцитах обнаруживается гиалин (стрелка).
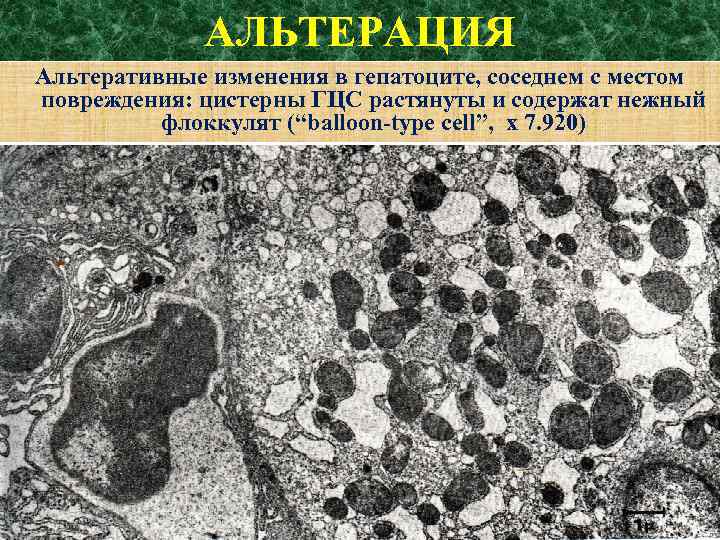 АЛЬТЕРАЦИЯ Альтеративные изменения в гепатоците, соседнем с местом повреждения: цистерны ГЦС растянуты и содержат нежный флоккулят (“balloon-type cell”, х 7. 920) )
АЛЬТЕРАЦИЯ Альтеративные изменения в гепатоците, соседнем с местом повреждения: цистерны ГЦС растянуты и содержат нежный флоккулят (“balloon-type cell”, х 7. 920) )
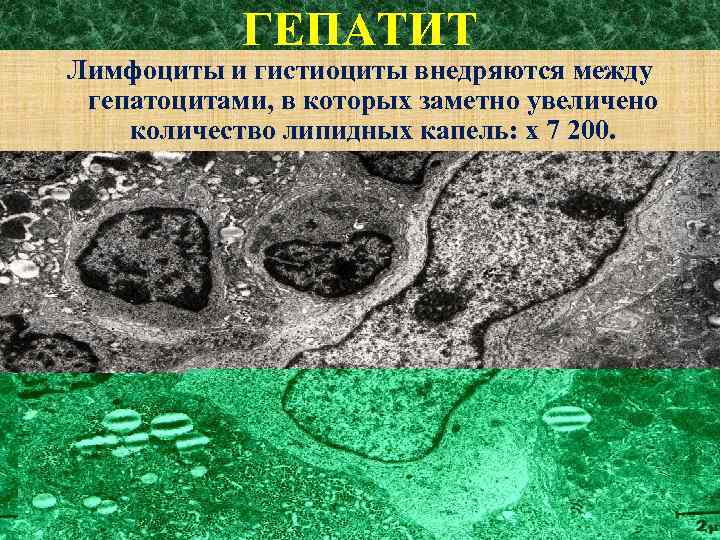 ГЕПАТИТ Лимфоциты и гистиоциты внедряются между гепатоцитами, в которых заметно увеличено количество липидных капель: х 7 200. (х 7, 200)
ГЕПАТИТ Лимфоциты и гистиоциты внедряются между гепатоцитами, в которых заметно увеличено количество липидных капель: х 7 200. (х 7, 200)
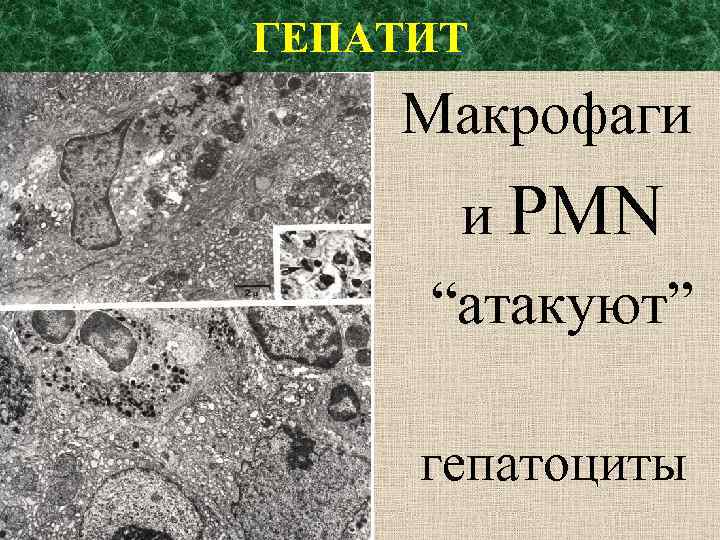 ГЕПАТИТ Макрофаги и PMN “атакуют” гепатоциты
ГЕПАТИТ Макрофаги и PMN “атакуют” гепатоциты
 ЭКССУДАТИВНЫЙ КОМПОНЕНТ
ЭКССУДАТИВНЫЙ КОМПОНЕНТ
 ЭКССУДАЦИЯ ФЛОГОГЕН ИШЕМИЯ АРТЕРИАЛЬНАЯ ГИПЕРЕМИЯ СМЕШАННАЯ ГИПЕРЕМИЯ ВЕНОЗНАЯ ГИПЕРЕМИЯ СТАЗ Сосудистым реакциям сопутствуют: маргинация (PMN, monocyte) трансмиграция (PMN, monocyte) фагоцитарная реакция формирование экссудата ( «экссудация» в узком смысле)
ЭКССУДАЦИЯ ФЛОГОГЕН ИШЕМИЯ АРТЕРИАЛЬНАЯ ГИПЕРЕМИЯ СМЕШАННАЯ ГИПЕРЕМИЯ ВЕНОЗНАЯ ГИПЕРЕМИЯ СТАЗ Сосудистым реакциям сопутствуют: маргинация (PMN, monocyte) трансмиграция (PMN, monocyte) фагоцитарная реакция формирование экссудата ( «экссудация» в узком смысле)
 Повреждение эндотелия обнажение базальной мембраны активация f. XII активация коагуляции, антикоагуляции, комплемента, кининов
Повреждение эндотелия обнажение базальной мембраны активация f. XII активация коагуляции, антикоагуляции, комплемента, кининов
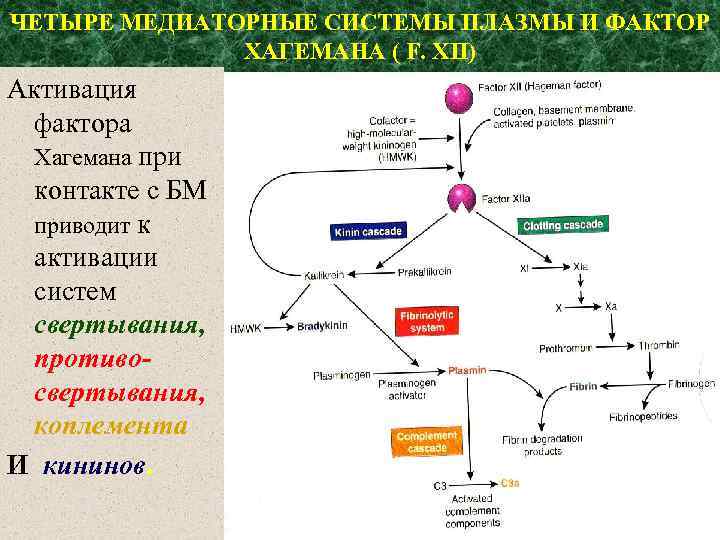 ЧЕТЫРЕ МЕДИАТОРНЫЕ СИСТЕМЫ ПЛАЗМЫ И ФАКТОР ХАГЕМАНА ( F. XII) Активация фактора Хагемана при контакте с БМ приводит к активации систем свертывания, противосвертывания, коплемента И кининов.
ЧЕТЫРЕ МЕДИАТОРНЫЕ СИСТЕМЫ ПЛАЗМЫ И ФАКТОР ХАГЕМАНА ( F. XII) Активация фактора Хагемана при контакте с БМ приводит к активации систем свертывания, противосвертывания, коплемента И кининов.
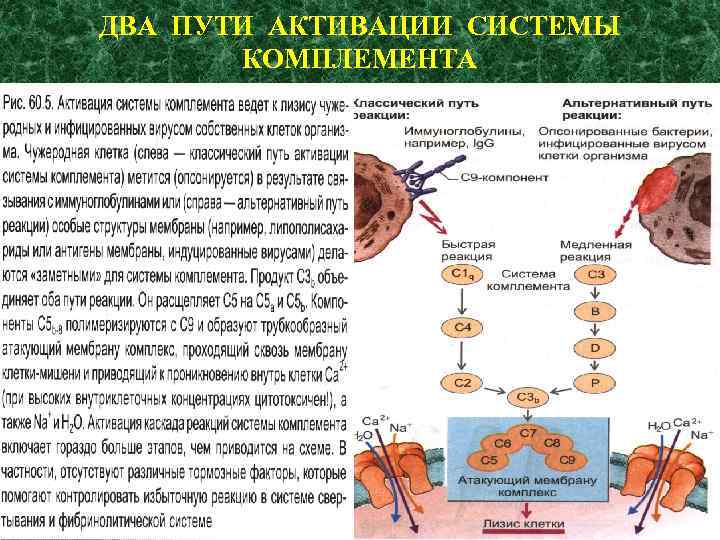 ДВА ПУТИ АКТИВАЦИИ СИСТЕМЫ КОМПЛЕМЕНТА
ДВА ПУТИ АКТИВАЦИИ СИСТЕМЫ КОМПЛЕМЕНТА
 НЕКОТОРЫЕ ЭФФЕКТЫ АКТИВИРОВАННОЙ СИСТЕМЫ КОМПЛЕМЕНТА И ЕЕ ОТДЕЛЬНЫХ КОМПОНЕНТОВ проницаемости сосудов (С 3 а и С 5 а) Сокращение гладкой мускулатуры Дегрануляция тучных клеток
НЕКОТОРЫЕ ЭФФЕКТЫ АКТИВИРОВАННОЙ СИСТЕМЫ КОМПЛЕМЕНТА И ЕЕ ОТДЕЛЬНЫХ КОМПОНЕНТОВ проницаемости сосудов (С 3 а и С 5 а) Сокращение гладкой мускулатуры Дегрануляция тучных клеток
 Опсонизация к последующему фагоцитозу бактерий и иммунных комплексов Активация PMN и хемотаксиса Лизис бактерий Лизис клеток, «помеченных» Ig G и М
Опсонизация к последующему фагоцитозу бактерий и иммунных комплексов Активация PMN и хемотаксиса Лизис бактерий Лизис клеток, «помеченных» Ig G и М
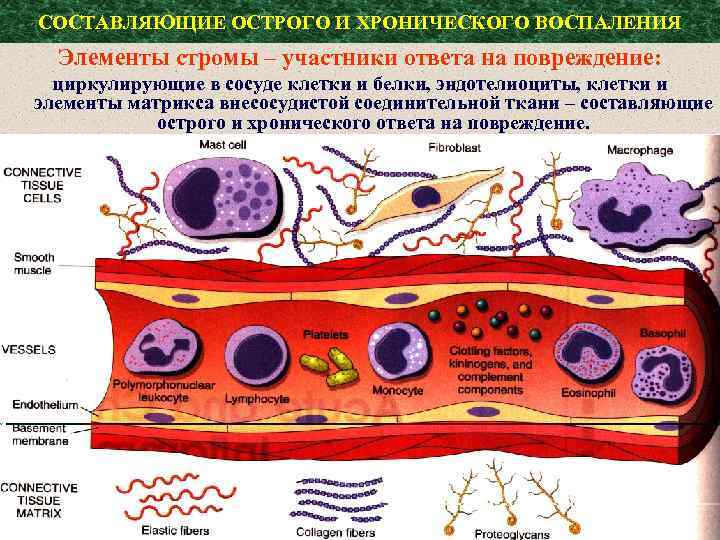 СОСТАВЛЯЮЩИЕ ОСТРОГО И ХРОНИЧЕСКОГО ВОСПАЛЕНИЯ Элементы стромы – участники ответа на повреждение: циркулирующие в сосуде клетки и белки, эндотелиоциты, клетки и элементы матрикса внесосудистой соединительной ткани – составляющие острого и хронического ответа на повреждение.
СОСТАВЛЯЮЩИЕ ОСТРОГО И ХРОНИЧЕСКОГО ВОСПАЛЕНИЯ Элементы стромы – участники ответа на повреждение: циркулирующие в сосуде клетки и белки, эндотелиоциты, клетки и элементы матрикса внесосудистой соединительной ткани – составляющие острого и хронического ответа на повреждение.
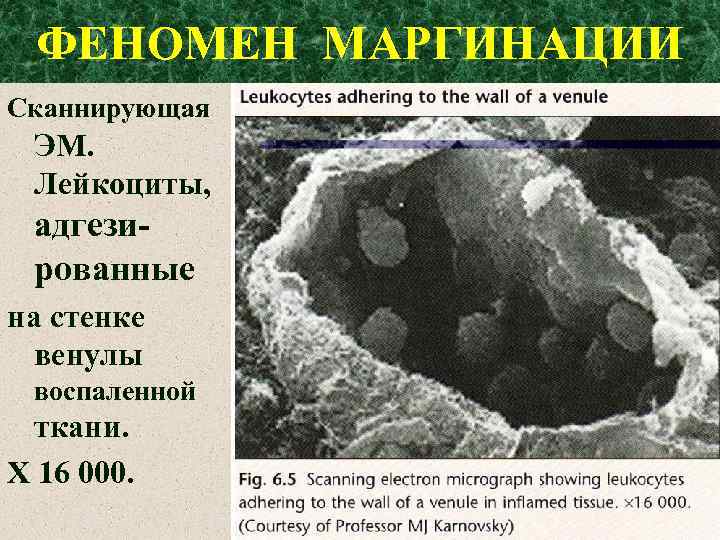 ФЕНОМЕН МАРГИНАЦИИ Сканнирующая ЭМ. Лейкоциты, адгезированные на стенке венулы воспаленной ткани. Х 16 000.
ФЕНОМЕН МАРГИНАЦИИ Сканнирующая ЭМ. Лейкоциты, адгезированные на стенке венулы воспаленной ткани. Х 16 000.
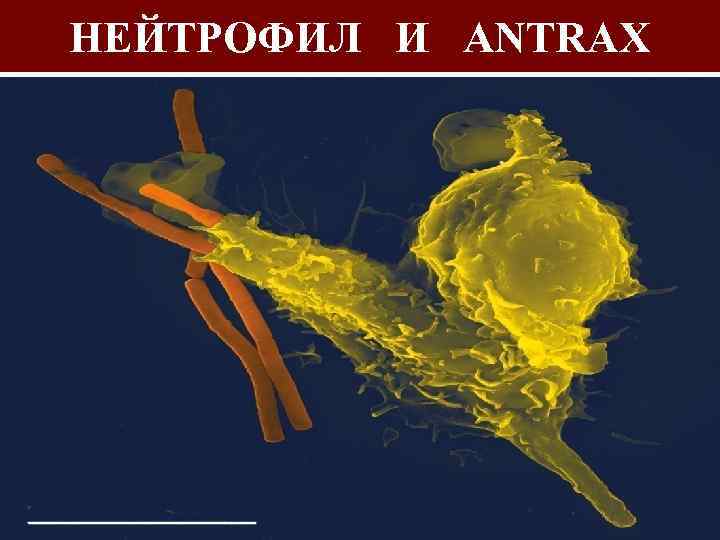 НЕЙТРОФИЛ И ANTRAX
НЕЙТРОФИЛ И ANTRAX
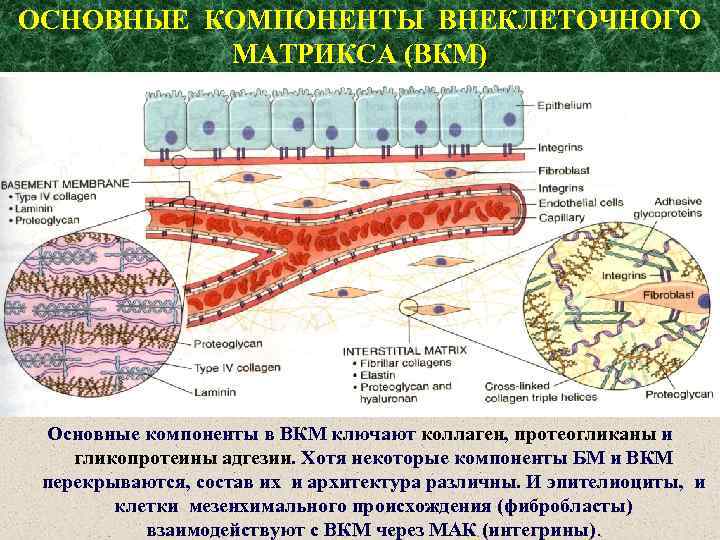 ОСНОВНЫЕ КОМПОНЕНТЫ ВНЕКЛЕТОЧНОГО МАТРИКСА (ВКМ) Основные компоненты в ВКМ ключают коллаген, протеогликаны и гликопротеины адгезии. Хотя некоторые компоненты БМ и ВКМ перекрываются, состав их и архитектура различны. И эпителиоциты, и клетки мезенхимального происхождения (фибробласты) взаимодействуют с ВКМ через МАК (интегрины).
ОСНОВНЫЕ КОМПОНЕНТЫ ВНЕКЛЕТОЧНОГО МАТРИКСА (ВКМ) Основные компоненты в ВКМ ключают коллаген, протеогликаны и гликопротеины адгезии. Хотя некоторые компоненты БМ и ВКМ перекрываются, состав их и архитектура различны. И эпителиоциты, и клетки мезенхимального происхождения (фибробласты) взаимодействуют с ВКМ через МАК (интегрины).
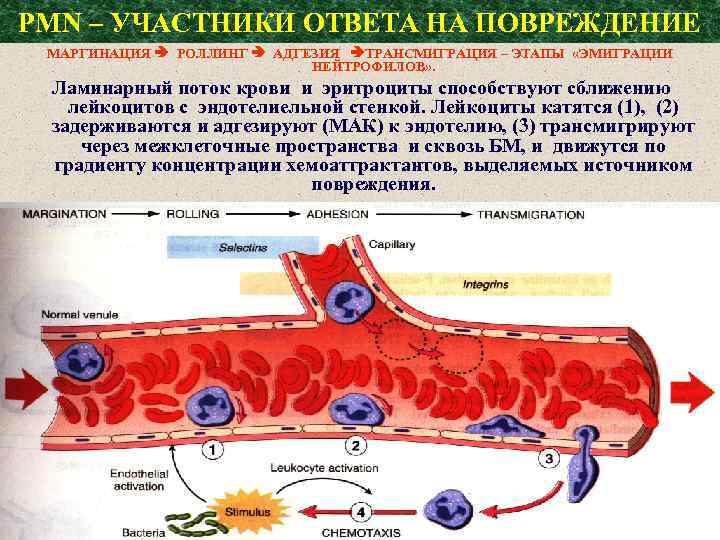 PMN – УЧАСТНИКИ ОТВЕТА НА ПОВРЕЖДЕНИЕ МАРГИНАЦИЯ РОЛЛИНГ АДГЕЗИЯ ТРАНСМИГРАЦИЯ – ЭТАПЫ «ЭМИГРАЦИИ НЕЙТРОФИЛОВ» . Ламинарный поток крови и эритроциты способствуют сближению лейкоцитов с эндотелиельной стенкой. Лейкоциты катятся (1), (2) задерживаются и адгезируют (МАК) к эндотелию, (3) трансмигрируют через межклеточные пространства и сквозь БМ, и движутся по градиенту концентрации хемоаттрактантов, выделяемых источником повреждения.
PMN – УЧАСТНИКИ ОТВЕТА НА ПОВРЕЖДЕНИЕ МАРГИНАЦИЯ РОЛЛИНГ АДГЕЗИЯ ТРАНСМИГРАЦИЯ – ЭТАПЫ «ЭМИГРАЦИИ НЕЙТРОФИЛОВ» . Ламинарный поток крови и эритроциты способствуют сближению лейкоцитов с эндотелиельной стенкой. Лейкоциты катятся (1), (2) задерживаются и адгезируют (МАК) к эндотелию, (3) трансмигрируют через межклеточные пространства и сквозь БМ, и движутся по градиенту концентрации хемоаттрактантов, выделяемых источником повреждения.
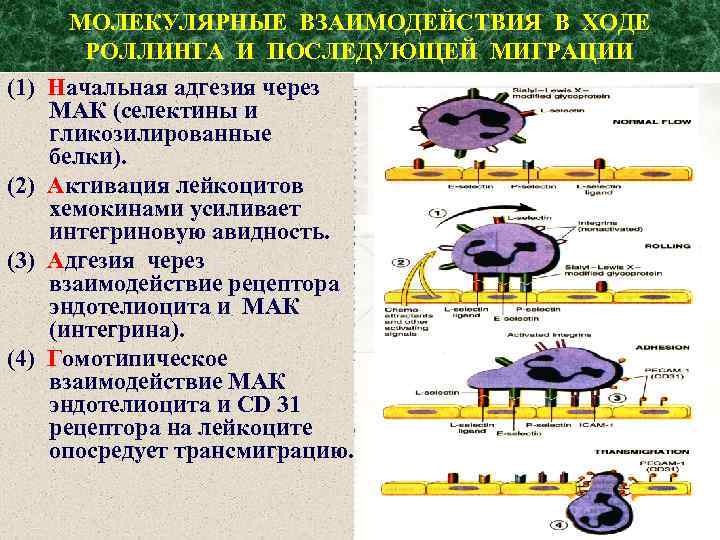 МОЛЕКУЛЯРНЫЕ ВЗАИМОДЕЙСТВИЯ В ХОДЕ РОЛЛИНГА И ПОСЛЕДУЮЩЕЙ МИГРАЦИИ (1) Начальная адгезия через МАК (селектины и гликозилированные белки). (2) Активация лейкоцитов хемокинами усиливает интегриновую авидность. (3) Адгезия через взаимодействие рецептора эндотелиоцита и МАК (интегрина). (4) Гомотипическое взаимодействие МАК эндотелиоцита и CD 31 рецептора на лейкоците опосредует трансмиграцию.
МОЛЕКУЛЯРНЫЕ ВЗАИМОДЕЙСТВИЯ В ХОДЕ РОЛЛИНГА И ПОСЛЕДУЮЩЕЙ МИГРАЦИИ (1) Начальная адгезия через МАК (селектины и гликозилированные белки). (2) Активация лейкоцитов хемокинами усиливает интегриновую авидность. (3) Адгезия через взаимодействие рецептора эндотелиоцита и МАК (интегрина). (4) Гомотипическое взаимодействие МАК эндотелиоцита и CD 31 рецептора на лейкоците опосредует трансмиграцию.
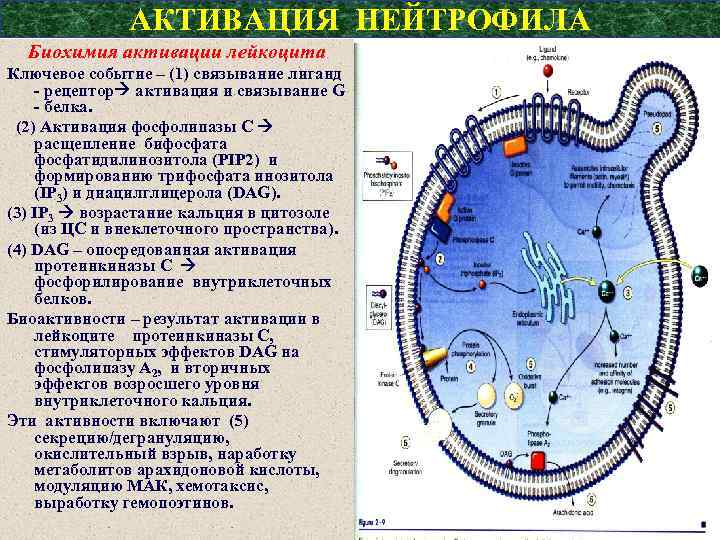 АКТИВАЦИЯ НЕЙТРОФИЛА Биохимия активации лейкоцита Ключевое событие – (1) связывание лиганд - рецептор активация и связывание G - белка. (2) Активация фосфолипазы C расщепление бифосфата фосфатидилинозитола (РIP 2) и формированию трифосфата инозитола (IP 3) и диацилглицерола (DAG). (3) IP 3 возрастание кальция в цитозоле (из ЦС и внеклеточного пространства). (4) DAG – опосредованная активация протеинкиназы С фосфорилирование внутриклеточных белков. Биоактивности – результат активации в лейкоците протеинкиназы С, стимуляторных эффектов DAG на фосфолипазу А 2, и вторичных эффектов возросшего уровня внутриклеточного кальция. Эти активности включают (5) секрецию/дегрануляцию, окислительный взрыв, наработку метаболитов арахидоновой кислоты, модуляцию МАК, хемотаксис, выработку гемопоэтинов.
АКТИВАЦИЯ НЕЙТРОФИЛА Биохимия активации лейкоцита Ключевое событие – (1) связывание лиганд - рецептор активация и связывание G - белка. (2) Активация фосфолипазы C расщепление бифосфата фосфатидилинозитола (РIP 2) и формированию трифосфата инозитола (IP 3) и диацилглицерола (DAG). (3) IP 3 возрастание кальция в цитозоле (из ЦС и внеклеточного пространства). (4) DAG – опосредованная активация протеинкиназы С фосфорилирование внутриклеточных белков. Биоактивности – результат активации в лейкоците протеинкиназы С, стимуляторных эффектов DAG на фосфолипазу А 2, и вторичных эффектов возросшего уровня внутриклеточного кальция. Эти активности включают (5) секрецию/дегрануляцию, окислительный взрыв, наработку метаболитов арахидоновой кислоты, модуляцию МАК, хемотаксис, выработку гемопоэтинов.
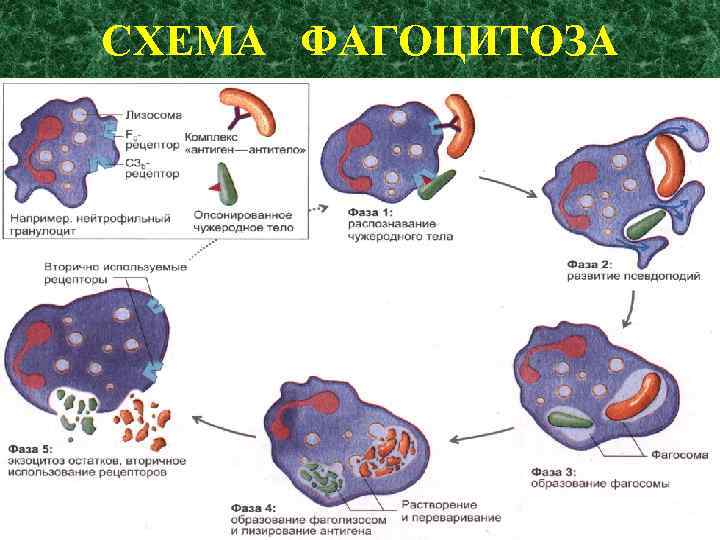 СХЕМА ФАГОЦИТОЗА
СХЕМА ФАГОЦИТОЗА
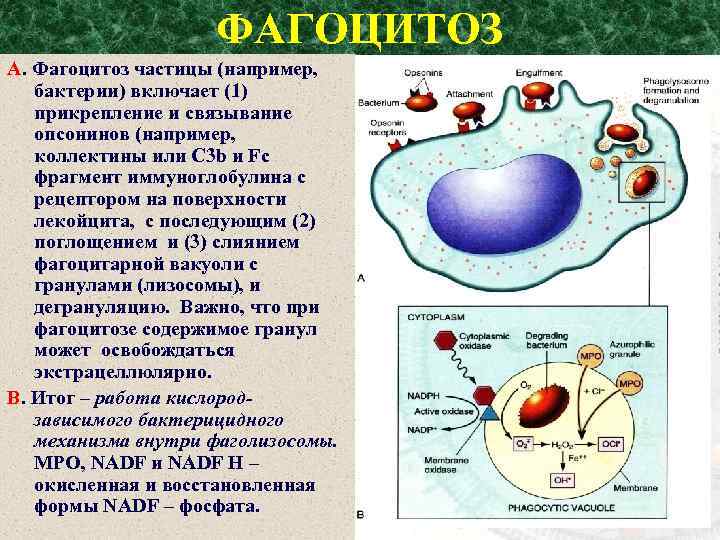 ФАГОЦИТОЗ А. Фагоцитоз частицы (например, бактерии) включает (1) прикрепление и связывание опсонинов (например, коллектины или C 3 b и Fc фрагмент иммуноглобулина с рецептором на поверхности лекойцита, с последующим (2) поглощением и (3) слиянием фагоцитарной вакуоли с гранулами (лизосомы), и дегрануляцию. Важно, что при фагоцитозе содержимое гранул может освобождаться экстрацеллюлярно. В. Итог – работа кислородзависимого бактерицидного механизма внутри фаголизосомы. MPO, NADF и NADF H – окисленная и восстановленная формы NАDF – фосфата.
ФАГОЦИТОЗ А. Фагоцитоз частицы (например, бактерии) включает (1) прикрепление и связывание опсонинов (например, коллектины или C 3 b и Fc фрагмент иммуноглобулина с рецептором на поверхности лекойцита, с последующим (2) поглощением и (3) слиянием фагоцитарной вакуоли с гранулами (лизосомы), и дегрануляцию. Важно, что при фагоцитозе содержимое гранул может освобождаться экстрацеллюлярно. В. Итог – работа кислородзависимого бактерицидного механизма внутри фаголизосомы. MPO, NADF и NADF H – окисленная и восстановленная формы NАDF – фосфата.
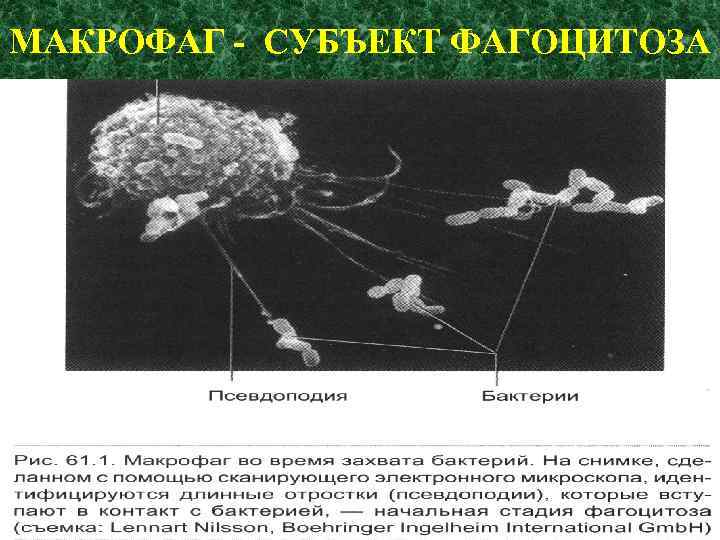 МАКРОФАГ - СУБЪЕКТ ФАГОЦИТОЗА
МАКРОФАГ - СУБЪЕКТ ФАГОЦИТОЗА
 МОРФОЛОГИЯ ЭКССУДАЦИИ Гиперемия сосудов И Маргинация нейтрофилов
МОРФОЛОГИЯ ЭКССУДАЦИИ Гиперемия сосудов И Маргинация нейтрофилов
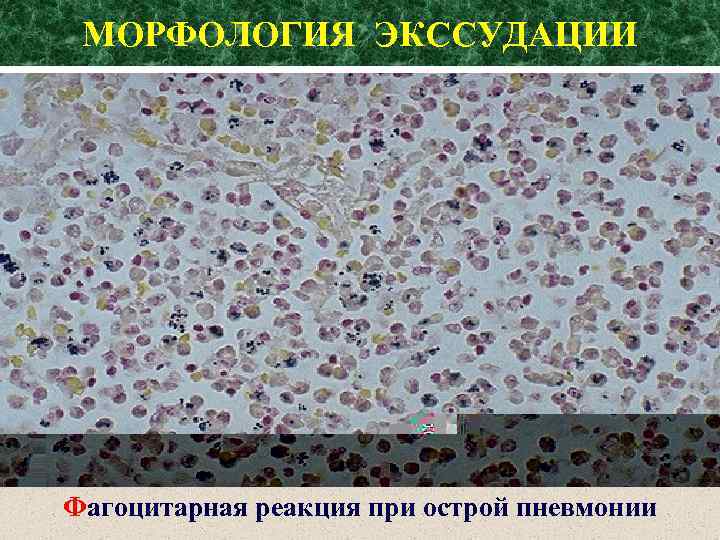 МОРФОЛОГИЯ ЭКССУДАЦИИ Фагоцитарная реакция при острой пневмонии
МОРФОЛОГИЯ ЭКССУДАЦИИ Фагоцитарная реакция при острой пневмонии
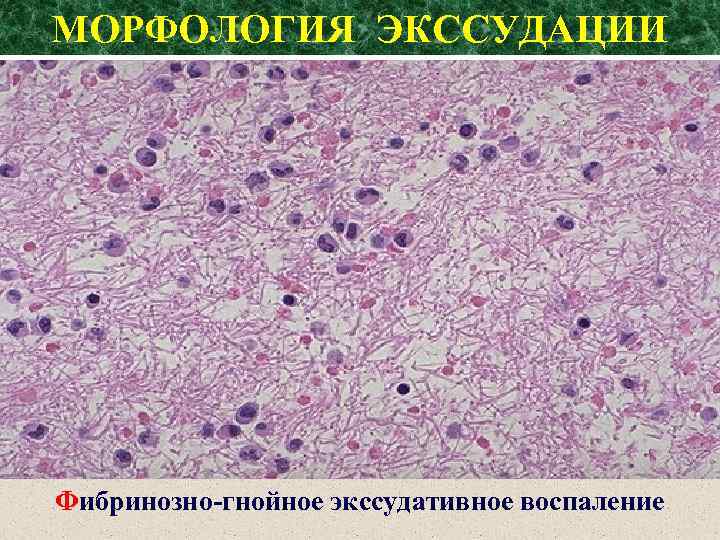 МОРФОЛОГИЯ ЭКССУДАЦИИ Фибринозно-гнойное экссудативное воспаление
МОРФОЛОГИЯ ЭКССУДАЦИИ Фибринозно-гнойное экссудативное воспаление
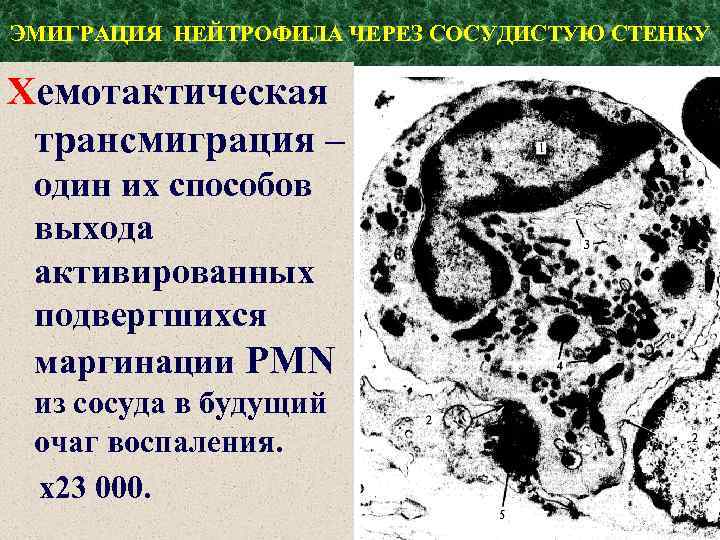 ЭМИГРАЦИЯ НЕЙТРОФИЛА ЧЕРЕЗ СОСУДИСТУЮ СТЕНКУ Хемотактическая трансмиграция – один их способов выхода активированных подвергшихся маргинации PMN из сосуда в будущий очаг воспаления. х23 000.
ЭМИГРАЦИЯ НЕЙТРОФИЛА ЧЕРЕЗ СОСУДИСТУЮ СТЕНКУ Хемотактическая трансмиграция – один их способов выхода активированных подвергшихся маргинации PMN из сосуда в будущий очаг воспаления. х23 000.
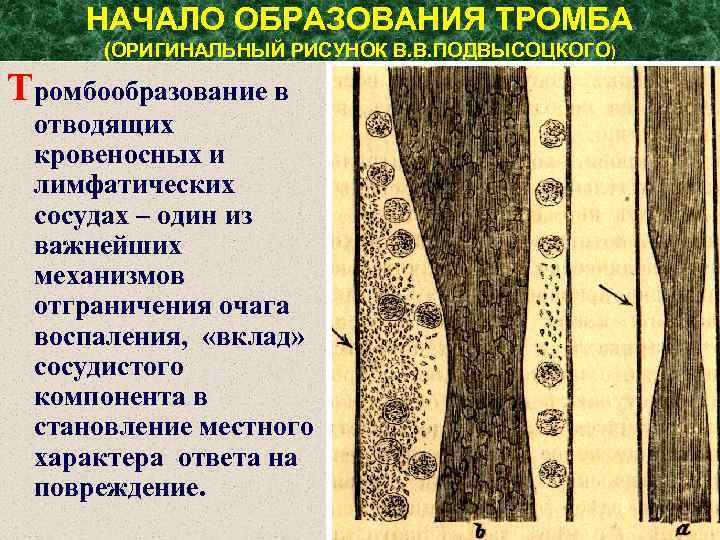 НАЧАЛО ОБРАЗОВАНИЯ ТРОМБА (ОРИГИНАЛЬНЫЙ РИСУНОК В. В. ПОДВЫСОЦКОГО) Тромбообразование в отводящих кровеносных и лимфатических сосудах – один из важнейших механизмов отграничения очага воспаления, «вклад» сосудистого компонента в становление местного характера ответа на повреждение.
НАЧАЛО ОБРАЗОВАНИЯ ТРОМБА (ОРИГИНАЛЬНЫЙ РИСУНОК В. В. ПОДВЫСОЦКОГО) Тромбообразование в отводящих кровеносных и лимфатических сосудах – один из важнейших механизмов отграничения очага воспаления, «вклад» сосудистого компонента в становление местного характера ответа на повреждение.
 ПРОЛИФЕРАТИВНЫЙ КОМПОНЕНТ
ПРОЛИФЕРАТИВНЫЙ КОМПОНЕНТ
 На первых этапах ответа на повреждение пролиферативный компонент, как и другие компоненты воспаления, способствует локализации повреждения: флогоген ишемия гипоксия размножение фибробластов и местных тканевых макрофагов
На первых этапах ответа на повреждение пролиферативный компонент, как и другие компоненты воспаления, способствует локализации повреждения: флогоген ишемия гипоксия размножение фибробластов и местных тканевых макрофагов
 По мере затухания острых альтеративных и экссудативных изменений (деструкция или устранение флогогена!) проявляется действие противовоспалительных медиаторов.
По мере затухания острых альтеративных и экссудативных изменений (деструкция или устранение флогогена!) проявляется действие противовоспалительных медиаторов.
 противовоспалительные медиаторы: гепарин аденозин хондроитин-сульфаты апопротеин Е ингибиторы протеаз
противовоспалительные медиаторы: гепарин аденозин хондроитин-сульфаты апопротеин Е ингибиторы протеаз
 антиоксиданты полиамины действие гистамина на Н 2 – рецепторы липоксины инактиваторы медиаторов воспаления
антиоксиданты полиамины действие гистамина на Н 2 – рецепторы липоксины инактиваторы медиаторов воспаления
 ПРОЛИФЕРАЦИЯ Процессы пролиферации и дифференцировки обусловлены эффектами факторов роста и дифференцировки: фактор роста эпидермиса фактор роста тромбоцитов инсулиноподобные факторы роста 1 и 2 (соматомедины А и С)
ПРОЛИФЕРАЦИЯ Процессы пролиферации и дифференцировки обусловлены эффектами факторов роста и дифференцировки: фактор роста эпидермиса фактор роста тромбоцитов инсулиноподобные факторы роста 1 и 2 (соматомедины А и С)
 фактор роста эндотелиоцитов факторы роста фибробластов (кислый, основный) гемопоэтины (G-CSF, GMCSF, M-CSF, IL – 3) интерлейкины (1, 2, 3, 4, 5, 6, 7) TNF alpha
фактор роста эндотелиоцитов факторы роста фибробластов (кислый, основный) гемопоэтины (G-CSF, GMCSF, M-CSF, IL – 3) интерлейкины (1, 2, 3, 4, 5, 6, 7) TNF alpha
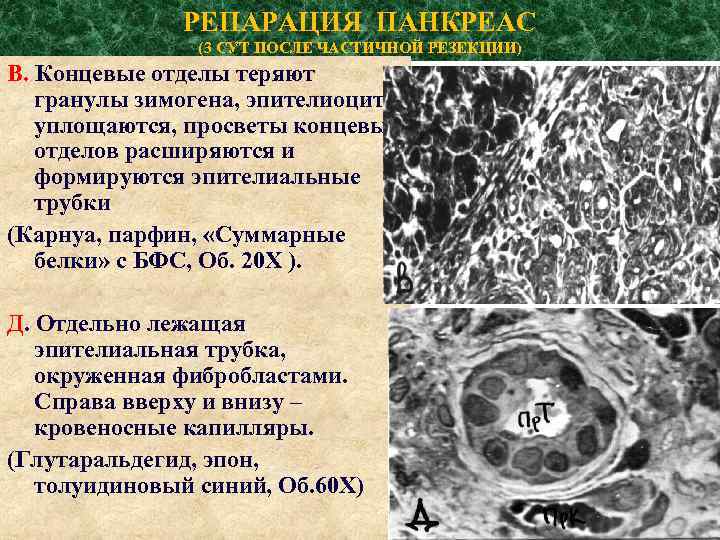 РЕПАРАЦИЯ ПАНКРЕАС (3 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) В. Концевые отделы теряют гранулы зимогена, эпителиоциты уплощаются, просветы концевых отделов расширяются и формируются эпителиальные трубки (Карнуа, парфин, «Суммарные белки» с БФС, Об. 20 Х ). Д. Отдельно лежащая эпителиальная трубка, окруженная фибробластами. Справа вверху и внизу – кровеносные капилляры. (Глутаральдегид, эпон, толуидиновый синий, Об. 60 Х)
РЕПАРАЦИЯ ПАНКРЕАС (3 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) В. Концевые отделы теряют гранулы зимогена, эпителиоциты уплощаются, просветы концевых отделов расширяются и формируются эпителиальные трубки (Карнуа, парфин, «Суммарные белки» с БФС, Об. 20 Х ). Д. Отдельно лежащая эпителиальная трубка, окруженная фибробластами. Справа вверху и внизу – кровеносные капилляры. (Глутаральдегид, эпон, толуидиновый синий, Об. 60 Х)
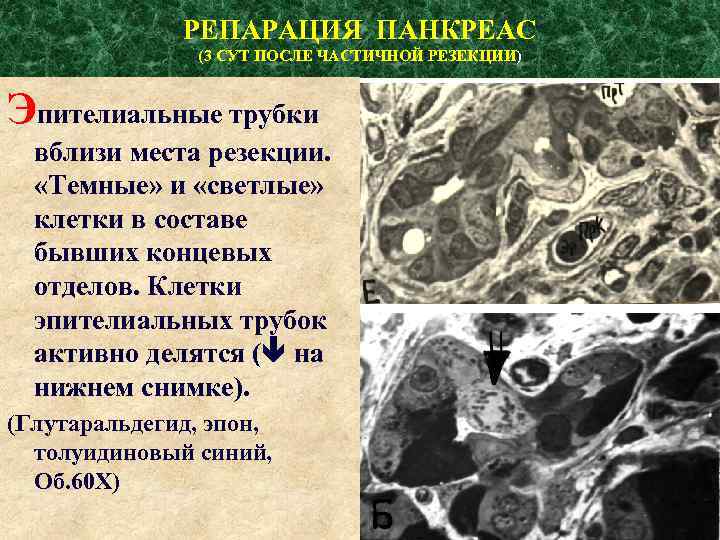 РЕПАРАЦИЯ ПАНКРЕАС (3 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) Эпителиальные трубки вблизи места резекции. «Темные» и «светлые» клетки в составе бывших концевых отделов. Клетки эпителиальных трубок активно делятся ( на нижнем снимке). (Глутаральдегид, эпон, толуидиновый синий, Об. 60 Х)
РЕПАРАЦИЯ ПАНКРЕАС (3 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) Эпителиальные трубки вблизи места резекции. «Темные» и «светлые» клетки в составе бывших концевых отделов. Клетки эпителиальных трубок активно делятся ( на нижнем снимке). (Глутаральдегид, эпон, толуидиновый синий, Об. 60 Х)
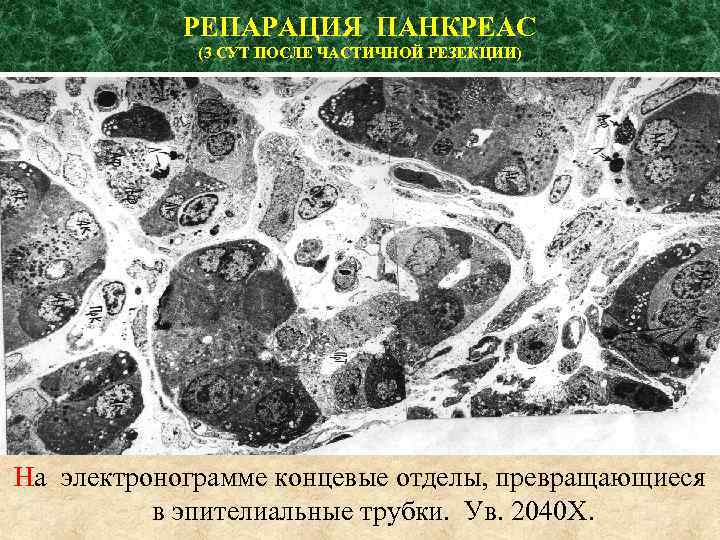 РЕПАРАЦИЯ ПАНКРЕАС (3 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) На электронограмме концевые отделы, превращающиеся в эпителиальные трубки. Ув. 2040 Х.
РЕПАРАЦИЯ ПАНКРЕАС (3 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) На электронограмме концевые отделы, превращающиеся в эпителиальные трубки. Ув. 2040 Х.
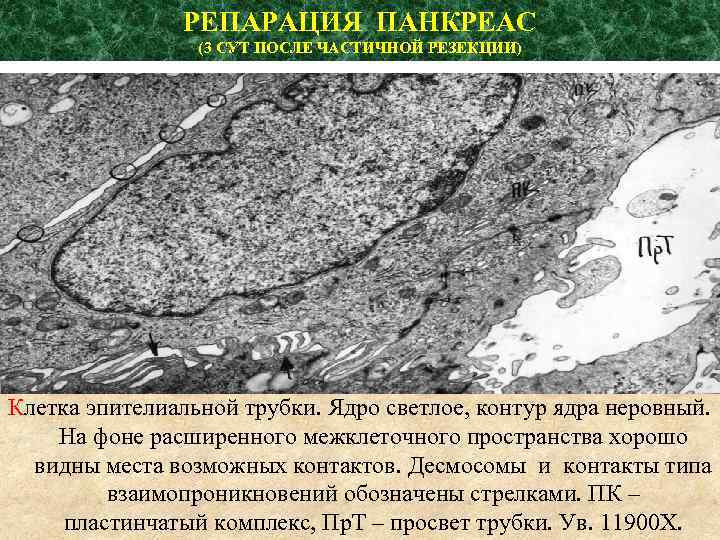 РЕПАРАЦИЯ ПАНКРЕАС (3 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) Клетка эпителиальной трубки. Ядро светлое, контур ядра неровный. На фоне расширенного межклеточного пространства хорошо видны места возможных контактов. Десмосомы и контакты типа взаимопроникновений обозначены стрелками. ПК – пластинчатый комплекс, Пр. Т – просвет трубки. Ув. 11900 Х.
РЕПАРАЦИЯ ПАНКРЕАС (3 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) Клетка эпителиальной трубки. Ядро светлое, контур ядра неровный. На фоне расширенного межклеточного пространства хорошо видны места возможных контактов. Десмосомы и контакты типа взаимопроникновений обозначены стрелками. ПК – пластинчатый комплекс, Пр. Т – просвет трубки. Ув. 11900 Х.
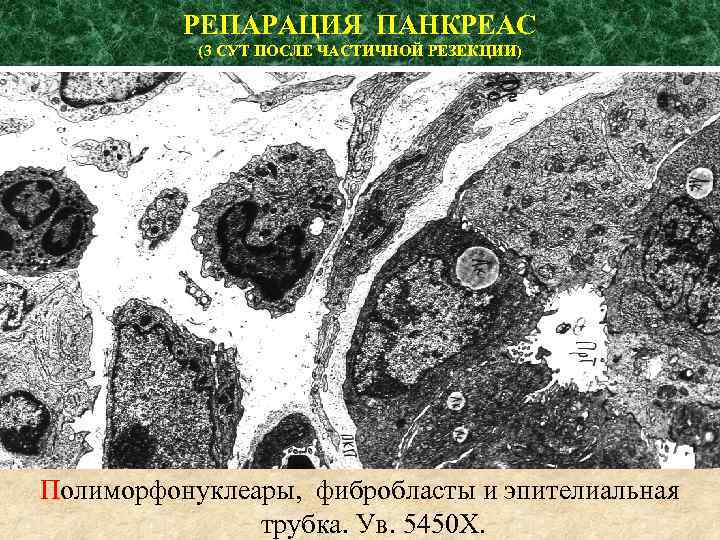 РЕПАРАЦИЯ ПАНКРЕАС (3 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) Полиморфонуклеары, фибробласты и эпителиальная трубка. Ув. 5450 Х.
РЕПАРАЦИЯ ПАНКРЕАС (3 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) Полиморфонуклеары, фибробласты и эпителиальная трубка. Ув. 5450 Х.
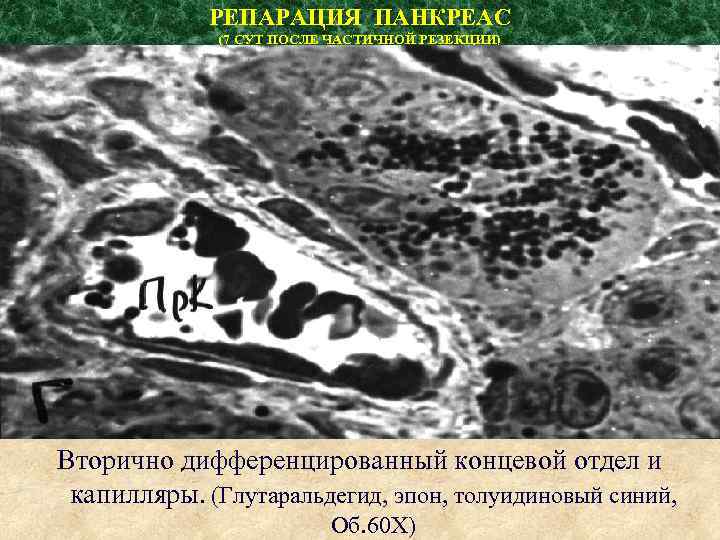 РЕПАРАЦИЯ ПАНКРЕАС (7 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) Вторично дифференцированный концевой отдел и капилляры. (Глутаральдегид, эпон, толуидиновый синий, Об. 60 Х)
РЕПАРАЦИЯ ПАНКРЕАС (7 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) Вторично дифференцированный концевой отдел и капилляры. (Глутаральдегид, эпон, толуидиновый синий, Об. 60 Х)
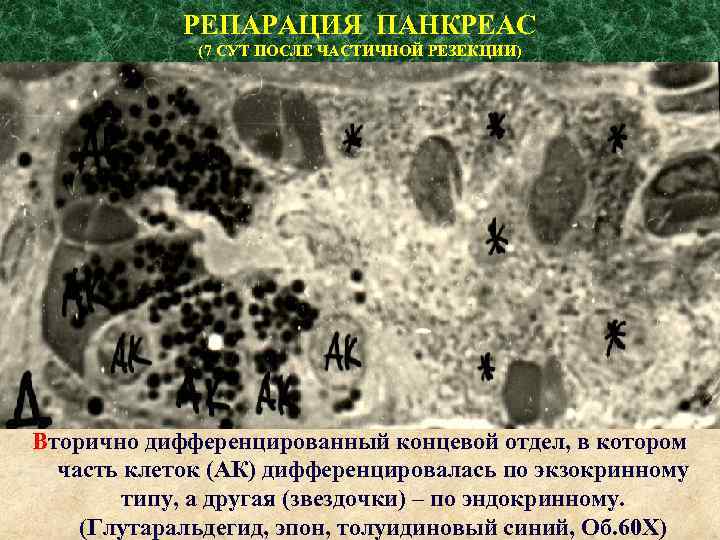 РЕПАРАЦИЯ ПАНКРЕАС (7 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) Вторично дифференцированный концевой отдел, в котором часть клеток (АК) дифференцировалась по экзокринному типу, а другая (звездочки) – по эндокринному. (Глутаральдегид, эпон, толуидиновый синий, Об. 60 Х)
РЕПАРАЦИЯ ПАНКРЕАС (7 СУТ ПОСЛЕ ЧАСТИЧНОЙ РЕЗЕКЦИИ) Вторично дифференцированный концевой отдел, в котором часть клеток (АК) дифференцировалась по экзокринному типу, а другая (звездочки) – по эндокринному. (Глутаральдегид, эпон, толуидиновый синий, Об. 60 Х)
 РЕПАРАЦИЯ ЭНДОКРИННОЙ ФУНКЦИИ ПАНКРЕАС (ФЕНОМЕН АЦИНО-ИНСУЛЯРНОЙ ТРАНСФОРМАЦИИ) «Смешанная» ацинарно-островковая клетка, содержащая в цитоплазме гранулы зимогена, А-, В- и Д-гранулы. Участок панкреас, удаленный от места частичной резекции.
РЕПАРАЦИЯ ЭНДОКРИННОЙ ФУНКЦИИ ПАНКРЕАС (ФЕНОМЕН АЦИНО-ИНСУЛЯРНОЙ ТРАНСФОРМАЦИИ) «Смешанная» ацинарно-островковая клетка, содержащая в цитоплазме гранулы зимогена, А-, В- и Д-гранулы. Участок панкреас, удаленный от места частичной резекции.
 «СМЕШАННАЯ» КЛЕТКА НА ПЕРИФЕРИИ ПАНКРЕАТИЧЕСКОГО ОСТРОВКА Смешанная экзо – эндокринная клетка содержит и гранулы зимогена, и эндокринные А - и В –гранулы. На вставке – А –, В – и «светлые» гранулы. Рядом с эндокринной А – гранулой - типичная для синтезирующей эндокринной клетки цистерна ГЦС с электронно плотным содержимым, на котором располагаются рибосомы.
«СМЕШАННАЯ» КЛЕТКА НА ПЕРИФЕРИИ ПАНКРЕАТИЧЕСКОГО ОСТРОВКА Смешанная экзо – эндокринная клетка содержит и гранулы зимогена, и эндокринные А - и В –гранулы. На вставке – А –, В – и «светлые» гранулы. Рядом с эндокринной А – гранулой - типичная для синтезирующей эндокринной клетки цистерна ГЦС с электронно плотным содержимым, на котором располагаются рибосомы.
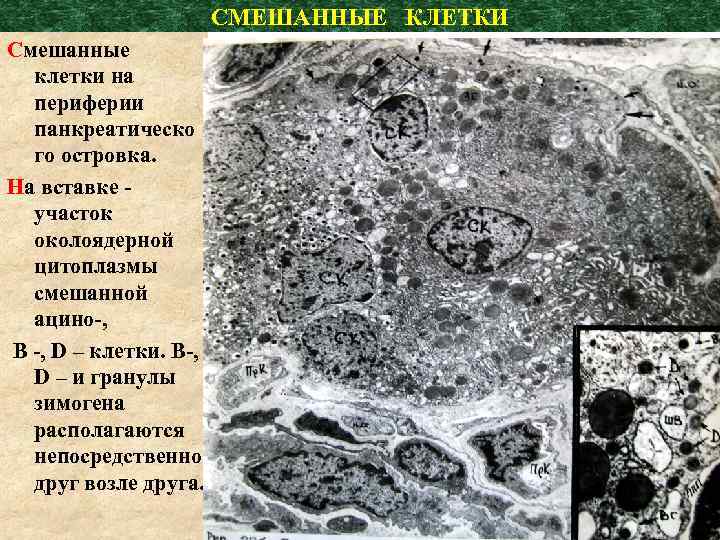 СМЕШАННЫЕ КЛЕТКИ Смешанные клетки на периферии панкреатическо го островка. На вставке - участок околоядерной цитоплазмы смешанной ацино-, В -, D – клетки. В-, D – и гранулы зимогена располагаются непосредственно друг возле друга.
СМЕШАННЫЕ КЛЕТКИ Смешанные клетки на периферии панкреатическо го островка. На вставке - участок околоядерной цитоплазмы смешанной ацино-, В -, D – клетки. В-, D – и гранулы зимогена располагаются непосредственно друг возле друга.
 ВИДЫ ВОСПАЛЕНИЯ
ВИДЫ ВОСПАЛЕНИЯ
 В ЗАВИСИМОСТИ ОТ РЕАКТИВНОСТИ Нормергическое (типично протекающее) Гипергическое (вялое) Гиперергическое (необычно бурное)
В ЗАВИСИМОСТИ ОТ РЕАКТИВНОСТИ Нормергическое (типично протекающее) Гипергическое (вялое) Гиперергическое (необычно бурное)
 ПО ПРЕОБЛАДАНИЮ КОМПОНЕНТА • Альтеративное (некротическое) • Экссудативное • Пролиферативное (продуктивное)
ПО ПРЕОБЛАДАНИЮ КОМПОНЕНТА • Альтеративное (некротическое) • Экссудативное • Пролиферативное (продуктивное)
 ПО ХАРАКТЕРУ ТЕЧЕНИЯ ♥ Острое ( процесс аутохтонный) ♥ Хроническое (процесс неаутохтонный)
ПО ХАРАКТЕРУ ТЕЧЕНИЯ ♥ Острое ( процесс аутохтонный) ♥ Хроническое (процесс неаутохтонный)
 Острое воспаление
Острое воспаление
 ОСТРОЕ ВОСПАЛЕНИЕ относительно короткое течение (минуты – до нескольких недель) ХАРАКТЕРНЫЕ ПРИЗНАКИ: * выраженная интенсивность и преобладание какого-либо из компонентов * экссудация жидкости и белков плазмы в интерстициальное пространство (ОТЕК)
ОСТРОЕ ВОСПАЛЕНИЕ относительно короткое течение (минуты – до нескольких недель) ХАРАКТЕРНЫЕ ПРИЗНАКИ: * выраженная интенсивность и преобладание какого-либо из компонентов * экссудация жидкости и белков плазмы в интерстициальное пространство (ОТЕК)
 * эмиграция лейкоцитов, преимущественно нейтрофилов * самопроизвольно заканчивается при условии удаления флогогена
* эмиграция лейкоцитов, преимущественно нейтрофилов * самопроизвольно заканчивается при условии удаления флогогена
 ИСХОДЫ: • Полное восстановление (restitution ad integrum) • Рубцевание • Образование абсцесса • Переход в хроническое
ИСХОДЫ: • Полное восстановление (restitution ad integrum) • Рубцевание • Образование абсцесса • Переход в хроническое
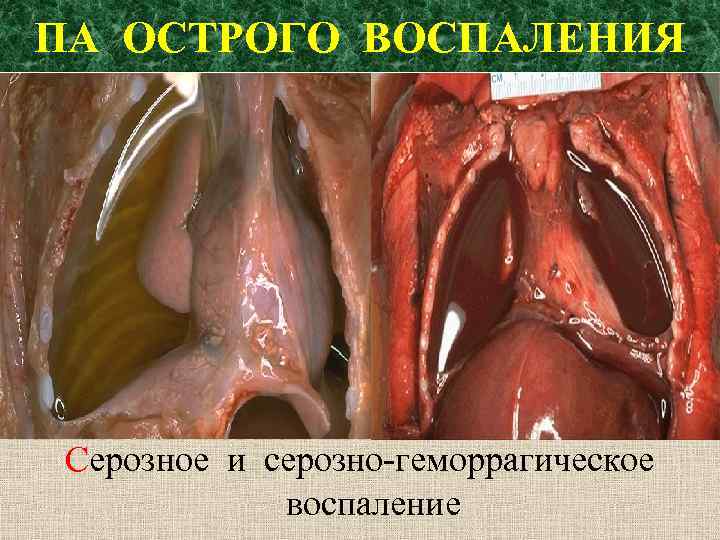 ПА ОСТРОГО ВОСПАЛЕНИЯ Серозное и серозно-геморрагическое воспаление
ПА ОСТРОГО ВОСПАЛЕНИЯ Серозное и серозно-геморрагическое воспаление
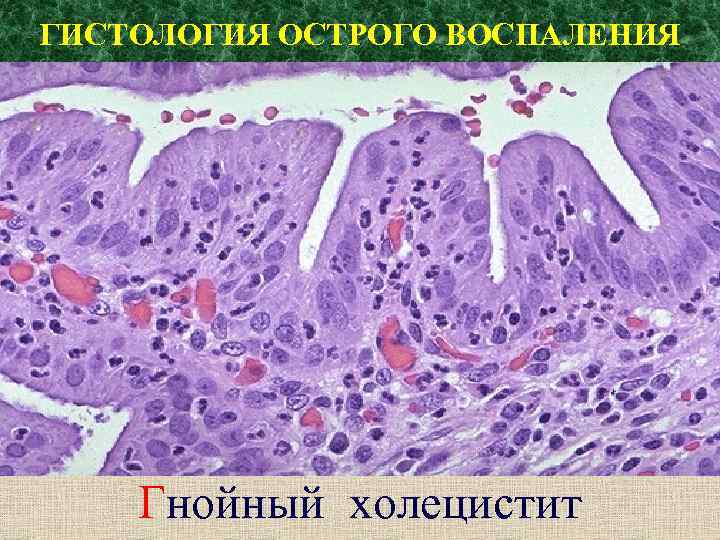 ГИСТОЛОГИЯ ОСТРОГО ВОСПАЛЕНИЯ Гнойный холецистит
ГИСТОЛОГИЯ ОСТРОГО ВОСПАЛЕНИЯ Гнойный холецистит
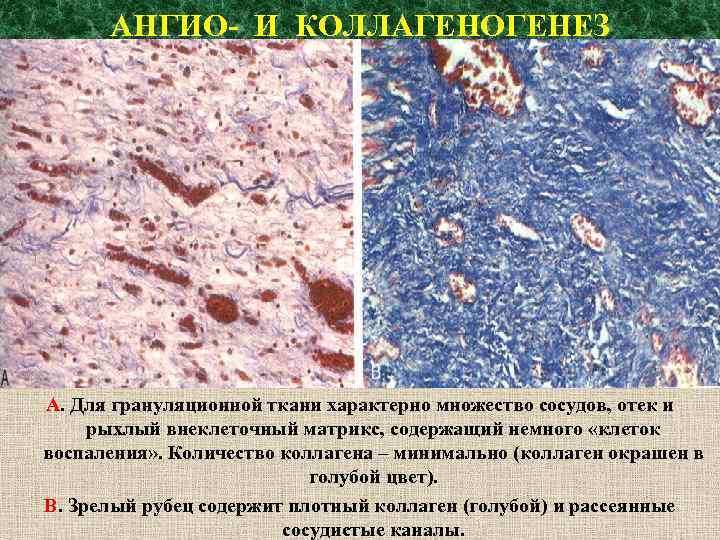 АНГИО- И КОЛЛАГЕНОГЕНЕЗ А. Для грануляционной ткани характерно множество сосудов, отек и рыхлый внеклеточный матрикс, содержащий немного «клеток воспаления» . Количество коллагена – минимально (коллаген окрашен в голубой цвет). В. Зрелый рубец содержит плотный коллаген (голубой) и рассеянные сосудистые каналы.
АНГИО- И КОЛЛАГЕНОГЕНЕЗ А. Для грануляционной ткани характерно множество сосудов, отек и рыхлый внеклеточный матрикс, содержащий немного «клеток воспаления» . Количество коллагена – минимально (коллаген окрашен в голубой цвет). В. Зрелый рубец содержит плотный коллаген (голубой) и рассеянные сосудистые каналы.
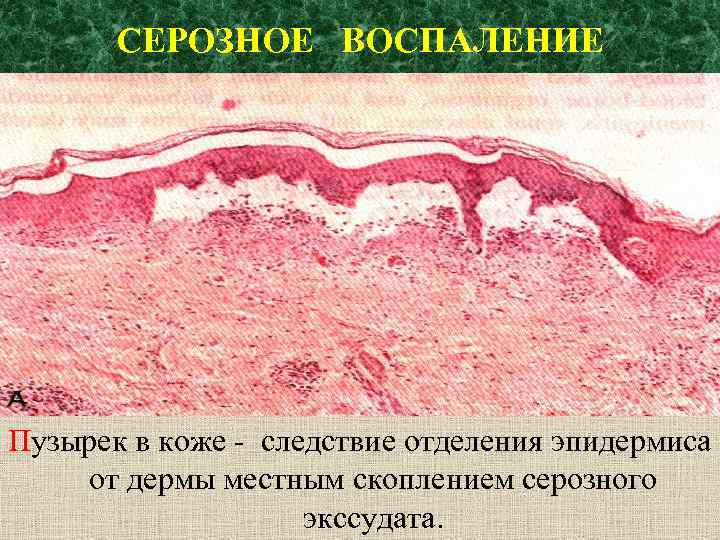 СЕРОЗНОЕ ВОСПАЛЕНИЕ Пузырек в коже - следствие отделения эпидермиса от дермы местным скоплением серозного экссудата.
СЕРОЗНОЕ ВОСПАЛЕНИЕ Пузырек в коже - следствие отделения эпидермиса от дермы местным скоплением серозного экссудата.
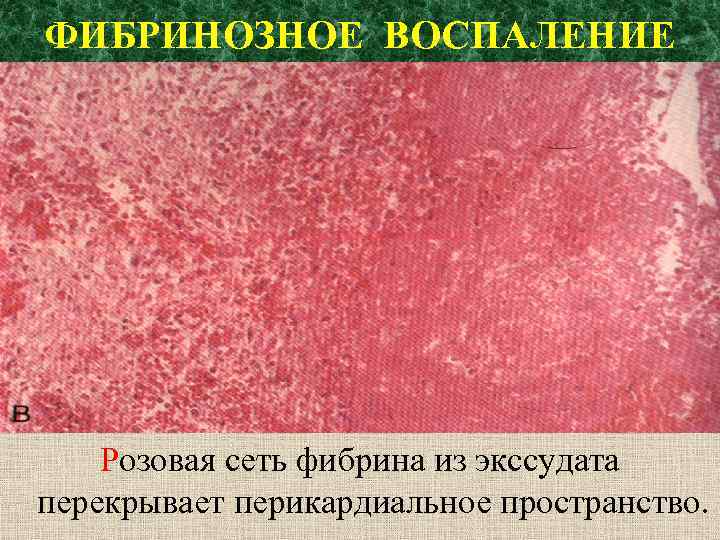 ФИБРИНОЗНОЕ ВОСПАЛЕНИЕ Розовая сеть фибрина из экссудата перекрывает перикардиальное пространство.
ФИБРИНОЗНОЕ ВОСПАЛЕНИЕ Розовая сеть фибрина из экссудата перекрывает перикардиальное пространство.
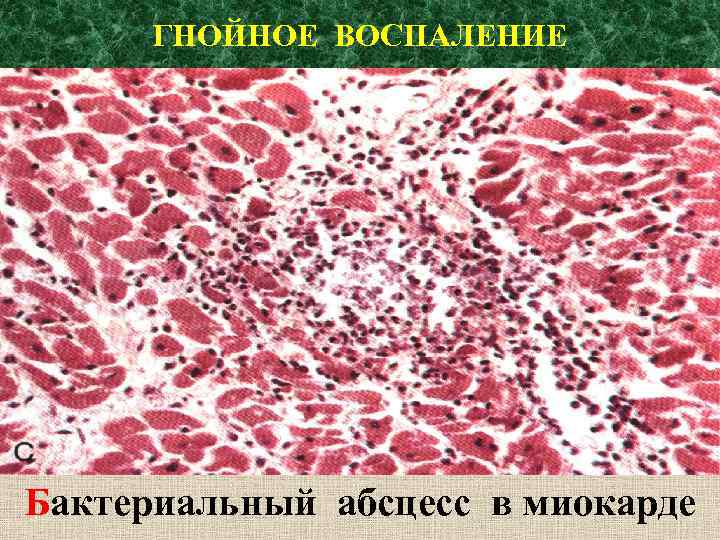 ГНОЙНОЕ ВОСПАЛЕНИЕ Бактериальный абсцесс в миокарде
ГНОЙНОЕ ВОСПАЛЕНИЕ Бактериальный абсцесс в миокарде
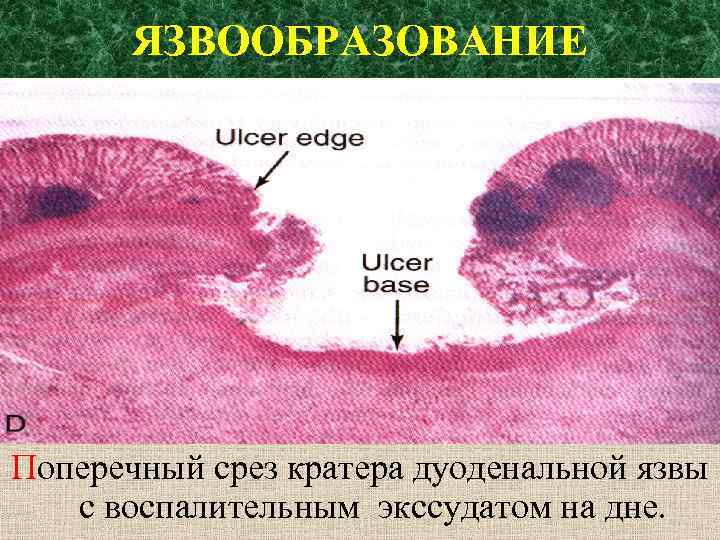 ЯЗВООБРАЗОВАНИЕ Поперечный срез кратера дуоденальной язвы с воспалительным экссудатом на дне.
ЯЗВООБРАЗОВАНИЕ Поперечный срез кратера дуоденальной язвы с воспалительным экссудатом на дне.
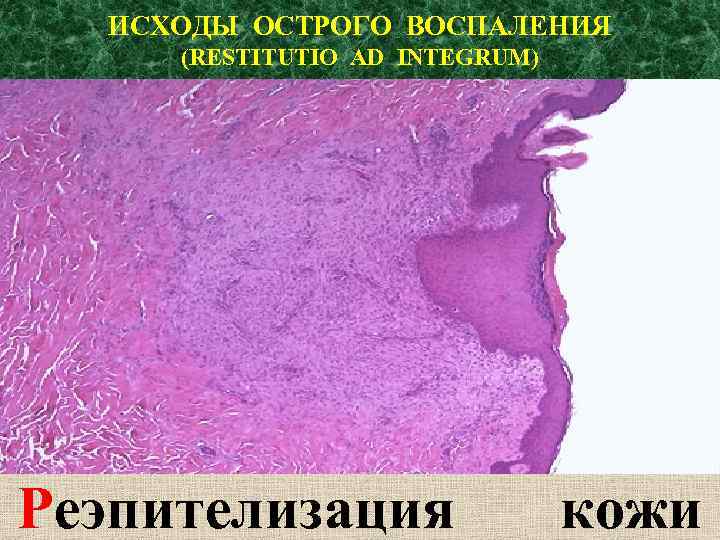 ИСХОДЫ ОСТРОГО ВОСПАЛЕНИЯ (RESTITUTIO AD INTEGRUM) Реэпителизация кожи
ИСХОДЫ ОСТРОГО ВОСПАЛЕНИЯ (RESTITUTIO AD INTEGRUM) Реэпителизация кожи
 ИСХОДЫ ОСТРОГО ВОСПАЛЕНИЯ (СКЛЕРОЗИРОВАНИЕ) Печень, цирротический узел, расширенные пространства Диссе, коллагеновые фибриллы в пространстве Диссе
ИСХОДЫ ОСТРОГО ВОСПАЛЕНИЯ (СКЛЕРОЗИРОВАНИЕ) Печень, цирротический узел, расширенные пространства Диссе, коллагеновые фибриллы в пространстве Диссе
 Хроническое воспаление
Хроническое воспаление
 ХРОНИЧЕСКОЕ ВОСПАЛЕНИЕ Сочетание волнообразных острых альтеративноэкссудативных явлений, КОИП (ГЗТ) и Фиброплазии
ХРОНИЧЕСКОЕ ВОСПАЛЕНИЕ Сочетание волнообразных острых альтеративноэкссудативных явлений, КОИП (ГЗТ) и Фиброплазии
 ПАТОГЕНЕЗ ФИБРОПЛАЗИИ Персистирующий стимул хронического воспаления активация макрофагов и лимфоцитов продукция факторов роста (PDGF, FGF, TGF beta) и цитокинов (TNF, IL 1, 4, 13), усиление синтеза коллагена. Образование коллагена возрастает при сниженной активности металлопротеиназ, что ослабляет распад коллагена.
ПАТОГЕНЕЗ ФИБРОПЛАЗИИ Персистирующий стимул хронического воспаления активация макрофагов и лимфоцитов продукция факторов роста (PDGF, FGF, TGF beta) и цитокинов (TNF, IL 1, 4, 13), усиление синтеза коллагена. Образование коллагена возрастает при сниженной активности металлопротеиназ, что ослабляет распад коллагена.
 ХРОНИЧЕСКОЕ ВОСПАЛЕНИЕ (характерные признаки) Вялотекущий процесс с преобладанием дистрофических и пролиферативных процессов
ХРОНИЧЕСКОЕ ВОСПАЛЕНИЕ (характерные признаки) Вялотекущий процесс с преобладанием дистрофических и пролиферативных процессов
 иммуноповреждение Мононуклеарная инфильтрация лимфоцитами и макрофагами
иммуноповреждение Мононуклеарная инфильтрация лимфоцитами и макрофагами
 ХРОНИЧЕСКОЕ ВОСПАЛЕНИЕ (варианты формирования) & возбудитель персистирует в тканях (tbc) & флогоген не метаболизируется (асбестоз)
ХРОНИЧЕСКОЕ ВОСПАЛЕНИЕ (варианты формирования) & возбудитель персистирует в тканях (tbc) & флогоген не метаболизируется (асбестоз)
 и & ммунная атака против конституционального антигена, который не может быть устранен (нативная двухцепочечная ДНК при СКВ) продолжение альтерации и экссудации на фоне незавершенной репарации
и & ммунная атака против конституционального антигена, который не может быть устранен (нативная двухцепочечная ДНК при СКВ) продолжение альтерации и экссудации на фоне незавершенной репарации
 ХРОНИЧЕСКОЕ ВОСПАЛЕНИЕ (разновидности) первично хроническое персистирующее воспаление. вторично хроническое, формируемое после начального острого периода.
ХРОНИЧЕСКОЕ ВОСПАЛЕНИЕ (разновидности) первично хроническое персистирующее воспаление. вторично хроническое, формируемое после начального острого периода.
 При хроническом воспалении всегда формируется иммунодефицитное состояние.
При хроническом воспалении всегда формируется иммунодефицитное состояние.
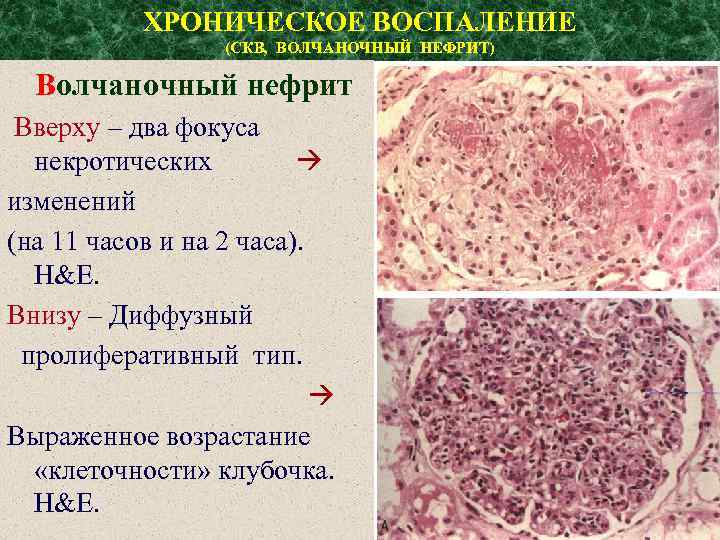 ХРОНИЧЕСКОЕ ВОСПАЛЕНИЕ (СКВ, ВОЛЧАНОЧНЫЙ НЕФРИТ) Волчаночный нефрит Вверху – два фокуса некротических изменений (на 11 часов и на 2 часа). H&E. Внизу – Диффузный пролиферативный тип. Выраженное возрастание «клеточности» клубочка. H&E.
ХРОНИЧЕСКОЕ ВОСПАЛЕНИЕ (СКВ, ВОЛЧАНОЧНЫЙ НЕФРИТ) Волчаночный нефрит Вверху – два фокуса некротических изменений (на 11 часов и на 2 часа). H&E. Внизу – Диффузный пролиферативный тип. Выраженное возрастание «клеточности» клубочка. H&E.
 ПЕРВИЧНО ХРОНИЧЕСКОЕ ПЕРСИСТИРУЮЩЕЕ ВОСПАЛЕНИЕ вялое течение при недостаточной интенсивности иммунного ответа и регенерации
ПЕРВИЧНО ХРОНИЧЕСКОЕ ПЕРСИСТИРУЮЩЕЕ ВОСПАЛЕНИЕ вялое течение при недостаточной интенсивности иммунного ответа и регенерации
 Этому способствуют: региональные нарушения лимфо- и гемоциркуляции (e. g. , диабетическая ангиопатия, варикозная б-нь, региональная ишемия вследствие склеротических изменений в сосудах), полигиповитаминозы, дефицит микроэлементов (особенно цинка)
Этому способствуют: региональные нарушения лимфо- и гемоциркуляции (e. g. , диабетическая ангиопатия, варикозная б-нь, региональная ишемия вследствие склеротических изменений в сосудах), полигиповитаминозы, дефицит микроэлементов (особенно цинка)
 ИСХОДЫ ХРОНИЧЕСКОГО ВОСПАЛЕНИЯ неполная регенерация + фиброплазия + некрозы. Нарушение архитектуры органа (абсцесс, рубец, цирроз).
ИСХОДЫ ХРОНИЧЕСКОГО ВОСПАЛЕНИЯ неполная регенерация + фиброплазия + некрозы. Нарушение архитектуры органа (абсцесс, рубец, цирроз).
 формирование гранулем под влиянием TNF alpha
формирование гранулем под влиянием TNF alpha
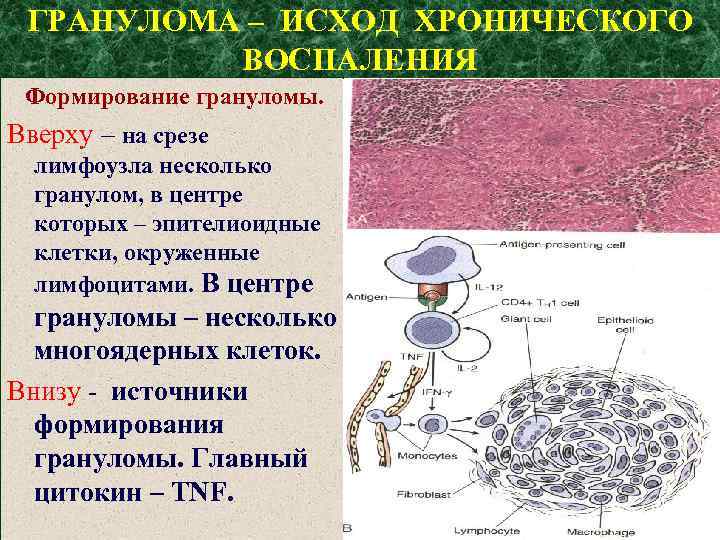 ГРАНУЛОМА – ИСХОД ХРОНИЧЕСКОГО ВОСПАЛЕНИЯ Формирование грануломы. Вверху – на срезе лимфоузла несколько гранулом, в центре которых – эпителиоидные клетки, окруженные лимфоцитами. В центре грануломы – несколько многоядерных клеток. Внизу - источники формирования грануломы. Главный цитокин – ТNF.
ГРАНУЛОМА – ИСХОД ХРОНИЧЕСКОГО ВОСПАЛЕНИЯ Формирование грануломы. Вверху – на срезе лимфоузла несколько гранулом, в центре которых – эпителиоидные клетки, окруженные лимфоцитами. В центре грануломы – несколько многоядерных клеток. Внизу - источники формирования грануломы. Главный цитокин – ТNF.
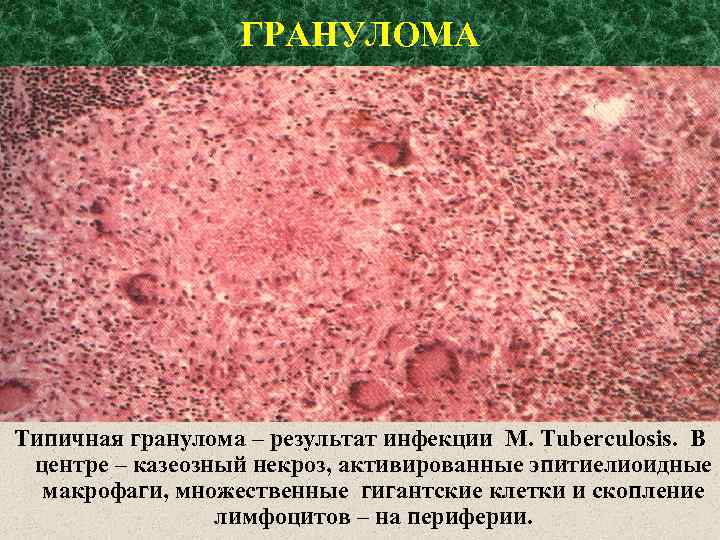 ГРАНУЛОМА Типичная гранулома – результат инфекции M. Tuberculosis. В центре – казеозный некроз, активированные эпитиелиоидные макрофаги, множественные гигантские клетки и скопление лимфоцитов – на периферии.
ГРАНУЛОМА Типичная гранулома – результат инфекции M. Tuberculosis. В центре – казеозный некроз, активированные эпитиелиоидные макрофаги, множественные гигантские клетки и скопление лимфоцитов – на периферии.
 СИСТЕМНЫЕ ЭФФЕКТЫ ВОСПАЛЕНИЯ (МЕСТНОЕ И ОБЩЕЕ)
СИСТЕМНЫЕ ЭФФЕКТЫ ВОСПАЛЕНИЯ (МЕСТНОЕ И ОБЩЕЕ)
 СИСТЕМНЫЕ ЭФФЕКТЫ ВОСПАЛЕНИЯ (ОБЩИЕ ЗАМЕЧАНИЯ) Системное действие медиаторов воспаления может наступить, если суммарная поверхность очагов ВОСПАЛЕНИЯ очень велика и барьеры не сдерживают распространения аутокоидов (обширные ожоги, общее радиационное облучение, множественные травмы. . ).
СИСТЕМНЫЕ ЭФФЕКТЫ ВОСПАЛЕНИЯ (ОБЩИЕ ЗАМЕЧАНИЯ) Системное действие медиаторов воспаления может наступить, если суммарная поверхность очагов ВОСПАЛЕНИЯ очень велика и барьеры не сдерживают распространения аутокоидов (обширные ожоги, общее радиационное облучение, множественные травмы. . ).
 Системное действие медиаторов воспаления приводит к развитию плюриорганной недостаточности, ШОКУ.
Системное действие медиаторов воспаления приводит к развитию плюриорганной недостаточности, ШОКУ.
 ЛИХОРАДКА –ВОЗМОЖНЫЙ ЭЛЕМЕНТ ОТВЕТА НА ПОВРЕЖДЕНИЕ Лихорадка – общий ТПП, ОТВЕТ ЦЕНТРОВ ТЕРМОРЕГУЛЯЦИИ НА ЭНДОПИРОГЕНЫ (IL-1, TNF), СЕКРЕТИРУЕМЫЕ ЛЕЙКОЦИТАМИ В ХОДЕ РАЗВИТИЯ ВОСПАЛИТЕЛЬНОЙ РЕАКЦИИ.
ЛИХОРАДКА –ВОЗМОЖНЫЙ ЭЛЕМЕНТ ОТВЕТА НА ПОВРЕЖДЕНИЕ Лихорадка – общий ТПП, ОТВЕТ ЦЕНТРОВ ТЕРМОРЕГУЛЯЦИИ НА ЭНДОПИРОГЕНЫ (IL-1, TNF), СЕКРЕТИРУЕМЫЕ ЛЕЙКОЦИТАМИ В ХОДЕ РАЗВИТИЯ ВОСПАЛИТЕЛЬНОЙ РЕАКЦИИ.
 При лихорадке усиливается фагоцитоз, снижается устойчивость микроорганизмов к лекарственной терапии.
При лихорадке усиливается фагоцитоз, снижается устойчивость микроорганизмов к лекарственной терапии.
 «Реакции острой фазы» ( «ответ острой фазы» , «преиммунный ответ» ) - это комплекс изменений, управляемых цитокинами. Цитокины несут информацию о повреждении и обусловливают перестройку нейро-эндокринной регуляции и метаболизма.
«Реакции острой фазы» ( «ответ острой фазы» , «преиммунный ответ» ) - это комплекс изменений, управляемых цитокинами. Цитокины несут информацию о повреждении и обусловливают перестройку нейро-эндокринной регуляции и метаболизма.
 Проявления «реакций острой фазы» : сонливость; снижение аппетита; усиленный распад белков; гипотензия и др. гемодинамические изменения; синтез печенью белков острой фазы.
Проявления «реакций острой фазы» : сонливость; снижение аппетита; усиленный распад белков; гипотензия и др. гемодинамические изменения; синтез печенью белков острой фазы.
 Цитокины (IL-1, TNF, INF) моноциты, фибробласты, эндотелиоциты IL-6 гепатоциты «белки острой фазы» ( «глобулины острой фазы» )
Цитокины (IL-1, TNF, INF) моноциты, фибробласты, эндотелиоциты IL-6 гепатоциты «белки острой фазы» ( «глобулины острой фазы» )
 «ГЛОБУЛИНЫ ОСТРОЙ ФАЗЫ» С-РЕАКТИВНЫЙ БЕЛОК, АМИЛОИДЫ А И В, ГАПТОГЛОБИН, ЦЕРУЛЛОПЛАЗМИН, АНТИГЕМОФИЛЬНЫЙ ГЛОБУЛИН (F. VIII: C), F. VII, F. IX,
«ГЛОБУЛИНЫ ОСТРОЙ ФАЗЫ» С-РЕАКТИВНЫЙ БЕЛОК, АМИЛОИДЫ А И В, ГАПТОГЛОБИН, ЦЕРУЛЛОПЛАЗМИН, АНТИГЕМОФИЛЬНЫЙ ГЛОБУЛИН (F. VIII: C), F. VII, F. IX,
 АНТИКОАГУЛЯЦИОННЫЕ БЕЛКИ С И S, АНТИТРОМБИН III, ПЛАЗМИНОГЕН, АЛЬФА – 2 - МАКРОГЛОБУЛИН, КИСЛЫЙ АЛЬФА-1 -ГЛИКОПРОТЕИН, АЛЬФА 2 – МАКРОФЕТОПРОТЕИН, ТРАНСКОБАЛАМИН 2, ФЕРРИТИН, ОРОЗОМУКОИД
АНТИКОАГУЛЯЦИОННЫЕ БЕЛКИ С И S, АНТИТРОМБИН III, ПЛАЗМИНОГЕН, АЛЬФА – 2 - МАКРОГЛОБУЛИН, КИСЛЫЙ АЛЬФА-1 -ГЛИКОПРОТЕИН, АЛЬФА 2 – МАКРОФЕТОПРОТЕИН, ТРАНСКОБАЛАМИН 2, ФЕРРИТИН, ОРОЗОМУКОИД
 «Глобулины острой фазы» Диспротеинемия падение содержания трансферрина; макрофаги улавливают Fe и Zn гипоферремия, гипоцинкемия
«Глобулины острой фазы» Диспротеинемия падение содержания трансферрина; макрофаги улавливают Fe и Zn гипоферремия, гипоцинкемия
 ограничивается поступление железа и цинка в ткани = снижается доступность их для микроорганизмов (Fe, Zn – ростовые факторы микроорганизмов!!!)
ограничивается поступление железа и цинка в ткани = снижается доступность их для микроорганизмов (Fe, Zn – ростовые факторы микроорганизмов!!!)
 ДРУГИЕ ОБЩИЕ ЭФФЕКТЫ Лейкоцитоз со "сдвигом влево" обусловлен а) освобождением клеток из постмитотического резервного пула костного мозга (действие IL-1 и TNF) б) возросшей продукцией колониестимулирующих факторов (GM-CSF, G-CSF, M-CSF) опосредованной действием IL-1 и TNF.
ДРУГИЕ ОБЩИЕ ЭФФЕКТЫ Лейкоцитоз со "сдвигом влево" обусловлен а) освобождением клеток из постмитотического резервного пула костного мозга (действие IL-1 и TNF) б) возросшей продукцией колониестимулирующих факторов (GM-CSF, G-CSF, M-CSF) опосредованной действием IL-1 и TNF.
 Большинство бактериальных инфекций дают нейтрофилию, но инфекционный мононуклеоз или свинка дают лимфоцитоз, бронхиальная астма, сенная лихорадка, паразитарные инфекции - эозинофилию.
Большинство бактериальных инфекций дают нейтрофилию, но инфекционный мононуклеоз или свинка дают лимфоцитоз, бронхиальная астма, сенная лихорадка, паразитарные инфекции - эозинофилию.
 Лейкопения Тиф, инфекции, вызываемые вирусами, риккетсиями и определенные протозойные инфекции ассоциируются с лейкопенией.
Лейкопения Тиф, инфекции, вызываемые вирусами, риккетсиями и определенные протозойные инфекции ассоциируются с лейкопенией.
 Ускорение СОЭ есть следствие - снижения отрицательного заряда эритроцитов, - увеличения вязкости крови, - изменения белкового спектра, - повышения температуры.
Ускорение СОЭ есть следствие - снижения отрицательного заряда эритроцитов, - увеличения вязкости крови, - изменения белкового спектра, - повышения температуры.
 Изменение содержания гормонов: медиаторы воспаления (цитокины: монокины, лимфокины, лейкокинины) способны активировать функцию гипоталамуса, гипофиза, коры надпочечников возрастает концентрация КАТЕХОЛАМИНОВ и ГЛЮКОКОРТИКОИДОВ.
Изменение содержания гормонов: медиаторы воспаления (цитокины: монокины, лимфокины, лейкокинины) способны активировать функцию гипоталамуса, гипофиза, коры надпочечников возрастает концентрация КАТЕХОЛАМИНОВ и ГЛЮКОКОРТИКОИДОВ.
 Более того, флогогенный стимул обусловливает подъем уровня кортикостероидов даже у гипофизэктомированных животных.
Более того, флогогенный стимул обусловливает подъем уровня кортикостероидов даже у гипофизэктомированных животных.
 ГОРМОНЫ И ВОСПАЛЕНИЕ
ГОРМОНЫ И ВОСПАЛЕНИЕ
 ГЛЮКОКОРТИКОИДЫ УГНЕТАЮТ КОМПОНЕНТЫ ВОСПАЛЕНИЯ (эффекты) Aльтеративного: стимулируют синтез липокортинов угнетают синтез фосфолипазы А 2 “de facto” стабилизируют мембрану
ГЛЮКОКОРТИКОИДЫ УГНЕТАЮТ КОМПОНЕНТЫ ВОСПАЛЕНИЯ (эффекты) Aльтеративного: стимулируют синтез липокортинов угнетают синтез фосфолипазы А 2 “de facto” стабилизируют мембрану
 Экссудативного: угнетают: образование кининов, активацию медиаторных систем (комплемента, коагуляции, антикоагуляции), проницаемость капилляров блокируют адгезию, миграцию лейкоцитов и фагоцитоз.
Экссудативного: угнетают: образование кининов, активацию медиаторных систем (комплемента, коагуляции, антикоагуляции), проницаемость капилляров блокируют адгезию, миграцию лейкоцитов и фагоцитоз.
 Пролиферативного: подавляют пролиферацию лимфоцитов и тормозят высвобождение ими лимфокинов c последующим торможением миграции макрофагов и
Пролиферативного: подавляют пролиферацию лимфоцитов и тормозят высвобождение ими лимфокинов c последующим торможением миграции макрофагов и
 выделения ими монокинов, стимулирующих рост и деление эндотелиоцитов, фибробластов, синтез коллагена, неоваскуляризацию и рубцевание.
выделения ими монокинов, стимулирующих рост и деление эндотелиоцитов, фибробластов, синтез коллагена, неоваскуляризацию и рубцевание.
 ингибируют синтез глюкуроновой кислоты с последующим снижением синтеза коллагена.
ингибируют синтез глюкуроновой кислоты с последующим снижением синтеза коллагена.
 Механизмы, лежащие в основе эффектов глюкокортикоидов Угнетение: ♠ продукции белков МНС ♠ освобождения IL-2, 3, 5; GM-CSF и ♠ образования IL 4 ♠ лейкоцитарного прайминга Эоз и Нейтрофилов ♠ активности гистидиндекарбоксилазы и 5 - окситриптаминдекарбоксилазы
Механизмы, лежащие в основе эффектов глюкокортикоидов Угнетение: ♠ продукции белков МНС ♠ освобождения IL-2, 3, 5; GM-CSF и ♠ образования IL 4 ♠ лейкоцитарного прайминга Эоз и Нейтрофилов ♠ активности гистидиндекарбоксилазы и 5 - окситриптаминдекарбоксилазы
 Подавление продукции IL-1 и TNF Регуляция активности AP-1 Пермиссивные эффекты (для КА)
Подавление продукции IL-1 и TNF Регуляция активности AP-1 Пермиссивные эффекты (для КА)
 Минералокортикоиды и воспаление Оказывают провоспалительное действие через: усиление проницаемости сосудистой стенки активацию энергетического обмена в клетках - участниках воспаления
Минералокортикоиды и воспаление Оказывают провоспалительное действие через: усиление проницаемости сосудистой стенки активацию энергетического обмена в клетках - участниках воспаления
 ускорение размножения клеток новообразование капилляров синтез основного вещества соединительной ткани мононуклеары имеют рецепторы к минералокортикоидам
ускорение размножения клеток новообразование капилляров синтез основного вещества соединительной ткани мононуклеары имеют рецепторы к минералокортикоидам
 Катехоламины и воспаление КА мозгового вещества надпочечников и адреномиметики через бета-адренорецепторы тормозят секрецию протеаз макрофагами.
Катехоламины и воспаление КА мозгового вещества надпочечников и адреномиметики через бета-адренорецепторы тормозят секрецию протеаз макрофагами.
 Тироидные гормоны и воспаление Усиливают: производство интерферона синтез гормонов тимуса иммунный ответ (синтез антител)
Тироидные гормоны и воспаление Усиливают: производство интерферона синтез гормонов тимуса иммунный ответ (синтез антител)
 Стимулируют: включение 3 Н-тимидина, митотическую активность, Фагоцитоз Тироциты продуцируют IL 1 - подобные и тимоцитстимулирующие факторы
Стимулируют: включение 3 Н-тимидина, митотическую активность, Фагоцитоз Тироциты продуцируют IL 1 - подобные и тимоцитстимулирующие факторы
 При хронических инфекциях в крови снижается содержание активного Т 3 (дейодирование идет через дейодиназу внутреннего кольца с образованием большей доли менее активного реверсивного Т 3, что de facto снижает периферические эффекты тироидных гормонов)
При хронических инфекциях в крови снижается содержание активного Т 3 (дейодирование идет через дейодиназу внутреннего кольца с образованием большей доли менее активного реверсивного Т 3, что de facto снижает периферические эффекты тироидных гормонов)
 Применение Тз снижает летальность при сепсисе, сокращает сроки лечения вирусного гепатита и менингококковой инфекции.
Применение Тз снижает летальность при сепсисе, сокращает сроки лечения вирусного гепатита и менингококковой инфекции.
 Инсулин и воспаление Снижение уровней инсулина при сахарном диабете резко снижает показатели неспецифической резистентности: фагоцитарную активность, активность пероксидазы, опсонический индекс, активность аденилат-циклазной системы.
Инсулин и воспаление Снижение уровней инсулина при сахарном диабете резко снижает показатели неспецифической резистентности: фагоцитарную активность, активность пероксидазы, опсонический индекс, активность аденилат-циклазной системы.
 Гормоны тимуса оказывают влияние на воспаление через регуляцию функций иммунной системы: * тимозин и его фракции усиливают киллерную активность лимфоцитов * тимозин повышает выработку IL 2 и рецепторов к нему.
Гормоны тимуса оказывают влияние на воспаление через регуляцию функций иммунной системы: * тимозин и его фракции усиливают киллерную активность лимфоцитов * тимозин повышает выработку IL 2 и рецепторов к нему.


