на предзащиту.pptx
- Количество слайдов: 21
 Воронежский государственный университет Химический факультет Кафедра аналитической химии Галлямова Валерия Данияровна СОРБЦИЯ ФОСФАТИДИЛХОЛИНА КАТИОНООБМЕННИКАМИ Научные руководители: д. х. н. , проф. Селеменев В. Ф. асс. Назарова А. А. Воронеж 2015
Воронежский государственный университет Химический факультет Кафедра аналитической химии Галлямова Валерия Данияровна СОРБЦИЯ ФОСФАТИДИЛХОЛИНА КАТИОНООБМЕННИКАМИ Научные руководители: д. х. н. , проф. Селеменев В. Ф. асс. Назарова А. А. Воронеж 2015
 Цель и задачи исследования Цель: изучение процессов сорбции фосфатидилхолина на сильно- и слабокислотных катионообменных сорбентах «КУ-2 -8» и «КБ-4» в зависимости от p. H среды. Задачи: 1. Разработать методику количественного определения фосфатидилхолина методом тонкослойной хроматографии (ТСХ). 2. Получить градуировочные графики ФХ при p. H 7 и p. H 2 методом ТСХ в области концентраций 0, 01 -0, 50 мг/мл. 3. Получить изотермы сорбции ФХ на ионообменных сорбентах «КУ-2 -8» и «КБ-4» при варьировании p. H среды, провести математическую обработку полученных данных. 4. Выяснить механизм образования межмолекулярных связей между сорбентом и ФХ методом ИК-спектроскопии. 2
Цель и задачи исследования Цель: изучение процессов сорбции фосфатидилхолина на сильно- и слабокислотных катионообменных сорбентах «КУ-2 -8» и «КБ-4» в зависимости от p. H среды. Задачи: 1. Разработать методику количественного определения фосфатидилхолина методом тонкослойной хроматографии (ТСХ). 2. Получить градуировочные графики ФХ при p. H 7 и p. H 2 методом ТСХ в области концентраций 0, 01 -0, 50 мг/мл. 3. Получить изотермы сорбции ФХ на ионообменных сорбентах «КУ-2 -8» и «КБ-4» при варьировании p. H среды, провести математическую обработку полученных данных. 4. Выяснить механизм образования межмолекулярных связей между сорбентом и ФХ методом ИК-спектроскопии. 2
 Объекты исследования Рис. 1. Фосфатидилхолин (ФХ) 3
Объекты исследования Рис. 1. Фосфатидилхолин (ФХ) 3
 Объекты исследования Сорбенты: КУ-2 -8 КБ-4 4
Объекты исследования Сорбенты: КУ-2 -8 КБ-4 4
 Физико-химические характеристики полимерных сорбентов Сорбент Тип сорбента КУ-2 -8 КБ-4 Катионообменный Размер зерна, мм 0, 315 -1, 25 0, 315 -1, 6 Объемная доля рабочей фракции, %, не менее: 95 90 Эффективный размер зерен, мм, не более: 0, 35 -0, 55 0, 5 Удельный объем в Н-форме, см /г, не более: 2, 8 2, 5 Полная обменная емкость (по H+), моль·экв/г 5, 8 4, 9 Полная обменная емкость (в пересчете на ФХ), мг/г 4, 4 3, 7 5
Физико-химические характеристики полимерных сорбентов Сорбент Тип сорбента КУ-2 -8 КБ-4 Катионообменный Размер зерна, мм 0, 315 -1, 25 0, 315 -1, 6 Объемная доля рабочей фракции, %, не менее: 95 90 Эффективный размер зерен, мм, не более: 0, 35 -0, 55 0, 5 Удельный объем в Н-форме, см /г, не более: 2, 8 2, 5 Полная обменная емкость (по H+), моль·экв/г 5, 8 4, 9 Полная обменная емкость (в пересчете на ФХ), мг/г 4, 4 3, 7 5
 Диаграмма распределения ионных форм ФХ 1 0. 5 1 0 0. 00 2 5. 00 3 10. 00 р. Н Рис. 2. Характеристика ионных форм ФХ в водных растворах при изменении величины р. Н: 1 – однозарядный катион, 2 – цвиттер-ион, 3 – однозарядный анион 6
Диаграмма распределения ионных форм ФХ 1 0. 5 1 0 0. 00 2 5. 00 3 10. 00 р. Н Рис. 2. Характеристика ионных форм ФХ в водных растворах при изменении величины р. Н: 1 – однозарядный катион, 2 – цвиттер-ион, 3 – однозарядный анион 6
 Определение ФХ методом ТСХ • Элюирующая система: хлороформ – метанол – уксусная кислота – вода (20: 12: 3, 2: 1, 6) • Пластина: Сорбфил ПТСХ-ПЭТФ • Объем наносимой пробы: 10 мкл • Интервал концентраций (0, 01 – 0, 50) мг/мл. • Проявитель: 5%-ный раствор фосфорномолибденовой кислоты • Программа количественной Videodensitometer обработки данных: Sorbfil 7
Определение ФХ методом ТСХ • Элюирующая система: хлороформ – метанол – уксусная кислота – вода (20: 12: 3, 2: 1, 6) • Пластина: Сорбфил ПТСХ-ПЭТФ • Объем наносимой пробы: 10 мкл • Интервал концентраций (0, 01 – 0, 50) мг/мл. • Проявитель: 5%-ный раствор фосфорномолибденовой кислоты • Программа количественной Videodensitometer обработки данных: Sorbfil 7
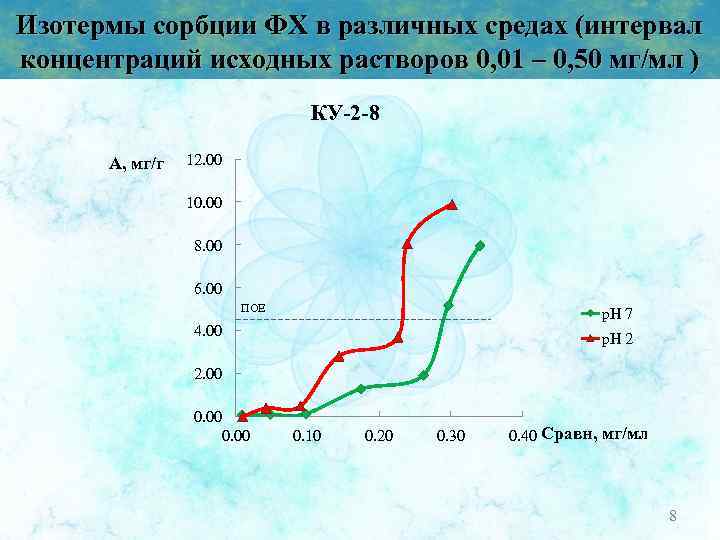 Изотермы сорбции ФХ в различных средах (интервал концентраций исходных растворов 0, 01 – 0, 50 мг/мл ) КУ-2 -8 A, мг/г 12. 00 10. 00 8. 00 6. 00 ПОЕ p. H 7 4. 00 p. H 2 2. 00 0. 10 0. 20 0. 30 0. 40 Cравн, мг/мл 8
Изотермы сорбции ФХ в различных средах (интервал концентраций исходных растворов 0, 01 – 0, 50 мг/мл ) КУ-2 -8 A, мг/г 12. 00 10. 00 8. 00 6. 00 ПОЕ p. H 7 4. 00 p. H 2 2. 00 0. 10 0. 20 0. 30 0. 40 Cравн, мг/мл 8
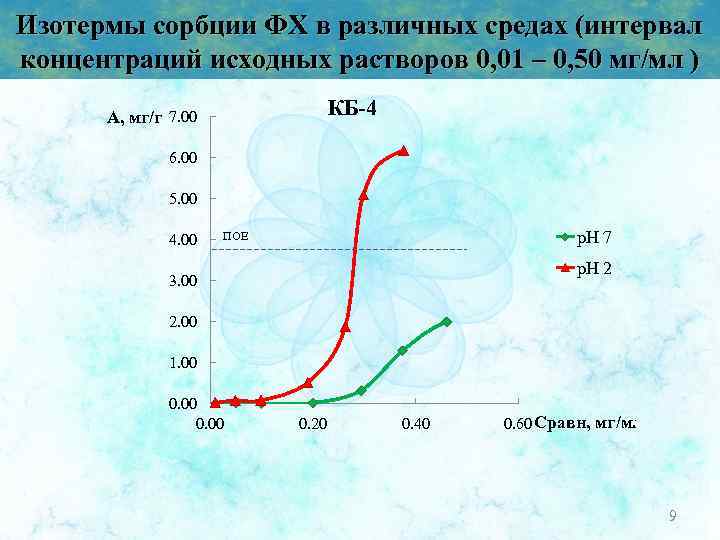 Изотермы сорбции ФХ в различных средах (интервал концентраций исходных растворов 0, 01 – 0, 50 мг/мл ) КБ-4 A, мг/г 7. 00 6. 00 5. 00 4. 00 p. H 7 ПОЕ p. H 2 3. 00 2. 00 1. 00 0. 20 0. 40 0. 60 Cравн, мг/мл 9
Изотермы сорбции ФХ в различных средах (интервал концентраций исходных растворов 0, 01 – 0, 50 мг/мл ) КБ-4 A, мг/г 7. 00 6. 00 5. 00 4. 00 p. H 7 ПОЕ p. H 2 3. 00 2. 00 1. 00 0. 20 0. 40 0. 60 Cравн, мг/мл 9
 Сравнение изотерм сорбции ФХ на различных сорбентах (интервал концентраций исходных растворов 0, 01 – 0, 50 мг/мл) р. Н 7 A, мг/г 9. 00 8. 00 7. 00 6. 00 5. 00 КУ-2 -8 ПОЕ (КУ-2 -8) КБ-4 4. 00 3. 00 ПОЕ (КБ-4) 2. 00 1. 00 0. 20 0. 40 0. 60 Cравн, мг/мл 10
Сравнение изотерм сорбции ФХ на различных сорбентах (интервал концентраций исходных растворов 0, 01 – 0, 50 мг/мл) р. Н 7 A, мг/г 9. 00 8. 00 7. 00 6. 00 5. 00 КУ-2 -8 ПОЕ (КУ-2 -8) КБ-4 4. 00 3. 00 ПОЕ (КБ-4) 2. 00 1. 00 0. 20 0. 40 0. 60 Cравн, мг/мл 10
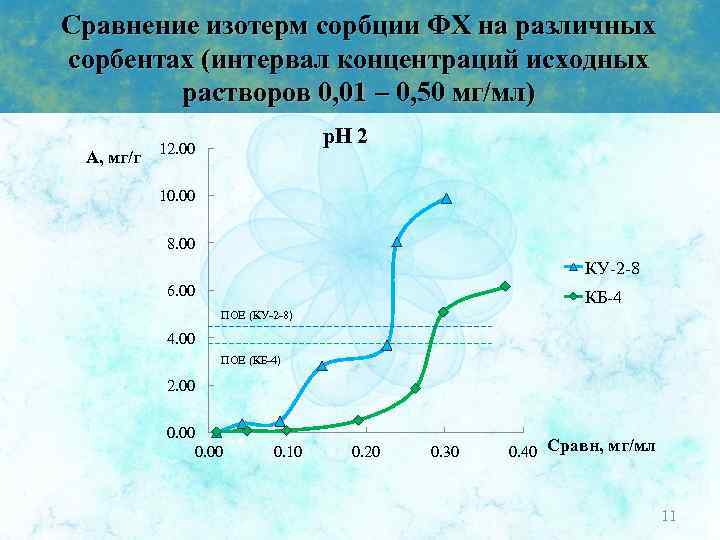 Сравнение изотерм сорбции ФХ на различных сорбентах (интервал концентраций исходных растворов 0, 01 – 0, 50 мг/мл) A, мг/г р. Н 2 12. 00 10. 00 8. 00 КУ-2 -8 6. 00 КБ-4 ПОЕ (КУ-2 -8) 4. 00 ПОЕ (КБ-4) 2. 00 0. 10 0. 20 0. 30 0. 40 Cравн, мг/мл 11
Сравнение изотерм сорбции ФХ на различных сорбентах (интервал концентраций исходных растворов 0, 01 – 0, 50 мг/мл) A, мг/г р. Н 2 12. 00 10. 00 8. 00 КУ-2 -8 6. 00 КБ-4 ПОЕ (КУ-2 -8) 4. 00 ПОЕ (КБ-4) 2. 00 0. 10 0. 20 0. 30 0. 40 Cравн, мг/мл 11
 ИК-спектры ФХ до и после сорбции на «КУ-2 -8» при варьировании р. Н среды – – – чист. «КУ-2 -8» , ······· «КУ-2 -8 + ФХ» (р. Н 7), ── «КУ-2 -8 + ФХ» (р. Н 2) 12
ИК-спектры ФХ до и после сорбции на «КУ-2 -8» при варьировании р. Н среды – – – чист. «КУ-2 -8» , ······· «КУ-2 -8 + ФХ» (р. Н 7), ── «КУ-2 -8 + ФХ» (р. Н 2) 12
 ИК-спектры ФХ до и после сорбции на «КБ-4» при варьировании р. Н среды – – – чист. «КБ-4» , ······· «КБ-4 + ФХ» (р. Н 7), ── «КБ-4 + ФХ» (р. Н 2) 13
ИК-спектры ФХ до и после сорбции на «КБ-4» при варьировании р. Н среды – – – чист. «КБ-4» , ······· «КБ-4 + ФХ» (р. Н 7), ── «КБ-4 + ФХ» (р. Н 2) 13
 Отнесение полос поглощения в спектрах КУ-2 -8 Функциональная Частота, см-1 группа чист. p. H 7 p. H 2 S – O 833 (ν) S = O 1035 (ν) – SO 3 H 1127, 1168 1127, 1158 1353 (δ) 1353(δ) 1452 (δ), 2911 (ν) 1452 (δ), 1479 1452 (δ), 2915 (ν) (ножничные), 2899 (ν) 1495, 1513, 1601 1642 1495, 1513, 1574, 1601 1642 1495, 1601 14
Отнесение полос поглощения в спектрах КУ-2 -8 Функциональная Частота, см-1 группа чист. p. H 7 p. H 2 S – O 833 (ν) S = O 1035 (ν) – SO 3 H 1127, 1168 1127, 1158 1353 (δ) 1353(δ) 1452 (δ), 2911 (ν) 1452 (δ), 1479 1452 (δ), 2915 (ν) (ножничные), 2899 (ν) 1495, 1513, 1601 1642 1495, 1513, 1574, 1601 1642 1495, 1601 14
 Отнесение полос поглощения в спектрах КБ-4 Частота, см-1 Функциональная группа чист. – P – O- - p. H 7 p. H 2 1042 C – O 1271 1276 1271 – OH 1390 – COO- 1483, 1546, 1562 1486, 1540, 1559 1708 1702 1450 (δ), 2853 (νs) 2922 (νas) 1452 (δ), 2887 (νs) 1456 (δ), 2905 (νs) 2950 (νas) 2942 (νas) 15
Отнесение полос поглощения в спектрах КБ-4 Частота, см-1 Функциональная группа чист. – P – O- - p. H 7 p. H 2 1042 C – O 1271 1276 1271 – OH 1390 – COO- 1483, 1546, 1562 1486, 1540, 1559 1708 1702 1450 (δ), 2853 (νs) 2922 (νas) 1452 (δ), 2887 (νs) 1456 (δ), 2905 (νs) 2950 (νas) 2942 (νas) 15
 Выводы 1. Разработана методика количественного определения фосфатидилхолина методом тонкослойной хроматографии (ТСХ) в следующих условиях: • Элюирующая система: хлороформ – метанол – уксусная кислота – вода (20 : 12 : 3, 2 : 1, 6) • Пластина: Сорбфил ПТСХ-ПЭТФ • Объем наносимой пробы: 10 мкл • Интервал концентраций (0, 01 – 0, 50) мг/мл. • Проявитель: 5%-ный раствор фосфорномолибденовой кислоты • Программа количественной обработки данных: Sorbfil Videodensitometer 2. Получены градуировочные графики ФХ при различных значениях р. Н среды, проведена математическая обработка. 3. Получены изотермы сорбции ФХ на катионоонообменных сорбентах при варьировании p. H среды, показано, что на сорбенте КУ-2 -8 реализуется механизм полимолекулярной сорбции, на первом этапе формирование монослоя идет преимущественно по ионообменному механизму, второго слоя – за счет гидрофобных и сорбат-сорбатных взаимодействий. При использовании КБ-4 оба типа взаимодействий реализуются одновременно. 4. Изучены ИК-спектры сорбентов, показано, что имеются сдвиги в области полос поглощения как функциональных групп, так и групп матрицы сорбента, что говорит о 16 двух типах взаимодействий.
Выводы 1. Разработана методика количественного определения фосфатидилхолина методом тонкослойной хроматографии (ТСХ) в следующих условиях: • Элюирующая система: хлороформ – метанол – уксусная кислота – вода (20 : 12 : 3, 2 : 1, 6) • Пластина: Сорбфил ПТСХ-ПЭТФ • Объем наносимой пробы: 10 мкл • Интервал концентраций (0, 01 – 0, 50) мг/мл. • Проявитель: 5%-ный раствор фосфорномолибденовой кислоты • Программа количественной обработки данных: Sorbfil Videodensitometer 2. Получены градуировочные графики ФХ при различных значениях р. Н среды, проведена математическая обработка. 3. Получены изотермы сорбции ФХ на катионоонообменных сорбентах при варьировании p. H среды, показано, что на сорбенте КУ-2 -8 реализуется механизм полимолекулярной сорбции, на первом этапе формирование монослоя идет преимущественно по ионообменному механизму, второго слоя – за счет гидрофобных и сорбат-сорбатных взаимодействий. При использовании КБ-4 оба типа взаимодействий реализуются одновременно. 4. Изучены ИК-спектры сорбентов, показано, что имеются сдвиги в области полос поглощения как функциональных групп, так и групп матрицы сорбента, что говорит о 16 двух типах взаимодействий.
 СПАСИБО ЗА ВНИМАНИЕ! 17
СПАСИБО ЗА ВНИМАНИЕ! 17
 S, мм 450 400 350 300 250 200 150 100 50 0 -0. 1 0. 3 0. 5 C, мг/мл Рис. 3. Градуировочный график для определения концентрации растворов ФХ методом ТСХ при p. H 7 в интервале концентраций 0, 01 -0, 50 мг/мл 18
S, мм 450 400 350 300 250 200 150 100 50 0 -0. 1 0. 3 0. 5 C, мг/мл Рис. 3. Градуировочный график для определения концентрации растворов ФХ методом ТСХ при p. H 7 в интервале концентраций 0, 01 -0, 50 мг/мл 18
 S, мм 500 450 400 350 300 250 200 150 100 50 0 0 0. 1 0. 2 0. 3 0. 4 0. 5 C, мг/мл Рис. 4. Градуировочный график для определения концентрации растворов ФХ методом ТСХ при p. H 2 в интервале концентраций 0, 01 -0, 50 мг/мл 19
S, мм 500 450 400 350 300 250 200 150 100 50 0 0 0. 1 0. 2 0. 3 0. 4 0. 5 C, мг/мл Рис. 4. Градуировочный график для определения концентрации растворов ФХ методом ТСХ при p. H 2 в интервале концентраций 0, 01 -0, 50 мг/мл 19
 A, мг/г 12. 00 10. 00 8. 00 6. 00 p. H 7 ПОЕ p. H 2 4. 00 2. 00 0. 00 -0. 10 0. 30 0. 50 Cравн, мг/мл Рис. 5. Изотермы сорбции ФХ на сорбенте КУ-2 -8 в нейтральной и кислой средах 20
A, мг/г 12. 00 10. 00 8. 00 6. 00 p. H 7 ПОЕ p. H 2 4. 00 2. 00 0. 00 -0. 10 0. 30 0. 50 Cравн, мг/мл Рис. 5. Изотермы сорбции ФХ на сорбенте КУ-2 -8 в нейтральной и кислой средах 20
 A, мг/г 7. 00 6. 00 5. 00 ПОЕ 4. 00 p. H 7 3. 00 p. H 2 2. 00 1. 00 0. 00 -0. 10 0. 30 0. 50 Cравн, мг/мл Рис. 6. Изотермы сорбции ФХ на сорбенте КБ-4 в нейтральной и кислой средах 21
A, мг/г 7. 00 6. 00 5. 00 ПОЕ 4. 00 p. H 7 3. 00 p. H 2 2. 00 1. 00 0. 00 -0. 10 0. 30 0. 50 Cравн, мг/мл Рис. 6. Изотермы сорбции ФХ на сорбенте КБ-4 в нейтральной и кислой средах 21


