ВОП.pptx
- Количество слайдов: 180
Воробьев А. В. ОНКОУРОЛОГИЯ Санкт-Петербург 2014

2005 ----- создана Общероссийская общественная организация «Российское Общество Онкоурологов» (64 региональных отделения) «Онкоурология» – ежеквартальный журнал с 2005 Конгрессы РООУ --- ежегодно в Москве «Клинические Рекомендации Европейской Ассоциации Урологов» --- в переводе на русский язык ежегодно с 2009 года

По традиции опухоли почек у взрослых принято ассоциировать исключительно с почечноклеточным ( «гипернефроидным» ) раком

Опухоли почек разнообразны по: • гистологической структуре • прогнозу • чувствительности к лучевой и лекарственной терапии • тактике лечения и диспансерного наблюдения

Наиболее совершенна Классификация ВОЗ, принятая в результате консенсуса, достигнутого на конференции в Лионе 14— 18 декабря 2002 года. Классификация издана Международным Агенством по изучению рака (IARC) в 2004 году

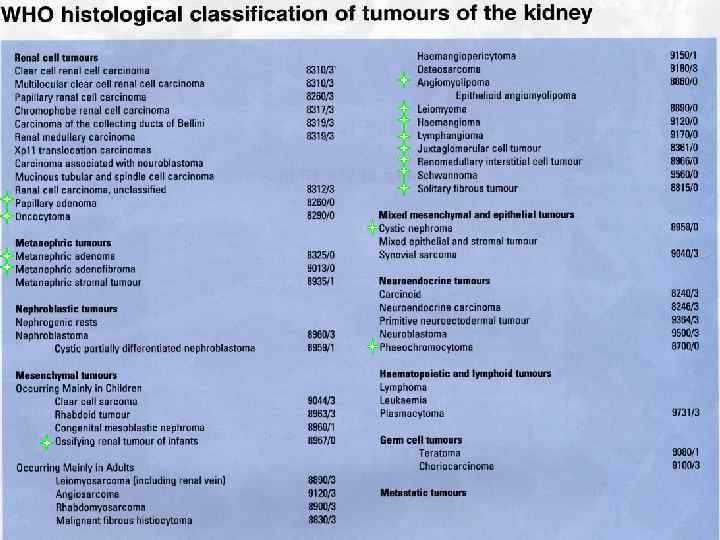

Классификация ВОЗ группирует опухоли в соответствии с тканевой принадлежностью • Почечноклеточные • • Метанефрогенные Нефробластические Мезенхимальные Нейроэндокринные Герминогенные Опухоли смешанного строения Опухоли гемопоэтической и лимфоидной ткани

Цифры после косой черточки (/) обозначают степень злокачественности опухоли • 0 ---доброкачественная • 3 ---злокачественная • 1 ---новообразование пограничной или точно не установленной злокачественности
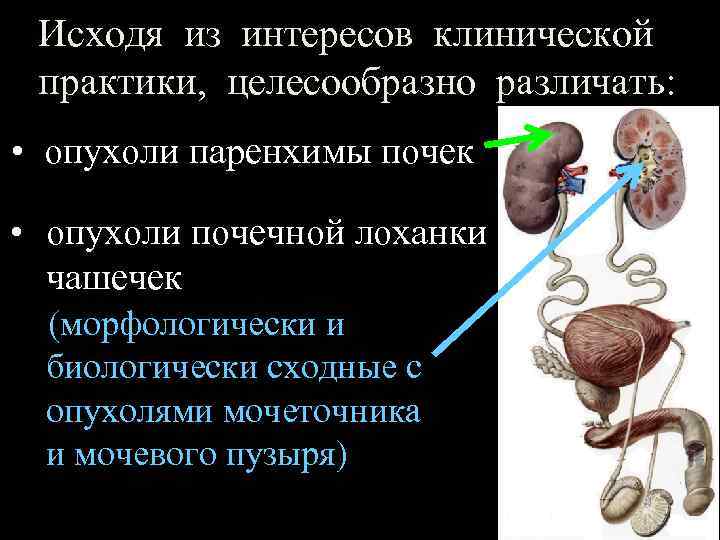
Исходя из интересов клинической практики, целесообразно различать: • опухоли паренхимы почек • опухоли почечной лоханки чашечек (морфологически и биологически сходные с опухолями мочеточника и мочевого пузыря) и

Опухоли почек: • первичные • метастатические (вторичные) • поражение почек при системных неопластических процессах (лимфомы)
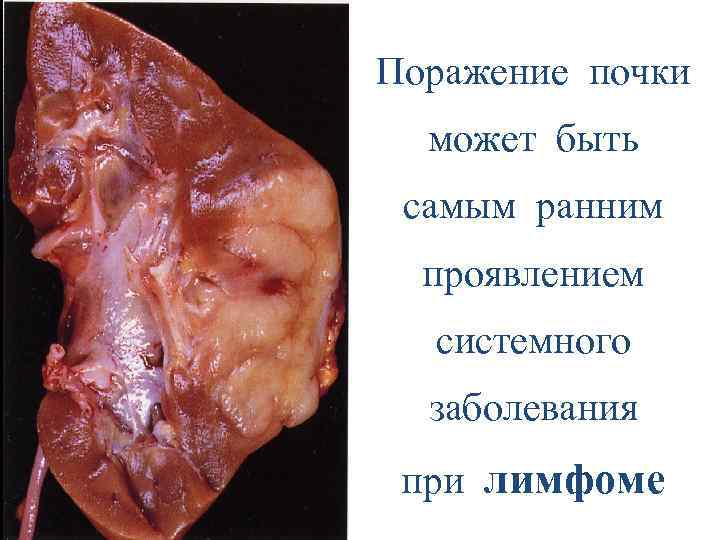
Поражение почки может быть самым ранним проявлением системного заболевания при лимфоме

Почечноклеточный рак -- наиболее актуальная проблема, ОДНАКО…. . • Грамотное, адекватное характеру патологии оказание помощи больным не может быть осуществлено без учета особенностей, присущих доброкачественным новообразованиям почек

Наиболее частая и значимая для клинической практики доброкачественная опухоль -- ангиомиолипома • Этиология и патогенез во многом неясны • Может возникать спорадически • Часто ассоциирована с наследственной патологией --- туберозным склерозом
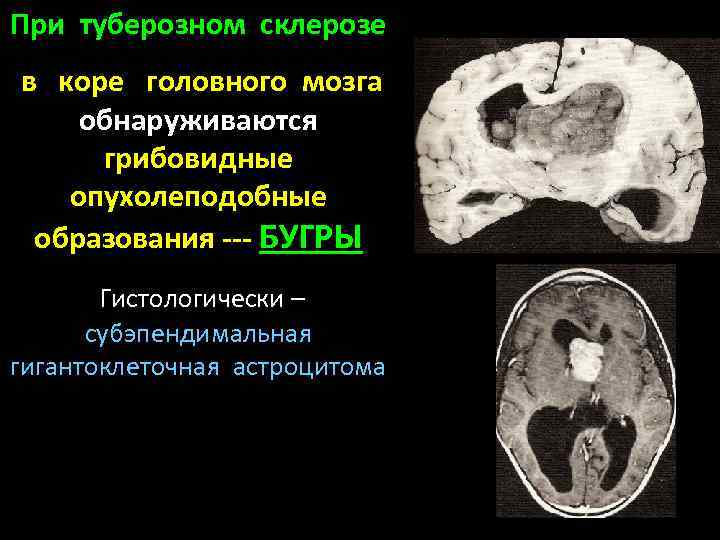
При туберозном склерозе в коре головного мозга обнаруживаются грибовидные опухолеподобные образования --- БУГРЫ Гистологически – субэпендимальная гигантоклеточная астроцитома
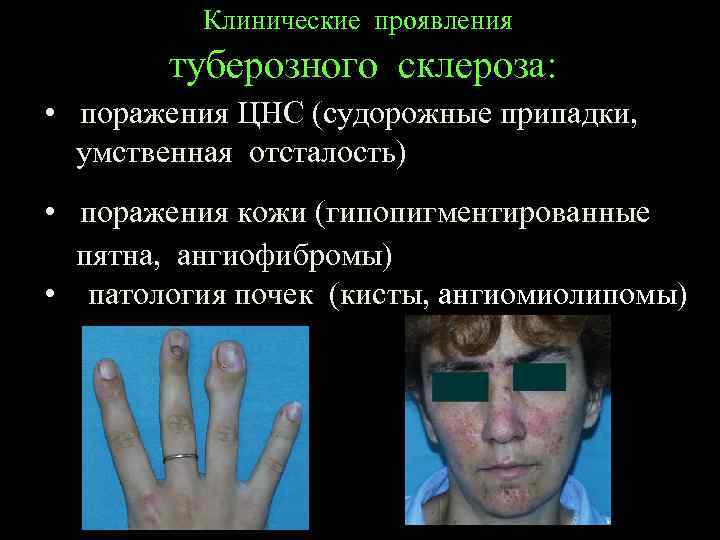
Клинические проявления туберозного склероза: • поражения ЦНС (судорожные припадки, умственная отсталость) • поражения кожи (гипопигментированные пятна, ангиофибромы) • патология почек (кисты, ангиомиолипомы)

У 15% больных имеется двухстороннее поражение почек ангиомиолипомой, что следует помнить, планируя «органоуносящую» операцию --- нефрэктомию

Ангиомиолипомы • обычно четко отграничены • обладают экспансивным ростом (раздвигая и сдавливая окружающие ткани) • НЕ метастазируют • (известны случаи инвазивного роста с инфильтрацией почечной капсулы и паранефральной клетчатки) • Возможно развитие почечноклеточного рака на фоне ангиомиолипомы
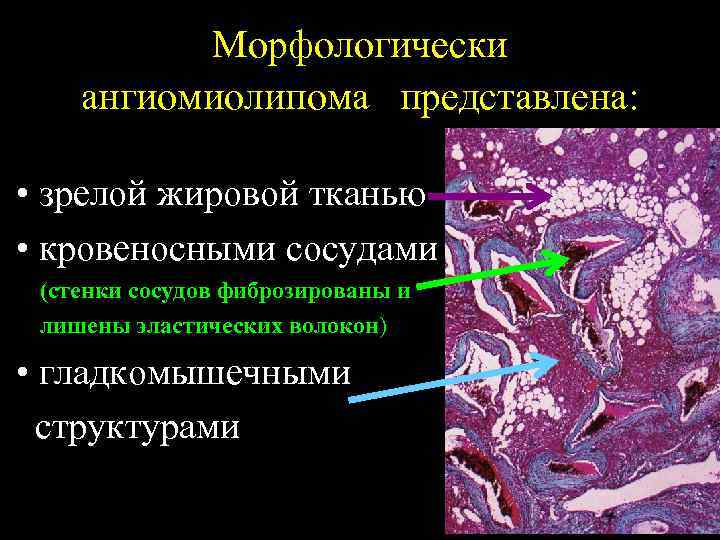
Морфологически ангиомиолипома представлена: • зрелой жировой тканью • кровеносными сосудами (стенки сосудов фиброзированы и лишены эластических волокон) • гладкомышечными структурами
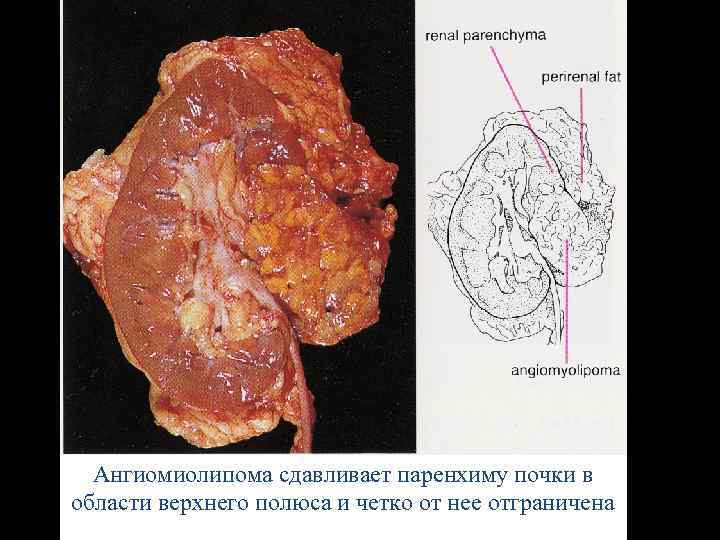
Ангиомиолипома сдавливает паренхиму почки в области верхнего полюса и четко от нее отграничена
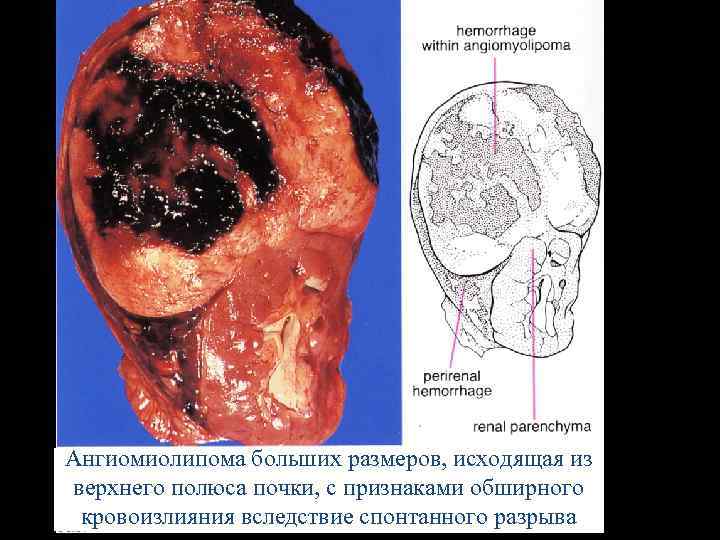
Ангиомиолипома больших размеров, исходящая из верхнего полюса почки, с признаками обширного кровоизлияния вследствие спонтанного разрыва

Первым проявлением ангиомиолипомы почки может быть внезапно возникшая интенсивная боль, вызванная спонтанным разрывом опухоли и формированием обширной забрюшинной гематомы

Боль при спонтанном разрыве ангиомиолипомы сопровождается признаками внутреннего кровотечения, симулирует картину «острого живота» , является основанием для экстренной госпитализации в хирургическую клинику и экстренной операции (резекции почки или нефрэктомии)

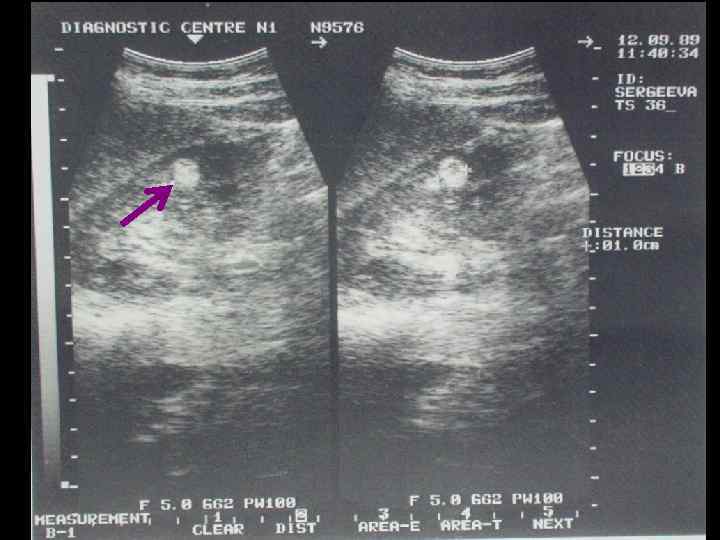
Чем больше диаметр АМЛ почки, тем больше вероятность ее спонтанного разрыва. Неосложненная разрывом АМЛ почки протекает бессимптомно и выявляется при УЗИ, характеризуясь гиперэхогенной структурой; особенно высокой эхоплотностью отличаются АМЛ небольших размеров.
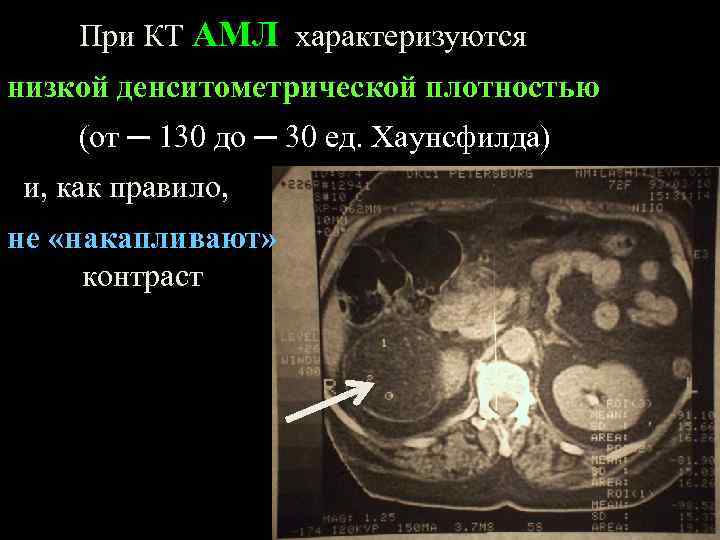
При КТ АМЛ характеризуются низкой денситометрической плотностью (от ─ 130 до ─ 30 ед. Хаунсфилда) и, как правило, не «накапливают» контраст

Опухоли диаметром до 4 --5 см растут очень медленно и не дают осложнений; больные подлежат наблюдению ─ ─ УЗИ (при необходимости, КТ) 1 раз в год

При АМЛ более 5 см в диаметре значительно возрастает угроза спонтанного разрыва опухоли; целесообразна органосохраняющая операция --- резекция почки (или нефрэктомия)
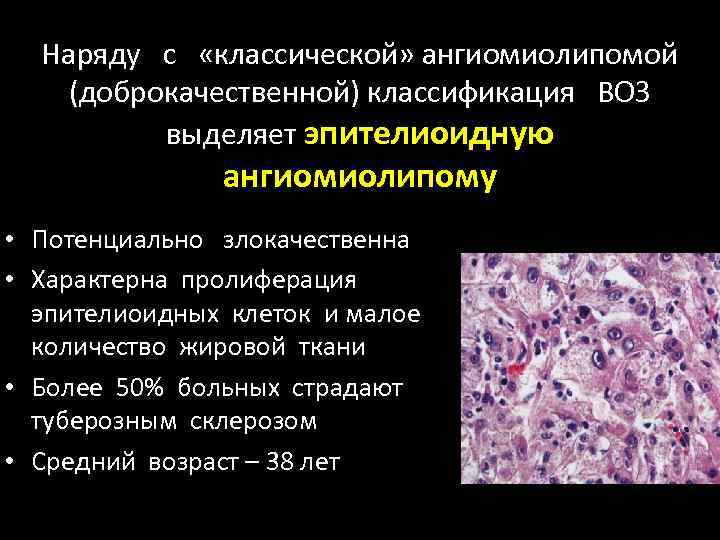
Наряду с «классической» ангиомиолипомой (доброкачественной) классификация ВОЗ выделяет эпителиоидную ангиомиолипому • Потенциально злокачественна • Характерна пролиферация эпителиоидных клеток и малое количество жировой ткани • Более 50% больных страдают туберозным склерозом • Средний возраст – 38 лет

Эпителиоидная ангиомиолипома • Методами лучевой диагностики визуализируется как почечноклеточный рак • Может иметь очаги некроза • В 1/3 наблюдений способна к метастазированию (лимфоузлы, печень, легкие) • Характеризуется мутацией Р 53

Гемангиомы почек (и лимфангиомы) • обычно располагаются на верхушке почечных пирамид • имеют диаметр 3 ─ 4 мм • часто бывают множественными и двухсторонними • в 95% проявляются макрогематурией и сопровождающей кровотечение почечной коликой

Онкоцитома ─ ─ эпителиальная опухоль из крупных светлых эозинофильных клеток, богатых митохондриями (греч. корень onkos характеризует клетку как “вздутую” или “объемную”) Клиническое течение доброкачественно, прогноз благоприятный

ОНКОЦИТОМА • ~5% от общего числа опухолей паренхимы почек • встречается в 20 раз реже, чем почечноклеточный рак • не метастазирует (иногда отмечается инвазивный рост с инфильтрацией капсулы почки) • выявляется «случайно» при УЗИ, КТ или ангиографии
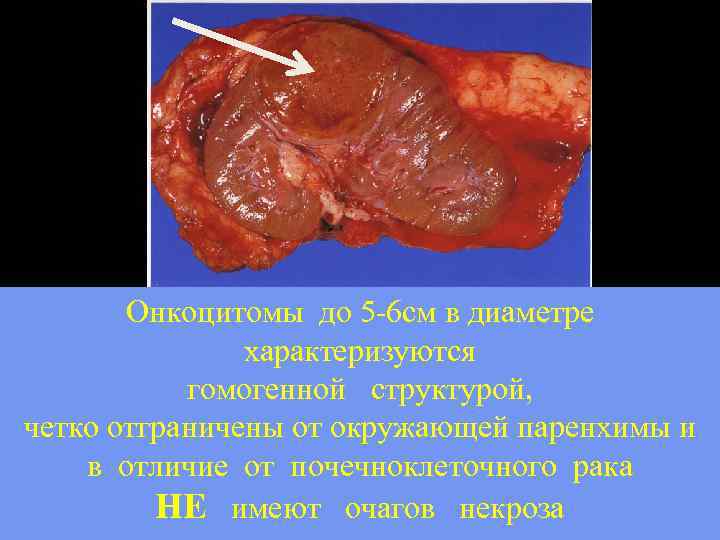
Онкоцитомы до 5 -6 см в диаметре характеризуются гомогенной структурой, четко отграничены от окружающей паренхимы и в отличие от почечноклеточного рака НЕ имеют очагов некроза
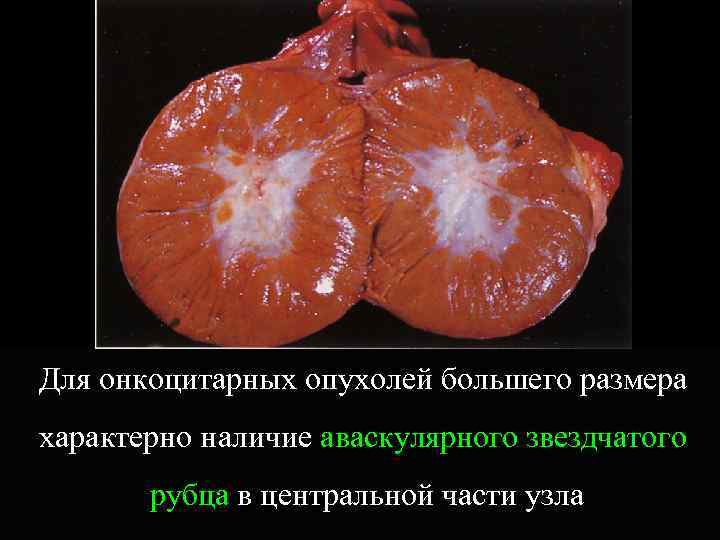
Для онкоцитарных опухолей большего размера характерно наличие аваскулярного звездчатого рубца в центральной части узла
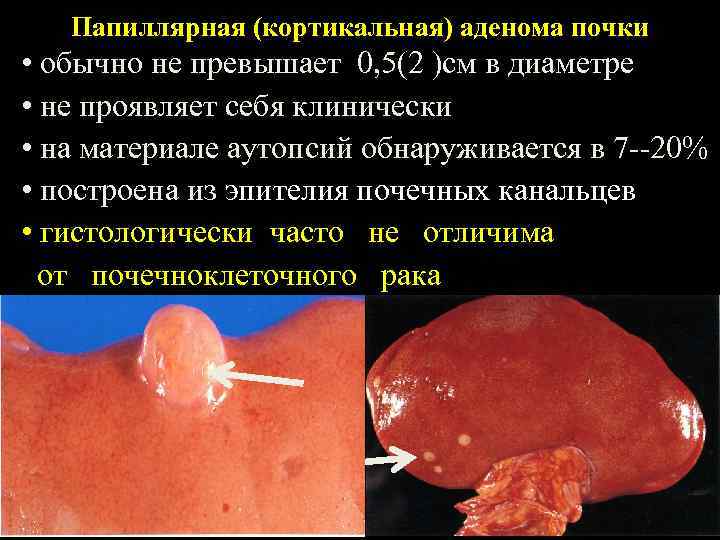
Папиллярная (кортикальная) аденома почки • обычно не превышает 0, 5(2 )см в диаметре • не проявляет себя клинически • на материале аутопсий обнаруживается в 7 --20% • построена из эпителия почечных канальцев • гистологически часто не отличима от почечноклеточного рака
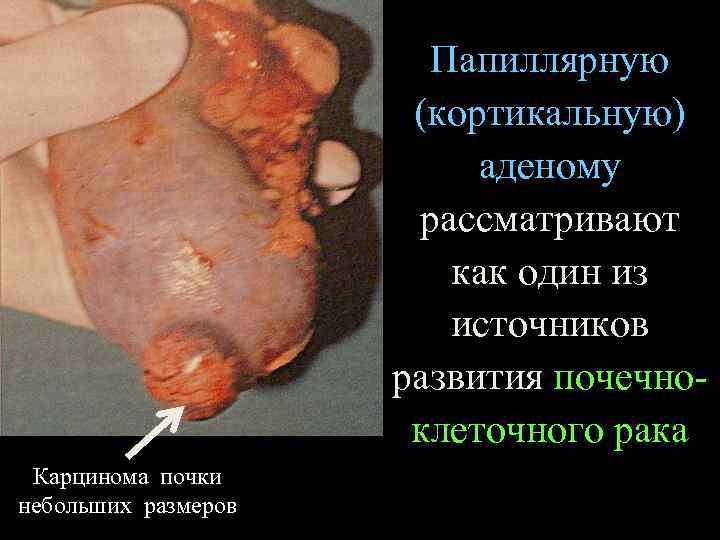
Папиллярную (кортикальную) аденому рассматривают как один из источников развития почечноклеточного рака Карцинома почки небольших размеров

В последние годы доминирует точка зрения, согласно которой любое новообразование из эпителия почечных канальцев следует считать злокачественным, рассматривая опухоли диаметром более 5 мм как латентный рак

Кисты почек --- в отличие от большинства опухолей АВАСКУЛЯРНЫ Morton A Bosniak, M. D. (Professor of Radiology NEW YORK) ---- создатель классификации кист почек и автор рекомендаций по тактике ведения больных
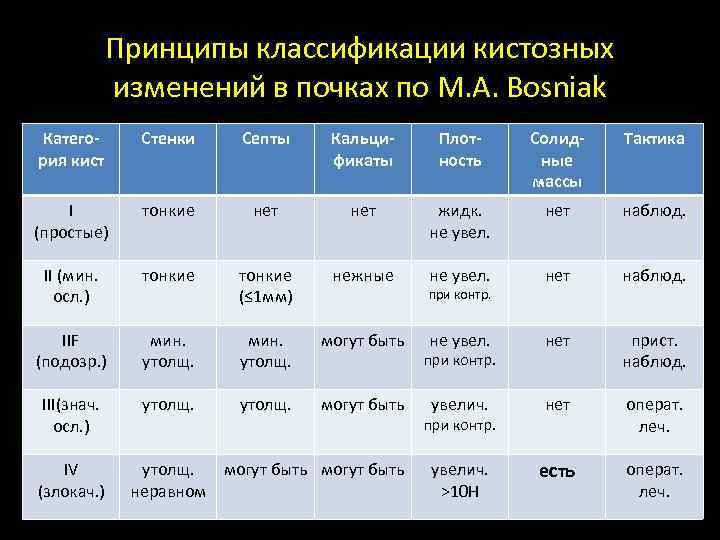
Принципы классификации кистозных изменений в почках по M. A. Bosniak Категория кист Стенки Септы Кальцификаты Плотность Солидные массы Тактика I (простые) тонкие нет жидк. не увел. нет наблюд. II (мин. осл. ) тонкие (≤ 1 мм) нежные не увел. нет наблюд. IIF (подозр. ) мин. утолщ. могут быть не увел. нет прист. наблюд. III(знач. осл. ) утолщ. могут быть увелич. нет операт. леч. увелич. >10 H есть операт. леч. IV (злокач. ) утолщ. могут быть неравном при контр.

ПОЧЕЧНОКЛЕТОЧНЫЙ РАК (аденокарцинома почки, «гипернефроидный рак» , «гипернефрома» , опухоль Гравитца), Renal Cell Carcinoma (RCC)

В России в 2008 г. заболеваемость на 100 000 населения – 12, 37. Прирост абсолютного числа заболевших с 1998 г. – 41% Мужчины / женщины = 2/1 Средний возраст 62 года ~1/3 больных почечноклеточным раком умирает от этого заболевания

Факторы, предрасполагающие к заболеванию раком почки: • болезнь фон Хиппель-Линдау (мутация гена-супрессора опухолевого роста--VHL-ген) • курение табака • контакт с асбестом • избыточный вес + артериальная гипертензия • гемодиализ по поводу почечной недостаточности

Варианты почечноклеточного рака • Светлоклеточная почечноклеточная карцинома • Мультилокулярная светлоклеточная почечноклеточная карцинома • Папиллярная почечноклеточная карцинома • Хромофобная почечноклеточная карцинома* • Карцинома из собирательных трубочек Беллини* • Медуллярная карцинома почки* • Карциномы, ассоциированные с транслокацией хромосомы Хр11 • Карцинома, ассоциированная с нейробластомой • Муцинозная тубулярная и веретеноклеточная карцинома • Почечноклеточная карцинома, неклассифицируемая • *отличаются наиболее агрессивным течением и неблагоприятным прогнозом


В 60% наблюдений диагноз опухоли почки устанавливается при полном отсутствии клинических проявлений, т. е. «случайно» на основании УЗИ, выполненного профилактически или по поводу другого заболевания
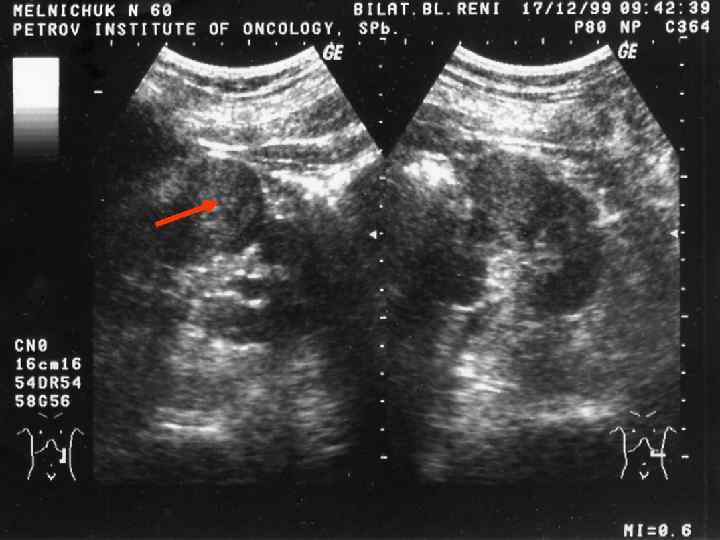

Учитывая решающую роль УЗИ в выявлении патологии почек, надпочечников, забрюшинных лимфоузлов и неорганных забрюшинных опухолей, следует всегда стремиться к максимально полному и тщательному исследованию; к сожалению, этот принцип часто не соблюдается

20% --- первые проявления --- общие симптомы (снижение веса, повышение температуры) или признаки метастазов (изменения при ФЛГ, боли в костях, патологические переломы). 5% --- паранеопластический синдром (гиперкальциемия, полицитемия, амилоидоз, синдром Штофера)

Синдром Штофера (Stauffer) -- нарушения функции печени у больных карциномой почки: • повышение активности щелочной фосфатазы • удлинение протромбинового времени • диспротеинемия • слабость • анорексия • кахексия • гипотензия • увеличение печени (и селезенки) ВСЕ проявления исчезают после удаления опухоли почки

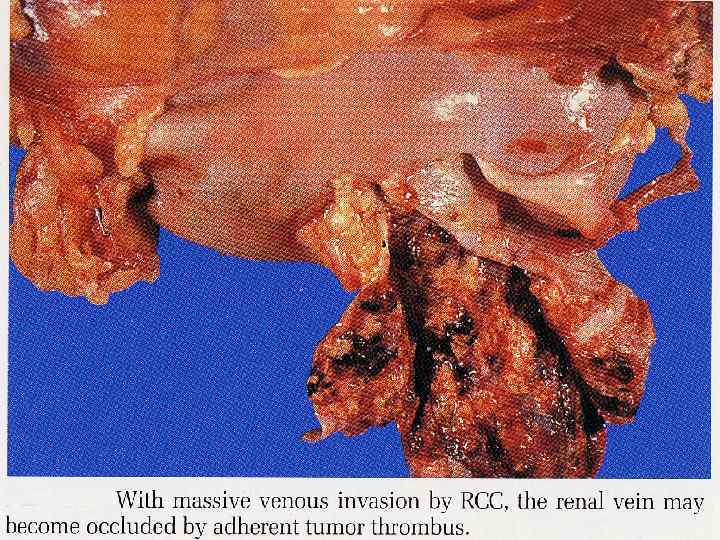
Ткань опухоли может содержать обширные очаги некроза

КТ -- основной метод уточняющей диагностики рака почки; КТ выявляет размеры и локализацию опухоли, рапсространение на крупные сосуды, метастатическое поражение забрюшинных лимфоузлов, контрлатеральной почки и печени, прорастание в прилежащие органы

Чувствительность КТ в диагностике рака почки ~ 90 -95%. Ткань опухоли имеет гетерогенную плотность; плотность увеличивается после введения контрастного вещества

ЛЕЧЕНИЕ локализованного рака паренхимы почки (T 1 a-T 1 b, ǿ опухоли <7 см) 1. Радикальная нефрэктомия больше НЕ является «золотым стандартом» 2. Стандарт лечения -- открытая резекция почки 3. Для предотвращения рецидива достаточно минимального отступа от границы опухоли 4. Лапароскопическую резекцию почки должны выполнять опытные хирурги

ЛЕЧЕНИЕ локализованного рака паренхимы почки стадии T 2 1. Требуется радикальная лапароскопическая нефрэктомия 2. Адреналэктомия НЕ показана при отсутствии поражения надпочечника по КТ или МРТ перед операцией 3. Расширенная лимфодиссекция НЕ способствует улучшению отдаленной выживаемости
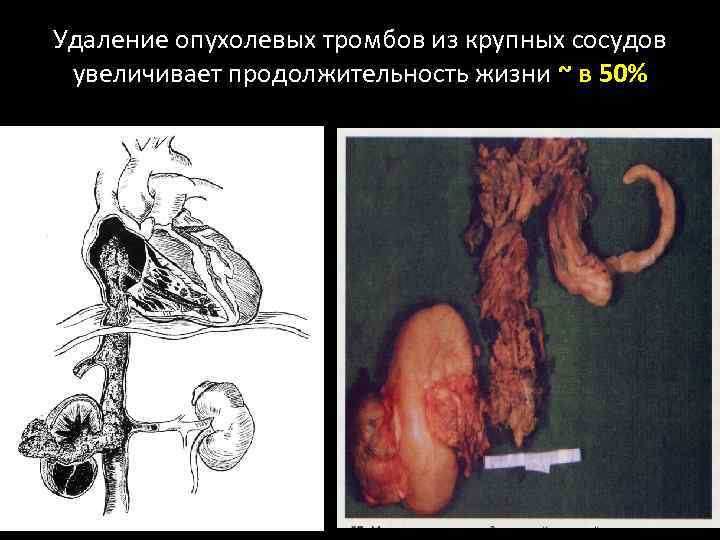
Удаление опухолевых тромбов из крупных сосудов увеличивает продолжительность жизни ~ в 50%

Робот – ассистированная нефрэктомия применяется широко; Робот-ассистированная резекция почки---- новая технология, которая только проходит оценку

Адъювантная терапия после радикального хирургического лечения рака паренхимы почки НЕ показана (вне рамок клинических исследований) Клинические рекомендации EAU, 2010

Почечноклеточный рак резистентен к химиотерапии (80% клеток почечноклеточного рака экспрессируют ген множественной лекарственной резистентности, кодирующий Р-гликопротеин) Стандартных режимов цитостатической терапии больных раком почки НЕ существует. Любая химиотерапия --- клинический эксперимент

Случаи успешного клинического применения интерферона и интерлейкина-2 стимулировали интерес к иммунотерапии диссеминированного рака почки, однако пока результаты нельзя считать удовлетворительными

Наиболее перспективны таргетные препараты: • Ингибиторы тирозинкиназ – сунитиниб (сутент) сорафениб (нексавар) пазопаниб (вотриент) • Ингибиторы (авастин) ангиогенеза – БЕВАЦИЗУМАБ • Ингибиторы m – TOR – темсиролимус (торизел) эверолимус (афинитор)
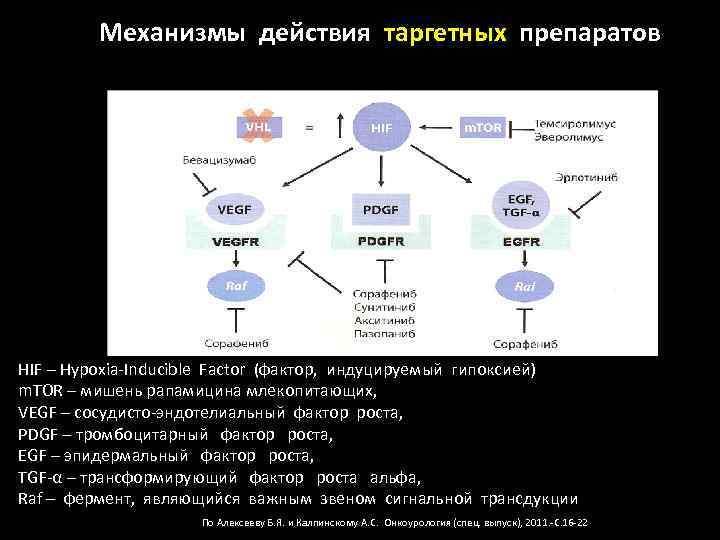
Механизмы действия таргетных препаратов HIF – Hypoxia-Inducible Factor (фактор, индуцируемый гипоксией) m. TOR – мишень рапамицина млекопитающих, VEGF – сосудисто-эндотелиальный фактор роста, PDGF – тромбоцитарный фактор роста, EGF – эпидермальный фактор роста, TGF-α – трансформирующий фактор роста альфа, Raf – фермент, являющийся важным звеном сигнальной трансдукции По Алексееву Б. Я. и Калпинскому А. С. Онкоурология (спец. выпуск), 2011. -С. 16 -22
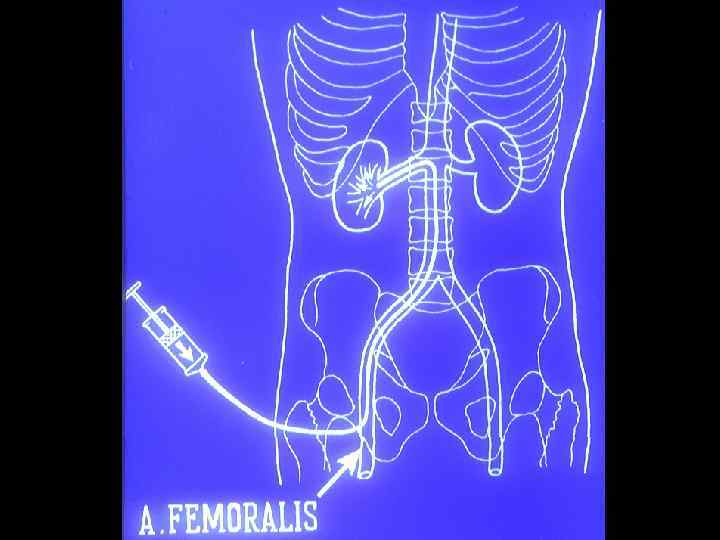

Эмболизация способна: • ликвидировать (предотвратить) макрогематурию • снизить проявления интоксикации • уменьшить интенсивность болей • улучшить самочувствие
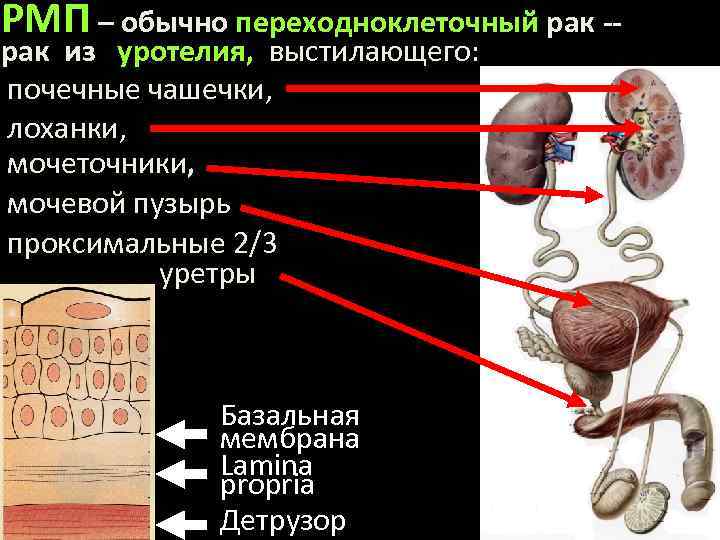
РМП – обычно переходноклеточный рак -рак из уротелия, выстилающего: почечные чашечки, лоханки, мочеточники, мочевой пузырь проксимальные 2/3 уретры Базальная мембрана Lamina propria Детрузор

70 – 80% уротелиальных опухолей диагностируются на неинвазивных стадиях, причем 30 -85% поверхностных опухолей рецидивируют после первичного лечения; 10 – 30% поверхностных опухолей прогрессируют в мышечно-инвазивные и метастатические карциномы. 20 – 30 % уротелиальных опухолей уже при выявлении характеризуются инвазивным ростом
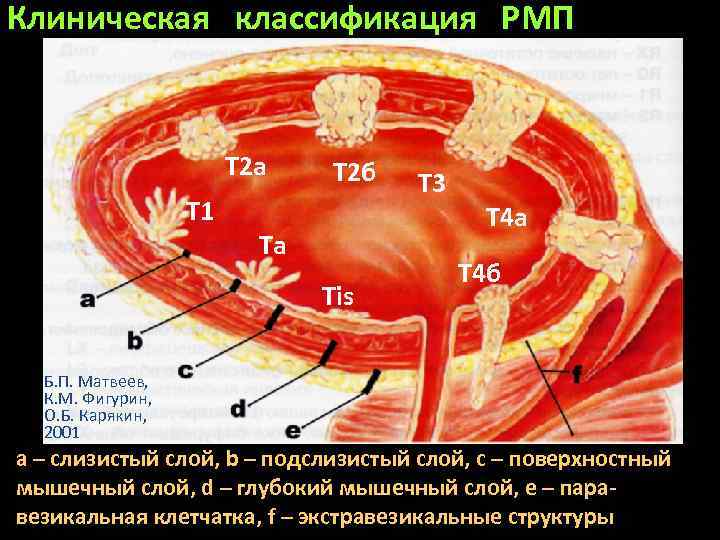
Клиническая классификация РМП T 2 a T 1 T 2 б Ta Tis T 3 T 4 a T 4 б Б. П. Матвеев, К. М. Фигурин, О. Б. Карякин, 2001 а – слизистый слой, b – подслизистый слой, с – поверхностный мышечный слой, d – глубокий мышечный слой, e – паравезикальная клетчатка, f – экстравезикальные структуры
Клинические симптомы РМП: - макрогематурия - дизурия - боли (над лобком, в промежности, в области крестца) -уретеропиелоэктазия пиелонефрит почечная недостаточность гидронефроз

Цистоскопия выявляет: • анатомическую форму роста опухоли (экзофитную, эндофитную, смешанную) и косвенно -- глубину инвазии • размеры опухолей, их число и локализацию в мочевом пузыре • обеспечивает визуальный контроль в процессе биопсии
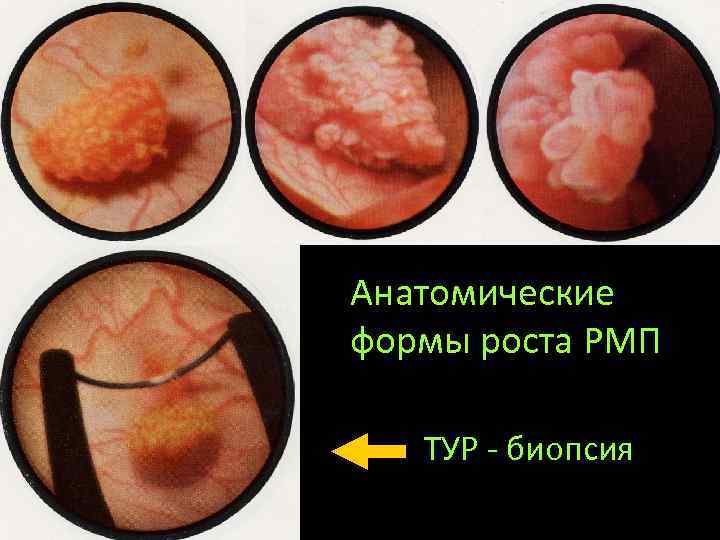
Анатомические формы роста РМП ТУР - биопсия
Биопсия МП «холодная биопсия» (в т. ч. “рандомизированная” биопсия для диагностики очагов Tis) ТУР-биопсия (в т. ч. одновременно с радикальным удалением опухоли)

Цитологическое исследование осадка мочи * неинвазивность * высокая достоверность (40 --83%) * дешевизна * эффективность при Tis * скрининг РМП * метод мониторинга после лечения поверхностных ОМП
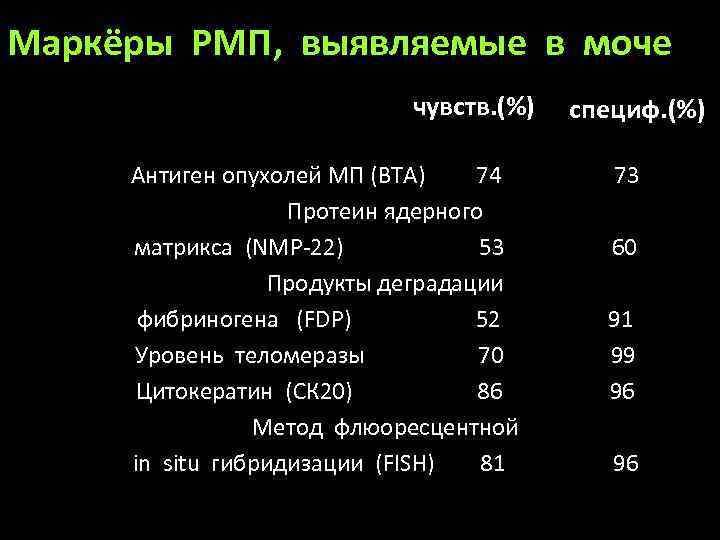
Маркёры РМП, выявляемые в моче чувств. (%) Антиген опухолей МП (ВТА) 74 Протеин ядерного матрикса (NMP-22) 53 Продукты деградации фибриногена (FDP) 52 Уровень теломеразы 70 Цитокератин (СК 20) 86 Метод флюоресцентной in situ гибридизации (FISH) 81 специф. (%) 73 60 91 99 96 96
Ультразвуковая томография (трансабдоминальная, трансректальная, трансвагинальная, трансуретральная)
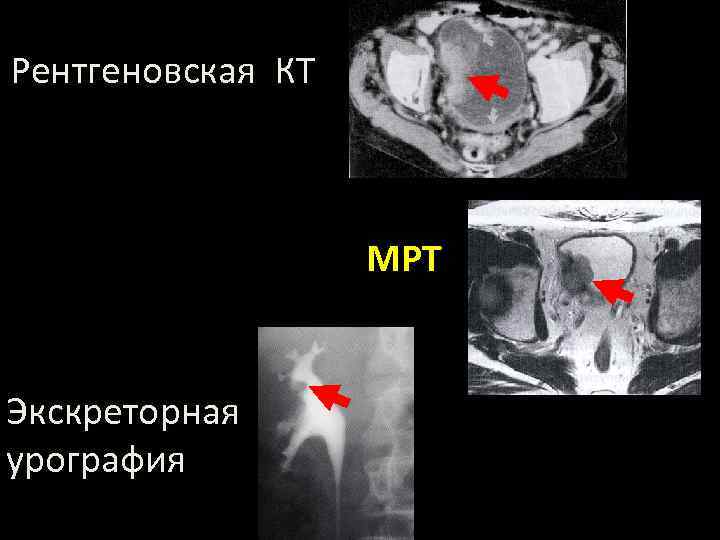
Рентгеновская КТ МРТ Экскреторная урография

Поверхностные опухоли: -Та -- неинвазивная папиллярная карцинома - Тis -- интраэпителиальный рак, «плоская опухоль» -Т 1 -- инфильтрация ограничена субэпителиальной соединительной тканью

Основной метод лечения поверхностных опухолей мочевого пузыря – -- ТУР + адъювантная терапия инстилляциями в мочевой пузырь вакцины БЦЖ или цитостатических препаратов (митомицин С, доксорубицин)

Основной метод лечения мышечно-инвазивного РМП --- радикальная цистэктомия Альтернатива -- -- органосохраняющее лечение ( «трехмодальный подход» ) --- сочетание трансуретральной резекции, лучевой и системной химиотерапии

Три группы операций: 1. Создание ортотопического мочевого пузыря 2. Внутреннее дренирование (отведение мочи в кишечник) 3. Наружное дренирование (создание уростомы)
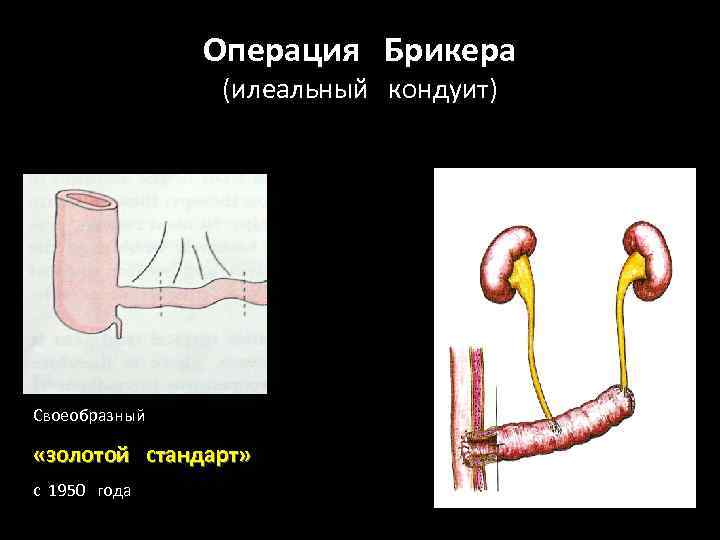
Операция Брикера (илеальный кондуит) Своеобразный «золотой стандарт» с 1950 года

Местнораспространенный и диссеминированный РМП -- -- системная химиотерапия: M-VAC Метотрексат 30 мг/м² в/в в 1 -й день Винбластин 3 мг/м² в/в во 2 -й день Доксорубицин 30 мг/м² в/в во 2 -й день Цисплатин 70 мг/м² в/в капельно во 2 -й день Циклы повторяются каждые 4 недели; метотрексат и винбластин повторяют на 15 -й и 22 -й день при нормальных показателях крови. GP Цисплатин 50 -60 мг/м² в/в капельно в 1 -й день Гемцитабин 800 -1000 мг/м² в/в капельно в 1 -й и 8 -й день Повторные курсы на 28 день
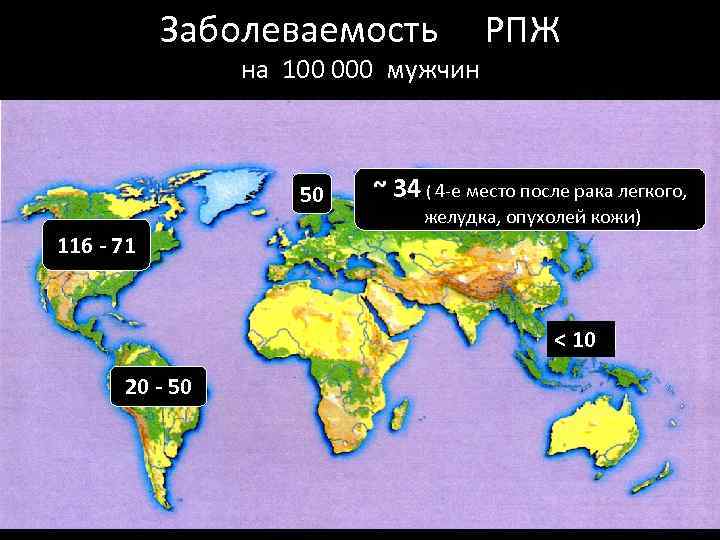
Заболеваемость на 100 000 мужчин 50 РПЖ ~ 34 ( 4 -е место после рака легкого, желудка, опухолей кожи) 116 - 71 < 10 20 - 50

Факторы, увеличивающие риск заболевания РПЖ • Возраст • Этническая принадлежность • Миграция в регионы с высокой заболеваемостью • Наличие РПЖ у кровных родственников • Алиментарный фактор (употребление жиров животного происхождения) • Воспаление ? ? ?

Подавляющее большинство больных старше 50 лет, однако молодой возраст нельзя считать аргументом для исключения РПЖ

ЗАБОЛЕВАЕМОСТЬ РПЖ в США (на 100. 000 мужчин) Афроамериканцы --116 Белые -- 71 На протяжении жизни 1 из 5 мужчин заболевает и 1 из 33 умирает от РПЖ Pienta K. & Smith D. , 2005

ЗАБОЛЕВАЕМОСТЬ РПЖ (на 100. 000 мужчин) изменяется в результате миграции МИГРАЦИЯ В США Япония -5, 1 16, 5 Китай – 1, 8 14, 9 РОЛЬ ВНЕШНИХ ФАКТОРОВ ! Prezioso et al, 2004

Если родственник 1 -й степени родства болен РПЖ, риск возрастает вдвое; Если больны 2 родственника 1 -й степени родства и более, риск возрастает в 5 -11 раз. Gronberg H. et al. , Cancer (1996) Jan; 77(1): 138 -43

Факторы, снижающие риск прогрессии латентного РПЖ в клинически значимый: Фитоэстрогены---диета, богатая соей Фитоэстрогены Лейкопены, полифенолы, селен, цинк Ограничение жиров животного происхождения • Финастерид и Дутастерид (ингибиторы • 5 -α-редуктазы) --- препарат ы , рекомендованные для медикаментозной профилактики РПЖ в группах повышенного риска (снижение риска ~ 24, 8%) • • •

Важнейшая биологическая особенность РПЖ --многообразие форм естественного развития болезни: • Латентный рак • Клинически манифестированные формы

РЕЙНБЕРГ Самуил Аронович (1897 -1966) • …остеопластические метастазы пояснично - крестцовой области у пожилого мужчины …. можно считать почти доказанным первичный РПЖ

Открытие простатоспецифического антигена и широкое внедрение исследования ПСА в сыворотке крови значительно улучшило диагностику РПЖ, особенно, локализованных и доклинических форм, поддающихся радикальному лечению

Достигнутые успехи породили МИФ о том, что ключевые моменты выявления и лечения РПЖ полностью раскрыты

Основанный на уровне ПСА скрининг мужского населения, населения широкое внедрение пункционной биопсии и радикальной простатэктомии (РПЭ) НЕ привели к снижению смертности и НЕ оправдали первоначальных надежд (Otto S. J. , Roobol M. J. , 2006)

>30 лет РПЖ в центре внимания мировой науки проблема не теряет … актуальности и далека от разрешения

Причины «неудачи» • Недостаточная специфичность ПСА как маркера рака предстательной железы • Невозможность четко дифференцировать агрессивные формы болезни от «клинически незначимых» (индолентных) вариантов РПЖ, не приводящих к смерти

Основные методы диагностики 1. Анализ крови---- на ПСА (PSA) 2. Пальцевое ректальное исследование ---------------ПРИ (DRE) 3. Ультразвуковая диагностика ------------------ТРУЗИ (TRUS) Необходимо морфологическое подтверждение диагноза --- пункционная биопсия (ТУР, аденомэктомия)
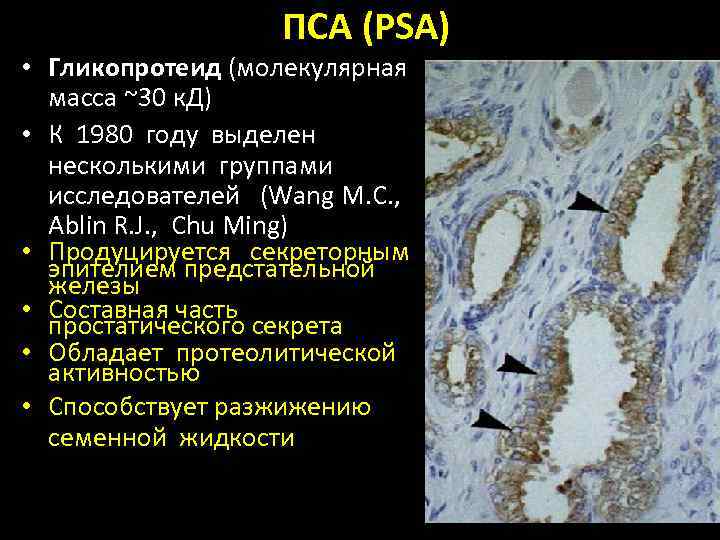
ПСА (PSA) • Гликопротеид (молекулярная масса ~30 к. Д) • К 1980 году выделен несколькими группами исследователей (Wang M. C. , Ablin R. J. , Chu Ming) • Продуцируется секреторным эпителием предстательной железы • Составная часть простатического секрета • Обладает протеолитической активностью • Способствует разжижению семенной жидкости
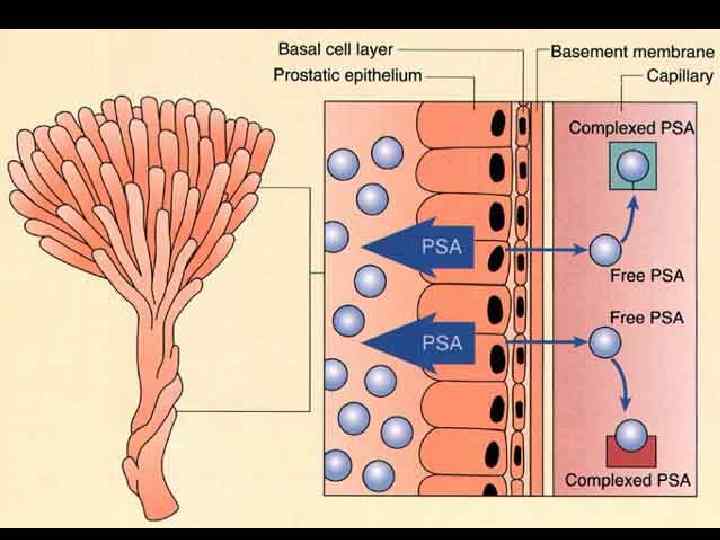

• ПСА специфичен для ткани предстательной железы, но не может рассматриваться как специфический опухолевый маркер для р а н н е й диагностики РПЖ ! ! ! • ПСА – надежный показатель рецидива РПЖ после радикального лечения (особенно, хирургического) • Уровень ПСА повышается: при ДГПЖ, простатите, после эякуляции, после трансуретральных манипуляций, массажа предстательной железы, ТРУЗИ и пальцевого ректального исследования

Уровень ПСА • увеличивается: с возрастом (допустимые “нормальные” значения) Возраст (лет) 40 -49 50 -59 60 -69 70 -79 ПСА (нг/мл) 2, 5 3, 5 4, 5 6, 5 с увеличением объема ПЖ • Снижению ПСА способствуют: гипохолестеринэмические препараты (статины) финастерид, дутастерид избыточная масса тела

• Пальцевое ректальное исследование (ПРИ) непригодно для выявления опухолей 1 -й стадии (непальпируемых) Метод не потерял значения для диагностики более распространённых форм рака предстательной железы (при объеме опухоли > 0, 2 мл)
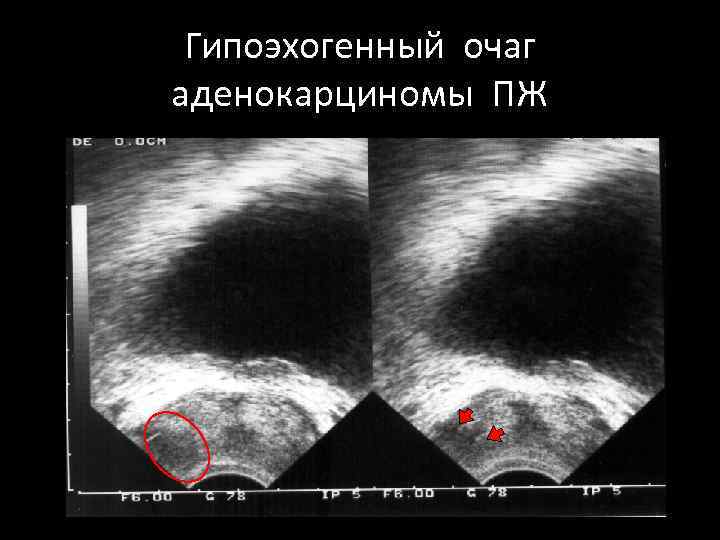
Гипоэхогенный очаг аденокарциномы ПЖ

Доминирующий доступ • Трансректальный (под контролем ТРУЗИ) • Значительно реже (в рутинной практике)--- трансперинеальный (например, после БПЭ прямой кишки)
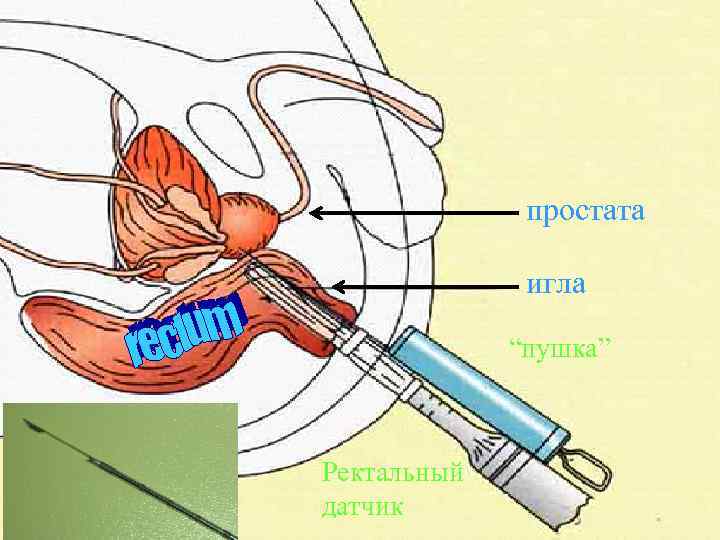
простата игла “пушка” Ректальный датчик

«…почти все опухоли простаты объемом ≥ 0, 5 мл можно выявить при использовании трансректальной пункционной биопсии с количеством биоптатов 14 – 18 и длиною биоптата 22 мм» Kanao K. , Eastham J. A. , Scardino P. T. e t al. Can transrectal needly biopsy be optimised to detect nearly all prostate cancer with a volume of ≥ 0, 5 ml? A three – demensional analysis/ British Journal of Urology. 2013 (112) 7

Трансперинеальная мультифокальная биопсия простаты с использованием шаблона – template biopsy – -картированная биопсия Применяется в последние годы в связи с распространением брахитерапии и разработкой методов фокальной деструкции небольших по объему очагов опухоли
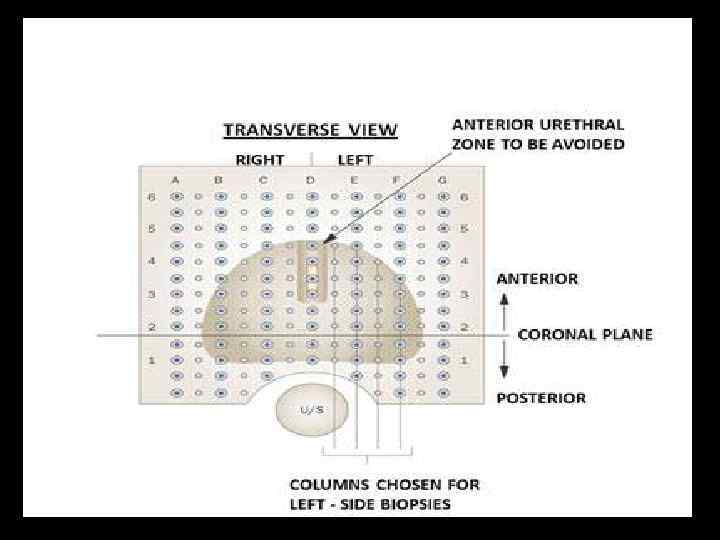

Уровень дифференцировки аденокарциномы предстательной железы принято отражать по шкале Глисона
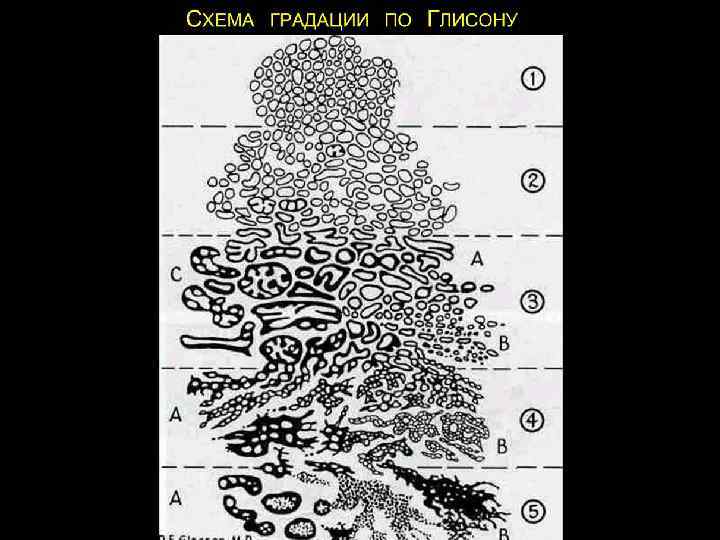

Градация по Глисону отображается в виде суммы степеней нарушения структуры в основной (преобладающей) и второстепенной (меньшей по площади) зонах. минимальная сумма 1+1=2 максимальная сумма 5+5=10
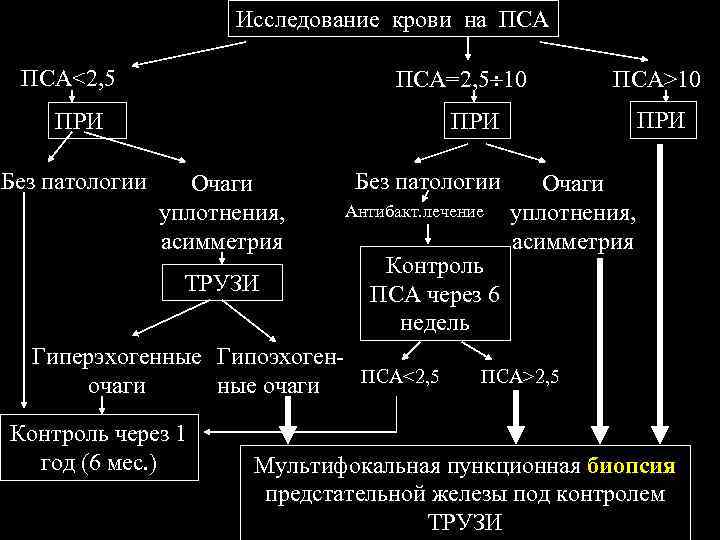
Исследование крови на ПСА<2, 5 ПСА=2, 5 10 ПРИ Без патологии ПСА>10 ПРИ Очаги уплотнения, асимметрия ТРУЗИ Без патологии Антибакт. лечение Контроль ПСА через 6 недель Гиперэхогенные Гипоэхоген. ПСА<2, 5 очаги ные очаги Контроль через 1 год (6 мес. ) Очаги уплотнения, асимметрия ПСА>2, 5 Мультифокальная пункционная биопсия предстательной железы под контролем ТРУЗИ

Совершенствование гистологического исследования Наиболее значимый для практики тканевый маркер рака предстательной железы---AMACR или железы. P 504 S (α-Methylacyl Coenzyme A Racemase) Чувствительность теста колеблется в пределах 82 ---100% Специфичность теста 79 ---100% (независимо от уровня дифференцировки опухоли)
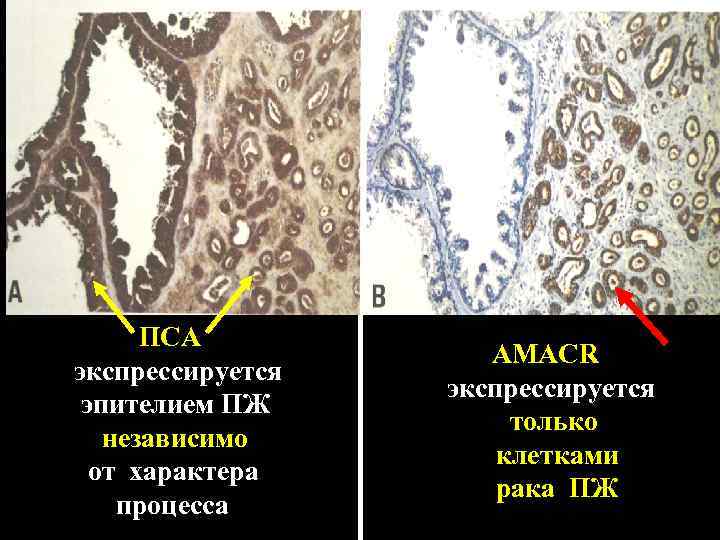
ПСА экспрессируется эпителием ПЖ независимо от характера процесса AMACR экспрессируется только клетками рака ПЖ

Методы лечения РПЖ • Выжидательная тактика • Радикальная простатэктомия (позадилонная, промежностная, лапароскопическая, робот-ассистированная) • Локальная деструкция опухоли • Лучевая терапия -- наружное облучение, кибер-нож, брахитерапия, системная лучевая терапия (метастрон, альфарадин) • Эндокринная терапия • Химиотерапия • Симптоматическое лечение

Главный фактор, определяющий тактику лечения РПЖ – стадия процесса (+ группа прогноза)

Локализованный – возможно излечение T 1 – T 2 N 0/XM 0/X Местнораспространенный T 3 -4 N 0/XM 0/X возможна длительная ремиссия (но не излечение) Диссеменированный Tлюбая N-1 M 0, N 0 M 1, N 1 M 1

Метод выбора лечения локализованного РПЖ – позадилонная радикальная простатэктомия (P. C. Walsh, 1983)

После РПЭ – диспансерное наблюдение Контроль PSA – 1 раз в 3 месяца в течение 3 -х лет PSA >0, 2 нг/мл “биохимический рецидив” Локальный рецидив Метастатическое Лимфатических узлов поражение скелета

Лечение «биохимических» рецидивов • Антиандрогенная терапия (антиандрогены, аналоги РГ-ЛГ, ингибиторы 5 -α-редуктазы) • «Спасительная» лучевая терапия (локальных рецидивов)
Лучевая терапия • Дистанционная (конвенциальная, 3 D-конформная, стереотаксическая) • Брахитерапия стандартная высокодозная промежностная параректальная • Брахитерапия + дистанционное облучение
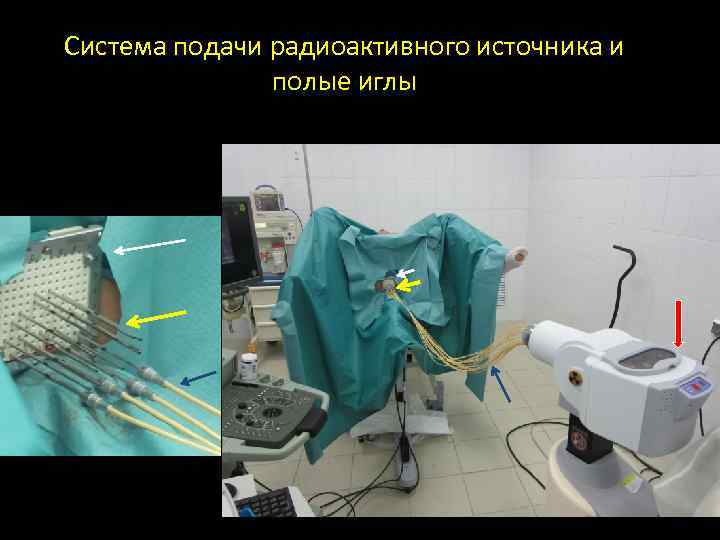
Система подачи радиоактивного источника и полые иглы

Технология КИБЕР – НОЖ (CYBER KNIFE)

Альтернативные методы лечения локализованного рака предстательной железы (локальная деструкция) • Криоабляция • Гипертермия • Лазеротерапия • Высокоинтенсивный сфокусированный ультразвук (HIFU – High-Intensity Focused Ultrasound)

…в Орловской, Костромской, Курской, Ивановской, Камчатской, Тверской, Владимирской, Тульской областях доля больных ранними стадиями НЕ превышала 20% от общего числа выявленных случаев рака простаты (Аксель Е. М. , 2005) В 2011 году опухоли III –IY стадии выявлены в 50% в среднем по России

• РПЖ --- одно из немногих онкологических заболеваний, при которых даже в IV стадии возможно получение глубокой и длительной ремиссии • НЕ оставляйте больного без специального лечения !!!

Чарлз Хаггинс создатель гормонотерапии рака человека (1901 -1998)
Цель эндокринной терапии РПЖ – устранение влияния андрогенов на предстательную железу Кастрация Антиандрогены (нарушение воздействия гормонов на ткань опухоли)
Кастрация хирургическая медикаментозная орхиэктомия энуклеация паренхимы яичек Аналоги (агонисты) и антагонисты РГ-ЛГ

Антиандрогены нарушают взаимодействие дигидротестостерона с рецепторами андрогенов в ядрах опухолевых клеток (действие на уровне органа -- мишени)
Антиандрогены нестероидные • Бикалутамид (касодекс) • Флутамид (флуцином) Ципротерона ацетат (андрокур)

Продолжительность и качество жизни больных РПЖ зависят от того, как долго удается сохранить способность опухоли реагировать на кастрацию (медикаментозную или хирургическую)

Кастрационно-резистентный РПЖ • Диагноз «кастрационно - резистентный рак предстательной железы» устанавливается при наличии роста уровня ПСА крови и/или каких-либо других признаков прогрессирования заболевания при адекватной андрогенной блокаде с подтвержденным достоверным кастрационным уровнем тестостерона.

Химиотерапевтические препараты для лечения РПЖ, резистентного к кастрации • митоксантрон + кортикостероиды • таксаны (доцетаксел, кабазитаксел)

В 2004 году профессор лондонского Института исследования рака Йоханн де Боно предположил, что резистентность опухоли к кастрации еще не означает ее резистентности к гормонам, в частности, к андрогенам, вырабатываемым непосредственно тканью предстательной железы. Это привело к разработке новых препаратов, эффективность которых в настоящее время можно считать доказанной. • Абиратерона ацетат (Zytiga) --- пероральный ингибитор синтеза андрогенов, селективно подавляющий активность фермента CYP – 17 • Энзалутамид ---ингибитор андрогенных рецепторов (MDV 3100) одобрен FDA в 2012 для пациентов, получавших доцетаксел

Иммунотерапия кастрационно – резистентного РПЖ • Сипулейцел – Т (Provenge) -- вакцина, приготовленная из собственных антигенпрезентирующих клеток пациента; разрешена для применения в США и Европе • Блокирование цитотоксического ассоциированного с Тлимфоцитами антигена-4 (CTLA-4) с целью активации опухолеспецифичных Т-клеток (человеческое моноклональное антитело --- ИПИЛИМУМАБ); находится на III стадии клинических испытаний.

Симптоматическая терапия РПЖ Боли в костях 1. Локальное облучение, внутривенное введение радионуклидных препаратов 2. Бисфосфонаты –золедроновая кислота 3. Таргетный препарат – деносумаб 4. Стероиды (преднизолон per os) 5. Анальгетики (нестероидные противовоспалительные препараты, наркотические анальгетики) Патологические переломы – хирургическая стабилизация

Симптоматическая терапия РПЖ Обструкция нижних мочевых путей 1. Гормональная терапия 2. α - адреноблокаторы 3. ТУР 4. Установка уретрального катетера 5. Эпицистостомия

Симптоматическая терапия РПЖ Обструкция мочеточников 1. Эндокринная терапия 2. Лучевая терапия 3. Перкутанная нефростомия 4. Установка уретерального стента

Симптоматическая терапия РПЖ Синдром сдавления спинного мозга 1. Стероиды (внутривенно или внутривенно + per os) 2. Задняя ламинэктомия 3. Лучевая терапия

Симптоматическая терапия РПЖ ДВС -- синдром Стандартная терапия ДВС – синдрома (введение гепарина, эпсилонаминокапроновой кислоты, переливание эритроцитарной массы, свежезамороженной плазмы и т. д. )

Симптоматическая терапия РПЖ Анемия 1. Препараты железа и витамины 2. Эритропоэтины 3. Трансфузионная терапия Joseph A. et al, 1999.

Симптоматическая терапия РПЖ Отеки 1. Тугое бинтование, эластические гольфы 2. Возвышенное положение нижних конечностей 3. Диуретики

Симптоматическая терапия

Опухоли яичка 1. Герминогенные: carcinoma in situ (cis) семинома «несеминомные» опухоли 2. Опухоли стромы полового тяжа: лейдигома сертолиома гранулёзоклеточная опухоль 3. Гонадобластома – клетки Сертоли + элементы семиномы + соединительная ткань 4. Аденокарцинома сети яичка 5. Вторичные опухоли яичка (при лимфомах, при раке лёгкого, раке почки, опухолях ЖКТ) 95%

Герминогенные опухоли яичка • Развиваются из семенного эпителия • В России - 0, 5% (в Западной Европе 1%-2%) злокачественных новообразований у мужчин • Преимущественный возраст 14 — 44 года • Есть тенденция к росту заболеваемости (в Европе и Северной Америке ~на 30% за 5 лет) • Частота полного излечения достигает 90% (благодаря появлению эффективных схем химиотерапии и усовершенствованию диагностики)

Диагностика часто несвоевременна На момент обращения к врачу: • процесс ограничен яичком ----- 40% • метастазы в забрюшинных лимфатических узлах ----- 40% • отдаленные метастазы ---- 20%

Причины поздней диагностики: • традиционное стремление скрывать изменения в области половых органов • отсутствие неприятных субъективных ощущений в ранних стадиях • низкий уровень санитарной культуры и невнимательное отношение к здоровью
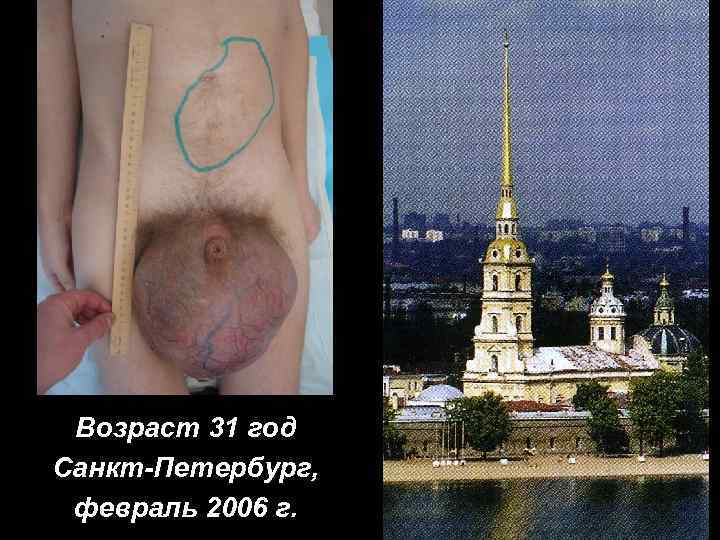
Возраст 31 год Санкт-Петербург, февраль 2006 г.

Опухоль яичка --редкое заболевание • Недостаточная осведомленность врачей общей практики, хирургов поликлиник, хирургов медицинских комиссий при военкоматах

Врач, прежде всего, думает о банальных процессах: • • Гидроцеле Гематоцеле Орхоэпидидимите Перекруте семенного канатика или придатка яичка • Поэтому часто не выполняются исследования, направленные на диагностику опухоли (УЗИ мошонки и забрюшинных лимфатических узлов, определение уровня опухолевых маркеров).

Эпидемиологические риска: факторы Крипторхизм Атрофия (гипотрофия) яичка (V≤ 12 мл) Синдром Клайнфельтера Новообразования яичка у кровных родственников (отца, братьев) • Опухоль противоположного яичка (в т. ч. Carcinoma in situ) • Бесплодие • •

Убедительно не доказана роль: • Травмы мошонки • Вирусного орхита после эпидемического паротита (эти факторы могут иметь значение как причина атрофии яичка) • Изучается этиологическая роль инфицирования вирусом иммунодефицита человека

Роль крипторхизма в патогенезе ГО яичка во многом остается неизученной • Врачи любой специальности, осуществляющие диспансеризацию мужской части населения, должны быть знакомы с онкологическими аспектами проблемы крипторхизма • В яичке, задержавшемся в паховом канале, ГО развивается ~ в 2% случаев • При внутрибрюшном крипторхизме ГО возникают значительно чаще, чем при паховом

Крипторхизм (продолжение) • Риск развития ГО яичка существенно уменьшается, если успешная орхипексия выполнена в возрасте до 11 лет • При неудачной операции показана повторная попытка низведения яичка или орхиэктомия Herrinton L. J. et al. , 2003

Крипторхизм (продолжение) • Если яичко расположено в паховом канале, легко доступно исследованию и сохранена его эндокринная функция допустимо ограничиться наблюдением • Если яичко находится в брюшной полости и не может быть подвергнуто адекватному исследованию или орхипексии, показана орхиэктомия Bosl G. J. et al. , 2005

Крипторхизм (продолжение) • При выявлении крипторхизма • у взрослых орхиэктомия рекомендуется как основной метод лечения во всех случаях, когда нет серьезных психологических или косметических препятствий Dominguez A. F. J. et al. , 2005

Революцию в лечении совершили: • Блеомицин • Этопозид • Препараты платины (цисплатин)

Пациенты молоды, не отягощены сопутствующей патологией --- могут переносить многократные курсы ПХТ в жестких режимах, дистанционную лучевую терапию, обширные хирургические вмешательства в забрюшинном пространстве

Актуальная проблема ! • Возможность иметь детей после завершения лечения • Восстановление сперматогенеза после окончания ХТ ~ у 50% больных • Индивидуальное предсказание несовершенно • Криопрезервация спермы должна стать стандартной процедурой у больных репродуктивного возраста Magelssen H. et al. , 2005

Magelssen H. и соавторы (2005) рекомендуют: • Консервацию 2 -3 образцов спермы, полученных в период между орхофуникулэктомией и началом лучевого или лекарственного лечения • Сперма замораживается с помощью жидкого азота • Для хранения ─ специально оборудованные банки • Использование: искусственное внутриматочное оплодотворение либо оплодотворение in vitro, либо интрацитоплазмаическое введение

Факторы риска развития герминогенных опухолей 1. Генетическая предрасположенность (для братьев пациентов вероятность заболевания увеличивается в 8— 10 раз) 2. Атрофия яичка (крипторхизм, травма, «идиопатическая» атрофия) 3. Воздействие эстрогенов ?

Доминирующая точка зрения: Все гистологические варианты герминогенных опухолей имеют единого предшественника ---- герминогенную внутрипротоковую неоплазию (carcinoma in situ) --- результат опухолевой трансформации сперматогенных клеток (гоноцитов)
Carcinoma in situ семинома «несеминомные опухоли» хориокарцинома Эмбриональная карцинома опухоль желточного мешка тератома

В диагностике, мониторинге эффективности лечения и уточнении прогноза герминогенных опухолей исключительно важную роль играют опухолевые маркеры: • Альфа-фетопротеин (АФП) • Бета-субъединица хорионического гонадотропина (β-ХГ) • Лактатдегидрогеназа (ЛДГ) (в основном, для прогнозирования течения) • Дополнительные маркеры ( «необязательные» ): NSE — нейронспецифическая энолаза и PLAP─плацентарная щелочная фосфатаза ─ имеют ограниченное значение при мониторинге больных чистой семиномой

Альфа-фетопротеин (АФП) • гликопротеин с молекулярной массой 70 к. Д • в норме секретируется желточным мешком, печенью и желудочно-кишечным трактом плода • в возрасте старше 1 года верхняя граница нормы концентрации АФП в сыворотке крови 15 нг/мл • уровень АФП повышается при ГО, содержащих элементы желточного мешка (эндодермального синуса) • повышение уровня АФП может иметь место, при гепатоцеллюлярном раке, опухолях желудка, желчного пузыря, поджелудочной железы, легких

Хорионический гонадотропин (ХГ) • гликопротеин с молекулярной массой 46 к. Д • состоит из двух субъединиц -- α и β (для диагностики важна β-субъединица ХГ (β-ХГ) • верхняя граница нормы в сыворотке крови взрослых мужчин <5 Ме/л (м. Ме/мл) у • в герминогенных опухолях синтезируется трофобластическими структурами • уровень ХГ может повышаться также при опухолях поджелудочной железы, печени, желудка, легких, молочной железы, почек

Лактатдегидрогеназа (ЛДГ) • фермент с молекулярной массой 134 к. Д • в большом количестве вырабатывается мышечной тканью • имеет 5 изомеров; ЛДГ-1─ изофермент, часто вырабатываемый опухолями яичка • в норме уровень ЛДГ 90— 280 МЕ/л • чувствительность и специфичность маркера при опухолях яичка НЕвысока • реальный признак опухоли яичка ─концентрация ЛДГ в сыворотке крови >2000 МЕ/л • используется, главным образом, как фактор прогноза (уровень ЛДГ пропорционален объему опухолевой ткани)

НЕ продуцируют АФП и ХГ: 1. Семиномы 2. Зрелые тератомы 3. Эмбриональные ( «чистого» типа) карциномы

• Чаще всего герминогенные опухоли имеют смешанное строение, т. е. содержат элементы различных гистологических типов. 80% герминогенных опухолей являются маркер -продуцирующими • Поэтому

Метастазирование герминогенных опухолей яичка • отмечается рано • преимущественно лимфогенное • чаще поражаются ипсилатеральные забрюшинные лимфоузлы • перекрёстное и билатеральное метастазирование чаще наблюдается при опухолях правого яичка • хориокарцинома гематогенно метастазирует

Из внутренних органов метастазами поражаются чаще всего лёгкие, печень, головной мозг, почки

Клиническая картина ГО яичка • Болей обычно НЕ бывает (в начальных стадиях) • Пальпаторно ─безболезненный участок • уплотнения ткани яичка В редких случаях упорные боли предшествуют пальпаторным изменениям и должны быть основанием для УЗИ Comiter C. V. et al. , 1995

По мере роста опухоли: • Асимметрия мошонки • Яичко и придаток сливаются в единый конгломерат • Опухолевая инфильтрация семенного канатика (утолщение и уплотнение) • Наличие гидроцеле НЕ исключает диагноза опухоли

УЗИ мошонки • Датчик с частотой 7, 5 MHz • Опухоль представлена одним или несколькими ГИПОЭХОГЕННЫМИ ОЧАГАМИ • Размеры опухоли ─ от 2 -3 мм до 10 см и > • Чувствительность УЗИ в распознавании тестикулярных опухолей приближается к 100%

Выполнение УЗИ яичек обязательно, если у молодого мужчины выявлены: • признаки забрюшинной опухоли, метастазы во внутренних органах, • повышенный уровень β-ХГ и/или АФП Albers P. et al. , 2005

МРТ мошонки • Чувствительность и специфичность при опухолях яичка ─ 95 -100% • Широкое практическое использование метода вряд ли оправдано из-за высокой стоимости

Стадирование (в упрощенном виде) • I стадия---процесс ограничен мошонкой • II стадия—процесс ограничен лимфоузлами забрюшинного пространства • III стадия---вовлечение лимфоузлов выше диафрагмы или внутренних органов или значительное повышение уровня маркеров

IY стадии для опухолей яичка НЕ существует !!! Только семинома чувствительна к лучевой терапии !!! Первый этап лечения --- хирургическое удаление яичка и его придатка с пересечением семенного канатика на уровне внутреннего отверстия пахового канала. После уточнения гистологической структуры опухоли и стадии заболевания ---- химиотерапия и/или лучевое лечение. При наличии остаточных ( «резидуальных» ) опухолевых масс ---- забрюшинная лимфаденэктомия (+ удаление отдаленных метастазов)
ВОП.pptx