Лекции по оптике для ИМ 4.ppt
- Количество слайдов: 69
 Волновые свойства микрочастиц
Волновые свойства микрочастиц
 Двойственность в природе света n Корпускулярно-волновой дуализм в свойствах света выражают уравнения А. Эйнштейна:
Двойственность в природе света n Корпускулярно-волновой дуализм в свойствах света выражают уравнения А. Эйнштейна:
 n 1923 г. – гипотеза о волновых свойствах микрочастиц (Л. Де Бройль). λ – длина волны де Бройля, m - масса частицы, V - ее скорость. Л. де Бройль (1892 -1987, фр. ) ЛНП 1929 г.
n 1923 г. – гипотеза о волновых свойствах микрочастиц (Л. Де Бройль). λ – длина волны де Бройля, m - масса частицы, V - ее скорость. Л. де Бройль (1892 -1987, фр. ) ЛНП 1929 г.
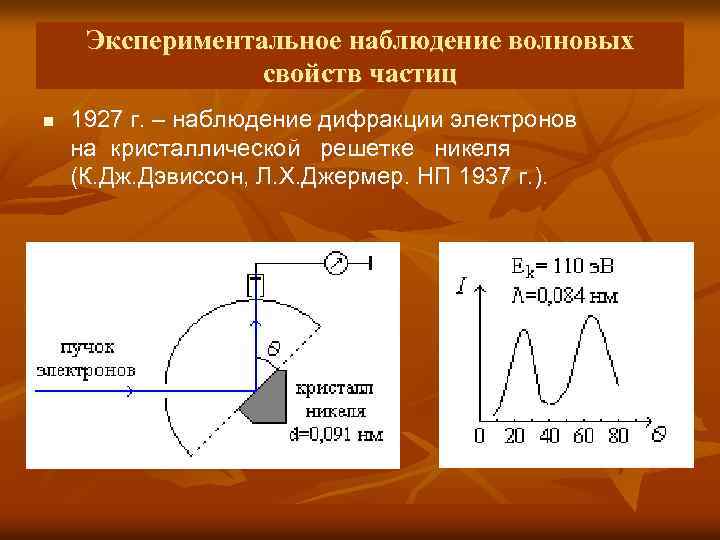 Экспериментальное наблюдение волновых свойств частиц n 1927 г. – наблюдение дифракции электронов на кристаллической решетке никеля (К. Дж. Дэвиссон, Л. Х. Джермер. НП 1937 г. ).
Экспериментальное наблюдение волновых свойств частиц n 1927 г. – наблюдение дифракции электронов на кристаллической решетке никеля (К. Дж. Дэвиссон, Л. Х. Джермер. НП 1937 г. ).
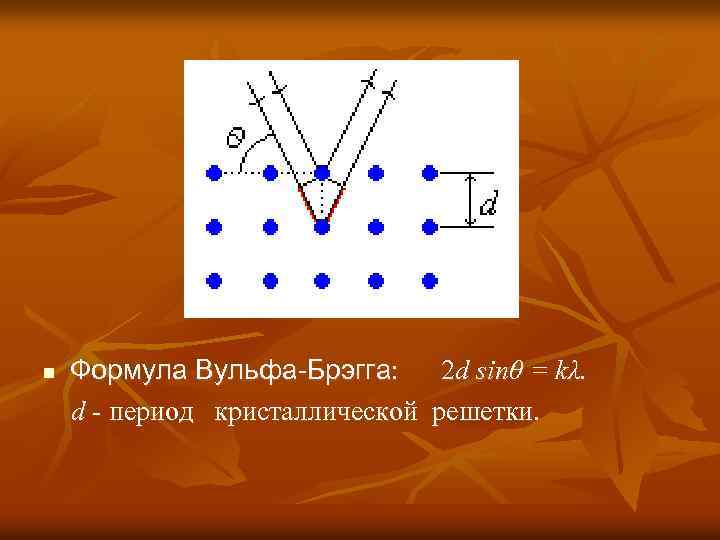 n Формула Вульфа-Брэгга: d - период кристаллической 2 d sinθ = kλ. решетки.
n Формула Вульфа-Брэгга: d - период кристаллической 2 d sinθ = kλ. решетки.
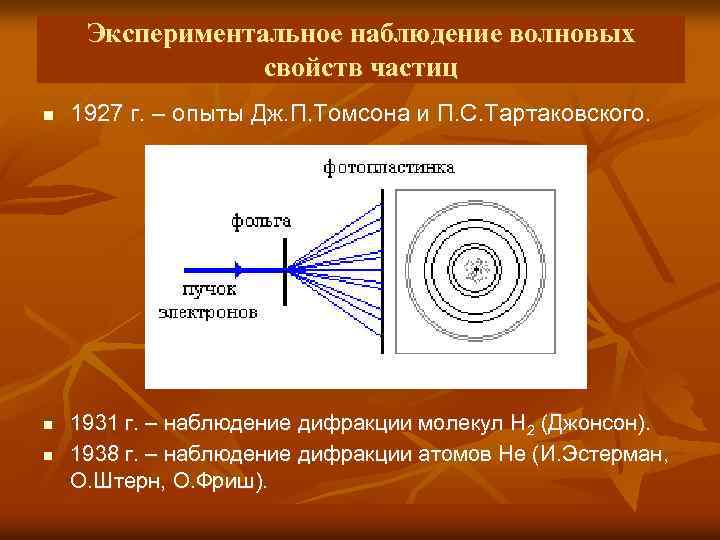 Экспериментальное наблюдение волновых свойств частиц n n n 1927 г. – опыты Дж. П. Томсона и П. С. Тартаковского. 1931 г. – наблюдение дифракции молекул Н 2 (Джонсон). 1938 г. – наблюдение дифракции атомов Не (И. Эстерман, О. Штерн, О. Фриш).
Экспериментальное наблюдение волновых свойств частиц n n n 1927 г. – опыты Дж. П. Томсона и П. С. Тартаковского. 1931 г. – наблюдение дифракции молекул Н 2 (Джонсон). 1938 г. – наблюдение дифракции атомов Не (И. Эстерман, О. Штерн, О. Фриш).
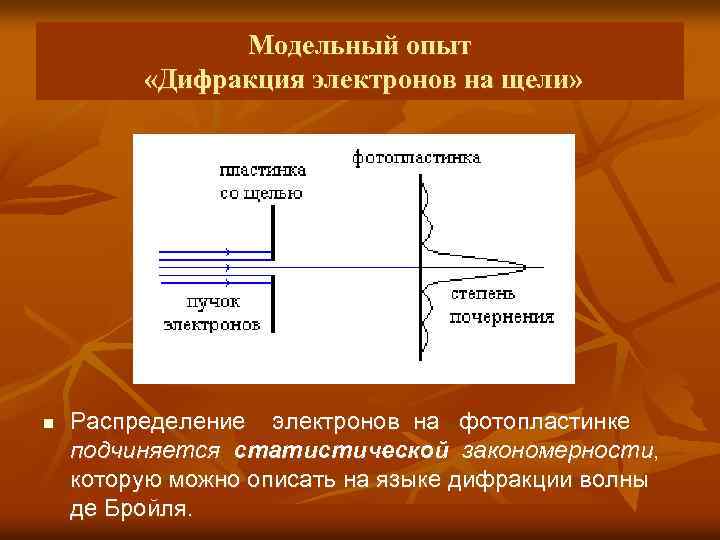 Модельный опыт «Дифракция электронов на щели» n Распределение электронов на фотопластинке подчиняется статистической закономерности, которую можно описать на языке дифракции волны де Бройля.
Модельный опыт «Дифракция электронов на щели» n Распределение электронов на фотопластинке подчиняется статистической закономерности, которую можно описать на языке дифракции волны де Бройля.
 n n Волновые свойства микрочастиц проявляются в их вероятностном, статистическом поведении, которое можно описать на языке волн – волн де Бройля. Свободно движущейся частице, имеющей энергию Е и импульс р, соответствует волна де Бройля, уравнение которой имеет вид: На рисунке приведен график этой функции для фиксированного момента времени.
n n Волновые свойства микрочастиц проявляются в их вероятностном, статистическом поведении, которое можно описать на языке волн – волн де Бройля. Свободно движущейся частице, имеющей энергию Е и импульс р, соответствует волна де Бройля, уравнение которой имеет вид: На рисунке приведен график этой функции для фиксированного момента времени.
 Стационарное уравнение Шредингера
Стационарное уравнение Шредингера
 n n Состояние частицы, совершающей движение в трехмерном пространстве описывается волновой функцией, зависящей от координат x, y, z и времени t. Квадрат модуля волновой функции в произвольной точке пространства определяет объемную плотность вероятности нахождения частицы в этой точке в соответствующий момент времени. Т. о. , вероятность нахождения частицы в элементарном объеме d. V = dx·dy·dz дается выражением:
n n Состояние частицы, совершающей движение в трехмерном пространстве описывается волновой функцией, зависящей от координат x, y, z и времени t. Квадрат модуля волновой функции в произвольной точке пространства определяет объемную плотность вероятности нахождения частицы в этой точке в соответствующий момент времени. Т. о. , вероятность нахождения частицы в элементарном объеме d. V = dx·dy·dz дается выражением:
 n n В стационарных состояниях частицы плотность вероятности ее нахождения во всех точках пространства от времени не зависит (зависит от координат!). Если частица находится в силовом поле, в котором ее потенциальная энергия описывается функцией U(x, y, z), то вид волновой функции и полную энергию Е частицы в стационарных состояниях находят путем решения уравнения Шредингера:
n n В стационарных состояниях частицы плотность вероятности ее нахождения во всех точках пространства от времени не зависит (зависит от координат!). Если частица находится в силовом поле, в котором ее потенциальная энергия описывается функцией U(x, y, z), то вид волновой функции и полную энергию Е частицы в стационарных состояниях находят путем решения уравнения Шредингера:
 n В 1926 г. Э. Шредингер разработал теорию движения микрочастиц – волновую механику, в основу которой положил уравнение, играющее в атомных процессах такую же роль, как законы Ньютона в классической механике и ввел для описания состояния микрообъекта волновую функцию, или Ψ-функцию. Э. Шредингер (1887 -1961, австр. ) ЛНП 1932 г.
n В 1926 г. Э. Шредингер разработал теорию движения микрочастиц – волновую механику, в основу которой положил уравнение, играющее в атомных процессах такую же роль, как законы Ньютона в классической механике и ввел для описания состояния микрообъекта волновую функцию, или Ψ-функцию. Э. Шредингер (1887 -1961, австр. ) ЛНП 1932 г.
 Частица в потенциальном ящике n Модель одномерного потенциального ящика: в интервале х от 0 до а потенциальная энергия частицы постоянна, вне этого интервала обращается в бесконечность. Внутри ящика силы на частицу не действуют. В точках х=0 и х=а на частицу действуют бесконечно большие возвращающие силы. (Локализованная частица: шарик между двумя упругими стенками). По классической механике кинетическая (и полная) энергия частицы может быть любой; вероятность ее нахождения во всех точках внутри ящика одинакова.
Частица в потенциальном ящике n Модель одномерного потенциального ящика: в интервале х от 0 до а потенциальная энергия частицы постоянна, вне этого интервала обращается в бесконечность. Внутри ящика силы на частицу не действуют. В точках х=0 и х=а на частицу действуют бесконечно большие возвращающие силы. (Локализованная частица: шарик между двумя упругими стенками). По классической механике кинетическая (и полная) энергия частицы может быть любой; вероятность ее нахождения во всех точках внутри ящика одинакова.
 n Решение задачи о состояниях частицы в ящике на основе уравнения Шредингера приводит к принципиально другим результатам: Полная энергия частицы квантуется: n = 1, 2, 3, … квантовое число. n n Волновая функция в n-м квантовом состоянии имеет вид: Вероятность нахождения частицы в разных точках внутри ящика различна.
n Решение задачи о состояниях частицы в ящике на основе уравнения Шредингера приводит к принципиально другим результатам: Полная энергия частицы квантуется: n = 1, 2, 3, … квантовое число. n n Волновая функция в n-м квантовом состоянии имеет вид: Вероятность нахождения частицы в разных точках внутри ящика различна.
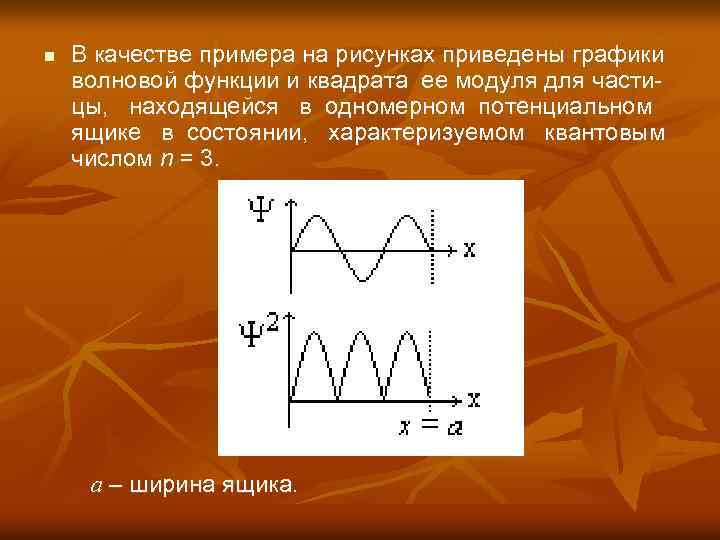 n В качестве примера на рисунках приведены графики волновой функции и квадрата ее модуля для частицы, находящейся в одномерном потенциальном ящике в состоянии, характеризуемом квантовым числом n = 3. а – ширина ящика.
n В качестве примера на рисунках приведены графики волновой функции и квадрата ее модуля для частицы, находящейся в одномерном потенциальном ящике в состоянии, характеризуемом квантовым числом n = 3. а – ширина ящика.
 Соотношение неопределенностей Гейзенберга
Соотношение неопределенностей Гейзенберга
 Соотношение неопределенностей Гейзенберга n В. Гейзенберг (1901 -1976, нем) ЛНП 1932 г. Не существует таких состояний микрочастицы, в которых координата и соответствующая проекция импульса имели бы одновременно определенные значения. При этом их неопределенности связаны соотношением:
Соотношение неопределенностей Гейзенберга n В. Гейзенберг (1901 -1976, нем) ЛНП 1932 г. Не существует таких состояний микрочастицы, в которых координата и соответствующая проекция импульса имели бы одновременно определенные значения. При этом их неопределенности связаны соотношением:
 Следствия из соотношения неопределенностей n n Состояние покоя микрочастицы (характеризуемое определенным значением координаты) в природе не реализуется. Невозможно реализовать такой эксперимент, который бы позволил одновременно измерить координату и сопряженную проекцию импульса микрочастицы.
Следствия из соотношения неопределенностей n n Состояние покоя микрочастицы (характеризуемое определенным значением координаты) в природе не реализуется. Невозможно реализовать такой эксперимент, который бы позволил одновременно измерить координату и сопряженную проекцию импульса микрочастицы.
 Пример применения соотношения неопределенностей n Оценим кинетическую энергию Ek нуклона в ядре атома, учитывая, что линейные размеры ядра (r ≈ 3· 10 -15 м) могут служить оценкой неопределенности в координате нуклона: Δx ≈ r. Соответствующую неопределенность импульса нуклона найдем из соотношения Гейзенберга: Тогда для Ek получим:
Пример применения соотношения неопределенностей n Оценим кинетическую энергию Ek нуклона в ядре атома, учитывая, что линейные размеры ядра (r ≈ 3· 10 -15 м) могут служить оценкой неопределенности в координате нуклона: Δx ≈ r. Соответствующую неопределенность импульса нуклона найдем из соотношения Гейзенберга: Тогда для Ek получим:
 Соотношение неопределенностей для энергии и времени Δt – время жизни микрочастицы в квантовом состоянии; ΔE – неопределенность энергии частицы в этом состоянии.
Соотношение неопределенностей для энергии и времени Δt – время жизни микрочастицы в квантовом состоянии; ΔE – неопределенность энергии частицы в этом состоянии.
 АТОМ ВОДОРОДА в квантовой механике
АТОМ ВОДОРОДА в квантовой механике
 n n В квантовой механике решение задачи о состояниях атома водорода проводится на основе стационарного уравнения Шредингера. Оно приводит к следующим результатам: Квантовое состояние электрона в атоме, задается набором из трех квантовых чисел – n, l и m:
n n В квантовой механике решение задачи о состояниях атома водорода проводится на основе стационарного уравнения Шредингера. Оно приводит к следующим результатам: Квантовое состояние электрона в атоме, задается набором из трех квантовых чисел – n, l и m:
 n n = 1, 2, 3, … - главное квантовое число; l = 0, 1, 2, … (n-1) – орбитальное квантовое число; m = 0, ± 1, ± 2, … ± l - магнитное квантовое число (всего 2 l +1 значений). Разным наборам этих квантовых чисел соответствуют отличающиеся друг от друга волновые функции: (r, θ, φ – полярные координаты точки). Т. о. , от набора квантовых чисел зависит форма электронного облака - |ψnlm(r, θ, φ)|2.
n n = 1, 2, 3, … - главное квантовое число; l = 0, 1, 2, … (n-1) – орбитальное квантовое число; m = 0, ± 1, ± 2, … ± l - магнитное квантовое число (всего 2 l +1 значений). Разным наборам этих квантовых чисел соответствуют отличающиеся друг от друга волновые функции: (r, θ, φ – полярные координаты точки). Т. о. , от набора квантовых чисел зависит форма электронного облака - |ψnlm(r, θ, φ)|2.
 n Главное квантовое число n определяет энергию электрона в стационарном состоянии атома: (Это выражение совпадает с формулой, полученной в теории Бора). n С ростом n растет энергия атома и увеличиваются размеры электронного облака.
n Главное квантовое число n определяет энергию электрона в стационарном состоянии атома: (Это выражение совпадает с формулой, полученной в теории Бора). n С ростом n растет энергия атома и увеличиваются размеры электронного облака.
 n Орбитальное квантовое число l определяет момент импульса электрона в стационарном состоянии и орбитальный магнитный момент: (В теории Бора где n = 1, 2, 3, …).
n Орбитальное квантовое число l определяет момент импульса электрона в стационарном состоянии и орбитальный магнитный момент: (В теории Бора где n = 1, 2, 3, …).
 n Используется буквенная индексация состояний: l 0 L 0 Инд. s 1 2 3 p d f
n Используется буквенная индексация состояний: l 0 L 0 Инд. s 1 2 3 p d f
 n Магнитное квантовое число определяет проекцию момента импульса на физически выделенное направление в пространстве (как правило, на направление магнитного поля): m = 0, ± 1, ± 2, ± 3, … ±l. На рисунке показаны возможные ориентации вектора L при l=2.
n Магнитное квантовое число определяет проекцию момента импульса на физически выделенное направление в пространстве (как правило, на направление магнитного поля): m = 0, ± 1, ± 2, ± 3, … ±l. На рисунке показаны возможные ориентации вектора L при l=2.
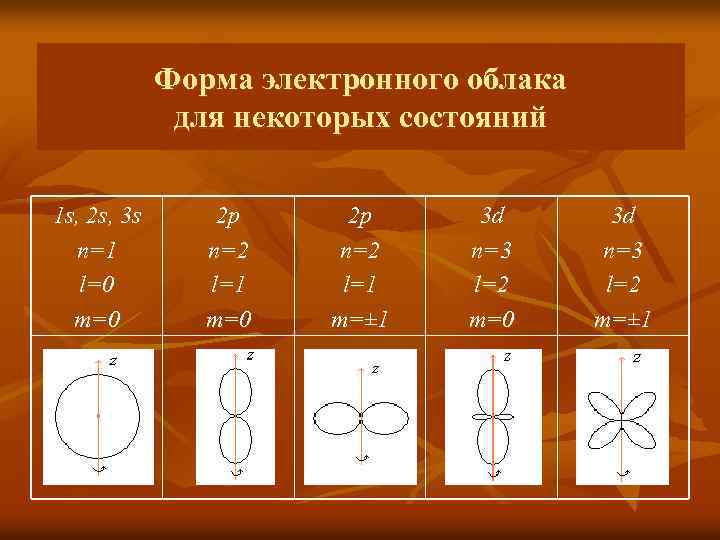 Форма электронного облака для некоторых состояний 1 s, 2 s, 3 s n=1 l=0 m=0 2 p n=2 l=1 m=± 1 3 d n=3 l=2 m=0 3 d n=3 l=2 m=± 1
Форма электронного облака для некоторых состояний 1 s, 2 s, 3 s n=1 l=0 m=0 2 p n=2 l=1 m=± 1 3 d n=3 l=2 m=0 3 d n=3 l=2 m=± 1
 n n Некоторым квантовым состояниям электрона в атоме (c отличающимися волновыми функциями) соответствует одно и то же значение энергии En. (Форма электронного облака разная, а энергия состояния одна и та же). В таком случае говорят о вырождении квантовых состояний. Количество волновых функций, соответствующих одной и той же энергии, определяет кратность вырождения N. Так, значению n=2 (En=-3, 4 э. В) соответствуют четыре состояния: 1) l=0, m=0; 2) l=1, m=0; 3) l=1, m =+1; 4) l=1, m=-1. В общем случае N = n 2.
n n Некоторым квантовым состояниям электрона в атоме (c отличающимися волновыми функциями) соответствует одно и то же значение энергии En. (Форма электронного облака разная, а энергия состояния одна и та же). В таком случае говорят о вырождении квантовых состояний. Количество волновых функций, соответствующих одной и той же энергии, определяет кратность вырождения N. Так, значению n=2 (En=-3, 4 э. В) соответствуют четыре состояния: 1) l=0, m=0; 2) l=1, m=0; 3) l=1, m =+1; 4) l=1, m=-1. В общем случае N = n 2.
 Спин электрона n n В 1922 г. установлено, что пучок атомов, находящихся в s-состоянии (когда орбитальный магнитный момент атома равен нулю), при прохождении через неоднородное магнитное поле расщепляется на два пучка. (О. Штерн, В. Герлах). В спектрах излучения атомов некоторые линии расщеплены на две близкие компоненты. (Например, в спектре атомов ртути наблюдается желтый дублет).
Спин электрона n n В 1922 г. установлено, что пучок атомов, находящихся в s-состоянии (когда орбитальный магнитный момент атома равен нулю), при прохождении через неоднородное магнитное поле расщепляется на два пучка. (О. Штерн, В. Герлах). В спектрах излучения атомов некоторые линии расщеплены на две близкие компоненты. (Например, в спектре атомов ртути наблюдается желтый дублет).
 n Анализ экспериментальных результатов привел к выводу о существовании у электрона собственного момента импульса – спина и соответствующего ему собственного магнитного момента (Д. Уленбек, С. Гаудсмит, 1925 г. ): n s = ½ - спиновое квантовое число. Возможны лишь две проекции спина на направление внешнего поля: n ms = ±½ – магнитное квантовое число для спина.
n Анализ экспериментальных результатов привел к выводу о существовании у электрона собственного момента импульса – спина и соответствующего ему собственного магнитного момента (Д. Уленбек, С. Гаудсмит, 1925 г. ): n s = ½ - спиновое квантовое число. Возможны лишь две проекции спина на направление внешнего поля: n ms = ±½ – магнитное квантовое число для спина.
 n n Таким образом, состояние электрона в атоме водорода характеризуется набором из четырех квантовых чисел: n = 1, 2, 3, … - главное квантовое число; l = 0, 1, 2, … (n-1) – орбитальное квантовое число; m = 0, ± 1, ± 2, … ± l - магнитное квантовое число; ms = ± 1/2 – магнитное квантовое число для спина. С учетом спина кратность вырождения состояний атома по энергии N = 2 n 2.
n n Таким образом, состояние электрона в атоме водорода характеризуется набором из четырех квантовых чисел: n = 1, 2, 3, … - главное квантовое число; l = 0, 1, 2, … (n-1) – орбитальное квантовое число; m = 0, ± 1, ± 2, … ± l - магнитное квантовое число; ms = ± 1/2 – магнитное квантовое число для спина. С учетом спина кратность вырождения состояний атома по энергии N = 2 n 2.
 многоэлектронный АТОМ
многоэлектронный АТОМ
 n Ядро атома химического элемента, имеющего номер Z в Периодической таблице, имеет заряд, равный Zе. Кулоновская сила взаимодействия электрона с ядром в Z раз больше, чем в атоме водорода. По теории Бора радиусы стационарных орбит в этом случае (без учета взаимодействия электронов между собой) будут в Z раз меньше:
n Ядро атома химического элемента, имеющего номер Z в Периодической таблице, имеет заряд, равный Zе. Кулоновская сила взаимодействия электрона с ядром в Z раз больше, чем в атоме водорода. По теории Бора радиусы стационарных орбит в этом случае (без учета взаимодействия электронов между собой) будут в Z раз меньше:
 n n Общего решения задачи о состояниях многоэлектронного атома в квантовой механике не существует. Трудно учесть в уравнении Шредингера взаимодействие электронов между собой. В грубом приближении полагают, что энергия взаимодействия электронов друг с другом много меньше суммарной энергии их взаимодействия с ядром. В таком случае состояние каждого отдельного электрона будет водородоподобным, и будет описываться набором из четырех квантовых чисел:
n n Общего решения задачи о состояниях многоэлектронного атома в квантовой механике не существует. Трудно учесть в уравнении Шредингера взаимодействие электронов между собой. В грубом приближении полагают, что энергия взаимодействия электронов друг с другом много меньше суммарной энергии их взаимодействия с ядром. В таком случае состояние каждого отдельного электрона будет водородоподобным, и будет описываться набором из четырех квантовых чисел:
 n = 1, 2, 3, … - главное квантовое число: l = 0, 1, 2, … (n-1) – орбитальное квантовое число: m = 0, ± 1, ± 2, … ± l - магнитное квантовое число: ms = ± 1/2 – магнитное квантовое число для спина:
n = 1, 2, 3, … - главное квантовое число: l = 0, 1, 2, … (n-1) – орбитальное квантовое число: m = 0, ± 1, ± 2, … ± l - магнитное квантовое число: ms = ± 1/2 – магнитное квантовое число для спина:
 n n n При этом наиболее вероятное расстояние электрона от ядра в некотором состоянии в Z раз меньше, чем в атоме водорода. Энергетическому уровню с номером n соответствуют 2 n 2 состояний, отличающихся набором квантовых чисел l, m и ms. Распределение электронов по квантовым состояниям в атоме происходит в соответствии с двумя принципами: 1. Принцип Паули: в состоянии, характеризуемом определенным набором квантовых чисел n, l, m и ms может находиться только один электрон.
n n n При этом наиболее вероятное расстояние электрона от ядра в некотором состоянии в Z раз меньше, чем в атоме водорода. Энергетическому уровню с номером n соответствуют 2 n 2 состояний, отличающихся набором квантовых чисел l, m и ms. Распределение электронов по квантовым состояниям в атоме происходит в соответствии с двумя принципами: 1. Принцип Паули: в состоянии, характеризуемом определенным набором квантовых чисел n, l, m и ms может находиться только один электрон.
 2. Принцип минимума энергии: прежде всего заполняются те свободные состояния в атоме, в которых энергия электрона меньше. n В соответствии с принципом Паули в n–ом энергетическом состоянии атома могут находиться 2 n 2 электронов. Говорят, что эти электроны образуют оболочку атома, или электронный слой. Оболочкам присваиваются буквенные символы.
2. Принцип минимума энергии: прежде всего заполняются те свободные состояния в атоме, в которых энергия электрона меньше. n В соответствии с принципом Паули в n–ом энергетическом состоянии атома могут находиться 2 n 2 электронов. Говорят, что эти электроны образуют оболочку атома, или электронный слой. Оболочкам присваиваются буквенные символы.
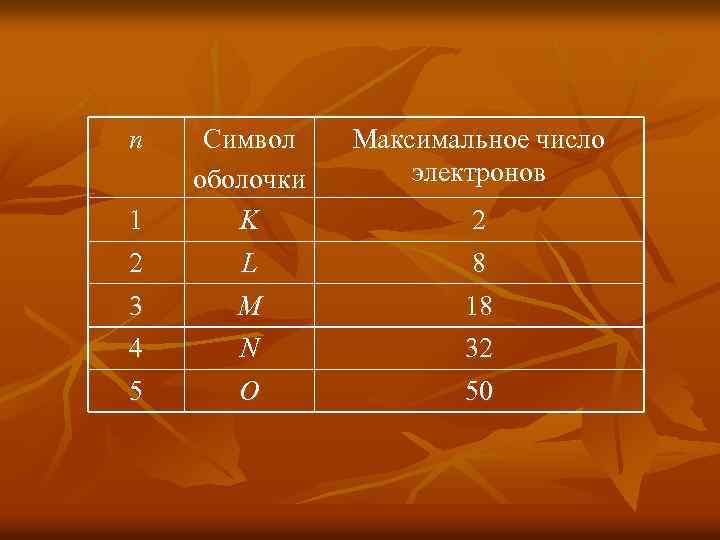 n Максимальное число электронов 1 2 Символ оболочки K L 3 4 M N 18 32 5 O 50 2 8
n Максимальное число электронов 1 2 Символ оболочки K L 3 4 M N 18 32 5 O 50 2 8
 n n Электроны, занимающие состояния с определенным значением орбитального квантового числа l, образуют в электронном слое подоболочку. Количество подоболочек в слое равно n, поскольку l принимает значения от 0 до n-1. Максимальное число электронов в подоболочке равно 2(2 l +1). Подоболочкам присваиваются те же символы, что и для соответствующих состояний атома водорода.
n n Электроны, занимающие состояния с определенным значением орбитального квантового числа l, образуют в электронном слое подоболочку. Количество подоболочек в слое равно n, поскольку l принимает значения от 0 до n-1. Максимальное число электронов в подоболочке равно 2(2 l +1). Подоболочкам присваиваются те же символы, что и для соответствующих состояний атома водорода.
 l Максимальное число электронов 0 1 Символ подобол. s p 2 3 d f 10 14 2 6
l Максимальное число электронов 0 1 Символ подобол. s p 2 3 d f 10 14 2 6
 Электронная конфигурация для атомов некоторых химических элементов n n n n n H He Li Be B C N O F Ne 1 s 1 1 s 22 s 22 p 1 1 s 22 p 2 1 s 22 p 3 1 s 22 p 4 1 s 22 p 5 1 s 22 p 6 n n n Na Mg Al 1 s 22 p 63 s 1 1 s 22 s 22 p 63 s 23 p 1 Последовательность заполнения состояний нарушается, начиная с 19 -го химич. элемента – калия: n K 1 s 22 p 63 s 23 p 64 s 04 p 1 n Ca 1 s 22 p 63 s 23 p 64 s 04 p 2
Электронная конфигурация для атомов некоторых химических элементов n n n n n H He Li Be B C N O F Ne 1 s 1 1 s 22 s 22 p 1 1 s 22 p 2 1 s 22 p 3 1 s 22 p 4 1 s 22 p 5 1 s 22 p 6 n n n Na Mg Al 1 s 22 p 63 s 1 1 s 22 s 22 p 63 s 23 p 1 Последовательность заполнения состояний нарушается, начиная с 19 -го химич. элемента – калия: n K 1 s 22 p 63 s 23 p 64 s 04 p 1 n Ca 1 s 22 p 63 s 23 p 64 s 04 p 2
 n n Периодичность в химических свойствах элементов связана с повторяемостью в структуре внешних оболочек у атомов родственных элементов. Квантовая механика показала, что валентность химического элемента определяется числом неспаренных спинов электронов во внешней оболочке соответствующего атома.
n n Периодичность в химических свойствах элементов связана с повторяемостью в структуре внешних оболочек у атомов родственных элементов. Квантовая механика показала, что валентность химического элемента определяется числом неспаренных спинов электронов во внешней оболочке соответствующего атома.
 Основные свойства и строение ядра атома
Основные свойства и строение ядра атома
 n Эрнест Резерфорд (1871 -1937, англ. ) В 1919 г. Э. Резерфорд осуществил первую искусственную ядерную реакцию: при облучении α -частицами азот превращался в кислород. В качестве второго продукта в этой реакции был зарегистрирован протон:
n Эрнест Резерфорд (1871 -1937, англ. ) В 1919 г. Э. Резерфорд осуществил первую искусственную ядерную реакцию: при облучении α -частицами азот превращался в кислород. В качестве второго продукта в этой реакции был зарегистрирован протон:
 n Джеймс Чэдвик (1891 -1974, англ. ) ЛНП 1935 г. В 1932 г. Дж. Чэдвик, исследуя излучение, возникающее при облучении бериллия αчастицами, показал, что оно является потоком электрически нейтральных частиц – нейтронов.
n Джеймс Чэдвик (1891 -1974, англ. ) ЛНП 1935 г. В 1932 г. Дж. Чэдвик, исследуя излучение, возникающее при облучении бериллия αчастицами, показал, что оно является потоком электрически нейтральных частиц – нейтронов.
 Дефект массы и энергия связи ядра n Масса ядра меньше, чем сумма масс составляющих его нуклонов. Дефект массы Δm = (Zmp + Nmn) – mя.
Дефект массы и энергия связи ядра n Масса ядра меньше, чем сумма масс составляющих его нуклонов. Дефект массы Δm = (Zmp + Nmn) – mя.
 Дефект массы и энергия связи ядра n Масса ядра меньше, чем сумма масс составляющих его нуклонов. Дефект массы Δm = (Zmp + Nmn) – mя. n В соответствии с законом взаимосвязи между массой и энергией, величина Δm·с2 выражает энергию, выделяющуюся при слиянии нуклонов в ядро. Для разделения ядра на составные части необходимо затратить такое же количество энергии. Таким образом, энергия связи ядра Eсв= Δm·с2.
Дефект массы и энергия связи ядра n Масса ядра меньше, чем сумма масс составляющих его нуклонов. Дефект массы Δm = (Zmp + Nmn) – mя. n В соответствии с законом взаимосвязи между массой и энергией, величина Δm·с2 выражает энергию, выделяющуюся при слиянии нуклонов в ядро. Для разделения ядра на составные части необходимо затратить такое же количество энергии. Таким образом, энергия связи ядра Eсв= Δm·с2.
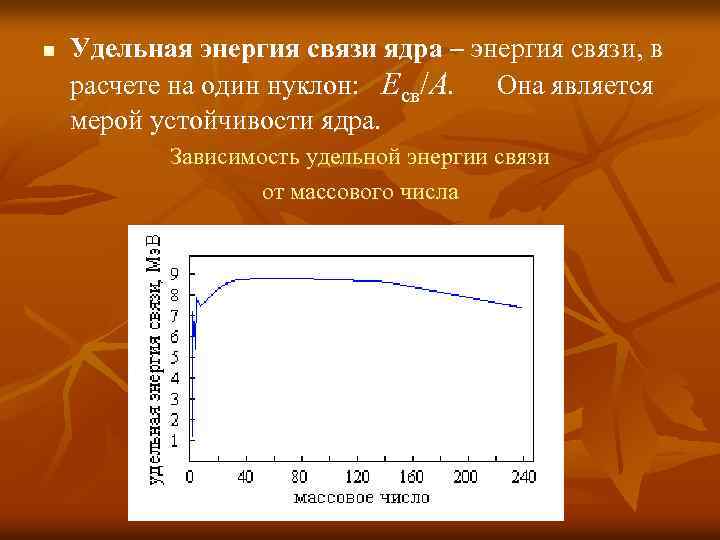 n Удельная энергия связи ядра – энергия связи, в расчете на один нуклон: Eсв/A. Она является мерой устойчивости ядра. Зависимость удельной энергии связи от массового числа
n Удельная энергия связи ядра – энергия связи, в расчете на один нуклон: Eсв/A. Она является мерой устойчивости ядра. Зависимость удельной энергии связи от массового числа
 Ядерные силы n n v v Ядерные силы намного превышают гравитационные и электромагнитные взаимодействия и не сводятся к ним. Они относятся к классу сильных взаимодействий. Свойства ядерных сил: это силы притяжения; они являются короткодействующими (r ≈10 -15 м); обладают свойством зарядовой независимости; обладают свойством насыщения: каждый нуклон взаимодействует с ограниченным числом ближайших соседей.
Ядерные силы n n v v Ядерные силы намного превышают гравитационные и электромагнитные взаимодействия и не сводятся к ним. Они относятся к классу сильных взаимодействий. Свойства ядерных сил: это силы притяжения; они являются короткодействующими (r ≈10 -15 м); обладают свойством зарядовой независимости; обладают свойством насыщения: каждый нуклон взаимодействует с ограниченным числом ближайших соседей.
 Реакции деления и синтеза ядер. Ядерная энергетика
Реакции деления и синтеза ядер. Ядерная энергетика
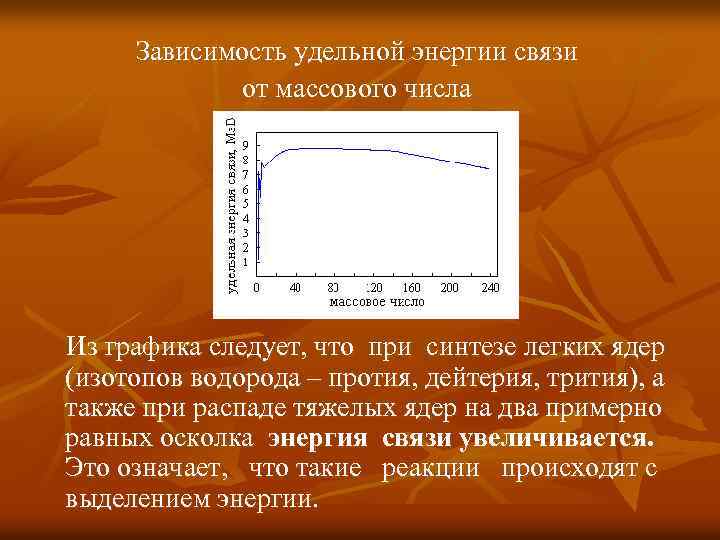 Зависимость удельной энергии связи от массового числа Из графика следует, что при синтезе легких ядер (изотопов водорода – протия, дейтерия, трития), а также при распаде тяжелых ядер на два примерно равных осколка энергия связи увеличивается. Это означает, что такие реакции происходят с выделением энергии.
Зависимость удельной энергии связи от массового числа Из графика следует, что при синтезе легких ядер (изотопов водорода – протия, дейтерия, трития), а также при распаде тяжелых ядер на два примерно равных осколка энергия связи увеличивается. Это означает, что такие реакции происходят с выделением энергии.
 Реакции деления ядер n В конце 30 -х годов ХХ века было установлено, что при облучении урана нейтронами образуются элементы из середины периодической системы – лантан и барий ( Э. Ферми, О, Ган, Ф. Штрассман, О. Фриш, Л. Мейтнер, Г. Н. Флеров, К. Н. Петржак). Q≈200 Мэ. В! (При химич. реакции горения Q≈4 э. В).
Реакции деления ядер n В конце 30 -х годов ХХ века было установлено, что при облучении урана нейтронами образуются элементы из середины периодической системы – лантан и барий ( Э. Ферми, О, Ган, Ф. Штрассман, О. Фриш, Л. Мейтнер, Г. Н. Флеров, К. Н. Петржак). Q≈200 Мэ. В! (При химич. реакции горения Q≈4 э. В).
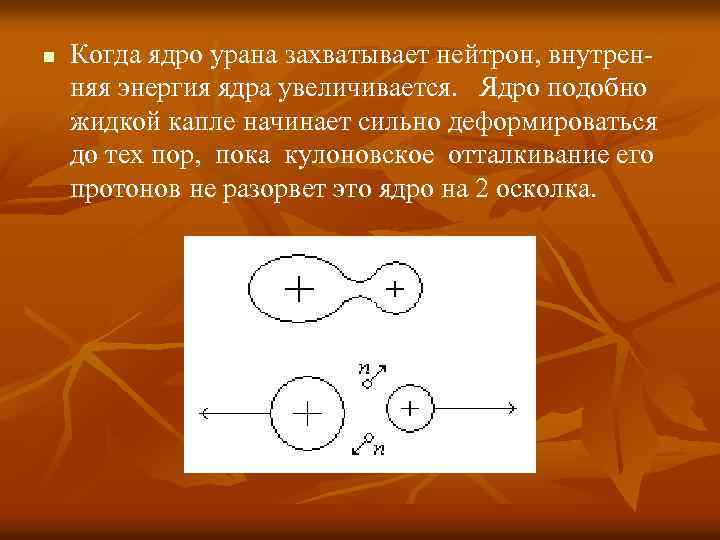 n Когда ядро урана захватывает нейтрон, внутренняя энергия ядра увеличивается. Ядро подобно жидкой капле начинает сильно деформироваться до тех пор, пока кулоновское отталкивание его протонов не разорвет это ядро на 2 осколка.
n Когда ядро урана захватывает нейтрон, внутренняя энергия ядра увеличивается. Ядро подобно жидкой капле начинает сильно деформироваться до тех пор, пока кулоновское отталкивание его протонов не разорвет это ядро на 2 осколка.
 n Другая реакция: Т. о. , деление ядра сопровождается рождением двух-трех новых нейтронов, которые могут вызвать деление следующих ядер. Количество делящихся ядер лавинообразно нарастает. При этом выделяется огромная энергия, которая перераспределяется между ядрами-осколками, нейтронами и другими частицами, рождающимися в ядерной реакции. При определенных условиях возникает ядерный взрыв.
n Другая реакция: Т. о. , деление ядра сопровождается рождением двух-трех новых нейтронов, которые могут вызвать деление следующих ядер. Количество делящихся ядер лавинообразно нарастает. При этом выделяется огромная энергия, которая перераспределяется между ядрами-осколками, нейтронами и другими частицами, рождающимися в ядерной реакции. При определенных условиях возникает ядерный взрыв.
 n Управление цепной реакцией в ядерном реакторе осуществляется с помощью специальных стержней из материалов, сильно поглощающих нейтроны (бор, кадмий). Замедлителем нейтронов и теплоносителем является вода (D 2 O). В качестве топлива используются уран, плутоний, торий.
n Управление цепной реакцией в ядерном реакторе осуществляется с помощью специальных стержней из материалов, сильно поглощающих нейтроны (бор, кадмий). Замедлителем нейтронов и теплоносителем является вода (D 2 O). В качестве топлива используются уран, плутоний, торий.
 n Содержание изотопов урана в руде: 235 U – 0, 7%; 238 U – 99, 3% 238 U используется в реакторах на быстрых нейтронах (≈7 Мэ. В) в качестве сырья для производства плутония:
n Содержание изотопов урана в руде: 235 U – 0, 7%; 238 U – 99, 3% 238 U используется в реакторах на быстрых нейтронах (≈7 Мэ. В) в качестве сырья для производства плутония:
 n n Э. Ферми (1901 -1954, ит. ) ЛНП 1938 г. Первый в мире атомный реактор построен в Чикагском университете под руководством Э. Ферми и запущен 2 декабря 1942 г. В нем: 52 т урана, 472 т графита, 5 контролирующих стержней, покрытых кадмием.
n n Э. Ферми (1901 -1954, ит. ) ЛНП 1938 г. Первый в мире атомный реактор построен в Чикагском университете под руководством Э. Ферми и запущен 2 декабря 1942 г. В нем: 52 т урана, 472 т графита, 5 контролирующих стержней, покрытых кадмием.
 n Курчатов Игорь Васильевич (1903 -1960, СССР) В СССР под руководством И. В. Курчатова были построены атомный реактор (1946 г. ) и первая в мире атомная электростанция в г. Обнинске мощностью 5 МВт, которая введена в эксплуатацию в 1954 г.
n Курчатов Игорь Васильевич (1903 -1960, СССР) В СССР под руководством И. В. Курчатова были построены атомный реактор (1946 г. ) и первая в мире атомная электростанция в г. Обнинске мощностью 5 МВт, которая введена в эксплуатацию в 1954 г.
 Проблемы ядерной энергетики n n Возможность аварии (с радиоактивным заражением окружающей среды, нанесением непоправимого вреда здоровью людей. Яркий пример – авария на Чернобыльской АЭС). Хранение, переработка радиоактивных отходов.
Проблемы ядерной энергетики n n Возможность аварии (с радиоактивным заражением окружающей среды, нанесением непоправимого вреда здоровью людей. Яркий пример – авария на Чернобыльской АЭС). Хранение, переработка радиоактивных отходов.
 Реакции слияния ядер n n При слиянии легких ядер энергия связи в расчете на один нуклон увеличивается. Это соответствует выделению энергии. Для того, чтобы произошла реакция слияния, ядра, обладающие одноименными зарядами, должны сблизиться до расстояния порядка 10 -1410 -15 м. При r = 10 -14 м сила кулоновского отталкивания ядер огромна: F ≈ 3 Н! Т. о. , ядра должны обладать большой кинетической энергией. Нужны сверхвысокие температуры плазмы: Т = 108 – 109 К. Поэтому реакции слияния ядер называются термоядерными реакциями.
Реакции слияния ядер n n При слиянии легких ядер энергия связи в расчете на один нуклон увеличивается. Это соответствует выделению энергии. Для того, чтобы произошла реакция слияния, ядра, обладающие одноименными зарядами, должны сблизиться до расстояния порядка 10 -1410 -15 м. При r = 10 -14 м сила кулоновского отталкивания ядер огромна: F ≈ 3 Н! Т. о. , ядра должны обладать большой кинетической энергией. Нужны сверхвысокие температуры плазмы: Т = 108 – 109 К. Поэтому реакции слияния ядер называются термоядерными реакциями.
 Реакции слияния ядер n n n Примеры реакций слияния ядер: В реакциях слияния ядер радиоактивные отходы не образуются! Термоядерная реакция впервые осуществлена в водородной бомбе (СССР, 1953 г. ).
Реакции слияния ядер n n n Примеры реакций слияния ядер: В реакциях слияния ядер радиоактивные отходы не образуются! Термоядерная реакция впервые осуществлена в водородной бомбе (СССР, 1953 г. ).
 n n n Для реализации УТС необходимо обеспечить при Т > 108 К nτ > 1014. τ – время удержания частиц в плазме, n – их концентрация. Термоядерные реакции – источники звездной энергии. Проблема УТС успешно решается на установках «Токамак» .
n n n Для реализации УТС необходимо обеспечить при Т > 108 К nτ > 1014. τ – время удержания частиц в плазме, n – их концентрация. Термоядерные реакции – источники звездной энергии. Проблема УТС успешно решается на установках «Токамак» .
 Фундаментальные физические взаимодействия и элементарные частицы
Фундаментальные физические взаимодействия и элементарные частицы
 n n n Все объекты природы построены из элементарных частиц, которые взаимодействуют между собой. Взаимопревращение элементарных частиц – характерное их свойство. При этом выполняются известные, а также специфические законы сохранения. Распад ЭЧ на совокупность частиц не означает, что она из них состоит!
n n n Все объекты природы построены из элементарных частиц, которые взаимодействуют между собой. Взаимопревращение элементарных частиц – характерное их свойство. При этом выполняются известные, а также специфические законы сохранения. Распад ЭЧ на совокупность частиц не означает, что она из них состоит!
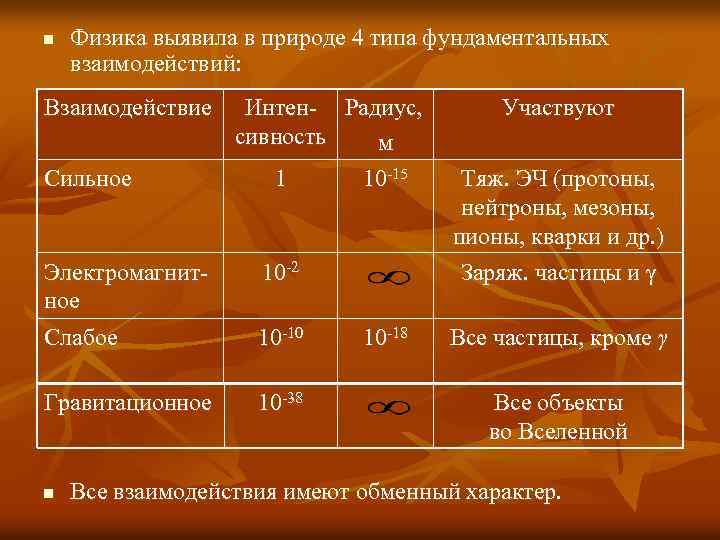 n Физика выявила в природе 4 типа фундаментальных взаимодействий: Взаимодействие Сильное Интен- Радиус, сивность м 1 10 -15 Электромагнитное Слабое 10 -10 Гравитационное 10 -38 n 10 -2 10 -18 Участвуют Тяж. ЭЧ (протоны, нейтроны, мезоны, пионы, кварки и др. ) Заряж. частицы и γ Все частицы, кроме γ Все объекты во Вселенной Все взаимодействия имеют обменный характер.
n Физика выявила в природе 4 типа фундаментальных взаимодействий: Взаимодействие Сильное Интен- Радиус, сивность м 1 10 -15 Электромагнитное Слабое 10 -10 Гравитационное 10 -38 n 10 -2 10 -18 Участвуют Тяж. ЭЧ (протоны, нейтроны, мезоны, пионы, кварки и др. ) Заряж. частицы и γ Все частицы, кроме γ Все объекты во Вселенной Все взаимодействия имеют обменный характер.
 Элементарные частицы n n В настоящее время физике известны более 350 ЭЧ. Они наблюдаются в космических лучах, возникают при столкновениях электронов и протонов, ускоренных до гигантских энергий ≈ 1012 э. В. Коллайдеры – циклические ускорители на встречных пучках. Самый крупный, с длиной кольца 26, 7 км, находится на территории двух стран – Швейцарии и Франции. Здесь же завершается строительство более крупного коллайдера на 7 Тэ. В.
Элементарные частицы n n В настоящее время физике известны более 350 ЭЧ. Они наблюдаются в космических лучах, возникают при столкновениях электронов и протонов, ускоренных до гигантских энергий ≈ 1012 э. В. Коллайдеры – циклические ускорители на встречных пучках. Самый крупный, с длиной кольца 26, 7 км, находится на территории двух стран – Швейцарии и Франции. Здесь же завершается строительство более крупного коллайдера на 7 Тэ. В.
 Проблема элементарности в микрофизике: какие ЭЧ являются действительно неделимыми? n v v В настоящее время к фундаментальным частицам относятся фермионы: 3 кварка (u, c, t), имеющих электрический заряд +(2/3)е и 3 соответствующих антикварка, 3 кварка (d, s, b) с зарядом –(1/3)е и 3 антикварка, лептоны e, μ, τ, с зарядом –е и их античастицы, лептоны нейтральные ve, vμ, vτ и их античастицы,
Проблема элементарности в микрофизике: какие ЭЧ являются действительно неделимыми? n v v В настоящее время к фундаментальным частицам относятся фермионы: 3 кварка (u, c, t), имеющих электрический заряд +(2/3)е и 3 соответствующих антикварка, 3 кварка (d, s, b) с зарядом –(1/3)е и 3 антикварка, лептоны e, μ, τ, с зарядом –е и их античастицы, лептоны нейтральные ve, vμ, vτ и их античастицы,
 v q q фундаментальные бозоны: - фотон - переносчик электромагнитного взаимодействия, - глюон – переносчик сильного взаимодействия, - нейтральный и заряженные векторные бозоны Z 0, W+, W- – переносчики слабого взаимодействия. Все известные тяжелые частицы – адроны – состоят из кварков. Так кварковая структура - протона – (uud), - нейтрона – (ddu). Поиск фундаментальных частиц продолжается.
v q q фундаментальные бозоны: - фотон - переносчик электромагнитного взаимодействия, - глюон – переносчик сильного взаимодействия, - нейтральный и заряженные векторные бозоны Z 0, W+, W- – переносчики слабого взаимодействия. Все известные тяжелые частицы – адроны – состоят из кварков. Так кварковая структура - протона – (uud), - нейтрона – (ddu). Поиск фундаментальных частиц продолжается.


