Volfram_i_molibden.ppt
- Количество слайдов: 39

Вольфрам і Молібден Виконала: Співак Анастасія 4 к н/х

Історія відкриття молібдену • Назва «молібден» походить від грецького слова «молібдос» , що означає «свинець» . 1778 г. К. В. Шеєле відкрив новий елемент – молібден. Розкладаючи молібденіт азотною кислотою, виділив молібденову кислоту, отримав триоксид і деякі солі молібдена. 1782 г. П. Гельєм отримав металічний порошок молібдену відновленням триоксиду молібдену деревним вугіллям. Більш чистий метал був отриманий в 1817 г. И. Берцеліусом відновленням Мо. О 3 воднем.

Історія відкриття вольфраму В 1781 г. Шеєле, досліджуючи мінерал шеєліт, встановив, що він є сполукою кальцію з невідомою кислотою (зараз називається вольфрамовою). Цю же кислоту в 1783 г. визначили брати д‘Елуяр в іншому мінералі -в вольфраміті. Отримавши цю кислоту із вольфраміту, брати д‘Елуяр за допомогою вуглецю вилучили новий елемент в вигляді чистого металу, який по аналогії з вихідним мінералом був названий вольфрамом.
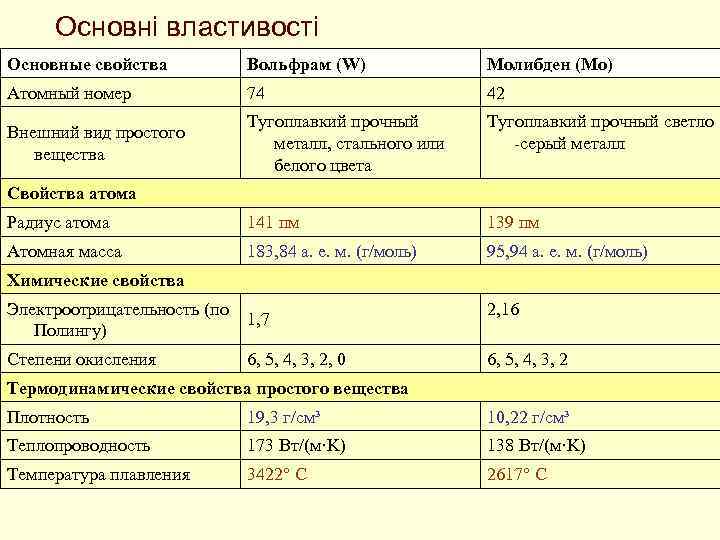
Основні властивості Основные свойства Вольфрам (W) Молибден (Mo) Атомный номер 74 42 Внешний вид простого вещества Тугоплавкий прочный металл, стального или белого цвета Тугоплавкий прочный светло -серый металл Радиус атома 141 пм 139 пм Атомная масса 183, 84 а. е. м. (г/моль) 95, 94 а. е. м. (г/моль) Свойства атома Химические свойства Электроотрицательность (по 1, 7 Полингу) 2, 16 Степени окисления 6, 5, 4, 3, 2, 0 Термодинамические свойства простого вещества Плотность 19, 3 г/см³ 10, 22 г/см³ Теплопроводность 173 Вт/(м·K) 138 Вт/(м·K) Температура плавления 3422° С 2617° С

Основні властивості молібдену • На повітрі при звичайній температурі молібден стійкий. Начало окиснення спостерігається при 400 °С. Починаючи з 600 °С метал швидко окиснюється з утворенням Mo. O 3. • Пари води при температурах віще 700 °С інтенсивно окиснюють його до Mo. O 2. • При підвищених температурах з молібденом взаємодіють сера, селен, арсен, азот, вуглець і багато інших неметалів. • В соляній і сірчанійй кислотах молібден трохи розчинний лише при 80— 100 °С. Азотна кислота, царская горілка і перекис водню швидко розчиняють метал при нагреванні. Хорошим розчинником молібдену є суміш азотної і сірчаної кислот.

Основні властивості вольфраму • В звичайних умовах вольфрам хімічно стійкий. • При 400— 500°С помітно окиснюється на повітрі до WO 3. • Пари води інтенсивно окиснюють його вище 600°С до WO 2. • Галогени, сірка, вуглець, кремній, бор взаємодіють з вольфрамом при високих температурах. • При звичайних умовах вольфрам стійкий до хлоридної, сірчаної, азотної і плавикової (HF) кислотам, а також до царскої горілки. • Швидко розчиняється в суміші плавикової і азотної кислот. • В сполуках вольфрам проявляє валентність від 2 до 6, найбільш стійкі сполуки вищої валентності.

Основні мінерали-носії молібдену • Відомо близько 20 мінералів молібдену. Найбільш часто зустрічаються такі : - молібденіт Мо. S 2; молібденіт - повеліт Са. Мо. O 4; повеліт - молібдит (ферримолибдит) Fе 2(Мо. O 4)3· n. Н 2 O; молібдит - вульфеніт Pb. Мо 04; вульфеніт - молібдо-шеєліт Са(W, Мо)O 4; молібдо-шеєліт - чилагіт Рb(Мо, W)04; чилагіт - кьохлініт Вi 2(Мо 04)02; - ліндгреніт Сu 3(Мо. O 4)2(ОН)2; ліндгреніт - ільземаніт Мо. O 3·SO 3·5 Н 2 O; ільземаніт - ураномолібдат UO 2·UO 3·2 Мо. O 3 и др. ураномолібдат • Промислове значення мають лише перші чотири мінерали.

1 1) Вульфеніт Pb. Мо 04 2) Молібденіт Мо. S 2 3) Повеліт Са. Мо 04 3 2

Основні мінерали-носії вольфраму • Відомо 20 вольфрамових мінералів. Найбільш розповсюджені мінерали групи вольфраміту Mn. WO 4 – Fe. WO 4 і шеєліт Ca. WO 4, що мають промислове значення. • Рідше зустрічаються сульфід вольфраму - тунгстеніт WS 2, а також соединения - тунгстіт, феро- і купротунгстит, гідротунгстит. Досить широко купротунгстит дротунгстит розповсюджені псиломелани - з високим вмістом вольфраму. • В екзогенних умовах утворюються мінерали групи вульфеніту: штольцит - βРb. WO 4, ізоструктурний з штольцит шеєлітом і його моноклінний різновид - распіт – α-Рb. WO 4.

1 2 1) Вольфраміт Mn. WO 4 – Fe. WO 4 2) Шеєліт Ca. WO 4

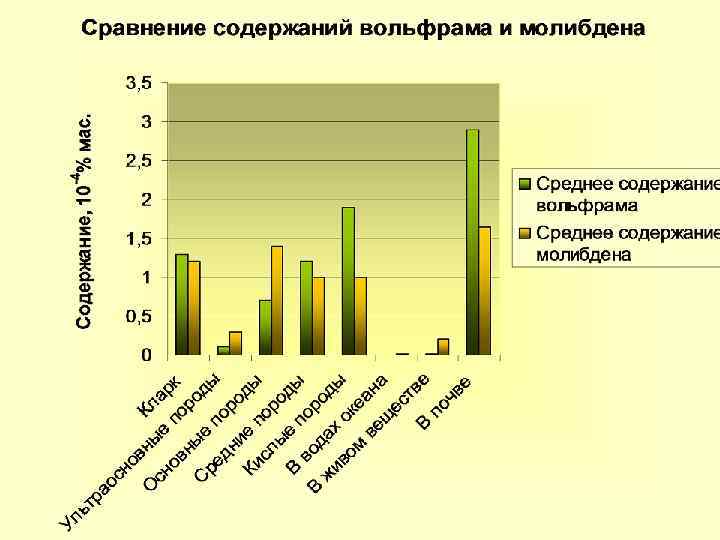
Форми знаходження молібдену • В вільному вигляді молібден не зустрічається. В земній корі молібден розповсюджений відносно рівномірно, деяке підвищення спостерігається тільки в кислих вивержених породах і особливо в осадкових породах, багатих органічною речовиною. Ультраосновні породи містять менше молібдену, чим інші типи порід. • В зонах окиснення переважають кисневі сполуки шестивалентного молібдену (молібдати), утворені в результате окиснення молібденіту. • В земній корі максимальні концентрації молібдену створюються в результаті гідротермальної діяльності інтрузій гранітоїдної магми. • В екзогенних умовах молібден (в формі кисневих сполук) концентруются в осадкових породах, особливо в кремній-вугільних глинистих сланцях і углях, де він тісно зв*язаний з органічною речовиною. Значні концентрації молібдену відомі також в нафті і твердих нафтобітумах.

Поведінка молібдену в водному і повітряному середовищі • В біосфері Мо енергійно мігрує і концентрується, його геохімія тут тісно пов*язана з живою речовиною і продуктами його розкладу. • В кисневих водах Мо порівняно слабкий водний мігрант, що підтверджується постійністю його вмісту в більшості ґрунтів. • В річних водах Мо мало, поступаючи зі стоком в океан, він слабко накопичується в морській воді, частково іде в мул. В мулах з сірководневим зараженням місцями відбувається значне накопичення Мо.

Форми знаходження вольфраму • Вольфрам мало поширений в природі, вміст в земній корі 1, 3· 10 -4% мас. Вольфрам зустрічається в природі головним чином в вигляді окиснених складних сполук, утворених WO 3 і оксидами заліза і мангану чи кальцію, а інколи плюмбуму , міді, торію і рідкоземельних елементів. • Всі вольфрамові родовища мають магматичне чи гідротермальне походження. • Вольфрам генетично зв*язаний з гранітоїдами, що характеризуються перенасиченістю глиноземом, високою кислотністю і підвищеним вмістом олова і фтору. Він легко утворює леткі сполуки з фтором, хлором, бором і накопичується в продуктах остаточної кристалізації гранітних магм. • В екзогених умовах мінерали вольфраму відносно стійкі і здатні утворювати розсипи. В процесі утворення осаду концентрація вольфраму відбувається в морських теригенних, рідше карбонатних відкладах , збагаченими Fe, Мn.

Поведінка вольфраму в водному і вольфраму повітряному середовищах • Хоча вольфрам не такий рідкісний в земной коре, вміст цього елементу в водах зони гіпергенеза дуже малі. Процеси сорбційного осадження утвореного гіпергеними мінералами виключають міграцію вольфраму. • Його сорбують гідрооксиди заліза, мангану, а також солі кальцію. • Крім цього, вольфрам частково осаджується з вод в вигляді малорозчинних вольфраматів і вольфрамітів. • Сприятливі для міграції вольфраму є лужні натрієві води. Він накопичується в озерних водах зі збільшенням рівня загальної мінералізації.

Основні типи родовищ молібдену • Розрізняють декілька видів молібденових руд: • Прості кварцево-молібденові руди, в яких молібден залягає в кварцевих жилах. • Кварцево-молібдено-вольфрамітові руди, які містять вольфраміт. • Скарнові руди. В рудах цього типу молібденіт часто з шеєлітом і деякими сульфідами (пірит, халькопірит) залягають в кварцевих жилах, які заповнюють тріщини в скарнах. • Мідно-молібденові руди, в яких молібден сполучається з сульфідами міді і заліза. Це найбільш важливе джерело отримання молібдену. На нього доводиться більше 60% запасів молібдену. Найбільш значні родовища молібденових руд в зарубіжних країнах зосереджені в західній частині США. • Вульфенітові руді виникають в результаті переробки мінералів свинцю Мовмісними розчинами. Родовища вульфеніту є в США Арізоне, Алжирі, Австралії, Югославії, Казахстані.
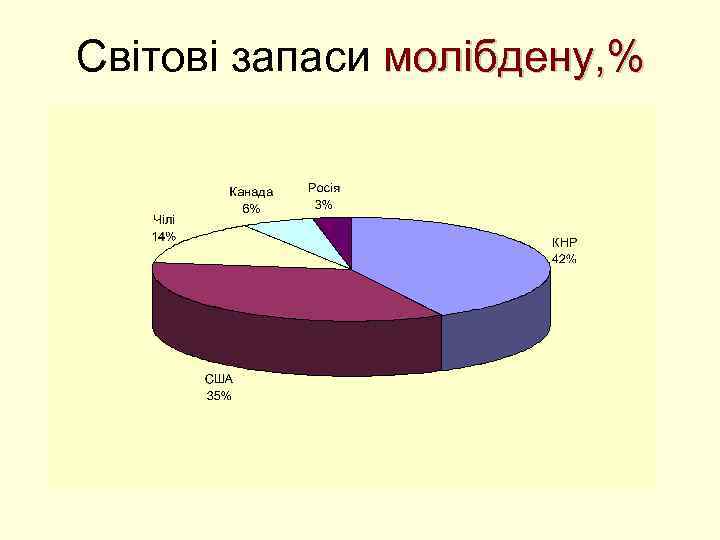
Світові запаси молібдену, %

Основні типи родовищ вольфраму • Вольфрамоворудні родовища по головній складовій їх мінералу ділять на вольфрамітові і шеєлітові. • Вольфрамітові родрвища зазвичай пов*язані з проходженням в переважно алюмосилікатному середовищі грейзеного процесу чи, середовищі, багатому на залізо, пізніх етапів гідротермального мінералоутворення. В жилах вольфраміт кристалізується одним із перших. • Утворення вольфраміту відбувається в умовах підвищення лужності слабкокислого чи нейтрального мінералоутворюючого розчину. • Відкладення шеєліту відбувається внаслідок знижения лужності мінералоутворюючого розчину в ході взаємодії його з плагіоклазовими породами.
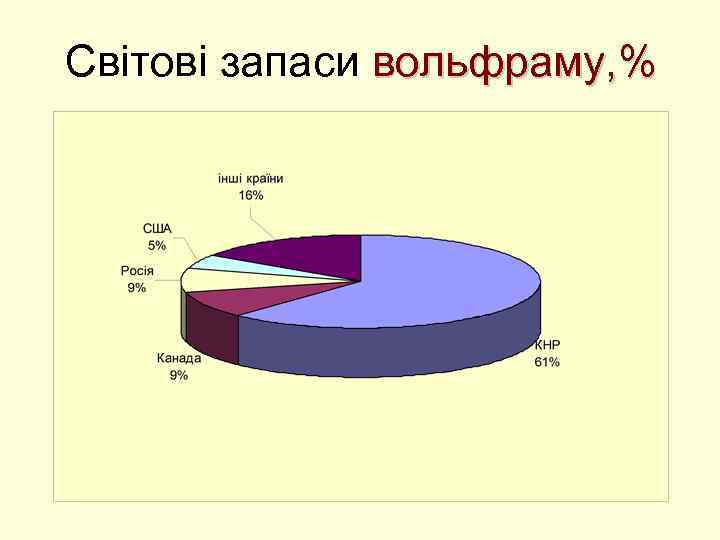
Світові запаси вольфраму, %

Області застосування молібдену • Сталі, леговані молібденом, застосовуються для виготовлення інструментів і деталей в автомобільній, авіаціонній і інших галузях промисловості. • Металічний молібден застосовується в електричних лампах, при виготовленні радіоламп, рентгенівських трубок, а також в вигляді проволоки в високотемпературних електричних печах. • Сполуки молібдену — сульфід, оксиди, молібдати — є каталізаторами хімічних реакцій, пігментами барвників, компонентами глазурі. • Легкрозчинні сполуки молібдену знайшли застосування в сільському господарстві (мікродобрива).

Області застосування вольфраму • Металічний вольфрам застосовується для виготовлення ниток розжарювання в електролампах, електродів для водневого зварювання, заміняючи платину, для нагрівачів високотемпературних електропечей, працюючих при температурі вище 3000 ° С, термопар, роторів в гіроскопах оптичних пірометрів для катодів рентгенівських трубок, електровакуумної апаратури, радіоприборів, випрямлячів і гальванометрів. • В виробництві сталей в якості легуючої добавки, в твердих жаростійких сплавах, в електротехніці, в виробництві кислотостійких і спеціальных сплавів, в хімічній промисловості. • Сполуки вольфраму застосовуються в якості барвників, для надання тканинам вогнестійкості і водостійкості.

Переробка вольфрамових концентратів Для: • Феровольфрам • Триоксид вольфраму (для добування W, WC) 1) Вольфрамові концентрати спікають з содою чи обробляють розчином соди а автоклавах. 2) Розклад Na. OH 3) Розклад кислотами (отримують Na. WO 3 для добування HWO 3)

Спікання з содою • Взаємодія вольфраміту з содою в присутності кисню при 800 -900 0 • Взаємодія шеєліту з содою при 800900 0 (для зниження витрат соди додають кварцевий пісок

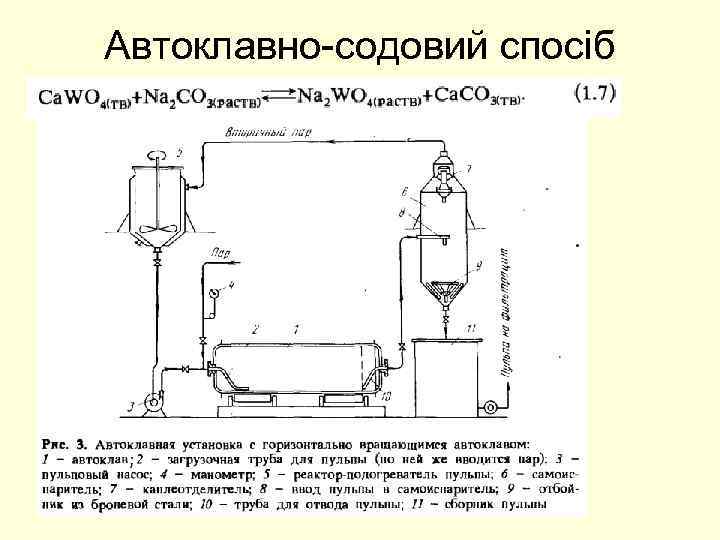
Автоклавно-содовий спосіб

• Розклад лугом • Розклад кислотою • 25 -40%-й розчин лугу • 110 -1200 • Надлишок лугу –більше 50% • Лише для обробки високосортних концентратів (бо інакше утворюються домішки і забруднені розчини) • • 100 -1100 4 -12 годин 0, 2 -0, 3 % домішки Мо; Недоліки: 1) велика витрата кислоти; 2)великий об`єм відходів розчинів хлористого кальцію і їх утилізація

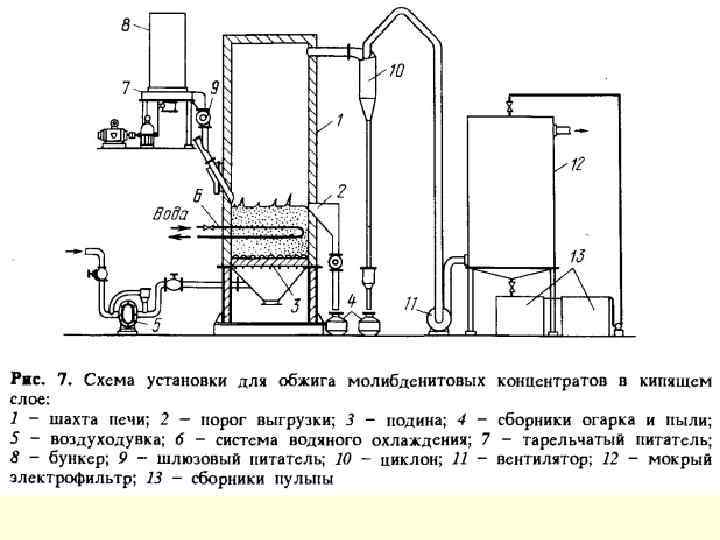
Переробка молібденових концентратів Окислювальне обпалювання молібденових концентратів:
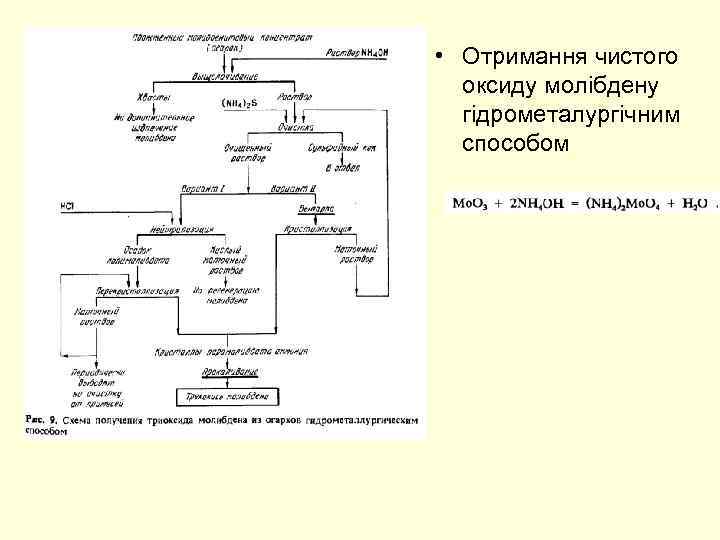
• Отримання чистого оксиду молібдену гідрометалургічним способом

1) Виділення Молібдену з аміачних розчинів (спосіб упарювання): Спосіб нейтралізації: 2) Термічний розклад парамолібдату амонію: 3) Азотнокислий спосіб переробки концентратів :

Виробництво порошків Мо і W
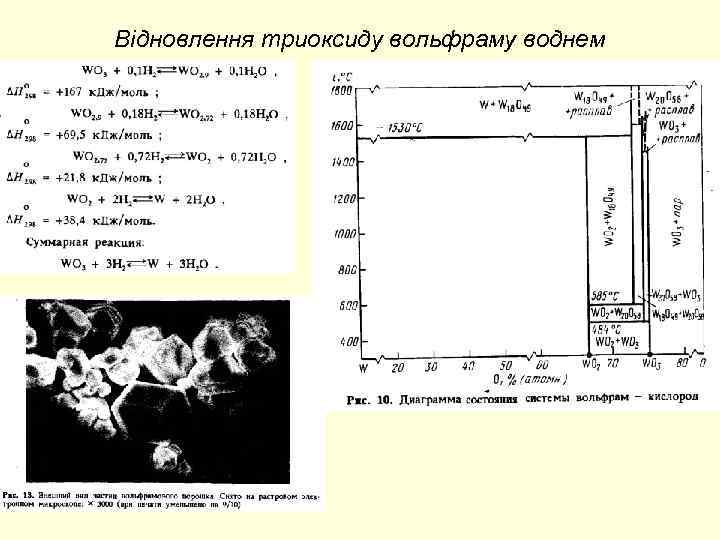
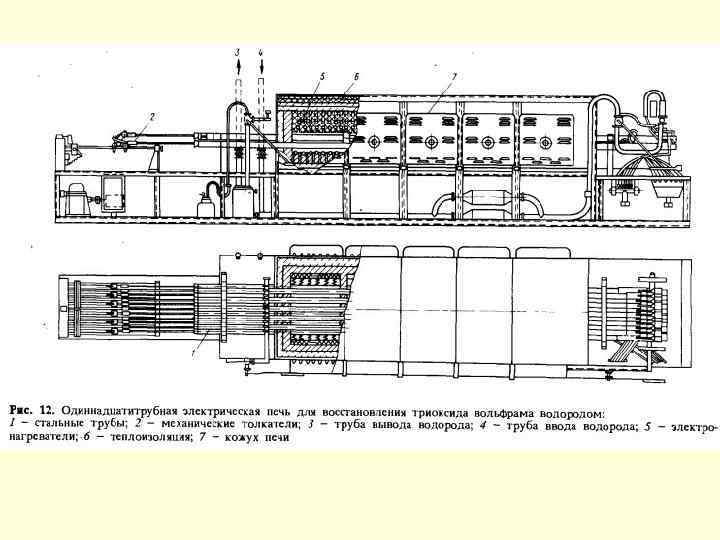
Відновлення триоксиду вольфраму воднем
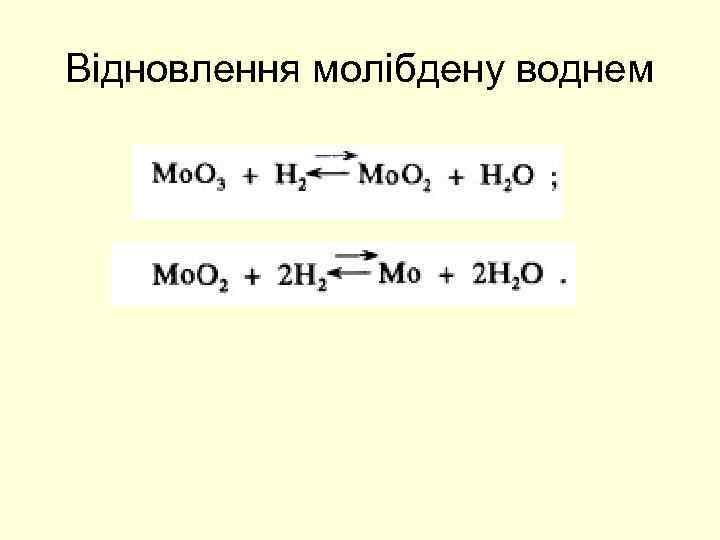
Відновлення молібдену воднем

Виробництво методом порошкової металургії • Пресування заготовок із зразків • Спікання заготовок • Механічна обробка з отриманням виробів
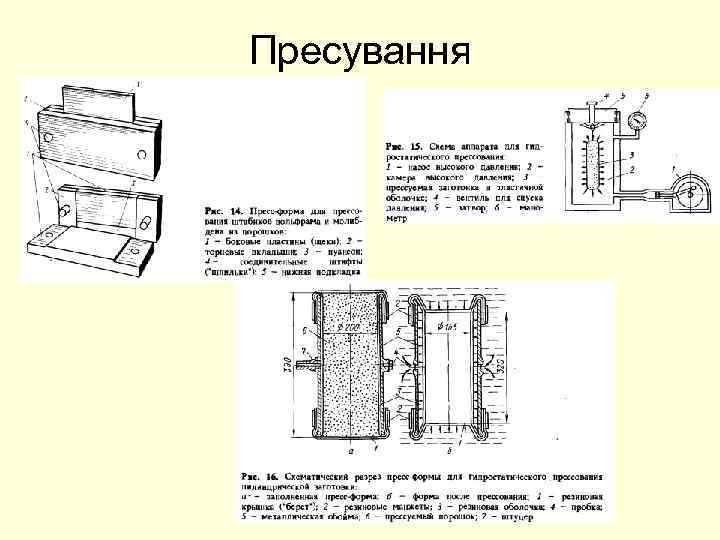
Пресування
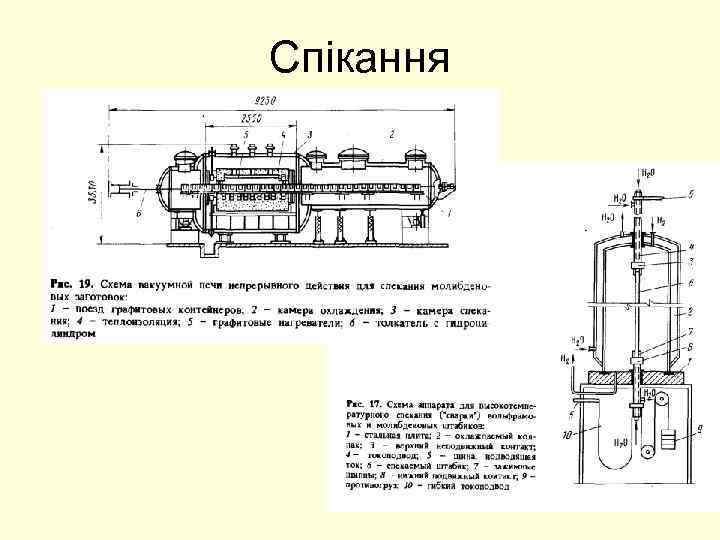
Спікання

Плавка Мо і W • Дугова • Електронно-променева

Дякую за увагу!
Volfram_i_molibden.ppt