Водородная связь.ppt
- Количество слайдов: 8

Водородная связь Legame idrogeno Hydrogen bond Liaison hydrogène Wasserstoff-Bindung Enlaces de hidrógeno
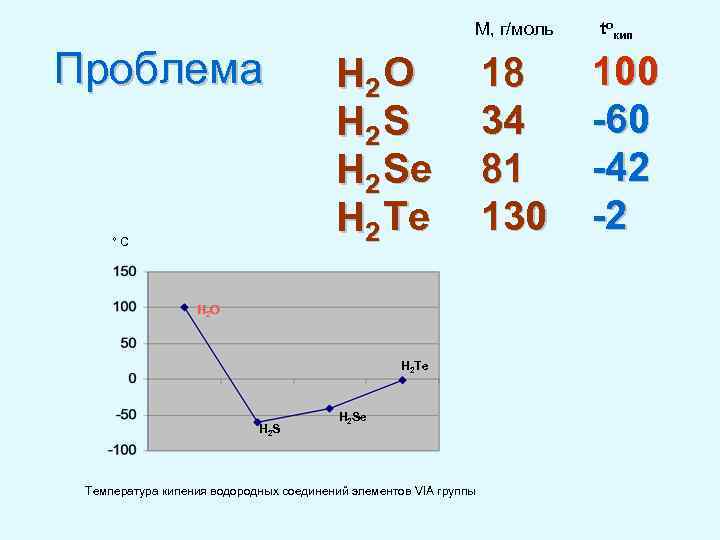
M, г/моль Проблема °C H 2 O H 2 Se H 2 Te H 2 O H 2 Te H 2 Se Температура кипения водородных соединений элементов VIA группы 18 34 81 130 toкип 100 -60 -42 -2
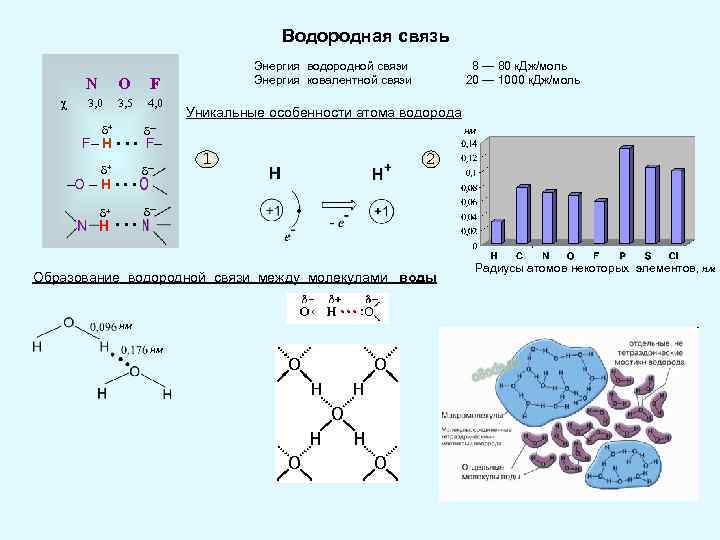
Водородная связь N χ O F 3, 0 3, 5 4, 0 Энергия водородной связи Энергия ковалентной связи + ─ Уникальные особенности атома водорода ─ + 8 — 80 к. Дж/моль 20 — 1000 к. Дж/моль F– H • • • F– –O – H • • • • нм 1 2 • Образование водородной связи между молекулами воды нм нм Радиусы атомов некоторых элементов, нм

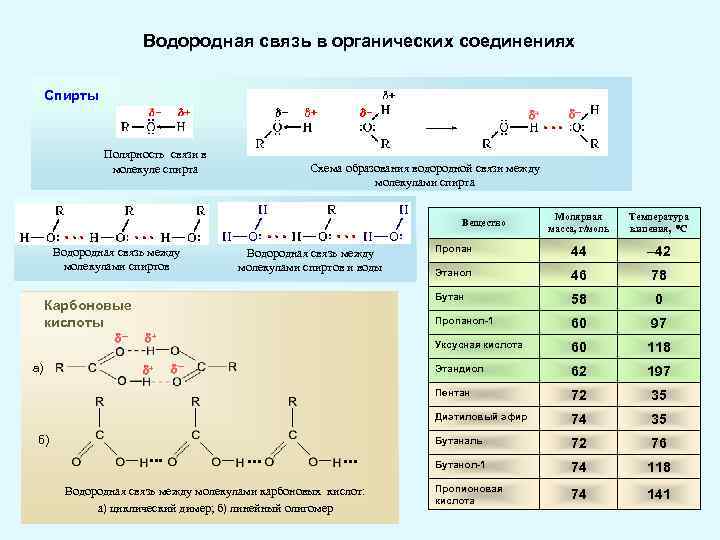
Водородная связь в органических соединениях Спирты + Полярность связи в молекуле спирта ─ Схема образования водородной связи между молекулами спирта Молярная масса, г/моль Температура кипения, С Пропан 44 – 42 Этанол 46 78 Бутан 58 0 Пропанол-1 60 97 Уксусная кислота 60 118 Этандиол 62 197 Пентан 72 35 Диэтиловый эфир 74 35 Бутаналь 72 76 Бутанол-1 74 118 Пропионовая кислота 74 141 Вещество Водородная связь между молекулами спиртов и воды Карбоновые кислоты ─ а) + + ─ б) • • • Водородная связь между молекулами карбоновых кислот: а) циклический димер; б) линейный олигомер
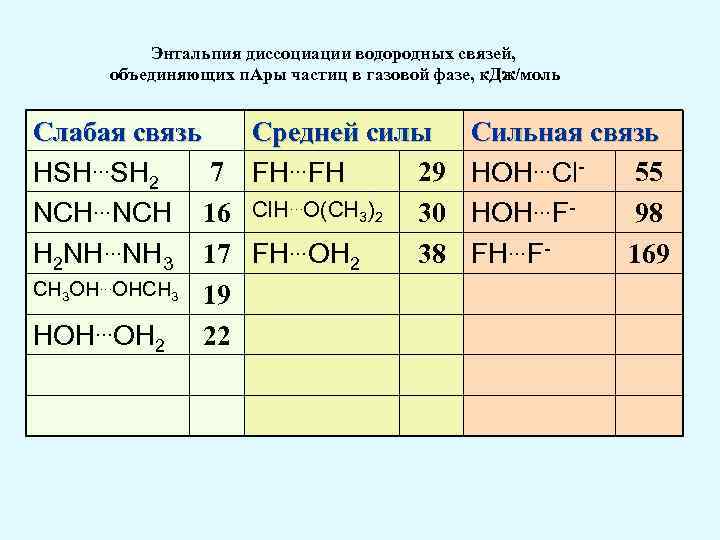
Энтальпия диссоциации водородных связей, объединяющих п. Ары частиц в газовой фазе, к. Дж/моль Слабая связь Средней силы 7 FH…FH 29 HSH…SH 2 NCH…NCH 16 Cl. H…O(CH 3)2 30 38 H 2 NH…NH 3 17 FH…OH 2 CH 3 OH…OHCH 3 19 HOH…OH 2 22 Сильная связь 55 HOH…Cl 98 HOH…F 169 FH…F-
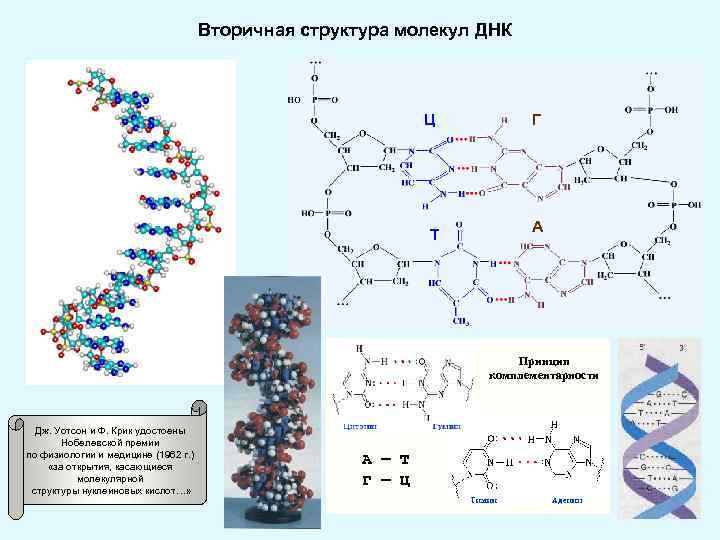
Вторичная структура молекул ДНК Ц Г Т А Принцип комплементарности Дж. Уотсон и Ф. Крик удостоены Нобелевской премии по физиологии и медицине (1962 г. ) «за открытия, касающиеся молекулярной структуры нуклеиновых кислот…» A — T Г — Ц

Водородная связь.ppt