Водородная энергетика _лекция_4 курс_2013.ppt
- Количество слайдов: 42

ВОДОРОДНАЯ ЭНЕРГЕТИКА Химические аспекты профессор Б. М. Булычев кафедра химической технологии и новых материалов Химического факультета МГУ

Что есть ВОДОРОДНАЯ ЭНЕРГЕТИКА ? l 2 H 2 + O 2 → 2 H 2 O + е- + Q l William Robert Grove (1811 -1896) W. R. Grove. On Voltaic Series and the Combination of Gases by Platinum. // Phil. Mag. , 14, 127 -130 (1839)
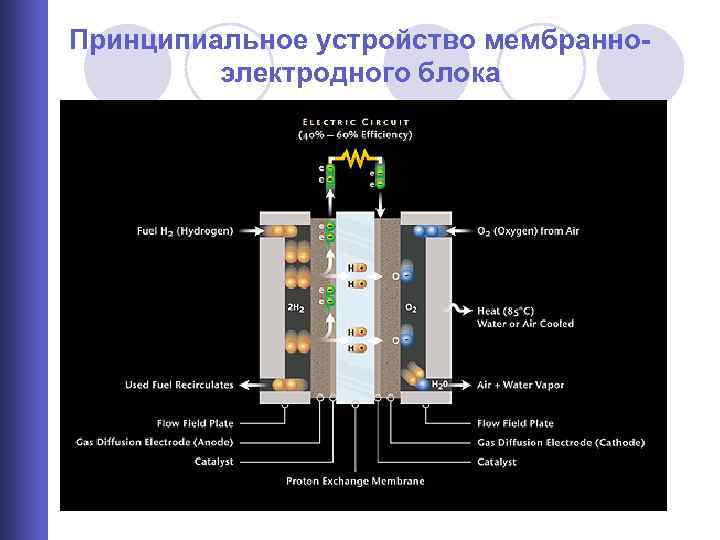
Принципиальное устройство мембранноэлектродного блока

Основные и паразитные электрохимические реакции
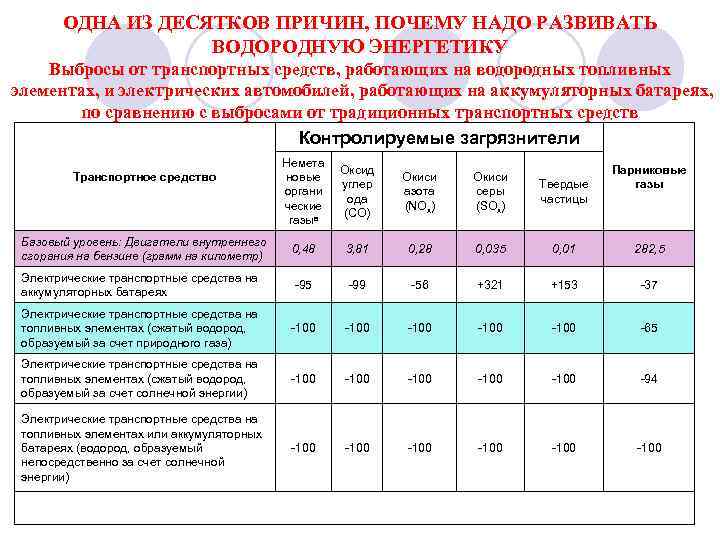
ОДНА ИЗ ДЕСЯТКОВ ПРИЧИН, ПОЧЕМУ НАДО РАЗВИВАТЬ ВОДОРОДНУЮ ЭНЕРГЕТИКУ Выбросы от транспортных средств, работающих на водородных топливных элементах, и электрических автомобилей, работающих на аккумуляторных батареях, по сравнению с выбросами от традиционных транспортных средств Контролируемые загрязнители Немета новые органи ческие газыв Оксид углер ода (СО) Окиси азота (NOx) Окиси серы (SOx) Твердые частицы Базовый уровень: Двигатели внутреннего сгорания на бензине (грамм на километр) 0, 48 3, 81 0, 28 0, 035 0, 01 282, 5 Электрические транспортные средства на аккумуляторных батареях -95 -99 -56 +321 +153 -37 Электрические транспортные средства на топливных элементах (сжатый водород, образуемый за счет природного газа) -100 -100 -65 Электрические транспортные средства на топливных элементах (сжатый водород, образуемый за счет солнечной энергии) -100 -100 -94 Электрические транспортные средства на топливных элементах или аккумуляторных батареях (водород, образуемый непосредственно за счет солнечной энергии) -100 -100 Транспортное средство Парниковые газы

Основные преимущества топливных элементов l Высокая эффективность (> 60%) l Экологическая чистота ? ? Ха-Ха l Простота и надежность (отсутствуют подвижные части) l Бесшумность l Возможность миниатюризации
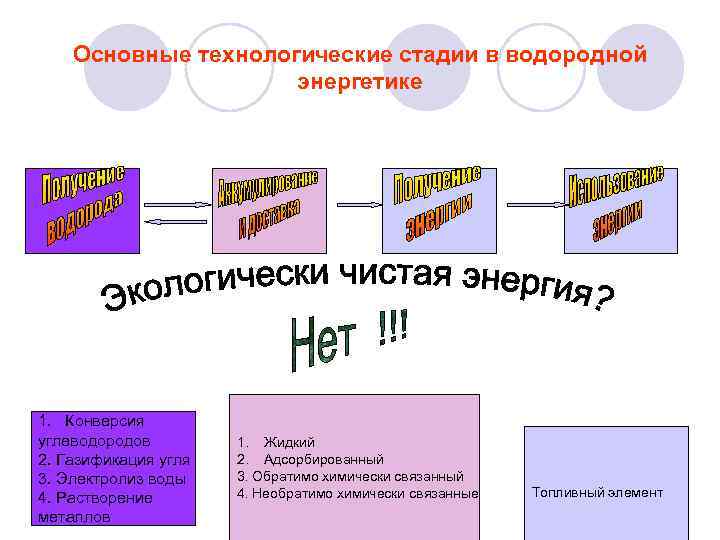
Основные технологические стадии в водородной энергетике 1. Конверсия углеводородов 2. Газификация угля 3. Электролиз воды 4. Растворение металлов 1. Жидкий 2. Адсорбированный 3. Обратимо химически связанный 4. Необратимо химически связанные Топливный элемент
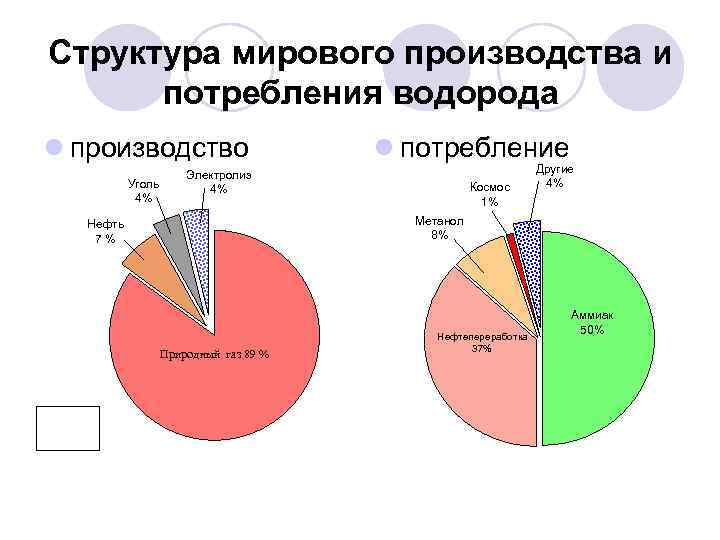
Структура мирового производства и потребления водорода l производство Уголь 4% l потребление Электролиз 4% Космос 1% Другие 4% Метанол 8% Нефть 7 % Природный газ 89 % Нефтепереработка 37% Аммиак 50%
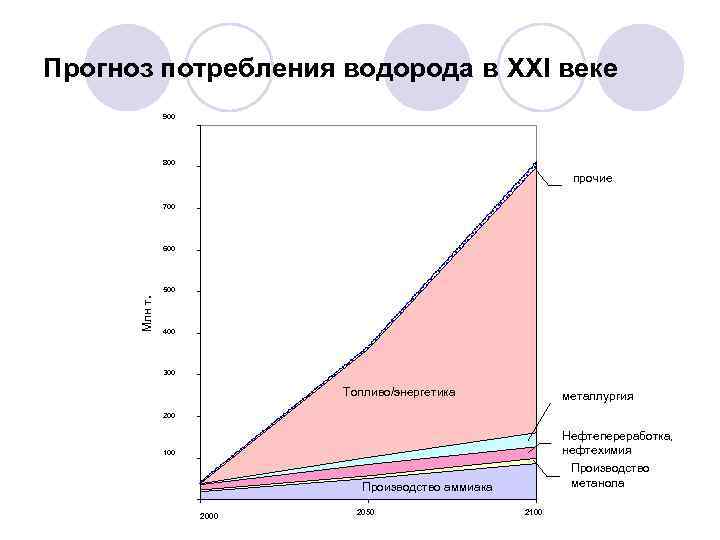
Прогноз потребления водорода в XXI веке 900 800 прочие 700 600 Млн т. 500 400 300 Топливо/энергетика металлургия 200 Нефтепереработка, нефтехимия 100 Производство метанола Производство аммиака 2000 2050 2100
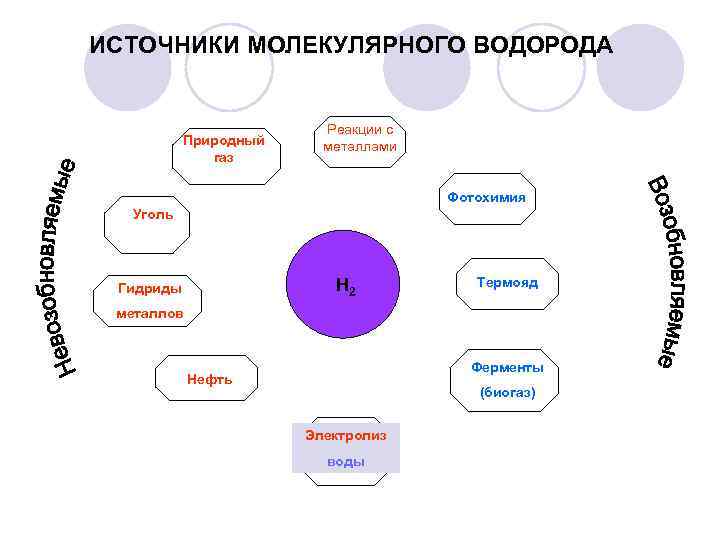
ИСТОЧНИКИ МОЛЕКУЛЯРНОГО ВОДОРОДА Природный газ Реакции с металлами Фотохимия Уголь Н 2 Гидриды Термояд металлов Ферменты Нефть (биогаз) Электролиз воды
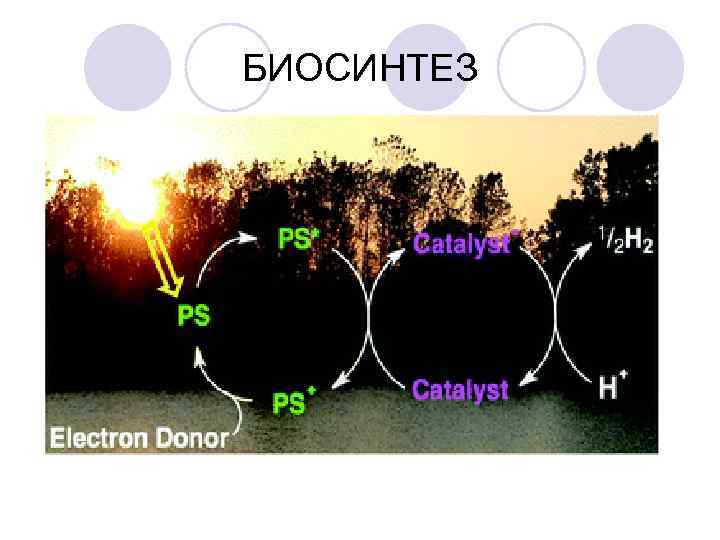
БИОСИНТЕЗ
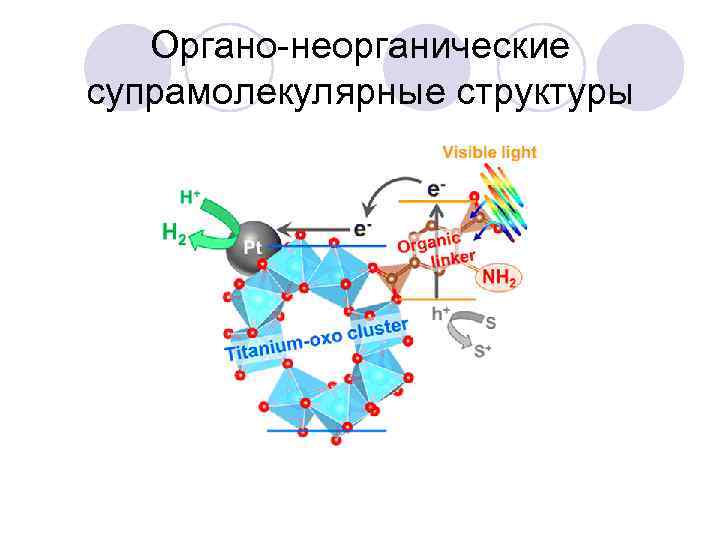
Органо-неорганические супрамолекулярные структуры
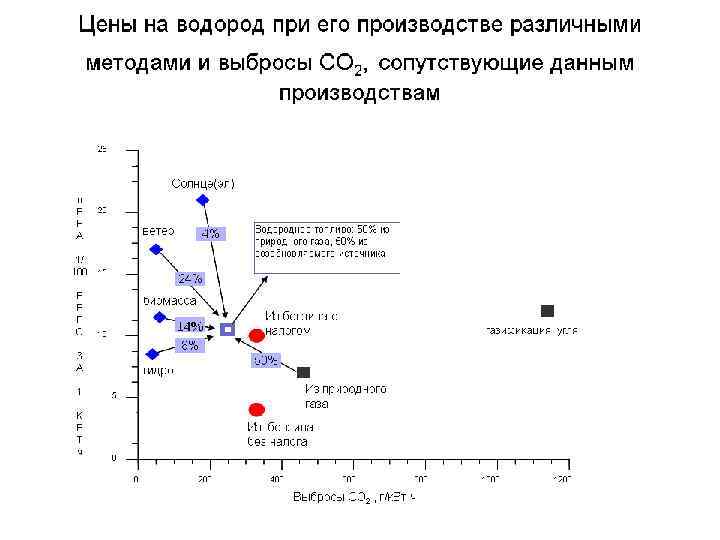
Цены на водород при его производстве различными методами и выбросы CO 2, сопутствующие данным производствам 25 Солнце(эл) ц Е Н А 1/ 100 Е В Р О 20 ветер 15 К В Т ч Водородное топливо: 50% из природного газа, 50% из возобновляемого источника 24% биомасса 14% 10 Из бензина с налогом Водород из угля 8% З А 1 4% 50% гидро Из природного газа 5 Из бензина без налога 0 0 200 400 600 800 Выбросы СО 2 , г/к. Вт ч 1000 1200
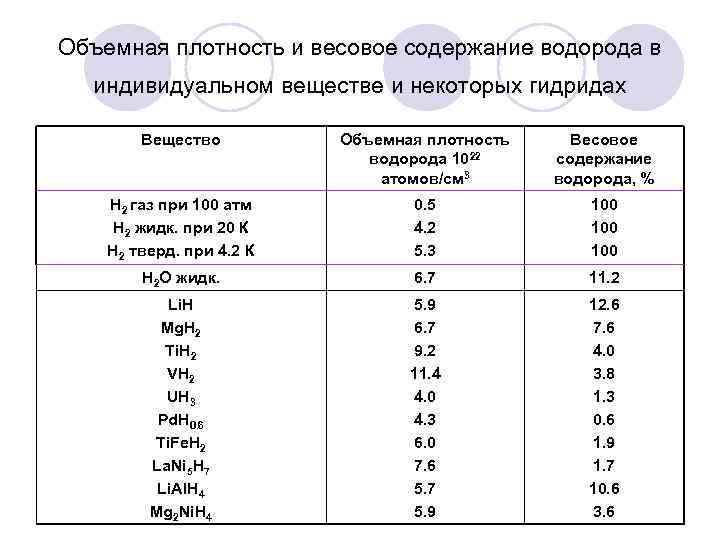
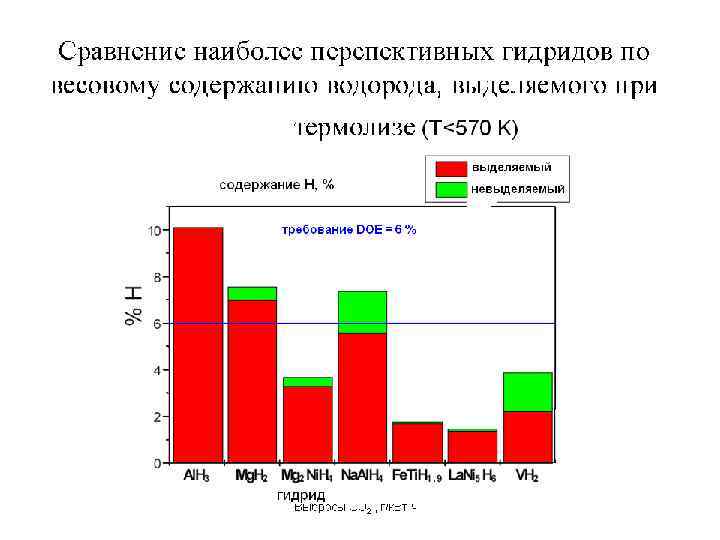
Объемная плотность и весовое содержание водорода в индивидуальном веществе и некоторых гидридах Вещество Объемная плотность водорода 1022 атомов/см 3 Весовое содержание водорода, % Н 2 газ при 100 атм Н 2 жидк. при 20 К Н 2 тверд. при 4. 2 К 0. 5 4. 2 5. 3 100 100 Н 2 О жидк. 6. 7 11. 2 Li. H Mg. H 2 Ti. H 2 VH 2 UH 3 Pd. H 0. 6 Ti. Fe. H 2 La. Ni 5 H 7 Li. Al. H 4 Mg 2 Ni. H 4 5. 9 6. 7 9. 2 11. 4 4. 0 4. 3 6. 0 7. 6 5. 7 5. 9 12. 6 7. 6 4. 0 3. 8 1. 3 0. 6 1. 9 1. 7 10. 6 3. 6

Основные требования к аккумулятору водорода при его использовании в качестве мобильного источника на борту автомобиля l 1. Количество водорода, выделяемого из материала, не менее 6 масс %. l 2. Количество водорода, запасенного в устройстве, не менее 45 кг на 100 кг общего веса. l 3. Температура выделения водорода ≤ 150 о. С. l 4. Обратимость процесса «заправка-выделение» (не менее 500 циклов). l 5. Заправка не более 5 минут. l 4. Безопасность материала и устройства.

Методы аккумулирования элементного водорода l Сжатый газообразный водород: l газовые баллоны; l стационарные массивные системы хранения, включая подземные резервуары; l для хранения 0. 5 кг Н 2 требуется баллон массой 53 кг. Прогресс в материаловедении даёт возможность снизить массу материала баллона до 8 – 10 кг с одновременным увеличением давления до 1000 атм. l Жидкий водород: стационарные и транспортные криогенные контейнеры l Главная часть криогенной системы хранения водорода – теплоизолированные сосуды, масса которых примерно в 4 – 5 раз меньше массы баллонов высокого давления при равном количестве хранимого водорода.

Композитные баллоны для хранения сжатого водорода
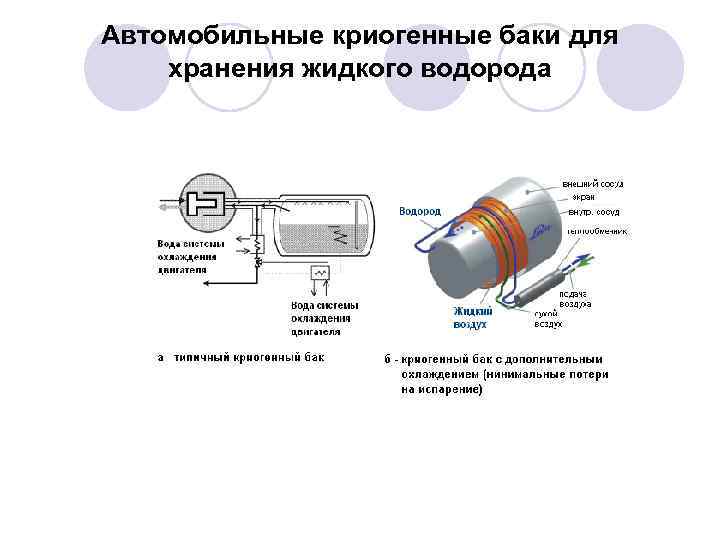
Автомобильные криогенные баки для хранения жидкого водорода


Методы аккумулирования водорода, основанные на физической адсорбции газа l в цеолиты и родственные соединения; l в активированный уголь; l в углеродные наноматериалы; l водно-органические клатраты; lв пористые координационные соединения (MOF структуры); lв металлические сплавы и ИМС.
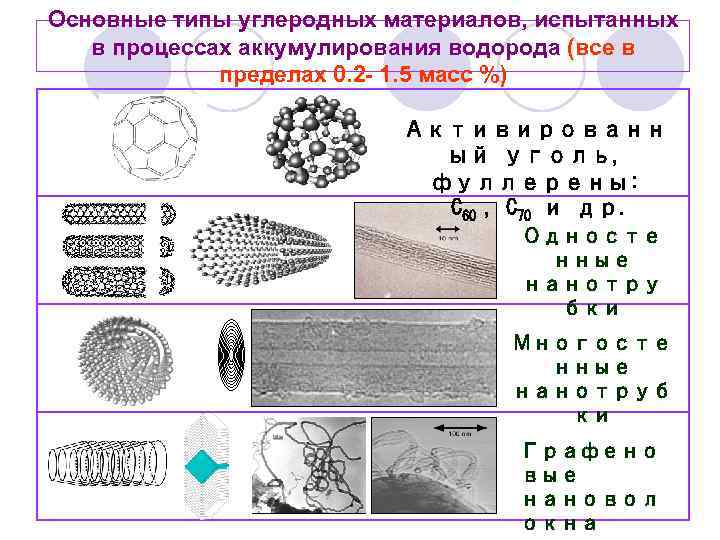
Основные типы углеродных материалов, испытанных в процессах аккумулирования водорода (все в пределах 0. 2 - 1. 5 масс %) Активированн ый уголь, фуллерены: C 60 , C 70 и др. Односте нные нанотру бки Многосте нные нанотруб ки Графено вые нановол окна
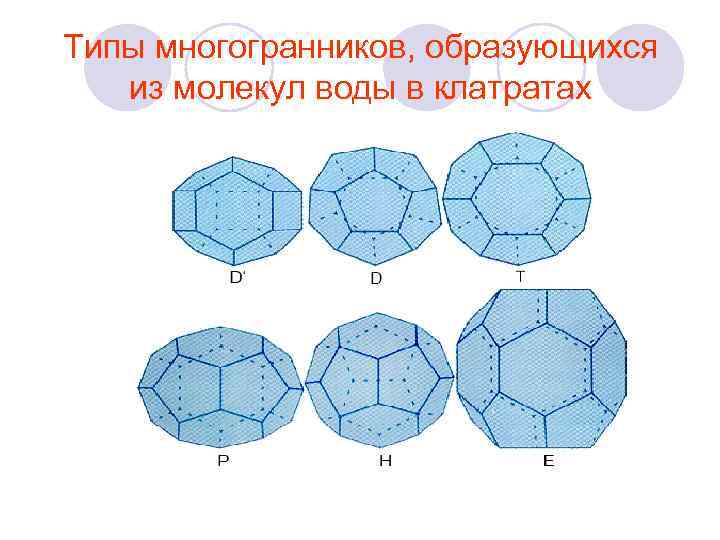
Типы многогранников, образующихся из молекул воды в клатратах
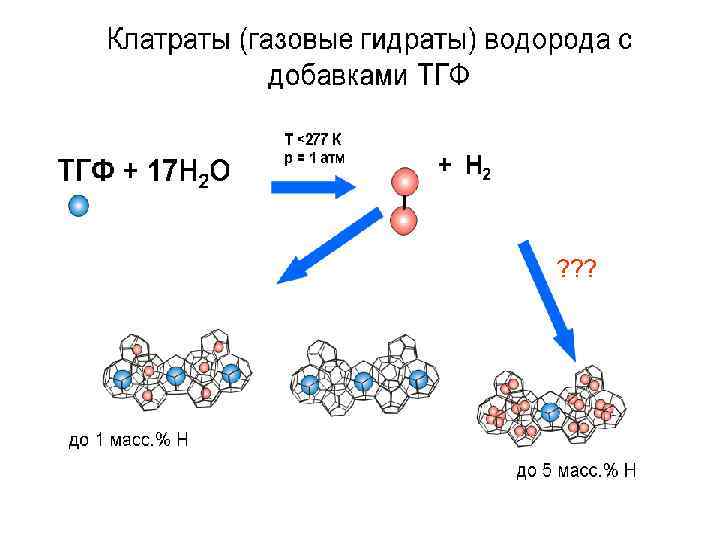
Клатраты (газовые гидраты) водорода с добавками ТГФ + 17 Н 2 О Т <277 К р = 1 атм + Н 2 ? ? ? до 1 масс. % Н до 5 масс. % Н
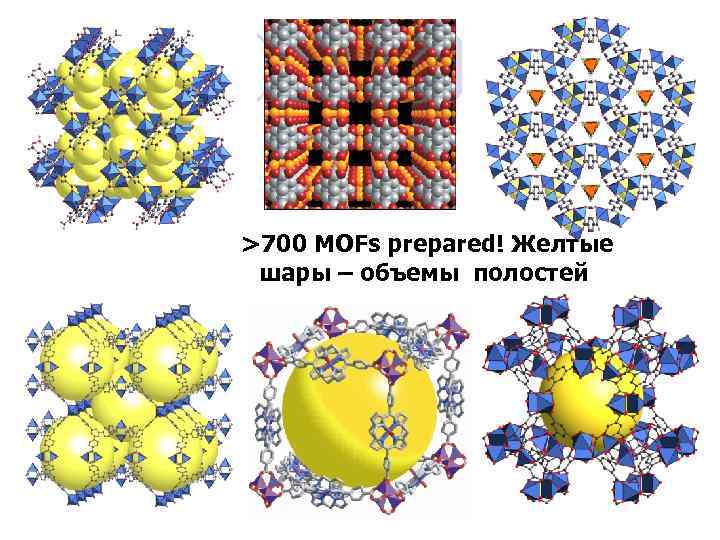
>700 MOFs prepared! Желтые шары – объемы полостей
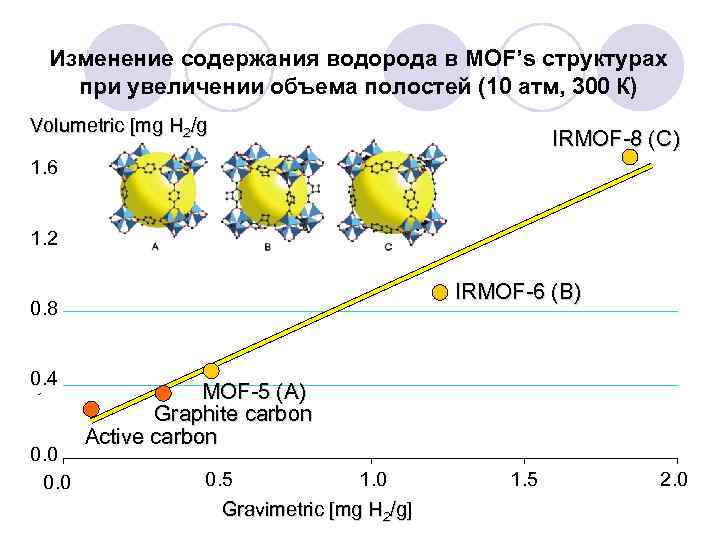
Изменение содержания водорода в MOF’s структурах при увеличении объема полостей (10 атм, 300 К) Volumetric [mg H 2/g IRMOF-8 (C) 1. 6 1. 2 IRMOF-6 (B) 0. 8 0. 4 0. 0 MOF-5 (A) Graphite carbon Active carbon 0. 5 1. 0 Gravimetric [mg H 2/g] 1. 5 2. 0
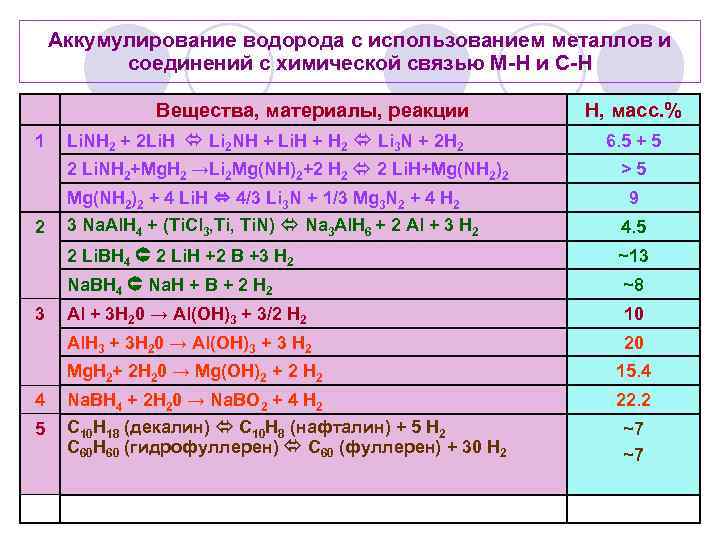
Аккумулирование водорода с использованием металлов и соединений с химической связью М-Н и С-Н Вещества, материалы, реакции 1 Li. NH 2 + 2 Li. H Li 2 NH + Li. H + H 2 Li 3 N + 2 H 2 2 Li. NH 2+Mg. H 2 →Li 2 Mg(NH)2+2 H 2 2 Li. H+Mg(NH 2)2 + 4 Li. H ⇔ 4/3 Li 3 N + 1/3 Mg 3 N 2 + 4 H 2 H, масс. % 6. 5 + 5 >5 9 4. 5 ~13 Na. BH 4 Na. H + B + 2 H 2 ~8 Al + 3 H 20 → Al(OH)3 + 3/2 H 2 10 Al. H 3 + 3 H 20 → Al(OH)3 + 3 H 2 3 3 Na. Al. H 4 + (Ti. Cl 3, Ti. N) Na 3 Al. H 6 + 2 Al + 3 H 2 2 Li. BH 4 2 Li. H +2 B +3 H 2 2 20 Mg. H 2+ 2 H 20 → Mg(OH)2 + 2 H 2 15. 4 4 Na. BH 4 + 2 H 20 → Na. BO 2 + 4 H 2 22. 2 5 C 10 H 18 (декалин) C 10 H 8 (нафталин) + 5 H 2 C 60 H 60 (гидрофуллерен) C 60 (фуллерен) + 30 H 2 ~7 ~7
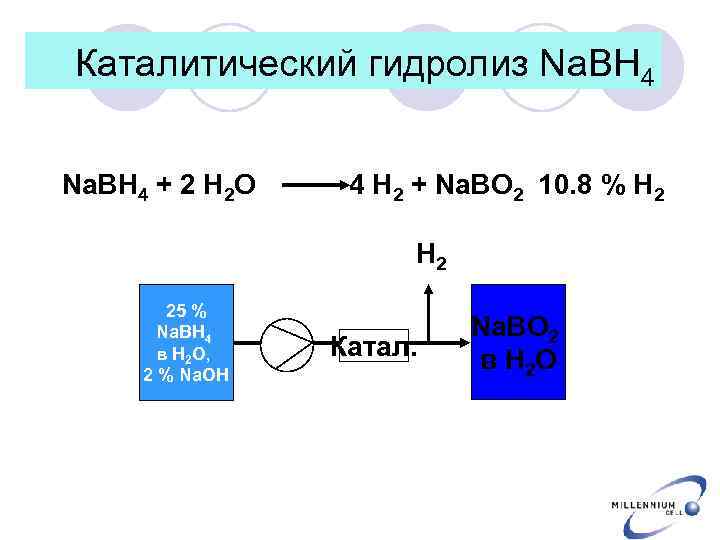
Каталитический гидролиз Na. BH 4 + 2 H 2 O 4 H 2 + Na. BO 2 10. 8 % H 2 25 % Na. BH 4 в H 2 O, 2 % Na. OH Катал. Na. BO 2 в H 2 O
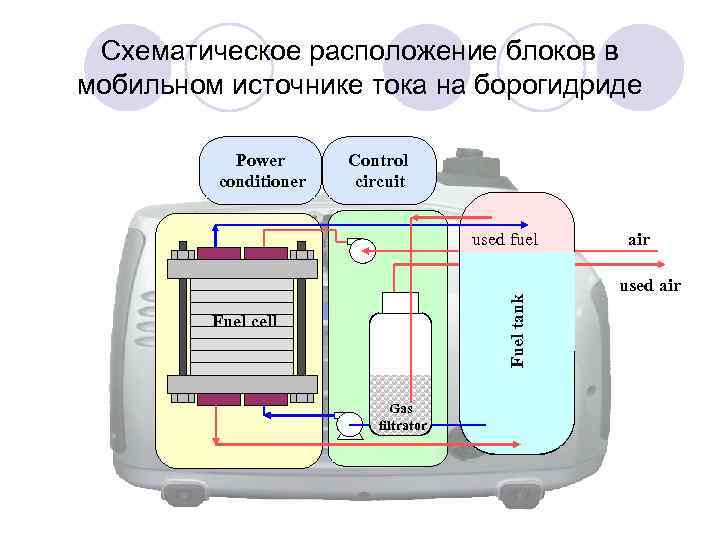
Схематическое расположение блоков в мобильном источнике тока на борогидриде Power conditioner Control circuit Fuel tank used fuel Fuel cell Gas filtrator air used air

Общий вид генератора на 200 W, работающего на борогидриде
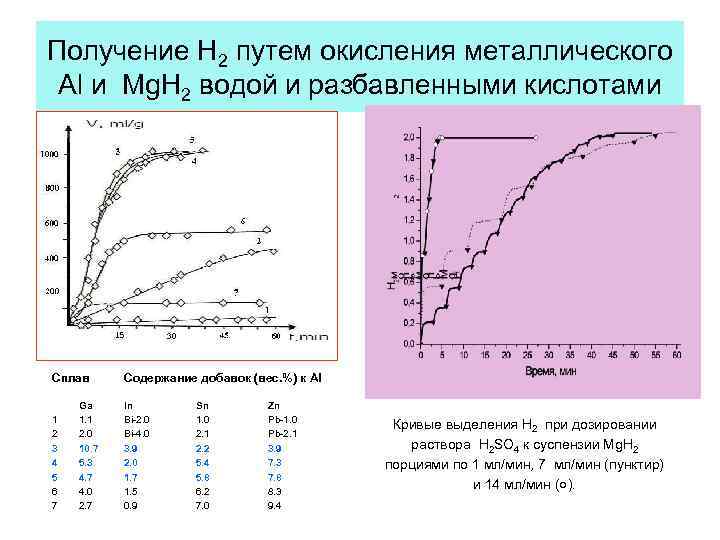
Получение Н 2 путем окисления металлического Al и Mg. H 2 водой и разбавленными кислотами Сплав 1 2 3 4 5 6 7 Ga 1. 1 2. 0 10. 7 5. 3 4. 7 4. 0 2. 7 Содержание добавок (вес. %) к Al In Bi-2. 0 Bi-4. 0 3. 9 2. 0 1. 7 1. 5 0. 9 Sn 1. 0 2. 1 2. 2 5. 4 5. 8 6. 2 7. 0 Zn Pb-1. 0 Pb-2. 1 3. 9 7. 3 7. 8 8. 3 9. 4 Кривые выделения H 2 при дозировании раствора H 2 SO 4 к суспензии Mg. H 2 порциями по 1 мл/мин, 7 мл/мин (пунктир) и 14 мл/мин (○).
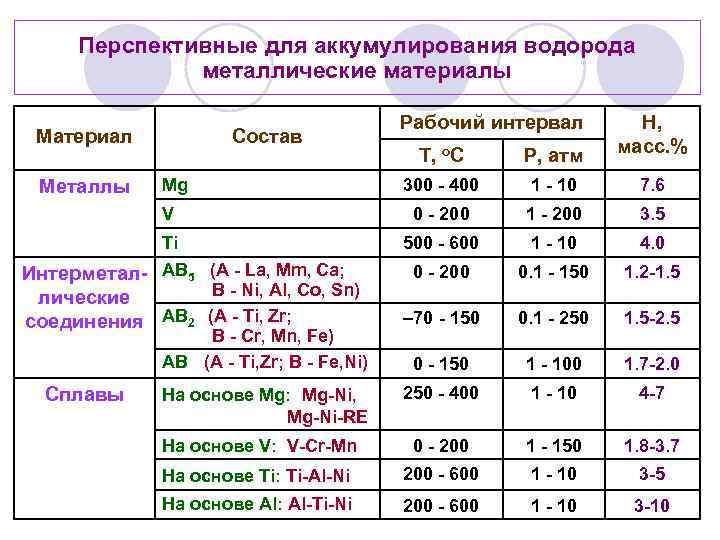
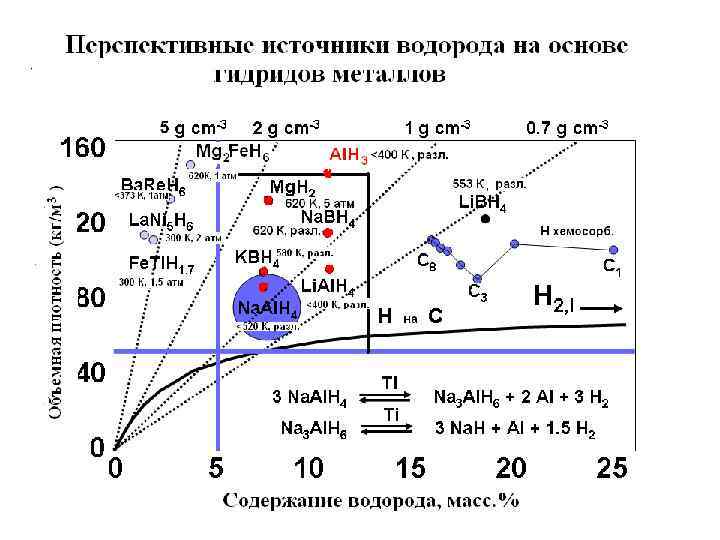
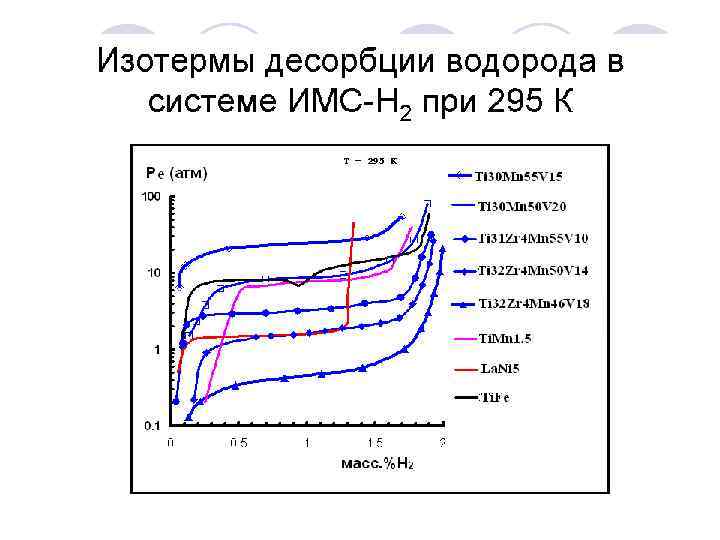
Перспективные для аккумулирования водорода металлические материалы Материал Состав Рабочий интервал H, масс. % P, атм 300 - 400 1 - 10 7. 6 V 0 - 200 1 - 200 3. 5 Ti Металлы T, o. C 500 - 600 1 - 10 4. 0 0 - 200 0. 1 - 150 1. 2 -1. 5 – 70 - 150 0. 1 - 250 1. 5 -2. 5 0 - 150 1 - 100 1. 7 -2. 0 250 - 400 1 - 10 4 -7 На основе V: V-Cr-Mn 0 - 200 1 - 150 1. 8 -3. 7 На основе Ti: Ti-Al-Ni 200 - 600 1 - 10 3 -5 На основе Al: Al-Ti-Ni 200 - 600 1 - 10 3 -10 Mg Интерметал- AB 5 (A - La, Mm, Ca; B - Ni, Al, Co, Sn) лические соединения AB 2 (A - Ti, Zr; B - Cr, Mn, Fe) AB (A - Ti, Zr; B - Fe, Ni) Сплавы На основе Mg: Mg-Ni, Mg-Ni-RE

Примеры сборок топливных элементов Amfc 4 c stack 20 ячеек, Электроды: 10 x 10 cm 40 ячеек, Электроды: 16 x 16 cm
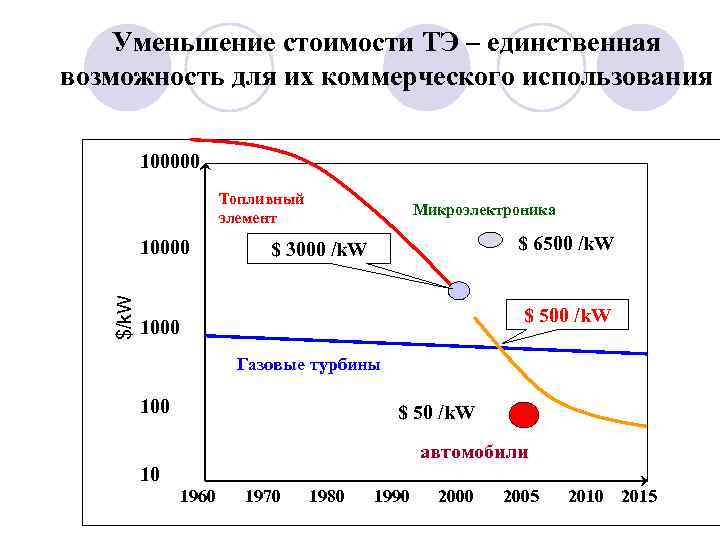
Уменьшение стоимости ТЭ – единственная возможность для их коммерческого использования 100000 Топливный элемент $/k. W 10000 Микроэлектроника $ 6500 /k. W $ 3000 /k. W $ 500 /k. W 1000 Газовые турбины 100 $ 50 /k. W автомобили 10 1960 1970 1980 1990 2005 2010 2015

Цели для гражданского применения Mobile Audio Cellular Phone 1 W PDA Digital Camera 3 W завтра 5 W Video Camera 10 W 30 W Цели сегодняшнего дня Notebook computer 50 W Cordless tools 50 k. W FC Car 2 k. W 1 k. W UPS Home power generator 300 W Electric bicycle 100 W Steam Cleaner Codeless cleaner

Устройство для зарядки сотовых телефонов фирмы Angstrom на водороде
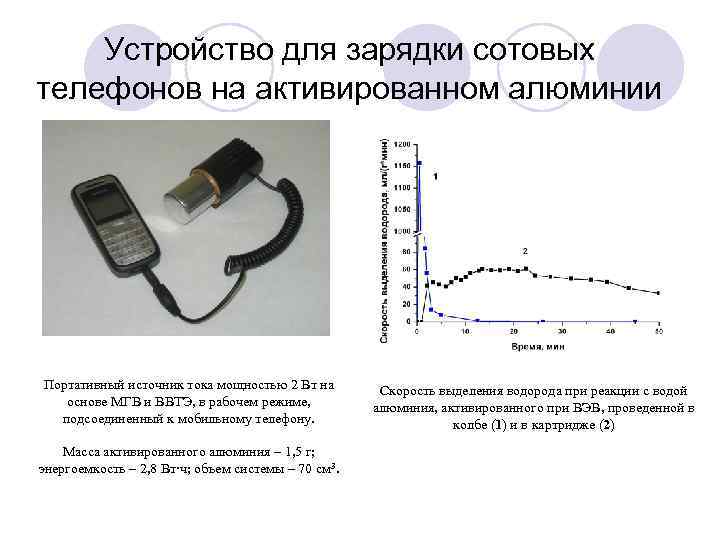
Устройство для зарядки сотовых телефонов на активированном алюминии Портативный источник тока мощностью 2 Вт на основе МГВ и ВВТЭ, в рабочем режиме, подсоединенный к мобильному телефону. Масса активированного алюминия – 1, 5 г; энергоемкость – 2, 8 Вт∙ч; объем системы – 70 см 3. Скорость выделения водорода при реакции с водой алюминия, активированного при ВЭВ, проведенной в колбе (1) и в картридже (2)

Немецкая подводная лодка типа 212 с энергетической установкой на топливных элементах Атакующая субмарина U 212 / U 214 Два 120 k. W топливных элемента фирмы Siemens Автономность плавания 2 недели Резервуары Н 2 и О 2 расположены вне основного корпуса

Development of Fuel Cell-Based Power Plants at RSC Energia 2000 2001 RSC Energia, UEIP, Auto. VAZ Power Plant with forced alkaline ECG FOTON and compressed hydrogen and oxygen storage for fivedoor NIVA LADA-ANTEL-1 Nlong-dur = 15 к. W, Npeak = 25 к. W, U = 115 150 V, Р = 300 кg/сm 2, one fueling range= 220 кm ECG control unit Oxygen Supply Unit Hydrogen tank Nitrogen Tank Hydrogen Supply Unit ECG Power Unit Control System Oxygen Tank

Проблемы водородной энергетики (вопросы на экзамене) 1. Методы получения водорода: преимущества, недостатки. 2. Методы хранения водорода, основанные на физических процессах. 3. Методы хранения водорода, основанные на хемосорбционных процессах и реакциях. 4. Типы и свойства аккумулирующих материалов на основе гидридов. 5. Типы химических источников тока. Водородный топливный элемент, принцип действия, проблемы
Водородная энергетика _лекция_4 курс_2013.ppt