09_vodorod.ppt
- Количество слайдов: 24
 Водород Н – самый распространенный элемент Вселенной, 5 место на Земле. Вода, минералы, все живые существа. Положение в ПС: Н: 1 s 1, 1 группа или 17 группа? 1 группа: один валентный электрон образует H+, но неметалл. 17 группа: H- – гидрид ион (X-), H 2 (Х 2)
Водород Н – самый распространенный элемент Вселенной, 5 место на Земле. Вода, минералы, все живые существа. Положение в ПС: Н: 1 s 1, 1 группа или 17 группа? 1 группа: один валентный электрон образует H+, но неметалл. 17 группа: H- – гидрид ион (X-), H 2 (Х 2)
 Изотопы водорода 1 H – протий; 2 H – дейтерий (D); 3 H – тритий (T) T – радиоактивный изотоп, 1/2 = 12, 4 года производство трития для термоядерного оружия. Ткип для Н 2 = -252, 8 о. С; Ткип для D 2 = -249, 7 о. С. Ткип для Н 2 O = 100, 00 о. С; Ткип для D 2 O = 101, 42 о. С
Изотопы водорода 1 H – протий; 2 H – дейтерий (D); 3 H – тритий (T) T – радиоактивный изотоп, 1/2 = 12, 4 года производство трития для термоядерного оружия. Ткип для Н 2 = -252, 8 о. С; Ткип для D 2 = -249, 7 о. С. Ткип для Н 2 O = 100, 00 о. С; Ткип для D 2 O = 101, 42 о. С
 Изотопный эффект Влияние на скорости реакций (образуются или разрываются связи с участием водорода): 2 H+ + 2 e H 2; 2 D+ + 2 e D 2 идет медленнее c D, можно сконцентрировать D 2 O! Колебательная спектроскопия: частота колебаний связи Э–D всегда меньше, чем для связи Э–Н:
Изотопный эффект Влияние на скорости реакций (образуются или разрываются связи с участием водорода): 2 H+ + 2 e H 2; 2 D+ + 2 e D 2 идет медленнее c D, можно сконцентрировать D 2 O! Колебательная спектроскопия: частота колебаний связи Э–D всегда меньше, чем для связи Э–Н:
 Получение диводорода Газификация угля ( «водяной газ» , 1000 о. С): C + H 2 O CO + H 2 (соотношение 1: 1); для увеличения доли диводорода (450ºС, Fe 2 O 3 кат-р): CO + H 2 O CO 2 + H 2; (отмывка от СО 2 водой или р-ром К 2 СО 3) Каталитическая конверсия метана водяным паром ( «синтез-газ» , Ni кат-р, 1000 ºС): CH 4 + H 2 O CO + 3 H 2 (соотношение 1: 3); электролиз воды (электролит H 2 SO 4, Na. OH, Na 2 SO 4): H 2 O H 2 + 1/2 O 2
Получение диводорода Газификация угля ( «водяной газ» , 1000 о. С): C + H 2 O CO + H 2 (соотношение 1: 1); для увеличения доли диводорода (450ºС, Fe 2 O 3 кат-р): CO + H 2 O CO 2 + H 2; (отмывка от СО 2 водой или р-ром К 2 СО 3) Каталитическая конверсия метана водяным паром ( «синтез-газ» , Ni кат-р, 1000 ºС): CH 4 + H 2 O CO + 3 H 2 (соотношение 1: 3); электролиз воды (электролит H 2 SO 4, Na. OH, Na 2 SO 4): H 2 O H 2 + 1/2 O 2
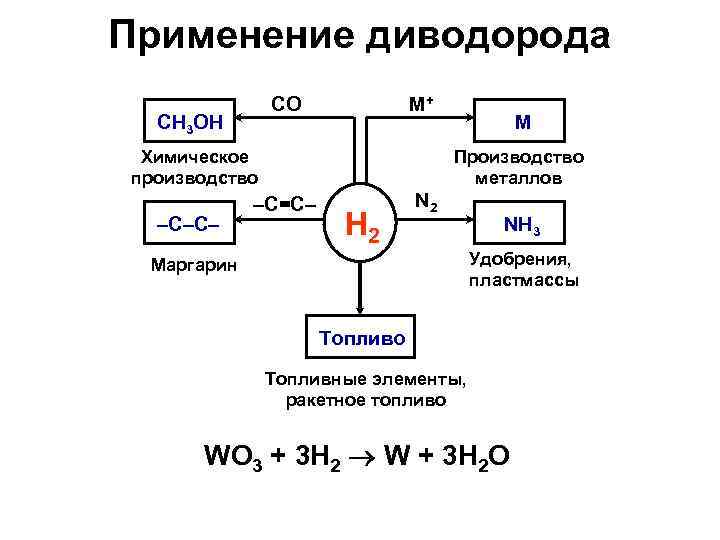 Применение диводорода CO CH 3 OH M+ Химическое производство –C–C– M Производство металлов –C=C– H 2 NH 3 Удобрения, пластмассы Маргарин Топливо Топливные элементы, ракетное топливо WO 3 + 3 H 2 W + 3 H 2 O
Применение диводорода CO CH 3 OH M+ Химическое производство –C–C– M Производство металлов –C=C– H 2 NH 3 Удобрения, пластмассы Маргарин Топливо Топливные элементы, ракетное топливо WO 3 + 3 H 2 W + 3 H 2 O
 Водородная энергетика Основной вид топлива – диводород, получаемый из воды (электролиз воды или фотохимическое разложение воды в присутствии солнечного света и катализаторов типа Ti. O 2). 2 H 2 + O 2 2 H 2 O Проблема глобального потепления (? )
Водородная энергетика Основной вид топлива – диводород, получаемый из воды (электролиз воды или фотохимическое разложение воды в присутствии солнечного света и катализаторов типа Ti. O 2). 2 H 2 + O 2 2 H 2 O Проблема глобального потепления (? )
 Основные типы соединений Степень окисления Электронная конфиг. Примеры Ox/red свойства 0 H, 1 s 1 H 2, H восстановитель, редко окислитель +1 H+ H 2 O, HCl, KOH только окислитель -1 H-, 1 s 2 Na. H, Ca. H 2, сильный Na. BH 4 восстановитель
Основные типы соединений Степень окисления Электронная конфиг. Примеры Ox/red свойства 0 H, 1 s 1 H 2, H восстановитель, редко окислитель +1 H+ H 2 O, HCl, KOH только окислитель -1 H-, 1 s 2 Na. H, Ca. H 2, сильный Na. BH 4 восстановитель
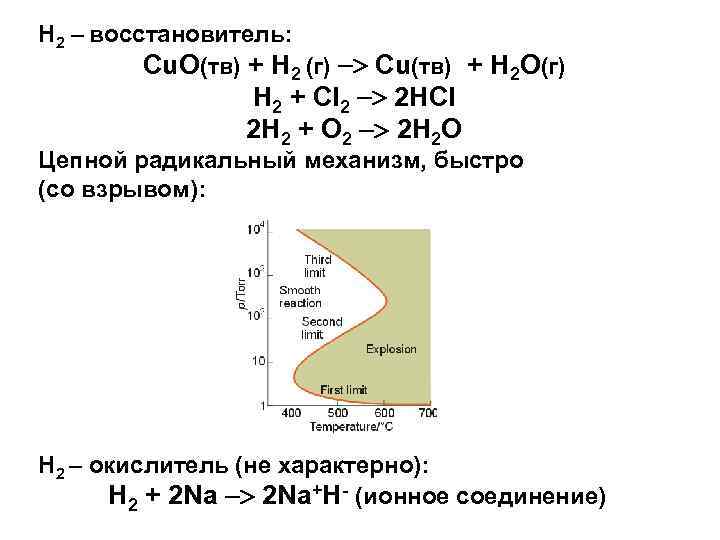 Н 2 – восстановитель: Cu. O(тв) + H 2 (г) Cu(тв) + H 2 O(г) H 2 + Cl 2 2 HCl 2 H 2 + O 2 2 H 2 O Цепной радикальный механизм, быстро (со взрывом): Н 2 – окислитель (не характерно): H 2 + 2 Na+H- (ионное соединение)
Н 2 – восстановитель: Cu. O(тв) + H 2 (г) Cu(тв) + H 2 O(г) H 2 + Cl 2 2 HCl 2 H 2 + O 2 2 H 2 O Цепной радикальный механизм, быстро (со взрывом): Н 2 – окислитель (не характерно): H 2 + 2 Na+H- (ионное соединение)
 Н+ - только окислитель: 2 HCl + Zn Zn. Cl 2 + H 2 2 H+ + 2 e H 2 Н- – сильный восстановитель: Na. H + H 2 O Na. OH + H 2 Способность к комплексообразованию: Н+– акцептор электронной пары – Н 3 О+, NH 4+; H– – донор электронной пары – [BH 4]-, [Al. H 4]-
Н+ - только окислитель: 2 HCl + Zn Zn. Cl 2 + H 2 2 H+ + 2 e H 2 Н- – сильный восстановитель: Na. H + H 2 O Na. OH + H 2 Способность к комплексообразованию: Н+– акцептор электронной пары – Н 3 О+, NH 4+; H– – донор электронной пары – [BH 4]-, [Al. H 4]-
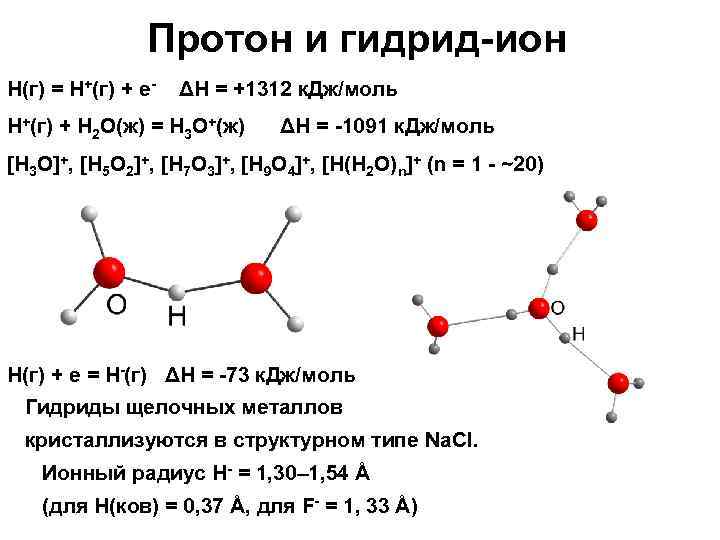 Протон и гидрид-ион H(г) = Н+(г) + е- ΔН = +1312 к. Дж/моль H+(г) + H 2 O(ж) = H 3 O+(ж) ΔН = -1091 к. Дж/моль [H 3 O]+, [H 5 O 2]+, [H 7 O 3]+, [H 9 O 4]+, [H(H 2 O)n]+ (n = 1 - ~20) H(г) + е = Н-(г) ΔН = -73 к. Дж/моль Гидриды щелочных металлов кристаллизуются в структурном типе Na. Cl. Ионный радиус Н- = 1, 30– 1, 54 Å (для Н(ков) = 0, 37 Å, для F- = 1, 33 Å)
Протон и гидрид-ион H(г) = Н+(г) + е- ΔН = +1312 к. Дж/моль H+(г) + H 2 O(ж) = H 3 O+(ж) ΔН = -1091 к. Дж/моль [H 3 O]+, [H 5 O 2]+, [H 7 O 3]+, [H 9 O 4]+, [H(H 2 O)n]+ (n = 1 - ~20) H(г) + е = Н-(г) ΔН = -73 к. Дж/моль Гидриды щелочных металлов кристаллизуются в структурном типе Na. Cl. Ионный радиус Н- = 1, 30– 1, 54 Å (для Н(ков) = 0, 37 Å, для F- = 1, 33 Å)
 Реакции диводорода Низкая реакционная способность H 2. Гомолитический разрыв связи Н–Н: H–H H. + H. ΔHo = 434 к. Дж/моль
Реакции диводорода Низкая реакционная способность H 2. Гомолитический разрыв связи Н–Н: H–H H. + H. ΔHo = 434 к. Дж/моль
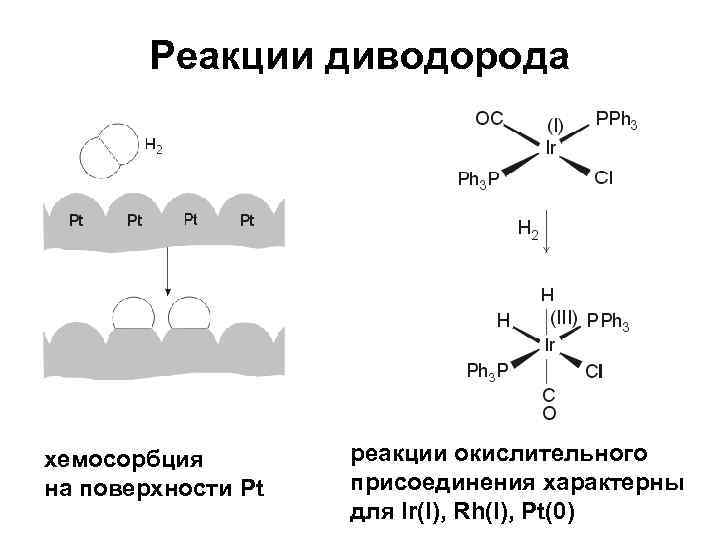 Реакции диводорода хемосорбция на поверхности Pt реакции окислительного присоединения характерны для Ir(I), Rh(I), Pt(0)
Реакции диводорода хемосорбция на поверхности Pt реакции окислительного присоединения характерны для Ir(I), Rh(I), Pt(0)
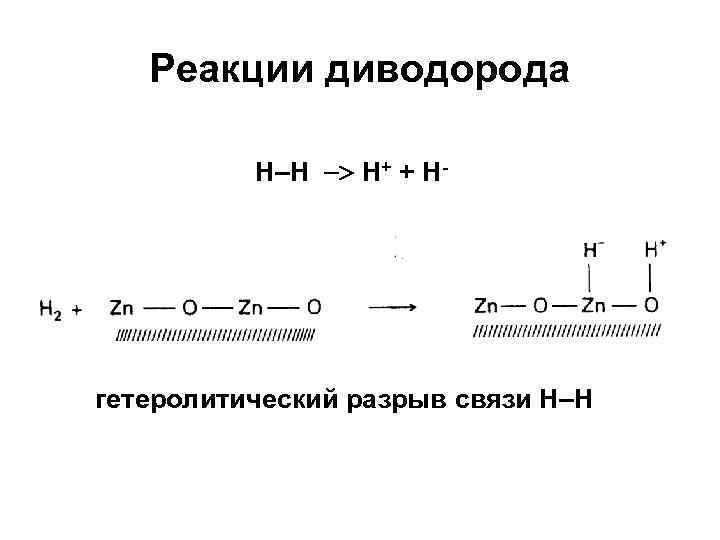 Реакции диводорода H–H H+ + H- гетеролитический разрыв связи Н–Н
Реакции диводорода H–H H+ + H- гетеролитический разрыв связи Н–Н
![Диводород как лиганд [W(CO)3(H 2)(i-Pr 3 P)2] Диводород как лиганд [W(CO)3(H 2)(i-Pr 3 P)2]](https://present5.com/presentation/-101808234_421403513/image-14.jpg) Диводород как лиганд [W(CO)3(H 2)(i-Pr 3 P)2]
Диводород как лиганд [W(CO)3(H 2)(i-Pr 3 P)2]
 Бинарные соединения с водородом • • • Молекулярные соединения; Ионные гидриды; Металлоподобные гидриды
Бинарные соединения с водородом • • • Молекулярные соединения; Ионные гидриды; Металлоподобные гидриды
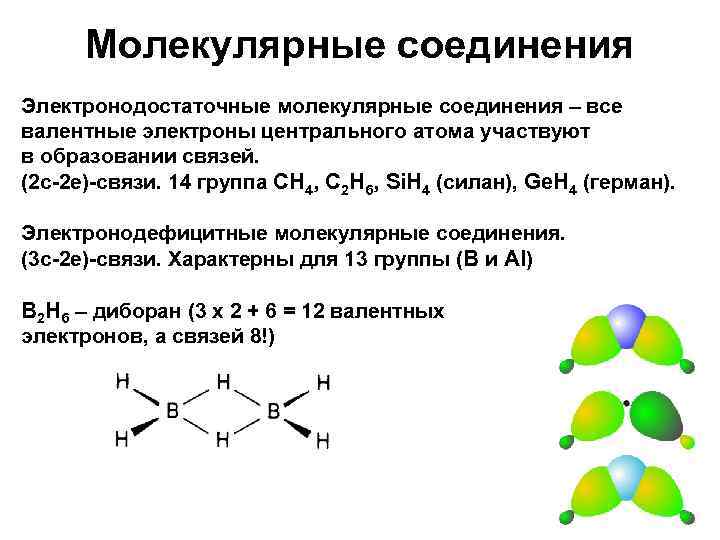 Молекулярные соединения Электронодостаточные молекулярные соединения – все валентные электроны центрального атома участвуют в образовании связей. (2 с-2 е)-связи. 14 группа CH 4, C 2 H 6, Si. H 4 (силан), Ge. H 4 (герман). Электронодефицитные молекулярные соединения. (3 с-2 е)-связи. Характерны для 13 группы (B и Al) B 2 H 6 – диборан (3 х 2 + 6 = 12 валентных электронов, а связей 8!)
Молекулярные соединения Электронодостаточные молекулярные соединения – все валентные электроны центрального атома участвуют в образовании связей. (2 с-2 е)-связи. 14 группа CH 4, C 2 H 6, Si. H 4 (силан), Ge. H 4 (герман). Электронодефицитные молекулярные соединения. (3 с-2 е)-связи. Характерны для 13 группы (B и Al) B 2 H 6 – диборан (3 х 2 + 6 = 12 валентных электронов, а связей 8!)
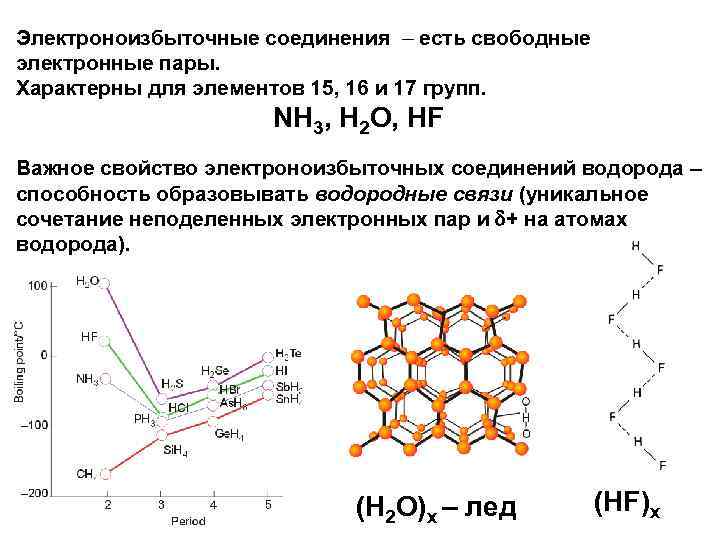 Электроноизбыточные соединения – есть свободные электронные пары. Характерны для элементов 15, 16 и 17 групп. NH 3, H 2 O, HF Важное свойство электроноизбыточных соединений водорода – способность образовывать водородные связи (уникальное сочетание неподеленных электронных пар и + на атомах водорода). (H 2 O)x – лед (HF)x
Электроноизбыточные соединения – есть свободные электронные пары. Характерны для элементов 15, 16 и 17 групп. NH 3, H 2 O, HF Важное свойство электроноизбыточных соединений водорода – способность образовывать водородные связи (уникальное сочетание неподеленных электронных пар и + на атомах водорода). (H 2 O)x – лед (HF)x
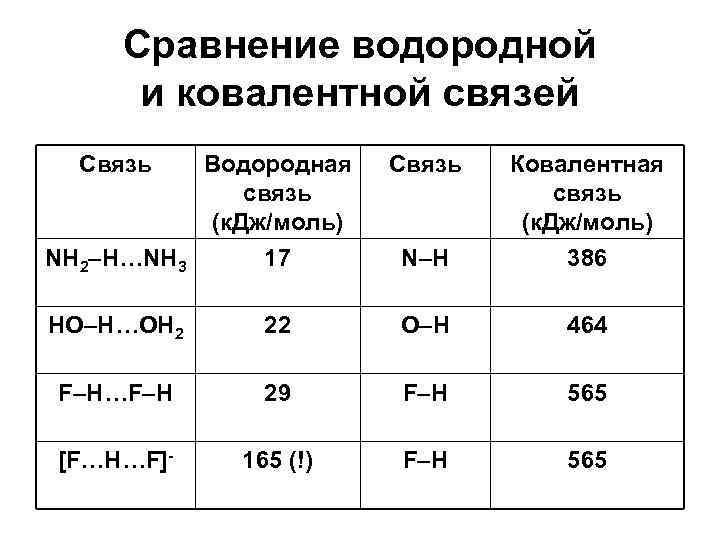 Сравнение водородной и ковалентной связей Связь NH 2–H…NH 3 Водородная связь (к. Дж/моль) 17 N–H Ковалентная связь (к. Дж/моль) 386 HO–H…OH 2 22 O–H 464 F–H…F–H 29 F–H 565 [F…H…F]- 165 (!) F–H 565
Сравнение водородной и ковалентной связей Связь NH 2–H…NH 3 Водородная связь (к. Дж/моль) 17 N–H Ковалентная связь (к. Дж/моль) 386 HO–H…OH 2 22 O–H 464 F–H…F–H 29 F–H 565 [F…H…F]- 165 (!) F–H 565
![[Cl–H…. Cl]1, 37 Å 1, 85 Å [F…. H…. F]1, 13 Å [Cl–H…. Cl]1, 37 Å 1, 85 Å [F…. H…. F]1, 13 Å](https://present5.com/presentation/-101808234_421403513/image-19.jpg) [Cl–H…. Cl]1, 37 Å 1, 85 Å [F…. H…. F]1, 13 Å
[Cl–H…. Cl]1, 37 Å 1, 85 Å [F…. H…. F]1, 13 Å
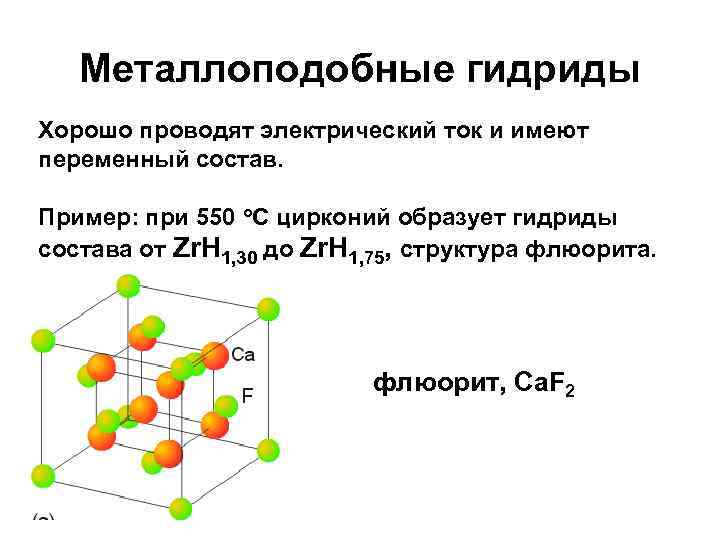 Металлоподобные гидриды Хорошо проводят электрический ток и имеют переменный состав. Пример: при 550 о. С цирконий образует гидриды состава от Zr. H 1, 30 до Zr. H 1, 75, структура флюорита. флюорит, Ca. F 2
Металлоподобные гидриды Хорошо проводят электрический ток и имеют переменный состав. Пример: при 550 о. С цирконий образует гидриды состава от Zr. H 1, 30 до Zr. H 1, 75, структура флюорита. флюорит, Ca. F 2
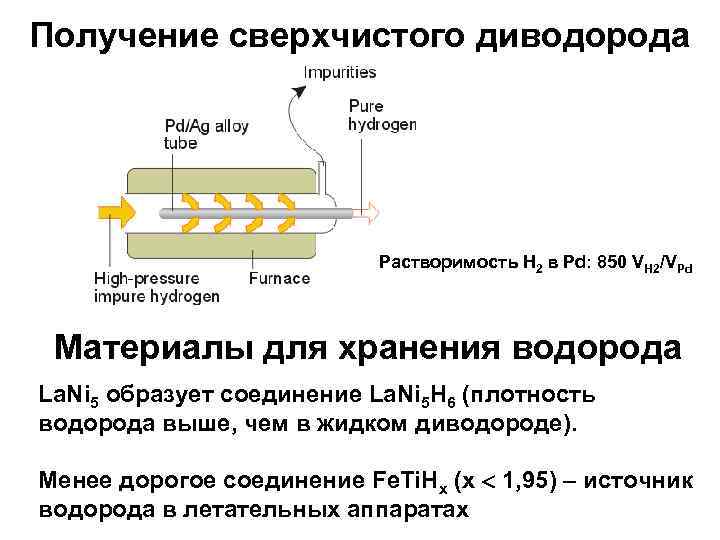 Получение сверхчистого диводорода Растворимость Н 2 в Pd: 850 VH 2/VPd Материалы для хранения водорода La. Ni 5 образует соединение La. Ni 5 H 6 (плотность водорода выше, чем в жидком диводороде). Менее дорогое соединение Fe. Ti. Hx (x 1, 95) – источник водорода в летательных аппаратах
Получение сверхчистого диводорода Растворимость Н 2 в Pd: 850 VH 2/VPd Материалы для хранения водорода La. Ni 5 образует соединение La. Ni 5 H 6 (плотность водорода выше, чем в жидком диводороде). Менее дорогое соединение Fe. Ti. Hx (x 1, 95) – источник водорода в летательных аппаратах
 Атомарный водород “Н” Более реакционноспособен, чем Н 2. Получение: 1) из диводорода в электрическом разряде; 2) водород в момент выделения Mn. O 4 - + H 2 + H+ НЕТ реакции Mn. O 4 - + 5”H” + 3 H+ Mn 2+ + 4 H 2 O
Атомарный водород “Н” Более реакционноспособен, чем Н 2. Получение: 1) из диводорода в электрическом разряде; 2) водород в момент выделения Mn. O 4 - + H 2 + H+ НЕТ реакции Mn. O 4 - + 5”H” + 3 H+ Mn 2+ + 4 H 2 O
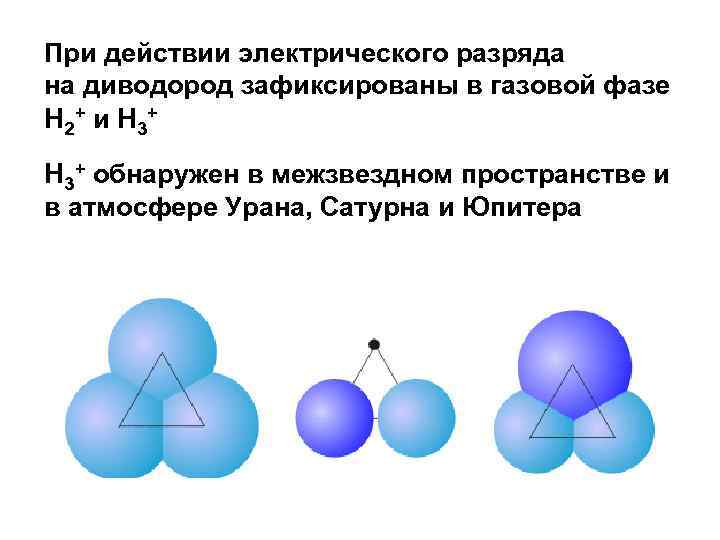 При действии электрического разряда на диводород зафиксированы в газовой фазе H 2+ и H 3+ обнаружен в межзвездном пространстве и в атмосфере Урана, Сатурна и Юпитера
При действии электрического разряда на диводород зафиксированы в газовой фазе H 2+ и H 3+ обнаружен в межзвездном пространстве и в атмосфере Урана, Сатурна и Юпитера
 Орто- и параводород T = 200 o. C; 25 % пара-H 2 T = -253 o. C; 99, 8 % пара-H 2 Катализатор активированный уголь. Технология получения пара-H 2 (чл. -корр. РАН Р. А. Буянов)
Орто- и параводород T = 200 o. C; 25 % пара-H 2 T = -253 o. C; 99, 8 % пара-H 2 Катализатор активированный уголь. Технология получения пара-H 2 (чл. -корр. РАН Р. А. Буянов)


