 ВОДНЫЙ РЕЖИМ РАСТИТЕЛЬНОЙ КЛЕТКИ 1. ЗАКОНОМЕРНОСТИ ОСМОСА. 2. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ. 3. РАСТИТЕЛЬНАЯ КЛЕТКА КАК ОСМОТИЧЕСКАЯ СИСТЕМА.
ВОДНЫЙ РЕЖИМ РАСТИТЕЛЬНОЙ КЛЕТКИ 1. ЗАКОНОМЕРНОСТИ ОСМОСА. 2. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ. 3. РАСТИТЕЛЬНАЯ КЛЕТКА КАК ОСМОТИЧЕСКАЯ СИСТЕМА.
 ЗАКОНОМЕРНОСТИ ОСМОСА Рене Жоакен Анри Дютроше (Rene Joachim Henri Dutrochet, 1776 -1847) Французский врач, ботаник и физиолог. Известен многочисленными работами по физиологии животных и растений. осмометр Дютроше Вильгельм Пфеффер (Wilhelm Friedrich Philipp Pfeffer, 1845 -1920) Немецкий химик, ботаник, физиолог растений. Исследовал обмен веществ и превращение энергии в растениях. Ряд важных работ посвящены осмосу и его роли в дыхании и питании растений. осмометр ( «искусственная клетка» ) Пфеффера
ЗАКОНОМЕРНОСТИ ОСМОСА Рене Жоакен Анри Дютроше (Rene Joachim Henri Dutrochet, 1776 -1847) Французский врач, ботаник и физиолог. Известен многочисленными работами по физиологии животных и растений. осмометр Дютроше Вильгельм Пфеффер (Wilhelm Friedrich Philipp Pfeffer, 1845 -1920) Немецкий химик, ботаник, физиолог растений. Исследовал обмен веществ и превращение энергии в растениях. Ряд важных работ посвящены осмосу и его роли в дыхании и питании растений. осмометр ( «искусственная клетка» ) Пфеффера
 ОСМОС Осмос – процесс диффузии растворителя (т. е. воды) в раствор, отделённый полупроницаемой мембраной. При осмосе вода движется через мембрану по градиенту осмотического потенциала, т. е. в сторону более концентрированного раствора. Осмотический потенциал (Ψосм) – энергетический показатель молекул воды, определяющий направление тока воды через мембрану. Чем выше концентрация растворенных веществ, тем Ψосм меньше. Осмотическое давление (Pосм или π) – это давление, которое оказывает раствор на мембрану в осмотической системе. Численно равно давлению, которое нужно приложить к раствору, чтобы прекратилось поступление в него воды.
ОСМОС Осмос – процесс диффузии растворителя (т. е. воды) в раствор, отделённый полупроницаемой мембраной. При осмосе вода движется через мембрану по градиенту осмотического потенциала, т. е. в сторону более концентрированного раствора. Осмотический потенциал (Ψосм) – энергетический показатель молекул воды, определяющий направление тока воды через мембрану. Чем выше концентрация растворенных веществ, тем Ψосм меньше. Осмотическое давление (Pосм или π) – это давление, которое оказывает раствор на мембрану в осмотической системе. Численно равно давлению, которое нужно приложить к раствору, чтобы прекратилось поступление в него воды.
 ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ Якоб Хендрик Вант-Гофф (Jacobus Henricus (Henry) van't Hoff, 1852 -1911) Голландский химик, один из основателей стереохимии и химической кинетики. Первый лауреат Нобелевской премии по химии (1901 г. ) «В знак признания огромной важности открытия законов химической динамики и осмотического давления в растворах» . Pосм = RTci, где: Pосм – осмотическое давление [Па, атм, бар*] R – универсальная газовая постоянная [8, 31· 10 -3 к. Дж/град·моль] T – температура [К (273 + °С)] c – концентрация раствора [моль/л] i – изотонический коэффициент [отражает диссоциацию молекул в растворе, равен 1+α· (n-1), где α – степень электролитической диссоциации, n – число ионов, на которые распадается молекула электролита] * 1 Па = 1· 10 -3 к. Па = 1· 10 -6 м. Па = 9, 87· 10 -6 атм = 1· 10 -5 бар = 0, 0075 мм. рт. ст.
ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ Якоб Хендрик Вант-Гофф (Jacobus Henricus (Henry) van't Hoff, 1852 -1911) Голландский химик, один из основателей стереохимии и химической кинетики. Первый лауреат Нобелевской премии по химии (1901 г. ) «В знак признания огромной важности открытия законов химической динамики и осмотического давления в растворах» . Pосм = RTci, где: Pосм – осмотическое давление [Па, атм, бар*] R – универсальная газовая постоянная [8, 31· 10 -3 к. Дж/град·моль] T – температура [К (273 + °С)] c – концентрация раствора [моль/л] i – изотонический коэффициент [отражает диссоциацию молекул в растворе, равен 1+α· (n-1), где α – степень электролитической диссоциации, n – число ионов, на которые распадается молекула электролита] * 1 Па = 1· 10 -3 к. Па = 1· 10 -6 м. Па = 9, 87· 10 -6 атм = 1· 10 -5 бар = 0, 0075 мм. рт. ст.
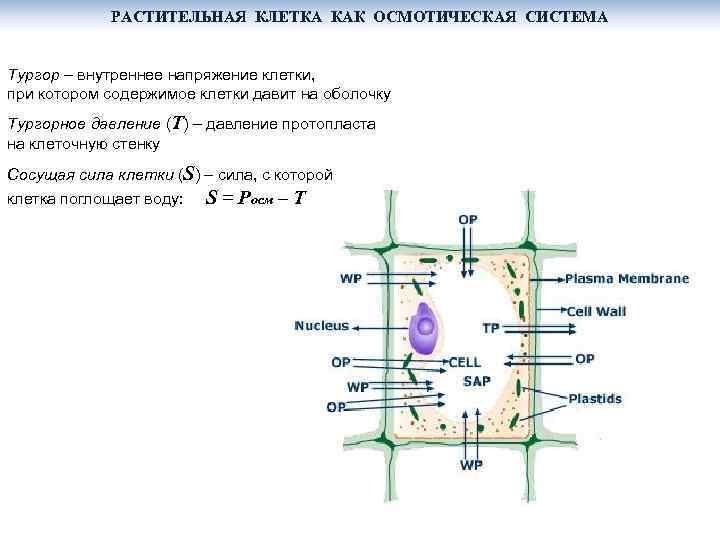 РАСТИТЕЛЬНАЯ КЛЕТКА КАК ОСМОТИЧЕСКАЯ СИСТЕМА Тургор – внутреннее напряжение клетки, при котором содержимое клетки давит на оболочку Тургорное давление (T) – давление протопласта на клеточную стенку Сосущая сила клетки (S) – сила, с которой клетка поглощает воду: S = Pосм – T
РАСТИТЕЛЬНАЯ КЛЕТКА КАК ОСМОТИЧЕСКАЯ СИСТЕМА Тургор – внутреннее напряжение клетки, при котором содержимое клетки давит на оболочку Тургорное давление (T) – давление протопласта на клеточную стенку Сосущая сила клетки (S) – сила, с которой клетка поглощает воду: S = Pосм – T
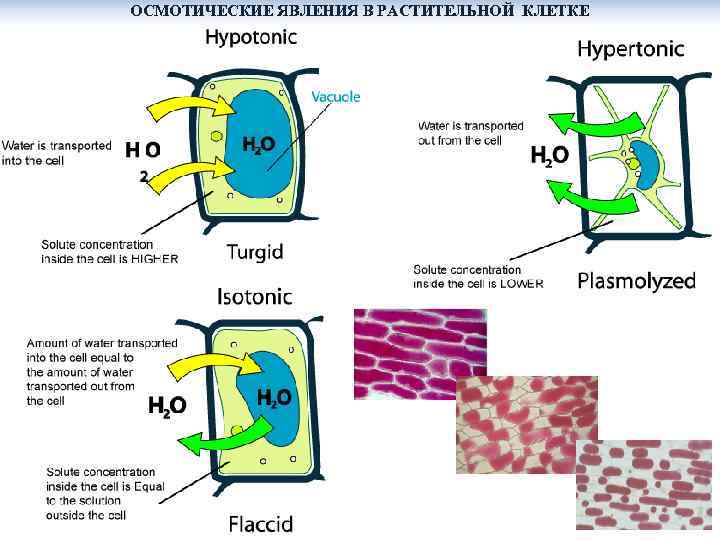 ОСМОТИЧЕСКИЕ ЯВЛЕНИЯ В РАСТИТЕЛЬНОЙ КЛЕТКЕ
ОСМОТИЧЕСКИЕ ЯВЛЕНИЯ В РАСТИТЕЛЬНОЙ КЛЕТКЕ
 ОСМОТИЧЕСКИЕ ПОКАЗАТЕЛИ У РАСТЕНИЙ РАЗНЫХ ЭКОЛОГИЧЕСКИХ ГРУПП Травянистые растения: Гидратофиты Гигрофиты Мезофиты Суккуленты Настоящие ксерофиты Галофиты 1 -10 атм (менее 1, 0 м. Па) 5 -15 атм (0, 5 -1, 5 м. Па) 5 -30 атм (0, 5 -3, 0 м. Па) 5 -20 атм (0, 5 -2, 0 м. Па) 15 -40 атм (1, 5 -4, 0 м. Па) 25 -50 атм (2, 5 -5, 0 м. Па) Древесные растения и кустарники: 10 -60 атм (1, 0 -6, 0 м. Па)
ОСМОТИЧЕСКИЕ ПОКАЗАТЕЛИ У РАСТЕНИЙ РАЗНЫХ ЭКОЛОГИЧЕСКИХ ГРУПП Травянистые растения: Гидратофиты Гигрофиты Мезофиты Суккуленты Настоящие ксерофиты Галофиты 1 -10 атм (менее 1, 0 м. Па) 5 -15 атм (0, 5 -1, 5 м. Па) 5 -30 атм (0, 5 -3, 0 м. Па) 5 -20 атм (0, 5 -2, 0 м. Па) 15 -40 атм (1, 5 -4, 0 м. Па) 25 -50 атм (2, 5 -5, 0 м. Па) Древесные растения и кустарники: 10 -60 атм (1, 0 -6, 0 м. Па)