водный режим-1.ppt
- Количество слайдов: 38

ВОДНЫЙ ОБМЕН-1

Функции воды в растении Жизнь на Земле зародилась только благодаря воде. Водная среда является основой для протекания большинства процессов, происходящих в клетках животных и растительных организмов. Вводная фаза объединяет все клетки и ткани организма в единое целое. Вода составляет от 80 до 95% массы растущих тканей, в семенах же ее - 5 до 15%. Для увеличения биомассы на 1 г через растение «прокачивается» до 500 г воды. ВОДА: участвует в построении и упорядочении мембран; гидратирует белки, нуклеиновые кислоты и полисахариды; является основным растворителем и активным метаболитом многих биохимических процессов; служит донором электронов и протонов при фотосинтезе; принимает участие в процессах гидролиза, окисления, а в ряде случаев и синтеза. Передвижение веществ по растению в сосудах ксилемы и ситовидных трубках осуществляется в водной среде. Обладая высокой теплоемкостью и большой удельной теплотой парообразования, вода обеспечивает терморегуляцию растительного организма. Благодаря явлениям осмоса и тургорному давлению вода обеспечивает упругое состояние клеток и тканей их защиту при механических воздействиях.

Структура и свойства воды В молекуле воды атом кислорода ковалентно связан с двумя атомами водорода. Две ковалентные связи О Н в молекуле воды формируют угол 105 о. Атом кислорода обладает большей способностью оттягивать на себя электроны ковалентной связи. В результате со стороны кислорода образуется отрицательный заряд, а со стороны каждого атома водорода положительный.
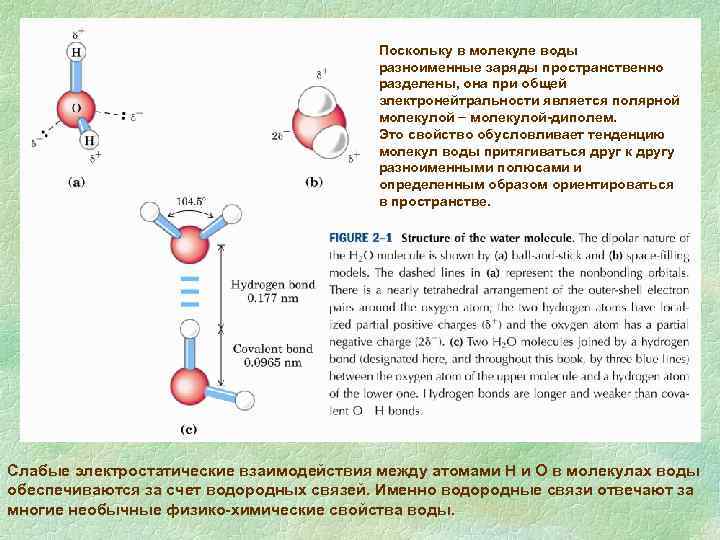
Поскольку в молекуле воды разноименные заряды пространственно разделены, она при общей электронейтральности является полярной молекулой-диполем. Это свойство обусловливает тенденцию молекул воды притягиваться друг к другу разноименными полюсами и определенным образом ориентироваться в пространстве. Слабые электростатические взаимодействия между атомами Н и О в молекулах воды обеспечиваются за счет водородных связей. Именно водородные связи отвечают за многие необычные физико-химические свойства воды.
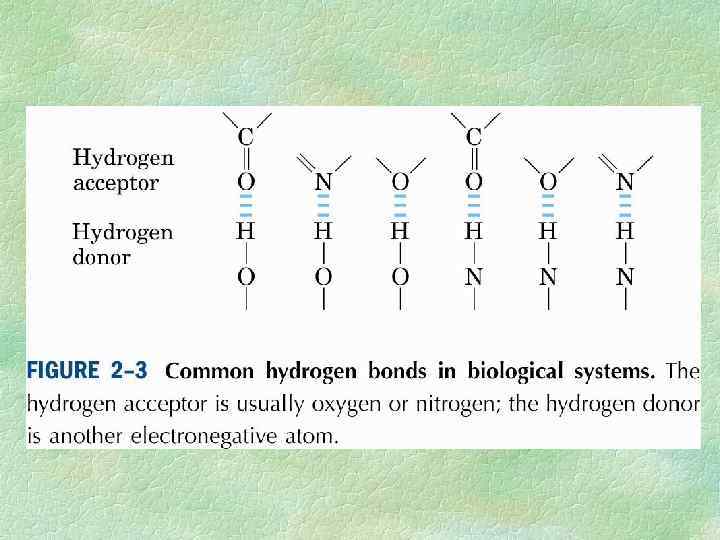
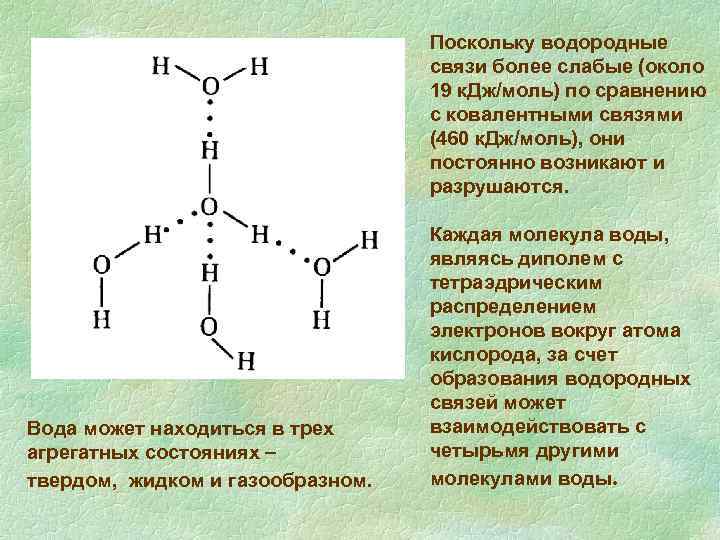
Поскольку водородные связи более слабые (около 19 к. Дж/моль) по сравнению с ковалентными связями (460 к. Дж/моль), они постоянно возникают и разрушаются. Вода может находиться в трех агрегатных состояниях твердом, жидком и газообразном. Каждая молекула воды, являясь диполем с тетраэдрическим распределением электронов вокруг атома кислорода, за счет образования водородных связей может взаимодействовать с четырьмя другими молекулами воды.
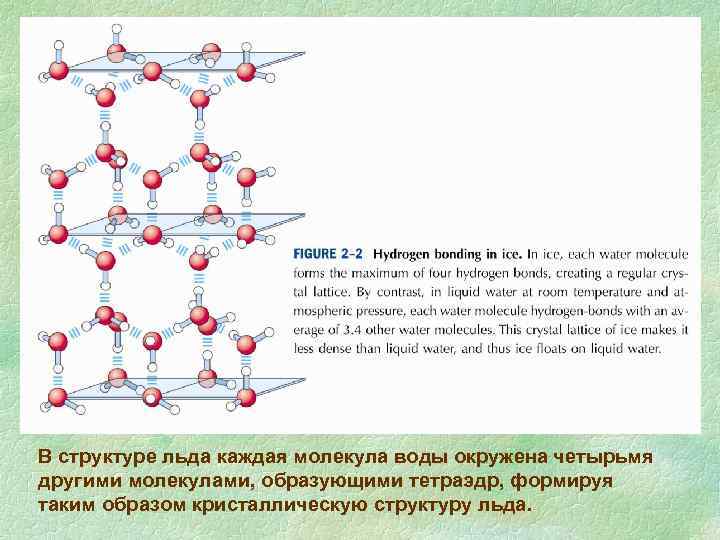
В структуре льда каждая молекула воды окружена четырьмя другими молекулами, образующими тетраэдр, формируя таким образом кристаллическую структуру льда.
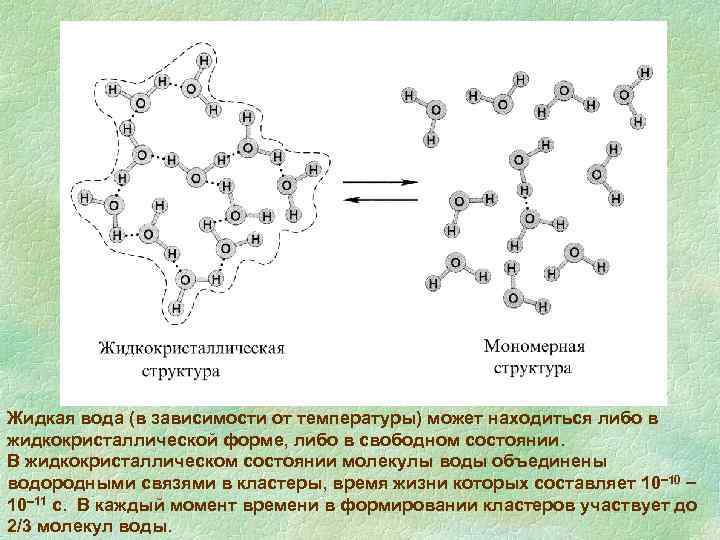
Жидкая вода (в зависимости от температуры) может находиться либо в жидкокристаллической форме, либо в свободном состоянии. В жидкокристаллическом состоянии молекулы воды объединены водородными связями в кластеры, время жизни которых составляет 10 10 11 с. В каждый момент времени в формировании кластеров участвует до 2/3 молекул воды.

Ионизация воды Поскольку электроны в молекуле воды сильнее связаны с кислородом, чем с водородом, происходит диссоциация воды: Н 2 О ↔ Н+ + ОН Однако свободный протон не способен к самостоятельному существованию и гидратируется молекулой воды с образованием иона гидроксония: Н+ + Н 2 О ↔ Н 3 О + Обычно ион Н+ переходит от одной молекулы воды к другой с образованием гидроксильного иона и иона гидроксония. Поэтому суммарная реакция запишется следующим образом: Н 2 О + Н 2 О ↔ ОН + Н 3 О+
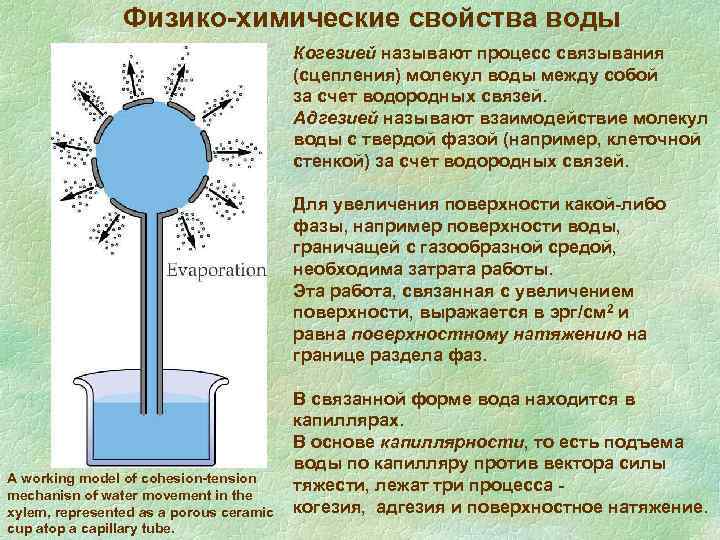
Физико-химические свойства воды Когезией называют процесс связывания (сцепления) молекул воды между собой за счет водородных связей. Адгезией называют взаимодействие молекул воды с твердой фазой (например, клеточной стенкой) за счет водородных связей. Для увеличения поверхности какой-либо фазы, например поверхности воды, граничащей с газообразной средой, необходима затрата работы. Эта работа, связанная с увеличением поверхности, выражается в эрг/см 2 и равна поверхностному натяжению на границе раздела фаз. A working model of cohesion-tension mechanisn of water movement in the xylem, represented as a porous ceramic cup atop a capillary tube. В связанной форме вода находится в капиллярах. В основе капиллярности, то есть подъема воды по капилляру против вектора силы тяжести, лежат три процесса когезия, адгезия и поверхностное натяжение.
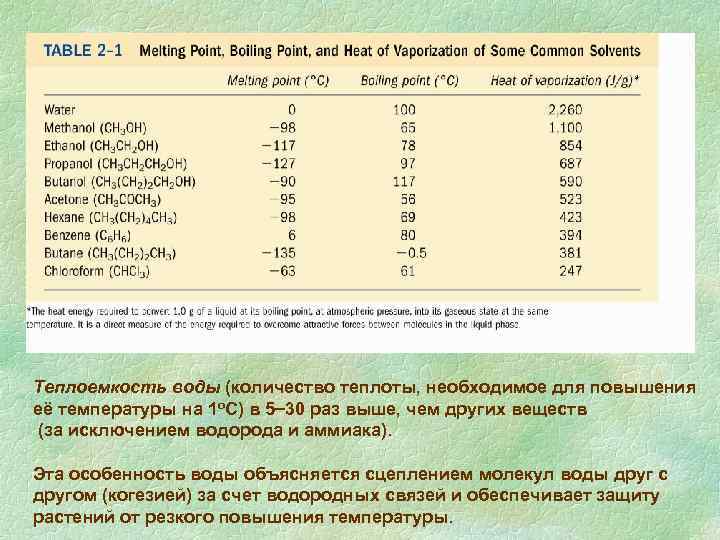
Теплоемкость воды (количество теплоты, необходимое для повышения её температуры на 1 о. С) в 5 30 раз выше, чем других веществ (за исключением водорода и аммиака). Эта особенность воды объясняется сцеплением молекул воды друг с другом (когезией) за счет водородных связей и обеспечивает защиту растений от резкого повышения температуры.
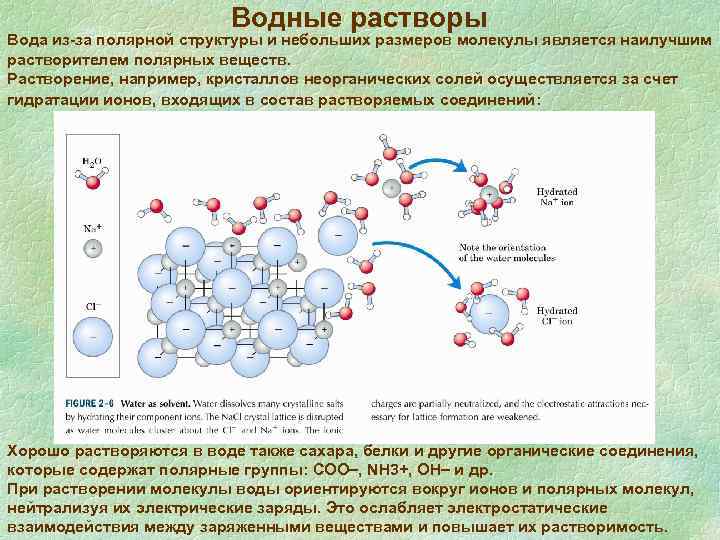
Водные растворы Вода из-за полярной структуры и небольших размеров молекулы является наилучшим растворителем полярных веществ. Растворение, например, кристаллов неорганических солей осуществляется за счет гидратации ионов, входящих в состав растворяемых соединений: Хорошо растворяются в воде также сахара, белки и другие органические соединения, которые содержат полярные группы: СОО , NН 3+, ОН и др. При растворении молекулы воды ориентируются вокруг ионов и полярных молекул, нейтрализуя их электрические заряды. Это ослабляет электростатические взаимодействия между заряженными веществами и повышает их растворимость.
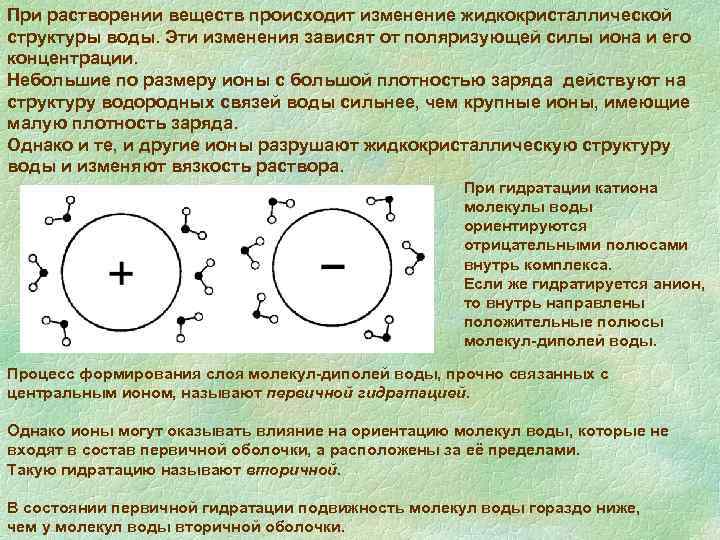
При растворении веществ происходит изменение жидкокристаллической структуры воды. Эти изменения зависят от поляризующей силы иона и его концентрации. Небольшие по размеру ионы с большой плотностью заряда действуют на структуру водородных связей воды сильнее, чем крупные ионы, имеющие малую плотность заряда. Однако и те, и другие ионы разрушают жидкокристаллическую структуру воды и изменяют вязкость раствора. При гидратации катиона молекулы воды ориентируются отрицательными полюсами внутрь комплекса. Если же гидратируется анион, то внутрь направлены положительные полюсы молекул-диполей воды. Процесс формирования слоя молекул-диполей воды, прочно связанных с центральным ионом, называют первичной гидратацией. Однако ионы могут оказывать влияние на ориентацию молекул воды, которые не входят в состав первичной оболочки, а расположены за её пределами. Такую гидратацию называют вторичной. В состоянии первичной гидратации подвижность молекул воды гораздо ниже, чем у молекул воды вторичной оболочки.

Вода, связанная с ионами, называется связанной осмотически и является важным элементом осмотического давления в клетках растений. При концентрации раствора более 1, 5 2 моль/л вторичные гидратные оболочки вокруг ионов начинают перекрываться и вода переходит в новую форму кристаллогидрат. Чем больше ионов в растворе, тем больше нарушается структура воды, меньше необходимо энергии для разрушения оставшихся водородных связей и тем меньше теплоемкость раствора.

Вода, оказавшаяся внутри макромолекул (иммобилизованная), может находиться в двух формах. Одна часть ее формирует слой первичной гидратации, а вторая сохраняет свойства обычной воды, но с ограниченной подвижностью. Молекулы белков гидратируются только в местах расположения полярных и ионизированных групп. Растворимость белков в воде варьирует в широких пределах и зависит от концентрации солей и р. Н.

Водный обмен растительных клеток Поглощение воды из внешней среды является обязательным условием существования любого живого организма. Поступление воды в клетки идет в результате осмоса, набухания биоколлоидов и увеличения степени их гидратации, а также активным путем. В тургесцентных клетках центральная вакуоль плотно прижимает цитоплазму к клеточной стенке, тем самым способствуя поддержанию формы клетки в мягких органах растения, например в листьях. При недостатке влаги вода выходит из вакуоли, что приводит к утрате тургора и увяданию.

Формы воды в растительных клетках Вода может находиться в клетках и тканях в двух состояниях: свободном и связанном. Свободная вода это чистая, лишенная каких-либо примесей вода с высокой подвижностью. Под связанной подразумевают содержащуюся в гетерогенных системах воду, которая не может служить растворителем и имеет ограниченную подвижность. Различают три формы связанного состояния воды: осмотически, коллоидно и капиллярно. Осмотически связанная вода участвует в гидратации растворяемых веществ. Коллоидно связанная вода включает интрамицеллярную воду и интермицеллярную воду. Т. о. может быть связано до 30 г воды на 1 г геля (например, сухого желатина). Даже при сильном обезвоживании большие количества воды удерживаются коллоидами, ионами и др. осмотически активными веществами. Капиллярно связанная вода находится в клеточных стенках и сосудах проводящей системы. В фазе клеточных стенок вода может находиться в свободном и связанном состоянии. Вода, удерживаемая в микрокапиллярах, а также связанная водородными связями с полисахаридами, малоподвижна. Свободная вода легко перемещается в крупных капиллярах между микрофибриллами целлюлозы.

Больше всего воды в растительной клетке (до 98%) концентрируется в вакуоли. Вакуолярный сок содержит сахара, органические кислоты, ионы, белки и другие соединения, которые связывают воду осмотически и как биоколлоиды. Вода в клетке может быть связана также пластидами, митохондриями и ядром, которые способны к самостоятельному регулированию своего водообмена за счет набухания или удерживания воды при обезвоживании клетки. В отличие от цитоплазмы содержание воды в пластидах и митохондриях обычно ниже (около 50%), что объясняется присутствием в них большого количества липидов и гидрофобных веществ.
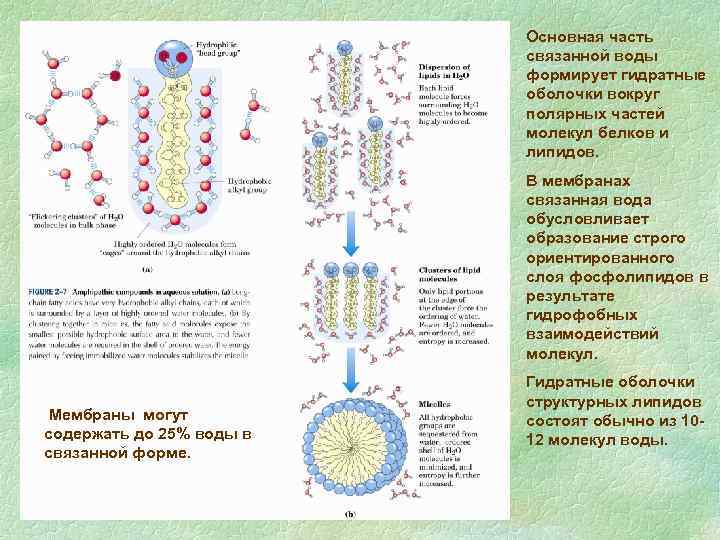
Основная часть связанной воды формирует гидратные оболочки вокруг полярных частей молекул белков и липидов. В мембранах связанная вода обусловливает образование строго ориентированного слоя фосфолипидов в результате гидрофобных взаимодействий молекул. Мембраны могут содержать до 25% воды в связанной форме. Гидратные оболочки структурных липидов состоят обычно из 1012 молекул воды.

Водный потенциал Энергетический уровень воды, как и любого другого вещества, отражаемый скоростью диффузии, называют химическим потенциалом, или, применительно к воде, водным потенциалом ( w). Водный потенциал является термодинамическим показателем состояния воды в системе и характеризует способность воды диффундировать, испаряться или поглощаться. Водный потенциал имеет размерность энергии, деленной на объем, его величину выражают в атмосферах, барах (1 бар 0. 987 атм) или паскалях (1 МПа = 10 атм). Направление диффузии молекул воды, или массового водного тока, определяется градиентом водного потенциала. Водный потенциал складывается, как минимум, из четырех компонентов: w = s + p + g + m Наибольшая величина водного потенциала у чистой воды. Она условно принята за "0". Водный потенциал растворов, растительных клеток и тканей, почвы, атмосферы, как правило, имеет отрицательное значение.

s осмотический потенциал, определяется концентрацией растворенного вещества. s = с. RT, где с концентрация вещества в молях, R газовая постоянная, Т абсолютная температура, знак “ ” указывает на то, что растворенное вещество уменьшает водный потенциал раствора. С увеличением его концентрации осмотический потенциал становится все более отрицательным. Осмотический потенциал величина равная, но обратная по знаку осмотическому давлению. p потенциал давления, отражает влияние на активность воды механического (гидростатического) давления. В растительной клетке потенциал давления представляет собой тургорное противодавление клеточной оболочки, возникающее при ее эластичном растяжении. Потенциал давления по абсолютной величине равен тургорному давлению, но противоположен ему по знаку. g гравитационный потенциал, отражает влияние на активность воды силы тяжести, заставляет воду двигаться вниз до тех пор, пока силе гравитации не будет противостоять равная ей по величине другая сила. Поэтому водный потенциал зависит от веса воды. Гравитационный потенциал заметно сказывается на водном потенциале при поднятии воды на относительно большую высоту, например у высоких деревьев. m потенциал набухания биоколлоидов (матричный потенциал), связан с поглощением воды клетками за счет гидратации белков и других биоколлоидов.

Водный потенциал и его отдельные компоненты оказывают сильное воздействие на процесс фотосинтеза и продуктивность сельскохозяйственных растений. Подобно температуре тела человека, он служит хорошим интегральным показателем “здоровья” растения. Поэтому исследователи постоянно предпринимают попытки создания простых, но точных приборов, позволяющих регистрировать водный статус растения. Для измерения w, s и p на практике обычно используют такое оборудование, как психрометр, осмотическая ячейка, криоскопический осмометр и различные типы датчиков, которые позволяют регистрировать гидростатическое давление растительных клеток.

Осмосом называют процесс диффузии воды в раствор, отделенный полупроницаемой мембраной, которая пропускает молекулы растворителя, но не растворенных веществ. Существуют также активные механизмы поглощения воды клетками. Основной движущей силой водных потоков в клетках и тканях растений является градиент осмотического потенциала. Численно осмотический потенциал равен тому давлению, которое необходимо приложить к раствору, чтобы предотвратить поступление в него воды. Если вода диффундирует в раствор, отделенный от нее полупроницаемой мембраной, возникает давление (осмотическое давление), равное по величине, но противоположное по знаку исходному осмотическому потенциалу. Для расчета осмотического давления используют формулу, предложенную Вант-Гоффом: Росм = i·c·RT, i изотонический коэффициент, равный 1+α (n 1), где α – степень электролитической диссоциации; n – количество ионов, на которые распадается молекула электролита. Из уравнения следует, что осмотическое давление определяется концентрацией растворенного вещества. Осмотическое давление выражают в паскалях.
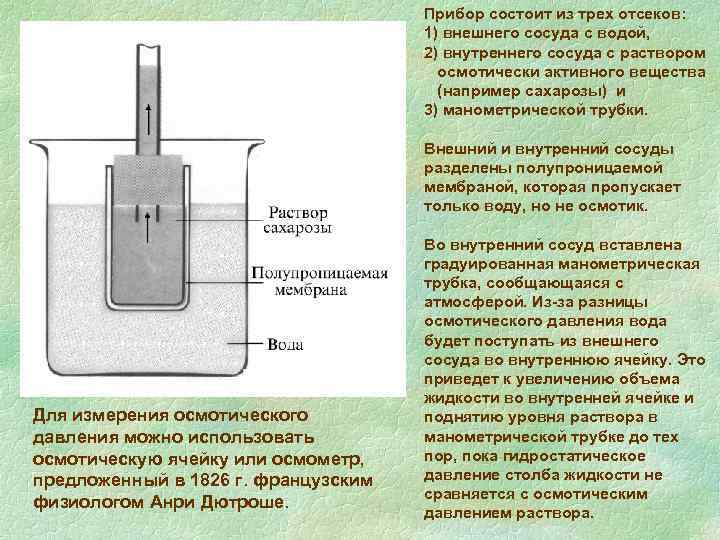
Прибор состоит из трех отсеков: 1) внешнего сосуда с водой, 2) внутреннего сосуда с раствором осмотически активного вещества (например сахарозы) и 3) манометрической трубки. Внешний и внутренний сосуды разделены полупроницаемой мембраной, которая пропускает только воду, но не осмотик. Для измерения осмотического давления можно использовать осмотическую ячейку или осмометр, предложенный в 1826 г. французским физиологом Анри Дютроше. Во внутренний сосуд вставлена градуированная манометрическая трубка, сообщающаяся с атмосферой. Из-за разницы осмотического давления вода будет поступать из внешнего сосуда во внутреннюю ячейку. Это приведет к увеличению объема жидкости во внутренней ячейке и поднятию уровня раствора в манометрической трубке до тех пор, пока гидростатическое давление столба жидкости не сравняется с осмотическим давлением раствора.
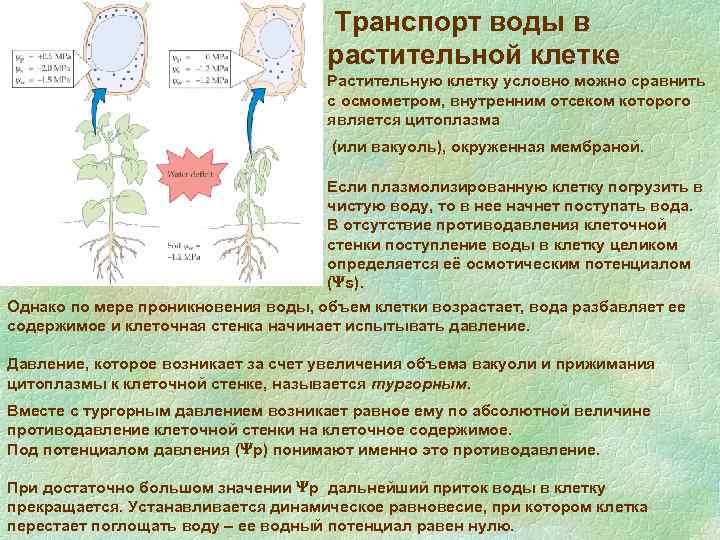
Транспорт воды в растительной клетке Растительную клетку условно можно сравнить с осмометром, внутренним отсеком которого является цитоплазма (или вакуоль), окруженная мембраной. Если плазмолизированную клетку погрузить в чистую воду, то в нее начнет поступать вода. В отсутствие противодавления клеточной стенки поступление воды в клетку целиком определяется её осмотическим потенциалом ( s). Однако по мере проникновения воды, объем клетки возрастает, вода разбавляет ее содержимое и клеточная стенка начинает испытывать давление. Давление, которое возникает за счет увеличения объема вакуоли и прижимания цитоплазмы к клеточной стенке, называется тургорным. Вместе с тургорным давлением возникает равное ему по абсолютной величине противодавление клеточной стенки на клеточное содержимое. Под потенциалом давления ( р) понимают именно это противодавление. При достаточно большом значении р дальнейший приток воды в клетку прекращается. Устанавливается динамическое равновесие, при котором клетка перестает поглощать воду ее водный потенциал равен нулю.

Теперь рассмотрим ситуацию, когда растение испытывает недостаток влаги и водный потенциал клеточной стенки ниже, чем внутри клетки. В таком случае вода выходит из вакуоли, клетки теряют тургор, становятся вялыми и мягкими. В искусственных условиях потери тургора можно добиться при погружении растительных тканей в более концентрированные растворы, чем клеточное содержимое. При этом может происходить отделение плазмалеммы от клеточной стенки и сокращение объема протопласта. Явление потери тургора клетками в гипертонической среде называют плазмолизом.

Зависимость транспорта воды от водного потенциала клетки и внешенй среды. в. При погружении подвядшей клетки (с w 0, 732 МПа) в 0. 1 М раствор сахарозы ( w = 0, 244 МПа) клетка начинает набирать воду. w клетки постепенно возрастает и наступает состояние равновесия. В результате клетка имеет положительное тургорное давление, равное разности ее водного и осмотического потенциалов: p= w s = ( 0, 244) ( 0, 732) = 0, 448 МПа. г. Погружение тургесцентной клетки (с w = 0, 244 МПа) в 0. 3 М раствор сахарозы ( w = 0, 732 МПа) приводит к потере воды клеткой и ее плазмолизу. Тургорное давление клетки при этом падает: p = w s = ( 0, 732) = 0.

Аквапорины Молекулы воды малы и проходят через клеточные мембраны намного быстрее, чем молекулы других веществ. Для транспорта воды служат белки аквапорины, формирующие в мембране селективные каналы, которые облегчают передвижение воды через мембрану. Такой тип модулирования активности аквапорина влияет только на скорость транспорта воды через мебрану, но не на направление водного потока. Транспортная активность аквапоринов регулируется их фосфорилированием.
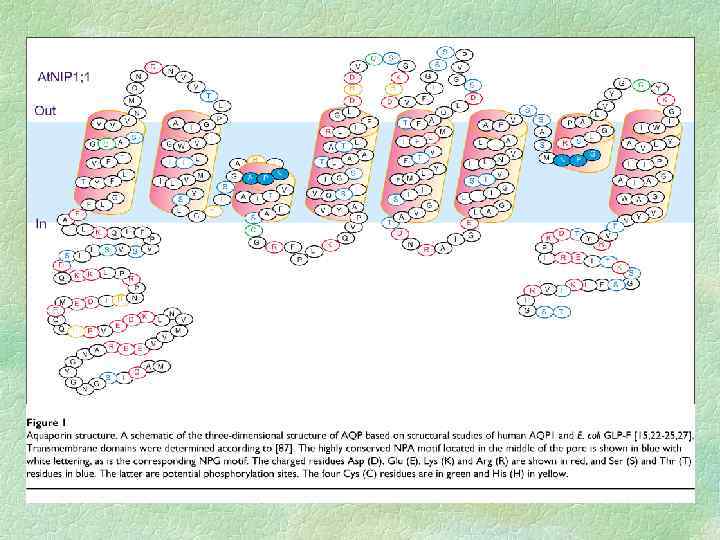
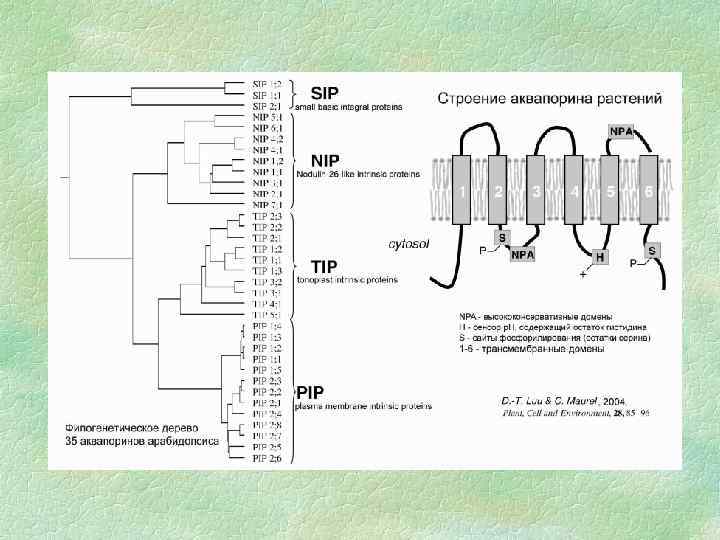
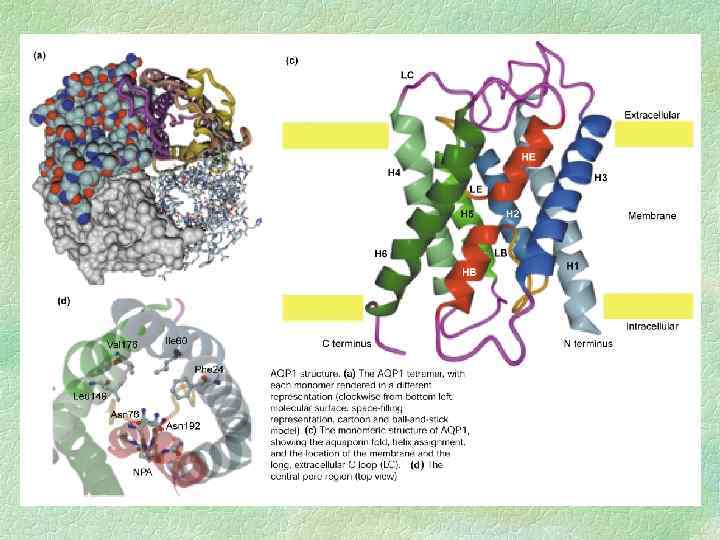
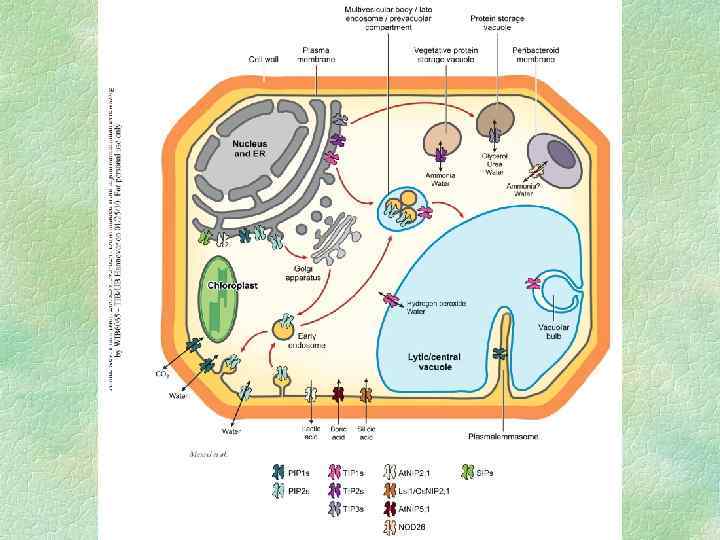
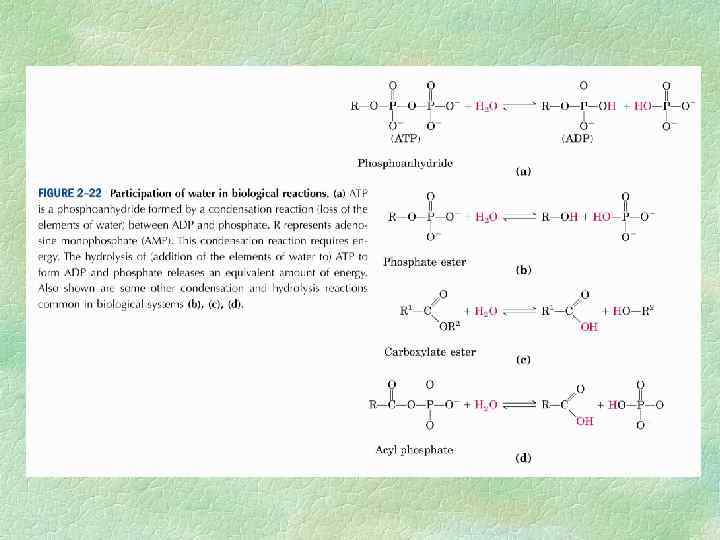
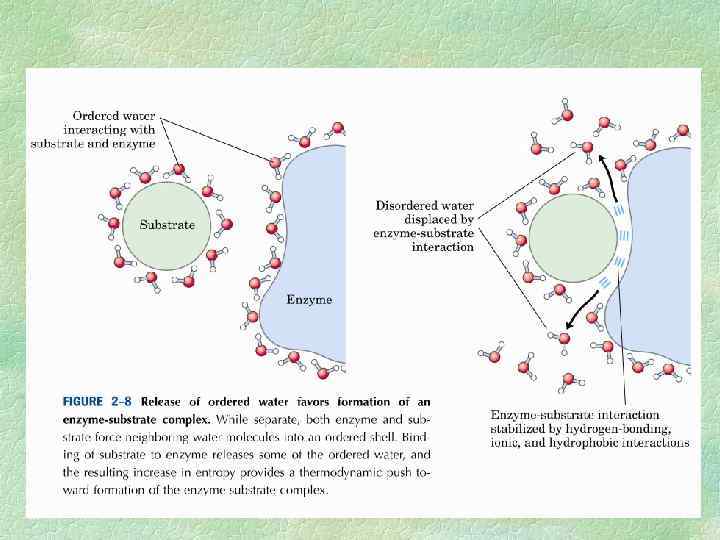
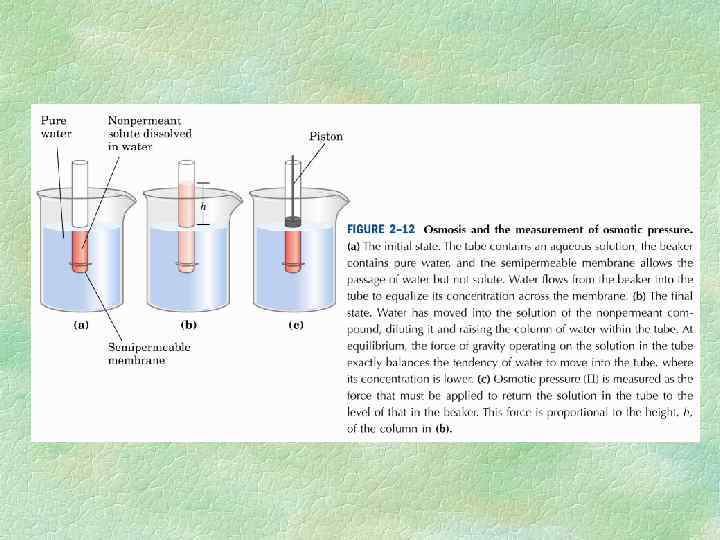

Очень часто, особенно в отечественной литературе, cилу, с которой вода входит в клетку, называют сосущей. Сосущая сила определяется как разность осмотического давления и тургорного. Если осмотическое давление выше тургорного, клетка будет набирать воду до тех пор, пока не произойдет их выравнивание. В условиях, когда клетка полностью насыщена водой, ее тургорное давление равно осмотическому, и поэтому сосущая сила равна 0. Это наблюдается при большой влажности почвы и воздуха. Сосущая сила равна по абсолютной величине водному потенциалу клетки, но противоположна ему по знаку. Поэтому сосущую силу можно определить также и через водный потенциал: ( w = s p)
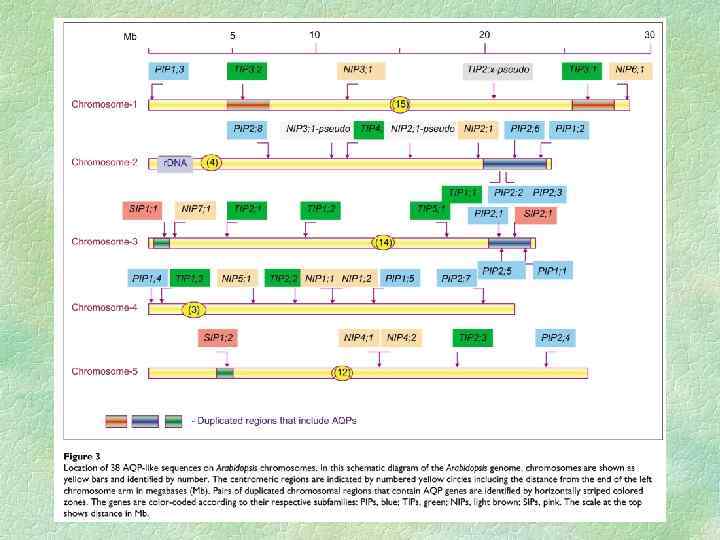

водный режим-1.ppt