MedChem_1-3.ppt
- Количество слайдов: 15

Водневий показник. Гідроліз солей

Йонний добуток води 1

p. H 2

3 p. H Методи визначення р. Н: • за допомогою кислотно-основного індикатора (органічна сполука, яка змінює забарвлення залежно від концентрації йонів Н+) • йонометричний метод за допомогою р. Н-метра (вимірювання ЕРС електричного ланцюга, що вкючає електрод, потенціал якого залежить від концентрації йонів Н+) Шкала значень р. Н нейтральний розчин кислий розчин р. Н 0 [H+] 1 [OH-] 10 -14 р. Н 1 р. Н 2 р. Н 3 [H+] 10 -3 [OH-] 10 -11 р. Н 4 р. Н 5 р. Н 6 р. Н 7 [H+] 10 -7 [OH-] 10 -7 лужний розчин р. Н 8 р. Н 9 р. Н 10 р. Н 11 [H+] 10 -11 [OH-] 10 -3 р. Н 12 р. Н 13 р. Н 14 [H+] 10 -14 [OH-] 1

4 p. H Речовина р. Н Концентровані кислоти <1. 0 Шлунковий сік 1, 65 (0, 9 -2, 0) Лимонний сік (5% р-н 2, 0± 0, 3 лимонної кислоти) Оцет 2, 4 Кока-кола 3, 0± 0, 3 Яблучний сік 3, 0 Пиво 4, 5 Кава 5, 0 Шампунь 5, 5 Чай 5, 5 Шкіра 5, 5 Слина 6, 75 (5, 6 -7, 9) Молоко 6, 6 -6, 9 Речовина р. Н Чиста вода 7, 0 Кров 7, 36 (7, 25 -7, 44) Морська вода 8, 0 Сік підшлункової 8, 65 (8, 6 -9, 0) залози Мило для рук 9, 0 -10, 0 Нашатирний спирт 11, 5 Хлорне вапно 12, 5 (відбілювач) Концентрований луг >13

5 Теорії кислот і основ Теорія Aрреніуса
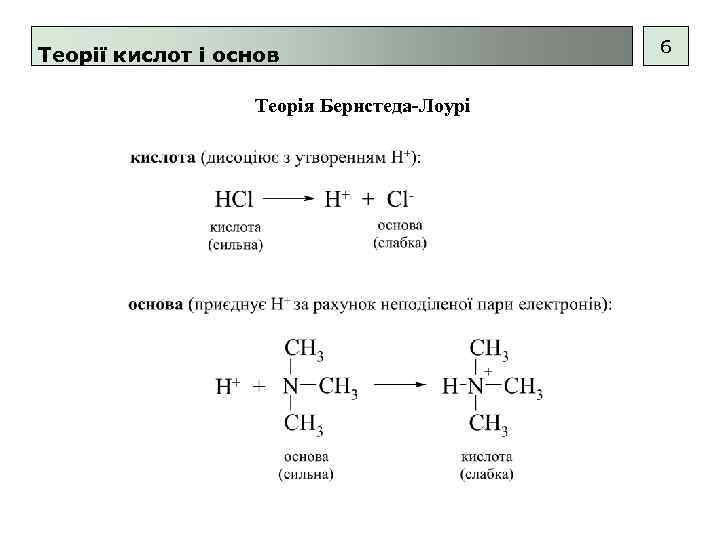
Теорії кислот і основ Теорія Бернстеда-Лоурі 6

7 Теорії кислот і основ Теорія Льюїса

Протолітичні реакції. Гідроліз Сила кислот та основ, константа дисоціації (протолізу) 8

Протолітичні реакції. Гідроліз – взаємодія речовини з водою. 9

Протолітичні реакції. Гідроліз 10

Протолітичні реакції. Гідроліз 11

Протолітичні реакції. Гідроліз 12
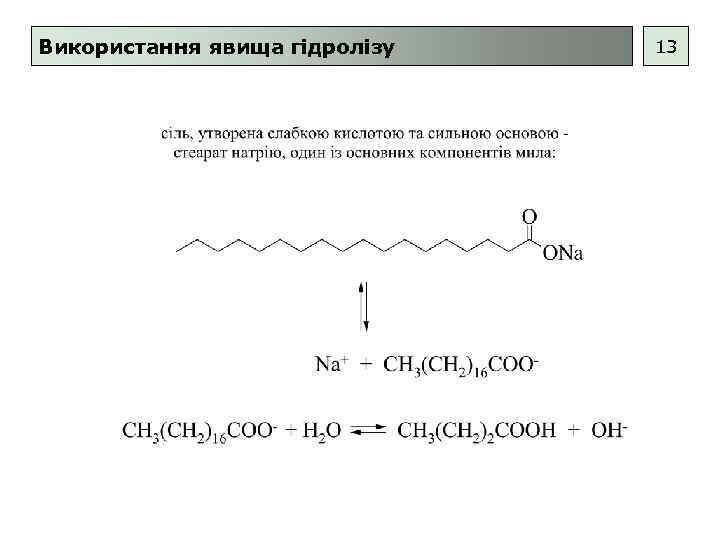
Використання явища гідролізу 13

Гідроліз в біологічних системах 14
MedChem_1-3.ppt