 Вода знакомая загадочная
Вода знакомая загадочная
 То, что неясно следует выяснить. То, что трудно творить, следует делать с величайшей настойчивостью. Конфуций.
То, что неясно следует выяснить. То, что трудно творить, следует делать с величайшей настойчивостью. Конфуций.
 Вода растворитель. Растворы. • Растворы – однородные системы, состоящие • • из молекул растворителя и частиц растворенного вещества, между которыми происходит физические и химические взаимодействия. Кроме растворов существуют мутные смесивзвеси. Со временем отстаиваются.
Вода растворитель. Растворы. • Растворы – однородные системы, состоящие • • из молекул растворителя и частиц растворенного вещества, между которыми происходит физические и химические взаимодействия. Кроме растворов существуют мутные смесивзвеси. Со временем отстаиваются.
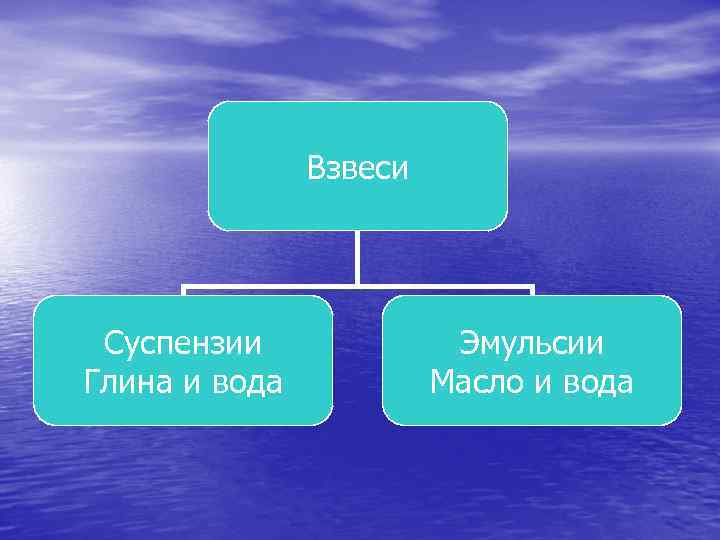 Взвеси Суспензии Глина и вода Эмульсии Масло и вода
Взвеси Суспензии Глина и вода Эмульсии Масло и вода
 Растворимость веществ в воде • Растворимость( коэффициент растворимости – • • • максимально возможное число граммов вещества, которое может раствориться в 100 г растворителя при данной температуре. Растворимость небезгранично Для большинства твердых веществ с повышением температуры растворимость увеличивается Растворимость газов с повышением температуры уменьшается.
Растворимость веществ в воде • Растворимость( коэффициент растворимости – • • • максимально возможное число граммов вещества, которое может раствориться в 100 г растворителя при данной температуре. Растворимость небезгранично Для большинства твердых веществ с повышением температуры растворимость увеличивается Растворимость газов с повышением температуры уменьшается.
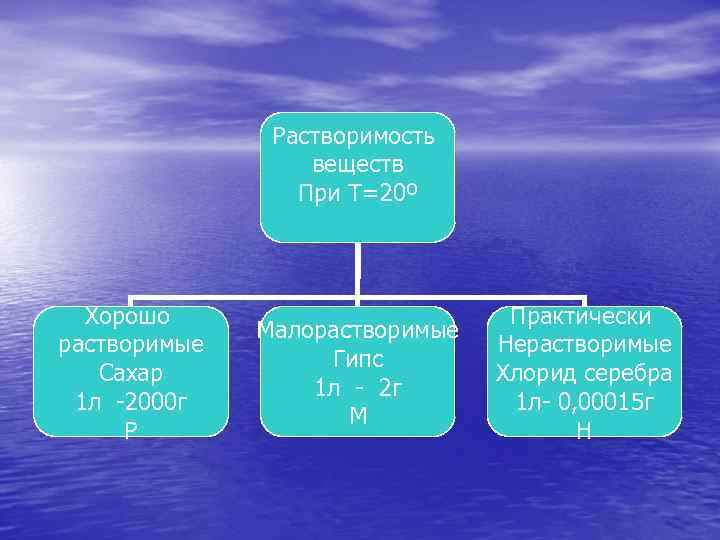 Растворимость веществ При Т=20º Хорошо растворимые Сахар 1 л -2000 г Р Малорастворимые Гипс 1 л - 2 г М Практически Нерастворимые Хлорид серебра 1 л- 0, 00015 г Н
Растворимость веществ При Т=20º Хорошо растворимые Сахар 1 л -2000 г Р Малорастворимые Гипс 1 л - 2 г М Практически Нерастворимые Хлорид серебра 1 л- 0, 00015 г Н
 Растворы • Насыщенные – раствор , в котором данное • • • вещество при данной температуре больше не растворяется. Ненасыщенные – раствор, в котором данное вещество при данной температуре еще может растворятся Концентрированный- в растворе много растворенного вещества Разбавленный – в растворе мало растворенного вещества
Растворы • Насыщенные – раствор , в котором данное • • • вещество при данной температуре больше не растворяется. Ненасыщенные – раствор, в котором данное вещество при данной температуре еще может растворятся Концентрированный- в растворе много растворенного вещества Разбавленный – в растворе мало растворенного вещества
 Выражение количественного состава растворов • Массовая доля растворенного вещества- это • отношение массы растворенного вещества к массе раствора (процентная концентрация). mр. в. ω – массовая доля ω р. в =───── · 100% растворенного вещества mр-ра mр. в – растворенного в-ва mр-ра – раствора mр-ра = m р. в. + m H 2 O
Выражение количественного состава растворов • Массовая доля растворенного вещества- это • отношение массы растворенного вещества к массе раствора (процентная концентрация). mр. в. ω – массовая доля ω р. в =───── · 100% растворенного вещества mр-ра mр. в – растворенного в-ва mр-ра – раствора mр-ра = m р. в. + m H 2 O
 Решение задач • Вычислить массовую долю растворенного • • вещества если было взято 20 г поваренной соли и 400 г воды? Вычислить массу растворенного вещества в 500 г раствора с массовой долей растворенного вещества 30% ? При выпаривании 10%раствора массой 100 г осталось раствора 80 г. Вычислить массовую долю растворенного вещества нового раствора
Решение задач • Вычислить массовую долю растворенного • • вещества если было взято 20 г поваренной соли и 400 г воды? Вычислить массу растворенного вещества в 500 г раствора с массовой долей растворенного вещества 30% ? При выпаривании 10%раствора массой 100 г осталось раствора 80 г. Вычислить массовую долю растворенного вещества нового раствора
 Решение задач • При разбавлении 500 г 20% раствора • добавили 300 г воды. Вычислить массовую долю растворенного вещества нового раствора. Масса воды в растворе составляет 200 г а массовая доля растворенного вещества 20% вычислите массу растворенного вещества и массу раствора.
Решение задач • При разбавлении 500 г 20% раствора • добавили 300 г воды. Вычислить массовую долю растворенного вещества нового раствора. Масса воды в растворе составляет 200 г а массовая доля растворенного вещества 20% вычислите массу растворенного вещества и массу раствора.
 Плотность раствора m ρ – плотность раствора(г/см³) • ρ = ──── m – масса раствора(г) V V – объем раствора(мл, см³) ρ (Н 2 О) = 1 г/мл ; 1 г/см³
Плотность раствора m ρ – плотность раствора(г/см³) • ρ = ──── m – масса раствора(г) V V – объем раствора(мл, см³) ρ (Н 2 О) = 1 г/мл ; 1 г/см³
 Упражнения • 1. Вычислить массу раствора объемом 600 мл и плотностью 1, 4 г/мл • 2. Вычислить объем раствора массой 450 г и плотностью 1, 05 г/мл • 3. Вычислить плотность раствора массой 400 г и объемом 380 мл
Упражнения • 1. Вычислить массу раствора объемом 600 мл и плотностью 1, 4 г/мл • 2. Вычислить объем раствора массой 450 г и плотностью 1, 05 г/мл • 3. Вычислить плотность раствора массой 400 г и объемом 380 мл
 Молярная концентрация ∂ • С = ──── V ∂ -количество вещества(моль) V – объем (л) С – молярная концентрация
Молярная концентрация ∂ • С = ──── V ∂ -количество вещества(моль) V – объем (л) С – молярная концентрация
 Упражнения • Вычислить молярную концентрацию раствора количеством вещества 5 молей и 500 мл раствора • Молярная концентрация раствора 2 моль/л объем раствора составляет 300 мл Вычислить массу хлорида натрия в данном растворе(Na. Cl).
Упражнения • Вычислить молярную концентрацию раствора количеством вещества 5 молей и 500 мл раствора • Молярная концентрация раствора 2 моль/л объем раствора составляет 300 мл Вычислить массу хлорида натрия в данном растворе(Na. Cl).
 Задачи (домашнее задание) • Вычислить массу растворенного вещества и воды, которая содержится в 400 г раствора содержащего 12% сахара. • Вычислить молярную концентрацию раствора поваренной соли массой 550 г с массовой долей растворенного вещества 10% и плотностью 1, 2 г/мл.
Задачи (домашнее задание) • Вычислить массу растворенного вещества и воды, которая содержится в 400 г раствора содержащего 12% сахара. • Вычислить молярную концентрацию раствора поваренной соли массой 550 г с массовой долей растворенного вещества 10% и плотностью 1, 2 г/мл.
 Появление воды на планете.
Появление воды на планете.
 Гипотеза v. Вода – универсальное вещество на Земле
Гипотеза v. Вода – универсальное вещество на Земле
 • Изучив литературу, мы узнали, что миллиарды лет назад в холодном газопылевом облаке уже содержалась вода. Исходные элементы для образования воды: кислород и водород в нашей Галактике принадлежат к шести самым распространенным веществам космоса. Скопление молекул обнаружены за пределами Солнечной системы.
• Изучив литературу, мы узнали, что миллиарды лет назад в холодном газопылевом облаке уже содержалась вода. Исходные элементы для образования воды: кислород и водород в нашей Галактике принадлежат к шести самым распространенным веществам космоса. Скопление молекул обнаружены за пределами Солнечной системы.

 • Скопления молекул воды обнаружены за пределами Солнечной системы. Исследуя геологические процессы на Земле, учёные установили, что вода и составляющие её элементы играли определяющую роль во всей геологической истории Земли.
• Скопления молекул воды обнаружены за пределами Солнечной системы. Исследуя геологические процессы на Земле, учёные установили, что вода и составляющие её элементы играли определяющую роль во всей геологической истории Земли.
 • В недрах Земли происходят физико – химические процессы, под давлением и высокой температуры образуются парои газообразные соединения, в том числе и вода. Водяной пар через наземные и под водные трещины и разломы выделяются на поверхность. Часть воды покинула поверхность планеты, часть постепенно образовала гидросферу. Таким образом появились благоприятные условия для появления жизни на планете.
• В недрах Земли происходят физико – химические процессы, под давлением и высокой температуры образуются парои газообразные соединения, в том числе и вода. Водяной пар через наземные и под водные трещины и разломы выделяются на поверхность. Часть воды покинула поверхность планеты, часть постепенно образовала гидросферу. Таким образом появились благоприятные условия для появления жизни на планете.
 Кислород Водород
Кислород Водород
 Вода на планете Гидросфера • Реки • Моря • Озёра • Болота • Атмосферная влага • Океаны
Вода на планете Гидросфера • Реки • Моря • Озёра • Болота • Атмосферная влага • Океаны
 Нахождение воды на планете • Подземные льды • Криологи(концентрированные • • • природные рассолы, они создают природный холодильник. Гейзеры – горячие источники, температура воды достигает 90 градусов С Подземные воды Минеральные источники
Нахождение воды на планете • Подземные льды • Криологи(концентрированные • • • природные рассолы, они создают природный холодильник. Гейзеры – горячие источники, температура воды достигает 90 градусов С Подземные воды Минеральные источники
 Интересные факты • Большая пресной воды находится на полюсах • • земли в ледниках(85%) В древней Индии накаленные серебряные стержни погружали в воду и потом ее использовали для обмывания ран. Подумайте, что бы произошло в природе если бы замерзание рек и озер начиналось со дна.
Интересные факты • Большая пресной воды находится на полюсах • • земли в ледниках(85%) В древней Индии накаленные серебряные стержни погружали в воду и потом ее использовали для обмывания ран. Подумайте, что бы произошло в природе если бы замерзание рек и озер начиналось со дна.
 Способы очистки воды • • 1. 2. 3. 4. 5. Вода всегда содержит примеси. Очистка воды Отстаивание Фильтрование Хлорирование(озонирование, УФ лучи) Насосы Водопровод в город рис. 50 стр. 83.
Способы очистки воды • • 1. 2. 3. 4. 5. Вода всегда содержит примеси. Очистка воды Отстаивание Фильтрование Хлорирование(озонирование, УФ лучи) Насосы Водопровод в город рис. 50 стр. 83.
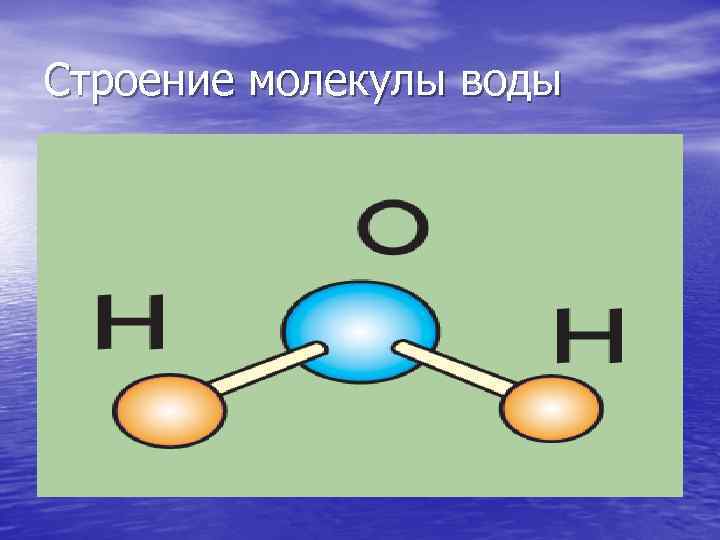 Строение молекулы воды
Строение молекулы воды
 Физические свойства воды • Чистая вода – бесцветная жидкость, без вкуса и запаха, Ткип=100ºС, Т з=0 ºС, плотность 1 г/мл. Лед имеет молекулярную кристаллическую решетку. Легче воды.
Физические свойства воды • Чистая вода – бесцветная жидкость, без вкуса и запаха, Ткип=100ºС, Т з=0 ºС, плотность 1 г/мл. Лед имеет молекулярную кристаллическую решетку. Легче воды.
 Химические свойства воды I. Взаимодействие воды с простыми веществами с металлами Li; Na; K; Ca; Ba; Al; Mg 2 Na + 2 H 2 O =2 Na. OH+H 2 с металлами Zn; Cr; Fe; Pb; Sn при нагревании Zn + H 2 O = Zn. O + H 2 оксид цинка Не реагирует с Cu; Hg; Au; Pt II. Взаимодействие воды со сложными веществами 1. С основными оксидами Са. О + H 2 O =Ca(OH)2 гидроксид кальция
Химические свойства воды I. Взаимодействие воды с простыми веществами с металлами Li; Na; K; Ca; Ba; Al; Mg 2 Na + 2 H 2 O =2 Na. OH+H 2 с металлами Zn; Cr; Fe; Pb; Sn при нагревании Zn + H 2 O = Zn. O + H 2 оксид цинка Не реагирует с Cu; Hg; Au; Pt II. Взаимодействие воды со сложными веществами 1. С основными оксидами Са. О + H 2 O =Ca(OH)2 гидроксид кальция
 Химические свойства воды 2. Взаимодействует с кислотными оксидами Р 2 О 5 + 3 Н 2 О = 2 Н 3 РО 4 фосфорная кислота 3. Под действием тока или высокой температуры 2000º разлагается 2 Н 2 О = 2 Н 2 + О 2
Химические свойства воды 2. Взаимодействует с кислотными оксидами Р 2 О 5 + 3 Н 2 О = 2 Н 3 РО 4 фосфорная кислота 3. Под действием тока или высокой температуры 2000º разлагается 2 Н 2 О = 2 Н 2 + О 2
 Соответствие основных оксидов основаниям • Li 2 O - Li. OH гидроксид лития • Na 2 O – Na. OH гидроксид натрия • K 2 O - KOH ? • Rb 2 O – Rb. OH ? • Cs 2 O – Cs. OH ? • Ca. O - Ca(OH)2 ? • Ba. O - Ba(OH)2 ? • Sr. O - Sr(OH)2 ?
Соответствие основных оксидов основаниям • Li 2 O - Li. OH гидроксид лития • Na 2 O – Na. OH гидроксид натрия • K 2 O - KOH ? • Rb 2 O – Rb. OH ? • Cs 2 O – Cs. OH ? • Ca. O - Ca(OH)2 ? • Ba. O - Ba(OH)2 ? • Sr. O - Sr(OH)2 ?
 • CO 2 - H 2 CO 3 угольная кислота • P 2 O 5 - H 3 PO 4 фосфорная кислота • SO 2 - H 2 SO 3 сернистая кислота • SO 3 - H 2 SO 4 серная кислота • N 2 O 5 - HNO 3 азотная кислота • Si. O 3 не взаимод. с водой H 2 Si. O 3 кремниевая к-та
• CO 2 - H 2 CO 3 угольная кислота • P 2 O 5 - H 3 PO 4 фосфорная кислота • SO 2 - H 2 SO 3 сернистая кислота • SO 3 - H 2 SO 4 серная кислота • N 2 O 5 - HNO 3 азотная кислота • Si. O 3 не взаимод. с водой H 2 Si. O 3 кремниевая к-та
 Выводы • Вода – активный созидатель нашей планеты, один из основных «строительных материалов» • Н 2 О
Выводы • Вода – активный созидатель нашей планеты, один из основных «строительных материалов» • Н 2 О
 Вода – универсальный растворитель различных веществ
Вода – универсальный растворитель различных веществ
 2/3 нашей планеты занято водой, однако питьевой воды мало. её необходимо беречь
2/3 нашей планеты занято водой, однако питьевой воды мало. её необходимо беречь
 Вода – достаточно активное химическое вещество
Вода – достаточно активное химическое вещество
 Безбрежная ширь океана И тихая заводь пруда, Струя водопада и брызги фонтана И всё это- только вода.
Безбрежная ширь океана И тихая заводь пруда, Струя водопада и брызги фонтана И всё это- только вода.
 Применение воды В быту Вода В промышленности Растворитель
Применение воды В быту Вода В промышленности Растворитель
 Какие применения воды вы знаете? • В помощь • Стр. № 87 схема 9
Какие применения воды вы знаете? • В помощь • Стр. № 87 схема 9
 Вопросы и упражнения • Составьте уравнения реакций с водой следующих веществ калия , кальция , оксида бария, оксида фосфора V. • Даны вещества: Ca. O; Si. O 2; Cu; Na; Hg С какими из данных веществ вода вступает в химические реакции.
Вопросы и упражнения • Составьте уравнения реакций с водой следующих веществ калия , кальция , оксида бария, оксида фосфора V. • Даны вещества: Ca. O; Si. O 2; Cu; Na; Hg С какими из данных веществ вода вступает в химические реакции.
 Упражнения Решить цепочку превращений • H 2 ← Н 2 О → Na. OH ↓ HNO 3 Решить цепочку превращений • Н 2 О → О 2→ Са. О→ Са(ОН)2 • P→P 2 O 5→H 3 PO 4
Упражнения Решить цепочку превращений • H 2 ← Н 2 О → Na. OH ↓ HNO 3 Решить цепочку превращений • Н 2 О → О 2→ Са. О→ Са(ОН)2 • P→P 2 O 5→H 3 PO 4
 Используемая литература • Л. А. Кульский «Вода знакомая и загадочная» М. «Просвещение» 1998 г. • Словарь юного химика М. » Просвещение» 1996 год
Используемая литература • Л. А. Кульский «Вода знакомая и загадочная» М. «Просвещение» 1998 г. • Словарь юного химика М. » Просвещение» 1996 год
 Решение задач • Вычислить массу воды и массу растворенного вещества в 800 г раствора с массовой долей растворенного вещества 30% • Вычислить объем водорода который выделится при взаимодействии 4, 6 г натрия с водой.
Решение задач • Вычислить массу воды и массу растворенного вещества в 800 г раствора с массовой долей растворенного вещества 30% • Вычислить объем водорода который выделится при взаимодействии 4, 6 г натрия с водой.
 Самостоятельно • Вычислить молярную концентрацию раствора объемом 500 мл в котором растворено 80 г гидроксида натрия (Na. OH) • Решить цепочку превращений. Определить тип реакции. • Ca→Ca. O→Ca(OH)2
Самостоятельно • Вычислить молярную концентрацию раствора объемом 500 мл в котором растворено 80 г гидроксида натрия (Na. OH) • Решить цепочку превращений. Определить тип реакции. • Ca→Ca. O→Ca(OH)2
 Подготовка к контрольной работе • Составьте уравнения реакций с водой следующих веществ: натрия , бария. кальция , оксида калия, оксида магния, оксида серы IV, оксида серы VI. • Закончить уравнения реакций H 2 O = Li + H 2 O = Na 2 O + H 2 O= P 2 O 5 + H 2 O=
Подготовка к контрольной работе • Составьте уравнения реакций с водой следующих веществ: натрия , бария. кальция , оксида калия, оксида магния, оксида серы IV, оксида серы VI. • Закончить уравнения реакций H 2 O = Li + H 2 O = Na 2 O + H 2 O= P 2 O 5 + H 2 O=
 • Решить цепочку превращений H 2 O→O 2→P 2 O 5→H 3 PO 4 S →SO 2→SO 3→H 2 SO 4
• Решить цепочку превращений H 2 O→O 2→P 2 O 5→H 3 PO 4 S →SO 2→SO 3→H 2 SO 4
 Решение задач • Рассчитать массу кислорода образующуюся в результате разложений 54 г воды • Рассчитайте объем водорода, который выделиться при взаимодействии 20 г кальция с водой.
Решение задач • Рассчитать массу кислорода образующуюся в результате разложений 54 г воды • Рассчитайте объем водорода, который выделиться при взаимодействии 20 г кальция с водой.
 Задачи • В 500 г воды растворили 100 г соли. Рассчитайте массовую долю растворенного вещества. • Рассчитайте массу сахара и воды , которые нужно взять для приготовления 500 г раствора с массовой долей растворенного вещества 5 %
Задачи • В 500 г воды растворили 100 г соли. Рассчитайте массовую долю растворенного вещества. • Рассчитайте массу сахара и воды , которые нужно взять для приготовления 500 г раствора с массовой долей растворенного вещества 5 %
 Задачи • Вычислить молярную концентрацию вещества , если в 600 мл раствора растворено 112 г гидроксида калия ( КОН) • Вычислить массу раствора объемоо 300 мл и плотностью 1, 1 г/ мл.
Задачи • Вычислить молярную концентрацию вещества , если в 600 мл раствора растворено 112 г гидроксида калия ( КОН) • Вычислить массу раствора объемоо 300 мл и плотностью 1, 1 г/ мл.
 Спасибо за внимание
Спасибо за внимание
 Цели: • Изучить историю появления воды на планете Земля. • Познакомиться с нахождением воды на планете. • Исследовать растворимость веществ в воде. • Исследовать химические свойства воды.
Цели: • Изучить историю появления воды на планете Земля. • Познакомиться с нахождением воды на планете. • Исследовать растворимость веществ в воде. • Исследовать химические свойства воды.


